2. 贵州师范大学化学与材料科学学院,贵阳 550001
我国南方土壤酸化日益严重,已对当地农业发展和生态环境构成严重威胁,对于土壤酸化过程的研究迫在眉睫[1]。其中,关于土壤酸敏感值、酸害容量有较多的研究,但这些指标只是简单宏观定量土壤对酸化的缓冲能力[2]。要弄清楚土壤酸化的微观机制,对土壤表面酸碱性质的研究至关重要[3]。土壤的酸碱性质指土壤与环境中质子发生的质子化、去质子化反应能力,主要包括表面质子反应活性位点密度、电荷零点以及质子化、去质子化平衡常数[4-5],能够用于定量土壤酸碱缓冲能力。将这些酸碱性质参数带入MINTEQ[6-9]等形态模拟软件,能够模拟土壤对酸化的缓冲机理,从微观层次解释土壤酸化过程。此外,土壤表面酸碱性质显著影响着阳离子和阴离子在土壤固液间的分配,是控制微量元素移动性和生物有效性的重要土壤性质之一[10]。
酸敏感值等酸化缓冲指标通过绘制酸缓冲曲线即可获得,向土壤中加入不同量的酸平衡后测定悬液的pH,将pH对加入的相应酸量作图绘成曲线即为土壤的酸缓冲曲线[2]。而土壤表面酸碱性质的获得,除了酸碱实验还需要借助模型的方法[11]。表面络合模型(Surface complexation model,SCM)法能够充分考虑到与表面吸附反应有关的表面活性位点类型、密度、络合常数、吸附形态等信息,有助于深入研究吸附机制,逐渐用于土壤活性成分金属氧化物、有机物、黏土矿物的研究[12-13],获得了丰富的数据[14-15]。SCM在原有经典的恒定容量模型(CCM)、双层模型(DLM)及三层模型(TLM),增加了考虑到表面吸附位点的异质性和多样性的电荷分布-多位点络合(CD-MUSIC)模型[16-18]以及考虑到竞争吸附的存在的非理想竞争吸附-杜南(NICA-Donnan)模型[19-20]。然而自然土壤由于组成复杂,表面活性位点多样,增加了模拟计算的复杂性,表面酸碱性质研究相对困难[13, 21]。
近十年来,逐渐有研究者采用组分添加法(Component addition, CA)、广义复合法(Generalized composite, GC)在此方向上取得突破。CA法假设土壤表面酸碱性质主要由其活性成分如铁、铝氧化物和黏土矿物决定,研究者们建立矿物聚合物、矿物有机物聚合物模型进行研究[22-24]。GC法假设土壤所有表面官能团的性质是通用的,可以代表所有组分的平均性质。现在已从1-site/2-pKa发展为n-site/n-pKa实现了更好的拟合[25]。此外,一种广义回归模型被建立,实现了简单通过土壤基本化学性质(如阳离子交换量CEC、有机碳含量OC、铁氧化物含量Fe等)就可以预测表面络合常数[26]。所以,本文在阐述了土壤表面酸碱性质参数及获取方法的基础上,重点综述了组分添加法CA和广义复合法GC两种方法的研究进展,并进一步展望了未来相关研究的发展。
1 可变电荷土壤表面酸碱性质理论土壤酸化除受酸沉降和不合理的农业措施等人为因素影响外,其自身性质也是影响酸化程度的重要因素[4]。关于土壤自身对酸化缓冲能力的研究,研究者们曾提出了生态系统对酸沉降临界负荷的概念,其中临界负荷通过阳离子交换量CEC等表示[1, 27]。很显然这种方法更适合恒电荷土壤,因为可变电荷土壤中可以交换的阳离子已经很少存在。而王敬华等[2]针对我国可变电荷土壤的特性提出酸碱缓冲曲线法,以及土壤的酸害容量和土壤的酸敏感值两个概念,但这些指标只是简单宏观定量土壤对酸化的缓冲能力。要弄清楚土壤酸化的微观机制,对土壤表面酸碱性质的研究至关重要。
事实上,已酸化的可变电荷土壤中缓冲酸化的碳酸盐、盐基离子已很少存在,但含有较多的次生矿物和铁铝氧化物[4]。所以可变电荷土壤中质子主要有三个去向,转化为表面正电荷、释放水溶态铝、转化为交换性酸。土壤表面质子化的反应速度较后两者快得多,在氢离子的消耗中占有较高的相对贡献,从10.3%到48.8%,因土壤类型而有差异[28]。后两者释放有毒三价铝离子会影响植物生长而制约农业生产,所以表面质子化是酸缓冲的重要机制,对于研究土壤酸化具有重要意义[3-4]。土壤表面质子化,其实是土壤中有机质、黏土矿物以及铁铝氧化物的表面羟基基团与质子发生的吸附反应,这种能力由土壤表面酸碱性质体现。
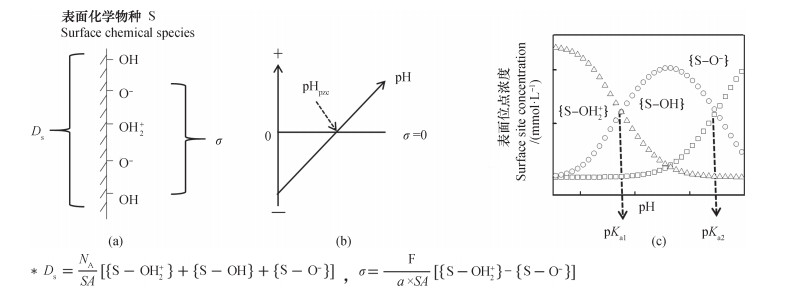
土壤表面酸碱性质主要包括表面质子反应活性位点密度Ds(site·nm-2)、电荷零点pHpzc及质子化、去质子化平衡常数pKa[4-5]。Ds是土壤重要的表面性质,是表面铁、硅、铝等羟基官能团的≡S-OH2+、≡S-OH、≡S-O-三种化学物种浓度的总和,如图 1a。它不仅是质子吸附位点,能用于定量土壤酸缓冲能力,也是其他无机、有机污染物的吸附位点[29]。pHpzc是指土壤表面电荷密度σ为零时对应的pH,如图 1b。土壤表面羟基质子化缓冲酸化过程主要发生在pHpzc > pH时,所以pHpzc是判定土壤酸缓冲能力的重要标准。土壤pHpzc主要由组成决定,金属氧化物具有较高pHpzc,黏土矿物和有机物pHpzc较低[3, 4, 30]。此外,在重金属等离子吸附研究中,常用土壤pHpzc的转变来解释内层络合机制[11]。pKa是指土壤表面各种官能团的平衡常数,可用于判定各种官能团的酸碱缓冲范围,代入形态模拟软件可揭示土壤酸化机理,从微观层次解释土壤酸化过程,如图 1c。常见形态模拟软件有ECOSAT[31]、WHAM 6[32]、PHREEQE[33]、MINTEQ[6-9]及ORCHESTRA[34]。此外,土壤表面酸碱性质数据是研究土壤水界面Pb[35]等重金属离子、磷酸[13]等阴离子吸附情况的基础,而其技术手段和模型方法的发展也会推动土壤对其他离子吸附机制的研究[36-37]。
|
注:NA为阿伏伽德罗常数;SA为表面积;F为法拉第常数;a为悬浊液浓度。 Note: NA stands for Avogadro’s number; SA for surface area; F for Faraday constant; and a for concentration of the suspended solution. 图 1 可变电荷土壤表面酸碱性质参数示意图 Fig. 1 A schematic diagram of surface acid-base properties of the tested variable charge soils |
土壤表面酸碱性质包括表面质子反应活性位点浓度Hs、密度Ds、电荷零点pHpzc以及质子化、去质子化平衡常数pKa,这些基本参数是在SCM基础上通过各种计算方法处理宏观实验数据获得的,如图 1。为更好地避免实验中干扰因素的影响,实验经过不断地改善,而计算方法也经过优化,形成了一套适合土壤表面酸碱性质研究的方法体系。
2.1 表面质子反应活性位点密度Ds表面质子反应活性位点密度Ds由土壤各组分的表面活性羟基总数Hs(mol·kg-1)和表面积SA(m2·g-1)决定:
Ds=(Hs×NA)/SA
其中NA为阿伏伽德罗常数。在对土壤SA的测定方法中,氮气吸附法是最常用的方法,但由于氮气不会进入膨胀性黏土矿物晶层之间,很难反映土壤真实的SA[38-39]。所以也有采用乙二醇己醚[38, 40-41]、亚甲基蓝[23, 42]或水[39]吸附法测定土壤SA。获取Ds有多种方法,如晶体学计算、氟化物吸附以及酸碱电位滴定等[41, 43]。其中酸碱电位滴定法获得土壤的Ds存在一定偏差,因为在表面位点达到饱和时部分氧化物、有机物质可能溶解[43-44]。但相对其他方法,实验操作简单、误差较小,相关研究还是以酸碱电位滴定方法为主[20, 43]。具体方法是通过Gran函数处理电位滴定实验数据获得,Gran函数最初由Gran[45]提出,是判断氧化还原、络合、酸碱等反应终点常用的方法。在很多文献中[46-49],已被用于计算体系表面活性位点浓度,具体是以NaOH标准液滴加体积Vb为横坐标,以溶液中H+、OH-物质的量为纵坐标,绘制Gran函数图,外推两条Gran函数线与横坐标的交点分别是去质子化反应的起点Ve1和终点Ve2,则表面活性位点浓度Hs=(Ve2-Ve1)Cb/2m。这种方法,不需要太多数据,在有金属离子的情况下也可以进行,并且获得数据比较精确[45]。表面位点密度Ds也有一些更粗略的计算方法,如等价于阳离子价换量CEC[35, 50],等价于水铁矿等矿物的Ds[44]。Goldberg[41]则以Davis和Kent[51]建议值2.31site·nm-2作为自己研究各种土壤的Ds。此外,也可以用土壤各组分Ds加和获得,在组分添加部分将详细介绍。
2.2 电荷零点pHpzc电位滴定法是研究土壤表面性质的主要表征手段,通过向不同浓度电解质悬浊液中缓慢滴加酸、碱可以获得体系在不同pH下的表面电荷密度σ以及电荷零点pHpzc等信息。早期比较经典的是Parks[52]的工作。滴定实验必须在惰性环境中进行,一般从较低的pH开始碱滴,因为酸性环境下CO2易被排除。滴定pH范围一般在pHpzc附近,不建议太大以排除过酸过碱造成溶解。其中针铁矿[53](pH 4~10)、三水铝石[53](pH 5~10)、蒙脱石[54](pH 4.5~9.5)获得较好的滴定实验结果。对于酸化土壤,低pHpzc的高岭土、有机质使得土壤pHpzc偏低,所以一般从pH 3左右开始碱滴[3-4, 55]。在已有文献中,滴定速率范围研究比较宽泛,快的有3~5 min一个平衡点,慢的也有几天一个平衡[53]。现多采用快速滴定法,相比于慢速滴定其对固体的溶解和再结晶过程比较敏感,但可能质子化和去质子化过程未完全完成。关于平衡时间对滴定曲线的影响,文献[36]中已有报道。由于滴定实验的每一步都可能导致pHpzc或大或小发生改变,Szekeres和Tombácz[56]制定了专门的流程,充分考虑到了电极、溶解、专性离子吸附对实验的影响[53, 56]。对于自然土壤在滴定实验前还需要纯化,纯化首先需要在水中分散以获得富含黏土的颗粒(< 2 μm),其次用酸洗去碳酸盐、用H2O2除去有机物。Gu等[57]以及Kaiser和Guggenberger[58]均建议用NaClO除有机物,因为其相比H2O2法更能保持无定型氧化物矿物原始形态和表面积。最后洗涤、干燥,可以在低温下保存在水中,也保存冷冻干燥后的样品。对于原体系的研究,有的只是简单用低浓度NaCl洗涤,除去酸碱杂质[23]。
2.3 质子化与去质子化平衡常数pKa对于简单的1-site/2-pKa模型,Stumm等[59]和Cheng等[4]将滴定曲线外推到电荷零点,获得的截距即为表面羟基基团质子化和去质子化的两个常数。对于n-stie/n-pKa模型,Pagnanelli等[25]和王代长等[10]认为滴定曲线应有拐点和平台,拐点反映吸附位点的分布,一个拐点对应一个pKa值。所以可以通过滴定曲线的一阶导数图中几个峰值确定具体pKa值,但一般要先对滴定曲线进行平滑处理,排除假峰的干扰。Tan等[60]将这种求导曲线称为质子亲和分布曲线,其中峰面积表示表面位点密度,峰宽表示位点化学异质性,峰值为位点平均质子亲和常数。而Goldberg等[61]直接选用铁铝氧化物的酸碱络合常数pKa作为土壤的pKa。
以上方法获得pKa时未考虑到固液界面离子间静电力的影响,而CCM、DLM、TLM等表面络合模型对双电层有不同的描述,每种模型假定一种特殊的界面结构,须考虑到各种不同的表面反应和质量平衡的静电校正因子,如电容值C。电容值C 无法通过实验确定,被视为可调节参数,一般C会经过计算机软件优化以适应实验数据。常用的表面络合模型计算机软件有FITEQL[11, 21]、PROTOFIT[62]、FIT[60, 63]等,这些计算软件以最小二乘法为基础,可以对实验数据进行拟合和优化,不断调节各种参数下实现计算数据和实验数据拥有较小的误差。
3 可变电荷土壤表面酸碱性质研究方法土壤表面酸碱性质需要通过宏观吸附实验和模型方法进行研究[11]。表面络合模型SCM发展使土壤活性成分金属氧化物、有机物、黏土矿物(图 2a)表面酸碱性质得到较多的研究,获得了丰富的数据[14-15]。自然可变电荷土壤由于组成复杂,表面活性位点多样,增加了模拟计算的复杂性,表面酸碱性质研究相对困难。近年来,组分添加法CA、广义复合法GC(图 2b)逐渐提出,才使得此方向的研究取得重要突破。CA法假设土壤表面酸碱性质主要由其活性组分如铁、铝氧化物和黏土矿物决定,矿物聚合物模型、矿物-有机物模型被建立来模拟可变电荷土壤中矿物和有机物表面质子吸附,而LCD模型将活性组分间的相互作用和离子间的竞争吸附一并考虑在内,获得更为准确的模拟结果。GC法假设土壤所有表面官能团的性质是通用的,可以代表所有组分的平均性质,已从1-site/2-pKa向n-site/n-pKa发展,实现了更好的模拟。

|
图 2 可变电荷土壤的主要活性组分及表面酸碱性质模型 Fig. 2 Main active components and surface acid-base properties models of the tested variable charge soils |
组分添加法又叫机械混合法(表 1),是指为获得复杂土壤的表面酸碱性质,可以通过收集各组分纯净物的表面酸碱性质,并根据各组分含量进行加和计算,主要包括矿物聚合物模型和矿物-有机物聚合物模型。这种方法假定土壤表面是由多个物相表面组成,它们的表面性质可从各自独立的研究中获得。目前已有大量金属氧化物、黏土矿物表面酸碱性质数据,并不断有数据库建立,例如Dzombak和Morel建立的铁氧化物数据库[14],Milne等的腐殖质数据库[15],Brendler等的矿物数据库[64]以及Kosmulski的pHpzc数据库[53]。
|
|
表 1 用于可变电荷土壤酸碱性质研究的模型的特点 Table 1 Characteristics of models for study on acid-base properties of the tested various charge soils |
矿物聚合物模型主要研究土壤矿物表面酸碱性质的加和。Pagnanelli等[25, 49]和Stamberg等[22]用单一矿物的表面可变电荷量及矿物质量分数来模拟矿物混合物表面电荷,即QH(simul)=∑pjQHj,其中pj为矿物的质量分数,QHj为每个矿物的表面电荷。这个模拟足够代表矿物混合的实验趋势,表明矿物聚合物的表面酸碱性质是每个矿物性质的加和。然而,Taubaso等[38]则认为当一个无孔的石英和一个多孔的氧化铝等质量混合时,毫无疑问混合物的表面电荷主要由氧化铝控制,因为表面电荷是一种表面行为,依赖于表面积更合理。所以他们认为混合体系表面电荷密度是各组分表面电荷密度和表面积分数的函数,即σtotal=σafa +σbfb。同时他们提出H2O吸附比表面积较N2吸附比表面积更能体现土壤表面积,因为对于蒙脱石N2很难进入蒙脱石层间[39]。两种方法均是单纯地通过加和来计算聚合物表面酸碱性质,所以也称为线性加和模型LAM(Line Additivity Model)。两种方法虽然拟合计算过程不同,但根据他们的实验结果均表明通过各组分酸碱性质评估混合体系的方法是可行的。拟合好坏的判断,两条滴定曲线直观判断是最简单的,还有回归系数R2、p-level也可以作为判断标准[38]。但最严谨的应是总方差VY=WSOS/DF(加权平方差/自由度)判断标准,如果0.1 < VY < 20,实验数据和计算数据则有较好的拟合[11, 22]。Taubaso等[38]采用除去有机物和无定型铁的土壤以及矿物机械混合物作为样品,通过统计分析,所有的实验曲线和计算曲线均具有较好的相关性,回归系数R2 > 0.95,且P值为0。Stamberg等[22]对7种聚合物以及1种机械混合的酸碱滴定曲线研究,利用Brendler等[64]的数据库里纯净矿物的参数,通过组分添加法得到的混合物的滴定曲线,5个的WSOS/DF在0.1~20范围内,2个在范围外,具有较好的拟合效果。这种方法的拟合好坏,取决于输入参数的可信度和实用性。最好的方法是从给定的混合物中分离出所需矿物,或者找到与给定混合物中矿物相似的矿物。但是常常不能得到所有的数据或者不能保证矿物在混合中能否保持原有的化学性质。
矿物-有机物聚合物模型相对于矿物聚合物模型能更真实描述土壤表面性质,因为有机物分子结构中含有多种官能团,具有多种活性位点和pKa值,表现出丰富的表面性质[65-66]。但研究表明矿物-有机物聚合物模型中离子吸附反应表现出不可加性,这些研究都很好地模拟了各个组分的加和,所以不可加性不可能是模型制定或参数不足的原因[67-68]。Vermeer等[69]认为有机分子在矿物表面的反应对两者表面性质产生很大的改变,可能是造成这种现象的原因。Filius等[66]研究FA和针铁矿的吸附反应时,从其可能存在的上千种表面物种中选用8种进行模拟,然而为了缩减可调节的参数,最后只选择了4种。这种表面物种的限制性使得使得模型缺乏真实性,而对于大分子如胡敏酸(HA),表面物种数量更难以确定。随后,Filius等[70]提出用LCD模型描述有机物在针铁矿上的吸附,LCD模型是非理想竞争吸附模型-杜南(NICA-Donnan)模型和电荷分布-多位点络合(CD-MUSIC)模型的结合。LCD模型已超越了严格相加的概念,对于理解聚合物中矿物和有机物之间复杂作用非常有用。LCD模型能够更精确计算有机物在矿物表面和溶液间的分布,以及被吸附和溶解成分的表面物种,并能将浓度、pH、离子强度、静电作用等因素的影响也考虑在内[71-72]。LCD模型已经成功应用于FA-针铁矿聚合物对H、Pb的吸附[37, 71],HA-针铁矿聚合物对H、磷酸盐的吸附[20, 67],以及自然农田土壤对众多离子的吸附[24]。这些研究将LCD模型结果与线性加和模型(LAM)结果比较,LCD模型能够很好地解释加和结果过低或高的原因。
3.2 广义复合法土壤表面官能团通常太复杂而难以判定,若假设土壤表面官能团是“通用”的,则表面络合模型很容易描述土壤表面质子反应[41, 44]。这种将土壤表面性质均一化的方法叫广义复合法,其由混合物的所有表面积和整体的吸附位点做支撑,所获得参数必须依赖于所用土壤的实验数据(表 1)。
Cheng等[4]和Wang等[3]采用1-site/2-pKa模型模拟中国红壤可变电荷矿物及红壤的表面酸碱反应,根据模型所获得两个pKa,利用pHpzc=1/2(pKa1+pKa2)计算得到pHpzc结果和酸碱电位滴定所得pHpzc一致,说明此模型试用于这种红壤,但没有考虑到溶解等因素对实验的影响。刘文新等[55]研究中国黄土表面酸碱性质时,同样假定黄土表面呈现单一类型表面活性位点且均匀分布。考虑到溶解的硅酸和铝离子可进一步与黄土表面位点反应,所以采用了2-site/2-pKa模型,使用FITEQL软件拟合实验数据,总体方差VY表征的拟合度显示模型能满意地描述黄土表面的酸碱反应结果。Nagy和Kónya [29]认为土壤表面羟基基团由1种两性的≡Al-OH和1种酸性的≡Si-OH组成,建立了2-site/3-pKa模型,并对酸性森林土等多种类型土壤的表面酸碱性质进行了研究。Pagnanelli等[25]在研究河流沉积土中各矿物在质子吸附上的具体贡献时,认为沉积土中白云母、斜绿泥石表面由1种两性和1种酸性位点组成,针铁矿、赤铁矿表面位点为两性,石英表面位点为酸性,包含这些矿物的沉积土应由两性位点和酸性位点组成。以上研究结果列于表 2。
|
|
表 2 各种土壤表面位点模型及表面酸碱性质 Table 2 Surface site models and surface acid-base properties of various soils |
Goldberg等[61, 73]提出一种广义回归模型,使用能够直接测定的化学性质,包括阳离子交换量CEC、表面积SA、有机碳含量OC、无机碳含量IC、铝氧化物含量Al和铁氧化物含量Fe,就可以得出土壤表面络合常数pKa。回归模型方程定义为: logKji(int)= β0+β1(lnCECi)+β2(lnSAi)+ β3(lnOCi)+β4(lnICi)+β5(lnAli)+β6(lnFei)+εi。其中logKji(int)指第j元素的第i个表面络合常数,βi表示经验回归系数,εi表示随机误差。这种广义复合法提供了一种完全独立的评估模型,已广泛应用于多种土壤对质子[26, 61]、硼[61]等物质的吸附反应。Goldberg等[61]在土壤对硼的吸附研究中,认为使用1个位点1个深度的土壤样品来代表整个区域土壤的性质是不合理的。其利用3个采样点的5个深度的土壤样品的化学性质以及质子和硼的吸附常数pKa建立例如适宜的广义回归模型。这种模型能够根据土壤的化学性质和模型方程对3个采样点内所有土壤对硼及质子的吸附做出预测。其中质子化和去质子化络合常数为logK+=7.85-0.102 ln(OC)-0.198ln(IC)-0.622ln(Al);logK-=-11.97 +0.302 ln(OC)+0.0584ln(IC)+ 0.302ln(Al)。模型方程只适合对化学性质范围内的土壤的离子吸附情况进行预测,不适合范围外的外推。对其他位点土壤的研究,需要依靠此种方法建立适宜的回归模型方程。
4 需要关注的科学问题及展望对于土壤表面酸碱性质的研究,是解析土壤酸碱缓冲能力、揭露土壤中包括质子在内众多离子吸附机制的重要工作。对于此研究,有一下几个指的关注的方面:
1)土壤表面位点类型、络合物分子形态(内外层、单多齿、单多核等)是进行可靠建模的基础,现仍多采用FTIR光谱表征土壤表面羟基基团,而Raman光谱[74]和In-Situ ATR-FTIR[75]光谱技术能够进行水溶液条件下的原位吸附测试,可与FTIR光谱互为补充。此外,XPS、XAS技术[16]能够从原子层次给出土壤表面结构信息,包括原子组成、价态、健长、配位数等。
2)宏观酸碱滴定实验在很多情况下难以避免溶解等因素,日益先进的计算机模拟技术则能够从微观层次对黏土矿物表面性质进行分析,且不依赖经验理论和实验数据。Sulpizi等[76]和Liu等[77]利用量子力学模拟黏土矿物和水界面反应时,在土壤矿物酸碱性质研究上取得了新的进展。土壤各成分微观结构的进一步认识,将为宏观分析提供更详细、精准的信息。
3)自然聚合物离子吸附的预测结果相对于合成聚合物准确性较差,主要由于自然系统表征的不确定性。建议加强不确定性、差异性研究,实现不确定性定量。如土壤活性成分含量的测定,它是实现组分加和法预测土壤表面酸碱性质的关键,但土壤成分复杂且多数结晶较差,XRD图谱会发生重叠,定量结果非常差。制备定向片以及Rietveld技术[78]的发展可以提供较为准确的定量结果。
4)在表面络合模型未来研究中需要更广泛的数据库,包括有机物、铁铝氧化物、黏土矿物以及各种母质、化学性质的自然土壤。其中活性成分大量的数据库为实现组分添加更完好的预测提供基础,而土壤数据库包括各地土壤酸碱缓冲能力,可以为当地土壤酸化预测和阻控提供依据[4]。
5)将表面络合模型应用到土壤体系中所有重要离子的吸附研究,以及考虑到在自然体系中它们间的竞争吸附对吸附结果的影响。其中LCD模型是这方面的重大突破,但现在多用于铁矿物和有机质聚合物表面吸附研,在未来要加强LCD模型的研究。
| [1] |
徐仁扣. 土壤酸化及其调控研究进展. 土壤, 2015, 47(2): 238-244. Xu R K. Research progresses in soil acidification and its control (In Chinese). Soils, 2015, 47(2): 238-244. (  0) 0) |
| [2] |
王敬华, 张效年, 于天仁. 华南红壤对酸雨敏感性的研究. 土壤学报, 1994, 31(4): 348-355. Wang J H, Zhang X N, Yu T R. Study on sensitivity of red soils to acid rain in south China (In Chinese). Acta Pedologica Sinica, 1994, 31(4): 348-355. (  0) 0) |
| [3] |
Wang Y, Cheng P, Li F, et al. Variable charges of a red soil from different depths:Acid-base buffer capacity and surface complexation model . Applied Clay Science, 2018, 159: 107-115. DOI:10.1016/j.clay.2017.08.003
(  0) 0) |
| [4] |
Cheng P, Wang Y, Cheng K, et al. The acid-base buffer capacity of red soil variable charge minerals and its surface complexation model . Acta Chimica Sinica, 2017, 75(6): 637-644. DOI:10.6023/A17020056
(  0) 0) |
| [5] |
Adekola F, Fédoroff M, Geckeis H, et al. Characterization of acid–base properties of two gibbsite samples in the context of literature results . Journal of Colloid and Interface Science, 2011, 354(1): 306-317. DOI:10.1016/j.jcis.2010.10.014
(  0) 0) |
| [6] |
Liu T, Li X, Waite T D. Depassivation of aged FeO by divalent cations:Correlation between contaminant degradation and surface complexation constants . Environmental Science & Technology, 2014, 48(24): 14564-14571.
(  0) 0) |
| [7] |
Liu T, Li X, Waite T D. Depassivation of aged FeO by ferrous ions:implications to contaminant degradation . Environmental Science & Technology, 2013, 47(23): 13712-13720.
(  0) 0) |
| [8] |
Liu T, Li X, Waite T D. Depassivation of aged FeO by inorganic salts:Implications to contaminant degradation in seawater . Environmental Science & Technology, 2013, 47(13): 7350-7356.
(  0) 0) |
| [9] |
Liu T, Li X, Zhang W, et al. Fe(Ⅲ)oxides accelerate microbial nitrate reduction and electricity generation by Klebsiella pneumoniae L17 . Journal of Colloid and Interface Science, 2014, 423(6): 25-32.
(  0) 0) |
| [10] |
王代长, 蒋新, 贺纪正, 等. 应用Multi-Langmuir模型评价土壤的表面电荷特性. 土壤学报, 2009, 46(4): 611-616. Wang D C, Jiang X, He J Z, et al. Evaluation of surface charge characteristics of soils using mutl-langmuir model (In Chinese). Acta Pedologica Sinica, 2009, 46(4): 611-616. DOI:10.3321/j.issn:0564-3929.2009.04.007 (  0) 0) |
| [11] |
Goldberg S. Macroscopic experimental and modeling evaluation of selenite and selenate adsorption mechanisms on gibbsite . Soil Science Society of America Journal, 2014, 78(2): 473-479. DOI:10.2136/sssaj2013.06.0249
(  0) 0) |
| [12] |
杨航, 李敏. 表面络合模式在天然体系中的应用研究进展. 环境科学与技术, 2012, 35(S2): 189-193. Yang H, Li M. Advances in research of surface complexation models for natural system (In Chinese). Environmental Science & Technology, 2012, 35(S2): 189-193. (  0) 0) |
| [13] |
Pérez C, Antelo J, Fiol S, et al. Modeling oxyanion adsorption on ferralic soil, part 1:Parameter validation with phosphate ion . Environmental Toxicology and Chemistry, 2014, 33(10): 2208-2216. DOI:10.1002/etc.2612
(  0) 0) |
| [14] |
Dzombak D A, Morel F. Surface complexation modeling: Hydrous ferric oxide. New York: John Wiley and Sons, 1990
(  0) 0) |
| [15] |
Milne C J, Kinniburgh D G, van Riemsdijk W H, et al. Generic NICA - Donnan model parameters for metal-ion binding by humic substances . Environmental Science & Technology, 2003, 37(5): 958-971.
(  0) 0) |
| [16] |
杨敏, 豆小敏, 张昱. 固液吸收机制和模型. 环境科学学报, 2006, 26(10): 1581-1585. Yang M, Dou X M, Zhang Y. Mechanism and models of adsorption process on solid/water interface (In Chinese). Acta Scientiae Circumstantiae, 2006, 26(10): 1581-1585. DOI:10.3321/j.issn:0253-2468.2006.10.001 (  0) 0) |
| [17] |
Mangold J E, Park C M, Liljestrand H M, et al. Surface complexation modeling of Hg(Ⅱ)adsorption at the goethite/water interface using the Charge Distribution Multi-Site Complexation(CD-MUSIC)model . Journal of Colloid and Interface Science, 2014, 418: 147-161. DOI:10.1016/j.jcis.2013.10.066
(  0) 0) |
| [18] |
Xie J, Gu X, Tong F, et al. Surface complexation modeling of Cr(Ⅵ)adsorption at the goethite–water interface . Journal of Colloid and Interface Science, 2015, 455: 55-62. DOI:10.1016/j.jcis.2015.05.041
(  0) 0) |
| [19] |
López R, Gondar D, Antelo J, et al. Study of the acid-base properties of a peat soil and its humin and humic acid fractions . European Journal of Soil Science, 2012, 63(4): 487-494. DOI:10.1111/ejss.2012.63.issue-4
(  0) 0) |
| [20] |
Groenenberg J E, Lofts S. The use of assemblage models to describe trace element partitioning, speciation, and fate:A review . Environmental Toxicology and Chemistry, 2014, 33(10): 2181-2196. DOI:10.1002/etc.2642
(  0) 0) |
| [21] |
Vithanage M, Rajapaksha A U, Dou X, et al. Surface complexation modeling and spectroscopic evidence of antimony adsorption on iron-oxide-rich red earth soils . Journal of Colloid and Interface Science, 2013, 406: 217-224. DOI:10.1016/j.jcis.2013.05.053
(  0) 0) |
| [22] |
Stamberg K, Drtinová B, Filipská H, et al. Modelling of acid-base titration curves of mineral assemblages . Open Chemistry, 2016, 14(1): 316-323.
(  0) 0) |
| [23] |
Borgnino L, Garcia M G, del Hidalgo M V, et al. Modeling the acid-base surface properties of aquatic sediments . Aquatic Geochemistry, 2010, 16(2): 279-291. DOI:10.1007/s10498-009-9079-y
(  0) 0) |
| [24] |
Weng L, Vega F A, van Riemsdijk W H. Competitive and synergistic effects in pH dependent phosphate adsorption in soils:LCD modeling . Environmental Science & Technology, 2011, 45(19): 8420-8428.
(  0) 0) |
| [25] |
Pagnanelli F, Bornoroni L, Toro L. Proton binding onto soil by nonelectrostatic models:Isolation and identification of mineral contributions . Environmental Science & Technology, 2004, 38(20): 5443-5449.
(  0) 0) |
| [26] |
Goldberg S, Lesch S M, Suarez D L. Predicting selenite adsorption by soils using soil chemical parameters in the constant capacitance model . Geochimica et Cosmochimica Acta, 2007, 71(23): 5750-5762. DOI:10.1016/j.gca.2007.04.036
(  0) 0) |
| [27] |
徐仁扣, 季国亮, 王敬华. 我国东部七省(闽、浙、赣、湘、鄂、苏、皖)生态系统对酸沉降的临界负荷的研究1.临界负荷的确定. 土壤, 2000, 32(3): 120-129. Xu R K, Ji G L, Wang J H. Study on the critical load of acid deposition in seven provinces of the eastern China(Fujian, Zhejiang, Jiangxi, Hunan, Hubei, Jiangsu, Anhui)1. Determination of critical load (In Chinese). Soils, 2000, 32(3): 120-129. DOI:10.3321/j.issn:0253-9829.2000.03.002 (  0) 0) |
| [28] |
Zhang F S, Zhang X N, Yu T R. Reactions of hydrogen ions with variable charge soils:I. Mechanisms of reaction . Soil Science, 1991, 151(6): 436-443. DOI:10.1097/00010694-199106000-00005
(  0) 0) |
| [29] |
Nagy N M, Kónya J. Study of pH-dependent charges of soils by surface acid-base properties . Journal of Colloid and Interface Science, 2007, 305(1): 94-100. DOI:10.1016/j.jcis.2006.09.040
(  0) 0) |
| [30] |
Luo C, Xie Y, Li F, et al. Adsorption of arsenate on iron oxides as influenced by humic acids . Journal of Environment Quality, 2015, 44(6): 1729-1737. DOI:10.2134/jeq2014.11.0491
(  0) 0) |
| [31] |
Keizer M G, van Riemsdijk W H. ECOSAT: equilibrium calculation of speciation and transport. Wageningen: Wageningen University, 1994
(  0) 0) |
| [32] |
Ge Y, MacDonald D, Sauvé S, et al. Modeling of Cd and Pb speciation in soil solutions by WinHumicV and NICA-Donnan model . Environmental Modelling & Software, 2005, 20(3): 353-359.
(  0) 0) |
| [33] |
Crawford M B. PHREEQEV:The incorporation of a version of Model V for organic complexation in aqueous solutions into the speciation code PHREEQE . Computers & Geosciences, Elsevier, 1996, 22(2): 109-116.
(  0) 0) |
| [34] |
Meeussen J C L. ORCHESTRA:An object-oriented framework for implementing chemical equilibrium models . Environmental Science & Technology, 2003, 37(6): 1175-1182.
(  0) 0) |
| [35] |
Gu X, Sun J, Evans L J. The development of a multi-surface soil speciation model for Cd(Ⅱ)and Pb(Ⅱ):Comparison of two approaches for metal adsorption to clay fractions . Applied Geochemistry, 2014, 47: 99-108. DOI:10.1016/j.apgeochem.2014.05.014
(  0) 0) |
| [36] |
Janot N, Pinheiro J P, Botero W G, et al. PEST-ORCHESTRA, a tool for optimising advanced ion-binding model parameters:Derivation of NICA-Donnan model parameters for humic substances reactivity . Environmental Chemistry, 2017, 14(1): 31-38.
(  0) 0) |
| [37] |
Xiong J, Koopal L K, Weng L, et al. Effect of soil fulvic and humic acid on binding of Pb to goethite-water interface:Linear additivity and volume fractions of HS in the Stern layer . Journal of Colloid and Interface Science, 2015, 457: 121-130. DOI:10.1016/j.jcis.2015.07.001
(  0) 0) |
| [38] |
Taubaso C, Afonso M D S, Sánchez R M T. Modelling soil surface charge density using mineral composition . Geoderma, 2004, 121(1-2): 123-133. DOI:10.1016/j.geoderma.2003.11.005
(  0) 0) |
| [39] |
Sposito G. The surface chemistry of soils . Oxford: Oxford University Press, 1984.
(  0) 0) |
| [40] |
吕海波, 钱立义, 常红帅, 等. 黏性土几种比表面积测试方法的比较. 岩土工程学报, 2016, 38(1): 124-130. Lü H B, Qian L Y, Chang H S, et al. Comparison of several methods for determining specific surface area of clayey soils (In Chinese). Chines Journal of Geotechnical Engineering, 2016, 38(1): 124-130. (  0) 0) |
| [41] |
Goldberg S. Application of surface complexation models to anion adsorption by natural materials . Environmental Toxicology and Chemistry, 2014, 33(10): 2172-2180. DOI:10.1002/etc.2566
(  0) 0) |
| [42] |
Hegyesi N, Vad R T, Pukánszky B. Determination of the specific surface area of layered silicates by methylene blue adsorption:The role of structure, pH and layer charge . Applied Clay Science, 2017, 146: 50-55. DOI:10.1016/j.clay.2017.05.007
(  0) 0) |
| [43] |
Groups S F. Surface chemistry and colloidal stability//The iron oxides. Weinheim, FRG: Wiley-VCH Verlag GmbH & Co. KGaA, 2003: 221-252
(  0) 0) |
| [44] |
Davis J A, Coston J A, Kent D B, et al. Application of the surface complexation concept to complex mineral assemblages . Environmental Science & Technology, 1998, 32(19): 2820-2828.
(  0) 0) |
| [45] |
Gran G. Determination of the equivalent point in potentiometric titrations . Acta Chemica Scandinavica, 1950, 4: 559-577. DOI:10.3891/acta.chem.scand.04-0559
(  0) 0) |
| [46] |
Jolsterå R, Gunneriusson L, Forsling W. Adsorption and surface complex modeling of silicates on maghemite in aqueous suspensions . Journal of Colloid and Interface Science, 2010, 342(2): 493-498. DOI:10.1016/j.jcis.2009.10.080
(  0) 0) |
| [47] |
Frini-Srasra N, Kriaa A, Srasra E. Acid-base properties of Tunisian palygorskite in aqueous medium . Russian Journal of Electrochemistry, 2007, 43(7): 795-802. DOI:10.1134/S1023193507070099
(  0) 0) |
| [48] |
吴震生, 张卫民, 孙中溪, 等. 介孔α-Fe2O3表面配合反应平衡常数测定. 化学学报, 2010, 68(8): 769-774. Wu Z S, Zhang W M, Sun Z X, et al. Surface complexation constants of mesoporous Fe2O3 (In Chinese). Acta Chimica Sinica, 2010, 68(8): 769-774. (  0) 0) |
| [49] |
Pagnanelli F, Bornoroni L, Moscardini E, et al. Non-electrostatic surface complexation models for protons and lead(Ⅱ)sorption onto single minerals and their mixture . Chemosphere, 2006, 63(7): 1063-1073. DOI:10.1016/j.chemosphere.2005.09.017
(  0) 0) |
| [50] |
Davranche M, Lacour S, Bordas F, et al. An easy determination of the surface chemical properties of simple and natural solids . Journal of Chemical Education, 2003, 80(1): 76-78. DOI:10.1021/ed080p76
(  0) 0) |
| [51] |
Davis J A, Kent D B. Surface complexation modeling in aqueous geochemistry . Reviews in Mineralogy, 1990, 23(1): 177-260.
(  0) 0) |
| [52] |
Parks G A. The isoelectric points of solid oxides, solid hydroxides, and aqueous hydroxo complex systems . Chemical Reviews, 1965, 65(2): 177-198.
(  0) 0) |
| [53] |
Kosmulski M. The pH-dependent surface charging and points of zero charge . Journal of Colloid and Interface Science, 2011, 353(1): 1-15. DOI:10.1016/j.jcis.2010.08.023
(  0) 0) |
| [54] |
Tournassat C, Davis J A, Chiaberge C, et al. Modeling the acid-base properties of montmorillonite edge surfaces . Environmental Science & Technology, 2016, 50(24): 13436-13445.
(  0) 0) |
| [55] |
刘文新, 储昭升, 汤鸿霄, 等. 黄土表面酸碱性质的研究. 环境科学学报, 2003, 23(1): 6-10. Liu W X, Chu Z S, Tang H X, et al. Study on surface acid-base properties of Chinese loess (In Chinese). Acta Scientiae Circumstantiae, 2003, 23(1): 6-10. (  0) 0) |
| [56] |
Szekeres M, Tombácz E. Surface charge characterization of metal oxides by potentiometric acid-base titration, revisited theory and experiment . Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2012, 414: 302-313.
(  0) 0) |
| [57] |
Gu X, Xie J, Wang X, Wang X R, et al. A simple model to predict chromate partitioning in selected soils from China . Journal of Hazardous Materials, 2017, 322: 421-429. DOI:10.1016/j.jhazmat.2016.10.033
(  0) 0) |
| [58] |
Kaiser K, Guggenberger G. Mineral surfaces and soil organic matter . European Journal of Soil Science, 2003, 54(2): 219-236.
(  0) 0) |
| [59] |
Stumm W. Chemistry of the solid-water interface: processes at the mineral-water and particle-water interface in natural systems. John Wiley & Son Inc, 1992
(  0) 0) |
| [60] |
Tan W, Xiong J, Li Y, et al. Proton binding to soil humic and fulvic acids:Experiments and NICA-Donnan modeling . Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2013, 436: 1152-1158. DOI:10.1016/j.colsurfa.2013.08.010
(  0) 0) |
| [61] |
Goldberg S, Suarez D L, Basta N T, et al. Predicting boron adsorption isotherms by midwestern soils using the constant capacitance model . Soil Science Society of America Journal, 2004, 68(3): 795-801. DOI:10.2136/sssaj2004.7950
(  0) 0) |
| [62] |
Turner B F, Fein J B. Protofit:A program for determining surface protonation constants from titration data . Computers & Geosciences, 2006, 32(9): 1344-1356.
(  0) 0) |
| [63] |
Kinniburgh D G. Technical report WD/93/23: FIT user guide. British Geological Survey, 1993
(  0) 0) |
| [64] |
Brendler V, Vahle A, Arnold T, et al. RES3T-Rossendorf expert system for surface and sorption thermodynamics . Journal of Contaminant Hydrology, 2003, 61(1-4): 281-291. DOI:10.1016/S0169-7722(02)00129-8
(  0) 0) |
| [65] |
Hruška J, Köhler S, Laudon H, et al. Is a universal model of organic acidity possible:Comparison of the acid/base properties of dissolved organic carbon in the boreal and temperate zones . Environmental Science & Technology, 2003, 37(9): 1726-1730.
(  0) 0) |
| [66] |
Filius J D, Lumsdon D G, Meeussen J C L, et al. Adsorption of fulvic acid on goethite . Geochimica et Cosmochimica Acta, 2000, 64(1): 51-60. DOI:10.1016/S0016-7037(99)00176-3
(  0) 0) |
| [67] |
Weng L, van Riemsdijk W H, Hiemstra T. Effects of fulvic and humic acids on arsenate adsorption to goethite:Experiments and modeling . Environmental Science & Technology, 2009, 43(19): 7198-7204.
(  0) 0) |
| [68] |
Weng L, van Riemsdijk W H, Hiemstra T. Humic nanoparticles at the oxide-water interface:Interactions with phosphate ion adsorption . Environmental Science & Technology, 2008, 42(23): 8747-8752.
(  0) 0) |
| [69] |
Vermeer A W, McCulloch J K, van Riemsdijk W H, et al. Metal ion adsorption to complexes of humic acid and metaloxides :Deviations from the additivity rule . Environmental Science & Technology, 1999, 33(21): 3892-3897.
(  0) 0) |
| [70] |
Filius J D, Meeussen J C L, Lumsdon D G, et al. Modeling the binding of fulvic acid by goethite:The speciation of adsorbed FA molecules . Geochimica et Cosmochimica Acta, 2003, 67(8): 1463-1474. DOI:10.1016/S0016-7037(02)01042-6
(  0) 0) |
| [71] |
Ye Y, Chen Z, Montavon G, et al. Surface complexation modeling of Eu(Ⅲ)adsorption on silica in the presence of fulvic acid . Science China Chemistry, 2014, 57(9): 1276-1282. DOI:10.1007/s11426-014-5120-0
(  0) 0) |
| [72] |
Cui Y, Weng L. Arsenate and phosphate adsorption in relation to oxides composition in soils:LCD Modeling . Environmental Science & Technology, 2013, 47(13): 7269-7276.
(  0) 0) |
| [73] |
Goldberg S, Lesch S M, Suarez D L, et al. Predicting arsenate adsorption by soils using soil chemical parameters in the constant capacitance model . Soil Science Society of America Journal, 2005, 69(5): 1389-1398. DOI:10.2136/sssaj2004.0393
(  0) 0) |
| [74] |
Djomgoue P, Njopwouo D. FT-IR spectroscopy applied for surface clays characterization . Journal of Surface Engineered Materials and Advanced Technology, 2013, 3(4): 275-282. DOI:10.4236/jsemat.2013.34037
(  0) 0) |
| [75] |
Hong Z N, Li J Y, Jiang J, et al. Competition between bacteria and phosphate for adsorption sites on gibbsite:An in-situ ATR-FTIR spectroscopic and macroscopic study . Colloids & Surfaces B Biointerfaces, 2016, 148: 496-502.
(  0) 0) |
| [76] |
Sulpizi M, Gaigeot M P, Sprik M. The silica-water interface:How the silanols determine the surface acidity and modulate the water properties . Journal of Chemical Theory and Computation, 2012, 8(3): 1037-1047. DOI:10.1021/ct2007154
(  0) 0) |
| [77] |
Liu X, Cheng J, Sprik M, et al. Surface acidity of 2:1-type dioctahedral clay minerals from first principles molecular dynamics simulations . Geochimica et Cosmochimica Acta, 2014, 140: 410-417. DOI:10.1016/j.gca.2014.05.044
(  0) 0) |
| [78] |
Prandel L V, Saab S C, Brinatti A M, et al. Mineralogical analysis of clays in hardsetting soil horizons, by X-ray fluorescence and X-ray diffraction using Rietveld method . Radiation Physics and Chemistry, 2014, 95: 65-68. DOI:10.1016/j.radphyschem.2012.12.017
(  0) 0) |
2. School of Chemistry and Materials Science, Guizhou Normal University, Guiyang 550001, China
 2019, Vol. 56
2019, Vol. 56


