2. 土壤与农业可持续发展国家重点实验室(中国科学院南京土壤研究所),南京 210008;
3. 中国科学院大学,北京 100049
土壤结构对氮素的周转起着重要的作用[1]。土壤团聚体的破碎和团聚过程通常伴随着土壤有机氮的矿化和累积。土壤孔隙的数量、大小和形态等直接影响着水分、空气的运动以及土壤微生物的活动[2],孔隙结构的变化对土壤氮素周转过程也具有重要影响。有研究发现,土体经过不同方式扰动后,产生的氮矿化量高于原土体[3-5]。但也有一些研究报道土体扰动后产生的氮矿化量并无显著增加[6-7]。搅浆是稻田耕作的重要方式,这个过程会改变土壤的团聚体和孔隙结构,进而可能影响氮转化过程。但是,有关水稻土结构改变对有机氮矿化的影响尚不明确。
由于研究方法的限制,对水稻土结构进行研究比较困难[8]。近年来,高分辨率X射线计算机断层扫描(CT)技术快速发展,可以快速、定量地分析土壤内部三维结构[9-11]。本研究通过室内搅动模拟稻田打浆,利用显微CT技术和常规分析方法,研究水稻土经搅拌后的孔隙形态和团聚体分布与有机氮矿化的关系,旨在探明土壤结构对稻田土壤供氮能力的影响,为稻田科学耕作提供理论依据。
1 材料与方法 1.1 供试材料供试土壤采自中国科学院常熟农业生态试验站宜兴基地。于2016年5月作物收获后采集稻田表层土壤(0~15 cm)。土样在室温下风干,挑去细根后过5 mm筛。供试土壤为湖白土型水稻土。砂粒(0.2~0.02 mm)、粉粒(0.02~0.002 mm)、黏粒(< 0.002 mm)的含量分别为83 g·kg-1、815 g·kg-1和102 g·kg-1。有机质、全氮含量分别为15.4 g·kg-1和1.79 g·kg-1,pH为6.05,阳离子交换量为10.65 cmol·kg-1。
1.2 试验设计在室内用搅拌器模拟稻田土壤搅浆,设置不搅动(CK)、低强度搅动(LIS,200 r·min-1,搅动3 min)和高强度搅动(HIS,200 r·min-1,搅动10 min)3个处理。由于培养试验采用的土柱(高7 cm,内径2.2 cm,聚氯乙烯(PVC)材质)较小,不能在其中开展搅浆操作,所以先在大土柱(高19.5 cm,内径15 cm,PVC材质)内搅浆,然后在其中采集小土柱样品用于后期试验。详细过程如下:首先将过5 mm筛的风干土样填装于3个大土柱中(每个大土柱填装1 700 g,土壤高度约为8 cm),然后加水浸泡48 h。之后开始搅拌处理,其中1个大土柱不搅动(CK),另外2个大土柱用数显电动搅拌器搅动土壤,搅拌器转速为200 r·min-1,搅动时间分别为3 min(LIS处理)和10 min (HIS处理)。搅动结束后将大土柱置于沙箱上平衡(-10 cm水势)24 h。然后用小土柱采集大土柱内原状土样,采样深度为0~4.5 cm,每个大土柱内采集15个小土柱样品。采样后迅速用保鲜膜包裹小土柱防止水分蒸发。每个处理随机选3个小土柱进行CT扫描,另外12个小土柱用于培养法测定矿化量(具体方法见下文)。培养期间4次取样,每次取3个重复。大土柱内剩余土样用于团聚体分布、含水量和初始无机氮含量的测定。
土壤有机氮矿化培养:采用改进的Waring和Bremner[12]连续淹水密闭法。将原状小土柱装入50 mL离心管中,管中加入25 mL的蒸馏水,使水层淹没土层3 cm左右,拧好盖子,随机排列,于25 ℃恒温培养28 d,每处理三次重复。于培养后7 d、14 d、21 d和28 d取样,将离心管中的水和小土柱中土一并转入150 mL三角瓶中,用75 mL 2.68 mol·L-1的KCl冲洗离心管3次,150 r·min-1震荡40 min,过滤,收集上清液,测定培养后的无机氮(铵态氮和硝态氮)。
1.3 CT扫描与图形处理利用X射线显微CT(NanotomS,GE,Sensing and Inspection Technologies, GmbH, Wunstorf,德国)扫描原状小土柱。电压110 kV,电流110 µA,曝光时间1.25 s。将小土柱固定于样品台上,从0到360°匀速旋转,在此过程中采集1 200幅投影图像。然后利用Datosx2 Rec软件进行图像重建,再利用VG Studio Max2.2软件生成2 302张8位灰度图像(分辨率为0.013 mm),存储为tiff格式。利用ImageJ软件进行图像处理。为了避免采样过程对样品边缘的影响,仅选择三维图像中部的800×800×800体元作为感兴趣区域(Region of interest, ROI),ROI实际大小为10.4 mm×10.4 mm×10.4 mm。利用目视法进行图像分割。图像二值化后,土柱孔隙结构的三维可视化通过ImageJ软件的3Dviewer插件实现。利用Quantim软件(www.quantim.ufz.de)分析土壤孔隙结构特征,包括孔隙度、孔隙大小分布和连通性。其中,孔隙度为孔隙所占体素图像数量与样品大小的比例,孔隙大小分布利用数学形态学的开运算(Opening)来获取。孔隙系统的连通性采用欧拉值(Euler number)来表示,欧拉值越小则孔隙连通性越高。
1.4 测定项目及方法团聚体分级采用改进的Le Bissonnais[13]方法进行测定。室温下,称取25 g土样于蒸发皿中用95%酒精浸泡10 min,然后转移至套筛上,自上而下筛子孔径分别为1.0 mm、0.25 mm、0.053 mm。套筛上下振动每分钟20次(振幅为2 cm),震荡2 min。收集各级土筛上的土壤,获得大于1 mm、1~0.25 mm和0.25~0.053 mm的水稳性团聚体,小于0.053 mm的团聚体通过沉降法收集。将各级筛上团聚体全部冲洗至已知质量的铝盒中,40 ℃干燥箱中干燥,称重,准确至0.01 g。每个样品重复三次。根据各级团聚体所占比例计算平均重量直径(Mean weight diameter,MWD):
| $ {\rm{MWD}} = \sum\limits_{i = 1}^{i = n} {\frac{{{r_{i - 1}} + {r_i}}}{2}} \times {m_i} $ | (1) |
式中,n为筛子的个数; ri为第i个筛子孔径,mm; ri-1为第i-1个筛子孔径,mm; mi为第i个筛子的团聚体重量所占比例,%。
土壤全氮、无机氮(铵态氮和硝态氮)分别采用微量凯氏法和连续流动分析仪(AA3,德国布朗卢比公司)测定。
有机氮矿化模型是由Stanford和Smith[14]通过长期间歇淋洗培养法获得的,用来描述累积矿化氮量与时间关系的模型,其积分形式为
| $ {N_t} = {{\rm{N}}_0}\left( {1 - {{\rm{e}}^{ - {{\rm{k}}_0}t}}} \right) $ | (2) |
式中,t为培养天数,d; Nt为培养t d后的累积矿化氮量,g·kg-1; N0为土壤氮素矿化势,是指一定条件下土壤中易矿化的有机态氮数量的最大值,用来表示土壤供氮潜力; k0为一阶相对矿化速率常数,d-1[15],表示单位时间内矿化氮量占土壤可矿化氮量总量的比值,是衡量土壤中有机氮矿化快慢的参数。
1.5 数据处理利用SPSS19.0对数据进行统计分析。数据处理间差异采用单因素方差分析(One-way ANOVA),并用最小差异显著(LSD)法进行多重比较,显著性水平为5%。相关分析采用皮尔森(Pearson)双侧检验法。
2 结果 2.1 搅拌对团聚体分布的影响搅拌处理显著降低土壤的大团聚体数量和平均重量直径MWD(表 1)。与CK处理相比,LIS处理中大于1 mm大团聚体含量降低60.6%(P < 0.05)、1~0.25 mm团聚体含量降低5.3%(P > 0.05),0.25~0.053 mm和小于0.053 mm的微团聚体含量分别增加了12.4%和4.4%;HIS处理中大于1 mm大团聚体含量降低74.7%(P < 0.05)、1~0.25 mm团聚体含量降低7.9%(P > 0.05),0.25~0.053 mm和小于0.053 mm的微团聚体含量分别增加2.6%和12.8%。CK处理的MWD值分别为LIS和HIS处理的1.8倍和2.2倍。
|
|
表 1 搅动对水稳性团聚体分布的影响 Table 1 Effects of stirring on size distribution of water stable aggregates |
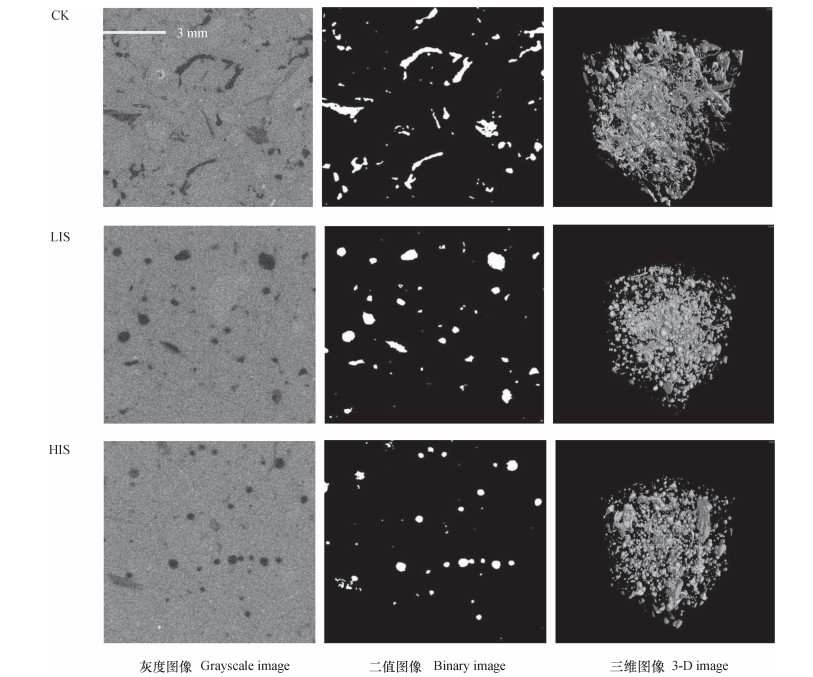
图 1为不同处理的二维灰度图像、二值图像和三维孔隙结构图像。灰度图中浅色部分为土壤基质,深色部分为土壤孔隙; 二值图像中白色部分代表孔隙,黑色部分代表土壤基质。由于分辨率的限制,从图像中获取的孔隙均为大于图像分辨率的孔隙。从灰度图中可以看出,CK处理的大孔隙数量较多,孔隙多呈长条状,孔隙的连通性较好。与CK处理相比,LIS和HIS两处理土壤孔隙主要为圆形孔隙,孔隙呈孤立分散状,连通性较差。三维图像进一步显示,CK处理条状大孔隙多,孔隙之间连通性高,而搅动处理(LIS和HIS处理)孔隙多为离散球状孔隙,连通性明显降低。
|
图 1 搅动对水稻土二维(10.4×10.4 mm)和三维(10.4×10.4×10.4 mm)结构的影响 Fig. 1 Effects of stirring on 2-D(10.4×10.4 mm) and 3-D(10.4×10.4×10.4 mm) structure of paddy soil |
孔隙大小分布如图 2所示,CK、LIS和HIS处理的累积孔隙度分别为3.32%、3.23%和3.26%,处理间差异不显著。由孔隙分布图可见,CK处理在当量孔径为130 μm时孔隙度最高,显著高于其他处理。当孔隙当量直径大于311 μm时,CK处理的各粒级孔隙度均低于LIS和HIS两处理。LIS和HIS处理的变化趋势大体一致。与CK相比,LIS和HIS提高了当量直径大于311 μm的大孔径孔隙度。

|
图 2 搅动对水稻土累积孔隙度和孔隙大小分布的影响 Fig. 2 Effects of stirring on cumulative porosity and pore size distribution in paddy soil |
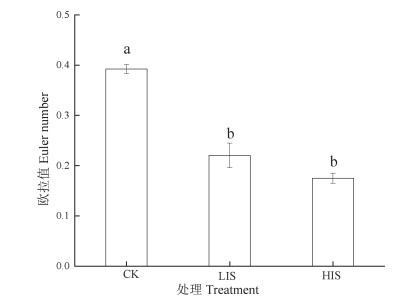
欧拉值是表征孔隙连通性的参数,但是在图像处理过程中,小孔隙的数量会受到分割和滤波等过程的影响,进而对欧拉值的计算产生很大的干扰,导致不能反映孔隙结构的实际连通性。因此,本研究仅针对直径大于200 μm的孔隙进行分析,结果如图 3所示,欧拉值指标与孔隙形态观察的结果一致,LIS和HIS处理欧拉值显著高于CK处理,说明搅拌降低了孔隙的连通性。CK处理的孔隙连通性最高,更有利于水分和气体的传输。
|
图 3 孔径200 μm处的欧拉值 Fig. 3 Euler number at 200 μm pore size |
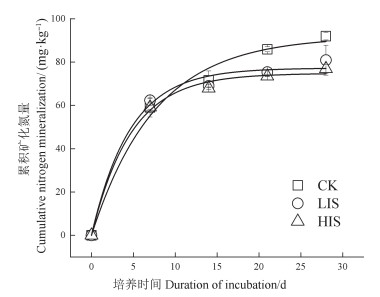
在培养第一周时,LIS和HIS处理的矿化氮量稍高于CK处理,但是差异不显著(图 4),随着培养时间延长,CK处理矿化量增加速率高于搅拌处理,至第三周,CK处理的累积矿化氮量显著高于搅拌处理(P < 0.05)。培养结束时,CK处理较LIS和HIS处理累积矿化量分别高13.7%和19.9%。
|
图 4 搅动对水稻土累积矿化氮量的影响 Fig. 4 Effects of stirring on cumulative nitrogen mineralization in paddy soil |
利用一级动力学方程,采用最小二乘法拟合了培养时间与累积矿化氮量的关系,决定系数均在0.98以上(表 2)。与CK处理相比,LIS和HIS处理的N0分别降低15.9%和18.6%(P < 0.05)。CK处理的N0/N值显著高于LIS和HIS处理(P < 0.05),LIS和HIS处理间差异不显著。矿化速率常数K0的变化范围在0.217~0.131 d-1之间,处理间差异不显著。
|
|
表 2 搅拌后土壤有机氮矿化的一级动力学参数及N0/N Table 2 Parameters of the first-order kinetics and N0/N values of soil organic nitrogen mineralization after stirring |
相关分析表明(表 3),土壤的氮矿化势N0与粒径大于0.25 mm的团聚体(A > 0.25)、当量孔径小于30 μm(P < 30)和30~100 μm(P30~100)的土壤孔隙数量呈极显著正相关(P < 0.01);土壤的累积矿化氮量(N28)与当量直径在30~100 μm(P30~100)的孔隙数量呈极显著正相关(P < 0.01)。
|
|
表 3 土壤团聚体和孔隙大小分布与氮矿化参数的相关性 Table 3 Correlation coefficients of soil mineralization parameters with aggregate size distribution and pore size distribution |
稻田搅浆会改变土壤团聚体的组成和稳定性,进而对土壤有效养分的供应产生影响。本研究中湿筛后大于0.25 mm大团聚体数量与有机氮矿化潜势N0和N0/Nt均成极显著正相关(P < 0.01),小于0.25 mm小团聚体数量与之成极显著负相关(P < 0.01),可见土壤的氮矿化能力确实受团聚体粒级分布的影响[16]。有研究[17]发现,土壤经搅动后前期矿化氮量高于未搅动土壤,本研究中经搅动后的土壤在培养一周内的矿化氮也表现出增加趋势(图 4),这可能是由于在搅动过程中,土壤中大团聚体会被破碎,包裹在团聚体内部的易矿化有机氮暴露于土壤环境中,进而被微生物矿化[18],导致短暂的矿化氮量提升。另一方面,搅动降低了水稻土的累积矿化氮量,这与Kristensen等[7]的研究结果一致。搅动虽然增加了微团聚体数量,但是微团聚体中的碳氮比较稳定[19],未引起累积矿化氮量的增加。
土壤孔隙的分布情况也影响着土壤的水分和空气流通能力,进而影响有机氮的矿化过程[20-22]。本研究中CK、LIS和HIS处理的孔隙度相差不明显,但孔隙大小分布有明显不同(图 2)。LIS和HIS处理在搅拌之后,土壤中原有的条状孔隙变成球状,呈离散分布,连通性显著降低(图 1),这种封闭式孔隙中水流和空气均难以进入,使微生物对有机氮进行分解矿化的速率降低[23]。而CK处理中连通性大孔隙的存在,能更多运输氧气,水气条件能更好地满足好氧微生物生长[24],促进有机氮的矿化分解。因此,CK处理累积氮矿化量相对较高。
此外,有研究发现,15~60 μm的孔隙可能对有机质保护作用最差[25],而这一范围内微生物丰度最高,活性最强[26-28]。本研究中,CK处理的30~100 μm孔隙数量显著高于LIS和HIS处理,且与N28、N0和N0/N均呈极显著正相关(P < 0.01),而大于100 μm孔隙的数量与各矿化参数均无显著相关性。由此可见,在本研究中30~100 μm孔隙可能更利于微生物活动,进而增加有机氮矿化。
本研究证实,搅拌过程确实通过改变土壤团聚体分布和孔隙结构,影响有机氮的矿化过程。但根据本研究结果,尚不能得出土壤中哪种结构因素(土壤团聚体和孔隙)主导有机氮的矿化。今后需要深入研究团聚体和孔隙结构的改变对有机氮矿化相关土壤微生物群体的作用,进一步揭示搅拌过程对土壤氮素转化过程的影响。
4 结论稻田土壤经搅动后,大团聚体数量减少,小团聚体数量增加。土壤孔隙结构改变,条状大孔隙消失,产生很多圆形气泡状孔隙,孔隙连通性显著降低。搅动处理降低了累积矿化氮量。大团聚体(大于0.25 mm)数量与N0、N0/N均呈极显著正相关关系; 当量直径在30~100 μm内的孔隙数量与N0、N28也呈极显著正相关关系。本研究中,团聚体与孔隙结构同时发生变化,尚不能区分它们在氮矿化过程中的作用,有待进一步研究。
| [1] |
Ladd J N, Foster R C, Skjemstad J O. Soil structure:Carbon and nitrogen metabolism . Geoderma, 1993, 56(1): 401-434.
(  0) 0) |
| [2] |
Dexter A R. Advances in characterization of soil structure . Soil & Tillage Research, 1988, 11(3): 199-238.
(  0) 0) |
| [3] |
Moberg D P, Johnson R L, Sullivan D M. Comparison of disturbed and undisturbed soil core methods to estimate nitrogen-mineralization rates in manured agricultural soils . Communications in Soil Science and Plant Analysis, 2013, 44(11): 1722-1732. DOI:10.1080/00103624.2013.783060
(  0) 0) |
| [4] |
Balesdent J, Chenu C, Balabane M. Relationship of soil organic matter dynamics to physical protection and tillage . Soil & Tillage Research, 2000, 53(3): 215-230.
(  0) 0) |
| [5] |
Dharmakeerthi R S, Kay B D, Beauchamp E G. Effect of soil disturbance on N availability across a variable landscape in southern Ontario . Soil & Tillage Research, 2004, 79(1): 101-112.
(  0) 0) |
| [6] |
Curtin D, Beare M H, Scott C L, et al. Mineralization of soil carbon and nitrogen following physical disturbance:A laboratory assessment . Soil Science Society of America Journal, 2014, 78(3): 925-935. DOI:10.2136/sssaj2013.12.0510
(  0) 0) |
| [7] |
Kristensen H L, Mccarty G W, Meisinger J J. Effects of soil structure disturbance on mineralization of organic soil nitrogen . Soil Science Society of America Journal, 2000, 64(1): 371-378. DOI:10.2136/sssaj2000.641371x
(  0) 0) |
| [8] |
李文昭, 周虎, 陈效民, 等. 基于同步辐射显微CT研究不同施肥措施下水稻土团聚体微结构特征. 土壤学报, 2014, 51(1): 67-74. Li W Z, Zhou H, Chen X M, et al. Characterization of aggregate microstructures of paddy soils under different patterns of fertilization with synchrotron radiation micro-CT (In Chinese). Acta Pedologica Sinica, 2014, 51(1): 67-74. (  0) 0) |
| [9] |
周虎, 李文昭, 张中彬, 等. 利用X射线CT研究多尺度土壤结构. 土壤学报, 2013, 50(6): 1226-1230. Zhou H, Li W Z, Zhang Z B, et al. Characterization of multi-scale soil structure with X-ray computed tomography (In Chinese). Acta Pedologica Sinica, 2013, 50(6): 1226-1230. (  0) 0) |
| [10] |
房焕, 李奕, 周虎, 等. 稻麦轮作区秸秆还田对水稻土结构的影响. 农业机械学报, 2018, 49(4): 297-302. Fang H, Li Y, Zhou H, et al. Effects of straw incorporation on paddy soil structure in rice-wheat rotation system (In Chinese). Transactions of the Chinese Society of Agricultural Machinery, 2018, 49(4): 297-302. (  0) 0) |
| [11] |
姜宇, 刘博, 范昊明, 等. 冻融条件下黑土大孔隙结构特征研究. 土壤学报, 2019, 56(2): 340-349. Jiang Y, Liu B, Fan H M, et al. Macropore structure characteristics of black soil under freeze-thaw condition (In Chinese). Acta Pedologica Sinica, 2019, 56(2): 340-349. (  0) 0) |
| [12] |
Waring S A, Bremner J M. Ammonium production in soil under waterlogged conditions as an index of nitrogen availability . Nature, 1964, 201(492): 951.
(  0) 0) |
| [13] |
Le Bissonnais Y. Aggregate stability and assessment of soil crustability and erodibility :Ⅰ. Theory and methodology . European Journal of Soil Science, 2016, 67(1): 11-21. DOI:10.1111/ejss.4_12311
(  0) 0) |
| [14] |
Stanford G, Smith S J. Nitrogen mineralization potentials of soils . Soil Science Society of America Journal, 1972, 36(3): 465-472. DOI:10.2136/sssaj1972.03615995003600030029x
(  0) 0) |
| [15] |
丛耀辉, 张玉玲, 张玉龙, 等. 黑土区水稻土有机氮组分及其对可矿化氮的贡献. 土壤学报, 2016, 53(2): 457-467. Cong Y H, Zhang Y L, Zhang Y L, et al. Soil organic nitrogen components and their contributions to mineralizable nitrogen in paddy soil of the black soil region (In Chinese). Acta Pedologica Sinica, 2016, 53(2): 457-467. (  0) 0) |
| [16] |
刘玮, 蒋先军. 耕作方式对土壤不同粒径团聚体氮素矿化的影响. 土壤, 2013, 45(3): 464-469. Liu W, Jiang X J. Effects of tillage on nitrogen mineralization in aggregate-size fractions of subtropical rice soil (In Chinese). Soils, 2013, 45(3): 464-469. DOI:10.3969/j.issn.0253-9829.2013.03.013 (  0) 0) |
| [17] |
Hassink J. Effects of soil texture and structure on carbon and nitrogen mineralization in grassland soils . Biology and Fertility of Soils, 1992, 14(2): 126-134. DOI:10.1007/BF00336262
(  0) 0) |
| [18] |
Marinari S, Lagomarsino A, Moscatelli M C, et al. Soil carbon and nitrogen mineralization kinetics in organic and conventional three-year cropping systems . Soil & Tillage Research, 2010, 109(2): 161-168.
(  0) 0) |
| [19] |
Puget P, Chenu C, Balesdent J. Dynamics of soil organic matter associated with particle-size fractions of water-stable aggregates . European Journal of Soil Science, 2000, 51(4): 595-605. DOI:10.1111/j.1365-2389.2000.00353.x
(  0) 0) |
| [20] |
Calderon F J, Jackson L E, Scow K M, et al. Short-term dynamics of nitrogen, microbial activity, and phospholipid fatty acids after tillage . Soil Science Society of America Journal, 2001, 65(1): 118-126. DOI:10.2136/sssaj2001.651118x
(  0) 0) |
| [21] |
窦森, 王帅. 不同微生物对形成不同腐殖质组分的差异性研究进展. 吉林农业大学学报, 2011, 33(2): 119-125. Dou S, Wang S. Review of different microorganisms effect on humus formation (In Chinese). Journal of Jilin Agricultural University, 2011, 33(2): 119-125. (  0) 0) |
| [22] |
Neve S D, Hartmann R, Hofman G. Temperature effects on N mineralization:Changes in soil solution composition and determination of temperature coefficients by TDR . European Journal of Soil Science, 2010, 54(1): 49-62.
(  0) 0) |
| [23] |
Young I M, Crawford J W, Nunan N, et al. Microbial distribution in soils:Physics and scaling . Advances in Agronomy, 2007, 100: 81-121.
(  0) 0) |
| [24] |
Kravchenko A N, Toosi E R, Guber A K, et al. Hotspots of soil N2O emission enhanced through water absorption by plant residue . Nature Geoscience, 2017, 10(7): 496-500. DOI:10.1038/ngeo2963
(  0) 0) |
| [25] |
Kravchenko A N, Negassa W C, Guber A K, et al. Protection of soil carbon within macro-aggregates depends on intra-aggregate pore characteristics . Scientific Reports, 2015(5): 16261.
(  0) 0) |
| [26] |
Kravchenko A N, Negassa W C, Guber A K, et al. Intra-aggregate pore structure influences phylogenetic composition of bacterial community in macroaggregates . Soil Science Society of America Journal, 2014, 78(6): 1924-1939. DOI:10.2136/sssaj2014.07.0308
(  0) 0) |
| [27] |
Ananyeva K, Wang W, Smucker A J M, et al. Can intra-aggregate pore structures affect the aggregate's effectiveness in protecting carbon? . Soil Biology & Biochemistry, 2013, 57(23): 868-875.
(  0) 0) |
| [28] |
Strong D T, Wever H D, Merckx R, et al. Spatial location of carbon decomposition in the soil pore system . European Journal of Soil Science, 2004, 55(4): 739-750. DOI:10.1111/j.1365-2389.2004.00639.x
(  0) 0) |
2. State Key Lab of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China
 2019, Vol. 56
2019, Vol. 56


