2. 昆明理工大学云南省食品安全研究院, 昆明 650500;
3. 云南省土壤固碳与污染控制重点实验室, 昆明 650500
腐殖酸是普遍存在于水体、土壤和沉积物中的一类天然有机质,极大地控制了污染物的迁移、转化和归趋等环境地球化学行为[1-3]。腐殖酸的结构和性质直接影响了土壤结构[4-5]、土壤生物活性[6]等土壤特性。然而,由于腐殖酸结构复杂、性质多样[7-8],目前对其分子结构和成分的研究仍未有定论。传统理论认为,腐殖酸是由带有官能团的芳香族和脂肪族通过共价键连接构成[9]。Engebretson和von Wandruszka[10]认为腐殖酸是可电解的聚合大分子。Piccolo等[9]在初期研究腐殖酸结构时,认为其是二级化学结构通过共价键结合而形成的大分子。Peuravuori等[11]通过固相核磁共振及热解试验,证明腐殖酸是由上百的碳水化合物及其含氮衍生物、多肽和连有羟基、羧基及甲氧基的脂肪族和芳香族有机物构成。以上研究均是建立在各组分间作用力为共价键的基础之上,称为分子化学聚合理论。然而,Piccolo等[12]后续研究发现,在腐殖酸中加入有机酸时,其分子量减小,紫外响应减弱,这是分子化学聚合理论所不能解释的。此外,这些研究者在用高效体积排阻色谱测定不同来源腐殖酸的分子量时,发现腐殖酸可能是由小分子较松散地聚合而成[13]。因此,Piccolo[14-15]通过一系列的研究提出了超分子(supramolecule)的概念。此观点认为,腐殖酸是由种类繁多的、大小不一的分子通过分子间的弱作用力自组装形成的超分子,这些弱作用力包括疏水作用、范德华力、π-π键作用和氢键作用等[15-16]。可以推测,这些作用力一旦受到外界更强作用力的干扰,腐殖酸的结构极有可能发生改变。
最近关于氢键的研究发现,弱酸与有机物之间的pKa相差较小时(∆pKa < 0.5),氢键所连接的电子供体(酸中的H-)与受体(有机物中的O-或N-)间质子转移所需能量较少,从而使分子间距更小,形成一种特殊的氢键,称为电荷辅助氢键(Charge- assistant hydrogen bonds,CAHB)[17]。其键长(约2.35~2.50 Å)较普通氢键键长(约2.70~2.85 Å)更短,因而键能(63~167 kJ·mol-1)较普通氢键(25~42 kJ·mol-1)更强,在矿物溶解、金属离子隔离、氧化还原反应和pH缓冲等地球化学过程中有重要作用[18]。Moustafa等[19]通过研究弱酸在带羟基的碳表面上的吸附,证明了CAHB在吸附过程中发挥的重要作用;Li等[20]指出由于苯甲酸与碳纳米管表面羟基间形成了CAHB,导致苯甲酸的吸附强于不能形成CAHB的硝基苯;类似地,Ling等[21]发现在弱碱性条件下,电离的磺胺甲基异恶唑与吸附剂表面的胺类物质之间形成了有利于前者吸附的CAHB。基于腐殖酸超分子结构中的作用力明显弱于共价键,而CAHB键能与共价键可比的事实,推测一旦在腐殖酸体系中加入能够与之形成CAHB的物质,因为弱作用力结合在一起的腐殖酸超分子聚合体可能会脱稳,从而分散成若干相对较小的分子,宏观上可能表现为腐殖酸的溶解性增大,分子量变小。
假设形成CAHB能力强的小分子有机酸可以打破腐殖酸超分子的结构,从而降低腐殖酸的分子量,增大腐殖酸的溶解性,基于此,本研究系统地考察不同小分子有机酸对腐殖酸分子量和溶解性的影响,探究电荷辅助氢键影响下腐殖酸分子量和溶解度的变化,对评价和预测与腐殖酸结合的污染物的迁移、转化行为提供新思路。
1 材料与方法 1.1 供试材料试验所用腐殖酸以胡敏酸为研究对象,采用碱液提取、酸沉淀方法于云南省滇池底泥中提取。试验所用盐酸、氢氧化钠、氯化钠、甲酸、乙酸、丙酸、L-抗坏血酸、苯甲酸、苯酚、和邻苯二酚均购置于上海阿拉丁生化科技股份有限公司,纯度为分析纯。
1.2 小分子酸影响腐殖酸分子量试验将2 mg腐殖酸溶于10 mL 0.1 mol·L-1的NaOH溶液中,分别用盐酸、甲酸(pKa = 3.75)、乙酸(pKa = 4.75)和丙酸(pKa = 4.87)4种小分子酸将腐殖酸溶液pH调至3.5。不加酸样品作为对照。所有样品在25℃下避光震荡24 h,采用凝胶色谱柱(G300 PW XL,粒径6 μm,孔径200 Å,规格300 mm×7.8 mm,TOSOH,Japan),在紫外254 nm(安捷伦1200)波长下测定溶质停留时间。流动相为:1.75 mg·L-1 NaCl、228.2 mg·L-1 K2HPO4和136.1 mg·L-1 KH2PO4的混合溶液;流速为1 mL·min-1;进样量为1 μmm。
1.3 小分子酸影响腐殖酸溶解性试验将50 mg腐殖酸溶解于40 mL分别含有1 mmol·L-1盐酸、甲酸、乙酸、丙酸4种小分子酸的0.1 mol·L-1 NaCl溶液。用0.1 mol·L-1 HCl或0.1 mol·L-1 NaOH溶液将上述腐殖酸溶液的pH调至2.6~5.0。全部样品在25℃下避光震荡24 h,然后采用3 000 r·min-1的速度离心10 min。取上清液测其pH及总有机碳含量(TOC)。TOC用来反映腐殖酸的溶解量。
1.4 紫外光谱表征CAHB存在试验50 g·L-1的抗坏血酸(pKa=4.04)、苯甲酸(pKa=4.20)、苯酚(pKa=9.99)和邻苯二酚(pKa=9.40)的40 mL溶液中加入少量等体积0.1 mol·L-1的甲酸(pKa=3.75),对照组加入与甲酸相同体积的超纯水,用0.1 mol·L-1 HCl或0.1 mol·L-1 NaOH溶液将试验组和对照组的pH均调到对应模型化合物的pKa附近。所有样品在25℃避光的条件下震荡24 h,测定溶液在200~400 nm处的紫外吸收光谱。
1.5 数据处理利用Excel2003软件进行分子量、TOC和紫外光谱的数据整理、绘制;采用二维相关光谱分析软件2Dshige(version 1.3)分析、绘制同步二维相关紫外光谱。
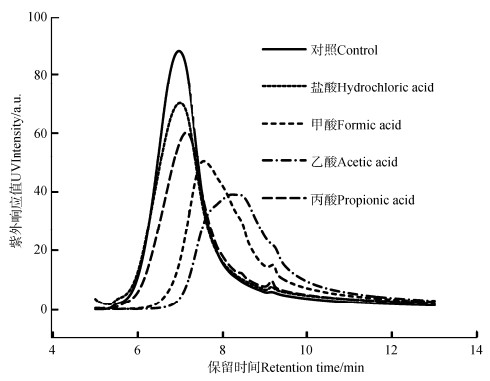
2 结果与讨论 2.1 小分子酸对腐殖酸分子量的影响盐酸、甲酸、乙酸、丙酸4种小分子酸对腐殖酸分子量分布的影响如图 1所示,其中保留时间越长,说明通过排阻色谱柱的有机物分子量越小。显然小分子有机酸的加入,一方面降低了腐殖酸的紫外响应,另一方面使腐殖酸的分子量明显减小。腐殖酸的分子量降低的越明显,其紫外响应的降低越显著。原因可能是腐殖酸小分子的芳香环上含氧官能团取代程度增大[22-23],其最大吸收波长发生了变化,偏离原腐殖酸大分子的254 nm,从而造成了紫外响应的降低。
|
图 1 小分子酸对腐殖酸分子量的影响 Fig. 1 Influence of small molecular acids on molecular weight of humic acid |
对比不同酸的影响可以发现,乙酸具有最大的降低腐殖酸分子量和紫外响应的能力,甲酸次之,丙酸的影响很小,而盐酸不会改变腐殖酸的分子量。其他研究者[12, 15, 24]也观察到了类似的试验结果,他们认为小分子有机酸的羧基与腐殖酸作用,破坏其原有结构,腐殖酸小分子通过普通氢键作用进行了重新组装。然而,土壤中的有机质通常带负电,并不利于普通氢键的形成;而且普通氢键的键能较小,不具备打破腐殖酸超分子稳态的能力,因此普通氢键的理论不能解释上述结果。结合电荷辅助氢键理论可以推测,乙酸的pKa可能与腐殖酸的某个pKa较为接近,容易形成高能量的CAHB,打破腐殖酸超分子的结构,导致其分子量减小;甲酸、丙酸的pKa可能与腐殖酸的pKa差别较大,CAHB形成能力较弱;而盐酸由于可以完全解离,没有形成CAHB的能力,因此不会改变腐殖酸的结构和分子量。后续的腐殖酸溶解性试验可以进一步证实CAHB能够在小分子酸和腐殖酸分子体系中形成,从而影响腐殖酸的溶解性。
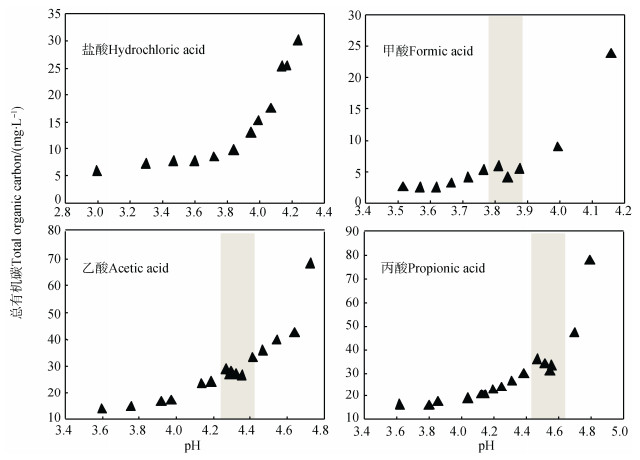
2.2 小分子酸对腐殖酸溶解性的影响不同小分子酸对腐殖酸溶解性的影响如图 2所示。4种小分子酸的加入,均导致腐殖酸体系pH的降低,从而降低了腐殖酸的溶解性。有意思的是,除了盐酸,其他3种小分子有机弱酸的加入,均使腐殖酸在3种弱酸各自的pKa附近形成了较高的溶解峰(图 2灰色区域所示)。CAHB理论启示我们,在3种小分子有机弱酸各自的pKa左右,腐殖酸与小分子有机酸的羧基官能团之间可以形成高能量的CAHB,从而破坏腐殖酸超分子的结构,导致小分子重组,增大溶解性。然而,盐酸没有形成CAHB的能力,因此腐殖酸在盐酸体系中没有观察到类似的溶解峰,该体系中腐殖酸的溶解性只与pH有关。
|
图 2 小分子酸对腐殖酸溶解性的影响 Fig. 2 Influence of small molecular acids on solubility of humic acid |
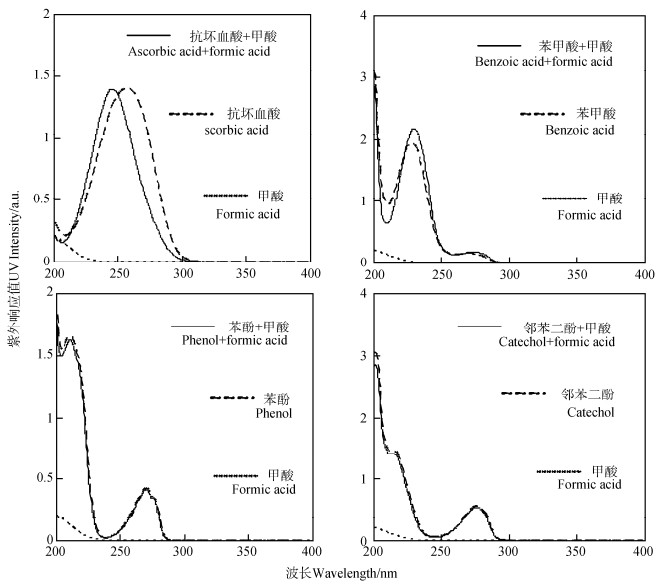
由图 3可以看出,在抗坏血酸、苯甲酸体系中加入甲酸后,抗坏血酸、苯甲酸的紫外吸收峰(已扣除甲酸本身的紫外吸收)分别发生了蓝移和红移,并且抗坏血酸的峰偏移程度更大;而在苯酚、邻苯二酚体系中加入甲酸后,两者的紫外吸收峰均没有发生变化。这些结果说明,甲酸可能与抗坏血酸、苯甲酸之间发生了较强的相互作用。根据CAHB理论,当两物质pKa之差(∆pKa)越接近于0,形成CAHB的能力越强。甲酸(pKa = 3.75)与抗坏血酸(pKa = 4.04)的∆pKa = 0.29,与苯甲酸(pKa = 4.2)的∆pKa = 0.45,前者形成CAHB的能力较后者更强,因此抗坏血酸受甲酸影响产生的紫外吸收峰偏移程度更大。甲酸羟基与抗坏血酸的羰基之间形成CAHB,使羰基的n→π*跃迁能量增大,出现最大紫外吸收峰蓝移现象[25];苯甲酸中加入甲酸,可能由于助色效应或超共轭效应使氢键中C-H延长,紫外吸收峰发生红移现象,吸收强度也有一定增大[26]。苯酚(pKa = 9.99)、邻苯二酚(pKa = 9.4)与甲酸的∆pKa分别为6.24和5.65,此时CAHB较难形成,因此苯酚和邻苯二酚的紫外吸收峰没有因甲酸的加入而发生变化。
|
图 3 甲酸对模型有机物紫外光谱的影响 Fig. 3 Influence of formic acid on ultraviolet spectra of model organic chemicals |
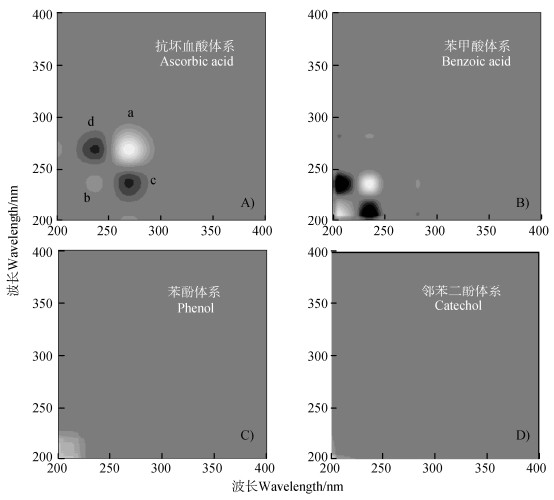
为提高紫外光谱的分辨率,区分一维光谱中的弱峰和重叠峰,绘制甲酸影响下的同步二维相关紫外光谱图(图 4),判断各波段代表的基团对于甲酸干扰的相应强度,从而更加准确鉴别和研究甲酸对模型化合物基团的相互作用[27]。如图 4所示,以甲酸为扰动外因,在200~400 nm波长范围内构建抗坏血酸同步二维相关紫外光谱图。以图 4A为例,其中出现了两个自动峰(a、b)和一对交叉峰(c、d)。自动峰a、b与外扰条件呈最直接相关性,产生的峰均为正峰(浅色区域);分别说明甲酸的加入使抗坏血酸270 nm和240 nm附近的紫外吸收有了明显的变化。交叉峰c、d则代表两个波数下光谱峰的变化存在关联,正峰表示两者变化方向一致,负峰(深色区域)表示两者变化方向相反;图中交叉峰均为负峰,说明270 nm和240 nm附近的紫外吸收受甲酸的影响是相反的。以上结果表明,低波长吸收增大而高波长吸收减小,说明整体跃迁所用能量增大,可能是由于抗坏血酸与甲酸间形成能量较高的CAHB,使其基态的能量降低,造成跃迁所需能量增大,与一维紫外光谱蓝移现象相符。通过比较可以发现,图 4中抗坏血酸与甲酸∆pKa最小,其紫外光谱在较大波长范围内发生了变化,但是变化强度不大;图 4中苯甲酸与甲酸∆pKa较小,其紫外光谱变化范围相比抗坏血酸小且波长更低,但同样浓度甲酸所产生的影响强度大,说明甲酸对苯甲酸中特征吸收波长在240 nm和210 nm附近的官能团作用大。图 4C、图 4D中未能观测到较明显的紫外吸收强度的变化,说明与甲酸∆pKa较大的苯酚和邻苯二酚分子结构并未受甲酸加入而发生变化。同步二维相关紫外光谱更加准确地反映了模型有机物分子结构受甲酸扰动下的不同变化,进一步说明基于∆pKa大小而判断的CAHB存在与否理论的正确性。
|
图 4 甲酸为扰动的模型有机物同步二维相关紫外光谱 Fig. 4 Synchronous 2D correlation ultraviolet spectra of model organic chemicals(formic acid as the disturber) |
小分子有机酸与腐殖酸之间可能形成CAHB,从而打破腐殖酸超分子的稳态结构,导致腐殖酸分子量明显降低。腐殖酸体系的pH接近小分子有机酸pKa时,两者之间形成CAHB的能力最强,可以更有效使腐殖酸超分子脱稳,从而增大腐殖酸溶解性。甲酸具有与抗坏血酸和苯甲酸接近的pKa,因此可能与抗坏血酸和苯甲酸形成CAHB,从而改变两者的紫外光谱特征。
| [1] |
Xing B. Sorption of naphthalene and phenanthrene by soil humic acids . Environmental Pollution, 2001, 111(2): 303-309. DOI:10.1016/S0269-7491(00)00065-8
(  0) 0) |
| [2] |
王朋, 张迪, 张凰, 等. 天然有机质对纳米碳管环境行为的影响研究进展. 材料导报, 2017, 31(1): 131-135, 148. Wang P, Zhang D, Zhang H, et al. Influence of natural organic matter on environmental behavior of carbon nanotubes:A review (In Chinese). Materials Review, 2017, 31(1): 131-135, 148. (  0) 0) |
| [3] |
王锐, 许海娟, 魏世勇, 等. 针铁矿和针铁矿-胡敏酸复合体对Se (Ⅳ)吸附机制. 土壤学报, 2018, 55(2): 399-410. Wang R, Xu H J, Wei S Y, et al. Selenite adsorption mechanisms of goethite and goethite-humic acid complex (In Chinese). Acta Pedologica Sinica, 2018, 55(2): 399-410. (  0) 0) |
| [4] |
Chefetz B, Tarchitzky J, Deshmukh A P, et al. Structural characterization of soil organic matter and humic acids in particle-size fractions of an agricultural soil . Soil Science Society of America Journal, 2002, 66(1): 129-141. DOI:10.2136/sssaj2002.1290
(  0) 0) |
| [5] |
Wang K, Xing B. Structural and sorption characteristics of adsorbed humic acid on clay minerals . Journal of Environmental Quality, 2005, 34(1): 342-349. DOI:10.2134/jeq2005.0342
(  0) 0) |
| [6] |
Atiyeh R M, Lee S, Edwards C A, et al. The influence of humic acids derived from earthworm-processed organic wastes on plant growth . Bioresource Technology, 2002, 84(1): 7-14. DOI:10.1016/S0960-8524(02)00017-2
(  0) 0) |
| [7] |
Francioso O, Sánchez-Cortés S, Casarini D, et al. Spectroscopic study of humic acids fractionated by means of tangential ultrafiltration . Journal of Molecular Structure, 2002, 609(1/3): 137-147.
(  0) 0) |
| [8] |
Novák F, Šestauberová M, Hrabal R. Structural features of lignohumic acids . Journal of Molecular Structure, 2015, 1093: 179-185. DOI:10.1016/j.molstruc.2015.03.054
(  0) 0) |
| [9] |
Piccolo A, Nardi S, Concheri G. Micelle-like conformation of humic substances as revealed by size exclusion chromatography . Chemosphere, 1996, 33(4): 595-602. DOI:10.1016/0045-6535(96)00210-X
(  0) 0) |
| [10] |
Engebretson R R, von Wandruszka R. Micro-organization in dissolved humic acids . Environmental Science & Technology, 1994, 28(11): 1934-1941.
(  0) 0) |
| [11] |
Peuravuori J, Simpson A J, Lam B, et al. Structural features of lignite humic acid in light of NMR and thermal degradation experiments . Journal of Molecular Structure, 2007, 826(2/3): 131-142.
(  0) 0) |
| [12] |
Piccolo A, Conte P, Cozzolino A. Effects of mineral and monocarboxylic acids on the molecular association of dissolved humic substances . European Journal of Soil Science, 1999, 50(4): 687-694. DOI:10.1046/j.1365-2389.1999.00276.x
(  0) 0) |
| [13] |
Conte P, Piccolo A. High Pressure Size Exclusion Chromatography (HPSEC) of humic substances:Molecular sizes, analytical parameters, and column performance . Chemosphere, 1999, 38(3): 517-528. DOI:10.1016/S0045-6535(98)00198-2
(  0) 0) |
| [14] |
Piccolo A. The supramolecular structure of humic substances . Soil Science, 2001, 166(11): 810-832. DOI:10.1097/00010694-200111000-00007
(  0) 0) |
| [15] |
Piccolo A. The supramolecular structure of humic substances: A novel understanding of humus chemistry and implications in soil science//Advances in Agronomy. San Diego: Academic Press, 2002.
(  0) 0) |
| [16] |
Gilli G, Gilli P. Towards an unified hydrogen-bond theory . Journal of Molecular Structure, 2000, 552(1/3): 1-15.
(  0) 0) |
| [17] |
Lopes Jesus A J, Redinha J S. Charge-assisted intramolecular hydrogen bonds in disubstituted cyclohexane derivatives . The Journal of Physical Chemistry A, 2011, 115(48): 14069-14077. DOI:10.1021/jp206193a
(  0) 0) |
| [18] |
Gilli P, Bertolasi V, Pretto L, et al. Outline of a transition-state hydrogen-bond theory . Journal of Molecular Structure, 2006, 790(1/3): 40-49.
(  0) 0) |
| [19] |
Moustafa A M, McPhedran K N, Moreira J, et al. Investigation of mono/competitive adsorption of environmentally relevant ionized weak acids on graphite:Impact of molecular properties and thermodynamics . Environmental Science & Technology, 2014, 48(24): 14472-14480.
(  0) 0) |
| [20] |
Li X, Gamiz B, Wang Y, et al. Competitive sorption used to probe strong hydrogen bonding sites for weak organic acids on carbon nanotubes . Environmental Science & Technology, 2015, 49(3): 1409-1417.
(  0) 0) |
| [21] |
Ling C, Li X, Zhang Z, et al. High adsorption of sulfamethoxazole by an amine-modified polystyrene-divinylbenzene resin and its mechanistic insight . Environmental Science & Technology, 2016, 50(18): 10015-10023.
(  0) 0) |
| [22] |
Fuentes M, González-Gaitano G, García-Mina J M. The usefulness of UV-visible and fluorescence spectroscopies to study the chemical nature of humic substances from soils and composts . Organic Geochemistry, 2006, 37(12): 1949-1959. DOI:10.1016/j.orggeochem.2006.07.024
(  0) 0) |
| [23] |
赵晨, 王崇臣, 李俊奇, 等. 径流雨水中不同分子量溶解性有机物分布及其与Cu2+相互作用. 环境化学, 2016, 35(4): 757-765. Zhao C, Wang C C, Li J Q, et al. Molecular weight distribution of dissolved organic matters in stormwater runoff and their interactions with Cu2+ (In Chinese). Environmental Chemistry, 2016, 35(4): 757-765. (  0) 0) |
| [24] |
Smejkalova D, Piccolo A. Aggregation and disaggregation of humic supramolecular assemblies by NMR diffusion ordered spectroscopy (DOSY-NMR) . Environmental Science & Technology, 2008, 42(3): 699-706.
(  0) 0) |
| [25] |
文彬, 曹晨忠. 醇溶剂地羰基(C=O)紫外吸收的定量影响. 有机化学, 1999, 19(1): 77-80. Wen B, Cao C Z. The quantified effecting of alcohol solvent on the carbonyl (C=O) ultraviolet absorption (In Chinese). Chinese Journal of Organic Chemistry, 1999, 19(1): 77-80. DOI:10.1016/S0144-8617(98)00119-2 (  0) 0) |
| [26] |
王素纹, 黎安勇. 吡啶与CHX3(X=F, Cl, Br, I)形成分子间红移和蓝移氢键的理论研究. 西南大学学报(自然科学版), 2007, 29(5): 26-30. Wang S W, Li A Y. Theoretical study of the red-shifting and blue-shifting hydrogen bonding between pyridine and CHX3(X=F, Cl, Br or I) (In Chinese). Journal of Southwest University (Natural Science Edition), 2007, 29(5): 26-30. (  0) 0) |
| [27] |
Noda I. Two-dimensional correlation spectroscopy (2DCOS) analysis of polynomials . Journal of Molecular Structure, 2016, 1124: 53-60. DOI:10.1016/j.molstruc.2016.01.091
(  0) 0) |
2. Yunnan Institute of Food Safety, Kunming University of Science & Technology, Kunming 650500, China;
3. Yunnan Key Laboratory of Carbon Sequestration and Pollution Controlling, Kunming 650500, China
 2020, Vol. 57
2020, Vol. 57


