大豆是一种重要的高蛋白农产品,在我国食用、饲用、医疗以及工业等领域被广泛利用,尤其在我国人体膳食结构中具有重要在不可替代性[1]。在过去20年中,中国本土消耗的大豆主要依靠进口[2],提升大豆自给力一直是重要的国家需求之一。2019年中央一号文件提出实施大豆振兴计划,多途径在我国本土扩种大豆[3-4];与此同时,我国农业农村发展进入新的历史阶段,土壤污染防治与质量提升在农业绿色和高质量发展中的作用更加凸显。围绕土壤功能的研究已从聚焦土壤肥力、追求作物产量,到更加突出土壤环境质量和健康以支撑农业高质量绿色发展的变化历程[5]。过去高投入的农业耕作模式造成各类污染物在农田系统中不断累积,加剧了土壤质量退化及农田生态系统稳定性降低,对大豆产地的土壤环境质量和微生态平衡构成威胁,极大程度限制了国家大豆振兴计划的有效实施。
近年来,我国大豆产区除草剂施用量整体呈上升趋势[6]。除草剂的土壤残留常危害后茬作物生长[7-8],环境友好型除草剂持续多年施用也可干扰生态环境,并可能通过对土壤微生态的负面影响导致大豆更易遭受病虫害侵袭[9-11];目前我国耕地重金属污染问题较为突出[12-14],使得近年来“镉麦”、“镉米”等农产品安全事件频发,大豆产地重金属污染对大豆品质安全造成的威胁不容忽视;大豆集约化种植过程连年单作导致土壤微生态失衡,地下病虫害日趋严重[15],不仅造成减产和经济损失,还加剧了种植过程对农药的依赖程度。因此,当前迫切需要从大豆种植条件下产地土壤环境与微生态演变出发,准确认识限制我国大豆产业高质量绿色健康发展的关键问题,在系统梳理国内外已有研究进展和研究重点的基础上提出未来研究方向,以推动我国大豆产业的健康发展。
有鉴于此,本文基于Web of Science(WOS)核心数据库,检索大豆产地土壤环境与微生态过程研究领域的所有文献,利用VOSviewer软件进行关键词共现分析,探讨全球近20年内国内外不同时期相关大豆种植体系中大豆生长受除草剂残留、重金属累积、地下病害发生等影响的研究热点和进展,为解决限制我国大豆高产创建和品质提升的大豆产区产地土壤环境与微生态问题提供研究思路。
1 材料与方法 1.1 数据来源国际文献计量的数据来自美国汤森路透公司(Thomson Reuters)WOS核心合集数据库。依据前期文献调研,并结合本文研究领域核心关键词制定英文检索式。除草剂相关研究的英文检索式为:(“soybean” or “glycine max”)and(“herbicide” or “glyphosate” or “imazethapyr” or “glufosinate” or “atrazine” or “dicamba”);重金属相关研究的英文检索式为:(“soybean” or “glycine max”)and(“heavy metal” or “heavy metals” or “cadmium” or “chromium” or “nickel” or “copper” or “arsenic” or “lead not lead to” or “mercury” or “zinc”);关于地下病害,结合相关文献以及第三版《中国农作物病虫害》[16],挑选出国内外典型的、危害严重的大豆地下病害并制定英文检索式,即:(“soybean” or “glycine max”)and(“soil borne disease” or “soilborne disease”)(此处省略地下病害病原菌及其具体名称);出版年为2000-2019年(2000年1月1日至2019年12月31日),选定文献类型为Article和Review。经检索,获得除草剂相关文献2 877篇,重金属相关文献2 329篇,地下病害相关文献2 447篇。此外,为深入分析从土壤科学领域开展的针对大豆产地环境与微生态过程的研究,在上述检索基础上,进一步将关于除草剂、重金属和地下病害检索关键词合并,并分别增加土壤为关键词(“soil” or “land” or “farmland”)进行综合搜索分析,得到相关文献2 119篇。
1.2 研究方法在WOS核心数据库导出以上关键词检索结果,通过VOSviewer进行关键词共现分析(Co-occurrence、All keywords,热图颜色深浅、网络节点大小代表关键词出现的次数),以反映关于该科学问题的研究热点;某个关键词出现次数越多,代表该研究领域越受到国家以及科学界的关注。对某些意义一致的关键词进行合并,包括相同名词单数和复数(例如herbicide与herbicides)、意义相同的名词或词组(例如soybean与glycine max、root rot与root-rot、crop rotation与rotation)、意义相同的缩写(例如zinc与Zn)等。
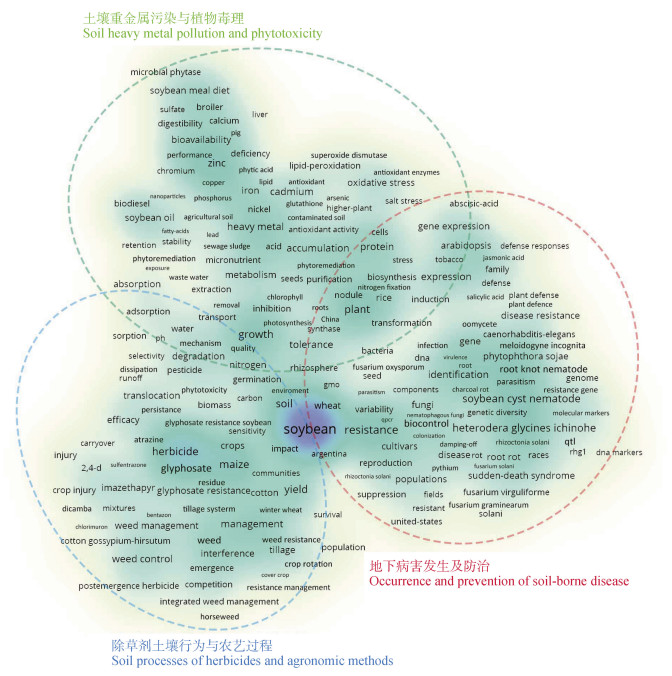
2 大豆产地土壤环境研究现状及趋势 2.1 “大豆与除草剂”研究图 1聚类圈中高频关键词的共现反映关于除草剂在大豆种植过程中的施用管控(management)、多种除草剂复合施用(mixture)以及对杂草控制(weed control、weed management)方面的功效(efficacy)、下茬作物易感性(sensitivity)和相关农艺过程(crop rotation,tillage)是该领域的重要研究方向之一;由于具有极强除草效果,环境友好型除草剂草甘膦及相关耐性作物品种的研究是近二十年来的研究热点[17]。通过关键词共现分析结果发现,杂草抗性(weed resistance)与草甘膦抗性(glyphosate resistance)等高频关键词联系紧密,反映出因利用耐草甘膦大豆品种进行生产导致的杂草抗性提高的相关问题受到学界重点关注[18-19]。除草剂对大豆植株的毒理效应(phytotoxicity)[20]以及解毒机制(mechanism)[21-22]也是学者重点关注对象;同时除草剂也会抑制根瘤菌活性,这将进一步影响根瘤菌的结瘤、发育及固氮功能[23-24],但相关研究较少。水(water)、吸附(sorption)、解吸(desorption)、消减(dissipation)、迁移(transport)、持久性(persistence)等高频关键词的出现反映基于物理化学污染过程的除草剂土-水界面吸附与迁移是研究热点之一[25-26]。多数研究表明,环境中农药降解过程通常由微生物主导[27],土壤中菌群间的互作极大程度促进除草剂的降解效率[28];然而目前关于残留除草剂在大豆种植土壤中生物降解过程的研究较少。同时现有研究指出,氟磺胺草醚会对大豆根际土壤微生物群落丰度及酶活性产生负面影响[29];在土壤中添加草甘膦后,耐草甘膦大豆根际微生物功能受到抑制[30];但针对除草剂胁迫下根际微生物群落组成、功能以及互作网络的响应鲜有报道,相关关键词词频基本低于25次。
|
注:图中出现的关键词频数大于30次。 Note:The keywords in the graph were higher than 30 in frequency of appearance. 图 1 近20年相关“大豆与除草剂、重金属及地下病害”研究热点及进展 Fig. 1 Hotspots and progress of the research on 'Soybean and Herbicide/Heavy metal/Soil-borne Diseases' in the recent 20 years |
农田土壤中(agricultural soil)重金属的毒害作用(toxicity)包括直接造成大豆组织(leaves、roots)损伤[31-32]以及抑制大豆对土壤氮(nitrogen)[33]、磷(phosphorus)[34]等养分的吸收(absorption)。除此之外,重金属在根瘤中的积累(accumulation)会抑制根瘤菌固氮活性(nitrogen fixation),这将进一步抑制大豆生长[33,35](图 1);而添加钙(calcium)等盐基离子则可以缓解重金属对大豆的毒害[36]。目前关于大豆解毒机制的研究主要集中于在缓解重金属引起的氧化胁迫(oxidative stress),包括抗氧化物(antioxidan)、金属螯合有机酸(citric acid、phytic acid)的分泌和金属螯合蛋白例如谷胱甘肽(glutathione)[37]的合成;重金属积累也会降低大豆籽粒质量(protein、lipid)[38-39],这可能会影响相关大豆产品品质(soybean oil、fatty-acid)[40],同时造成食物链安全风险(soybean meal diet、bioavailability)(图 1)。目前关于重金属在大豆产地土壤中的污染过程与修复的研究较少,对重金属土壤污染过程的研究大部分停留在土壤性质对重金属的迁移(transport)和吸附(adsorption);植物修复(phytoremediation)是一种绿色高效去除(removal)土壤中重金属的方法[41],因此更偏向于利用植物修复污染土壤(contaminated soil)(图 1)。大量研究指出,重金属污染会影响土壤微生物活性、生物量以及碳、氮、磷养分循环[42-45],进而影响土壤肥力和健康;但类似研究较少针对大豆产地土壤展开,因而,目前对重金属胁迫下大豆产地土壤肥力和健康功能如何演变、以及这种演变进一步对大豆产量产生何种影响还缺乏全面的认知。本研究结果发现铜、锌与猪(pig)、鸡(broiler)等畜禽关键词联系较为紧密,经查阅相关文献得出是部分研究探讨饲料大豆中铜、锌作为微量营养元素对畜禽生长的影响[46];本研究将铜、锌作为关键词之一进行检索,这可能是引起该误差的原因。
2.3 “大豆与地下病害”研究大豆胞囊线虫病(soybean cyst nematode)以及导致该病害发生的大豆胞囊线虫(Heterodera glycines Ichinohe)在所有关键词中出现频次最高,在我国主要分布在东北和黄淮海大豆主产区[16]。关键词频数排第三的是南方根结线虫(Meloidogyne incognita),该病原菌导致的病害为大豆根结线虫病(soybean root-knot nematode)(图 1)。关键词频数排第二的大豆病原菌是大豆疫霉菌(Phytophthora sojae),其引起的大豆疫霉根腐病是危害大豆生产的严重病害之一[47];此外,能够导致根腐病(root rot)的病原菌还包括禾谷镰孢(F. graminearum)和尖镰孢(F. oxysporum)[48]、腐皮镰孢(F. solani)以及腐霉菌属(Pythium)[47]、立枯丝核菌(Rhizoctonia solani)[49]等;由于地区性差异,各地报道的根腐病病原菌优势种各不相同。F. virguliforme引起的大豆猝死综合征(sudden-death syndrome)是美洲(图 1)大豆重要病害之一[50-51];除多种病原菌导致的根腐病外,也包括线虫-真菌-卵菌共侵染引起的病害问题[52]。聚类圈中出现种(races)、毒性(virulence)、鉴定(identification)、植物防御(plant defence)、水杨酸(salicylic acid)等高频关键词表明针对病原体不同亚种鉴定及其对不同大豆品种的毒性和探究植物抗病机理是各国学者重点关注的研究方向。目前关于大豆地下病害防治的研究方向主要有:1)农艺手段:与非宿主作物轮作[16,53]以及抗性品种的选育、种植[53];2)生物防治(biocontrol):利用食线虫真菌(nematophagous fungi)、寄生真菌(parasitism)[54]以及细菌(bacteria)[55]等进行线虫病防治是当前该领域研究重点(图 1)。越来越多的研究指出,植物根际关键微生物种群能够通过高效表达抗病基因抵御病原菌在根际的定植以有效保障植物健康[56-60],因此近年来针对豆科植物根际(rhizosphere)中细菌(bacteria)群落在抑制根腐病病原入侵中所起的关键作用受到各国学者重点关注[59-60];同时土壤病毒、真菌以及原生生物在地下病害防治中也起到重要作用[61-63],通过强化根际免疫能力防控地下病害发生是未来研究的重点。地下病害的发生不仅与种植季节气候相关(damping-off),也受田间耕作方式的影响[16]。除与共同宿主轮作外,除草剂的持续投入也会提高大豆染病风险:十年持续施用草甘膦会促进镰孢菌属在耐草甘膦大豆根系上的定殖[64];同时草甘膦的施用也会提高其他作物根腐病发病风险[9-10];这可能与草甘膦持续施用抑制土壤中重要拮抗菌活性导致大豆根际免疫下降有关[64-65]。但目前关于除草剂持续投入下土壤微生态的响应以及与地下病害的发病机制尚不清楚。
2.4 大豆相关研究中“产地土壤环境与微生态过程”方向成果产出地下土壤微生态系统与地上植物系统紧密联系,相互依存,共同决定着农业生产的特征、过程和农田系统功能,其中土壤微生物在植物-土壤物质交换、养分循环以及植物抗逆过程中起到关键作用[66-68]。为探讨除草剂、重金属以及地下病害引起的大豆产地土壤环境与微生态问题的国内外研究热点以及研究趋势,进一步将上述关于除草剂、重金属和地下病害检索关键词合并,并添加土壤为关键词(“soil” or “land” or “farmland”)进行综合搜索分析。
2.4.1 “产地土壤环境与微生态过程”方向的文献计量分析从关键词共现分析结果可以看出,近20年关于“产地土壤环境与微生态过程”的研究热点主要包括以下三个方面:
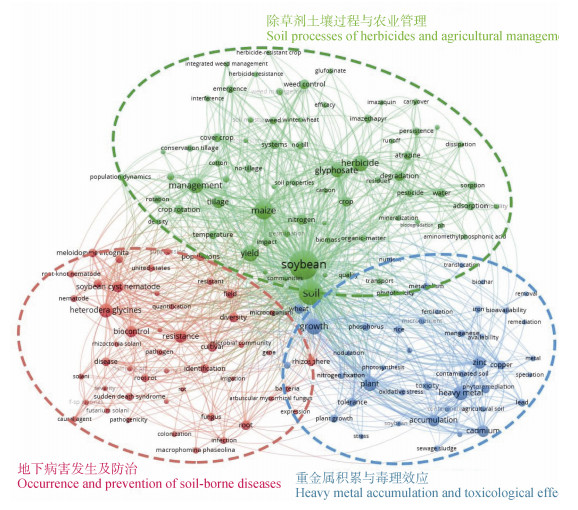
其一,除草剂的土壤环境过程与农业管理。从关键词共现分析图中出现的高频关键词可知,引起土壤污染的除草剂来源主要是在玉米-大豆轮作体系下进行相关杂草控制和农业管理过程中形成的除草剂土壤残留(residue),进而影响大豆的产量(impact、yield)(图 2)。由土壤污染引发的水环境二次污染问题以及基于物理化学过程的除草剂土-水界面吸附与迁移也是研究热点之一。同时在降解研究中,主要关注生物降解和矿化的过程与机制,针对除草剂胁迫下根际微生态过程的关注较少(图 2)。
|
注:图中出现的关键词频数大于20次。 Note:The keywords in the graph were all higher than 30 in frequency of appearance in the co-occurrence network. 图 2 增加引入“土壤”为合并检索关键词所得近20年国际上相关研究热点及进展 Fig. 2 Hotspots and progress of the research on introduction of 'soil' as a joint key word for retrieval in the recent 20 years |
其二,重金属积累与毒理效应。从图 2中可以看出,锌、镉、铜、铅是学者重点关注的大豆产地土壤重金属元素。聚类圈中出现了农田土壤(agricultural soil)、施肥(fertilizer、fertilization)、污水污泥(sewage sludge),反映学者们对农田土壤中重金属污染源有一定研究;同时学者着重探讨土壤中重金属对植物生长的影响机理,其中还涉及食品安全风险(food safety)。此外,针对大豆根际微生态过程对土壤重金属的响应,包括重金属对细菌、丛枝菌根真菌(arbuscular mycorrhizal fungus)等微生物的生态效应、以及对根瘤菌固氮(nitrogen fixation)、结瘤(nodulation)能力的探讨也是近20年的研究重点之一。为应对土壤重金属污染带来的大豆减产以及食物链安全风险,各国学者重点研究了土壤重金属污染生物修复技术(bioremediation),其中主要是利用植物提取(phytoextraction)的植物修复技术,研究的核心重点关注了修复技术应用前后对土壤重金属有效性(available)的影响。
其三,地下病害发生及防治。从图 2中可以得到,聚类圈中大豆胞囊线虫、大豆根结线虫及其病原菌相关关键词出现次数最多,表明在研究地下病害发生的土壤过程中,线虫病是近20年关注度最高的地下病害,其次是根腐病以及大豆猝死综合征;同时抗病品种选育以及生物防治以缓解地下病害仍是各国研究的重点。与生物防治以及根际联系紧密的有真菌、根腐病、胞囊线虫、根结线虫、细菌、捕食性真菌、微生物(microorganisms)、微生物群落(microbial community)、多样性(diversity)等,表明基于根际微生物群落组成以及功能多样性调控,通过提升根际免疫力以对地下病害进行生物防治是本阶段的研究热点(图 2)。
2.4.2 中国在“产地土壤环境与微生态过程”方向的研究特点及学术贡献近20年国际上关于除草剂、重金属以及地下病害引起的大豆土壤环境与微生态问题共计发表 2 119篇文献,h指数达76;发文量居前3位的国家分别是大豆主产国美国、中国以及巴西,共占总发文量的72.9%。美国关于该科学问题发文量最高,占比接近50%,h指数为63;中国发文量与美国差距较大,仅为美国的1/3(表 1)。然而,中国学者在近五年关于该科学问题的发文量超过2000-2014年发文量的总和,尤其是h指数在2010-2019时段内与美国差距甚微,这表明随着中国土壤科学的发展以及世界大豆贸易格局的变化,尤其是国家“大豆振兴计划”出台和实施,中国学者在本领域研究的数量和影响力迅速增大,这为后续立足当下国情实际,在保障主粮丰产增效的同时提升我国大豆自给力,实现大豆高产创建和品质安全,打下了坚实的理论基础。
|
|
表 1 2000-2019年大豆主产国关于“土壤环境与微生态过程”领域发文情况 Table 1 Publication of papers 'Soil Environment and Micro-ecological Process of soybean' in major soybean producing countries in 2000-2019 |
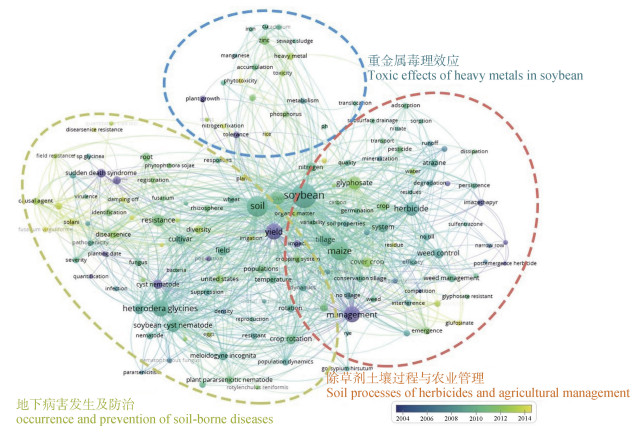
进一步以美国作为国际研究的代表,分析中国与国际上该方向研究特色与关注热点的差异。近20年美国学者相关研究中的关键词共现分析结果表明(图 3),美国关于除草剂引起的土壤环境与微生态问题的研究方向已经从农业管理向除草剂的土壤环境过程方面过渡,包括除草剂土-水界面的吸附、迁移、残留、消减以及降解;同时,因常年反复施用导致的除草剂残留对土壤养分循环过程的影响也是美国学者近年来研究的侧重点[69]。在土壤重金属污染引起的大豆土壤生态环境问题方面,美国学者仅关注重金属对植物的毒害作用以及食物链安全风险,关于土壤重金属污染过程以及生态效应等方面研究较少(图 3),这可能与美国大豆主产区耕地土壤质量相对优良,由土壤污染源引起大豆重金属污染的安全风险不典型有关;地下病害发生及防治也是美国学者的研究重点(图 3)。聚类圈中出现次数最多的地下病害关键词是大豆胞囊线虫病,其次是大豆猝死综合征以及根腐病。随着微生物测序手段的进步,关于地下病害的研究热点由宏观防控逐渐过渡到微观发病/抗病机理(针对具体病原菌)研究,尤其是在大豆根际微域中,微生物群落,包括细菌以及真菌群落多样性在植物抗性以及生物防治中起到的作用成为研究热点[70-71]。
|
注:图中出现的关键词频数大于10次。 Note:The frequency of keywords in the co-occurrence network is more than 10 times. 图 3 近20年美国学者关于“大豆土壤环境与微生态过程”研究热点及进展 Fig. 3 Hotspots and progress of the researches on 'Soil Environment and Micro-ecological Process of Soybean' accomplished by American scholars in the recent 20 years |
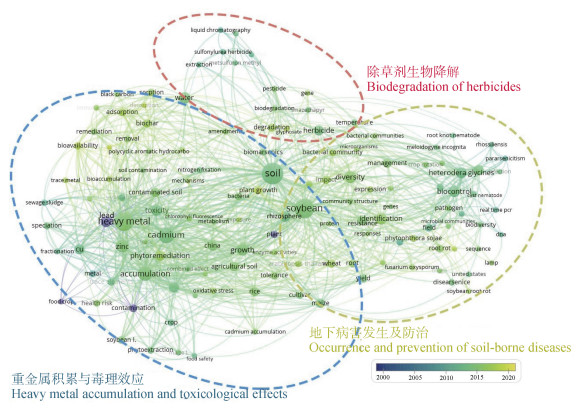
根据图 4关键词共现结果,可以总结近20年中国学者在该方向研究中取得的主要学术成就。对于土壤除草剂残留引发的大豆产地土壤环境与微生态问题,中国学者多聚焦于除草剂在土-水界面削减的生物化学过程,相关成果产出与美国差距较大。目前,我国大豆产区除草剂施用种类繁多,导致除草剂的土壤残留特征复杂、对土壤微生态过程以及土壤功能的影响未知,这将成为限制大豆高产创建的重要问题之一。
|
注:图中出现的关键词频数大于5次。 Note:The keywords in the graph were all higher than 30 in frequency of appearance in the co-occurrence network. 图 4 近20年中国学者关于“大豆土壤环境与微生态过程”研究热点及进展 Fig. 4 Hotspots and progress of the research on 'Soil Environment and Micro-ecological Process of Soybean' accomplished by Chinese scholars in the recent 20 years |
在土壤重金属污染与修复方面,中国学者则关注较多,推动了中国在该领域研究的长足发展。关键词共现分析结果表明,国内学者重点关注镉、锌、铅、铜等典型重金属元素,研究热点内容包括土壤重金属污染与修复、重金属形态及有效性、重金属吸附-解吸过程、植物积累与毒理效应、根际生物化学与微生物过程以及健康安全风险等;2014年《全国土壤污染状况调查公报》显示全国土壤环境状况总体不容乐观,耕地重金属污染问题较为突出[12-14],但具体针对大豆产地的重金属污染情况的调研还相当有限,对不同大豆产区主推品种的重金属富集能力也未可知,这是相关大豆品质安全的一大隐患。今后的工作亟待全面排查我国大豆产地重金属污染风险区,并因土而宜地在具有优良生产性状的大豆主推品种中进一步筛选兼具重金属低积累特性的品种,以保障重金属污染风险区的大豆安全生产。
在地下病害防控方面,中国与美国学者都十分重视。中国学者除了重点探讨大豆胞囊线虫病的防治外,针对大豆疫霉以及尖镰孢菌引起的大豆根腐病也是近年来中国学者研究侧重点。同时,对于大豆土壤微生物与病原体拮抗过程和机理,尤其是在根际土壤中微生物间分子互作机制近年来成为中国学者重点关注的研究内容[72-73]。在大豆实际生产中,除草剂持续投入可能破坏大豆根际微生态平衡,从而提高地下病原菌入侵的风险;结合我国不同大豆产地中不同耕作制度、除草剂施用背景和降解周期,探讨土壤微生物-地下病害致病菌互作机制,有助于理解不同农业管理过程中土壤功能演变对大豆增产和农业节本增效的影响。
3 分析结论与“十四五”研发展望大豆产地土壤环境与微生态过程的研究工作开展近20年以来,针对除草剂与重金属污染、以及地下病害发生与防治的研究已取得重大突破。2000年以来,国际上相关研究的主要热点可以概括归纳为除草剂的土-水界面吸附与迁移过程、重金属污染的食物链安全风险、大豆生长与污染毒理、地下病害防治等方面。目前,国际上更加关注影响大豆高产创建和品质安全的除草剂残药危害和重金属解毒生理机制,在地下病害生物防治方面,相关病原真菌/卵菌的侵染、寄生以及大豆抗病分子机理是主要的热点,病原菌与大豆根际土著微生物的网络互作关系也正在成为最新的研究前沿。但是,各国学者更多关注大豆抵抗污染胁迫和病害的逆境适应性生理调节机制,缺少对影响大豆生长和引起大豆减产的地下土壤过程的研究。中国近年来在本领域的研究主要围绕大豆重金属积累及解毒机制、重金属污染修复、病原体株系鉴定与大豆抗病机制等展开,虽然科研产出位于世界前列,尤其是近5年的成果质量逐渐向国际看齐,但结合文献计量分析来说,缺乏系统性,与国际水平尚存在差距,尤其是对于大豆产区的地下土壤环境过程与微生态效应的关注较少。
在当前的新形势下,国家粮食安全战略调整及农业供给侧结构性改革对我国大豆产业提出了更高要求,如何结合主粮丰产增效和污染耕地安全利用攻坚战,更加凸显产地土壤环境保护与功能提升在大豆绿色生产和高质量发展中的作用,以增强国产大豆自给力和竞争力,是当前大豆产业发展面临的巨大挑战。未来,围绕大豆产业的研究迫切需要注重从只聚焦土壤肥力、优化育种及栽培生理、追求大豆产量,向同时关注土壤安全与微生态健康、保证大豆质量安全、支撑大豆产业高质量绿色发展的重大转变。协同大豆产地土壤健康与污染防控的高产创建是实现这一转变并解决提升国产大豆自给力的“卡脖子”风险核心技术的关键纽带。有鉴于此,后续工作应更加注重除草剂、重金属和病原生物的地下过程研究,尤其是如何基于土壤环境与微生态过程的研究降低历史遗留或前茬残留除草剂的残药危害、减少重金属的食物链迁移、增强大豆抵抗病害的能力。建议在微观机制方面,从分子水平上探讨大豆产地土壤中功能微生物(含大豆内生微生物、根际微生物组)在除草剂残留/重金属污染胁迫下相关功能基因的表达,并从地下微生态动态响应与地下-地上适应反馈的角度,基于根际免疫调控的新思路,系统探讨污染物及病原生物根际过程对大豆高产创建和品质提升、土壤环境功能及健康质量的影响;在对接产业发展需求方面,通过产、学、研、政联合,以及岗岗联合、岗站对接,瞄准大豆产地土壤生态功能优化与高产创建的综合调控原理与技术研发来整体推进,系统开展相关共性、关键方法原理及技术的研究、集成、试验和示范,保障公众“舌尖上的安全”和维护大豆产地土壤生态系统平衡健康,引领国产大豆产业的健康有序发展。支撑上述研究的关键科学研发任务建议包括:
1)大豆产地土壤典型除草剂复合污染防控与修复
瞄准环境友好型除草剂残药危害的产业问题,调研国内大豆产地作物种植全周期除草剂施用状况,筛选建立适用于不同粮豆轮作制度的典型污染因子监测指标体系,探明东北、黄淮海及南方区域不同种植制度(含玉米-大豆轮作、小麦-大豆轮作、大豆单作)土壤中除草剂的复合污染与结合残留特征;评估环境友好型除草剂土壤系统结合残留的长期暴露效应与风险,重点关注宏观尺度下土壤生态网络与微观尺度下土壤生态功能的长期动态响应,厘清除草剂长期施用对土壤关键微生物调控养分循环和地力提升的影响机理,在分子生物学基因水平上阐明除草剂复合污染与结合残留的大豆高产障碍介导机制,基于同位素示踪的结合残留污染削减原理研究,构建大豆产地除草剂残药危害的绿色削减与轻简化阻控技术。
2)基于根际免疫的大豆病害综合防控新原理与方法
瞄准大豆地下病害频发的产业问题,定期对大豆产地地下病原体(细菌、真菌、病毒)进行普查,表征其丰度、多样性及区域分布特征,基于微流控技术超高通量挖掘土壤难培养病原体暗物质,提高对产地土壤病原体认知的精准度;搭建基于多组学技术的大豆根际微生物培养组学分析平台,深度挖掘大豆根际病原体关键拮抗微生物资源库;厘清大豆地下病害发病规律与生物、非生物因子间的潜在联系,明确病原体与土壤组分(含矿物、有机质)相互作用的多要素耦合界面过程、及其在调控土壤病毒-原核生物-原生动物多营养级微食物网动态演化过程中的影响作用,阐明环境/条件致病的土壤生态学机制,发展完善地下病害发病过程及土壤生态防控的基础理论;构建以生物防治为主的绿色防控技术,研发新型多功能微生物生防关键技术和核心产品,基于大豆根际免疫强化推进大豆地下病害防治的专业化、绿色化,形成大豆产地土壤地下病害绿色生态调控理论与技术体系。
3)南方重金属污染土壤上青贮大豆替代种植技术与强化应用的成套措施
结合主粮丰产增效和污染耕地安全利用,监测南方大豆产地土壤重金属污染特征,协同分析土壤与大豆籽粒中重金属累积的对应关系,评价大豆籽粒的重金属污染安全风险;在水稻产区不易或不能开展水稻安全种植的污染区域(如重金属地质高背景山区、重度污染区等)推行青贮大豆替代种植,开展重金属低积累青贮大豆育种、土宜性品种筛选及其污染适应性的生理与分子机制研究,在玉米产区推行玉米-大豆带状复合种植,通过重金属低积累耐阴大豆品种选育及配套间作效应优化,在保障玉米不减产的前提下增收大豆,提升污染耕地粮食种植利用率;在此基础上,协同大豆种植过程,开展基于水肥耦合优化的不同区域重金属污染同步钝化及其稳定性和安全性研究,构建重金属污染产地土壤高效钝化-农艺调控-大豆低吸耦合技术,集成适用于南方重金属污染土壤上青贮大豆替代种植的技术体系与强化应用成套措施。
| [1] |
Zeng X M. The strategic planning of soybean industry development in China (In Chinese)[J]. Chinese Journal of Agricultural Resources and Regional Planning, 2017, 38(9): 89-97. [曾学明. 我国大豆产业发展战略规划研究[J]. 中国农业资源与区划, 2017, 38(9): 89-97.]
(  0) 0) |
| [2] |
Gu Q P, Zhou J, Du J D. China's soybean industry safety analysis based on the perspective of trade (In Chinese)[J]. Soybean Science, 2015, 34(2): 314-319. [谷强平, 周静, 杜吉到. 基于贸易视角的中国大豆产业安全分析[J]. 大豆科学, 2015, 34(2): 314-319.]
(  0) 0) |
| [3] |
Teng F, Wang L M, Liu J. Analysis on the potential of soybean imports of China under the background of Sino-US trade friction (In Chinese)[J]. China Agricultural Informatics, 2018, 30(5): 102-109. [滕飞, 王利民, 刘佳. 中美贸易摩擦背景下中国大豆进口潜力分析[J]. 中国农业信息, 2018, 30(5): 102-109.]
(  0) 0) |
| [4] |
Cui G, Jiao Y P. China's soybean trade from the perspective of national food security (In Chinese)[J]. Social Science, 2019(2): 13-28. [崔戈, 焦玉平. 国家粮食安全视角下的中国大豆贸易[J]. 社会科学, 2019(2): 13-28.]
(  0) 0) |
| [5] |
Zhang T L, Wang X X. Prevention and remediation of soil contamination to strengthen the foundation for green and high-quality agricultural development in China (In Chinese)[J]. Acta Pedologica Sinica, 2019, 56(2): 251-258. [张桃林, 王兴祥. 推进土壤污染防控与修复厚植农业高质量发展根基[J]. 土壤学报, 2019, 56(2): 251-258.]
(  0) 0) |
| [6] |
Sun H, Yao Z T, Liu Y, et al. Research and analysis on pesticide amount and future trend of soybean field in Heilongjiang Province (In Chinese)[J]. Soybean Science, 2018, 37(6): 932-942. [孙浩, 姚中统, 刘洋, 等. 黑龙江省大豆田农药用量及未来变化趋势研究与分析[J]. 大豆科学, 2018, 37(6): 932-942.]
(  0) 0) |
| [7] |
Hill Z T, Norsworthy J K, Barber L T, et al. Assessing the potential for fluridone carryover to six crops rotated with cotton[J]. Weed Technology, 2016, 30(2): 346-354. DOI:10.1614/WT-D-15-00048.1
(  0) 0) |
| [8] |
Rose T J, van Zwieten L, Claassens A, et al. Phytotoxicity of soilborne glyphosate residues is influenced by the method of phosphorus fertiliser application[J]. Plant and Soil, 2018, 422(1/2): 455-465.
(  0) 0) |
| [9] |
Carranza C S, Aluffi M E, Benito N, et al. Effect of in vitro glyphosate on Fusarium spp. growth and disease severity in maize[J]. Journal of the Science of Food and Agriculture, 2019, 99(11): 5064-5072. DOI:10.1002/jsfa.9749
(  0) 0) |
| [10] |
Larson R L, Hill A L, Fenwick A, et al. Influence of glyphosate on Rhizoctonia and Fusarium root rot in sugar beet[J]. Pest Management Science, 2006, 62(12): 1182-1192. DOI:10.1002/ps.1297
(  0) 0) |
| [11] |
Köhler H R, Triebskorn R. Wildlife ecotoxicology of pesticides:Can we track effects to the population level and beyond?[J]. Science, 2013, 341(6147): 759-765. DOI:10.1126/science.1237591
(  0) 0) |
| [12] |
Shang E P, Xu E Q, Zhang H Q, et al. Spatial-temporal trends and pollution source analysis for heavy metal contamination of cultivated soils in five major grain producing regions of China (In Chinese)[J]. Environmental Science, 2018, 39(10): 4670-4683. [尚二萍, 许尔琪, 张红旗, 等. 中国粮食主产区耕地土壤重金属时空变化与污染源分析[J]. 环境科学, 2018, 39(10): 4670-4683.]
(  0) 0) |
| [13] |
Chen W P, Yang Y, Xie T, et al. Challenges and countermeasures for heavy metal pollution control in farmlands of China (In Chinese)[J]. Acta Pedologica Sinica, 2018, 55(2): 261-272. [陈卫平, 杨阳, 谢天, 等. 中国农田土壤重金属污染防治挑战与对策[J]. 土壤学报, 2018, 55(2): 261-272.]
(  0) 0) |
| [14] |
中华人民共和国环境保护部, 中华人民共和国国土资源部.全国土壤污染状况调查公报2014. State Environmental Protection Administration of China, State Land and Resources Administration. 2014. (  0) 0) |
| [15] |
Li M H, Wang Y Y, Chen J S, et al. Incidence and disease index of soybean diseases in the northeast of China in 2015 (In Chinese)[J]. Soybean Science, 2016, 35(4): 643-648, 671. [李沐慧, 王媛媛, 陈井生, 等. 2015年东北地区大豆田病害种类与危害程度调查研究[J]. 大豆科学, 2016, 35(4): 643-648, 671.]
(  0) 0) |
| [16] |
Executive Editorial Board of Crop Diseases and Insect Pests in China. Crop diseases and insect pests in China (In Chinese). Beijing: China Agriculture Press, 2015: 1307-1431. [中国农作物病虫害委员会. 中国农作物病虫害[M]. 北京: 农业出版社, 2015: 1307-1431.]
(  0) 0) |
| [17] |
Duke S O. The history and current status of glyphosate[J]. Pest Management Science, 2018, 74(5): 1027-1034. DOI:10.1002/ps.4652
(  0) 0) |
| [18] |
Cerdeira A L, Gazziero D L P, Duke S O, et al. Agricultural impacts of glyphosate-resistant soybean cultivation in south America[J]. Journal of Agricultural and Food Chemistry, 2011, 59(11): 5799-5807. DOI:10.1021/jf102652y
(  0) 0) |
| [19] |
Gould F, Brown Z S, Kuzma J. Wicked evolution:Can we address the sociobiological dilemma of pesticide resistance?[J]. Science, 2018, 360(6390): 728-732. DOI:10.1126/science.aar3780
(  0) 0) |
| [20] |
Zobiole L H S, Kremer R J, de Oliveira R S, et al. Glyphosate effects on photosynthesis, nutrient accumulation, and nodulation in glyphosate-resistant soybean[J]. Journal of Plant Nutrition and Soil Science, 2012, 175(2): 319-330. DOI:10.1002/jpln.201000434
(  0) 0) |
| [21] |
Xiao P Y, Liu Y, Cao Y P. Overexpression of G10-EPSPS in soybean provides high glyphosate tolerance[J]. Journal of Integrative Agriculture, 2019, 18(8): 1851-1858. DOI:10.1016/S2095-3119(18)62124-0
(  0) 0) |
| [22] |
Nandula V K, Reddy K N, Rimando A M, et al. Glyphosate-resistant and -susceptible soybean(Glycine max)and canola(Brassica napus)dose response and metabolism relationships with glyphosate[J]. Journal of Agricultural and Food Chemistry, 2007, 55(9): 3540-3545. DOI:10.1021/jf063568l
(  0) 0) |
| [23] |
Datta A, Sindel B M, Kristiansen P, et al. Effect of isoxaflutole on the growth, nodulation and nitrogen fixation of chickpea(Cicer arietinum L.)[J]. Crop Protection, 2009, 28(11): 923-927. DOI:10.1016/j.cropro.2009.07.009
(  0) 0) |
| [24] |
Fan L, Feng Y C, Weaver D B, et al. Glyphosate effects on symbiotic nitrogen fixation in glyphosate-resistant soybean[J]. Applied Soil Ecology, 2017, 121: 11-19. DOI:10.1016/j.apsoil.2017.09.015
(  0) 0) |
| [25] |
Alletto L, Benoit P, Bolognsi B, et al. Sorption and mineralisation of S-metolachlor in soils from fields cultivated with different conservation tillage systems[J]. Soil & Tillage Research, 2013, 128: 97-103.
(  0) 0) |
| [26] |
Soracco C G, Villarreal R, Lozano L A, et al. Glyphosate dynamics in a soil under conventional and no-till systems during a soybean growing season[J]. Geoderma, 2018, 323: 13-21. DOI:10.1016/j.geoderma.2018.02.041
(  0) 0) |
| [27] |
Fenner K, Canonica S, Wackett L P, et al. Evaluating pesticide degradation in the environment:Blind spots and emerging opportunities[J]. Science, 2013, 341(6147): 752-758. DOI:10.1126/science.1236281
(  0) 0) |
| [28] |
Xu X H, Zarecki R, Medina S, et al. Modeling microbial communities from atrazine contaminated soils promotes the development of biostimulation solutions[J]. The ISME Journal, 2019, 13(2): 494-508. DOI:10.1038/s41396-018-0288-5
(  0) 0) |
| [29] |
Hu H Y, Zhou H, Zhou S X, et al. Fomesafen impacts bacterial communities and enzyme activities in the rhizosphere[J]. Environmental Pollution, 2019, 253: 302-311. DOI:10.1016/j.envpol.2019.07.018
(  0) 0) |
| [30] |
Newman M M, Lorenz N, Hoilett N, et al. Changes in rhizosphere bacterial gene expression following glyphosate treatment[J]. Science of the Total Environment, 2016, 553: 32-41. DOI:10.1016/j.scitotenv.2016.02.078
(  0) 0) |
| [31] |
Chaca M V P, Vigliocco A, Reinoso H, et al. Effects of cadmium stress on growth, anatomy and hormone contents in Glycine max(L.)Merr.[J]. Acta Physiologiae Plantarum, 2014, 36(10): 2815-2826. DOI:10.1007/s11738-014-1656-z
(  0) 0) |
| [32] |
Baig M A, Ahmad J, Bagheri R, et al. Proteomic and ecophysiological responses of soybean(Glycine max L.)root nodules to Pb and hg stress[J]. BMC Plant Biology, 2018, 18: 283. DOI:10.1186/s12870-018-1499-7
(  0) 0) |
| [33] |
Haddad S A, Tabatabai M A, Abdel-Moneim A M A, et al. Inhibition of nodulation and nitrogen nutrition of leguminous crops by selected heavy metals[J]. Air, Soil and Water Research, 2015, 8.
(  0) 0) |
| [34] |
Milivojevic D B, Nikolic B R, Drinic G. Effects of arsenic on phosphorus content in different organs and chlorophyll fluorescence in primary leaves of soybean[J]. Biologia Plantarum, 2006, 50(1): 149-151. DOI:10.1007/s10535-005-0092-8
(  0) 0) |
| [35] |
Chen Y X, He Y F, Yang Y, et al. Effect of cadmium on nodulation and N2-fixation of soybean in contaminated soils[J]. Chemosphere, 2003, 50(6): 781-787. DOI:10.1016/S0045-6535(02)00219-9
(  0) 0) |
| [36] |
Chen B C, Wang P J, Ho P C, et al. Nonlinear biotic ligand model for assessing alleviation effects of Ca, Mg, and K on Cd toxicity to soybean roots[J]. Ecotoxicology, 2017, 26(7): 942-955. DOI:10.1007/s10646-017-1823-2
(  0) 0) |
| [37] |
Noctor G, Mhamdi A, Chaouch S, et al. Glutathione in plants:An integrated overview[J]. Plant, Cell & Environment, 2012, 35(2): 454-484.
(  0) 0) |
| [38] |
Malan H L, Farrant J M. Effects of the metal pollutants cadmium and nickel on soybean seed development[J]. Seed Science Research, 1998, 8(4): 445-453. DOI:10.1017/S0960258500004414
(  0) 0) |
| [39] |
Rodriguez J H, Salazar M J, Steffan L, et al. Assessment of Pb and Zn contents in agricultural soils and soybean crops near to a former battery recycling plant in Córdoba, Argentina[J]. Journal of Geochemical Exploration, 2014, 145: 129-134. DOI:10.1016/j.gexplo.2014.05.025
(  0) 0) |
| [40] |
Khan R, Srivastava R, Abdin M Z, et al. Effect of soil contamination with heavy metals on soybean seed oil quality[J]. European Food Research and Technology, 2013, 236(4): 707-714. DOI:10.1007/s00217-013-1926-9
(  0) 0) |
| [41] |
Sarwar N, Imran M, Shaheen M R, et al. Phytoremediation strategies for soils contaminated with heavy metals:Modifications and future perspectives[J]. Chemosphere, 2017, 171: 710-721. DOI:10.1016/j.chemosphere.2016.12.116
(  0) 0) |
| [42] |
Vásquez-Murrieta M, Migueles-Garduño I, Franco-Hernández O, et al. C and N mineralization and microbial biomass in heavy-metal contaminated soil[J]. European Journal of Soil Biology, 2006, 42(2): 89-98. DOI:10.1016/j.ejsobi.2005.10.002
(  0) 0) |
| [43] |
Xu Y L, Seshadri B, Bolan N, et al. Microbial functional diversity and carbon use feedback in soils as affected by heavy metals[J]. Environment International, 2019, 125: 478-488. DOI:10.1016/j.envint.2019.01.071
(  0) 0) |
| [44] |
Roy S, Bhattacharyya P, Ghosh A K. Influence of toxic metals on activity of acid and alkaline phosphatase enzymes in metal-contaminated landfill soils[J]. Australian Journal of Soil Research, 2004, 42(3): 339. DOI:10.1071/SR03044
(  0) 0) |
| [45] |
Oliveira A, Pampulha M E, Neto M M, et al. Mercury tolerant diazotrophic bacteria in a long-term contaminated soil[J]. Geoderma, 2010, 154(3/4): 359-363.
(  0) 0) |
| [46] |
Ao T, Pierce J L, Power R, et al. Effects of feeding different forms of zinc and copper on the performance and tissue mineral content of chicks[J]. Poultry Science, 2009, 88(10): 2171-2175. DOI:10.3382/ps.2009-00117
(  0) 0) |
| [47] |
Kamoun S, Furzer O, Jones J D G, et al. The Top 10 oomycete pathogens in molecular plant pathology[J]. Molecular Plant Pathology, 2015, 16(4): 413-434. DOI:10.1111/mpp.12190
(  0) 0) |
| [48] |
Dean R, van Kan J A L, Pretorius Z A, et al. The Top 10 fungal pathogens in molecular plant pathology[J]. Molecular Plant Pathology, 2012, 13(4): 414-430. DOI:10.1111/j.1364-3703.2011.00783.x
(  0) 0) |
| [49] |
Ajayi-Oyetunde O O, Bradley C A. Rhizoctonia solani:Taxonomy, population biology and management of Rhizoctonia seedling disease of soybean[J]. Plant Pathology, 2018, 67(1): 3-17. DOI:10.1111/ppa.12733
(  0) 0) |
| [50] |
Arruda G M T, Miller R N G, Ferreira M A S V, et al. Morphological and molecular characterization of the sudden-death syndrome pathogen of soybean in Brazil[J]. Plant Pathology, 2005, 54(1): 53-65. DOI:10.1111/j.1365-3059.2005.01116.x
(  0) 0) |
| [51] |
Hartman G L, Chang H X, Leandro L F. Research advances and management of soybean sudden death syndrome[J]. Crop Protection, 2015, 73: 60-66. DOI:10.1016/j.cropro.2015.01.017
(  0) 0) |
| [52] |
Back M, Haydock P, Jenkinson P. Disease complexes involving plant parasitic nematodes and soilborne pathogens[J]. Plant Pathology, 2002, 51(6): 683-697. DOI:10.1046/j.1365-3059.2002.00785.x
(  0) 0) |
| [53] |
Chen S Y, Porter P M, Reese C D, et al. Crop sequence effects on soybean cyst nematode and soybean and corn yields[J]. Crop Science, 2001, 41(6): 1843-1849. DOI:10.2135/cropsci2001.1843
(  0) 0) |
| [54] |
Haarith D, Bushley K E, Chen S Y. Fungal communities associated with Heterodera glycines and their potential in biological control:A current update[J]. Journal of Nematology, 2020, 52: 1-17.
(  0) 0) |
| [55] |
Zhao J, Liu D, Wang Y Y, et al. Evaluation of Bacillus aryabhattai Sneb517 for control of Heterodera glycines in soybean[J]. Biological Control, 2020, 142: 104147. DOI:10.1016/j.biocontrol.2019.104147
(  0) 0) |
| [56] |
Gu S H, Wei Z, Shao Z Y, et al. Competition for iron drives phytopathogen control by natural rhizosphere microbiomes[J]. Nature Microbiology, 2020, 5(8): 1002-1010. DOI:10.1038/s41564-020-0719-8
(  0) 0) |
| [57] |
Schulz-Bohm K, Gerards S, Hundscheid M, et al. Calling from distance:Attraction of soil bacteria by plant root volatiles[J]. The ISME Journal, 2018, 12(5): 1252-1262. DOI:10.1038/s41396-017-0035-3
(  0) 0) |
| [58] |
Kwak M J, Kong H G, Choi K, et al. Rhizosphere microbiome structure alters to enable wilt resistance in tomato[J]. Nature Biotechnology, 2018, 36: 1100-1109. DOI:10.1038/nbt.4232
(  0) 0) |
| [59] |
Mendes L W, Raaijmakers J M, de Hollander M, et al. Influence of resistance breeding in common bean on rhizosphere microbiome composition and function[J]. The ISME Journal, 2018, 12(1): 212-224. DOI:10.1038/ismej.2017.158
(  0) 0) |
| [60] |
Mendes L W, Mendes R, Raaijmakers J M, et al. Breeding for soil-borne pathogen resistance impacts active rhizosphere microbiome of common bean[J]. The ISME Journal, 2018, 12(12): 3038-3042. DOI:10.1038/s41396-018-0234-6
(  0) 0) |
| [61] |
Wang X F, Wei Z, Yang K M, et al. Phage combination therapies for bacterial wilt disease in tomato[J]. Nature Biotechnology, 2019, 37(12): 1513-1520. DOI:10.1038/s41587-019-0328-3
(  0) 0) |
| [62] |
Xiong W, Li R, Ren Y, et al. Distinct roles for soil fungal and bacterial communities associated with the suppression of vanilla Fusarium wilt disease[J]. Soil Biology & Biochemistry, 2017, 107: 198-207.
(  0) 0) |
| [63] |
Xiong W, Song Y Q, Yang K M, et al. Rhizosphere protists are key determinants of plant health[J]. Microbiome, 2020, 8: 27. DOI:10.1186/s40168-020-00799-9
(  0) 0) |
| [64] |
Kremer R J, Means N E. Glyphosate and glyphosate-resistant crop interactions with rhizosphere microorganisms[J]. European Journal of Agronomy, 2009, 31(3): 153-161. DOI:10.1016/j.eja.2009.06.004
(  0) 0) |
| [65] |
Zobiole L H S, Kremer R J, Oliveira R S Jr, et al. Glyphosate affects micro-organisms in rhizospheres of glyphosate-resistant soybeans[J]. Journal of Applied Microbiology, 2011, 110(1): 118-127. DOI:10.1111/j.1365-2672.2010.04864.x
(  0) 0) |
| [66] |
Chaparro J M, Sheflin A M, Manter D K, et al. Manipulating the soil microbiome to increase soil health and plant fertility[J]. Biology and Fertility of Soils, 2012, 48(5): 489-499. DOI:10.1007/s00374-012-0691-4
(  0) 0) |
| [67] |
Wei Z, Gu Y A, Friman V P, et al. Initial soil microbiome composition and functioning predetermine future plant health[J]. Science Advances, 2019, 5(9): eaaw0759. DOI:10.1126/sciadv.aaw0759
(  0) 0) |
| [68] |
de Vries F T, Griffiths R I, Knight C G, et al. Harnessing rhizosphere microbiomes for drought-resilient crop production[J]. Science, 2020, 368(6488): 270-274. DOI:10.1126/science.aaz5192
(  0) 0) |
| [69] |
Obour A K, Stahlman P W, Holman J D. Soil chemical properties as influenced by long-term glyphosate-resistant corn and soybean production in the central Great Plains, USA[J]. Geoderma, 2016, 277: 1-9. DOI:10.1016/j.geoderma.2016.04.029
(  0) 0) |
| [70] |
Liu B, Shen W S, Wei H, et al. Rhizoctonia communities in soybean fields and their relation with other microbes and nematode communities[J]. European Journal of Plant Pathology, 2016, 144(3): 671-686. DOI:10.1007/s10658-015-0805-6
(  0) 0) |
| [71] |
Wagner A, Norris S, Chatterjee P, et al. Aquatic pseudomonads inhibit oomycete plant pathogens of Glycine max[J]. Frontiers in Microbiology, 2018, 9: 1007. DOI:10.3389/fmicb.2018.01007
(  0) 0) |
| [72] |
Lu X X, Zhou D M, Chen X, et al. Isolation and characterization of Bacillus altitudinis JSCX-1 as a new potential biocontrol agent against Phytophthora sojae in soybean[Glycine max(L.)Merr.][J]. Plant and Soil, 2017, 416(1/2): 53-66.
(  0) 0) |
| [73] |
Wang J C, Wang J G, Bughio M A, et al. Flavonoid levels rather than soil nutrients is linked with Fusarium community in the soybean[Glycine max(L.)Merr.] rhizosphere under consecutive monoculture[J]. Plant and Soil, 2020, 450(1/2): 201-215.
(  0) 0) |
 2021, Vol. 58
2021, Vol. 58


