2. 中国科学院亚热带农业生态研究所农业生态系统过程重点实验室, 长沙 410125;
3. 中南林业科技大学环境科学与工程学院, 长沙 410004
2. Key Laboratory of Agro Ecological Processes in Subtropical Region, Institute of Subtropical Agriculture, Chinese Academy of Sciences, Changsha 410125, China;
3. School of Environmental Science and Engineering, Central South Forestry University, Changsha 410004, China
土壤有机碳(SOC)是土壤碳库的重要组成部分,其含量可以反映土壤肥力的高低,增加SOC含量对提高土壤肥力和作物产量具有重要意义[1]。在农田生态系统中,土壤有机碳主要来源于根系分泌物、作物残体以及人为施入有机肥等,并通过土壤微生物的分解与转化形成微生物残留物等最终贮存于土壤有机碳库中[2]。有机碳在土壤中的稳定性,主要受有机碳结构、微生物可接触性和土壤理化性质的影响[3-5]。其中,有机碳与土壤矿物相互作用,形成有机-无机复合物对土壤有机碳的形成与稳定至关重要。
铁氧化物特殊的物理化学性质(例如,比表面积大、吸附络合能力强、晶态结构复杂,并易于发生氧化还原转化和晶相转化),使其很容易与土壤有机碳通过表面吸附和物理包裹等形成有机-矿物复合物,构成了对亚热带土壤有机碳的特有矿物保护机制[6-8]。铁氧化物在土壤中的主要赋存形态包括:游离态氧化铁、络合态氧化铁,无定型态氧化铁和高结晶度稳定型氧化铁[9]。弱晶态的无定型氧化铁因其具有较大的比表面积和吸附位点,通常能吸附固定土壤中的有机碳,然而无定型铁氧化易于被还原溶解,所以吸附的有机碳会被重新释放到土壤中被微生物分解矿化,因而铁氧化物吸附态有机碳在土壤中的稳定较弱。而高结晶度氧化铁虽然对有机碳的吸附能力相对较弱,但是其在由低结晶度转化为高结晶度氧化铁过程中,能够通过次生铁矿的形成,逐层覆盖和包裹吸附在原来低结晶度氧化铁表面吸附的有机碳,这种被高结晶度氧化铁包裹的有机碳,较难被微生物利用,因而其稳定性也相对较高[7-8,10]。Barral等[11]及胡国成和章明奎[12]研究发现不同形态铁氧化物对团聚体稳定性的影响不同,且团聚体稳定性与游离态铁氧化物的含量成正相关关系,其主要通过络合作用的方式与有机碳结合形成化学稳定的有机络合物,从而提高有机碳的稳定性。Lalonde[10]和Kleber[13]等研究发现有机碳分子与铁离子之间的包裹态并非一次性完成的,而是随着铁、碳扩散聚集下多次反复形成一种类似于洋葱的结构,从而有利于减弱微生物对有机碳的分解[14]。因此,研究土壤中铁氧化物含量、含铁矿物结构及其与有机碳的结合形式,对探究土壤有机碳转化与稳定具有重要意义。
土壤中有机碳与矿物的吸附和解吸过程是动态的,而且由于铁矿的还原溶解和再成矿,使土壤中碳铁复合物处于一个动态形成与分解过程。因此,在土壤碳铁复合物中的有机碳也会参与土壤碳循环过程。Kalbitz等[15]通过培养试验研究表明,吸附态有机碳组分的矿化量可达到溶液中DOC矿化量的六分之一。Rumpel等[16]制备有机碳与铁矿形成包裹态复合物,重新加入土壤进行矿化实验,发现约有2%的有机碳被矿化释放。所以,不同结构态的碳铁复合物在土壤中的矿化速率取决于有机碳与铁矿的结合形式与稳定性。因此,通过研究有机无机复合物的矿化特征,可以判断其稳定性强度及其对土壤有机碳积累的贡献。
我国稻田土壤面积广阔,近30年来有机碳储量显著增加,显示出了较大的固碳潜力[17]。亚热带稻田土壤铁含量较高,由于自身的湿地属性和频繁的氧化-还原交替过程,使铁氧化物在有机碳的吸附固定过程中起着重要作用。同时,由于铁氧化物还原过程中会重新释放有机碳,所以稻田土壤中碳铁复合物的周转过程尤其复杂。因此,为研究稻田土壤中铁氧化物与有机碳结合的微生物矿化特征,及其对土壤原有有机碳矿化的激发效应,本研究选择13C标记葡萄糖作为典型小分子有机碳,通过制备针铁矿吸附态和包裹态葡萄糖,研究不同铁矿结合态有机碳的矿化特征及其激发效应,探究稻田土壤中碳铁复合物的稳定机制及其对土壤有机碳积累的贡献。
1 材料与方法 1.1 供试土壤供试土壤采自湖南省浏阳市龙伏镇龙伏社区(27°51′-28°34′ N,113°10′-114°15′ E)长期种植水稻的试验地,采样地主要为花岗闪长岩高度风化后发育的花岗岩红壤,属于亚热带季风湿润气候,年总日照天数64 d,年均降雨量1 592 mm,年均气温17.5℃。采集耕作层(0~20 cm)土壤样品,人工剔除可见的石块和动植物残体后运回实验室。一部分土壤样品风干后过2 mm和0.149 mm筛,用于土壤理化性质的测定(表 1)。剩余土样过2 mm筛,在25℃恒温、黑暗条件下淹水预培养30 d。
|
|
表 1 供试土壤基本理化性质 Table 1 Physiochemical properties of the soil |
针铁矿(Goe)的制备是将90 mL 5.0 mol·L–1的NaOH快速倒入盛有50 mL 1.0 mol·L–1的FeCl3·6H2O的水浴罐中,在70 ℃水浴锅中水浴60 h,期间搅拌2~3次,冷却后静置,倒去上清液,调节pH至6.5~7.5,烘干后过100目筛备用[18]。包裹态碳铁复合物(Goe*G)的制备是在加入NaOH溶液之前,将50 mL 13C-葡萄糖溶液(5 atom% 13C)加入1 L水浴罐中,其余步骤余与针铁矿制备方法一致。吸附态针铁矿(Goe-G)的制备方法是将60 g针铁矿倒入装有13C-葡萄糖溶液(5 atom % 13C)的震荡瓶中,在25℃下震荡24 h。震荡结束后离心,将下层沉淀冷冻干燥后备用。
1.3 土壤室内模拟培养实验通过13C标记葡萄糖和针铁矿,制备不同形态碳铁复合物。共设置5个处理:(1)土(Soil);(2)土+针铁矿(Soil + Goe);(3)土+葡萄糖(Soil + Glu);(4)土+吸附态针铁矿(Soil + Goe-G);(5)土+包裹态针铁矿(Soil + Goe*G),每个处理重复3次。具体步骤为:称取预培养土壤20 g(干土计)于500 mL厌氧瓶中,分别按上述处理对实验材料进行添加,添加量及其基本性质如表 2所示,再根据质量加入一定量的蒸馏水(水/土:1/1.5);在25℃黑暗条件下淹水培养。另设置一个完全空白对照(只添加水)。于培养后的1、3、5、7、10、15、20、25、30、35、40、45、50、55、60、70、80、90、100和120 d采集气体。
|
|
表 2 铁氧化物和碳铁复合物的基本性质 Table 2 Basic properties of the iron oxides and carbon-goethite association used in the experiment |
土壤pH采用电位法(水土比2.5∶1)测定;土壤黏粒含量采用吸管法测定;土壤有机碳(SOC)采用重铬酸钾外加热法测定;全氮(TN)采用半微量凯氏法测定;土壤溶解性有机碳(DOC)采用湿氧化法—有机碳分析仪(岛津Vwp,日本)测定;碱解氮(AN)采用碱解扩散法测定;全磷(TP)采用碱熔-钼锑抗比色法测定;有效磷(Olsen-P)采用0.05 mol·L–1HCl和0.025 mol·L–1(1/2H2SO4)浸提—钼锑抗比色法测定;土壤微生物生物量碳(MBC)采用氯仿熏蒸培养法和0.5 mol·L–1K2SO4溶液浸提后用湿氧化法—有机碳分析仪(岛津Vwp,日本)测定;CO2和CH4采用气象色谱法—温室气体气相色谱仪(7890 A Agilent GC6890,Agilent Technologies,Palo Alto,CA,USA)测定;13CO2和13CH4采用稳定性同位素质谱仪(MAT 253,Thermo Fisher Scientific,Waltham,MA,USA)测定;土壤全铁含量采用HF-HNO3-HClO4消煮—原子吸收分光光度法测定。
1.5 数据处理在土壤中添加不同形态13C-葡萄糖-铁矿复合物进行培养,土壤原有碳和外源碳矿化产生的CO2气体释放量计算公式为:
| $\begin{array}{l} {{\rm{C}}_{{\rm{SOC}}}}{\rm{ = }}{{\rm{C}}_{{\rm{measure}}}}{\rm{ \times (}}{{\rm{ \mathsf{ δ} }}^{{\rm{13}}}}{\rm{C}}{{\rm{O}}_{{\rm{2}}\;{\rm{measure}}}} - {{\rm{ \mathsf{ δ} }}^{{\rm{13}}}}{\rm{C}}{{\rm{O}}_{{\rm{2}}\;{\rm{glucose}}}})/\\ (\begin{array}{*{20}{l}} {{{\rm{ \mathsf{ δ} }}^{{\rm{13}}}}{\rm{C}}{{\rm{O}}_{{\rm{2}}\;{\rm{SOC}}}} - {{\rm{ \mathsf{ δ} }}^{{\rm{13}}}}{\rm{C}}{{\rm{O}}_{{\rm{2}}\;{\rm{glucose}}}})} \end{array} \end{array} $ | (1) |
| $\begin{array}{*{20}{l}} {{{\rm{C}}_{{\rm{glucose}}}}{\rm{ = }}{{\rm{C}}_{{\rm{measure}}}} - {{\rm{C}}_{{\rm{SOC}}}}} \end{array} $ | (2) |
式中,CSOC为来源于土壤原有有机碳(SOC)的释放的CO2量;Cmeasure为各处理释放的CO2-C总量(mg kg–1);δ13CO2 measure为总CO2的13C丰度;δ13CO2 SOC为SOC的13C丰度(自然丰度对照);δ13CO2 glucose为外源葡萄糖-13C的13C丰度;Cglucose为13C-葡萄糖释放的CO2量。
土壤原有碳和外源碳矿化作用产生的CH4释放量计算同上。
葡萄糖-13C的矿化率用各采样时间点的CO2-13C和CH4-13C总释放量与加入土壤中的葡萄糖13C总量比值表示。
激发效应(PE)计算公式:PE = C总-13C−CSOC式中,C总-13C为添加了葡萄糖-13C处理的中土壤原有有机碳释放的CO2量,CSOC为对照组土壤有机碳CO2释放量。
CH4激发效应同上。
葡萄糖-13C在土壤中的百分含量采用双库模型进行拟合,公式如下:
| $\begin{array}{*{20}{l}} {S = {{\rm{a}}_1} \times {{\rm{e}}^{-{\rm{K}}1t}} + {{\rm{a}}_2} \times {{\rm{e}}^{-{\rm{K}}2t}}} \end{array} $ | (3) |
| $\begin{array}{*{20}{l}} {{T_{1/2}} = \ln (2)/{{\rm{K}}_1}} \end{array} $ | (4) |
式中,a1、a2分别表示葡萄糖-13C的快库、慢库所占比例,S为13C在土壤中的比例,t为培养时间,K1、K2分别表示葡萄糖-13C快库、慢库的矿化速率常数。T1/2表示快库的半衰期。
以上计算均为3次重复的平均值,数据整理采用Microsoft Excel 2010,数据处理及方差分析采用SPSS18.0,采用Origin 8.5进行绘图及双库模型分析。
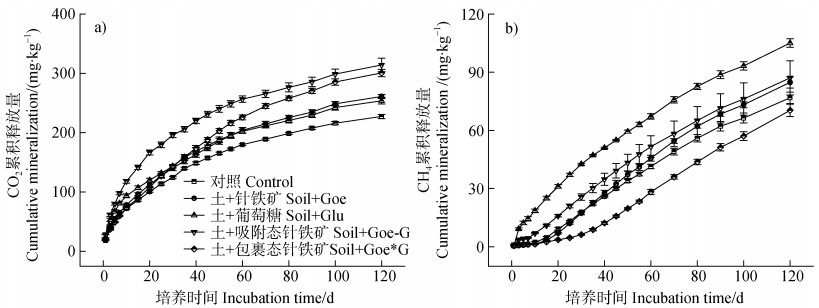
2 结果 2.1 不同结合态碳铁复合物对稻田土壤有机碳矿化的影响针铁矿、葡萄糖和碳铁复合物的添加显著增加了土壤CO2的累积释放量(图 1a)。在0~120 d培养期间,CO2累积释放量前期(0~10 d)快速增加,后期(80~120 d)趋于平缓。培养试验120 d时,Goe、Glu、Goe-G和Goe*G添加条件下CO2的累积释放量较对照处理分别增加了14.8%、11.6%、38.2%和32.3%。整体而言,葡萄糖与铁矿的添加促进了CO2的释放,具体表现为Goe-G > Goe*G > Goe > Glu。其中Goe-G和Goe*G处理CO2释放量显著大于Goe和Glu处理;但Goe-G和Goe*G处理,以及Goe和Glu处理间无显著差异。
|
图 1 不同形态碳铁复合物添加条件下CO2(a)和CH4(b)的累积释放量 Fig. 1 Cumulative release of CO2(a)and CH4(b)after addition of carbon-goethite association relative to form |
针铁矿和针铁矿吸附形成的碳铁复合物增加了土壤CH4的累积释放量(图 1b)。120 d时,在各个添加处理中,单独添加葡萄糖使CH4释放量增加了36.7%;针铁矿及其铁复合物的添加使CH4累积释放量在整个培养期内稳步释放,其中Goe和Goe-G添加处理使CH4的释放分别增加了7.95和10.24 mg·kg–1,Goe*G处理则使CH4的释放量减少了8.5%。
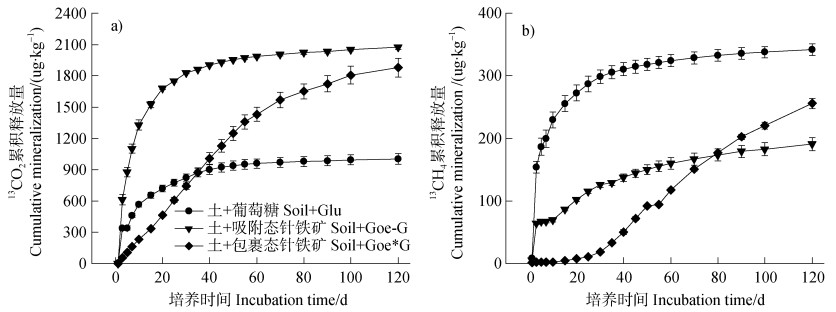
2.2 外源葡萄糖-13C和土壤原有有机碳的矿化率相较于单独添加葡萄糖处理,碳铁复合物中葡萄糖矿化生成13CO2的比例明显增加(图 2a),生成13CH4的比例却降低了(图 2b)。120 d时,只添加葡萄糖的处理中以13CO2的形式释放了35.08%的葡萄糖-13C,以13CH4的形式释放了11.95%的葡萄糖-13C;而添加Goe-G和Goe*G的处理则以13CO2的形式释放了53.45%和48.82%的葡萄糖-13C,以13CH4的形式释放了4.92%和6.65%的葡萄糖-13C。
|
图 2 不同碳铁复合物中葡萄糖的累积释放量 Fig. 2 Cumulative release of glucose-C in carbon-goethite association relative to form |
针铁矿及其碳铁复合物显著促进了土壤原有有机碳矿化生成CO2(图 3a),但降低了生成CH4的比例(图 3b)。相较于外源碳的矿化率,土壤原有有机碳(SOC)的矿化率整体上表现出了相一致的趋势,SOC矿化生成CO2的比例在前期(0~10 d)表现出快速升高,后期增长缓慢的趋势。120 d时,与只添加葡萄糖的处理相比,碳铁复合物的添加促进了土壤原有有机碳矿化生成CO2。与只添加Glu的处理相比,碳铁复合物添加抑制了CH4的产生。120 d后,Goe-G和Goe*G处理土壤原有有机碳释放CH4的比例率分别为0.61%和0.46%。

|
图 3 土壤原有有机碳矿化生成CO2(a)和CH4(b)的比例 Fig. 3 Percentage of the native SOC mineralized to CO2(a)and CH4(b) |
不同结构碳铁复合物-13C输入条件下其矿化速率、半衰期、快库和慢库的分配比例也存在差异(表 3)。运用一级动力学双指数模型对不同形态碳铁复合物-13C向快库和慢库的分配进行拟合,拟合结果显示:只添加Glu的处理,有38.5%葡萄糖-13C为快库,61.6%为慢库;而添加Goe-G和Goe*G的处理,则分别有52.6%和78.1%的葡萄糖-13C为快库,52.2%和24.6%为慢库;碳铁复合物的添加促进了外源碳向快库转化。而碳铁复合物的添加下葡萄糖-13C快库的半衰期(T1/2)、快库分解速率(K1)和慢库分解速率(K2)也存在差异;其中,只添加Glu的处理T1/2、K1和K2分别为5.7 d、44.5 d和0.5 d;而添加Goe*G处理的T1/2高于只添加葡萄糖和吸附态针铁矿处理为55.7 d,K1和K2则显著低于只添加葡萄糖和吸附态针铁矿处理,分别为4.6 d和0 d。总的来说,针铁矿及其复合物转化为快库的比例及半衰期高于单独添加葡萄糖,且Goe*G中有机碳的半衰期是单独葡萄糖的约10倍。
|
|
表 3 外源葡萄糖-13C的双库转化特征 Table 3 Characteristics of the shift of input glucose-13C between the two pools |
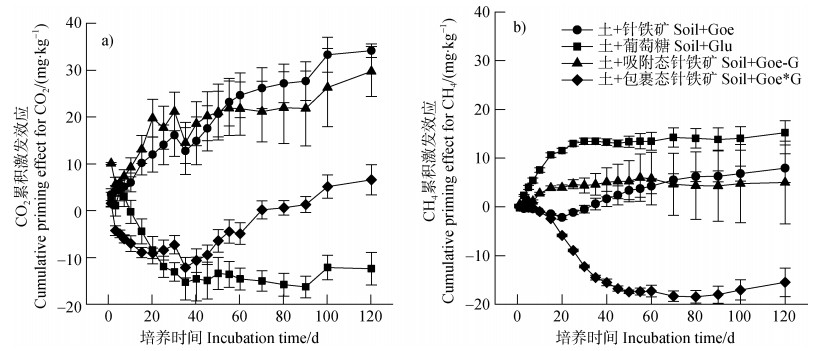
针铁矿、葡萄糖及其碳铁复合物加入土壤后,相对于对照处理均不同程度地影响了土壤原有有机碳的CO2和CH4的释放速率。在整个培养期内,只添加Glu的处理CO2为负累积激发效应,而添加不同形态铁氧化物及其碳铁复合物的处理表现为正累积激发效应;其中,Goe*G在前期(0~30 d)为负激发效应,后期逐渐变为正激发效应。120 d时,CO2累积激发效应大小顺序为:Goe > Goe-G > Goe*G > Glu(图 4a)。与只添加针铁矿的处理相比,Goe-G和Goe*G的添加均表现负PECO2和负PECH4;CH4累积激发效应大小顺序为:Glu > Goe > Goe-G > Goe*G(图 4b);120 d培养期内,针铁矿包裹态葡萄糖对土壤有机质CO2累积激发效应表现为较弱的正激发(6.44 mg·kg–1),而对土壤有机质CH4累积激发效应则表现为负激发(–15.49 mg·kg–1),即针铁矿包裹态葡萄糖的添加抑制了土壤原有有机碳的矿化总激发效应为(–9.05 mg·kg–1)。
|
图 4 不同碳铁复合物添加条件下CO2(a)和CH4(b)累积激发效应 Fig. 4 Cumulative priming effect of carbon-goethite association on CO2(a)and CH4(b)relative to form of the compound |
小分子有机碳是土壤有机碳库中的重要组成部分,尽管在土壤中含量较低但是其作为微生物碳源,在维持土壤微生物生长和土壤元素循环等过程中起重要作用[19]。然而,由于水稻土富含铁铝锰等变价金属元素及其氧化物,所以在水稻土干湿交替过程中,伴随在土壤矿物的晶相转化,土壤中可溶性的小分子有机质会以吸附或是包裹等形式与铁氧化物等结合形成复合物[20]。因此,相较于游离态的小分子有机碳,吸附态和矿物包裹态有机碳与微生物的可接触性以及可利用性均会相应降低。本研究结果表明针铁矿吸附的葡萄糖总矿化率达到了55.4%,显著高于针铁矿包裹态葡萄糖的矿化率(46.8%),这证实了包裹态有机碳的微生物可利用性更低。然而,同时也发现,单独添加葡萄糖处理的葡萄糖矿化率显著低于添加碳铁复合物处理的葡萄糖矿化率,这可能是因为针铁矿的加入为土壤提供了新的电子受体,促进了微生物对电子供体(葡萄糖)的利用[21]。此外,也可能是因为铁矿加入土壤后形成新的活性热区,使土壤微生物更容易接触到铁矿结合的葡萄糖,使针铁矿表面吸附的葡萄糖的矿化率更高。尽管铁矿的加入可以加快土壤微生物的呼吸,但是却显著抑制了甲烷的产生。此外,在培养试验的前80 d,铁矿吸附和包裹的葡萄糖矿化成CH4的比例低于单独添加葡萄糖的处理。这主要是因为土壤中铁的还原电势高于甲烷生成的电势,三价铁更易于获取电子发生还原反应,所以土壤中的铁还原菌优先进行铁还原,抑制了产甲烷过程。而在80 d后,当土壤中铁还原下降到较低速率的时候,产甲烷菌活性得以升高,并主导甲烷产生过程促进甲烷的释放[22-23]。
有机碳矿化动力学模型分析结果表明,碳铁复合物的添加使葡萄糖-13C的快库所占比例以及半衰期大于单独添加葡萄糖,而且针铁矿包裹态葡萄糖向快库转化的比例以及半衰期显著大于吸附态葡萄糖。这主要是因为针铁矿的比表面积较低且结晶度高,通过吸附或包裹态固定的碳很难被微生物利用,导致其半衰期较长,且快库分解速率和慢库分解速率较低。而吸附态与包裹态由于其碳铁结合的方式不同,包裹态是通过有机碳上的羧基与铁矿表面的羟基结合,形成一层一层类似于洋葱包裹的结构[24],从而抑制了微生物与碳的接触;因此,相较于吸附态,碳铁通过包裹态的方式结合更有利于在土壤固定。因此,通过包裹态方式形成的土壤矿物包裹态小分子有机物更易在土壤中长期固存。
3.2 不同结构态碳铁复合物对土壤有机质激发效应的影响伴随铁矿还原溶解过程,矿物结合态有机碳在矿化的同时也影响着土壤原有有机碳的矿化。土壤原有有机碳的激发效应受底物的可利用程度和含量影响,因此,碳铁复合物的结合形式所导致的葡萄糖可利用性影响着其激发效应的方向与强度。单独添加葡萄糖对CO2的产生表现出较强的负激发效应,这可能是因为游离态葡萄糖的输入使得土壤微生物优先利用葡萄糖,抑制了微生物对土壤原有有机碳的矿化,从而产生了负激发效应[25]。铁矿加入产生了明显的正激发效应,这是因为碳铁复合物的添加为铁还原菌提供了碳源和电子受体,形成碳铁耦合,促进铁的异化还原过程并释放CO2[26-27]。而相对于单独添加针铁矿的处理,碳铁复合物的正激发效应相对降低了,主要是因为碳铁复合物中释放出来的葡萄糖能够为微生物提供一定量的碳源,降低了微生物对土壤原有有机碳的矿化程度。相比于碳铁复合物对产生CO2的激发效应,其对CH4激发效应的规律相反,即针铁矿的加入相对于单独添加葡萄糖抑制了激发效应的强度。这也主要是因为铁矿优先竞争电子,抑制甲烷的产生。不同于针铁矿吸附态葡萄糖,针铁矿包裹态葡萄糖使CH4激发效应的方向为负。这可能是因为针铁矿包裹态葡萄糖复合物的制备过程中,葡萄糖的加入降低了针铁矿的结晶度,使得低结晶度的针铁矿较高结晶度的针铁矿更容易被微生物还原,因此对产甲烷的抑制作用也更强,所以对甲烷产生了负激发效应。
4 结论水稻土中添加不同结构碳铁复合物进行淹水培养,针铁矿包裹态碳铁复合物的快速矿化碳库和慢速矿化碳库的转化速率较单独添加葡萄糖和针铁矿吸附态碳铁复合物更低,且半衰期增加了约10倍,表明铁矿包裹态小分子有机碳具有更强的稳定性和滞留时间。针铁矿包裹态葡萄糖在一定程度上促进了CO2激发效应(6.44 mg·kg–1),却抑制了CH4激发效应(–15.49 mg·kg–1),即产生了总的负激发效应(–9.05 mg·kg–1),表明针铁矿包裹态葡萄糖的添加可增强土壤有机碳的积累。水稻土中与铁氧化结合的小分子有机碳相对于游离态的有机碳,具有更强的生物稳定性,而且在土壤有机碳矿化过程中产生负激发效应,有利于保护土壤原有有机碳,增加土壤的长期固碳效应。
| [1] |
张旭博. 中国农田土壤有机碳演变及其增产协同效应[D]. 北京: 中国农业科学院, 2016. Zhang X B. The synergistic effects of evolution of soil organic carbon on increment of crop yield in arable land in China[D]. Beijing: Chinese Academy of Agricultural Sciences, 2016. (  0) 0) |
| [2] |
Lal R. Soil carbon sequestration to mitigate climate change[J]. Geoderma, 2004, 123(1/2): 1-22.
(  0) 0) |
| [3] |
Wu Q B, Wang X K, Guo R. Soil organic carbon stability and influencing factors (In Chinese)[J]. Chinese Journal of Soil Science, 2005, 36(5): 743-747. DOI:10.3321/j.issn:0564-3945.2005.05.026 [吴庆标, 王效科, 郭然. 土壤有机碳稳定性及其影响因素[J]. 土壤通报, 2005, 36(5): 743-747.]
(  0) 0) |
| [4] |
Liu M Q, Chen X Y, Guo J H, et al. Soil biota on soil organic carbon stabilization (In Chinese)[J]. Advances in Earth Science, 2007, 22(2): 152-158. DOI:10.3321/j.issn:1001-8166.2007.02.005 [刘满强, 陈小云, 郭菊花, 等. 土壤生物对土壤有机碳稳定性的影响[J]. 地球科学进展, 2007, 22(2): 152-158.]
(  0) 0) |
| [5] |
An J, Deng B, Han J G, et al. A review: Stability of soil organic carbon (In Chinese)[J]. Grassland and Turf, 2009, 29(2): 82-87. DOI:10.3969/j.issn.1009-5500.2009.02.018 [安静, 邓波, 韩建国, 等. 土壤有机碳稳定性研究进展[J]. 草原与草坪, 2009, 29(2): 82-87.]
(  0) 0) |
| [6] |
Lützow M V, Kögel-Knabner I, Ekschmitt K, et al. Stabilization of organic matter in temperate soils: Mechanisms and their relevance under different soil conditions-A review[J]. European Journal of Soil Science, 2006, 57(4): 426-445. DOI:10.1111/j.1365-2389.2006.00809.x
(  0) 0) |
| [7] |
Wang L, Ying R R, Shi J Q, et al. Advancement in study on adsorption of organic matter on soil minerals and its mechanism (In Chinese)[J]. Acta Pedologica Sinica, 2017, 54(4): 805-818. [王磊, 应蓉蓉, 石佳奇, 等. 土壤矿物对有机质的吸附与固定机制研究进展[J]. 土壤学报, 2017, 54(4): 805-818.]
(  0) 0) |
| [8] |
Zhang Z Y, Zhang Y F. Compared study on different morphological iron and amorphous silica and alumium in the various soils (In Chinese)[J]. Journal of Heilongjiang August First Land Reclamation University, 1989(1): 19-24. [张之一, 张元福. 几种土壤中不同形态铁及无定形硅铝的比较研究[J]. 黑龙江八一农垦大学学报, 1989(1): 19-24.]
(  0) 0) |
| [9] |
Wang L Y, Qin L, Lü X G, et al. Progress in researches on effect of iron promoting accumulation of soil organic carbon (In Chinese)[J]. Acta Pedologica Sinica, 2018, 55(5): 1041-1050. [王璐莹, 秦雷, 吕宪国, 等. 铁促进土壤有机碳累积作用研究进展[J]. 土壤学报, 2018, 55(5): 1041-1050.]
(  0) 0) |
| [10] |
Lalonde K, Mucci A, Ouellet A, et al. Preservation of organic matter in sediments promoted by iron[J]. Nature, 2012, 483(7388): 198. DOI:10.1038/nature10855
(  0) 0) |
| [11] |
Barral M T, Arias M, Guérif J. Effects of iron and organic matter on the porosity and structural stability of soil aggregates[J]. Soil and Tillage Research, 1998, 46(3/4): 261-272.
(  0) 0) |
| [12] |
Hu G C, Zhang M K. Mineralogical evidence for strong cementation of soil particles by iron oxides (In Chinese)[J]. Chinese Journal of Soil Science, 2002, 33(1): 25-27. DOI:10.3321/j.issn:0564-3945.2002.01.007 [胡国成, 章明奎. 氧化铁对土粒强胶结作用的矿物学证据[J]. 土壤通报, 2002, 33(1): 25-27.]
(  0) 0) |
| [13] |
Kleber M, Mikutta R, Torn M S, et al. Poorly crystalline mineral phases protect organic matter in acid subsoil horizons[J]. European Journal of Soil Science, 2005, 56(6): 717-725.
(  0) 0) |
| [14] |
Guggenberger G, Kaiser K. Dissolved organic matter in soil: Challenging the paradigm of sorptive preservation[J]. Geoderma, 2003, 113(3/4): 293-310.
(  0) 0) |
| [15] |
Kalbitz K, Schwesig D, Schmerwitz J, et al. Changes in properties of soil-derived dissolved organic matter induced by biodegradation[J]. Soil Biology & Biochemistry, 2003, 35(8): 1129-1142.
(  0) 0) |
| [16] |
Rumpel C, Eusterhues K, Kögel-Knabner I. Non-cellulosic neutral sugar contribution to mineral associated organic matter in top- and subsoil horizons of two acid forest soils[J]. Soil Biology & Biochemistry, 2010, 42(2): 379-382.
(  0) 0) |
| [17] |
宋丹. 下辽河平原耕地土壤有机碳时空变化及固碳潜力估算[D]. 沈阳: 沈阳农业大学, 2013. Song D. Evolution of soil organic carbon and evaluation of carbon sequestration potential in cultivated land of lower reaches of Liaohe River Plain[D]. Shenyang: Shenyang Agricultural University, 2013. (  0) 0) |
| [18] |
McCormick M L, Adriaens P. Carbon tetrachloride transformation on the surface of nanoscale biogenic magnetite particles[J]. Environmental Science & Technology, 2004, 38(4): 1045-1053.
(  0) 0) |
| [19] |
王越. 不同分子量有机碳施加对土壤团聚体形成影响研究[D]. 南昌: 南昌大学, 2018. Wang Y. Effect of different molecular weights organic carbon on the formation of soil aggregates[D]. Nanchang: Nanchang University, 2018. (  0) 0) |
| [20] |
王莹. 红壤性水稻土铁氧化物的分异特征与固碳机制[D]. 南京: 南京农业大学, 2012. Wang Y. Disstribution of iron oxides and C sequestration in red paddy soil[D]. Nanjing: Nanjing Agricultural University, 2012. (  0) 0) |
| [21] |
谭中欣. 水稻土中铁还原及其电子传递特征研究[D]. 陕西杨凌: 西北农林科技大学, 2003. Tan Z X. Study of microbial iron reduction and electron transfer characteristic in paddy soil[D]. Yangling, Shannxi: Northwest A & F University, 2003. (  0) 0) |
| [22] |
王炳臣. 渤海及其入海河流沉积物中铁还原菌电活性及产甲烷菌多样性的研究[D]. 北京: 中国科学院大学(中国科学院烟台海岸带研究所), 2019. Wang B C. Electrochemical activity of iron reducing bacteria and diversity of methanogens in sediments of bohai sea and its coastal rivers[D]. Beijing: University of Chinese Academy of Sciences(Yantai Institute of Coastal Zone Research, Chinese Academy of Sciences), 2019. (  0) 0) |
| [23] |
赵立芳. 腐植酸、水铁矿及其共沉物对土壤镉的钝化效果研究[D]. 兰州: 兰州大学, 2019. Zhao L F. Study on the passivation effect of humic acid, ferrihydrite and their coprecipitates on cadmium in soils[D]. Lanzhou: Lanzhou University, 2019. (  0) 0) |
| [24] |
Ma X, Wei L, Tang M L, et al. Effects of varying long-term fertilization on organic carbon mineralization and priming effect of paddy soil (In Chinese)[J]. Environmental Science, 2018, 39(12): 5680-5686. [马欣, 魏亮, 唐美玲, 等. 长期不同施肥对稻田土壤有机碳矿化及激发效应的影响[J]. 环境科学, 2018, 39(12): 5680-5686.]
(  0) 0) |
| [25] |
Li L, Qu D. Effects of humic acid on microbial iron(Ⅲ) reduction in paddy soils (In Chinese)[J]. Acta Agriculturae Boreali-occidentalis Sinica, 2008, 17(6): 322-328. DOI:10.3969/j.issn.1004-1389.2008.06.068 [李丽, 曲东. 腐殖酸对水稻土中异化铁还原的影响[J]. 西北农业学报, 2008, 17(6): 322-328.]
(  0) 0) |
| [26] |
Song J X, Wu C, Qu D. The effect of organic carbon on microbial iron reduction in paddy soils (In Chinese)[J]. Journal of Agro-Environment Science, 2013, 32(2): 299-306. [宋建潇, 吴超, 曲东. 有机碳源对水稻土中微生物铁还原特征的影响[J]. 农业环境科学学报, 2013, 32(2): 299-306.]
(  0) 0) |
| [27] |
Zhang T J, Tang J, Zhuang L, et al. Effects of different iron oxides on methane emission in paddy soil as related to drying/wetting cycles (In Chinese)[J]. Environmental Science, 2014, 35(3): 901-907. [张天娇, 汤佳, 庄莉, 等. 干湿交替条件下不同晶型铁氧化物对水稻土甲烷排放的影响[J]. 环境科学, 2014, 35(3): 901-907.]
(  0) 0) |
 2021, Vol. 58
2021, Vol. 58


