2. 中国科学院大学, 北京 100049;
3. 河海大学农业科学与工程学院, 南京 210098
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. College of Agricultural Science and Engineering, Hohai University, Nanjing 210098, China
有机碳矿化是指土壤有机碳分解释放CO2的过程,认识有机碳的矿化规律和影响因素对于阐明土壤碳库的周转过程并对其进行有效调节具有重要作用[1]。土壤团聚体是土壤的基本组成单元,绝大部分的有机碳均以不同形式贮存在团聚体内部或者团聚体间的孔隙中[2],因此有机碳的矿化过程与团聚体的性质和土壤孔隙结构密切相关。
近年来,一些研究采用室内培养法分析了团聚体大小对有机碳矿化的影响,但是结果并不一致。有些研究发现团聚体破碎显著增加了有机碳的矿化量[3-4],也有研究发现团聚体破碎对有机碳矿化量无显著影响[5-7]。针对这些结果,学者们多从有机碳物理保护的角度解释,即团聚体破碎时,被团聚体包裹的有机碳释放出来,导致其矿化量增加[4];如果未破坏微团聚体(<0.25 mm的团聚体)结构,则不会影响有机碳矿化量[7]。然而,团聚体在外力作用下破碎时,也会较大程度地改变土壤孔隙结构[8-10]。孔隙结构影响土壤中水分运输、气体交换及微生物活性,从而可能间接参与有机碳矿化过程[11]。目前关于团聚体改变后引起的孔隙结构变化对有机碳矿化的影响的研究较少,团聚体变化对有机碳矿化的影响机理尚不清楚。孔隙结构的定量分析是阐明这一过程的重要前提。显微CT技术具有高分辨率和对样品非接触、无破损的优势,是准确量化土壤孔隙结构特征的有效方法[12]。因此,应用高分辨率CT技术结合先进的图像分析方法研究土壤孔隙结构,有利于阐明有机碳矿化过程与孔隙结构之间的关系。
红壤广泛分布于我国南方地区,其有机碳含量较低、团聚体结构不稳定[13]。通过施用有机肥等措施能够提高土壤有机碳含量,促进团聚过程,改变土壤结构[14]。本研究选取长期不同施肥处理的土壤样品,通过过筛改变其团聚体大小分布,然后填装土柱,分析其孔隙结构及有机碳矿化等指标,研究团聚体大小对孔隙结构和有机碳矿化的影响。研究将有助于深入探讨土壤团聚体、土壤孔隙结构和有机碳矿化之间的关系。
1 材料与方法 1.1 供试土壤样品土壤样品采集自位于江西省鹰潭市余江县的中国科学院红壤生态实验站(116°55′30″E,28°15′20″N)内的长期定位试验田。该区为中亚热带湿润季风气候,年均温度17.6℃,多年平均降雨量1 795 mm。土壤为第四纪红色黏土母质发育的红壤(黏化湿润富铁土),黏粒、粉粒和砂粒的含量分别为36.3%、42.5%和21.2%。长期定位试验开始于2002年,共有4个施肥处理。每个施肥处理设置3次重复,以顺序区组排列,小区大小为2 m×2 m。供试土壤取自其中3个处理:不施肥(CK);施低量有机肥(LM,N 150 kg·hm-2·a-1);施高量有机肥(HM,N 600 kg·hm-2·a-1)。有机肥为猪粪,来自试验站附近的养殖场,平均pH为7.72,全氮32.9 g·kg-1(干基,下同),全钾14.0 g·kg-1,全磷20.2 g·kg-1,全碳306.5 g·kg-1。种植作物为玉米,品种为苏玉24。每年4月中旬开始种植,7月下旬玉米收获后,至次年4月土地休闲。种植密度为每小区20株,相当于50 000株·hm-2。于2019年7月玉米收获后采集0~20 cm的表层土样,每个小区随机采集3个点混合为一个样品。新鲜土样在室温下风干,挑去根系、石块等,过8 mm筛备用。将同一施肥处理的风干土样均匀混合为CK、LM和HM土壤,基本性质见表 1[15]。
|
|
表 1 供试土壤的基本理化性质 Table 1 Soil physicochemical properties under three fertilization treatments |
将混合后的土样分成3份,分别过5 mm、2 mm和0.5 mm孔径的筛,并标记为S5、S2和S0.5。共得到9个处理:3种土壤(CK、LM和HM土壤)×3个过筛孔径(5 mm、2 mm和0.5 mm)。各处理团聚体大小分布通过干筛法测定,结果见表 2。将每个处理的土样分别填装至直径2.9 cm、高5 cm的聚氯乙烯(Polyvinyl chloride,PVC)环刀中,填装高度为4 cm,填装容重为1.3 g·cm-3。填装土柱时,环刀底部用500目的尼龙网扎紧,然后分两层填装,每层高度为2 cm,第一层填装之后,先将表面打毛,再填装第二层。每个处理填装7个土柱,其中3个用于测定田间持水量和CT扫描,4个用于室内培养测定土壤有机碳矿化量。
|
|
表 2 不同过筛处理下的土壤团聚体大小分布 Table 2 Aggregate size distribution after sieving |
培养试验前,将样品饱和,然后利用压力膜仪于33 kPa下平衡,测定田间持水量。将用于培养试验的土柱的含水量调节为田间持水量的75%,随后将土柱放在4℃的培养箱中平衡3 d,每天补充损失的水分。水平衡结束后,将土柱放入500 mL培养瓶中,将培养瓶随机排列置于22℃的恒温培养箱中避光培养57 d。在培养过程中,为减少土样中水分的损失,在瓶口覆保鲜膜并扎孔保持通气状态,每两天通过称重法补充损失的水分。分别在培养的第1、2、4、8、11、15、22、29、37、43、50和57天时采集培养瓶中的气体。每次采集气体前,先将培养瓶置于22℃室温下通风20min,更新瓶内气体,然后塞紧硅橡胶塞,并用硅橡胶密封瓶口,确保不漏气。塞紧硅橡胶塞后,向培养瓶中注入20 mL新鲜空气,混合均匀后,再从中抽取20 mL气体注入真空集气瓶;培养6 h后,再次向培养瓶中注入20 mL新鲜空气,混合均匀,然后采集20 mL气体。气体采集结束后,去除硅橡胶塞。采集的气体利用气相色谱(Gas chromatography,GC. Agilent 7890A,Agilent Technologies,Santa Clara,CA,USA)测定CO2浓度,进而计算CO2的产生速率(F,mg·kg-1·h-1)以及累积产生量。CO2产生速率的计算公式为[16]:
| $ F=\frac{\rho \times \Delta C \times V \times 273}{W \times \Delta t \times T} $ | (1) |
式中,ρ为标准状态下CO2的密度,0.536 kg·m-3;∆C为一天内两次采气的CO2的浓度差,单位为g·m-3;V为培养瓶中有效空间体积,单位为m3;W为烘干土质量,单位为kg;∆t为一天内两次采气的时间间隔,单位为h;T为培养温度,单位为K。CO2累积产生量为相邻两次测定气体的CO2产生速率的平均值与间隔时间乘积的累加值。
1.4 CT扫描与图像处理土柱在33 kPa下平衡后,利用X射线显微CT(Phoenix Nanotom X-ray μ-CT,GE Sensing and Inspection Technologies GmbH,Wunstorf,Germany)扫描。扫描电压为90 kV,电流为90 μA,曝光时间为1.25 s。样品在样品台水平匀速旋转360°,在此过程中共采集1 201幅投影图,空间分辨率为16 μm。利用Datos|x2 Rec软件进行图像重建,然后利用VG Studio Max 2.2软件生成2302张8位灰度图像,存储为tiff格式。利用ImageJ软件进行图像处理和分析。首先进行中值滤波降低图像的噪声。为减少边际效应和光束硬化引起的伪影,选择图像中心区域作为感兴趣区域(Region of interest,ROI)。ROI的大小为1 500×1 500×900体元,实际大小为24 mm×24 mm×14.4 mm。利用目视法确定阈值,将图像分割为基质和孔隙两部分。由于分辨率的限制,从图像中获取的孔隙均为大于分辨率(16μm)的孔隙,本文中称为大孔隙。孔隙大小分布利用“Thickness”插件计算,将孔隙大小划分为3个等级,分别为16~30 μm、30~100 μm以及>100 μm。孔隙的全局连通性通过下式计算[17]:
| $ \Gamma = \frac{{\sum\nolimits_{i = 0}^n {\left( {V_i^2} \right)} }}{{{{\left( {\sum\nolimits_{i = 0}^n V } \right)}^2}}} $ | (2) |
式中,Γ代表全局连通性,指两个孔隙为同一个孔隙的概率;n代表孔隙的个数,Vi代表每个孔隙的体积,孔隙的数量和体积利用“Particle analyzer”插件计算。
1.5 数据处理运用SPSS 21.0进行数据分析。采用双因素方差分析(Two-way ANOVA)考察施肥处理和团聚体大小分布以及它们的交互作用对孔隙结构及有机碳矿化量的影响;利用最小差异显著法(Least Significant Difference,LSD)进行多重比较,分析同一施肥土壤下不同团聚体处理之间以及同一团聚体处理下不同施肥土壤之间的差异,显著性水平为0.05。数据的正态性检验采用夏皮罗-威尔克检验(Shapiro-Wilk test),方差齐性检验采用列文检验(Levene-test)。
2 结果 2.1 团聚体大小分布对土壤孔隙结构的影响 2.1.1 团聚体大小分布对土壤二维形态特征的影响图 1为不同处理土壤样品的二维灰度图像,图中浅色部分代表土壤基质,深色部分代表土壤孔隙(箭头指向的区域)。从灰度图像可以看出,对于同一施肥处理土壤,S5的大孔隙较多,孔隙多呈长条状,孔隙的连通性较好;S2的孔隙结构与S5差异不明显;而S0.5中由于大团聚体被破坏,大孔隙很少,结构更加均质。

|
注:图中箭头指示的为土壤孔隙。 Note: Arrows indicate pores. 图 1 团聚体大小分布对土壤孔隙二维形态的影响 Fig. 1 Effect of aggregate size distribution on 2-D soil pore morphology |
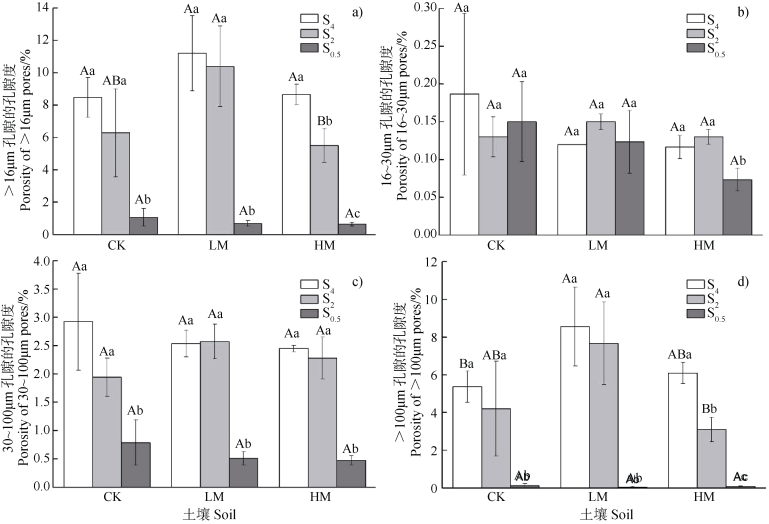
团聚体大小分布对土壤大孔隙度(>16 μm)有极显著的影响(P<0.001)(表 3)。S0.5的大孔隙度最低,较S5和S2分别低87.4%~93.9%和83.0%~93.4%。CK和LM土壤S2与S5的大孔隙度无显著差异(P>0.05),而HM土壤S2的大孔隙度较S5低36.4%(P<0.01)(图 2a)。
|
|
表 3 双因素方差分析结果 Table 3 The results of two-way ANOVA |
|
注:图中误差棒为标准差(n=3)。不同小写字母表示同一施肥土壤下不同团聚体处理之间的差异显著(P<0.05),不同大写字母表示同一团聚体处理下不同施肥土壤之间的差异显著(P<0.05)。 Note: Bars on columns are standard deviations(n=3). Different lowercase letters indicate a significant difference between aggregate size treatments(P<0.05);different uppercase letters indicate a significant difference between fertilization treatments(P<0.05). 图 2 团聚体大小分布对土壤大孔隙度(>16 μm)和孔隙大小分布的影响 Fig. 2 Effect of aggregate size distribution on soil image-based porosity(>16 μm)and pore size distribution |
孔隙大小分布的结果表明,团聚体大小分布对16~30 μm孔隙的孔隙度无显著影响(P>0.05),对30~100 μm和>100 μm孔隙的孔隙度有极显著的影响(P<0.001)(表 3)。S0.5的30~100 μm孔隙的孔隙度最低,较S5和S2分别减少73.1%~80.6%和59.5%~80.4%(P<0.05),而S5与S2之间无显著差异(P>0.05)(图 2c)。S0.5的>100 μm孔隙的孔隙度也显著低于S5和S2,降低的比例为96.9%~99.3%(P<0.05)。S5的>100 μm孔隙的孔隙度高于S2,但只在HM土壤表现出了显著差异(P<0.001)(图 2d)。
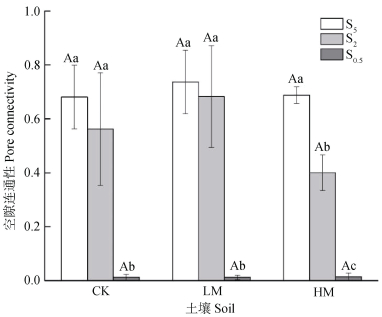
2.1.3 团聚体大小分布对土壤孔隙连通性的影响团聚体大小分布对土壤孔隙连通性有极显著的影响(P<0.001)(表 3)。S0.5的孔隙连通性显著低于S5和S2,降低比例超过95%(P<0.01)。在CK和LM土壤中,S2与S5的孔隙连通性无显著差异(P>0.05),而HM土壤中S2的孔隙连通性较S5低41.8%(P<0.001)(图 3)。
|
注:图中误差棒为标准差(n=3)。不同小写字母表示同一施肥土壤下不同团聚体处理之间的差异显著(P<0.05),不同大写字母表示同一团聚体处理下不同施肥土壤之间的差异显著(P<0.05)。 Note: Bars on columns are standard deviations(n=3). Different lowercase letters indicate a significant difference between aggregate size treatments(P<0.05);different uppercase letters indicate a significant difference between fertilization treatments(P<0.05). 图 3 团聚体大小分布对土壤孔隙连通性的影响 Fig. 3 Effect of aggregate size distribution on soil pore connectivity |
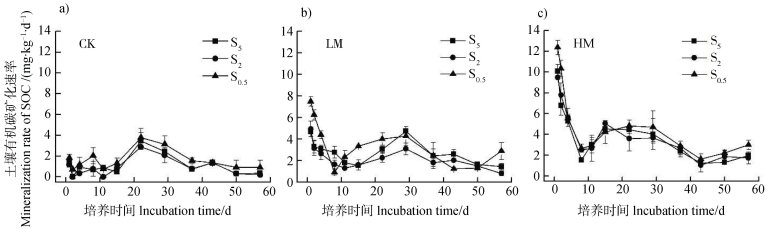
对于CK和HM土壤,S0.5的有机碳矿化速率基本上在整个培养过程中均最高,S5和S2之间无明显的大小顺序;而对于LM土壤,在培养的第8、29、37和43天时,S5的有机碳矿化速率最高,其他时间表现为S0.5处理的有机碳矿化速率最高(图 4)。
|
注:图中误差棒为标准差(n=3)。 Note: Bars are standard deviations(n=3). 图 4 团聚体大小分布对土壤有机碳矿化速率的影响 Fig. 4 Effect of aggregate size distribution on mineralization rate of SOC |
培养期间,CK土壤的有机碳矿化速率较低(<4 mg·kg-1·d-1),除第22和29天矿化速率相对其他时间较高外,其他时间矿化速率波动不大,基本低于2 mg·kg-1·d-1(图 4a)。LM和HM土壤的有机碳矿化速率表现出类似的变化规律,在培养第1天出现峰值,然后降低,至第8天开始回升,在第29天出现第二个峰值(图 4b,图 4c),之后矿化速率下降;但相同时间HM土壤的有机碳矿化速率基本高于LM处理,尤其是第1~4天时,两施肥处理差异最大,HM土壤的有机碳矿化速率较LM土壤高26.2%~147.0%。
2.2.2 团聚体大小分布对土壤有机碳累积矿化量的影响团聚体大小对57 d内的土壤有机碳累积矿化量有极显著的影响(P<0.001)(表 3)。对于CK和HM土壤,S0.5的有机碳累积矿化量显著高于S5和S2(P<0.01),但升高的比例差别较大。CK土壤S0.5的有机碳累积矿化量较S5和S2分别高64.2%和79.1%;HM土壤S0.5的有机碳累积矿化量较S5和S2分别高19.3%和14.1%;两种土壤S5和S2有机碳累积矿化量均无显著差异(P>0.05)。对于LM土壤,S0.5和S5的有机碳累积矿化量无显著差异(P>0.05),分别较S2高38.6%和29.9%(P<0.01)(图 5)。

|
注:图中误差棒为标准差(n=3)。不同小写字母表示同一施肥土壤下不同团聚体处理之间的差异显著(P<0.05),不同大写字母表示同一团聚体处理下不同施肥土壤之间的差异显著(P<0.05) Note: Bars are standard deviations(n=3). Different lowercase letters indicate a significant difference between aggregate size treatments(P<0.05);different uppercase letters indicate a significant difference between fertilization treatments(P<0.05). 图 5 团聚体大小分布对土壤有机碳累积矿化量的影响 Fig. 5 Effect of aggregate size distribution on cumulative SOC mineralization amount |
双因素方差分析显示,施肥处理显著增加了57 d内土壤有机碳的矿化量(P<0.01)(表 3)。同一团聚体处理下,不同施肥土壤的有机碳累积矿化量表现为HM>LM>CK(P<0.05)(图 5)。
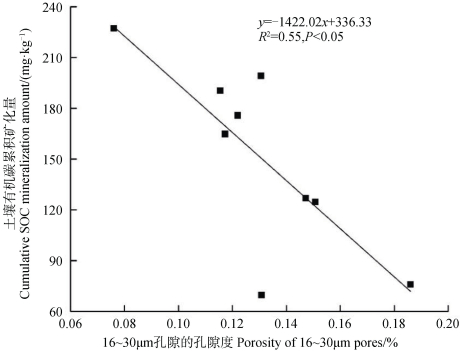
相关分析表明,57 d内的有机碳累积矿化量与16~30 μm孔隙的孔隙度呈显著的负相关关系(P<0.05)(图 6),而与其他孔隙结构参数相关性较弱(数据未列出)。
|
图 6 有机碳累积矿化量与16~30 μm孔隙的孔隙度之间的关系 Fig. 6 Relationship between cumulative SOC mineralization amount and porosity of 16~ 30 μm pores |
本研究中,对于不同施肥处理的土壤,S0.5的大孔隙度(>16 μm)、孔隙连通性以及30~100 μm和>100 μm孔隙的孔隙度均显著低于S5和S2处理(P<0.05)(图 2,图 3)。这是因为团聚体破碎之后,团聚体内的大孔隙会被破坏,形成较小的孔隙,孔隙度也会降低[8-10]。不同施肥处理土壤S5和S2的孔隙结构的差异不同。对于CK和LM土壤,S5和S2的孔隙结构无显著差异(P>0.05)(图 2,图 3);对于HM土壤,S2的大孔隙度、>100 μm孔隙的孔隙度以及孔隙连通性均显著低于S5处理(P<0.05)(图 2a,图 2d,图 3)。这是由于长期施用高量有机肥显著增加了土壤中大团聚体的比例以及团聚体的稳定性,HM土壤过5 mm筛后仍含有较高比例的2~5 mm的团聚体(47.7%)(表 1),而过2 mm筛后则将>2mm的团聚体破碎,导致S5和S2的团聚体的组成差异较大,孔隙结构的差异也较大。对于CK和LM土壤,5 mm过筛土中2~5 mm的团聚体的比例相对较小,分别为14.6%和38.1%(表 1),S5和S2处理的团聚体组成差异相对较小,从而导致其孔隙结构无显著差异(P>0.05)。这与Negassa等[9]的研究结果类似,组成差异较大的>0.5 mm与<0.5 mm的团聚体填装的土柱的孔隙结构有显著差异,而组成差异较小的0.5~1 mm和1~2 mm的团聚体填装的土柱的孔隙结构无显著差异。
培养期间,LM和HM土壤的有机碳矿化速率分别在第1天和第29天达到了高峰(图 4b,图 4c),这与李银坤等[18]的研究结果一致,出现两个矿化速率高峰可能是因为土壤中不同类型的有机物的降解性不同。施用有机肥显著增加了土壤有机碳的累积矿化量(P<0.05)(表 3,图 5),这是因为长期施用有机肥,土壤有机碳含量升高,增加了微生物碳源和微生物活性,促进了微生物对有机碳的分解[19-20]。对于CK和HM土壤,S0.5的有机碳累积矿化量显著高于S5和S2(P<0.01),S5和S2之间无显著差异(P>0.05)(图 5);对于LM土壤,S5和S0.5的有机碳累积矿化量显著高于S2(P<0.01),而S5和S0.5之间无显著差异(P>0.05)(图 5)。由于不同过筛土来源于同一份土样,有机碳含量无显著差异,因此不同过筛土之间有机碳矿化量的差异主要由土壤结构的差异导致。过筛破坏了土壤的团聚体结构,释放出被保护的活性有机碳[4],从而导致土壤有机碳矿化量在短时间内[3]或较长一段时间内[4]显著增加。然而,由于土壤有机碳主要储存在<0.25 mm的微团聚体中,因此能否破坏该尺寸的团聚体是影响土壤有机碳矿化量的关键[5-7]。本研究中,S0.5处理最接近0.25 mm,因此S0.5释放的有机碳较多,导致其有机碳矿化量高于S5和S2;而S5和S2均只破坏了>2 mm的团聚体,二者之间释放的有机碳差异不大,从而导致其有机碳矿化量无显著差异(LM土壤除外)。此外,CK土壤S0.5的有机碳累积矿化量较S5和S2处理分别高64.23%和79.06%;而HM处理下S0.5的有机碳累积矿化量较S5和S2处理分别高19.27%和14.13%,这可能是由于在养分含量相对较低的土壤中(CK和LM土壤),微生物处于养分限制状态,有机碳含量的增加会刺激微生物对养分的需求,从而加速土壤有机碳的矿化[21-22]。
LM土壤S5和S0.5的有机碳累积矿化量无显著差异,这可能是受到了孔隙结构的影响[23]。孔隙结构的结果表明,LM土壤中S5处理的大孔隙度(>16 μm)较S0.5处理高约1531%(这一值在CK土壤中为693%,在HM土壤中为1243%),已有的研究表明,土壤有机碳矿化量与大孔隙度呈显著的正相关关系[8],因此S5处理中较高的大孔隙度可能促进了土壤有机碳矿化,从而导致其和S0.5处理的有机碳累积矿化量无显著差异。
相关分析结果显示土壤有机碳累积矿化量与16~30 μm的孔隙度呈显著的负相关关系(P<0.05)(图 6),说明孔隙结构的变化也是影响有机碳矿化的一个重要因素。另有一些研究发现,30~90 μm的孔隙能保持较适宜的水分/气体条件,有利于养分运输和微生物活动,从而促进有机碳矿化[24-26]。还有研究表明有机碳矿化受到孔隙连通性的影响,Kravchenko等[25]发现团聚体内孔隙的连通性越好,有机碳的矿化量越大。而本研究中并未发现有机碳矿化同孔隙连通性之间存在显著的相关性,这可能是由于本研究为土柱尺度,观测到的仅是>16 μm的孔隙,因而与团聚体尺度的结果不一致。因此,为了更好的理解孔隙结构对有机碳特征的影响,在今后的研究中应该对不同尺度土壤样品开展研究,综合分析不同尺度孔隙结构对有机碳矿化的影响。
4 结论团聚体大小对孔隙结构和57 d内的土壤有机碳矿化量有极显著的影响。随着团聚体粒径的减小,土壤的大孔隙度(>16 μm)、孔隙连通性以及30~ 100 μm和>100 μm孔隙的孔隙度均有不同程度的降低。团聚体粒径减小释放出被保护的有机碳,从而增加土壤有机碳的矿化量,导致过0.5 mm筛(S0.5)处理的有机碳累积矿化量总体高于S5和S2处理,而后两者由于对大团聚体破坏较小,有机碳的矿化量无显著差异。土壤有机碳矿化量与16~30 μm的孔隙度成显著的负相关关系,说明团聚体大小改变导致的孔隙结构的变化可能是影响土壤有机碳矿化的另一个重要因素。
| [1] |
Lal R. Soil carbon sequestration impacts on global climate change and food security[J]. Science, 2004, 304(5677): 1623-1627. DOI:10.1126/science.1097396
(  0) 0) |
| [2] |
Peng X H, Zhang B, Zhao Q G. A review on relationship between soil organic carbon pools and soil structure stability (In Chinese)[J]. Acta Pedologica Sinica, 2004, 41(4): 618-623. [彭新华, 张斌, 赵其国. 土壤有机碳库与土壤结构稳定性关系的研究进展[J]. 土壤学报, 2004, 41(4): 618-623.]
(  0) 0) |
| [3] |
Franzluebbers A J. Potential C and N mineralization and microbial biomass from intact and increasingly disturbed soils of varying texture[J]. Soil Biology & Biochemistry, 1999, 31(8): 1083-1090.
(  0) 0) |
| [4] |
Gao F, Lin W, Cui X Y. Effects of sieving process on soil organic carbon mineralization for two forest types in Xiaoxing'an Mountains, Northeast China (In Chinese)[J]. Journal of Beijing Forestry University, 2017, 39(2): 30-39. [高菲, 林维, 崔晓阳. 过筛处理对小兴安岭2种森林类型土壤有机碳矿化的影响[J]. 北京林业大学学报, 2017, 39(2): 30-39.]
(  0) 0) |
| [5] |
Stenger R, Barkle G F, Burgess C P. Mineralisation of organic matter in intact versus sieved/refilled soil cores[J]. Soil Research, 2002, 40(1): 149. DOI:10.1071/SR01003
(  0) 0) |
| [6] |
Thomson B C, Ostle N J, McNamara N P, et al. Effects of sieving, drying and rewetting upon soil bacterial community structure and respiration rates[J]. Journal of Microbiological Methods, 2010, 83(1): 69-73. DOI:10.1016/j.mimet.2010.07.021
(  0) 0) |
| [7] |
Adekanmbi A A, Shaw L J, Sizmur T. Effect of sieving on ex situ soil respiration of soils from three land use types[J]. Journal of Soil Science and Plant Nutrition, 2020, 20(3): 912-916. DOI:10.1007/s42729-020-00177-2
(  0) 0) |
| [8] |
Mangalassery S, Sjögersten S, Sparkes D L, et al. The effect of soil aggregate size on pore structure and its consequence on emission of greenhouse gases[J]. Soil and Tillage Research, 2013, 132: 39-46. DOI:10.1016/j.still.2013.05.003
(  0) 0) |
| [9] |
Negassa W C, Guber A K, Kravchenko A N, et al. Properties of soil pore space regulate pathways of plant residue decomposition and community structure of associated bacteria[J]. PLoS One, 2015, 10(4): e0123999. DOI:10.1371/journal.pone.0123999
(  0) 0) |
| [10] |
Toosi E R, Kravchenko A N, Guber A K, et al. Pore characteristics regulate priming and fate of carbon from plant residue[J]. Soil Biology & Biochemistry, 2017, 113: 219-230.
(  0) 0) |
| [11] |
Kravchenko A N, Guber A K. Soil pores and their contributions to soil carbon processes[J]. Geoderma, 2017, 287: 31-39. DOI:10.1016/j.geoderma.2016.06.027
(  0) 0) |
| [12] |
Zhou H, Li W Z, Zhang Z B, et al. Characterization of multi-scale soil structure with X-ray computed tomography (In Chinese)[J]. Acta Pedologica Sinica, 2013, 50(6): 1226-1230. [周虎, 李文昭, 张中彬, 等. 利用X射线CT研究多尺度土壤结构[J]. 土壤学报, 2013, 50(6): 1226-1230.]
(  0) 0) |
| [13] |
Zhao Q G, Huang G Q, Ma Y Q. The problems in red soil ecosystem in southern of China and its countermeasures (In Chinese)[J]. Acta Ecologica Sinica, 2013, 33(24): 7615-7622. [赵其国, 黄国勤, 马艳芹. 中国南方红壤生态系统面临的问题及对策[J]. 生态学报, 2013, 33(24): 7615-7622.]
(  0) 0) |
| [14] |
Jiang C L, He Y Q, Liu X L, et al. Effect of long-term application of organic manure on structure and stability of aggregate in upland red soil (In Chinese)[J]. Acta Pedologica Sinica, 2010, 47(4): 715-722. [姜灿烂, 何园球, 刘晓利, 等. 长期施用有机肥对旱地红壤团聚体结构与稳定性的影响[J]. 土壤学报, 2010, 47(4): 715-722.]
(  0) 0) |
| [15] |
Jiang Y J, Zhou H, Chen L J, et al. Nematodes and microorganisms interactively stimulate soil organic carbon turnover in the macroaggregates[J]. Frontiers in Microbiology, 2018, 9: 2803. DOI:10.3389/fmicb.2018.02803
(  0) 0) |
| [16] |
Hu R G, Hatano R, Kusa K, et al. Soil respiration and net ecosystem production in an onion field in Central Hokkaido, Japan[J]. Soil Science and Plant Nutrition, 2004, 50(1): 27-33. DOI:10.1080/00380768.2004.10408449
(  0) 0) |
| [17] |
Zhang Z B, Liu K L, Zhou H, et al. Linking saturated hydraulic conductivity and air permeability to the characteristics of biopores derived from X-ray computed tomography[J]. Journal of Hydrology, 2019, 571: 1-10. DOI:10.1016/j.jhydrol.2019.01.041
(  0) 0) |
| [18] |
Li Y K, Chen M P, Mei X R, et al. Effects of soil moisture and nitrogen addition on organic carbon mineralization in a high-yield cropland soil of the North China Plain (In Chinese)[J]. Acta Ecologica Sinica, 2014, 34(14): 4037-4046. [李银坤, 陈敏鹏, 梅旭荣, 等. 土壤水分和氮添加对华北平原高产农田有机碳矿化的影响[J]. 生态学报, 2014, 34(14): 4037-4046.]
(  0) 0) |
| [19] |
钱海燕. 长期施用有机肥对红壤团聚体有机碳库及土壤二氧化碳排放的影响[D]. 南京: 中国科学院南京土壤研究所, 2015. Qian H Y. Effect of long-term manure application on organic carbon pools in red sol aggregates and soil CO2emission[D]. Nanjing: Institute of Soil Science, Chinese Academy of Sciences. 2015. (  0) 0) |
| [20] |
Li Y, Liu L L, Fang H, et al. Effects of long-term fertilization on paddy soil carbon and nitrogen mineralization and aggregates stability (In Chinese)[J]. Soils, 2019, 51(3): 451-457. [李奕, 刘玲玲, 房焕, 等. 长期施肥对水稻土碳氮矿化与团聚体稳定性的影响[J]. 土壤, 2019, 51(3): 451-457.]
(  0) 0) |
| [21] |
Qi R M, Zhao B Q, Li J, et al. Effects of cattle manure addition on soil organic carbon mineralization and priming effects under long-term fertilization regimes (In Chinese)[J]. Transactions of the Chinese Society of Agricultural Engineering, 2016, 32(S2): 118-127. [戚瑞敏, 赵秉强, 李娟, 等. 添加牛粪对长期不同施肥潮土有机碳矿化的影响及激发效应[J]. 农业工程学报, 2016, 32(S2): 118-127.]
(  0) 0) |
| [22] |
Lian T X, Jin J, Wang G H, et al. The fate of soybean residue-carbon links to changes of bacterial community composition in Mollisols differing in soil organic carbon[J]. Soil Biology & Biochemistry, 2017, 109: 50-58.
(  0) 0) |
| [23] |
Juarez S, Nunan N, Duday A C, et al. Effects of different soil structures on the decomposition of native and added organic carbon[J]. European Journal of Soil Biology, 2013, 58: 81-90. DOI:10.1016/j.ejsobi.2013.06.005
(  0) 0) |
| [24] |
Strong D T, Wever H D, Merckx R, et al. Spatial location of carbon decomposition in the soil pore system[J]. European Journal of Soil Science, 2004, 55(4): 739-750. DOI:10.1111/j.1365-2389.2004.00639.x
(  0) 0) |
| [25] |
Kravchenko A N, Negassa W C, Guber A K, et al. Protection of soil carbon within macro-aggregates depends on intra-aggregate pore characteristics[J]. Scientific Reports, 2015, 5: 16261. DOI:10.1038/srep16261
(  0) 0) |
| [26] |
Ananyeva K, Wang W, Smucker A J M, et al. Can intra-aggregate pore structures affect the aggregate's effectiveness in protecting carbon?[J]. Soil Biology & Biochemistry, 2013, 57: 868-875.
(  0) 0) |
 2022, Vol. 59
2022, Vol. 59


