2. 北京师范大学环境学院水环境模拟国家重点实验室, 北京 100875
2. State Key Laboratory of Water Environment Simulation, School of Environment, Beijing Normal University, Beijing 100875, China
在土壤/水体环境中,溶解性有机质(DOM)与矿物的相互作用普遍存在,二者的相互作用会造成DOM在矿物/水界面的分子分馏现象[1],对DOM的环境地球化学行为具有深远影响[2-5]。在早期的研究中,研究者用紫外(UV)-可见光光谱、傅里叶变换红外光谱(FTIR)、核磁共振(NMR)和近边X射线吸收精细结构(NEXAFS)光谱技术对DOM-矿物的相互作用进行研究,证实了矿物对DOM的结构分馏作用[6-7]。尽管上述光谱技术可给出DOM的总体化学官能团含量,但是难以给出分子尺度上的信息[1]。近年来兴起的高分辨率质谱,尤其是电喷雾电离-傅立叶变换离子回旋共振质谱(ESI-FT- ICR-MS),可准确地分析DOM溶液中上千种分子的分子式[8],进而有助于从分子水平上解析DOM在矿物/水界面的结构分馏特性。
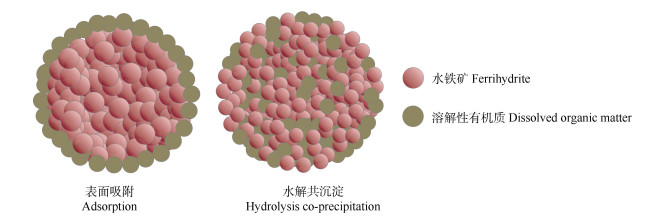
作为土壤形成过程中的主要产物,铁氧化物的比表面积大且表面活性强,以水铁矿尤为突出[9-10]。在自然环境中,DOM可通过表面吸附或与Fe(III)发生水解共沉淀反应的方式形成水铁矿-DOM复合体[11-12],二者均会诱发DOM在水铁矿/水界面的结构分馏[13-14],但目前研究主要聚焦于表面吸附过程[15-17]。例如,Wang等[16]和Lü等[17]采用ESI-FT-ICR- MS先后发现在表面吸附过程中,DOM中大分子量组分以及不饱和度高、富含氧的化合物(如多环芳烃、多酚、羧基化合物等)会优先与水铁矿发生作用,且该结构分馏现象在溶液碳/铁(C/Fe)比值较低时更加突出。相比较而言,针对水解共沉淀反应引发的DOM分子结构分馏的研究相对有限。目前研究已证实表面吸附和水解共沉淀方式形成的水铁矿-DOM复合体的结构有较大差异(如图 1所示,前者使得DOM主要分布于水铁矿表面,而后者会导致DOM镶嵌在水铁矿晶体孔隙间)[14,18],因此,表面吸附诱发的DOM在水铁矿/水界面的结构分馏行为不能直接类推到水解共沉淀。此外,由于水铁矿通常是在富含DOM的环境(如沉积物和土壤)中形成[18],在实际环境中,共沉淀是较为常见的水铁矿-DOM复合体的形成方式[13]。综上,亟需重点关注水解共沉淀过程,进一步阐明其引发的DOM分子结构分馏特性。因此,本文通过水解共沉淀方式在C/Fe比例不同的溶液中制备水铁矿-DOM复合体,将Fe K边X射线吸收光谱(XAS)与X射线光电子能谱(XPS)等相结合来剖析复合体的结构,并借助ESI-FT-ICR-MS技术解析反应过程中DOM分子组成和结构的变化,进而从分子水平探明由水解共沉淀所引发的DOM在水铁矿/水界面的分子分馏特性。
|
图 1 表面吸附和水解共沉淀形成的水铁矿-溶解性有机质(DOM)复合体结构示意图 Fig. 1 Schematic diagram of ferrihydrite-DOM complexes formed by adsorption and hydrolysis co-precipitation |
由于泥炭土中有机碳含量相对较高[19],较易提取到满足实验浓度的DOM溶液,因此,本研究从四川省甘孜藏族自治州理塘县采集了泥炭土。称取20 g风干过80目筛的土样和60 g去离子水置于250 mL的离心瓶中,混合振荡96 h后以4 000 r·min–1转速离心30 min,收集上清液,而后用0.22 μm微孔过滤膜过滤,过滤得到DOM,随后置于4 oC条件下避光保存[12,16,20]。
参照文献[13-14,18]报道的方法,称取一定量的Fe(NO3)3˙9H2O按照C/Fe摩尔比分别为0.3、1.5、4.5、8.0和16.0加入200 mL 100 mg·L–1的DOM溶液中,再用滴管逐滴滴入0.1 mol·L–1的NaOH溶液,调pH至5。Eusterhues等[14]发现pH为5时,Fe(III)和DOM的共沉淀反应最显著。所选择的五个C/Fe比例在实际土壤溶液的C/Fe比值范围内(0.2~25.0)[21-22]。以上每个处理设置3次重复。样品在避光混合振荡2、6和12 h后,在8 000 r·min–1转速下离心20 min,弃去上清液,用去离子水冲洗所得的固体,摇匀并离心30 min,如此重复5次,得到的固体冷干备用。所得到的水铁矿-DOM复合体(FhC)按照C/Fe比分别标记为FhC0.3、FhC1.5、FhC4.5、FhC8和FhC16。
1.2 DOM的表征通过总有机碳(TOC)分析仪(TOC-L CPN,岛津,日本)分析DOM溶液中TOC含量,采用紫外分光光度仪(DR6000型,哈希,美国)分析DOM溶液在250、254和365 nm下的吸光度,计算SUVA254(溶液在254 nm处的吸光度与TOC的比值)和E2/E3(溶液在250与365 nm处吸光度的比值)[23]。在进行ESI-FT-ICR-MS分析前,采取固相萃取(SPE)对DOM溶液进行前处理,以达到去盐去杂质和浓缩的目的,萃取柱选用的是Varian Bond Elute PPL(0.17 g·mL–1)。所用分析仪器为Bruker SolariX FT-ICR-MS(Solarix 15T,Bruker公司,美国),配备15.0 T的超导磁铁和ESI离子源。分析样品时,采集m/z范围在200 Da和1 000 Da之间的分子图谱。用溶解于50%异丙基醇的10 mmol·L–1甲酸钠进行校准。用Bruker Data分析软件对图谱中的峰进行分析。由于DOM主要含有C、H和O元素,而N、P、S含量较低[24],所以在本文计算中仅考虑C、H和O。按照C5-80H10-200O0-40的元素组成标准以及H/C < 2.0和O/C < 1.2的原子比例标准,得到信噪比(S/N)大于4的有机分子化学式,计算芳香度指数(AI,AI =(1+C–O/2–H/C)/(C–O/2))[17,25]。根据AI和H/C值,可将DOM中的有机分子分为以下四类[17]:燃烧过程中产生的致密多环芳香类化合物(AI > 0.66),维管束植物产生的多酚类化合物(0.50 < AI≤0.66)、高度不饱和的酚类化合物(AI≤0.50且H/C < 1.5)和脂质类化合物(AI≤0.50且1.5≤H/C≤2.0)。
1.3 水铁矿-DOM复合体的表征分别采用元素分析仪(Vario ELIII,Elementar公司,德国)和ICP-MS(Elan DRC-e型,Perkin-Elmer公司,美国)测定反应12 h后得到的FhC样品中的有机碳(OC)和Fe含量;用XPS测定表面C和Fe,获取C1s的精细谱,通过Avantage软件进行数据处理,得到表面不同含碳官能团的含量;在北京同步辐射装置(BSRF)采集样品和标准品中Fe的K边扩展X射线吸收精细结构(Fe-EXAFS),标准品包括各种铁矿物(水铁矿、针铁矿、赤铁矿和磁铁矿)和Fe(III)-有机络合物(柠檬酸铁和草酸铁)。所有样品碾磨成粉末,每个样品图谱至少扫描两次,取平均值,分析结果在FEFF8.0软件中进行。
1.4 统计与分析采用SPSS 9.0进行数据处理与统计分析,单因素方差分析(One-way ANOVA)法进行显著性分析。采用OriginPro 9.2进行数据绘图。
2 结果与讨论 2.1 水铁矿-DOM复合体的元素组成如表 1和图 2a)所示,随着初始C/Fe比值增大,FhC中OC的含量呈线性增加(P < 0.05),而Fe的含量呈现降低趋势(P < 0.05),包含5.1%~39.2%的OC和6.4%~59.5%的Fe。FhC的C/Fe比值(0.4~28.7)随初始C/Fe比增加而增加。除FhC16外,其他样品的C/Fe比值与初始C/Fe值接近。此外,考虑表面元素组成会影响FhC的物化性质,采用XPS分析了C和Fe在样品表面的分布,结果见表 1。样品表面的C含量远高于Fe,表面C/Fe比值介于3.5~27.8之间。随着初始C/Fe值增加,样品表面C/Fe比与整体C/Fe比值逐渐减小(P < 0.05)。对于初始C/Fe比小于8下形成的样品(FhC0.3、FhC1.5和FhC4.5),其表面C/Fe比与整体C/Fe比值均明显高于1,尤其是FhC0.3,其表面C/Fe比为整体C/Fe比值的8.8倍,显示OC主要分布于这些样品的表面。这一结果表明在该条件下,OC的固定可能部分源于水铁矿表面的吸附。对比之下,当初始C/Fe值为8.0和16.0时,样品表面C/Fe比与整体C/Fe比值趋近于1,表明在C/Fe值较高环境下形成的FhC中C和Fe的分布相对均匀。造成这一结果的主要原因可能是因为初始C/Fe值较高,意味着体系中DOM相对浓度较高,那么DOM与Fe(III)两者相互作用发生水解共沉淀反应的机会更大,导致形成的复合体中C和Fe的分布相对更均质。
|
|
表 1 水铁矿-溶解性有机质(DOM)复合体的整体和表面特性 Table 1 Bulk and surface property of ferrihydrite-DOM complex |

|
注:RSUVA254和RE2/E3是反应后DOM溶液的E2/E3和SUVA254与原始DOM E2/E3和SUVA254的比值;图b)中同一个颜色柱子上的不同字母表示不同处理间差异显著(P < 0.05)。 Note: RSUVA254和RE2/E3 is the ratio of E2/E3 and SUVA254 of the post-reaction DOM solution to that of the original sample, respectively; different letters in the column with the same color in the panel b indicate significant differences between treatments(P < 0.05). 图 2 复合体中有机碳的含量和DOM溶液中有机碳的去除率(a))及DOM溶液的RSUVA254和RE2/E3值(b))(图中DOM的SUVA254相关数据引自文献[1]) Fig. 2 Organic carbon(OC)content in the complex and OC removal rate(a)), RSUVA254 and RE2/E3 of DOM solution(b))(Data about SUVA254 of DOM in the figure were cited from the reference[1]) |
通过对XPS C1s精细谱进行分峰拟合处理,进一步获取了四种特征官能团(C-C/C=C、C-OH、C=O和COOH)在样品表面的分布。如表 1所示,所有样品表面含碳物质中C-C/C=C键所占的比例最大(72.6%~81.5%),而在三种含氧官能团中,COOH(12.7%~17.7%)的含量要高于C-OH(2.6%~6.4%)和C=O(2.4%~4.6%)。产生这一现象可能有两方面的原因:一是原始DOM溶液中羧基的含量更高[1];二是Fe(III)选择性共沉淀DOM中的羧基碳。
2.2 水铁矿-DOM复合体中Fe的存在形态为确定样品中Fe的存在形态及其具体组成比例,利用线性组合方法在Athena软件中使用标样组合(水铁矿、针铁矿、赤铁矿、磁铁矿、柠檬酸铁和草酸铁)对Fe-EXAFS谱线进行多次线性拟合分析,选取R值(即残差值:残差值越小,表明二者间的差别越小,拟合效果越好)较低的拟合曲线。如图 3和图 4所示,FhC中Fe主要以水铁矿的形式存在,其次是柠檬酸铁,而两者的相对比例与原始C/Fe比值有关。具体为,随着C/Fe比值的增加,水铁矿的相对比例逐渐减小,从95.9%下降至68.0%,而柠檬酸铁的比例逐渐上升,从4.1%上升至32.0%。造成这一现象的原因主要是由于当C/Fe比值较低时,Fe(III)的水解沉淀过程与水铁矿的形成过程类似,因此,形成的复合体主要以水铁矿的形式存在。但随着C/Fe比值的增加,DOM也会参与其中,与Fe(III)发生络合作用,阻碍水铁矿的形成,进而增加复合体中Fe(III)-DOM络合物的比例,降低水铁矿的相对比例[12]。

|
注:虚线为水铁矿和柠檬酸铁两者线性拟合曲线。 Note: Dotted line represents linear fitting curves of ferrihydrite and Fe(III)-citrate. 图 3 不同碳/铁摩尔比值下形成的水铁矿-DOM复合体的k3加权Fe K边的扩展X射线吸收精细结构谱图(图中柠檬酸铁和水铁矿的图谱数据引自文献[1]) Fig. 3 Iron k3-weighted extended X-ray absorption fine structure spectra of the ferrihydrite-DOM complex relative to C/Fe molar ratio in formation(Spectra of ferrihydrite and Fe(III)-citrate in the figure were cited from the reference[1]) |

|
图 4 复合体中水铁矿和柠檬酸铁的相对百分比 Fig. 4 Relative percentage of ferrihydrite and ferric citrate in the complex |
本文采用SUVA254和E2/E3分别表征DOM的相对芳香度和分子量的大小[23]。从图 2b)可以看出,当初始C/Fe比为0.5、1.5和4.5时,共沉淀反应后DOM溶液的SUVA254显著低于原始DOM(RSUVA254 < 1)(P < 0.05),表明溶液中的芳香碳被选择性地固定在FhC中。然而,反应后DOM的E2/E3值显著增加(RE2/E3 > 1)(P < 0.05)。由于E2/E3比值增加表明DOM分子量的减小[23,26],因此可知C/Fe比较低环境中,Fe(III)选择性共沉淀高分子量的DOM组分,该结果较好地解释了Fe-EXAFS分析中发现的Fe主要以柠檬酸铁为主,而不是草酸铁。尽管柠檬酸和草酸均为富含羰基的DOM组分,但柠檬酸的分子量为草酸的2倍左右,因此更优先与Fe(III)反应形成柠檬酸铁。此外,这一分子分馏结果与之前报道的因表面吸附引发的DOM在水铁矿/水界面的分馏现象基本一致[27-28],表明无论表面吸附还是共沉淀,水铁矿优先吸附高芳香性和高分子量的DOM。但当C/Fe比为8.0和16.0时,RSUVA254和RE2/E3均接近于1,暗示当溶液中C/Fe比较高时,水铁矿对DOM组分的选择性固定作用变弱。类似地,Zhou等[29]发现针铁矿对富里酸中大分子量物质的选择性吸附随着OC浓度的升高而减弱,Hur和Schlautman[30]观察到被高岭土和赤铁矿吸附后富里酸的平均分子量随着浓度的升高而增大,但始终小于富里酸空白值,这可能是由于随着OC浓度的升高,铁矿物的选择性吸附能力逐渐达到饱和。
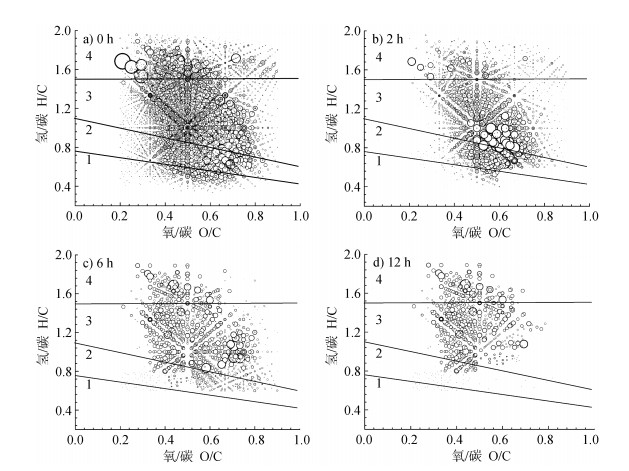
为了获取详细的分子结构信息,同时考虑少有研究解析DOM在水铁矿/水界面分子分馏的动态过程,本文以初始C/Fe比为4.5的反应为例,对反应不同时间后的DOM溶液进行ESI-FT-ICR-MS分析。基于分析结果,采用H/C和O/C原子比绘制出图 5,即范氏图。可以看出,随着反应的不断进行,DOM溶液中拥有高O/C和低H/C值的组分逐渐消失:反应2 h后,就可观察到明显的结构分馏现象,溶液中H/C < 0.6且O/C > 0.6组分消失;6 h后,消失的组分范围扩大至H/C < 0.8,而12 h后,溶液中H/C < 0.8或0.8 < H/C < 1.0且O/C > 0.5组分均消失,表明Fe(III)选择性共沉淀含有高O/C但低H/C值的DOM组分。
|
注:圈的大小代表相对峰强度;1、2、3和4分别代表组分1、组分2、组分3和组分4;组分1代表燃烧过程中产生的致密多环芳香类物质;组分2代表维管植物来源的多酚类物质;组分3代表不饱和度高的酚类物质;组分4代表脂质类物质。 Note: Size of the circle indicates relative peak intensity. 1, 2, 3 and 4 in graphs represents groups 1, 2, 3 and 4, respectively; Group 1 represents combustion-derived condensed polycyclic aromatic, Group 2, vascular plant-derived polyphenols, Group 3, highly unsaturated and phenolic compounds, and Group 4 aliphatic compounds. 图 5 碳铁摩尔比为4.5下反应不同时间后DOM溶液的范氏图 Fig. 5 Van Krevelen diagrams of DOM solution with C/Fe ratio of 4.5 relative to duration of the reaction |
基于AI指数和H/C值,将范氏图划分为四个部分:组分1(燃烧过程中产生的致密多环芳香类物质)、组分2(维管植物来源的多酚类物质)、组分3(不饱和度高的酚类物质)和组分4(脂质类物质)。如表 2所示,原始DOM由13.7%的组分1、22.5%的组分、47.2%的组分3以及16.5%的组分4组成。反应不同时间后,DOM溶液各个组分减少的程度均按以下顺序排列:组分1大于组分2,而组分3和组分4的相对比例有不同程度增加,这与SUVA254数据结果一致。具体为,反应2 h后,溶液中组分1优先被结合,其相对丰度降低至6.2%,到6 h,组分1已经完全消失。组分2所占比例也随反应时间的推移逐步下降,在反应12 h后下降至1.5%。相对比而言,在反应的不同阶段,组分3和组分4的相对丰度均高于原始DOM。根据以上结果可知,反应伊始,燃烧过程中产生的致密多环芳香类物质率先被固定在复合体中,随着反应的推进,维管植物来源的多酚类物质被固定,而不饱和度高的酚类和脂质类物质被选择性留在溶液中。该结果进一步验证了文献中提出的形容矿物和有机质相互作用的“洋葱皮模型”[31-32]:某类化合物(本文为燃烧过程中产生的致密多环芳香类物质)优先结合在矿物(水铁矿)表面后形成有机膜,改变了矿物的表面特性,其他物质(维管植物来源的多酚类物质)再依次吸附在有机膜上。之前研究指出水铁矿表面的羟基可与DOM中的羧基发生强烈的配体交换作用,而芳香结构可增加羧基的电子密度,促进配体交换反应的发生[10,33-34],这可能是造成水铁矿对DOM中致密多环芳香类和多酚类物质高选择性的主要原因,但相较于多酚类物质,致密多环芳香类物质更优先被水铁矿结合的原因仍待进一步探索。厘清这一问题的主要难点在于,DOM中具有不同分子结构的化学成分交织,造成其与水铁矿相互作用的反应体系相对复杂。因此,未来研究中可考虑通过筛选一组具有特征结构的模式化合物来简化反应体系,同时借助量子化学模拟计算等手段来明确模式化合物与水铁矿反应的主导机制,以此从根本上阐明造成DOM在水铁矿/水界面上发生结构分馏的内在机理。
|
|
表 2 通过电喷雾-傅立叶变换-离子回旋共振质谱获取的不同反应时间下DOM中各组分的相对丰度 Table 2 Relative abundance of DOM component obtained with the aid of the electrospray ionization Fourier transform ion cyclotron resonance mass spectrometry relative to duration of the reaction |
水铁矿-DOM复合体中Fe主要以水铁矿的形式存在,其次是柠檬酸铁,两者比例与溶液初始C/Fe比有关。共沉淀过程中,DOM中的芳香碳和高分子组分会被水铁矿选择性复合,随着初始C/Fe比的增加,分子分馏程度减弱并逐渐趋于稳定。与此同时,该结构选择随反应时间呈一定动态变化:反应伊始,燃烧过程中产生的致密多环芳香类物质优先被固定,随着反应推进,维管植物来源的多酚类物质随后被固定。本文研究结果将有助于深入理解水铁矿形成过程中,通过水解共沉淀作用对DOM进行结构分馏的分子机制,进而为预测DOM在水铁矿/水界面的环境地球化学行为提供科学依据。但是,在实际土壤环境中,DOM与水铁矿的相互作用十分复杂,会涉及铁氧化还原过程以及其他土壤矿物共存等情况,因此,在未来研究中,可尝试创造更切合自然状态的实验条件,以求更真实地反映DOM在土壤环境中的水铁矿/水界面上发生的结构分馏情形。
| [1] |
Han L F, Sun K, Keiluweit M, et al. Mobilization of ferrihydrite-associated organic carbon during Fe reduction: Adsorption versus coprecipitation[J]. Chemical Geology, 2019, 503: 61-68. DOI:10.1016/j.chemgeo.2018.10.028
(  0) 0) |
| [2] |
Schmidt M W I, Torn M S, Abiven S, et al. Persistence of soil organic matter as an ecosystem property[J]. Nature, 2011, 478(7367): 49-56. DOI:10.1038/nature10386
(  0) 0) |
| [3] |
Wang L, Ying R R, Shi J Q, et al. Advancement in study on adsorption of organic matter on soil minerals and its mechanism (In Chinese)[J]. Acta Pedologica Sinica, 2017, 54(4): 805-818. [土壤矿物对有机质的吸附与固定机制研究进展[J]. 土壤学报, 2017, 54(4): 805-818.]
(  0) 0) |
| [4] |
Chu B J, Yu G H, Liu F F, et al. Characterization of mineral-organic complex in soil microaggregates with synchrotron radiation infrared micro-imaging method (In Chinese)[J]. Acta Pedologica Sinica, 2017, 54(6): 1451-1458. [土壤微团聚体中矿物-有机复合体特征[J]. 土壤学报, 2017, 54(6): 1451-1458.]
(  0) 0) |
| [5] |
Zhou F L, Li F, Huang Y N, et al. Effects of adding Chinese milk vetch on soil aggregates composition and organic carbon distribution (In Chinese)[J]. Soils, 2020, 52(4): 781-788. [紫云英添加对土壤团聚体组成及有机碳分布的影响[J]. 土壤, 2020, 52(4): 781-788.]
(  0) 0) |
| [6] |
Cai P, Lin D, Peacock C L, et al. EPS adsorption to goethite: Molecular level adsorption mechanisms using 2D correlation spectroscopy[J]. Chemical Geology, 2018, 494: 127-135. DOI:10.1016/j.chemgeo.2018.07.028
(  0) 0) |
| [7] |
Wang K J, Xing B S. Structural and sorption characteristics of adsorbed humic acid on clay minerals[J]. Journal of Environmental Quality, 2005, 34(1): 342-349. DOI:10.2134/jeq2005.0342
(  0) 0) |
| [8] |
Zark M, Christoffers J, Dittmar T. Molecular properties of deep-sea dissolved organic matter are predictable by the central limit theorem: Evidence from tandem FT-ICR-MS[J]. Marine Chemistry, 2017, 191: 9-15. DOI:10.1016/j.marchem.2017.02.005
(  0) 0) |
| [9] |
Wang X M, Yang K G, Sun S F, et al. The structure and composition of ferrihydrite and its environmental geochemical behaviors (In Chinese)[J]. Earth Science Frontiers, 2011, 18(2): 339-347. [水铁矿的结构、组成及环境地球化学行为[J]. 地学前缘, 2011, 18(2): 339-347.]
(  0) 0) |
| [10] |
Bompoti N, Chrysochoou M, Machesky M. Surface structure of ferrihydrite: Insights from modeling surface charge[J]. Chemical Geology, 2017, 464: 34-45. DOI:10.1016/j.chemgeo.2016.12.018
(  0) 0) |
| [11] |
Mikutta R, Lorenz D, Guggenberger G, et al. Properties and reactivity of Fe-organic matter associations formed by coprecipitation versus adsorption: Clues from arsenate batch adsorption[J]. Geochimica et Cosmochimica Acta, 2014, 144: 258-276. DOI:10.1016/j.gca.2014.08.026
(  0) 0) |
| [12] |
Chen K Y, Chen T Y, Chan Y T, et al. Stabilization of natural organic matter by short-range-order iron hydroxides[J]. Environmental Science & Technology, 2016, 50(23): 12612-12620.
(  0) 0) |
| [13] |
Chen C M, Dynes J J, Wang J, et al. Properties of Fe-organic matter associations via coprecipitation versus adsorption[J]. Environmental Science & Technology, 2014, 48(23): 13751-13759.
(  0) 0) |
| [14] |
Eusterhues K, Rennert T, Knicker H, et al. Fractionation of organic matter due to reaction with ferrihydrite: Coprecipitation versus adsorption[J]. Environmental Science & Technology, 2011, 45(2): 527-533.
(  0) 0) |
| [15] |
Zhang P, Liu A J, Huang P, et al. Sorption and molecular fractionation of biochar-derived dissolved organic matter on ferrihydrite[J]. Journal of Hazardous Materials, 2020, 392: 122260.
(  0) 0) |
| [16] |
Wang Y, Zhang Z Y, Han L F, et al. Preferential molecular fractionation of dissolved organic matter by iron minerals with different oxidation states[J]. Chemical Geology, 2019, 520: 69-76. DOI:10.1016/j.chemgeo.2019.05.003
(  0) 0) |
| [17] |
Lü J, Zhang S, Wang S, et al. Molecular-scale investigation with ESI-FT-ICR-MS on fractionation of dissolved organic matter induced by adsorption on iron oxyhydroxides[J]. Environmental Science & Technology, 2016, 50(5): 2328-2336.
(  0) 0) |
| [18] |
Eusterhues K, Neidhardt J, Hädrich A, et al. Biodegradation of ferrihydrite-associated organic matter[J]. Biogeochemistry, 2014, 119(1/2/3): 45-50.
(  0) 0) |
| [19] |
Freeman C, Evans C D, Monteith D T, et al. Export of organic carbon from peat soils[J]. Nature, 2001, 412(6849): 785.
(  0) 0) |
| [20] |
Sheng H, Song D S, Wang C H, et al. Comparison and transform of soil Dissolved organic carbon measured by four methods (In Chinese)[J]. Soils, 2015, 47(6): 1049-1053. [土壤溶解性有机碳四种测定方法的对比和转换[J]. 土壤, 2015, 47(6): 1049-1053.]
(  0) 0) |
| [21] |
Riedel T, Zak D, Biester H, et al. Iron traps terrestrially derived dissolved organic matter at redox interfaces[J]. Proceedings of the National Academy of Sciences of the United States of America, 2013, 110(25): 10101-10105. DOI:10.1073/pnas.1221487110
(  0) 0) |
| [22] |
Chin Y P, Traina S J, Swank C R, et al. Abundance and properties of Dissolved organic matter in pore waters of a freshwater wetland[J]. Limnology and Oceanography, 1998, 43(6): 1287-1296. DOI:10.4319/lo.1998.43.6.1287
(  0) 0) |
| [23] |
Qian F, Wu J Y, Yu H B, et al. UV-visible spectra properties of DOM from Taizi River in Benxi City section by multivariable analysis (In Chinese)[J]. Environmental Science, 2016, 37(10): 3806-3812. [多元数理统计法研究太子河本溪城市段水体DOM紫外光谱特征[J]. 环境科学, 2016, 37(10): 3806-3812.]
(  0) 0) |
| [24] |
Cao D, Huang H G, Hu M, et al. Comprehensive characterization of natural organic matter by MALDI- and ESI-Fourier transform ion cyclotron resonance mass spectrometry[J]. Analytica Chimica Acta, 2015, 866: 48-58. DOI:10.1016/j.aca.2015.01.051
(  0) 0) |
| [25] |
Koch B P, Dittmar T. From mass to structure: An aromaticity index for high-resolution mass data of natural organic matter[J]. Rapid Communications in Mass Spectrometry, 2006, 20(5): 926-932. DOI:10.1002/rcm.2386
(  0) 0) |
| [26] |
Li P H, Hur J. Utilization of UV-Vis spectroscopy and related data analyses for Dissolved organic matter(DOM)studies: A review[J]. Critical Reviews in Environmental Science and Technology, 2017, 47(3): 131-154. DOI:10.1080/10643389.2017.1309186
(  0) 0) |
| [27] |
Coward E K, Ohno T, Plante A F. Adsorption and molecular fractionation of dissolved organic matter on iron-bearing mineral matrices of varying crystallinity[J]. Environmental Science & Technology, 2018, 52(3): 1036-1044.
(  0) 0) |
| [28] |
Liu M Q, Ding Y, Peng S M, et al. Molecular fractionation of dissolved organic matter on ferrihydrite: Effects of dissolved cations[J]. Environmental Chemistry, 2019, 16(2): 137. DOI:10.1071/EN18235
(  0) 0) |
| [29] |
Zhou Q H, Maurice P A, Cabaniss S E. Size fractionation upon adsorption of fulvic acid on goethite: Equilibrium and kinetic studies[J]. Geochimica et Cosmochimica Acta, 2001, 65(5): 803-812. DOI:10.1016/S0016-7037(00)00536-6
(  0) 0) |
| [30] |
Hur J, Schlautman M A. Molecular weight fractionation of humic substances by adsorption onto minerals[J]. Journal of Colloid and Interface Science, 2003, 264(2): 313-321. DOI:10.1016/S0021-9797(03)00444-2
(  0) 0) |
| [31] |
Chassé A W, Ohno T, Higgins S R, et al. Chemical force spectroscopy evidence supporting the layer-by-layer model of organic matter binding to iron(oxy)hydroxide mineral surfaces[J]. Environmental Science & Technology, 2015, 49(16): 9733-9741.
(  0) 0) |
| [32] |
Mitchell P, Simpson A, Soong R, et al. Nuclear magnetic resonance analysis of changes in dissolved organic matter composition with successive layering on clay mineral surfaces[J]. Soil Systems, 2018, 2(1): 8.
(  0) 0) |
| [33] |
Mikutta R, Mikutta C, Kalbitz K, et al. Biodegradation of forest floor organic matter bound to minerals via different binding mechanisms[J]. Geochimica et Cosmochimica Acta, 2007, 71(10): 2569-2590.
(  0) 0) |
| [34] |
Strobel B W. Influence of vegetation on low-molecular- weight carboxylic acids in soil solution-a review[J]. Geoderma, 2001, 99(3/4): 169-198.
(  0) 0) |
 2022, Vol. 59
2022, Vol. 59


