2. 云南省曲靖市土肥站, 云南曲靖 655000;
3. 中国科学院大学, 北京 100049
2. Soil and Fertilizer Station, Qujing, Yunnan 655000, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China
磷是植物生长必需的大量元素,也是限制生态系统生产力的主要因子[1-2]。由于土壤铁铝氧化物对磷的吸附固定、磷酸盐的淋溶、土壤母质和氮肥投入等原因[2],农田土壤中磷肥的利用率较低。据统计,磷肥的当季利用效率平均仅为10%~20%,大部分的磷肥(75%以上)被固定在土壤中[3]。此外,研究表明世界现有磷储量远低于农业磷需求,磷也被形容为“正在消失的元素”[4]。因此,探明土壤中已吸附固定的磷在多大程度和多长时间尺度上能被植物吸收利用(即“磷后效”)具有重要的现实意义。
土壤对磷的吸附遵循吸附平衡原理[5],即土壤中的“吸附态磷”也可以被重新交换进土壤溶液中供作物吸收利用。已有研究表明,单次施用大量磷肥后,依靠磷的后效依然可以达到增产的效果,但是磷的后效也高度依赖于土壤类型、施肥量、施肥方式和管理措施等[6-8]。如Ibrikci等[6]的研究表明单次施磷99 kg·hm–2后,在长达5年的时间内仍能显著促进作物产量和作物吸磷量。Eijk等[7]对五种不同母质发育的土壤进行磷后效实验发现,在3个生长季后,除磷丰富的母质发育的土壤外,一次性投入磷肥在其他4种土壤中均对玉米产量和土壤磷含量有显著的促进效应,少量穴施磷肥与在表层土中大量撒播磷肥对作物产量的促进效应相似,因此认为少量穴施磷肥是一种更为经济有效的施肥方式。但也有研究表明不同磷肥种类在不同作物上的后效表现不同[8]。此外,Kisinyo等[9]发现磷肥和其他措施配合(如石灰),在4个生长季后,仍具有显著增加土壤有效磷和作物产量的效果。这主要是由于石灰与磷肥共同使用增加了土壤pH,降低土壤交换性铝浓度和土壤对磷的吸附,增加了磷的生物有效性。Kamiri等[10]的研究则表明单次大量施磷配合后续少量磷添加可以更好地促进作物生长和营养吸收。基于作物功能性状的研究也表明在小麦/玉米/大豆间套作体系中依靠小麦季施加的磷肥就可以促进大豆籽粒产量、大豆总荚数和饱荚率,进而提高磷肥利用效率[11]。然而这些研究对土壤磷后效观测的时间较短(< 10年),不能在长时间尺度上反映磷的后期效应。其次,大量观测数据表明,生态系统中氮磷循环存在强烈的协同作用,氮添加可显著促进磷循环,提高植物可利用性磷含量,而磷添加可促进植物对氮的吸收[12]。此外,微生物是土壤养分循环转化的驱动者和土壤生态功能的执行者[13],微生物对氮素的转化过程与氮素的可利用性密切相关,土壤酶活和土壤呼吸等是表征土壤微生物代谢活性和土壤质量的重要指标,可以更全面地反映土壤生态功能和养分循环状况[14]。但以往的研究更多关注磷肥在作物产量、作物功能性状和土壤养分方面的后效,鲜有研究从土壤微生物活性和氮循环的角度探讨磷的后期效应。
本研究以云南曲靖红壤长期磷后效定位观测试验样地为研究对象,研究了短期投入不同浓度梯度的磷肥多年后,对土壤养分、磷循环相关酶活性、土壤微生物生物量以及氮循环过程的影响,并利用主成分分析、聚类分析和冗余分析探讨了其间的相互关系,以期从土壤酶活性、土壤微生物功能活性等角度评价磷的后效,为揭示红壤磷的固定和解析机制,为农田施肥管理提供科学依据和指导。
1 材料与方法 1.1 研究区概况和试验处理研究区位于云南省曲靖市麒麟区越州镇(25º18´6.8"N,103º53´55.4"E),海拔1 906 m,年均温13~15℃,年降雨量900~1 000 mm。该地区属于低纬高原季风气候,土壤类型为老冲积母质发育的山原红壤[15]。
长期定位试验始于1987年,共包括5个磷梯度处理:P0、P50、P100、P150、P1000,施磷量分别0、50、100、150、1 000 kg·hm–2(P2O5计),另设1个常规施肥处理(CK)。常规施肥处理三个小区重复,不同磷梯度处理一个小区重复,小区面积33.3 m2。自1987年种植玉米开始,P50、P100、P150和P1000处理分别施入对应剂量的过磷酸钙,连续施用6年后停施磷肥以观测后效。常规施肥处理每年施用磷肥120 kg·hm–2(过磷酸钙),同时配施与当地农田施肥水平一致的尿素(276 kg·hm–2·a–1)和30 t·hm–2·a–1的有机肥(农家肥)。有机肥中有机质含量约830 g·kg–1,全氮含量约22 g·kg–1,有效磷和速效钾含量分别约为6.1 g·kg–1和4.5 g·kg–1。有机肥作为底肥一次性穴施,尿素作为追肥,苗肥施30%,穗肥施70%。试验小区夏季种植玉米(4月中旬播种),品种均为当地推广的玉米杂交良种,冬季休耕。
1.2 土壤样品采集和理化性质测定土壤样品采集于2019年夏季(7月15日)和秋季(10月15日),分别代表了作物生长旺盛期和作物收获后期,在常规施肥处理每个小区五点法在两株玉米间采集0~20 cm的土壤,混合为一个土壤样品。不同磷梯度处理小区则沿3条平行线进行样品采集,每条平行线取3点混和为一个重复。样品于冰袋上运回实验室后过2 mm筛,一部分风干后用于测定土壤理化性质,另一部分储存在4 ℃的冰箱,用于测定生物化学活性指标。玉米产量由小区实测产量换算得到。由于不同磷梯度处理仅有一个小区重复,故本文选取了同一处理近三年(2017-2019年)的产量数据平均值作为该处理的产量重复。
土壤理化性质测定参考文献[16]:土壤pH(水土比2.5:1)采用酸度计电位法测定,土壤含水量采取烘干称重法测定;NH4+-N和NO3–-N采用1 mol·L–1的KCl浸提、连续流动分析仪测定(AA3,Bran + Luebbe,Germany),土壤有效磷(Available Phosphorus,AP)采用Olsen法测定,土壤全碳(Total Carbon,TC)和全氮(Total Nitrogen,TN)含量采用元素分析仪测定(Vario EL III-Elementar,Germany),土壤全磷(Total phosphorus,TP)含量采用H2SO4-HClO4消解,钼蓝比色法测定。
1.3 土壤微生物活性和氮循环相关过程速率和潜势分析土壤呼吸速率(Soil respiration,SR)[17]采用微宇宙培养法测定。微生物生物量碳(Microbial biomass carbon,MBC)采用氯仿熏蒸法进行测定[17]。土壤固氮酶活性(Soil Nitrogenase activity,SNA)采用乙炔还原法进行测定[18]。
酸性磷酸酶(Acid phosphatase,ACP)活性的测定采用荧光法[19]。称取2 g鲜土,按照水土比为125:1的比例加入50 mmol·L–1的醋酸钠缓冲液,并调节pH至土壤本底pH。用旋涡振荡器混匀,吸取土壤悬浊液200 μL置于酶标板中,并加入50 μL带有荧光标记的磷酸盐底物,于25 ℃黑暗培养2 h后,在激发波长为360 nm、接收波长为460 nm处测定吸光度。
氮矿化速率(Nitrogen mineralization,Nmin)[17]:称取20 g鲜土置于120 mL灭菌的血清瓶中,调整土壤含水量至田间持水量的60%,于25 ℃、黑暗下培养7 d,期间称重加入无菌水保持土壤水分恒定。培养结束后测定初始和培养结束后的土壤无机氮(NH4+-N和NO3–-N)含量,氮矿化速率以土壤无机氮的变化速率表示。
潜在硝化速率(Potential nitrification rate,PNR)的测定采用氯酸盐抑制法[20]。称取5 g鲜土置于50 mL离心管中,加入20 mL含1 mmol·L–1(NH4)2SO4和50 mg·L–1 KClO3的生理盐水(pH 7.0)(为避免磷酸缓冲液对磷的补给影响,本研究采用生理盐水替代磷酸缓冲液)。于室温(25 ℃)黑暗处180 r·min–1培养24 h,后加5 mL KCl(1 mol·L–1)溶液浸提NO2–,离心并过滤,上清液用于测定NO2–含量。潜在硝化速率以24 h内NO2–的变化速率表示。
潜在N2O排放速率(Potential N2O emission rate,PN2O)和净N2O排放速率(Net N2O emission rate,NN2O)[21]:分别设置两组处理(加乙炔和不加乙炔),称取5 g干土所对应的鲜土量于120 mL血清瓶中,加无菌水至总水量13 mL。用橡胶塞和铝盖封口后,在恒温摇床上180 r·min–1水平震荡20 min以排出土壤孔隙中的空气,后充高纯氮5 min排除血清瓶中的空气,然后向乙炔处理的血清瓶中充入10%(v/v)的乙炔。然后在加入含2 mg·L–1氯霉素的DEA溶液8 mL。置于恒温培养箱中25 ℃、黑暗条件下培养24 h,分别于12和24 h采集血清瓶上空气体样品,使用配备有火焰电离检测器(FID)和电子捕获检测器(µECD)的气相色谱仪(Agilent 7890,Santa Clara,CA,美国)测量气体样品中的N2O浓度,以单位时间内N2O浓度变化表征N2O的排放速率。潜在N2O排放速率以乙炔处理中的N2O排放速率表示,净N2O排放速率以不加乙炔处理中的N2O排放速率表示。
1.4 数据处理数据的单因素、双因素方差分析和差异显著性检验(Duncan,P < 0.05)以SPSS(Version 22)软件进行。采用R(Version 3.4.3)软件进行Spearman相关分析(Package=“Corrplot”)、主成分分析(PCA,Package=“stats”)、冗余分析(RDA,Package=“vegan”)、聚类分析(Package=“stats”)。
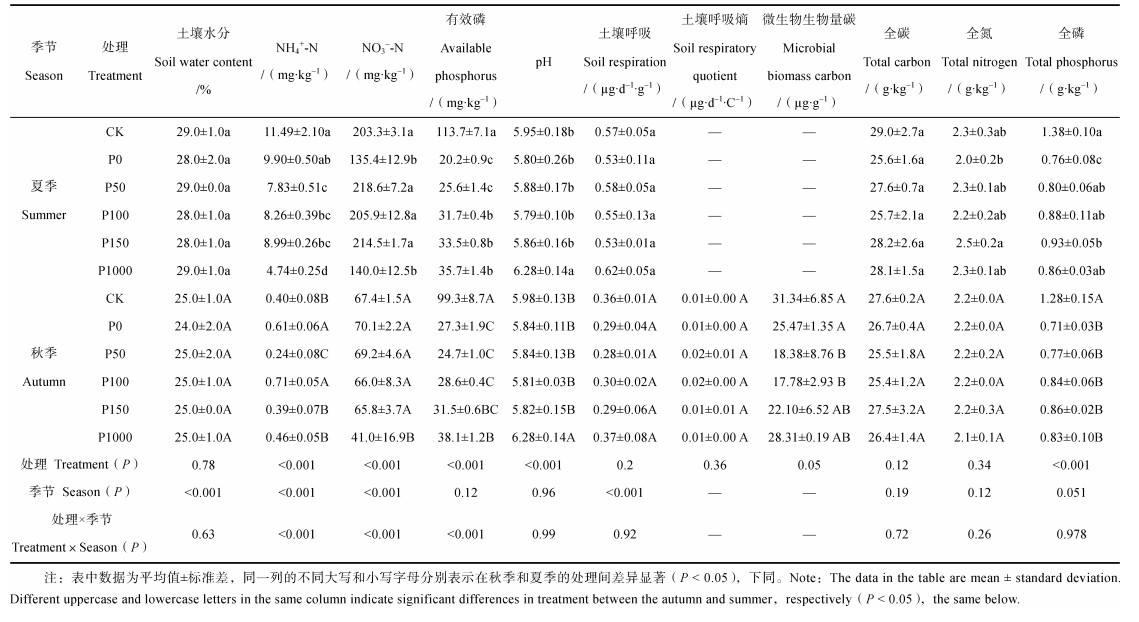
2 结果 2.1 不同磷处理对土壤理化性质和作物产量的影响土壤物理化学性质在不同处理间具有显著差异(表 1)。其中,土壤pH除在P1000处理中显著较高外(pH = 6.28),在其他处理均无显著差异(P < 0.001,表 1)。在夏季,土壤AP含量在常规施肥(CK)处理中最高,为113.7 mg·kg–1,在P100,P150和P1000处理中次之(31.67~35.66 mg·kg–1),在P50和P0处理中最低(P < 0.001,表 1)。在秋季,土壤AP表现出与夏季相似的趋势。在夏季,土壤TP含量在常规施肥处理中最高(1.38 g·kg–1),P50、P100、P150和P1000次之,在P0处理中最低(0.76 g·kg–1)(P < 0.001,表 1),且土壤TP含量在秋季的变化趋势与夏季类似。
|
|
表 1 长期不同施肥处理下土壤化学性质 Table 1 Soil chemical properties under different long-term fertilization treatment |
在夏季,NH4+-N含量在常规施肥和P0处理中最高(分别为11.49 mg·kg–1和9.90 mg·kg–1),P50、P100、P150处理中次之(7.83~8.99 mg·kg–1),P1000处理中最低(4.74 mg·kg–1)(P < 0.001,表 1)。在秋季,所有处理的NH4+-N含量显著降低至1.0 mg·kg–1以下(P < 0.001,表 1)。在夏季,土壤NO3–-N含量在常规施肥处理、P50、P100、P150中最高(203.3~218.6 mg·kg–1),在P0和P1000处理中最低(135.4~140.0 mg·kg–1)(P < 0.001,表 1)。在秋季,各处理中土壤NO3–-N含量显著低于夏季(P < 0.001,表 1),且在P1000处理中显著(41.04 mg·kg–1)低于其他处理。无论夏季还是秋季,土壤全碳(TC)、全氮(TN)、土壤呼吸(SR)和土壤呼吸熵(SQ)在不同处理间均无显著差异(P > 0.05,表 1)。
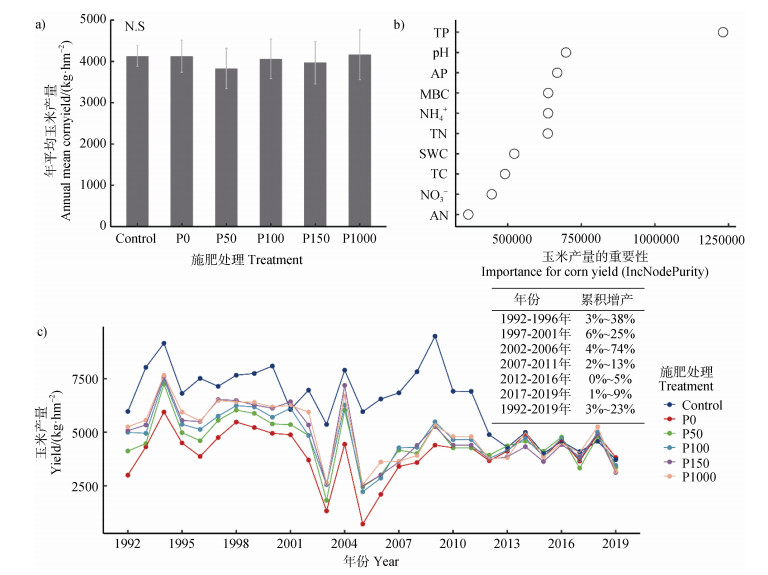
不同施肥处理下近三年(2017-2019)玉米平均产量无显著差异(3 828~4 164 kg·hm–2,P > 0.05,图 1a)。随机森林模型模拟分析结果表明,TP含量是玉米产量的主要预测因子,其次为土壤pH和AP(图 1b)。进一步汇总1992-2019年间的玉米产量数据,结果表明在1992-2011年期间,玉米产量均表现为常规施肥处理最高,P1000、P150、P100、P50处理依次降低,P0处理最低。但在2011年以后,玉米产量在不同处理间的差异较小(图 1c)。计算P1000处理相对其他磷梯度处理的累积增产效应,即P1000处理相对其他磷梯度处理(P0、P50、P100、P150)的产量增加百分比,发现P1000处理相对于其他磷梯度处理的增产效应在2006年之前最高(累积的增产效应可以达到4%~74%),但随着时间延长逐渐降低,2007-2011年间的增产效应仅为2%~13%,2011年以后进一步降低;在长期尺度上(1992-2019年),P1000处理相对于其他低磷处理累积增产效应达3%~23%(图 1c)。
|
注:NS代表处理间无显著性差异,下同;图 1c中的累积增产效应指P1000处理相对其他磷梯度处理(P0、P50、P100和P150)的增产百分比。 Note: NS represents no significant difference between treatments. The cumulative yield promotion effect in Fig.1c refers to the growth rate of maize yield in the P1000 treatment in comparison to other phosphorus treatments(P0, P50, P100 and P150). 图 1 不同施肥处理下近三年(2017-2019年)玉米年平均产量(a)、不同因子对近三年玉米产量的随机森林预测(b)以及1992-2019年间的玉米产量(c) Fig. 1 Maize mean yield in recent three years(2017-2019)under different fertilization treatments(a), random forest regression between crop yield and different soil factors(b), and corn yield during 1992-2019(c) |
土壤微生物生物量碳(MBC)在常规施肥处理中最高(31.34 µg·g–1),P150和P1000处理次之,P50和P100处理最低(表 1)。土壤呼吸(SR)和土壤呼吸熵(SQ)在不同处理间无显著性差异,但是SR在秋季显著降低(P < 0.05,表 1),这可能是由于作物收获后根际分泌物减少,微生物的生长代谢减弱所致。
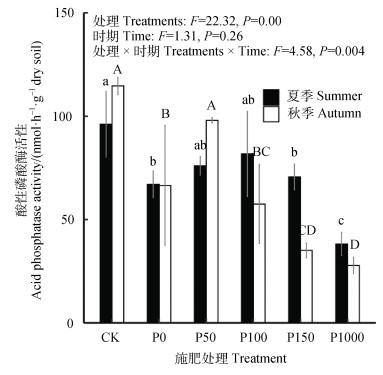
酸性磷酸酶(ACP)活性反映了土壤微生物对土壤磷的活化能力和磷供应能力,与土壤磷水平紧密相关。夏季,ACP活性在常规施肥处理中最高(96.08 nmol·h–1·g–1干土),P1000处理中最低(38.15 nmol·h–1·g–1干土,P < 0.001,图 2),秋季表现出类似的趋势。
|
注:不同小写和大写字母分别表示在夏季和秋季的处理间具有显著性差异(P < 0.05),下同。 Note: Different lowercase and uppercase letters indicated significant differences in treatment between the summer season and the autumn, respectively(P < 0.05). 图 2 不同磷处理下土壤酸性磷酸酶活性 Fig. 2 Soil acid phosphatase activity under different phosphorus treatments |
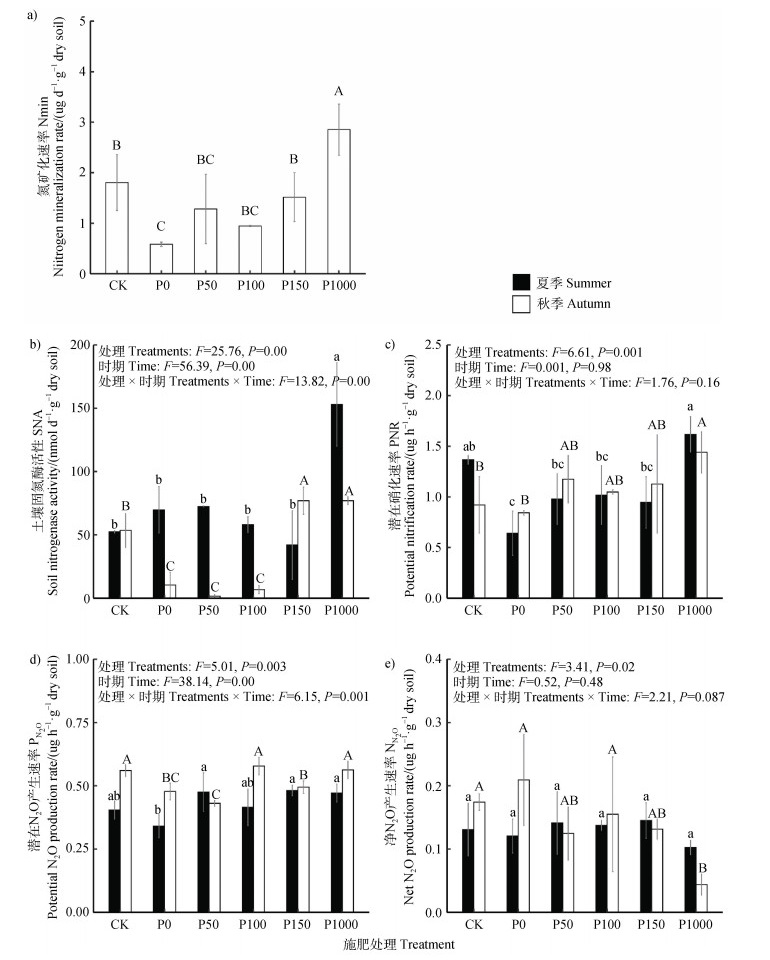
P1000处理土壤氮矿化速率(2.85 µg·d–1·g–1干土)显著高于其他处理(P < 0.05,图 3a)。与常规施肥处理相比,氮矿化速率在不施磷处理(P0,0.58 µg·d–1·g–1干土)中降低了67.6%(P < 0.05,图 3a),但在P50、P100、P150处理中与常规施肥处理无明显差异。在夏季,土壤固氮酶活性在P1000处理中达到最高(153.1 nmol·d–1·g–1干土),单在常规施肥、P0、P50、P100和P150处理中无显著差异(41.95~72.42 nmol·d–1·g–1干土)。在秋季,也表现为在P150和P1000处理中最高(76.9 nmol·d–1·g–1干土),并显著高于常规施肥处理(P < 0.05,图 3b)。
|
图 3 不同磷处理对氮循环过程的影响 Fig. 3 Nitrogen cycle process under different phosphorus treatments |
与土壤氮矿化速率一致,夏季土壤硝化潜势(PNR)在P1000处理中最高,达1.62 µg·h–1·g–1干土,在P50、P100和P150次之(0.95~1.02 µg·h–1·g–1干土),在P0处理中最低(0.64 µg·h–1·g–1干土,P < 0.05,图 3c)。土壤硝化潜势在秋季与夏季无明显差异,且趋势与夏季一致。
在夏季,土壤潜在N2O排放速率(PN2O)在P0处理中最低(0.34 µg·h–1·g–1干土,P < 0.05,图 3d),在其他处理中无显著性差异。在秋季,PN2O在常规施肥(CK)、P100和P1000处理中最高(0.56~0.58 µg·h–1·g–1干土),P150处理次之,P0和P50处理最低(P < 0.05,图 3d)。净N2O排放速率(NN2O)在夏季和秋季均表现为在P1000处理中最低(0.04~0.10 µg·h–1·g–1干土),其他处理无显著性差异(图 3e)。
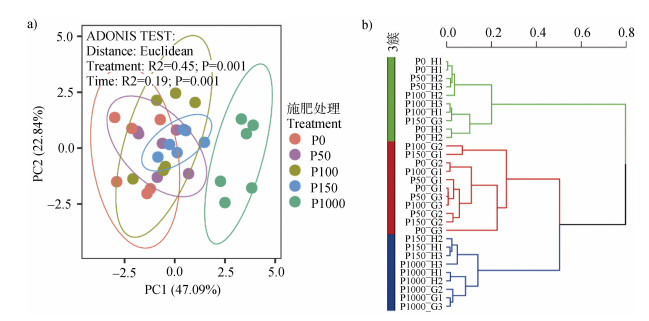
2.4 不同土壤及生物因子间的相互关系对土壤呼吸、磷酸酶活性和氮循环相关过程(SNA,PNR,PN2O和NN2O)进行主成分分析,前两个主成分解释了69.93%的变异(图 4a),P1000处理和其他处理在PC1轴上显著分开,不同采样时期在PC2轴上显著分开(处理:P = 0.001;时期:P = 0.001)。聚类分析进一步支持了主成分分析的结果,样本聚为三簇,P1000处理和秋季P150处理聚在一起,其他的样点按照不同采样时期分别聚为两簇(图 4b),表明P1000处理对土壤氮循环过程、土壤磷酸酶和土壤呼吸具有强烈的影响。
|
注:b)图字母H表示秋季,G表示夏季。 Note: The letter H represents autumn and G represents summer. 图 4 不同磷处理下土壤氮转化过程速率分布特征的主成分分析(a)和平均聚合聚类(方法:UPGMA)分析(b) Fig. 4 Principal component analysis(a)and cluster analysis(b)(UPGMA)for the potential rates of soil nitrogen transformation processes under different phosphorus treatments |
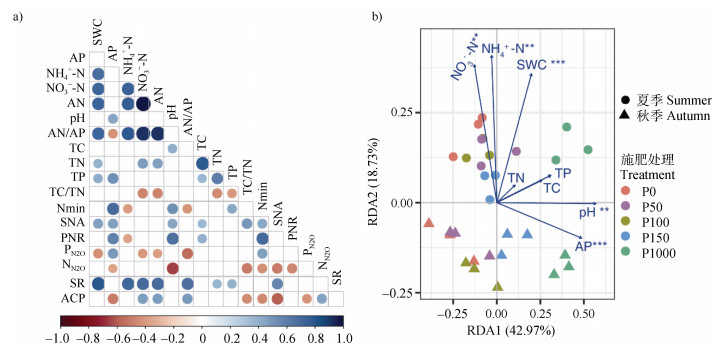
Spearman相关分析表明,土壤氮循环过程、磷酸酶活性和土壤呼吸速率与土壤AP、pH、NH4+-N、NO3–-N等均具有极显著的相关性(P < 0.05,图 5a)。冗余分析(RDA)结果表明pH和AP是影响氮循环过程、磷酸酶活性和土壤呼吸速率的主要环境因子(P < 0.05,图 5b)。说明土壤pH和AP对磷酸酶活性、土壤氮矿化、固氮作用、硝化和反硝化过程等均有显著影响。
|
注:图a中有圆圈的部分代表具有显著的相关性(P < 0.05),圆圈的大小和颜色分别代表了相关系数的大小和正负。图b中的*代表了具有显著性影响的环境因子。 Note: The circles in Fig. 5a represents significant correlation(P < 0.05). The size and color of circles represent the size, plus or minus of correlation coefficients, respectively. The"*"in Fig. 5b represents the environmental factors that have a significant impact. 图 5 土壤微生物活性、非生物因子间的Spearman相关分析(a)和微生物活性的冗余分析(b) Fig. 5 Spearman correlation analysis between soil microbial activity and non-biological factors(a)and Redundancy analysis for microbial activity(b) |
本研究表明,在短期内(6年)连续施加大量磷肥后,即使多年不再施磷肥,仍然可以将土壤肥力、pH维持在较高的水平,进而有益于土壤微生物活性和作物产量。戴茨华等[15]对本研究的长期定位试验前20年的土壤养分和产量数据分析结果表明,在短期大量施磷后,只依赖磷的后效仍然可以有效维持土壤磷水平、作物养分含量和作物产量,前20年累积增产达51%。本研究的进一步分析发现,与常规施肥处理相比,P1000处理27年后,仍能显著提高土壤pH,并使TC、TN和MBC含量维持在与常规施肥处理相似的水平。表明短期多次投入高剂量磷肥可以使土壤养分维持在较高的水平,并有效减缓了施氮肥导致的土壤pH降低。类似地,Chu等[22]的研究发现,在红壤稻田生态系统中施加磷肥可以促进土壤脱氢酶活性,增加多种土壤养分含量。Ibrikci等[6]的研究也表明单次施磷后,在后续的五年时间内显著增加了土壤有效磷含量和作物磷吸收量,对玉米的增产效应达8%~33%。所有这些研究均表明,短期施加大量磷肥可以在较长的时间尺度上维持较高的土壤肥力(例如AP、TC、TN和TP等)和养分供应潜能,表现出强烈的磷后期效应。这可能是由于在相对缺磷的红壤生态系统中,高剂量磷的添加缓解了磷限制,并通过促进作物生长增加了根际碳水化合物的释放,提高了微生物活性,进而促进了土壤养分释放[23]。对该试验平台2006年前的观测数据分析结果也表明,连续施磷6年停施多年后玉米籽粒、茎叶和土壤有效磷的含量与施磷量呈正相关,磷肥的残效随施磷量增加而增加[15]。但近年的玉米产量数据分析显示不同处理间无显著差异,一方面可能是磷肥的效应在缓慢减弱,另一方面可能是由于本研究中所有处理每年均有有机肥施入(30 t·hm–2·a–1),有机肥的添加补充了N、P、K养分,弱化了不同磷处理间作物产量差异。
酸性磷酸酶(ACP)活性反映了土壤微生物对土壤磷的活化能力和磷供应能力[24]。本研究发现ACP活性在常规施肥处理中最高,在其他磷梯度处理中较低。这可能是由于常规施肥处理中磷肥的大量投入增加了磷酸酶的底物可利用性,同时有机肥施加也为土壤微生物提供的充足的碳源和氮源,进而增加了土壤磷酸酶活性。类似地,Zhang等[24]对比了磷含量不同的两种森林土壤,结果表明磷酸酶活性在磷含量丰富的温带森林土壤中更高,而在相对缺磷的热带森林和亚热带森林土壤中较低,与土壤中磷的含量紧密相关,且与碳源和氮源的可利用性正相关[25]。然而,我们研究还发现在短期投入不同磷梯度的处理中,随着施磷量增加,ACP活性呈现下降趋势,并在P1000处理中最低,相关分析也表明ACP活性和AP显著负相关。与此相一致,Meta分析和相当多的研究结果均表明ACP活性常与无机磷含量负相关[26]。综上所述,磷酸酶活性在常规施肥处理中较高而在高磷梯度处理中较低,可能与不同土壤系统中磷的存在形态和微生物的可利用性等密切相关,其机制有待进一步解析。
微生物既是土壤养分循环的执行者,也是土壤中有效养分的储备库,因而可以作为土壤养分状况和土壤质量的表征[27]。本研究发现,与不施磷和低磷处理相比,P1000处理显著提高了土壤微生物碳含量,但与常规施肥处理无显著差异。这表明短期添加大量磷可以在较长时间尺度上促进微生物生长,提高土壤中微生物总生物量。与此类似,Chu等[22]在红壤稻田生态系统中的研究结果表明,磷肥添加可以显著增加土壤微生物量碳和土壤脱氢酶活性。Zheng等[28]的研究表明,相比长期不施磷肥,磷肥添加可以显著增加细菌、真菌和放线菌的数量,并且显著增加土壤微生物活性指标(例如,峰值功率Pmax、总热量输出Qt、出峰时间tmax和热量输出速率Qt/t)。这些研究结果表明短期大量施加磷肥可以在长时间尺度上增加土壤总微生物量,表现出强烈的磷后期效应。一方面可能是因为磷的添加缓解了红壤生态系统中的磷限制,另一方面可能是磷的添加提升了土壤养分含量,进而促进微生物的生长和活性。本研究中土壤呼吸和微生物代谢熵在不同磷处理中无显著差异,可能为有机肥添加整体刺激了土壤微生物的活性所致。
3.2 不同磷处理对氮循环过程的影响土壤矿化作用,生物固氮和硝化作用是土壤重要的氮素转化过程,决定中土壤中有效态氮的供应。本研究发现P1000处理中土壤氮矿化速率(Nmin)和固氮酶活性(SNA)均显著高于常规施肥处理和不施磷处理。与此类似,P1000处理中潜在硝化速率(PNR)也显著高于常规施肥处理和P0处理。表明短期大量磷添加可以在长时间尺度上促进红壤的有机氮矿化、固氮作用和硝化作用过程,表现出明显的磷后效。Chen等[23]的研究表明在红壤中合理施用磷肥(< 25 mg·kg–1)可以通过增加脲酶和脱氢酶活性促进氮的矿化。Mehnaz等[29]的研究也表明磷添加可以显著提升土壤的正激发效应,促进土壤有机质矿化。此外,Tang等[30]的结果表明在红壤农田中,磷的添加可以显著的促进nifH基因的表达和生物固氮速率。已有的多数研究结果也表明,磷肥添加可以显著促进土壤硝化潜势和氨氧化微生物的丰度[31]。这可能是由于短期大量磷添加一方面增加了土壤AP和TP,缓解了依赖于“磷元素”的能量供应限制,从而激活了参与氮循环的功能微生物的活性[23]。另一方面,我们的分析结果表明氮矿化、固氮酶活性和潜在硝化速率均与土壤pH呈显著正相关关系(P < 0.05,图 5),表明短期大量施肥磷肥通过提高土壤pH进而促进了土壤的矿化、固氮和硝化速率[32]。
反硝化作用是农田土壤温室气体N2O排放的主要来源,对于全球变暖具有重要的贡献[25]。本研究表明P1000处理中净N2O排放速率显著低于其他处理(P < 0.05,图 3e)。与之相类似,Baral等[12]通过室内培养实验表明磷添加可以通过促进植物对土壤中无机氮的吸收,进而降低了土壤N2O排放,原位分根实验进一步表明在植物根系存在时,磷添加可以降低N2O排放,而根系不存在时则表现为增加了N2O排放,这进一步证明了磷添加可以促进植物对土壤中无机氮的吸收,进而降低土壤N2O排放。施加磷肥降低土壤潜在N2O排放潜能,一方面可能是由于磷添加促进了植物对无机氮的吸收利用,减少了土壤无机氮含量,进而降低了N2O排放[12]。另一方面,可能是短期大量磷添加增加了土壤pH所致,已有研究表明较高的pH条件有利于N2O的还原,从而减少了N2O的净排放速率[33]。这些结果表明通过磷肥施用减少农田生态系统磷限制对于消减N2O具有及其重要的意义。
4 结论在酸性红壤中短期大量施用磷肥(1 000 kg·hm–2,P1000)多年后(长达27年),由于大量磷肥投入导致的土壤pH提升和磷的缓释效应,使得磷肥在提升土壤肥力、微生物活性、土壤氮循环功能活性以及维持产量方面表现出明显的后期效应。在酸性红壤中长期投入较高的磷肥后,应关注磷的残效及其对氮循环过程的影响。
| [1] |
Camenzind T, Hättenschwiler S, Treseder K K, et al. Nutrient limitation of soil microbial processes in tropical forests[J]. Ecological Monographs, 2018, 88(1): 4-21. DOI:10.1002/ecm.1279
(  0) 0) |
| [2] |
Du E Z, Terrer C, Pellegrini A F A, et al. Global patterns of terrestrial nitrogen and phosphorus limitation[J]. Nature Geoscience, 2020, 13(3): 221-226. DOI:10.1038/s41561-019-0530-4
(  0) 0) |
| [3] |
Cheng M F, He P, Jin J Y. Advance of phosphate recovery rate in Chinese main crops (In Chinese)[J]. Crops, 2010(1): 12-14. DOI:10.3969/j.issn.1001-7283.2010.01.004 [我国主要作物磷肥利用率的研究进展[J]. 作物杂志, 2010(1): 12-14.]
(  0) 0) |
| [4] |
Gilbert N. Environment: The disappearing nutrient[J]. Nature, 2009, 461(7265): 716-718. DOI:10.1038/461716a
(  0) 0) |
| [5] |
Weihrauch C, Opp C. Ecologically relevant phosphorus pools in soils and their dynamics: The story so far[J]. Geoderma, 2018, 325: 183-194. DOI:10.1016/j.geoderma.2018.02.047
(  0) 0) |
| [6] |
Ibrikci H, Ryan J, Ulger A C, et al. Maintenance of phosphorus fertilizer and residual phosphorus effect on corn production[J]. Nutrient Cycling in Agroecosystems, 2005, 72(3): 279-286. DOI:10.1007/s10705-005-3367-8
(  0) 0) |
| [7] |
Van der Eijk D, Janssen B H, Oenema O. Initial and residual effects of fertilizer phosphorus on soil phosphorus and maize yields on phosphorus fixing soils: A case study in south-west Kenya[J]. Agriculture, Ecosystems & Environment, 2006, 116(1/2): 104-120.
(  0) 0) |
| [8] |
Ojo O D, Akinrinde E A, Akoroda M O. Residual effects of phosphorus sources in grain amaranth production[J]. Journal of Plant Nutrition, 2010, 33(5): 770-783. DOI:10.1080/01904160903577648
(  0) 0) |
| [9] |
Kisinyo P O, Othieno C O, Gudu S O, et al. Immediate and residual effects of lime and phosphorus fertilizer on soil acidity and maize production in western Kenya[J]. Experimental Agriculture, 2014, 50(1): 128-143. DOI:10.1017/S0014479713000318
(  0) 0) |
| [10] |
Kamiri W M H, Pypers P, Vanlauwe B. Residual effects of applied phosphorus fertilizer on maize grain yield and phosphorus recovery from a long-term trial in western Kenya[M] Netherlands: Springer Netherlands, 2011.
(  0) 0) |
| [11] |
Chen Y X, Zhou T, Huang W, et al. Phosphrous aftereffects on soybean yield and nutrition status in wheat/maize/soybean intercropping system (In Chinese)[J]. Plant Nutrition and Fertilizer Science, 2013, 19(2): 331-339. [小麦/玉米/大豆间套作体系中小麦施磷后效对大豆产量、营养状况的影响[J]. 植物营养与肥料学报, 2013, 19(2): 331-339.]
(  0) 0) |
| [12] |
Baral B R, Kuyper T W, van Groenigen J W. Liebig's law of the minimum applied to a greenhouse gas: Alleviation of P-limitation reduces soil N2O emission[J]. Plant and Soil, 2014, 374(1/2): 539-548.
(  0) 0) |
| [13] |
Kuypers M M M, Marchant H K, Kartal B. The microbial nitrogen-cycling network[J]. Nature Reviews Microbiology, 2018, 16(5): 263-276. DOI:10.1038/nrmicro.2018.9
(  0) 0) |
| [14] |
Sinsabaugh R L, Follstad Shah J J. Ecoenzymatic stoichiometry and ecological theory[J]. Annual Review of Ecology, Evolution, and Systematics, 2012, 43(1): 313-343. DOI:10.1146/annurev-ecolsys-071112-124414
(  0) 0) |
| [15] |
Dai C H, Wang J S, Dai P. Studies on the residual effect of application phosphorus on red soil of a long-term experiment (In Chinese)[J]. Chinese Agricultural Science Bulletin, 2009, 25(11): 93-97. [从长期定位试验论红壤施磷的残效[J]. 中国农学通报, 2009, 25(11): 93-97.]
(  0) 0) |
| [16] |
Lu R K. Analytical methods for soil and ago-chemistry (In Chinese). Beijing: China Agricultural Science and Technology Press, 2000. [土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000.]
(  0) 0) |
| [17] |
Schinner F, Öhlinger R, Kandeler E, et al. Methods in soil biology . Berlin: Springer, 1995.
(  0) 0) |
| [18] |
Patra A K, Abbadie L, Clays-Josserand A, et al. Effects of management regime and plant species on the enzyme activity and genetic structure of N-fixing, denitrifying and nitrifying bacterial communities in grassland soils[J]. Environmental Microbiology, 2006, 8(6): 1005-1016. DOI:10.1111/j.1462-2920.2006.00992.x
(  0) 0) |
| [19] |
DeForest J L. The influence of time, storage temperature, and substrate age on potential soil enzyme activity in acidic forest soils using MUB-linked substrates and l-DOPA[J]. Soil Biology & Biochemistry, 2009, 41(6): 1180-1186.
(  0) 0) |
| [20] |
Kurola J, Salkinoja-Salonen M, Aarnio T, et al. Activity, diversity and population size of ammonia-oxidising bacteria in oil-contaminated landfarming soil[J]. FEMS Microbiology Letters, 2005, 250(1): 33-38. DOI:10.1016/j.femsle.2005.06.057
(  0) 0) |
| [21] |
Gardner L M, White J R. Denitrification enzyme activity as an indicator of nitrate movement through a diversion wetland[J]. Soil Science Society of America Journal, 2010, 74(3): 1037-1047. DOI:10.2136/sssaj2008.0354
(  0) 0) |
| [22] |
Chu H Y, Lin X G, Fujii T, et al. Soil microbial biomass, dehydrogenase activity, bacterial community structure in response to long-term fertilizer management[J]. Soil Biology & Biochemistry, 2007, 39(11): 2971-2976.
(  0) 0) |
| [23] |
Chen Y, Sun T T, Qian H Y, et al. Nitrogen mineralization as a result of phosphorus supplementation in long-term phosphate deficient soil[J]. Applied Soil Ecology, 2016, 106: 24-32. DOI:10.1016/j.apsoil.2016.04.019
(  0) 0) |
| [24] |
Zhang X Y, Yang Y, Zhang C, et al. Contrasting responses of phosphatase kinetic parameters to nitrogen and phosphorus additions in forest soils[J]. Functional Ecology, 2018, 32(1): 106-116. DOI:10.1111/1365-2435.12936
(  0) 0) |
| [25] |
Allison S D, Vitousek P M. Responses of extracellular enzymes to simple and complex nutrient inputs[J]. Soil Biology & Biochemistry, 2005, 37(5): 937-944.
(  0) 0) |
| [26] |
Marklein A R, Houlton B Z. Nitrogen inputs accelerate phosphorus cycling rates across a wide variety of terrestrial ecosystems[J]. New Phytologist, 2012, 193(3): 696-704. DOI:10.1111/j.1469-8137.2011.03967.x
(  0) 0) |
| [27] |
Sun B, Zhao Q G, Zhang T L, et al. Soil quality and sustainable environment-Ⅲ. Biological indicators for soil quality assessment (In Chinese)[J]. Soils, 1997, 29(5): 225-234. DOI:10.3321/j.issn:0253-9829.1997.05.001 [土壤质量与持续环境──Ⅲ. 土壤质量评价的生物学指标[J]. 土壤, 1997, 29(5): 225-234.]
(  0) 0) |
| [28] |
Zheng S X, Hu J L, Chen K, et al. Soil microbial activity measured by microcalorimetry in response to long-term fertilization regimes and available phosphorous on heat evolution[J]. Soil Biology & Biochemistry, 2009, 41(10): 2094-2099.
(  0) 0) |
| [29] |
Mehnaz K R, Corneo P E, Keitel C, et al. Carbon and phosphorus addition effects on microbial carbon use efficiency, soil organic matter priming, gross nitrogen mineralization and nitrous oxide emission from soil[J]. Soil Biology & Biochemistry, 2019, 134: 175-186.
(  0) 0) |
| [30] |
Tang Y F, Zhang M M, Chen A L, et al. Impact of fertilization regimes on diazotroph community compositions and N2-fixation activity in paddy soil[J]. Agriculture, Ecosystems & Environment, 2017, 247: 1-8.
(  0) 0) |
| [31] |
Chu H Y, Fujii T, Morimoto S, et al. Population size and specific nitrification potential of soil ammonia-oxidizing bacteria under long-term fertilizer management[J]. Soil Biology & Biochemistry, 2008, 40(7): 1960-1963.
(  0) 0) |
| [32] |
Wang C, Zheng M M, Song W F, et al. Impact of 25 years of inorganic fertilization on diazotrophic abundance and community structure in an acidic soil in Southern China[J]. Soil Biology & Biochemistry, 2017, 113: 240-249.
(  0) 0) |
| [33] |
McMillan A M S, Pal P, Phillips R L, et al. Can pH amendments in grazed pastures help reduce N2O emissions from denitrification? - The effects of liming and urine addition on the completion of denitrification in fluvial and volcanic soils[J]. Soil Biology & Biochemistry, 2016, 93: 90-104.
(  0) 0) |
 2022, Vol. 59
2022, Vol. 59