多环芳烃(polycyclic aromatic hydrocarbons,PAHs)是指含两个或两个以上苯环的碳氢化合物,广泛存在于大气、土壤、水体等环境介质中,是威胁生态安全和人类健康的一种典型持久性有机污染物,具有致癌、致畸、致突变性。美国国家环保局(USEPA)规定了16种优先控制PAHs,包括两环的萘,三环的蒽、菲、苊、苊烯、芴,四环的荧蒽、苯并[a]蒽、芘、
微生物降解是环境中PAHs削减的重要途径之一[1]。相关研究兴起之初,研究者主要关注好氧条件下的降解过程。大约从20世纪70年代开始,有研究者发现厌氧条件下PAHs同样能够发生微生物降解,但降解机理与好氧条件下不同[2]。土壤是环境中PAHs汇集和积累的重要场所,研究表明,我国表层土壤普遍受到PAHs污染[3],而许多受PAHs污染的土壤会经历甚至长期处于厌氧状态(例如底层土壤、稻田等)[4],因此,深入研究PAHs的厌氧降解对准确认知PAHs污染土壤的自净功能及修复原理具有重要意义。鉴于此,本文先以Web of Science核心数据库为数据源,利用VOSviewer和CiteSpace软件对PAHs厌氧微生物降解相关研究进行文献计量分析,并综述不同环境介质或研究体系中已开展的不同电子受体作用下PAHs厌氧微生物降解研究进展,梳理稳定同位素核酸探针(DNA-SIP)和组学(Omics)等新兴技术在该研究领域的最新应用案例。在此基础上,重点探讨土壤PAHs厌氧微生物降解研究领域的现存理论空白,并据此进行未来研究展望,为完善厌氧土壤中PAHs的污染自净与修复原理提供支撑。
1 材料与方法 1.1 数据来源数据来源于美国汤森路透公司(Thomson Reuters)Web of Science(WOS)核心合集数据库,检索时间为2021年1月29日。检索主题词为:("polycyclic aromatic hydrocarbon?" or "PAH?" or naphthalene or anthracene or phenanthrene or fluoranthene or pyrene or benzo[a]pyrene)AND(anaerobic or anoxic)AND(biodegradation or microbial degradation or bacteria degradation or microbial metabolism or bacteria metabolism),其中双引号(" ")作用是将词组作为一个整体进行检索;问号(?)表示任意字符,包括空字符。时间跨度选择所有年份。
1.2 研究方法利用WOS自带的“分析检索结果”功能进行各学科和各年份文献发文量统计;导出检索到的767篇文献的全纪录与引用的参考文献,利用VOSviewer.1.6.16进行关键词共现分析和频数统计(为确保分析结果的准确性,采用如下分析途径:分析类型选择“co-occurrence”,分析单元选择“author keywords”;关键词共现图中频数阈值设置为5,频数统计表不设置阈值;手动合并同义词);利用CiteSpace.5.7.R2,以5年为时间切片进行文献共被引分析。
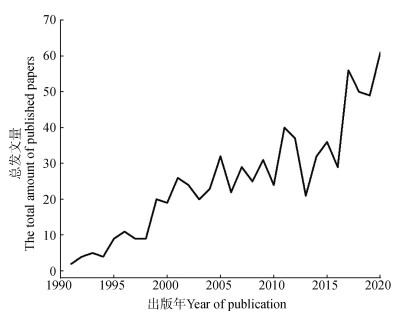
2 结果 2.1 PAHs厌氧微生物降解领域文献产出趋势和学科分布发文数量可反映一个研究领域受重视的程度及发展水平[5]。由于PAHs微生物降解相关的研究大多围绕好氧环境展开,较少关注厌氧环境,因此仅检索到767篇文献,发表年份最早为1991年。但从1991年至2020年,发文量整体呈波动式增长趋势(图 1)。
|
图 1 1991—2020年PAHs厌氧微生物降解领域发文量 Fig. 1 The amount of papers about PAHs anaerobic microbial degradation during 1991-2020 |
按照不同学科进行分类(表 1)可知,环境科学发文量(421)远高于其他学科,表明PAHs厌氧微生物降解与环境科学学科领域相关性最高。水资源学发文量(109)排名靠前,而土壤学却排在第22位,总发文量仅9篇(表中未列出)。
|
|
表 1 PAHs厌氧微生物降解领域发文量排名前五的学科 Table 1 Top 5 disciplines in terms of the amount of papers about PAHs anaerobic microbial degradation |
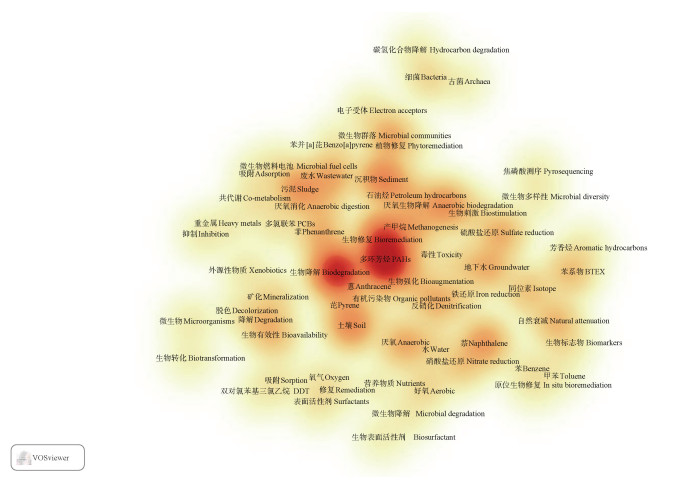
文献作者给出的关键词是对主旨的高度概括,因此进行关键词共现分析是了解研究热点的一种高效途径[6]。基于VOSviewer软件进行关键词共现分析(图 2),通过人为判断可知,该领域大致有以下几个热点内容:不同还原条件下的PAHs厌氧降解菌筛选及其特性研究(如关键词nitrate reduction、sulfate reduction、methanogenesis、iron reduction、bacteria、microbial communities等)、厌氧环境中PAHs转化途径及微生物修复策略(如关键词biotransformation、bioremediation、in situ bioremediation、bioaugmentation等)、影响PAHs厌氧微生物降解效率的因素(如关键词biostimulation、bioavailability、inhibition、nutrients、surfactants等)。
|
注:某关键词出现频率越高、相邻关键词个数越多,则其背景色越接近红色。 Note: The higher the occurrence frequency of a keyword and the more the number of its adjacent keywords, the closer its background color to red. 图 2 PAHs厌氧微生物降解领域关键词共现分析 Fig. 2 Keyword co-occurrence analysis of papers about PAHs anaerobic microbial degradation |
为直观地反映该领域研究的侧重点,对PAHs类型、还原条件、环境介质及新兴技术相关关键词频数进行分类统计(表 2)。在各类PAHs中,萘作为关键词出现的频数最高(频数43),其次是菲(频数28),而高环PAHs如芘(频数:13)和苯并[a]芘(频数7)出现的频数较低;常见的电子受体还原体系中,硝酸盐还原和反硝化作为关键词出现的总频数最高(频数48),其次是硫酸盐还原(频数31)和产甲烷(频数29),金属离子还原体系文献数量最少且几乎仅针对铁还原体系(频数12);在不同的环境介质中,水体(包括水、地下水和废水)作为关键词出现的总频数最高(频数76),这与学科发文量分析结果(表 1)一致;与新兴技术相关的关键词,如同位素(包括单体稳定同位素分析(CSIA)、DNA-SIP等)、组学、16s rRNA测序技术,出现频数均不高(低于23)。
|
|
表 2 PAHs厌氧微生物降解领域关键词分类统计 Table 2 Keywords classified statistic of papers about PAHs anaerobic microbial degradation |
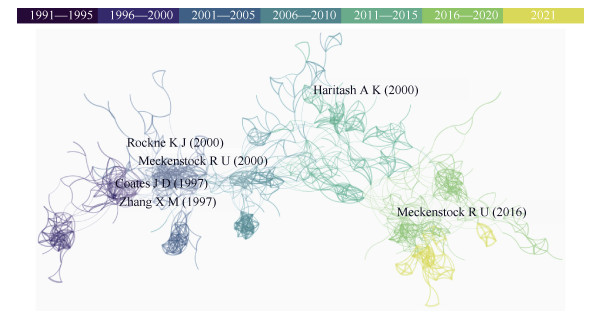
利用CiteSpace软件,进行文献共被引分析得到该领域被引频次最高的六篇文献(图 3),包括:1997年由Coates等[7]发表于Applied and Environmental Microbiology的研究论文,发现硫酸盐还原能够与多种PAHs的厌氧微生物降解相耦合;同年,由Zhang和Young[8]发表于同期刊的研究论文,首次提出羧化是硫酸盐还原条件下萘和菲微生物降解的活化途径;2000年,由Rockne等[9]发表于同期刊的研究论文,首次报道了纯培养条件下以硝酸盐为电子受体的萘降解;同年,由Meckenstock等[10]发表于同期刊的研究论文,对某菌群在硫酸盐还原条件下降解萘的途径进行探究,进而验证了Zhang和Young[8]的观点;2009年和2016年,由Haritash和Kaushik[11]与Meckenstock等[12]分别发表于Journal of Hazardous Material及Journal of Molecular Microbiology and Biotechnology的综述,对PAHs厌氧微生物降解的研究进展进行了系统的阐述。
|
图 3 PAHs厌氧微生物降解领域文献共被引分析 Fig. 3 Co-cited analysis of papers about PAHs anaerobic microbial degradation |
综上,PAHs厌氧微生物降解的研究在近30年间逐渐得到重视,但总发文量仍较少;最主要的发文学科为环境科学;研究热点主要包括不同还原条件下的PAHs厌氧降解菌筛选及降解机制研究、厌氧环境中PAHs迁移转化及原位微生物修复策略、影响PAHs厌氧微生物降解效率的因素等;在不同类型的PAHs中,萘得到了最广泛的关注,而高环PAHs相关文献较少;在常见的还原体系中,硝酸盐还原体系受到最多关注,硫酸盐还原体系次之,而产甲烷体系和金属离子还原体系文献数量较少;新兴技术在该领域的应用较少。此外,值得强调的是,综合表 1和表 2的数据可知,土壤学学科在该领域的发文量非常少,且针对土壤体系的研究少于水相和沉积物体系。
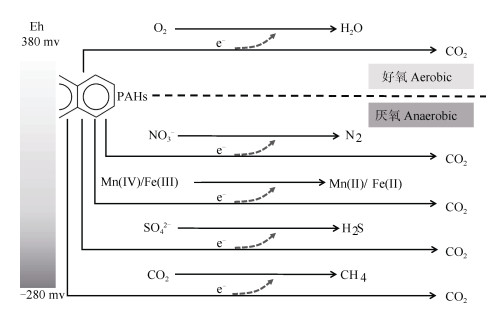
3 讨论基于上述文献计量分析,进一步对不同还原条件下PAHs厌氧微生物降解的研究进展进行剖析。好氧环境中,PAHs降解以氧气(O2)为电子受体;厌氧环境中O2缺乏,需要
|
注:图中Eh指pH=6.5时发生还原反应所需的氧化还原电位。其中,不同电子受体还原的Eh区间大致为:O2→H2O,Eh=380~320 mV; |
文献计量结果发现,针对反硝化(硝酸盐还原)体系的文献较多(表 2,频数48)。这是由于厌氧条件下硝酸盐作为电子受体具有优先利用性,环境中存在着许多可在反硝化条件下降解PAHs的细菌。例如,萘降解菌群NAP-3-1、NAP-3-2、NAP-4[9],以及菲降解菌PheN1[16]和菌群PheN9[17]等。这方面的研究多集中于探索降解菌特性或影响降解效率的因素,围绕降解机制的相对较少。例如,Qin等[18]提出反硝化条件下苯并[a]芘降解通过加氢还原活化,最终进入萘降解途径。Zhang等[16-17]结合基因组测序和降解产物分析,证实反硝化条件下菲降解存在羧化和甲基化两种活化方式。除NO3-和NO2-外,近期Zhang等[19]首次证实NO也可作为PAHs厌氧降解的电子受体。
3.2 金属离子还原体系PAHs厌氧微生物降解高价金属离子,特别是Fe(Ⅲ)和Mn(Ⅳ),也可作为PAHs厌氧微生物降解的电子受体。除铁锰之外,近期钒(V[V])被发现可作为菲厌氧微生物降解的电子受体[20]。根据文献计量结果,此方面研究数量最少(如表 2,频数12),已有的报道重点关注该还原体系中PAHs的降解途径。例如,Yan等[21]发现铁还原条件下苯并[a]芘降解会生成5-乙基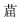
文献计量分析表明,针对硫酸盐还原体系的文献数量较多(表 2,频数31),仅次于反硝化体系。典型降解菌包括萘降解菌NaphS3、NaphS6[25]、菌群N47及菲降解菌PheS2[26]等。针对该体系,有较多研究对PAHs的降解机制展开了深入探讨。例如,Safinowski和Meckenstock[27]研究表明,甲基化是菌群N47降解萘的活化方式。而Musat等[25]则发现菌株NaphS3和NaphS6降解萘的活化方式为羧化。由此可知,硫酸盐还原条件下萘的微生物降解存在甲基化和羧化两种活化方式。还有研究者对萘的下游降解途径进行了探究,并证实该过程中有辅酶A参与[28-29]。部分研究者还借助组学技术研究了硫酸盐还原条件下PAHs降解的生物学机制。例如,Kraiselburd等[30]采用转录组学和蛋白组学的方法推断出硫酸盐还原菌群降解菲的途径。Qian等[31]采用宏基因组技术,揭示了硫酸盐还原条件下两种菌株协同降解复合PAHs污染的机制。
3.4 产甲烷体系PAHs厌氧微生物降解自然界中长期处于强还原条件的厌氧环境介质通常缺乏硫酸盐、硝酸盐或高价金属离子作为电子受体,而CO2或碳酸盐普遍存在,因此,产甲烷条件下的微生物降解是环境中PAHs削减的重要途径之一。而文献计量结果揭示出针对产甲烷体系的研究相对较少(表 2,频数29)。可能原因之一是该体系中PAHs微生物降解涉及甲烷的产生并伴随放热过程,使反应体系相对复杂。目前在该还原体系中分离得到的功能菌非常少,且已有研究鲜有涉及降解机制。有研究者[32]采用DNA-SIP、16S rRNA测序和基因组学技术,首次尝试对产甲烷条件下的PAHs微生物降解进行深入研究,但并未识别出具体降解机制。
3.5 已有研究的不足之处半个多世纪以来,研究者已从不同角度对PAHs的厌氧微生物降解进行了探究,取得了长足进展。但根据文献计量和综述的综合分析,目前该领域仍存在许多理论空白。首先,实际环境中PAHs污染常以复合形式存在。低环PAHs分子结构简单,相对易于被微生物直接作为碳源和能源进行呼吸代谢,因此得到了较广泛的研究。例如,萘结构简单,常被作为“模式PAH”,综合已有的报道可知,厌氧条件下萘主要通过甲基化或羧化途径活化,之后在脱氢酶、水合酶等一系列酶的催化下逐步断键、开环并最终转化为CO2。而高环PAHs分子结构复杂、性质稳定,难以被微生物直接利用,因此相关报道较少,导致其厌氧微生物降解机制仍不明确,目前可用于高环PAHs污染修复的微生物种类也十分有限。
其次,虽然研究者已分离出多种PAHs降解菌,但它们发挥降解功能通常依赖于菌群协作。由此可以预见,在受PAHs污染的实际厌氧环境中,微生物种类繁多、环境条件复杂多变,发挥降解功能的可能不是某一种或几种微生物,而是由PAHs降解菌和电子受体还原菌构成的菌群。前者降解PAHs产生的电子经过一系列中间反应最终传递给后者,二者相互依赖并共同发挥功能,在介导PAHs厌氧降解过程中,同步发生不同的还原反应。但截至目前,该领域围绕菌群协作的研究尚较缺乏。特别是产甲烷条件下,降解过程关联温室效应,更应受到重视。再者,关于降解机制的探讨大多仅通过检测降解产物来推断降解途径,而未深入挖掘内在的生物学机制,包括在微生物细胞中的转运过程、关键酶和功能基因、与微生物体内蛋白及小分子代谢产物的互作关系等。
此外,最重要的是,前已述及,已有研究多在纯培养物或水体等环境介质中进行,关注土壤体系的相对偏少,而土壤是环境中PAHs汇集和积累的重要场所,且许多土壤会经历甚至长期处于厌氧状态,这凸显了深入研究土壤PAHs厌氧微生物降解的必要性。然而,土壤是一个具有高度复杂性和多变性的动态体系,基于纯培养物和水体等简单体系研究所得的理论很大程度上并不适用于揭示土壤中发生的相关过程与机制。土壤微生物种类繁多,群落中各物种存在紧密互作,而现有研究大多仅关注个别发挥关键功能的微生物,忽略了微生物之间的网络关联,因此关于受PAHs污染的厌氧土壤中微生物如何“各司其职”、协同降解PAHs,如何进行电子传递,以及污染胁迫下微生物群落的响应和适应机制等,目前的认知仍十分有限。主要原因之一是难以在实验室中复刻自然土壤中的复杂微生物群落。宏基因组技术是研究复杂微生物群落的强大工具,不仅可用于揭示群落中大量微生物的遗传和功能特性,甚至可利用其设计培养基以分离培养原本未培养的微生物[33]。在芳香烃降解相关的报道中,有研究者利用该技术预测未培养微生物的污染物代谢能力[34-35],探讨自然削减过程中不同微生物类群所发挥的功能和互作关系[36],或揭示污染物与其他营养物质的共代谢机制[37]等,上述研究均证实了宏基因组技术的广阔前景。但文献计量和综述结果均表明,目前该技术在土壤PAHs厌氧微生物降解的研究中少有应用。此外,CSIA、DNA-SIP等技术也并未得到广泛应用。因此,该领域仍存在一定的发展空间。
4 结论以
土壤作为环境中PAHs汇集和积累的主要场所,应该受到重点关注,而实际情况并非如此,迫切需要研究跟进。未来的研究可将新兴技术与传统方法相结合,侧重从以下几个方面展开研究工作:(1)利用DNA-SIP技术发掘在厌氧条件下能够直接降解高环PAHs的新型菌株,并结合稳定同位素示踪技术研究具体降解途径;(2)筛选适应能力强、降解效率高的微生物,并研究其在不同厌氧土壤环境中的存活情况和适应能力,进而发掘能够用于厌氧土壤中复合PAHs污染原位修复的微生物,并探究提高修复效率的措施;(3)将宏基因组与蛋白组学、转录组学和代谢组学等多种组学技术相结合,研究与PAHs厌氧降解相关的基因、蛋白和小分子代谢物,进而探究降解菌同化PAHs的生物学机制;(4)利用基因组学技术,寻找能够指示PAHs厌氧降解菌的基因标志物;(5)利用稳定同位素示踪、DNA-SIP和组学等技术及微生物网络分析,研究实际厌氧土壤中微生物协同降解PAHs的机制,并结合电化学技术阐明PAHs厌氧降解与电子受体还原过程之间的耦合机制;(6)对多种典型降解菌进行降解产物鉴定,结合CSIA技术,研究不同还原条件下PAHs厌氧微生物降解途径及同位素分馏效应,明确降解途径是否与电子受体类型直接相关,并探究同位素富集系数能否用于判断PAHs厌氧降解途径。此外,最重要的是,无论从何种角度开展研究,最终均应回归土壤,将所得出的理论经验在土壤中进行验证,确保其适用于揭示土壤PAHs厌氧微生物降解相关过程与机制。只有这样才能准确认知厌氧土壤中PAHs的污染自净功能,完善发展厌氧土壤中PAHs污染的强化修复方法原理。
| [1] |
Davie-Martin C L, Stratton K G, Teeguarden J G, et al. Implications of bioremediation of polycyclic aromatic hydrocarbon-contaminated soils for human health and cancer risk[J]. Environmental Science & Technology, 2017, 51(17): 9458-9468.
(  0) 0) |
| [2] |
Williams P A, Catterall F A, Murray K. Metabolism of naphthalene, 2-methylnaphthalene, salicylate, and benzoate by Pseudomonas PG regulation of tangential pathways[J]. Journal of Bacteriology, 1975, 124(2): 679-685. DOI:10.1128/jb.124.2.679-685.1975
(  0) 0) |
| [3] |
Zhang P, Chen Y G. Polycyclic Aromatic Hydrocarbons contamination in surface soil of China: A review[J]. Science of the Total Environment, 2017, 605: 1011-1020.
(  0) 0) |
| [4] |
Han X, Wang F, Zhang D, et al. Nitrate-assisted biodegradation of Polycyclic Aromatic Hydrocarbons(PAHs)in the water-level-fluctuation zone of the three Gorges Reservoir, China: Insights from in situ microbial interaction analyses and a microcosmic experiment[J]. Environmental Pollution, 2021, 268: 115693. DOI:10.1016/j.envpol.2020.115693
(  0) 0) |
| [5] |
Yan K, Lou J, Wang H Z, et al. Research of contaminated sites based on knowledge graph analysis and its development trend (In Chinese)[J]. Acta Pedologica Sinica, 2020. DOI:10.11766/trxb202002280030 [严康, 楼骏, 汪海珍, 等. 基于知识图谱分析的污染场地研究现状与发展趋势[J]. 土壤学报, 2020.]
(  0) 0) |
| [6] |
He Y, Huang X W, Cheng Z Y, et al. Proposals for research on protection and functional improvement of soil environment in soybean producing area in face of the new situation (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 269-280. [何艳, 黄晓伟, 程中一, 等. 新形势下大豆产地土壤环境保护与功能提升的研发建议[J]. 土壤学报, 2021, 58(2): 269-280.]
(  0) 0) |
| [7] |
Coates J D, Woodward J, Allen J, et al. Anaerobic degradation of polycyclic aromatic hydrocarbons and alkanes in petroleum-contaminated marine harbor sediments[J]. Applied and Environmental Microbiology, 1997, 63(9): 3589-3593. DOI:10.1128/aem.63.9.3589-3593.1997
(  0) 0) |
| [8] |
Zhang X, Young L Y. Carboxylation as an initial reaction in the anaerobic metabolism of naphthalene and phenanthrene by sulfidogenic consortia[J]. Applied and Environmental Microbiology, 1997, 63(12): 4759-4764. DOI:10.1128/aem.63.12.4759-4764.1997
(  0) 0) |
| [9] |
Rockne K J, Chee-Sanford J C, Sanford R A, et al. Anaerobic naphthalene degradation by microbial pure cultures under nitrate-reducing conditions[J]. Applied and Environmental Microbiology, 2000, 66(4): 1595-1601. DOI:10.1128/AEM.66.4.1595-1601.2000
(  0) 0) |
| [10] |
Meckenstock R U, Annweiler E, Michaelis W, et al. Anaerobic naphthalene degradation by a sulfate-reducing enrichment culture[J]. Applied and Environmental Microbiology, 2000, 66(7): 2743-2747. DOI:10.1128/AEM.66.7.2743-2747.2000
(  0) 0) |
| [11] |
Haritash A K, Kaushik C P. Biodegradation aspects of Polycyclic Aromatic Hydrocarbons(PAHs): A review[J]. Journal of Hazardous Materials, 2009, 169(1—3): 1-15.
(  0) 0) |
| [12] |
Meckenstock R U, Boll M, Mouttaki H, et al. Anaerobic degradation of benzene and polycyclic aromatic hydrocarbons[J]. Journal of Molecular Microbiology and Biotechnology, 2016, 26(1/2/3): 92-118.
(  0) 0) |
| [13] |
Yang X N, Li E Z, Liu F F, et al. Interactions of PAH-degradation and nitrate-/sulfate-reducing assemblages in anaerobic sediment microbial community[J]. Journal of Hazardous Materials, 2020, 388: 122068. DOI:10.1016/j.jhazmat.2020.122068
(  0) 0) |
| [14] |
Nzila A. Biodegradation of high-molecular-weight polycyclic aromatic hydrocarbons under anaerobic conditions: Overview of studies, proposed pathways and future perspectives[J]. Environmental Pollution, 2018, 239: 788-802. DOI:10.1016/j.envpol.2018.04.074
(  0) 0) |
| [15] |
R W R, Brady N C, Brady N C. The nature and properties of soils . Fifteenth[M]. Columbus: Pearson, 2017.
(  0) 0) |
| [16] |
Zhang Z T, Sun J, Guo H J, et al. Anaerobic biodegradation of phenanthrene by a newly isolated nitrate-dependent Achromobacter denitrificans strain PheN1 and exploration of the biotransformation processes by metabolite and genome analyses[J]. Environmental Microbiology, 2021, 23(2): 908-923. DOI:10.1111/1462-2920.15201
(  0) 0) |
| [17] |
Zhang Z T, Guo H J, Sun J, et al. Investigation of anaerobic phenanthrene biodegradation by a highly enriched co-culture, PheN9, with nitrate as an electron acceptor[J]. Journal of Hazardous Materials, 2020, 383: 121191. DOI:10.1016/j.jhazmat.2019.121191
(  0) 0) |
| [18] |
Qin W, Zhu Y, Fan F, et al. Biodegradation of benzo[a]pyrene by Microbacterium sp strain under denitrification: Degradation pathway and effects of limiting electron acceptors or carbon source[J]. Biochemical Engineering Journal, 2017, 121: 131-138. DOI:10.1016/j.bej.2017.02.001
(  0) 0) |
| [19] |
Zhang D J, Han X K, Zhou S B, et al. Nitric oxide-dependent biodegradation of phenanthrene and fluoranthene: The co-occurrence of anaerobic and intra-aerobic pathways[J]. Science of the Total Environment, 2021, 760: 144032. DOI:10.1016/j.scitotenv.2020.144032
(  0) 0) |
| [20] |
Shi J X, Zhang B G, Cheng Y T, et al. Microbial vanadate reduction coupled to co-metabolic phenanthrene biodegradation in groundwater[J]. Water Research, 2020, 186: 116354. DOI:10.1016/j.watres.2020.116354
(  0) 0) |
| [21] |
Yan Z, Zhang Y, Wu H, et al. Isolation and characterization of a bacterial strain Hydrogenophaga sp PYR1 for anaerobic pyrene and benzo[a]pyrene biodegradation[J]. RSC Advances, 2017, 7(74): 46690-46698. DOI:10.1039/C7RA09274A
(  0) 0) |
| [22] |
Marozava S, Mouttaki H, Müller H, et al. Anaerobic degradation of 1-methylnaphthalene by a member of the Thermoanaerobacteraceae contained in an iron-reducing enrichment culture[J]. Biodegradation, 2018, 29(1): 23-39. DOI:10.1007/s10532-017-9811-z
(  0) 0) |
| [23] |
Kleemann R, Meckenstock R U. Anaerobic naphthalene degradation by Gram-positive, iron-reducing bacteria[J]. FEMS Microbiology Ecology, 2011, 78(3): 488-496. DOI:10.1111/j.1574-6941.2011.01193.x
(  0) 0) |
| [24] |
Zhang Z T, Guo H J, Sun J, et al. Exploration of the biotransformation processes in the biodegradation of phenanthrene by a facultative anaerobe, strain PheF2, with Fe(Ⅲ)or O2 as an electron acceptor[J]. Science of the Total Environment, 2021, 750: 142245. DOI:10.1016/j.scitotenv.2020.142245
(  0) 0) |
| [25] |
Musat F, Galushko A, Jacob J, et al. Anaerobic degradation of naphthalene and 2-methylnaphthalene by strains of marine sulfate-reducing bacteria[J]. Environmental Microbiology, 2009, 11(1): 209-219. DOI:10.1111/j.1462-2920.2008.01756.x
(  0) 0) |
| [26] |
Zhang Z, Sun J, Guo H, et al. Investigation of anaerobic biodegradation of phenanthrene by a sulfate-dependent Geobacter sulfurreducens strain PheS2[J]. Journal of Hazardous Materials, 2021, 409: 124522. DOI:10.1016/j.jhazmat.2020.124522
(  0) 0) |
| [27] |
Safinowski M, Meckenstock R U. Methylation is the initial reaction in anaerobic naphthalene degradation by a sulfate-reducing enrichment culture[J]. Environmental Microbiology, 2006, 8(2): 347-352. DOI:10.1111/j.1462-2920.2005.00900.x
(  0) 0) |
| [28] |
Weyrauch P, Heker I, Zaytsev A V, et al. The 5, 6, 7, 8-tetrahydro-2-naphthoyl-Coenzyme A reductase reaction in the anaerobic degradation of naphthalene and identification of downstream metabolites[J]. Applied and Environmental Microbiology, 2020, 86(15): e00996-20.
(  0) 0) |
| [29] |
Weyrauch P, Zaytsev A V, Stephan S, et al. Conversion of Cis-2-carboxycyclohexylacetyl-CoA in the downstream pathway of anaerobic naphthalene degradation[J]. Environmental Microbiology, 2017, 19(7): 2819-2830. DOI:10.1111/1462-2920.13806
(  0) 0) |
| [30] |
Kraiselburd I, Brüls T, Heilmann G, et al. Metabolic reconstruction of the genome of candidate Desulfatiglans TRIP1 and identification of key candidate enzymes for anaerobic phenanthrene degradation[J]. Environmental Microbiology, 2019, 21(4): 1267-1286. DOI:10.1111/1462-2920.14527
(  0) 0) |
| [31] |
Qian Y, Xu M, Deng T, et al. Synergistic interactions of Desulfovibrio and Petrimonas for sulfate-reduction coupling polycyclic aromatic hydrocarbon degradation[J]. Journal of Hazardous Materials, 2021, 407: 124385. DOI:10.1016/j.jhazmat.2020.124385
(  0) 0) |
| [32] |
Toth C R A, Berdugo-Clavijo C, O'farrell C M, et al. Stable isotope and metagenomic profiling of a methanogenic naphthalene-degrading enrichment culture[J]. Microorganisms, 2018, 6(3): 65. DOI:10.3390/microorganisms6030065
(  0) 0) |
| [33] |
Kwak M J, Kong H G, Choi K, et al. Rhizoshere microbiome structure alters to enable wilt resistance in tomato[J]. Nature Biotechnology, 2018, 36(11): 1100-1109. DOI:10.1038/nbt.4232
(  0) 0) |
| [34] |
Liu Y F, Qi Z Z, Shou L B, et al. Anaerobic hydrocarbon degradation in candidate Phylum 'Atribacteria'(JS1)inferred from genomics[J]. The ISME Journal, 2019, 13(9): 2377-2390. DOI:10.1038/s41396-019-0448-2
(  0) 0) |
| [35] |
Dong X Y, Greening C, Rattray J E, et al. Metabolic potential of uncultured bacteria and archaea associated with petroleum seepage in deep-sea sediments[J]. Nature Communications, 2019, 10(1): 1816. DOI:10.1038/s41467-019-09747-0
(  0) 0) |
| [36] |
Hu P, Tom L, Singh A, et al. Genome-resolved metagenomic analysis reveals roles for candidate phyla and other microbial community members in biogeochemical transformations in oil reservoirs[J]. MBio, 2016, 7(1): e01669-15.
(  0) 0) |
| [37] |
Sun Y, Liu L, Zeng J, et al. Enhanced cometabolism of benzo[a]anthracene by the lignin monomer vanillate is related to structural and functional responses of the soil microbiome[J]. Soil Biology & Biochemistry, 2020, 149: 107908.
(  0) 0) |
 2022, Vol. 59
2022, Vol. 59

