2. 西南大学长江经济带农业绿色发展研究中心, 重庆 400715;
3. 中国农业大学资源与环境学院, 植物-土壤相互作用教育部重点实验室, 北京 100193
2. Interdisciplinary Research Center for Agriculture Green Development in Yangtze River Basin, Southwest University, Chongqing 400716, China;
3. College of Resources and Environmental Sciences, Key Laboratory of Plant-Soil Interactions, Ministry of Education, China Agricultural University, Beijing 100193, China
土壤微生物是陆地生态系统植物多样性和生产力的重要驱动者,参与养分循环以及植物对养分的获取[1],是维持陆地生态系统地上-地下相互作用的纽带[2],也是土壤生产力的重要保证者[3-4]。土壤微生物的遗留(legacy)效应为长期受某一种特定因素的影响形成特定的微生物特性,当这一因素的影响终止后,其对微生物所产生的作用影响后续功能的发挥[5]。生物和非生物因素均会对土壤微生物产生影响[6]。生物因素如植物物种的多样性影响微生物的遗留效应。Schmid等[7]将连续11年单一种植或混合种植(8种不同植物)的根际土壤微生物分别接种至8种不同的植物根际,其中有7种植物在接种混合种植土壤中的微生物时,细菌的多样性增加,这表明细菌的优势类群及其数量受宿主植物种类的影响,植物物种多样性影响微生物的遗留效应。非生物因素如重金属、水份等也会对微生物产生遗留效应。例如,在长期高铜条件下驯化的Suillus luteus对高浓度铜产生遗留效应。将Suillus luteus接种于受铜污染的土壤中,增强了松树的耐铜性,促进松树的生长[8]。Meisner等[9]研究了干旱胁迫条件对土壤真菌和原核生物群落产生的遗留效应,发现干燥和再润湿会降低微生物群落的丰富度,但不会降低均匀度。Hinojosa等[10]研究了干旱对微生物群落结构和土壤功能的遗留效应,发现遗留效应对有效磷和酶活性产生显著影响,并且效应至少会持续2年。
在农业生产中,施肥作为重要的一种管理措施,显著影响微生物的群落结构和功能,微生物的遗留效应会影响后续植物的生长和养分吸收[11-12]。研究发现,在有效磷含量较低的土壤中筛选的解磷微生物菌株,能够提高有机磷的活化水平[13]。与正常施肥相比,长期缺氮或缺磷土壤中的AM真菌在氮、低磷胁迫时,AM真菌自身生物量较高,但对植物生长产生负效应[14]。Martín-Robles等[15]研究了不同磷水平驯化下27种植物及其野生型的菌根效应,结果发现,有效磷水平影响AM真菌与宿主植物之间的共生效应。整体而言,野生型品种与AM真菌形成有益的共生效应,不受供磷水平的影响,驯化品种的菌根效应与驯化时的磷供应水平有关。
施磷是缺磷土壤作物增产的常见措施。长期施用磷肥会导致磷在土壤中大量积累,而累积磷是潜在的环境污染源[16]。理解微生物对施肥的遗留效应对挖掘土壤微生物的潜力,提高资源利用效率具有重要意义。长期施磷对土壤微生物会产生怎样的驯化效果?微生物的遗留效应如何影响后续植物的生长和土壤过程? 试验以华北平原石灰性土壤长期不同供磷水平下的微生物为研究对象,通过盆栽接种微生物试验,探究微生物的遗留效应。
1 材料与方法 1.1 研究区概况与试验材料试验地位于中国农业大学上庄长期定位试验站(39°59'N,116°17'E),当地气候类型属于温带季风气候,年平均气温为13.2℃,降水量为213~840 mm。土壤类型为钙质冲积土,粉砂质壤土。土壤的pH为8.3(1︰5,土壤:水悬浮液),有机碳12 g·kg–1、全氮0.63 g·kg–1、有效磷(Olsen P)3 mg·kg–1、无机氮(NH4+-N和NO3–-N)15 mg·kg–1、速效钾(NH4OAc-K)110 mg·kg–1。试验为玉米连作体系,开始于2007年,每年施用过磷酸钙,施肥强度为P2O5 0、25、50、75、100、150、300 kg·hm–2。氮肥和钾肥作为基肥处理,氮肥(尿素)用量为N 225 kg·hm–2,钾肥(K2SO4)的用量为K 66 kg·hm–2。在播种前、拔节和吐丝期分别施用N 75 kg·hm–2的尿素。
1.2 试验设计盆栽试验在中国农业大学资源环境学院温室进行。接种菌剂取自长期定位试验中施肥量为P2O5 0、75和300 kg·hm2的3个处理,取样深度为0~20 cm。采集时按照“S”形每个小区随机抽取10个点,并将10个点的土样混合,每个磷水平菌剂采自4个小区,采集后将4份充分混合。基质土样采集于实验地周围空地,土壤风干后过2 mm筛,在北京辐射研究中心将基质土壤利用γ-射线(强度 > 25 Gray)灭菌72 h待用。同时,利用平板培养法检测土壤中细菌、真菌的数量,确定灭菌彻底。基质土的有效磷浓度为3.4 mg kg–1,设置不施磷(No P)和P 30 mg·kg–1(+ P)2个磷供应水平,磷肥供应形态为KH2PO4,氮肥和钾肥的施用量分别为N 100 mg·kg–1的NH4NO3和K 100 mg·kg–1的K2SO4。塑料盆内装1 kg的土,与N、P和K肥料完全混合。由100 g菌剂和900 g基质土均匀混合。100 g菌剂分别来自于大田三个施磷水平处理(分别施用P2O5 0、75和300 kg·hm–2)的土壤。接种菌剂处理包括:(1)原位菌剂,大田原位采集的三个供磷水平的土壤作为原位菌剂;(2)灭菌菌剂处理,即将大田原位采集土壤作为原位菌剂进行γ-射线灭菌后的土壤。
种植作物包括玉米郑单958(Zea mays L. cv. Zhengdan 958)和白三叶草(Trifolium repens L.),每个处理3次重复,共36盆。玉米和三叶草种子首先进行表面消毒(10% H2O2消毒30 min),后用蒸馏水冲洗,再用饱和CaSO4浸泡8 h,遮光培养24 h。将发芽的玉米种子种植于盆中,出苗后玉米每盆保留2株,三叶草每盆保留50株。用去离子水每3 d称重浇水,土壤含水量保持在田间最大持水量的60%。
玉米和三叶草植株分别在生长59 d、69 d时收获,将植株的地上部和根部分开收获。地上部首先在105℃下杀青30 min,然后在75℃条件下烘干72 h,称重。根系样品用蒸馏水清洗干净。
1.3 测定项目与方法采用H2SO4和H2O2消煮植物样品后,钼磷酸盐比色法测定植株磷含量[17]。土壤Olsen P用0.5 mmol·L–1 NaHCO3提取后,用比色法进行测定。碱性磷酸酶(Alkaline phosphatase)采用Tabatabai[18]的荧光微型板酶检测技术[19]。该技术的原理是不同酶的标准底物被水解后,产生4-甲基伞形酮(4- methylumbelliferyl),通过测定其荧光值的强度来表征土壤胞外酶的活性。其他的酶活性指标包括:α-葡糖苷酶,β-木糖苷酶,几丁质酶和过氧化物酶[20],测定的胞外酶α-葡糖苷酶,β-木糖苷酶,几丁质酶和过氧化物酶对应的底物分别为:4-MUB-α-D- glucosid、4-MUB-β-D-xyloside、Chitin和L-DOPA(MUB为4-甲基伞形酮,MUB = 4-methylumbelliferyl,DOPA为L-3,4-二羟基苯丙氨酸DOPA= L-3,4-dihydroxyphenylalanine)。使用多功能酶标仪(Scientific Fluuoroskan Ascent FL,Thermo)在激发波长365 nm、发射波长450 nm的条件下测定荧光。采用McGonigle等[21]描述的方法将进行根系菌根侵染率的测定。
1.4 统计分析统计分析使用统计软件IBM SPSS Statistics(22.0.0.0版),采用双因素分析方法,多重比较采用Duncan检验,在0.05水平上进行分析,试验结果以平均值±标准差(SE)表示。
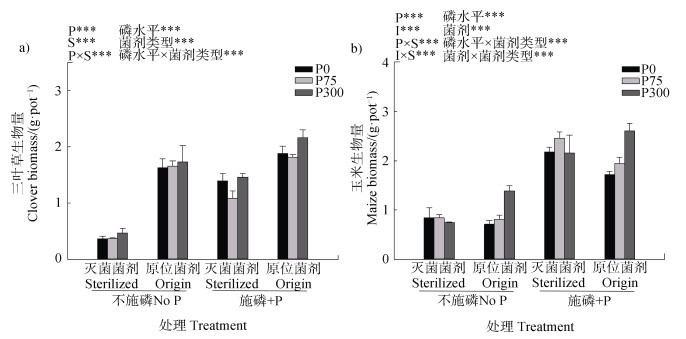
2 结果 2.1 植物地上部生物量和养分含量长期不同供磷水平驯化的土壤微生物对玉米和三叶草地上部生物量和磷吸收量的影响不同(图 1,图 2)。与对照(灭菌处理)相比,在2个基质磷水平下,接种原位菌剂(P0、P75和P300)处理三叶草地上部生物量和磷吸收量显著提高,但菌剂之间差异不显著(图 1a,图 2a)。在No P条件下,玉米地上部生物量接种原位菌剂相比于接种灭菌处理对玉米地上部生物量无显著影响,玉米的磷吸收量显著提高;在+P条件下,接种降低了玉米的地上部生物量,对玉米磷吸收量无显著影响,且接种P300处理的玉米生物量和磷吸收量均显著高于P0和P75处理(图 1b,图 2b)。三叶草和玉米地上部的微量元素(铁、锰、铜和锌)的含量在接种菌剂和灭菌处理间差异显著,但菌剂显著影响植株微量元素含量。其中,三叶草地上部铁和锰含量、以及玉米锌和锰含量接种在P75处理高于P0和P300处理,(图 3a-图 3f)。基质供磷水平显著影响三叶草和玉米植株锌含量,表现为No P处理显著高于+P处理(图 3g,图 3h)。
|
注:P0、P75和P300分别为P2O5 0、75和300 kg·hm–2,No P表示基质供磷水平为0 mg kg–1,+P表示基质供磷水平为30 mg kg–1。P,S和I分别代表磷水平(No P/+P),菌剂类型(灭菌菌剂/原位菌剂)和菌剂(P0/P75/P300)。因素及因素之间交互作用的显著性标在图的正上方,其中“*”代表P < 0.05,“**”代表P < 0.01,“***”代表P < 0.001。下同。 Note: P0, P75 and P300 represented indigenous microbial inocula from P2O5 0, 75 and 300 kg·hm–2 fertilization trials. No P represented the substrate P supplied rate: 0 mg·kg–1, +P represented the substrate P supplied rate: 30 mg·kg–1. P, S and I represented the phosphorus supplied rate(No P/+P), inoculum type(Sterilized/Origin)and inocula(P0/P75/P300). The significance of factors and their interactions was marked on the top of the figure. "*" represented P < 0.05, "**" represented P < 0.01, "***" represented P < 0.001. The same below. 图 1 不同供磷水平菌剂对三叶草和玉米地上部生物量的影响 Fig. 1 Shoot biomass of clover and maize as affected by soil inocula originated from different P fertilization treatments |
|
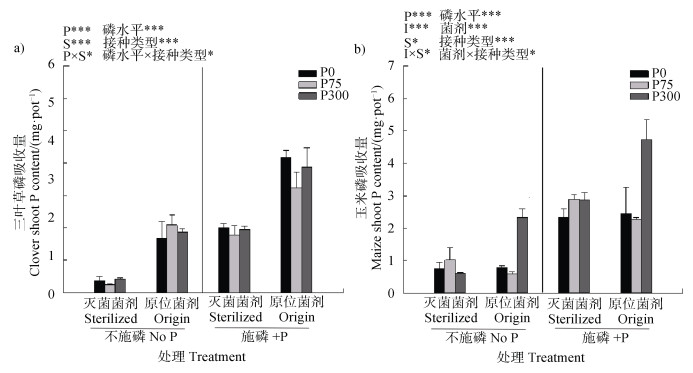
图 2 不同供磷水平菌剂对三叶草和玉米地上部磷吸收量的影响 Fig. 2 Shoot P content of clover and maize as affected by soil inocula originated from different P fertilization treatments |
|
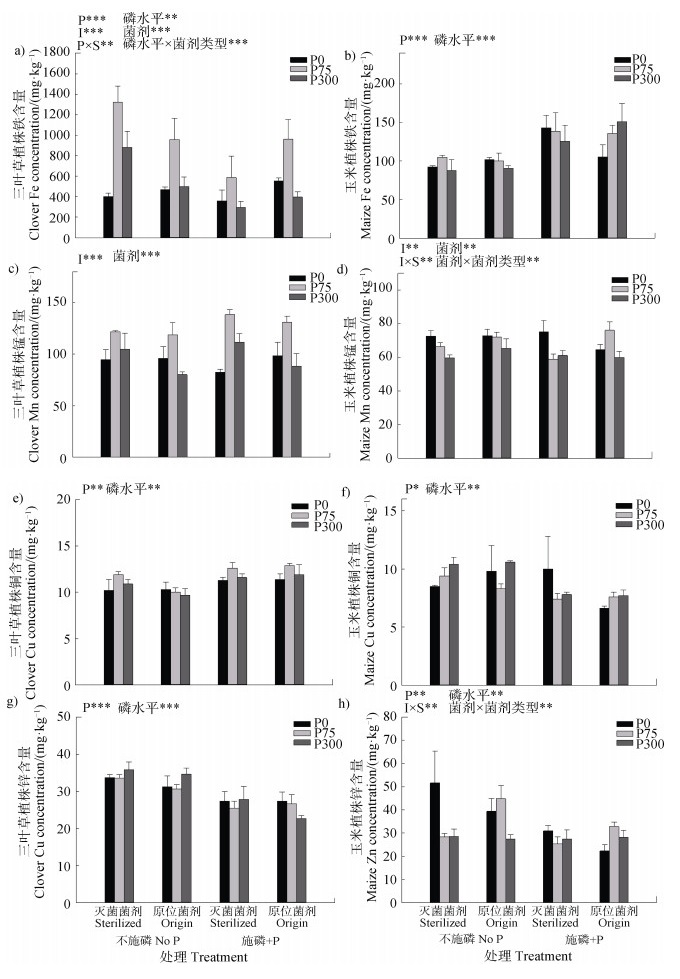
图 3 不同供磷水平菌剂对三叶草和玉米植株铁(a,b)、锰(c,d)、铜(e,f)和锌(g,h)吸收量的影响 Fig. 3 Fe(a, b), Mn(c, d), Cu(e, f)and Zn(g, h)concentrations of clover and maize plants as affected by soil inocula originated from different P fertilization treatments |
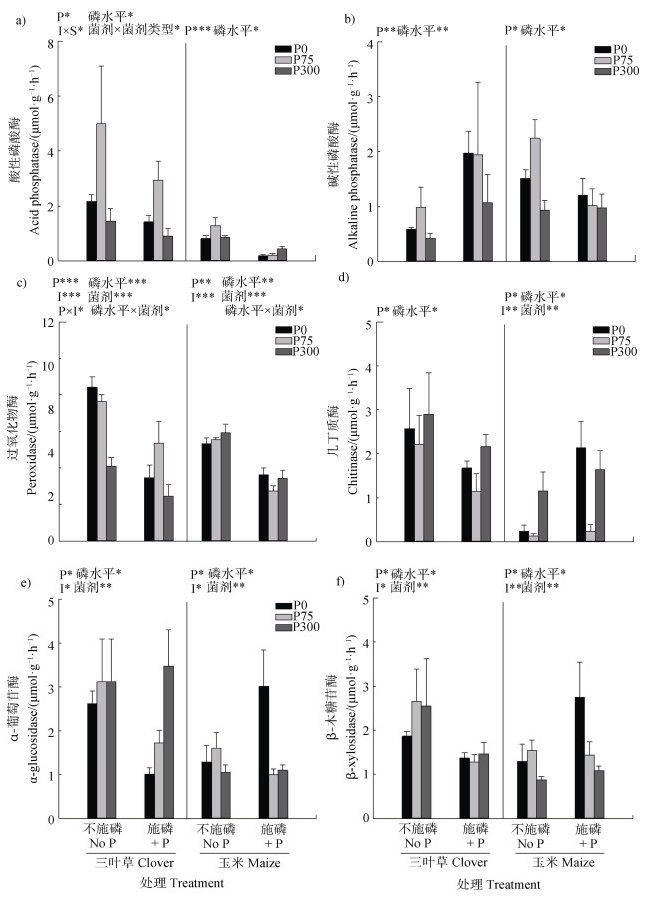
植物种类、基质磷水平和菌剂均影响接种原位菌剂处理土壤酶活性(图 4)。三叶草土壤中酸性磷酸酶、过氧化物酶、几丁质酶和β-葡糖苷酶的活性在No P处理显著高于+P处理,碱性磷酸酶活性则相反,α-葡糖苷酶活性在2个供磷水平下无显著差异(图 4a-图 4f)。玉米土壤中酸性磷酸酶、碱性磷酸酶和过氧化物酶的活性在No P处理高于+P处理,几丁质酶、α-葡糖苷酶和β-葡糖苷酶的活性在2个基质供磷水平下差异不显著。在No P土壤中,三叶草土壤中过氧化酶活性由高到低依次为接种P0菌剂、接种P75菌剂、接种P300菌剂(图 4c)。在+P土壤中,三叶草酸性磷酸酶的活性和过氧化物酶活性在接种P75时显著高于接种P0和P300菌剂(图 4a,图 4c)。在No P土壤中,玉米土壤中酸性磷酸酶活性在接种P75菌剂最高,过氧化物酶和几丁质酶活性在P300菌剂最高(图 4a,图 4c,图 4d),接种其他2种菌剂相应的酶活性显著低于P300菌剂。在+P土壤中,玉米α-葡糖苷酶和β-葡糖苷酶活性在接种P0菌剂最高,接种P75和P300菌剂显著低于P0菌剂(图 4e,图 4f)。
|
图 4 不同供磷水平菌剂对三叶草和玉米土壤酶活性的影响 Fig. 4 Soil enzyme activities of clover and maize as affected by soil inocula. Acid phosphatase(a), alkaline phosphatase(b), peroxidase(c), chitinase(d), α-glucosidase(e)and β-xylosidase(f)originated from different P fertilization treatments |
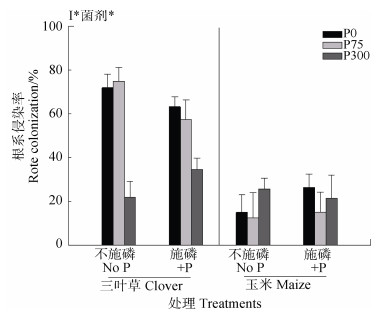
植物种类、基质磷水平和菌剂均影响根系的菌根侵染率(图 5)。三叶草根系的菌根侵染率在No P处理显著高于+P处理;而玉米根系菌根侵染率在2个基质磷供应水平间显著不差异(图 5)。接种P300菌剂显著降低了2种基质土壤中三叶草根系的菌根侵染率,而玉米根系的菌根侵染率接种菌剂的影响不显著(图 5)。
|
图 5 不同供磷水平的原位菌剂对三叶草和玉米根系侵染率的影响 Fig. 5 Root colonization of clover and maize plants as affected by soil inocula originated from different P fertilization treatments |
在农田生态系统中,减少磷肥用量、提高作物产量并维持环境可持续性是磷肥管理的目标。微生物组技术在促进作物生长、提高作物抗性中的作用越来越引起人们的关注。本研究结果表明,磷肥施用产生的土壤微生物遗留效应在玉米和三叶草植间存在差异:菌剂和基质供磷水平影响玉米生长,No P时接种P0和P75菌剂显著促进玉米生长,而+P处理时菌剂则表现为抑制作用,接种P300在2个基质磷水平均促进玉米生长(图 1,图 2)。与本试验类似,王超[22]发现盆栽试验条件下,将大田原位土壤和原位土壤灭菌后种植玉米,在高磷条件下,玉米生长在原位土壤中被抑制,而在低磷条件下,接种促进了玉米生长。转录组的结果进一步发现,充足供磷和供磷不足时,土壤病原微生物和有益微生物可能起不同的作用[22]。在本研究中,在2个基质磷水平供应时菌剂对显著促进三叶草的生长。可能是菌剂中的土壤微生物来源于连作玉米体系,当种植新的宿主作物时,土壤病原菌的累积效应减弱,轮作可清除连作土壤病原菌的累积[23]。
本试验中植物种类、基质供磷水平、菌剂在2种植物间差异显著,表明土壤微生物的遗留效应受多种因素的影响,具有一定的选择性(图 1,图 2)。有研究发现,宿主植物、环境条件以及微生物的群落结构和数量均显著影响植物-土壤-微生物的相互作用[24]。Griffiths等[25]通过将砂壤和黏土灭菌,将菌剂悬液交换接种于以上的2种基质土壤中,发现土壤类型是决定细菌群落结构的主要因素,而接种菌剂本身的特性次之。表明长期不同供磷水平驯化的土壤微生物的功能可能受其他多种因素的影响。
基质供磷水平显著影响植株锌含量,三叶草和玉米在No P处理植株锌含量显著高于+P处理(图 4g,图 4h)。这与之前的研究结果一致,供磷水平与植株锌含量存在拮抗关系,施用磷肥增加锌在植株根部的积累,同时降低了植株地上部的锌供应[26-27]。整体而言接种原位菌剂对玉米和三叶草微量元素的含量与灭菌对照相比无显著影响(图 4),接种菌剂P75相比于P0和P300显著提高了三叶草中铁和锰含量和玉米锌和锰含量(图 4a-图 4f),表明不同菌剂显著影响植株微量元素含量。豆科植物根际酸化和有机酸的分泌可以提高土壤中微量元素的活性,促进植物对于铁和锰等微量元素的吸收[28]。玉米对微量元素的吸收受菌剂显著影响,接种P300菌剂的玉米植株中铁、锰、铜和锌的吸收量显著高于接种P0和P75菌剂的玉米植株(图 3),表明高磷菌剂的微生物显著促进了玉米对微量元素的吸收。
3.2 长期不同供磷水平驯化的土壤微生物对土壤酶活性的影响土壤酶活性是土壤质量的重要指标,胞外酶可以调节土壤中养分的转化与利用。酸性磷酸酶主要由根系分泌,而碱性磷酸酶主要由微生物分泌[29-31],之前的研究发现,施用肥料显著降低磷酸酶的活性[32-33]。本试验中在2个基质磷水平下,+P处理降低了玉米和三叶草中酸性磷酸酶的活性(图 4a),表明土壤中磷相对充足的供应,植物分泌的酸性磷酸酶降低。土壤中过氧化物酶参与土壤呼吸过程的物质代谢,可表示土壤呼吸过程强度,是表征土壤微生物活力的重要指标之一。过氧化物酶在植物的抗性方面起着至关重要的作用[34]。施用氮、磷和钾肥可以降低过氧化物酶的活性[35]。本研究也发现+P处理接种菌剂的过氧化物酶活性相比于低磷水平显著降低(图 5c),菌剂对过氧化物酶活性的影响存在显著性差异,过氧化物酶浓度在接种P0菌剂的2个供磷水平条件下,均显著高于接种P75菌剂,同时,接种P75菌剂显著高于接种P300菌剂(图 5c),表明长期低磷胁迫过氧化物酶活性较强,而高磷胁迫过氧化物酶活性较弱;微生物诱导过氧化物酶活性调控植物体内的抗性响应。之前的研究发现几丁质酶可水解很多种病原菌细胞壁中的几丁质[36],是一种和抗性相关的酶,而玉米在+P条件下接种原位菌剂生长受到抑制的现象可能与微生物在这一条件下病原菌起主要作用有关,诱导了根系胁迫防御,从而抑制了植物的生长。
3.3 长期不同供磷水平驯化的土壤微生物接种后的菌根特征三叶草的根系侵染率接种P0显著低于P300,说明长期磷胁迫条件下土壤中AM真菌的菌根依赖性更强,但接种菌剂之间玉米根系侵染率无显著差异,可能是因为采用的玉米品种“郑单958”,通常在有效磷含量较高的条件下育种,而养分的供应条件对玉米品种亦会产生驯化作用,导致玉米的菌根依赖性降低。Qin等 [37]将长期施用不同水平有机肥(干牛粪)(0、6和12 t·hm–2)的土壤AM真菌接种于不同基质供磷水平中(0、20和250 mg·kg–1),菌根的生长效应和磷吸收效应均会随着基质供磷水平的提高由正效应转化为负效应,与菌剂来源的影响关系较弱,说明基质供磷水平显著影响植物的菌根特征,而长期不同中水平有机肥的驯化的土壤微生物对植物菌根特征的影响较弱。Martín-Robles等[15]测定了14种植物在不同有效磷的条件下驯化结果发现,有效磷影响AM真菌与宿主植物之间的共生效应,野生型品种在不同的有效磷条件下均与AM真菌形成有益的共生效应,而驯化品种只有在有效磷胁迫条件下才能与AM真菌形成有效的共生效应,长期供磷水平的驯化改变了AM真菌与宿主植物之间对资源分配的调节作用。
4 结论长期不同供磷水平驯化的土壤微生物对植物的生长,磷吸收量存在显著差异,接种原位菌剂显著提高了三叶草地上部生物量和磷吸收量,同时,对玉米地上部生物量在低磷和高磷基质土壤中分别是无显著影响和显著降低的作用;原位菌剂对三叶草生长和磷吸收的促进作用无显著差异,玉米的生长和磷吸收效应在接种P300菌剂有较强的正效应;原位菌剂对三叶草植株中铁和锰的含量,玉米植株中锰和锌的含量以及相应的酶活性如酸性磷酸酶、过氧化物酶、几丁质酶、α-葡糖苷酶和β-木糖苷酶活性产生显著影响;接种原位P300菌剂相比于接种原位P0和P75菌剂,显著降低了三叶草根系侵染率。综上,长期不同供磷水平驯化的微生物存在遗留效应,基质供磷水平及植物种类协同影响植物生长、养分吸收、土壤酶活性及菌根特征的效应。土壤微生物遗留效应的探究对于轮作设计有重要意义,选择适当的轮作植物可以促进微生物后续功能的发挥。
| [1] |
Shen R F, Zhao X Q. Role of soil microbes in the acquisition of nutrients by plants (In Chinese)[J]. Acta Ecologica Sinica, 2015, 35(20): 6584-6591. [沈仁芳, 赵学强. 土壤微生物在植物获得养分中的作用[J]. 生态学报, 2015, 35(20): 6584-6591.]
(  0) 0) |
| [2] |
Zhu Y G, Shen R F, He J Z, et al. China soil microbiome initiative: Progress and perspective (In Chinese)[J]. Bulletin of Chinese Academy of Sciences, 2017, 32(6): 554-565. [朱永官, 沈仁芳, 贺纪正, 等. 中国土壤微生物组: 进展与展望[J]. 中国科学院院刊, 2017, 32(6): 554-565.]
(  0) 0) |
| [3] |
Shen J B, Bai Y, Wei Z, et al. Rhizobiont: An interdisciplinary innovation and perspective for harmonizing resources, environment, and food security (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(4): 805-813. [申建波, 白洋, 韦中, 等. 根际生命共同体: 协调资源、环境和粮食安全的学术思路与交叉创新[J]. 土壤学报, 2021, 58(4): 805-813.]
(  0) 0) |
| [4] |
Smith J L, Paul E A. The significance of soil microbial biomass estimations[M]//Soil biochemistry. New York: Routledge, 1990.
(  0) 0) |
| [5] |
Lapsansky E R, Milroy A M, Andales M J, et al. Soil memory as a potential mechanism for encouraging sustainable plant health and productivity[J]. Current Opinion in Biotechnology, 2016, 38: 137-142. DOI:10.1016/j.copbio.2016.01.014
(  0) 0) |
| [6] |
Chen W B, Peng S L. Land-use legacy effects shape microbial contribution to N2O production in three tropical forests[J]. Geoderma, 2020, 358: 113979. DOI:10.1016/j.geoderma.2019.113979
(  0) 0) |
| [7] |
Schmid M W, Hahl T, van Moorsel S J, et al. Feedbacks of plant identity and diversity on the diversity and community composition of rhizosphere microbiomes from a long-term biodiversity experiment[J]. Molecular Ecology, 2019, 28(4): 863-878. DOI:10.1111/mec.14987
(  0) 0) |
| [8] |
Adriaensen K, Vrålstad T, Noben J P, et al. Copper-adapted Suillus luteus, a symbiotic solution for pines colonizing Cu mine spoils[J]. Applied and Environmental Microbiology, 2005, 71(11): 7279-7284. DOI:10.1128/AEM.71.11.7279-7284.2005
(  0) 0) |
| [9] |
Meisner A, Jacquiod S, Snoek B L, et al. Drought legacy effects on the composition of soil fungal and prokaryote communities[J]. Frontiers in Microbiology, 2018, 9: 294. DOI:10.3389/fmicb.2018.00294
(  0) 0) |
| [10] |
Hinojosa M B, Laudicina V A, Parra A, et al. Drought and its legacy modulate the post-fire recovery of soil functionality and microbial community structure in a Mediterranean shrubland[J]. Global Change Biology, 2019, 25(4): 1409-1427. DOI:10.1111/gcb.14575
(  0) 0) |
| [11] |
van der Bom F J T, McLaren T I, Doolette A L, et al. Influence of long-term phosphorus fertilisation history on the availability and chemical nature of soil phosphorus[J]. Geoderma, 2019, 355: 113909. DOI:10.1016/j.geoderma.2019.113909
(  0) 0) |
| [12] |
Lang M, Bei S K, Li X, et al. Rhizoplane bacteria and plant species co-determine phosphorus-mediated microbial legacy effect[J]. Frontiers in Microbiology, 2019, 10: 2856. DOI:10.3389/fmicb.2019.02856
(  0) 0) |
| [13] |
Mander C, Wakelin S, Young S, et al. Incidence and diversity of phosphate-solubilising bacteria are linked to phosphorus status in grassland soils[J]. Soil Biology & Biochemistry, 2012, 44(1): 93-101.
(  0) 0) |
| [14] |
Antunes P M, Lehmann A, Hart M M, et al. Long-term effects of soil nutrient deficiency on arbuscular mycorrhizal communities[J]. Functional Ecology, 2012, 26(2): 532-540. DOI:10.1111/j.1365-2435.2011.01953.x
(  0) 0) |
| [15] |
Martín-Robles N, Lehmann A, Seco E, et al. Impacts of domestication on the arbuscular mycorrhizal symbiosis of 27 crop species[J]. New Phytologist, 2018, 218(1): 322-334. DOI:10.1111/nph.14962
(  0) 0) |
| [16] |
Withers P J A, Clay S D, Breeze V G. Phosphorus transfer in runoff following application of fertilizer, manure, and sewage sludge[J]. Journal of Environmental Quality, 2001, 30(1): 180-188. DOI:10.2134/jeq2001.301180x
(  0) 0) |
| [17] |
Fixen P E, Grove J H. Testing soils for phosphorus[M]// Soil Testing and Plant Analysis. Madison: American Society of Agronomy and Soil Science Society of America, 1990.
(  0) 0) |
| [18] |
Tabatabai M A. Soil enzymes[M]// Methods of soil analysis. Madison: American Society of Agronomy, 1982.
(  0) 0) |
| [19] |
Koch O, Tscherko D, Kandeler E. Temperature sensitivity of microbial respiration, nitrogen mineralization, and potential soil enzyme activities in organic alpine soils[J]. Global Biogeochemical Cycles, 2007, 21(4): 125-129.
(  0) 0) |
| [20] |
Guan S Y. Soil enzymes and its research methods (In Chinese). Beijing: Agriculture Press, 1986. [关松荫. 土壤酶及其研究法[M]. 北京: 农业出版社, 1986.]
(  0) 0) |
| [21] |
McGonigle T P, Miller M H, Evans D G, et al. A new method which gives an objective measure of colonization of roots by vesicular-arbuscular mycorrhizal fungi[J]. New Phytologist, 1990, 115(3): 495-501. DOI:10.1111/j.1469-8137.1990.tb00476.x
(  0) 0) |
| [22] |
王超. 不同供磷量对玉米根系与土壤微生物互作及吐丝后地上部碳磷分配的影响[D]. 北京: 中国农业大学, 2017. Wang C. Influences of phosphorus supply on interactions between roots and soil microbes and post-silking partitioning of shoot carbon/phosphorus in field-grown maize[D]. Beijing: China Agricultural University, 2017 (  0) 0) |
| [23] |
Ocimati W, Tusiime G, Opio F, et al. Sorghum(Sorghum bicolor)as a bean intercrop or rotation crop contributes to the survival of bean root rot pathogens and perpetuation of bean root rots[J]. Plant Pathology, 2017, 66(9): 1480-1486. DOI:10.1111/ppa.12699
(  0) 0) |
| [24] |
Gosling P, Mead A, Proctor M, et al. Contrasting arbuscular mycorrhizal communities colonizing different host plants show a similar response to a soil phosphorus concentration gradient[J]. New Phytologist, 2013, 198(2): 546-556. DOI:10.1111/nph.12169
(  0) 0) |
| [25] |
Griffiths B S, Hallett P D, Kuan H L, et al. Functional resilience of soil microbial communities depends on both soil structure and microbial community composition[J]. Biology and Fertility of Soils, 2008, 44(5): 745-754. DOI:10.1007/s00374-007-0257-z
(  0) 0) |
| [26] |
张伟. 供磷水平对小麦玉米锌吸收、累积的影响及其作用机制[D]. 北京: 中国农业大学, 2017. Zhang W. The mechanisms of zinc uptake and accumulation in wheat and maize as affected by phosphorus levels[D]. Beijing: China Agricultural University, 2017 (  0) 0) |
| [27] |
Zhu X P, Wang Y B, Cao C Y, et al. Interaction of phosphorus and zinc in albic soil (In Chinese)[J]. Journal of Nanjing Agricultural University, 1995, 18(2): 69-73. [朱小平, 王义炳, 曹翠玉, 等. 白浆土磷锌关系的研究[J]. 南京农业大学学报, 1995, 18(2): 69-73.]
(  0) 0) |
| [28] |
Zuo Y M, Zhang F S, Li X L, et al. Studies on the improvement in iron nutrition of peanut by intercropping with maize on a calcareous soil[J]. Plant and Soil, 2000, 220(1/2): 13-25. DOI:10.1023/A:1004724219988
(  0) 0) |
| [29] |
Nannipieri P, Giagnoni L, Landi L, et al. Role of phosphatase enzymes in soil[M]//Soil biology. Berlin, Heidelberg: Springer, 2010: 215-243.
(  0) 0) |
| [30] |
Spohn M, Kuzyakov Y. Distribution of microbial- and root-derived phosphatase activities in the rhizosphere depending on P availability and C allocation - Coupling soil zymography with 14C imaging[J]. Soil Biology & Biochemistry, 2013, 67: 106-113.
(  0) 0) |
| [31] |
Zhao F Z, Ren C J, Han X H, et al. Changes of soil microbial and enzyme activities are linked to soil C, N and P stoichiometry in afforested ecosystems[J]. Forest Ecology and Management, 2018, 427: 289-295. DOI:10.1016/j.foreco.2018.06.011
(  0) 0) |
| [32] |
Fraser T D, Lynch D H, Bent E, et al. Soil bacterial phoD gene abundance and expression in response to applied phosphorus and long-term management[J]. Soil Biology & Biochemistry, 2015, 88: 137-147.
(  0) 0) |
| [33] |
Luo G W, Ling N, Nannipieri P, et al. Long-term fertilisation regimes affect the composition of the alkaline phosphomonoesterase encoding microbial community of a vertisol and its derivative soil fractions[J]. Biology and Fertility of Soils, 2017, 53(4): 375-388.
(  0) 0) |
| [34] |
Li J, Li R Q, Yuan W J. On the change of enzyme activites of cucumber leaf infected by Pseudoperonospora cubensis(berk. et ctrt)rosws (In Chinese)[J]. Acta Phytopathologica Sinica, 1991, 21(4): 277-283. [李靖, 利容千, 袁文静. 黄瓜感染霜霉病菌叶片中一些酶活性的变化[J]. 植物病理学报, 1991, 21(4): 277-283.]
(  0) 0) |
| [35] |
Xie Z S, Li B, Forney C F, et al. Changes in sugar content and relative enzyme activity in grape berry in response to root restriction[J]. Scientia Horticulturae, 2009, 123(1): 39-45.
(  0) 0) |
| [36] |
Mauch H, Brehmer W, Sonneborn H H, et al. Monoclonal antibodies selectively directed against the cell wall surface of Mycobacterium tuberculosis[J]. Journal of Clinical Microbiology, 1988, 26(9): 1691-1694.
(  0) 0) |
| [37] |
Qin Z F, Zhang H Y, Feng G, et al. Soil phosphorus availability modifies the relationship between AM fungal diversity and mycorrhizal benefits to maize in an agricultural soil[J]. Soil Biology & Biochemistry, 2020, 144: 107790.
(  0) 0) |
 2022, Vol. 59
2022, Vol. 59


