2. 教育部植物-土壤相互作用重点实验室, 北京 100193;
3. 农业农村部华北耕地保育重点实验室, 北京 100193
2. Key Laboratory of Plant-Soil Interactions, Ministry of Education, Beijing 100193, China;
3. Key Laboratory of Arable Land Conservation (North China), Ministry of Agriculture and Rural Affairs, Beijing 100193, China
生物炭是由生物质在无氧或限氧条件下经一定温度(通常小于700℃)裂解而成,具有比表面积大、孔隙度高、含碳量高等特点,同时还具有材料来源广泛、原料成本低等优点,因而生物炭有望在土壤固碳减排、土壤修复、农业废物管理和提高农业生产力上发挥巨大的潜力[1-2]。随着生物炭大面积应用,生物炭中的胶体颗粒将不可避免地释放到土壤中[3]。相比于生物炭大颗粒,这部分胶体态生物炭具有很强的反应性和稳定性,同时具有更强的移动性、吸附性和光化学反应活性,可以在土壤中向下迁移,参与更多地下环境中的生物地球化学过程[4-5]。生物炭物料来源、热解温度、颗粒粒径、pH、矿物质成分、可溶性有机质含量和性质对生物炭胶体在土壤中的稳定性、迁移和滞留规律均具有较大的影响[6-8]。
根系分泌物是植物光合作用的主要产物,是植物生长过程中由根系的不同部位溢出或分泌的一些无机离子、质子和有机化合物的统称,是根系固有的生理功能,被认为是根修复的驱动因子[9-10]。根系分泌物的种类繁多,成分复杂,最主要的有机成分是糖类(CHs),其次是氨基酸(AAs)和有机酸(OAs)[11]。根系分泌物在改善土壤理化性质、化感作用、环境胁迫缓解等方面具有重要的作用[12-13],它们可以直接影响土壤中的化学体系,如pH、离子强度和表面电荷,这些均对胶体或纳米颗粒的稳定性和迁移行为产生强烈的影响[14-15]。Du等[14]发现根系分泌物可以作为天然配体改变氧化石墨烯的表面形貌、大小分布和表面电荷,从而改变其在环境的归趋。Tian等[11]发现在高离子强度和低pH条件下,人工根系分泌物的存在降低了饱和多孔介质中蒙脱石胶体的稳定性和移动性。Ren等[16]研究了小麦根系分泌物及其组分对生物炭中有机污染物解吸的影响。此外,根系分泌物中的氨基酸可以通过减少表面电荷或表面桥联作用诱导胶体聚集,或通过增加静电和空间排斥作用来促进胶体稳定[17-18],而有机酸可通过增加表面负电荷来提高胶体的活性[19-20]。随着生物炭在土壤中的广泛施用,生物炭中的胶体颗粒不可避免地经过灌溉或降雨等过程发生迁移,从而与根系分泌物接触并发生相互作用。目前,关于根系分泌物对生物炭胶体在土壤中的聚集行为及迁移能力影响的研究十分有限,其相关相互作用过程和机制仍不清楚。因此,探究根际分泌物对生物炭胶体稳定性和迁移性的影响具有重要环境意义。
本实验选用常见的小麦与松树木屑作为生物炭原材料制备生物炭,旨在研究(1)典型的植物根系分泌物组分(半乳糖、赖氨酸以及乙酸等)对小麦和木屑生物炭胶体聚集动力学的影响;(2)典型的植物根系分泌物组分对小麦和木屑生物炭胶体在多孔介质中的迁移和滞留的影响。这为在土壤中存在植物根系分泌物的条件下生物炭胶体颗粒在土壤中聚集和迁移规律研究提供相关理论依据。
1 材料与方法 1.1 生物炭胶体制备生物炭原材料采用小麦秸秆和松树木屑。在限氧条件下,将生物炭原材料紧密填充于不锈钢容器中,在马弗炉(5-12型,上海光地仪器设备有限公司)中以600℃温度烧制1 h制得生物炭[21]。将制备好的生物炭用球磨仪反复研磨,得到粒径200 nm左右的小麦生物炭(WB)和松树木屑生物炭(PB)粉末。取0.25 g生物炭粉末至50 mL蒸馏水中,超声处理30 min以促进生物炭胶体分散。充分混匀后,将生物炭胶体悬浮液通过0.22 μm的滤膜(KENKER,美国)过滤,并收集滤液备用。用重量法测定生物炭胶体悬浊液浓度。
1.2 根系分泌物实验选用具有代表性的半乳糖(Gal)、赖氨酸(Lys)和乙酸(AcOH)模拟主要根系分泌物组分。半乳糖(C6H12O6)是单糖的一种,等电点为12.35,中性条件下不带电荷;赖氨酸(C6H14N2O2)是一种碱性氨基酸,等电点为9.74,中性条件下带正电荷;乙酸(C2H4O2)是一种有机一元酸,其水溶液呈弱酸性,等电点为4.75,中性条件下带负电荷。分别称取0.050 g半乳糖、赖氨酸(分析纯,国药集团化学试剂有限公司),吸取48 μL乙酸(冰醋酸,分析纯,国药集团化学试剂有限公司)于50 mL蒸馏水,配制成浓度为1 g·L–1的半乳糖、赖氨酸和乙酸溶液,储存备用。
1.3 多孔介质实验选择粒径范围425~600 μm的石英砂(高流镇明亮石英砂厂,新沂市)颗粒作为典型多孔介质。将石英砂在2 mol·L–1盐酸(分析纯,国药集团化学试剂有限公司)中浸泡加热至90℃并保持24 h,期间多次搅拌,以去除石英砂表面的铁氧化物、有机质和碳酸盐等杂质[22],然后用自来水和蒸馏水冲洗直至上清液电导率在2 μS·cm–1以下,在105℃烘箱(DHG-9030,上海一恒科学仪器有限公司)中烘干备用。
1.4 生物炭胶体表征采用动态光散射法(DLS)通过纳米粒度分析仪(Zetasizer Nano ZS 90,马尔文有限公司,英国)测定WB和PB胶体的水合粒径。通过透射电子显微镜(JEM-1230,JEOL,Japan)测定了WB和PB胶体的大小和形貌。通过纳米粒度分析仪测定不同处理下WB和PB胶体在NaCl溶液中的Zeta(ζ)电势以及石英砂的ζ电势。其中,生物炭胶体浓度为100 mg·L–1,根系分泌物浓度为10 mg·L–1。
1.5 聚集实验通过时间-动态光散射法(TR-DLS)测定生物炭胶体在不同离子强度NaCl溶液中的聚集能力[23]。将生物炭胶体悬浮液(100 mg·L–1)超声10 min,加入实验选定离子强度(范围为10~300 mM)的NaCl电解质溶液后迅速将悬浮液涡旋5 s,立即置于纳米粒度分析仪中进行水合粒径的测量。在加入根系分泌物组分(10 mg·L–1)的处理中,尽量将根系分泌物与生物炭胶体混合后,立刻加入电解质溶液[24]。在30 min的时间内,每30 s测定一次水合粒径。
临界聚沉浓度(CCC)是指引起快速聚集的最小电解质的浓度,是评估环境中胶体稳定性的关键因素,通过归一化水合粒径的初始增长速率计算得到[23]。聚集附着效率(α)表征生物炭胶体的聚集程度,当聚集速率与电解质浓度无关时,α为胶体初始聚集速率常数(k)与胶体有利聚集条件下的初始聚集速率常数(kfast)的比值[25],如式(1)所示:
| $ \alpha = \frac{1}{W} = \frac{k}{{{k_{{\text{fast}}}}}} = \frac{{{{\left( {\frac{{{\text{d}}{D_{\text{h}}}\left( t \right)}}{{{\text{d}}t}}} \right)}_{t \to 0}}}}{{{{\left( {\frac{{{\text{d}}{D_{\text{h}}}\left( t \right)}}{{{\text{d}}t}}} \right)}_{t \to 0, {\text{fast}}}}}} $ | (1) |
式中,W代表胶体稳定比,Dh为纳米颗粒生物炭的流体动力学粒径(nm),t为聚集时间(s)。
1.6 迁移实验迁移实验在垂直放置的不锈钢柱(柱长12.6 cm,内径2.6 cm)中进行,采用湿法按照1 cm的增量逐层填装石英砂,为保证容重一致,填装过程中均匀敲击柱壁[26]。在砂柱两端分别垫放两层80目孔径尼龙膜作为支撑材料用以分散水流[1]。水流通过蠕动泵(DHL-A型,上海沪西分析仪器厂有限公司)自下而上以1 mL·min–1的流速注入石英砂柱中。柱子装填完毕后,计算柱子的孔隙体积(PV),确定其孔隙度。本实验中,装填好的石英砂孔隙度为0.42~0.43,容重为1.52~1.53 g·cm–3。
迁移实验过程中,以5 mmol·L–1 NaCl作为背景溶液,持续通入5 PV背景溶液对砂柱进行预平衡,然后通入3 PV不同处理下的生物炭胶体悬浮液(生物炭胶体浓度为100 mg·L–1,根系分泌物组分浓度为10 mg·L–1),最后通入约5 PV的背景溶液进行淋洗,直至出流液中检测不出生物炭胶体为止。在实验过程中,生物炭悬浮液采用磁力搅拌器(90-1型,上海沪西分析仪器厂有限公司)持续进行搅拌,以保证胶体悬浮液的分散均匀性。出流液使用自动部分收集器(BSZ-100型,上海沪西分析仪器厂有限公司)收集,通过紫外分光光度计(TU-1900型,北京普析通用仪器公司)在波长234 nm处测定出流液中生物炭胶体的浓度,并以PV为横轴,出流液中溶液的相对浓度(Ci/C0)为纵轴绘制穿透曲线。
为了得到滞留在多孔介质中生物炭胶体的空间分布,淋洗结束后,将砂柱中填装的石英砂从上到下小心剖分成12等份装入三角瓶中,加入20 mL蒸馏水,将三角瓶置于振荡器(HY-4A型,金坛市科析仪器有限公司)上振荡4 h,取上层清液测定悬浮液吸光度。通过计算得到滞留在砂柱中的生物炭胶体的空间分布,绘制滞留曲线。根据质量守恒,计算出流液中和滞留在石英砂上的生物炭胶体的回收率。实验过程中,pH控制在7.2。
1.7 XDLVO理论由于生物炭胶体表面的疏水性,通过extended Derjaguin-Landau-Verwey-Overbeek(XDLVO)理论定性地描述生物炭胶体在饱和多孔介质中的迁移与滞留行为。XDLVO势能计算公式如下[27-28],其中式(2)为计算XDLVO势能(
| $ {\mathit{\Phi} ^{{\text{Total}}}} = {\mathit{\Phi} ^{{\text{LW}}}} + {\mathit{\Phi} ^{{\text{EDL}}}} + {\mathit{\Phi} ^{{\text{AB}}}} $ | (2) |
| $ {\mathit{\Phi} ^{{\text{LW}}}} = - \frac{{AR}}{{{\text{6}}h}}\left[ {{\text{1}} - \frac{{{\text{5}}{\text{.32}}h}}{{{\lambda _{\text{0}}}}}{\text{ln}}\left( {{\text{1}} + \frac{{{\lambda _{\text{0}}}}}{{{\text{5}}{\text{.32}}h}}} \right)} \right] $ | (3) |
| $ {\mathit{\Phi} ^{{\text{EDL}}}} = \pi \varepsilon R\left. {\left\{ {{\text{2}}{\varphi _{\text{p}}}{\varphi _{\text{s}}}{\text{ln}}\left[ {\frac{{{\text{1}} + {\text{exp}}\left( { - \kappa h} \right)}}{{{\text{1}} - {\text{exp}}\left( { - \kappa h} \right)}}} \right]} \right. + \left( {\varphi _{\text{p}}^{\text{2}} + \varphi _{\text{s}}^{\text{2}}} \right){\text{ ln}}\left[ {{\text{1}} - {\text{exp}}\left( { - {\text{2}}\kappa h} \right)} \right]} \right\} $ | (4) |
| $ {\mathit{\Phi} ^{{\text{AB}}}} = {\text{2}}\pi R{\lambda _{\text{w}}}\Delta G_{{{\text{h}}_{\text{0}}}}^{{\text{AB}}}{\text{exp}}\left( {\frac{{{h_{\text{0}}} - h}}{{{\lambda _{\text{w}}}}}} \right) $ | (5) |
式中,A为胶体的哈梅克常数(Hamaker constant);R表示生物炭胶体半径;h表示胶体与收集器表面间的距离;h0表示胶体与收集器表面之间的最小平衡距离;ε表示液体的介电常数;к表示德拜长度的倒数;φp表示小球的表面电势;φs表示平板的表面电势;λ0表示距离达到100 nm时的特征波长;λw表示路易斯酸碱相互作用的特征衰变长度;
当胶体达到快速聚集阶段(α=1),称为胶体的扩散控制聚集阶段(DLA);而在达到快速聚集阶段以前,聚集现象由颗粒间的XDLVO相互作用控制,称为胶体聚集的反应控制阶段(RLA)[29]。
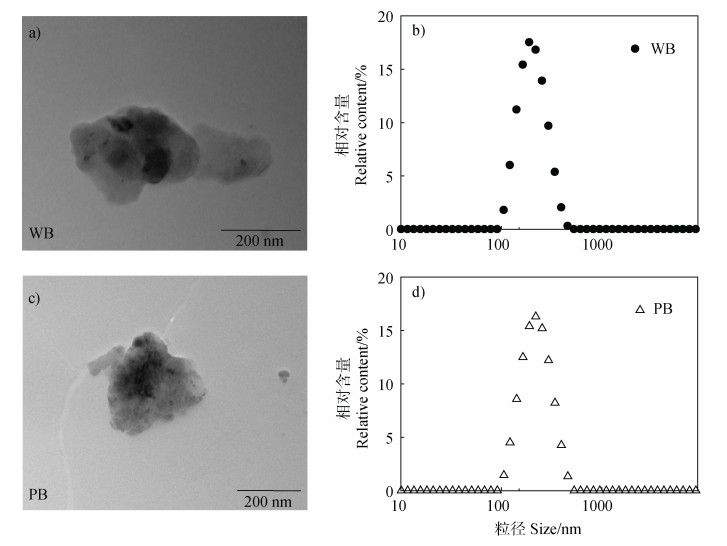
2 结果与讨论 2.1 生物炭的基本性质图 1为小麦和木屑生物炭胶体的形貌与粒径分布,可以看出实验选用的生物炭胶体形态不规则,表面粗糙,并且粒径在纳米级范围内(图 1a和图 1c)。生物炭胶体的平均水合粒径均为200 nm左右,粒径分布较窄,其中84.5%小麦生物炭胶体粒径集中在142~295 nm之间,7.8%颗粒粒径小于142 nm,7.7%颗粒粒径大于295 nm(图 1b)。80.2%的木屑生物炭胶体粒径集中在142~295 nm之间,6.0%的颗粒粒径小于142 nm,13.8%颗粒粒径大于295 nm(图 1d)。
|
图 1 WB和PB胶体的TEM图像(a,c)和粒径分布图(b,d) Fig. 1 TEM images(a, c)and particle size distributions(b, d)of WB and PB colloids |
本研究所用小麦与木屑生物炭在相同的热解温度和热解条件下具有相似的官能团类型及官能团相对含量,官能团类型主要包括C-C、C-H、芳香C、酚羟基或醚基C-O、酮基C=O和羧基-COOH[1,23]。由于裂解温度较高(600℃),生物炭含有较多的芳香烃组分,使其具有较高的反应惰性并保证了生物炭胶体表面较强的疏水性[23]。
2.2 典型根系分泌物组分对生物炭胶体ζ电势和粒径的影响在典型根系分泌物组分半乳糖、赖氨酸和乙酸浓度为10 mg·L–1条件下,生物炭胶体和石英砂的电动特性及相互作用势能如表 1所示,生物炭胶体和石英砂表面的zeta电位均为负值,反映了生物炭胶体和石英砂之间以及胶体和胶体颗粒之间具有一定的静电斥力。两种生物炭胶体电势相近,表明本实验中小麦秸秆和松树木屑来源对生物炭胶体表面携带电荷量影响不大。此外,加入半乳糖、赖氨酸后,两种生物炭胶体电势和粒径基本没有显著变化,加入乙酸后,两种生物炭胶体电势绝对值显著降低,粒径显著变大,可以看出不同处理下生物炭胶体水合粒径的变化符合其zeta电位的变化趋势,表明静电作用对生物炭胶体稳定性具有一定的影响。
|
|
表 1 不同实验条件下生物炭胶体和石英砂的电动特性、相互作用势能以及生物炭胶体的临界聚沉浓度 Table 1 Electrokinetic properties and interaction potentials of biochar colloids and quartz sand and critical coagulation concentrations of biochar colloids in different experiment conditions |
从XDLVO理论计算结果(表 1)看出生物炭-石英砂体系间的次级势阱范围为–0.022~–0.020 kT,显著小于胶体自身布朗运动的动能(1.5 kT),因此生物炭不会滞留在次级势阱区域[7]。与其他处理的生物炭胶体相比,WB-AcOH和PB-AcOH的最大排斥势垒显著降低,表明加入乙酸的生物炭胶体更容易跨过排斥势垒进入初级吸引势阱,生物碳颗粒一旦进入初级吸引势阱,很难从石英砂表面解吸进入液体中[21]。
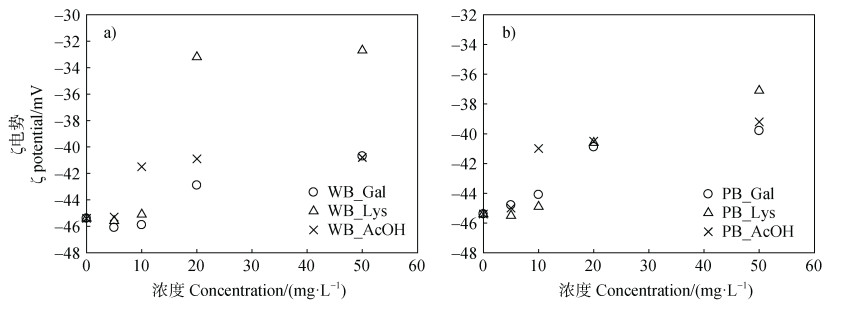
为了进一步验证根系分泌物组分浓度的重要性,本研究测定了不同根系分泌物组分浓度条件下小麦生物炭与木屑生物炭的ζ电势(图 2)。在半乳糖、赖氨酸浓度≤10 mg·L–1时,生物炭胶体电势未发生明显变化,在浓度>10 mg·L–1时,电势绝对值出现了降低的趋势。而乙酸在浓度≤5 mg·L–1时,生物炭胶体电势未发生明显变化,在浓度>5 mg·L–1时,电势绝对值出现降低的趋势。因此,在根系分泌物组分浓度为10 mg·L–1时,半乳糖、赖氨酸对生物炭胶体的ζ电势几乎没有影响,而乙酸显著降低了生物炭胶体ζ电势的绝对值。
|
图 2 不同根系分泌物组分浓度条件下WB(a)与PB(b)的ζ电势 Fig. 2 ζ potentials of WB(a)and PB(b)at different concentrations of root exudates |
图 3和图 4显示了不同实验条件下小麦生物炭和木屑生物炭胶体的聚集动力学。两种生物炭胶体规律相似,在电解质浓度<200 mmol·L–1的情况下,随着电解质浓度的增加,两种生物炭胶体的聚集速率相应增加。在电解质浓度>200 mmol·L–1的情况下,由于生物炭胶体已经发生聚集,电解质浓度的增加未进一步加剧两种生物炭胶体聚集。

|
图 3 在不同浓度NaCl溶液中WB(a)、WB-Gal(b)、WB-Lys(c)和WB-AcOH(d)胶体的聚集曲线 Fig. 3 Aggregation profiles of WB(a), WB-Gal(b), WB-Lys(c)and WB-AcOH(d)colloids at selected NaCl concentrations |

|
图 4 在不同浓度NaCl溶液中PB(a)、PB-Gal(b)、PB-Lys(c)和PB-AcOH(d)胶体的聚集曲线 Fig. 4 Aggregation profiles of PB(a), PB-Gal(b), PB-Lys(c)and PB-AcOH(d)colloids at selected NaCl concentrations |
根据不同实验条件下生物炭胶体水合粒径的聚集速率,计算得到对应离子强度下的α。不同处理下的两种生物炭胶体的α随着电解质浓度的增加而增加(图 5),这是因为当离子强度增加时,离子的双电层受到挤压,使得离子之间斥力减小,附着效率增加[30]。类似的现象也出现在其他胶体和纳米颗粒上,如碳纳米颗粒[3]和金属氧化物颗粒[31]。直到α趋于稳定(α=1),此时生物炭颗粒之间的排斥力消失,生物炭胶体颗粒已经聚集,达到DLA阶段。

|
图 5 不同处理下WB(a)和PB(b)胶体在NaCl溶液中的附着效率 Fig. 5 Attachment efficiencies of WB(a)and PB(b)colloids under different treatments in NaCl solution |
通过α可计算得到对应的生物炭胶体的临界聚沉浓度。小麦生物炭胶体的临界聚沉浓度为195 mmol·L–1,当根系分泌物组分(10 mg·L–1)存在时,小麦生物炭胶体的临界聚沉浓度分别为202 mmol·L–1(WB-Gal)、197 mmol·L–1(WB-Lys)和144 mmol·L–1(WB-AcOH)。木屑生物炭胶体的临界聚沉浓度为198 mmol·L–1,当根系分泌物组分(10 mg·L–1)存在时,木屑生物炭胶体的临界聚沉浓度分别为204 mmol·L–1(PB-Gal)、206 mmol·L–1(PB-Lys)和149 mmol·L–1(PB-AcOH)(图 5)。结果表明,加入乙酸对生物炭胶体的CCC值影响显著(表 1),使两种生物炭胶体的稳定性降低,聚集能力增强,可能因为加入乙酸后,增加了体系中有机酸根阴离子含量,液相中的有机酸根阴离子能够与生物炭表面含氧官能团(如-OH、-COOH等)形成氢键[32],从而引起聚集;或者生物炭胶体上吸附的乙酸能填塞生物炭中部分孔隙[33-34],减少了表面负电荷,引起聚集。本研究中半乳糖、赖氨酸对小麦生物炭和木屑生物炭的稳定性几乎没有影响(表 1),由图 2可以看出,可能由于加入半乳糖、赖氨酸浓度过低,与生物炭胶体几乎不发生任何作用,生物炭胶体的电势没有明显变化,因此不影响生物炭胶体的稳定性。Li等[35]的研究也发现根系分泌物浓度高低对氧化石墨烯的稳定性具有一定的影响,具体程度与根系分泌物种类有关。
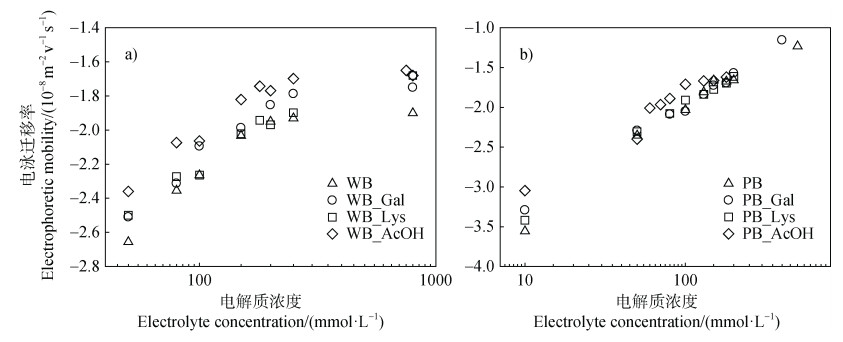
生物炭胶体电泳迁移率(EPM)的绝对值随着盐浓度的增加而减小(图 6),说明随着盐浓度的增加,胶体表面电荷的负电荷变小,生物炭胶体的ζ电势绝对值降低。当达到一定的离子强度后,不同处理下的两种生物炭胶体的EPMs值不再发生显著变化,即达到了CCC值。与其他处理相比,加入乙酸的两种生物炭胶体EPMs绝对值相对较小,更快的达到临界聚沉浓度,表明加入乙酸可以减少生物炭胶体表面的负电荷,使静电排斥力减弱,稳定性降低,更容易发生聚集。因此,WB-AcOH胶体的CCC值为144 mmol·L–1,PB-AcOH胶体的CCC值为149 mmol·L–1,远低于其他处理的CCC值,与前文聚集实验结果相符。
|
图 6 不同处理下WB(a)和PB(b)胶体的电泳迁移率(EPM) Fig. 6 Electrophoretic mobility(EPM)of WB(a)and PB(b)colloids under different treatments |
在聚集实验中,小麦生物炭胶体和木屑生物炭胶体表现出相同的规律,且相同处理下的WB与PB的临界聚沉浓度也相差甚微。可能由于两种原材料热裂解生成的生物炭官能团组成和含量类似,且携带电荷量相近,因此在聚集实验中,根系分泌物组分对小麦生物炭与木屑生物炭胶体的影响没有显著差异。
2.4 典型根系分泌物组分对生物炭胶体迁移的影响图 7a和图 7c显示了在5 mmol·L–1 NaCl和pH为7.2条件下,典型根系分泌物组分的添加对WB和PB在多孔介质中的穿透曲线的影响。两种生物炭胶体迁移规律比较相似,在通入0.8 PV左右生物炭胶体悬浮液时开始淋出,在1.5~3.8 PV达到穿透平台期,小麦生物炭胶体穿透平台峰值分别为0.8(WB)、0.8(WB-Gal)、0.8(WB-Lys)和0.6(WB-AcOH),木屑生物炭胶体穿透平台峰值分别为0.8(PB)、0.8(PB-Gal)、0.8(PB-Lys)和0.6(PB-AcOH)。在3.0 PV时,柱子开始用背景溶液淋洗,在3.8~4.1 PV左右胶体迁移速率迅速下降,5.0 PV以后出流液中几乎检测不出任何生物炭胶体。与未加入根系分泌物组分的生物炭胶体穿透曲线相比,半乳糖、赖氨酸对生物炭胶体穿透曲线峰值几乎没有影响,乙酸使两种生物炭胶体穿透曲线峰值降低,这表明乙酸存在条件下生物炭胶体在柱子中存在较多的滞留。图 7b和图 7d为典型根系分泌物组分存在下两种生物炭胶体在多孔介质中的滞留曲线,生物炭胶体滞留程度随着离入水口距离越近而逐渐增大。与其他处理下的生物炭胶体相比,乙酸造成生物炭胶体滞留程度明显较高,与穿透曲线规律相符合。

|
图 7 不同处理下WB和PB的穿透曲线(a,c)和滞留曲线(b,d) Fig. 7 Breakthrough curves(a, c)and retention curves(b, d)of WB and PB under different treatments |
结合ζ电势(表 1)进行分析,生物炭胶体与石英砂表面电势均为负值,存在较强静电斥力,因此,砂柱迁移实验是不利吸附条件[7]。加入半乳糖、赖氨酸后,两种生物炭胶体电势基本没有变化,加入乙酸后,两种生物炭胶体电势绝对值明显降低,最大排斥势垒变小,生物炭胶体与石英砂间静电斥力减小,从而更容易吸附在石英砂表面,使胶体滞留量增加。此外,乙酸的存在通过提高生物炭胶体的聚集,降低了胶体在石英砂柱中的迁移能力,与Li等[35]研究结果一致。
3 结论本研究通过聚集实验与饱和柱迁移实验,探究了半乳糖、赖氨酸及乙酸等典型植物根系分泌物组分对小麦和木屑生物炭胶体的稳定性和迁移能力的影响。主要结论如下:(1)与生物炭胶体本身的聚集特性相比,半乳糖和赖氨酸浓度较低时对生物炭胶体聚集行为影响较小,乙酸显著降低了生物炭胶体的稳定性;(2)小麦生物炭胶体与木屑生物炭胶体稳定性类似,三种典型根系分泌物组分对这两种生物炭胶体稳定性的影响也类似;(3)与生物炭胶体本身迁移性相比,半乳糖、赖氨酸浓度较低时对小麦生物炭和木屑生物炭胶体在饱和石英砂柱中的迁移能力几乎没有影响,乙酸较显著地减弱了生物炭胶体的迁移能力。
| [1] |
Wang Y, Zhang W, Shang J Y, et al. Chemical aging changed aggregation kinetics and transport of biochar colloids[J]. Environmental Science & Technology, 2019, 53(14): 8136-8146.
(  0) 0) |
| [2] |
Ren X Y, Zeng G M, Tang L, et al. Effect of exogenous carbonaceous materials on the bioavailability of organic pollutants and their ecological risks[J]. Soil Biology and Biochemistry, 2018, 116: 70-81. DOI:10.1016/j.soilbio.2017.09.027
(  0) 0) |
| [3] |
Chen M, Wang D J, Yang F, et al. Transport and retention of biochar nanoparticles in a paddy soil under environmentally-relevant solution chemistry conditions[J]. Environmental Pollution, 2017, 230: 540-549. DOI:10.1016/j.envpol.2017.06.101
(  0) 0) |
| [4] |
Obia A, Børresen T, Martinsen V, et al. Vertical and lateral transport of biochar in light-textured tropical soils[J]. Soil and Tillage Research, 2017, 165: 34-40. DOI:10.1016/j.still.2016.07.016
(  0) 0) |
| [5] |
Fang J, Jin L, Cheng L L, et al. Advancement in research on stability of biochar in the environment (In Chinese)[J]. Acta Pedologica Sinica, 2019, 56(5): 1034-1047. [方婧, 金亮, 程磊磊, 等. 环境中生物质炭稳定性研究进展[J]. 土壤学报, 2019, 56(5): 1034-1047.]
(  0) 0) |
| [6] |
Mia S, Dijkstra F A, Singh B. Long-term aging of biochar: A molecular understanding with agricultural and environmental implications[J]. Advances in Agronomy, 2017, 141: 1-51.
(  0) 0) |
| [7] |
汪登俊. 生物炭胶体和几种人工纳米粒子在饱和多孔介质中的迁移和滞留研究[D]. 北京: 中国科学院大学, 2014. Wang D J. Transport and retention of biochar colloids and representative engineered nanoparticles in saturated porous media[D]. Beijing: University of Chinese Academy of Sciences, 2014. (  0) 0) |
| [8] |
Rechberger M V, Kloss S, Rennhofer H, et al. Changes in biochar physical and chemical properties: Accelerated biochar aging in an acidic soil[J]. Carbon, 2017, 115: 209-219. DOI:10.1016/j.carbon.2016.12.096
(  0) 0) |
| [9] |
Wu L K, Lin X M, Lin W X. Advances and perspective in research on plant-soil-microbe interactions mediated by root exudates (In Chinese)[J]. Chinese Journal of Plant Ecology, 2014, 38(3): 298-310. [吴林坤, 林向民, 林文雄. 根系分泌物介导下植物-土壤-微生物互作关系研究进展与展望[J]. 植物生态学报, 2014, 38(3): 298-310.]
(  0) 0) |
| [10] |
Liao Q H, Liu H, Lu C, et al. Root exudates enhance the PAH degradation and degrading gene abundance in soils[J]. Science of the Total Environment, 2021, 764: 144436. DOI:10.1016/j.scitotenv.2020.144436
(  0) 0) |
| [11] |
Tian Y, Liu C H, Smucker A J M, et al. Plant root exudates decrease mobility of smectite colloids in porous media in contrast to humic acid[J]. Soil Science Society of America Journal, 2015, 79(2): 467-475. DOI:10.2136/sssaj2014.10.0412
(  0) 0) |
| [12] |
Tu S X, Sun J H, Guo Z F, et al. On relationship between root exudates and plant nutrition in rhizosphere (In Chinese)[J]. Soil and Environmental Sciences, 2000, 9(1): 64-67. DOI:10.3969/j.issn.1674-5906.2000.01.017 [涂书新, 孙锦荷, 郭智芬, 等. 植物根系分泌物与根际营养关系评述[J]. 土壤与环境, 2000, 9(1): 64-67.]
(  0) 0) |
| [13] |
Luo X M, Zhou S Y, Yang X. Classification and function of plant roots exudates (In Chinese)[J]. Journal of Anhui Agricultural Sciences, 2019, 47(4): 37-39. DOI:10.3969/j.issn.0517-6611.2019.04.009 [罗晓蔓, 周书宇, 杨雪. 植物根系分泌物的分类和作用[J]. 安徽农业科学, 2019, 47(4): 37-39.]
(  0) 0) |
| [14] |
Du J J, Hu X G, Mu L, et al. Root exudates as natural ligands that alter the properties of graphene oxide and environmental implications thereof[J]. RSC Advances, 2015, 5(23): 17615-17622. DOI:10.1039/C4RA16340K
(  0) 0) |
| [15] |
Servin A D, White J C. Nanotechnology in agriculture: Next steps for understanding engineered nanoparticle exposure and risk[J]. NanoImpact, 2016, 1: 9-12. DOI:10.1016/j.impact.2015.12.002
(  0) 0) |
| [16] |
Ren X H, Wang F, Cao F M, et al. Desorption of atrazine in biochar-amended soils: Effects of root exudates and the aging interactions between biochar and soil[J]. Chemosphere, 2018, 212: 687-693. DOI:10.1016/j.chemosphere.2018.08.124
(  0) 0) |
| [17] |
Molina R, Al-Salama Y, Jurkschat K, et al. Potential environmental influence of amino acids on the behavior of ZnO nanoparticles[J]. Chemosphere, 2011, 83(4): 545-551. DOI:10.1016/j.chemosphere.2010.12.020
(  0) 0) |
| [18] |
Zakaria H M, Shah A, Konieczny M, et al. Small molecule- and amino acid-induced aggregation of gold nanoparticles[J]. Langmuir: the ACS Journal of Surfaces and Colloids, 2013, 29(25): 7661-7673. DOI:10.1021/la400582v
(  0) 0) |
| [19] |
Slowey A J, Johnson S B, Rytuba J J, et al. Role of organic acids in promoting colloidal transport of mercury from mine tailings[J]. Environmental Science & Technology, 2005, 39(20): 7869-7874.
(  0) 0) |
| [20] |
Lowry G V, Shaw S, Kim C S, et al. Macroscopic and microscopic observations of particle-facilitated mercury transport from New Idria and Sulphur Bank mercury mine tailings[J]. Environmental Science & Technology, 2004, 38(19): 5101-5111.
(  0) 0) |
| [21] |
Yang W, Hao D D, Xu D H, et al. Transport and retention of biochar particles in saturated porous media (In Chinese)[J]. Chinese Journal of Soil Science, 2017, 48(2): 304-312. [杨雯, 郝丹丹, 徐东昊, 等. 生物炭颗粒在饱和多孔介质中的迁移与滞留[J]. 土壤通报, 2017, 48(2): 304-312.]
(  0) 0) |
| [22] |
Feng T T, Yang W, Liu K S, et al. Effect of ionic strength and humic acid on the collaborative transport of kaolinite and sulfamethazine (In Chinese)[J]. Journal of Agro-Environment Science, 2017, 36(9): 1804-1810. [冯桐桐, 杨雯, 刘克思, 等. 离子强度和腐植酸对高岭土协同磺胺二甲基嘧啶迁移的影响[J]. 农业环境科学学报, 2017, 36(9): 1804-1810.]
(  0) 0) |
| [23] |
Yang W, Shang J Y, Sharma P, et al. Colloidal stability and aggregation kinetics of biochar colloids: Effects of pyrolysis temperature, cation type, and humic acid concentrations[J]. Science of the Total Environment, 2019, 658: 1306-1315. DOI:10.1016/j.scitotenv.2018.12.269
(  0) 0) |
| [24] |
Shen M H, Yin Y G, Booth A, et al. Effects of molecular weight-dependent physicochemical heterogeneity of natural organic matter on the aggregation of fullerene nanoparticles in mono- and di-valent electrolyte solutions[J]. Water Research, 2015, 71: 11-20. DOI:10.1016/j.watres.2014.12.025
(  0) 0) |
| [25] |
Holthoff H, Egelhaaf S U, Borkovec M, et al. Coagulation rate measurements of colloidal particles by simultaneous static and dynamic light scattering[J]. Langmuir, 1996, 12(23): 5541-5549. DOI:10.1021/la960326e
(  0) 0) |
| [26] |
Yang W, Wang Y, Sharma P, et al. Effect of naphthalene on transport and retention of biochar colloids through saturated porous media[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2017, 530: 146-154.
(  0) 0) |
| [27] |
Gregory J. Approximate expressions for retarded van der waals interaction[J]. Journal of Colloid and Interface Science, 1981, 83(1): 138-145. DOI:10.1016/0021-9797(81)90018-7
(  0) 0) |
| [28] |
Gregory J. Interaction of unequal double layers at constant charge[J]. Journal of Colloid and Interface Science, 1975, 51(1): 44-51. DOI:10.1016/0021-9797(75)90081-8
(  0) 0) |
| [29] |
Zhu X, Chen H, Li W, et al. Aggregation kinetics of natural soil nanoparticles in different electrolytes[J]. European Journal of Soil Science, 2014, 65(2): 206-217. DOI:10.1111/ejss.12118
(  0) 0) |
| [30] |
Shrotri S, Somasundaran P. Particle deposition and aggregation, measurement, modeling and simulation[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 1997, 125(1): 93-94. DOI:10.1016/S0927-7757(97)89090-5
(  0) 0) |
| [31] |
Hua Z L, Zhang J N, Bai X, et al. Aggregation of TiO2-graphene nanocomposites in aqueous environment: Influence of environmental factors and UV irradiation[J]. Science of the Total Environment, 2016, 539: 196-205. DOI:10.1016/j.scitotenv.2015.08.143
(  0) 0) |
| [32] |
Li X Y, Pignatello J J, Wang Y Q, et al. New insight into adsorption mechanism of ionizable compounds on carbon nanotubes[J]. Environmental Science & Technology, 2013, 47(15): 8334-8341.
(  0) 0) |
| [33] |
Zhu B, Fan T X, Zhang D. Adsorption of copper ions from aqueous solution by citric acid modified soybean straw[J]. Journal of Hazardous Materials, 2008, 153(1/2): 300-308.
(  0) 0) |
| [34] |
Feng Y F, Dionysiou D D, Wu Y H, et al. Adsorption of dyestuff from aqueous solutions through oxalic acid-modified Swede rape straw: Adsorption process and disposal methodology of depleted bioadsorbents[J]. Bioresource Technology, 2013, 138: 191-197.
(  0) 0) |
| [35] |
Li X H, Gao B, Xu H X, et al. Effect of root exudates on the stability and transport of graphene oxide in saturated porous media[J]. Journal of Hazardous Materials, 2021, 413: 125362.
(  0) 0) |
 2023, Vol. 60
2023, Vol. 60


