土壤是地球陆地表面能够生长植物的疏松自然体,承载了地球关键带中生命存在形式和数量最丰富的生态系统[1]。土壤在地球物质元素和能量循环以及稳定地表生态系统功能中发挥着举足轻重的作用。这些作用的发挥,与土壤的“疏松”特性密切相关。“疏松”是由于土壤具有可变的复杂孔隙结构。土壤内部真实三维场景是极其复杂、可变形态的孔隙结构与生态-水文过程耦合的动态复杂体系。在这个体系中,土壤孔隙及其关联气-固-液复杂界面发挥着以下重要功能:(1)水分贮存与输运;(2)气体的扩散与传输;(3)溶质的输运;(4)为根系生长提供空间;(5)土壤动物和微生物的生境;(6)土壤化学和生物化学反应的场所。这些功能与孔隙大小密切相关,Brady和Weil[2]总结了它们之间的关系(表 1)。
|
|
表 1 土壤孔隙大小分级以及各级别的一些功能 Table 1 Soil pore size classification and some functions of each classification |
土壤孔隙结构取决于大小形状各异的土壤颗粒和土壤结构体在空间上的复杂排列方式,并受土壤微生物和动物(如蚯蚓、蚂蚁等)活动、植物根系生长、农业机械耕作和压实、干湿交替和冻融过程等生物和非生物因素作用而动态变化。因此,真实的土壤孔隙网络体系的时空变化非常复杂。传统物理技术很难直接观测和定量描述孔隙,更无法论及在这一网络体系中发生的水文与生态过程。进入21世纪以来,计算机技术、X射线CT扫描技术、生物技术和相关土壤性质原位观测和无损探测技术迅速发展,土壤物理、土壤化学及土壤生物学等方面的研究已经开始关注这方面的研究并取得了一定的进展[3-5],为被认为是“黑箱“的土壤孔隙网络的结构与功能研究打开了通道。本文认为“透明”土壤体的物理学已得到快速发展,土壤孔隙学(Soilporelogy)的时代已经启航。
1 传统认识—当量孔径及其分布与土壤结构土壤孔隙状况常用总孔隙度来衡量,即土壤孔隙体积占土壤总体积的比例。但总孔隙度指标仅反映了孔隙数量,不能反映土壤的孔隙大小和形态。由于土壤颗粒和结构体大小形状各异、排列方式错综复杂,土壤中形成的孔隙大小、形状和连通性各不相同。考虑到土壤孔隙的复杂性且很难获取,常通过某些近似和模型来研究土壤孔隙。假设立方和球状紧密排列组合产生的孔隙度在26%至48%之间。而对于实际土壤,根据多级团聚理论,土壤颗粒或团聚体可以在范德华力、氢键、静电力、有机无机胶结剂(如金属氧化物、黏粒表面吸附的有机聚合物、微生物和真菌碎屑)、真菌菌丝和根系等的作用下黏结形成各种大小、不同级别的土壤结构体。土壤结构体排列和结构非常复杂,会形成一个整体上有层次结构的复杂孔隙网络体系[6]。在良好结构的表层土壤中,总孔隙度可高达60%。
传统的土壤学研究中,由于准确地测定土壤孔隙十分困难,为了便于描述土壤中水分运动和溶质运移过程,常将土壤孔隙假设为一束直径不同的圆形毛细管,将圆形毛细管孔径(d)定义为土壤孔隙的当量孔径。根据毛细管理论[2],毛细管直径根据浸入液体的表面张力(σ)、压强差(Δp)、接触角(θ)计算:
| $ d = - \frac{{4\sigma \cos \theta }}{{\Delta p}} $ | (1) |
在上述假设基础上,可通过压汞曲线或水分特征曲线计算孔隙当量直径和孔隙大小分布,测定的孔径范围约为0.01微米至几十微米[7]。土壤中的纳米级孔隙则需要采用气体吸附(如氮气)的方法进行测定。根据当量孔径的大小,土壤孔隙可以分为大孔隙和微孔隙等不同类型(表 1)。有研究发现与圆形的毛细管相比,棱角状或狭缝状孔隙更能代表土壤孔隙[8]。无论对土壤孔隙形状进行何种假设,这些均对土壤真实的孔隙进行了过分的简化和近似。为了从微观机理上研究土壤孔隙中发生的物理、化学和生物学过程,准确定量真实的土壤孔隙分布是非常必要的。
2 土壤孔隙结构与功能认识趋向“透明” 2.1 复杂的土壤三维孔隙结构测定及表征探测土壤真实的三维孔隙结构一直是土壤学家感兴趣的研究方向。由于土壤不透明且容易破碎,获取三维的土壤孔隙结构非常困难。土壤微形态学研究中,首先用树脂将土壤固化,之后再制作土壤切片、拍照并进行图像处理,可以得到二维的土壤孔隙信息[9]。通过逐层切割固化后的土壤样品结合拍照的方法,能够获取土壤孔隙结构的序列图像,将序列图像叠加得到三维的孔隙结构。但是这种方法操作难度大、效率低。随着X射线CT扫描技术的发展和普及,为快速、无损获取土壤内部三维结构提供了条件。X射线CT类型较多,包括医用CT、工业CT和同步辐射显微CT等。其中,医用CT扫描速度快,扫描样品尺寸大,但是分辨率不高(一般为0.3~0.6 mm),可以用于土壤裂隙、土壤生物洞穴等大孔隙的研究。不同型号工业CT可以扫描直径从毫米到数十厘米直径的样品,相应的获取从微米至亚毫米分辨率的土壤孔隙信息。同步辐射显微CT主要针对毫米及以下尺寸小样品开展高分辨率的研究,其特点是单色光、能量大、成像速度快且效果好[10]。除X射线CT外,核磁、中子三维成像技术近年来也发展较快,现在主要用于水分和根系的研究,在土壤孔隙研究中应用不多。
利用图像处理技术可以区分孔隙并提取参数进行表征。X射线CT扫描获取的图像为灰度图,灰度值反映了物体的密度。孔隙中空气的密度与土壤其他物质组成密度存在差异,因而灰度值存在差异,进而可以通过图像分割区分出孔隙,并进行三维可视化。图 1是黑土经过11年免耕和翻耕后的三维孔隙结构,由于CT扫描分辨率为50 μm,图中的孔隙均为在这个分辨率下能够观测到的孔隙,不同颜色代表不同的孔隙大小。对分割后图像进行分析,可以获取表征孔隙三维结构特征的参数。通过统计孔隙所占体积比例可以计算CT图像识别到的孔隙度,此外还可以计算孔隙大小分布、弯曲度、连通性等形态学参数[11]。

|
图 1 长期免耕和翻耕处理黑土三维孔隙结构 Fig. 1 Three-dimensional pore structure of black soil under long-term no-tillage and tillage treatments |
土壤孔隙是土壤中流体贮存的场所和运动的通道,在获取土壤三维孔隙结构基础上,可以利用数学方法模拟计算土壤中水分、气体和溶质的运动。由于土壤孔隙结构的复杂性和无序性,导致基于传热、传质方程的解析方法不适用。作为一种替代解析解的方案,偏微分方程数值解及仿真被大量用于孔隙尺度传热传质研究。这些数值模拟方法以及软件(COMSOL,ANSYS)的使用,可以帮助确定土壤孔隙结构参数与浓度、温度等物理量的时空演化规律之间的关系[12]。特别是当几个因素共同影响一个物理过程时,使用数值模拟可以通过剥离其他因素的影响而逐一评估每个因素的贡献,这是其他实验方法无法比拟的。目前针对孔隙尺度的土壤传热、传质过程,主流数值模拟方法主要包括格子Boltzmann方法[13]和有限元方法[12]。
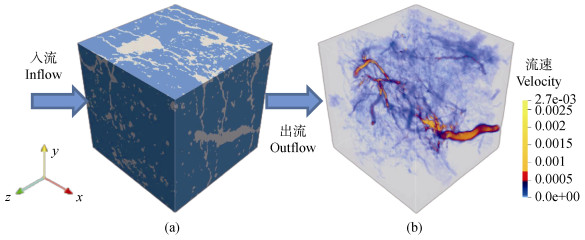
格子Boltzmann方法(LBM)是一种在类似晶格几何结构上模拟流体流动和热/质量传输的方法。LBM使用由晶格点组成的网格,而晶格间通过一定的结合规则相连。AlvarezRamirez等[14]和Weerts等[15]研究表明LBM可成功用于模拟多孔介质中的扩散问题。同时,LBM可以准确地捕捉到多相流条件下土壤和岩石孔隙内的输运过程,并且计算效率较高。已用于孔隙尺度下土壤生物和水分运动的数值模拟[16-18]。本文利用LBM模拟了2 cm×2 cm×2 cm(400体元)大小的黑土在饱和情形下的水分传导过程,获取了孔隙网络流场分布,可以直观显示土壤孔隙网络形态结构对水分传输的作用(图 2),且模拟值与实测值相吻合。
|
注:土壤样品为边长2cm(400体元)立方体。 Note: The soil sample is a cube with a side length of 2 cm(400 voxels). 图 2 二维格子Boltzmann方法(LBM)模拟土壤饱和导水率流场示意图 Fig. 2 Schematic diagram of the simulated soil saturated hydraulic conductivity flow field by the two-dimensional lattice Boltzmann method(LBM) |
对于复杂土壤三维孔隙的仿真模拟,可以用简化的网络模型来近似模拟孔隙结构,以降低计算量。有限元方法(FEM)作为一种主流数值计算方法,广泛用于求解偏微分方程的弱解形式问题。该方法可将复杂的几何形状分割成更简单的几何形状,并在每个有限元上近似求解偏微分方程。和LBM以及有限差分不同,FEM的主要优点是能够处理复杂的几何形状,且具有较高的计算精度[18]。例如,确定二维土壤网络状孔隙结构对扩散系数(图 3a)及热传导的影响[19],以及三维土壤大孔结构参数和饱和导水率等水力参数之间的关系(图 3b)。然而,大孔隙的复杂空间结构使得网格生成变得困难,继而导致FEM计算量大,计算成本高。特别是三维多相流以及流-固耦合问题。

|
图 3 有限元模拟(a)孔隙形态对二维气体扩散的影响[12],采用自由格式的三角形网格(参考红色方框对应区域)以离散化不规则几何体。(b)虫孔对三维水分入渗的影响[20] Fig. 3 Finite element simulation(a)The effect of pore shape on 2D gas diffusion[12], using a free-form triangular mesh(refer to the area corresponding to the red box)to discretize the irregular geometry, (b)Effect of wormholes on three-dimensional water infiltration[20] |
土壤孔隙网络及其形成的气固液复杂界面对土壤中的生物化学过程起着重要作用,例如吸附和解吸、离子交换、氧化还原反应、各种离子和化合物的扩散移动过程等。在单个土壤孔隙与孔隙网络体系中发生的生物化学过程既有联系又有区别。在单个孔隙中,生物化学过程主要发生在孔隙表面;在孔隙网络体系中,生物化学过程还包括孔隙之间的物质输运和反应。以土壤碳转化过程为例,秸秆降解时土壤中微生物的生长和代谢会导致土壤孔隙内局部氧气浓度下降、二氧化碳浓度升高,从而改变碳素氧化还原反应的速率和方向;而孔隙网络结构和水分状态决定的气体对流和扩散又对上述生物化学过程产生影响。
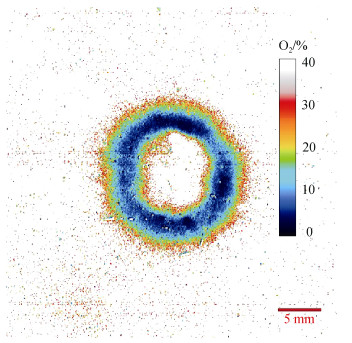
随着显微CT、平面光极(Planar Optode)、酶谱(Zymography)等原位观测技术的发展,可以实现对土壤孔隙尺度的氧气、pH和二氧化碳等物质浓度的动态观测[21],围绕土壤孔隙结构与有机质周转关系的研究取得了一系列进展。Zhu等[21]通过构建土壤微观试验模型,首次从土壤微观孔隙尺度观测了土壤中秸秆残体腐解的微观过程,发现秸秆残体降解过程导致土壤微观界面氧气浓度梯度剧增(图 4),从而促进氧化亚氮排放。Negassa等[22]和Toosi等[23]的结果均表明,在添加植物残体的土壤样品中,不同的土壤孔隙结构影响了土壤二氧化碳的累计排放量,而在未添加外源碳的土壤样品中,土壤二氧化碳的累计排放量之间的差异很小。植物残体降解的初始产物具有较强的可溶性和亲水性,这些降解产物是否会从添加源移动,或者移动距离的远近取决于邻近土壤的孔隙特征[22]。在小孔隙(< 10 μm)发育的土壤中,植物残体的分解产物很可能通过充满水的小孔隙进行扩散移动,进而可能被吸附在土壤颗粒表面,并被土壤微生物所利用。如果没有连通的小孔隙,这种物质扩散就会受到限制,大多数的初始分解产物将与剩余的植物残体物质一起在原位分解并消耗。此外,气体通量被认为是影响微生物群落功能的最重要因素之一[24],大孔隙占主导的土壤可以有较快的气体扩散速率,以及更高的氧气含量,进而有助于植物残体进行更完全的分解过程。因此,土壤孔隙网络特征也可能是影响碳激发效应存在和大小的因素之一[25]。
|
图 4 土壤中秸秆残体降解过程的土壤孔隙中氧气浓度分布图 Fig. 4 Oxygen concentration distribution in soil pores during the degradation process of straw residues in soil |
根系在一定程度上可以看作是土壤中“活的孔隙”,土壤孔隙和根系相互影响、相互促进。一方面,土壤孔隙结构通过直接或间接作用影响根系生长和根系构型。相对于土壤固相,土壤孔隙对作物根系的轴向应力可以认为是零。在紧实土壤中,根系伸长或变粗时,土壤向根系施加相应的反作用力,也就是根系所受到的机械阻力。当阻力大于根系细胞膨压时,根系生长将受到阻碍[26]。大孔隙可以作为根系生长的通道[27-28],促进植物根系的生长、提高水分、养分利用效率[29-32]。不过,也有研究发现根系并不能感知大孔隙并优先利用它在土壤中生长[33-35]。土壤孔隙结构决定了土壤水气条件,也间接调控根系构型。例如Fang等[36]发现,在通气孔隙度更高的水稻土中,主根长度、根毛数量和根系生物量均显著增加。另一方面,根系活动也是土壤孔隙形成的重要因素[37]。植物根系在土壤中伸长和加粗过程中对周围土壤挤压,根系分泌物及其引起的微生物活动促进土壤团聚进而改变根际土壤结构[38],这些过程均改变了根系周围土壤孔隙的大小和形态。而根系的死亡、分解过程也是孔隙形成的主要过程。不同植物的根系构型、生物量差异大,对土壤孔隙形成的作用也不同。通过种植穿透能力强、生物量大的根系,可以塑造土壤孔隙结构,缓解土壤压实。农田采用少免耕措施,可以保持根系形成的连通生物大孔隙(图 1),能够提高土壤的水气传输能力。现在通过X射线CT扫描等手段,可以提取土壤中根系的三维形态结构(图 5a)并进行定量表征[36];在获取根系三维构型基础上,结合土壤水分、养分监测和植物生长过程分析,国内外学者开展了根系吸收水分和养分的模拟研究[39-40](图 5b),对认识根土交互作用进而开展土壤和作物管理具有重要意义,同时也推动了对“活的孔隙”(根系)体系的透明化认识。

|
注:(a)通过CT技术提取水稻根系三维构型,(b)基于土壤水分运动方程的玉米根系三维结构与吸水功能模拟的可视化。 Note: (a)Extraction of the three-dimensional configuration of the rice root system by CT technology, (b)Visualization of three-dimensional structure and water absorption function simulation of maize root system Based on the soil water movement equation. 图 5 根系在土壤中的三维构型与吸水过程模拟 Fig. 5 Three-dimensional configuration of the root system in the soil and the simulation of the water absorption process |
土壤孔隙是很多较小型的土壤动物和微生物的栖息地。“水生”生物,特别是原生生物、线虫、轮虫和缓步动物,活动范围仅限于植物根部和土壤颗粒或团聚体周围充满水的孔隙和水膜。而其他分类群,如螨虫和弹尾虫,则活动于充满空气的土壤孔隙中。因此,土壤的孔隙网络及其可用性影响土壤动物和微生物群体的丰度、运动和分布[41]。与此同时,蚯蚓、蚂蚁等土壤动物活动是土壤生物孔隙的主要形成因素,且不同类型土壤动物形成的蚯蚓洞具有不同的形态特征[42]。近年来研究发现,线虫乃至土壤微生物通过生物化学过程也能改变自身的栖息地,推动孔隙结构的演化。
2.5 真实(准)孔隙网络体系中微生态过程土壤是地球关键带中生命存在形式最丰富的生态系统,土壤中的生命体均存在且活动于土壤孔隙网络中,从这个意义上而言,土壤生态系统主要为土壤孔隙的生态系统。土壤特有的孔隙结构造就了土壤这一特殊的生境,其孔隙结构及其决定的水分分布的非均质性及动态变化特性时刻影响着养分的分布与扩散运移、微生物的生长与运动以及种群之间的互作过程[43-45]。然而,由于土壤本身的复杂特性以及环境条件的动态变化特征,人们对土壤孔隙中真实发生的微观水文物理及微生态过程的认知仍然是土壤学研究领域的一个薄弱环节,也是当前土壤学尤其是土壤微生物学和微生态学研究的热点及国际前沿[46-47]。从土壤微观孔隙结构和个体细胞尺度剖析微生物生长和运动特征以及种群之间互作过程机制是深入理解土壤微生物生命形态特征及关联生态功能的关键。
得益于现代分子生态学和宏基因组学技术以及土壤原位试验观测技术的高速发展与广泛应用,使得从孔隙尺度探究土壤微生态过程及其关联生物地球化学过程成为可能[48-49]。有研究利用精细多孔陶土模拟土壤粗糙界面[50-51],在孔隙尺度实现了土壤微生物活动和种群互作过程的原位观测(图 6),发现微观界面水分动态变化过程引发的微观水动力学能够有效调控微生物的空间分布,并显著促进细菌种群之间的互作和基因交流[52]。Ruan等[53]将真菌菌丝形成的微观水域网络引入到细菌种群,发现真菌菌丝水域网络对微生物多样性的维持、区域扩张的程度以及水平基因转移均具有积极的影响。这些研究有助于从孔隙尺度微观水动力学的角度理解环境微生物群落组织的形成和群落互作的过程,为科学理解和模拟土壤微生物结构和功能多样性及复杂群落的演替规律提供了理论依据。Wang和Or[43]、Ebrahimi和Or[54]利用个体建模理论创建了基于个体细胞的土壤微生物过程计算机仿真模型,实现了对土壤微观孔隙结构和变化环境条件(如水分和氧气含量等)以及微生物活动过程的精确模拟,使得从机理层面探究微生物在动态变化环境中的活动轨迹,以及其与动态环境之间的互作过程成为可能。

|
注:图中灰白色为多孔陶土界面,橙色或绿色是细菌和真菌菌丝。 Note: Gray and white are porous clay interfaces, and orange or green are bacterial and fungal hyphae 图 6 土壤微生物在多孔陶土粗糙界面生长及群落分布图 Fig. 6 The growth and community distribution of soil microorganisms on the rough interface of porous clay |
土壤孔隙的形态结构是动态的,并与土壤的各种物理、化学和生物学过程相互作用。现代物理、信息、生命科学技术极大进步,使得土壤这个“黑箱”逐步透明化,本文能够定量表征三维土壤自然体中孔隙系统的形态结构,以及在其中发生的不同尺度水文生态互作过程。本文将基于土壤孔隙的土壤微观过程及机制研究定义为土壤孔隙学(Soilporelogy),它也已成为当前土壤学基础研究的一个前沿与热点研究领域。如果站在微生物个体考虑问题,对土壤孔隙学的研究就好比人类对自然地理学或景观生态学或土地科学的研究。在未来农业生产与生态保护的基础研究中,本文认为土壤孔隙学的研究越发重要。对此新兴领域研究本文作如下展望:
(1)精确重构和还原土壤孔隙结构,是土壤孔隙学研究的基础。X射线CT扫描技术是现阶段土壤三维孔隙结构定量分析的主要方法。利用不同类型的X射线CT进行扫描,可以获取亚微米至厘米级土壤三维孔隙信息。如何融合不同尺度的X-射线CT数据,获取土壤孔隙的整体信息,仍然需要技术和理论上的突破。图像处理方法的发展和孔隙定量表征参数的创新与标准化将会对X射线CT扫描技术在土壤孔隙研究中的应用和发展有重要作用。此外,核磁共振成像、中子成像、探地雷达以及其他地球物理方法在土壤孔隙研究中也取得了显著进展,这些方法的创新应用不但有助于快速获取多尺度土壤三维孔隙结构,同时能够同步研究土壤水分和根系分布等,让土壤结构和过程更加“透明”。
(2)基于孔隙三维结构的物理过程模拟,推动土壤传热、传质过程研究。X射线CT扫描发展迅速,但多尺度孔隙网络的高精度还原和重构,还需面对高昂的仿真模拟计算成本。对于多物理场耦合问题(固、液、气),通过优化三维孔隙空间结构的表征单元体,来降低计算的复杂性和成本。超级计算机计算能力的发展将提高多尺度孔隙仿真模拟能力,推动土壤水气运动、溶质运移、热量传输以及自然(干湿/冻融交替)或人为(耕作/压实)作用下土壤过程的仿真模拟和定量研究,揭示这些过程的物理机制。
(3)直接探索孔隙表面反应及过程,理解、量化和预测土壤生物化学过程和微生态过程。土壤孔隙及其网络结构对土壤生物化学和微生态过程的重要性从未被质疑过,但直到最近,土壤孔隙尺度原位观测、分子生态学和宏基因组学等技术的进步才使人们能够更直接、深入地研究其过程和作用。基于“孔隙驱动(pore-driven)”的土壤过程研究,将有助于更好地阐释土壤关键元素的转化过程和微观生态学过程。未来的研究可以集中在开发新的技术来原位观测土壤孔隙中的生物化学反应和生物群落互作过程等,认识土壤生物化学过程和微生态过程的发生机制和演变规律。
(4)开展土壤和生物(根系和土壤动物等)交互的原位研究,理解其互作机制,指导土壤管理。土壤孔隙是土壤生物的生境,同时土壤生物活动也会创造、改变土壤孔隙。利用无损探测手段,研究土壤中的各种生物活动、习性,理解土壤生态过程,将会推动对土壤生态系统的理解。根系作为土壤和植物交互作用发生的器官,其在土壤中的生长、发育乃至凋亡、分解均受到土壤孔隙的影响,同时也推动土壤结构的演化。在土壤孔隙、水分、养分和根系构型认识的基础上,开展土壤学、植物生理学和农学的交叉试验和模拟研究,深入探索土壤供给植物水分和养分的过程以及生物耕作等措施改良土壤结构的机制,将会对农田土壤和作物可持续利用管理提供帮助。
| [1] |
Young I M, Crawford J W. Interactions and self- organization in the soil-microbe complex[J]. Science, 2004, 304(5677): 1634-1637. DOI:10.1126/science.1097394
(  0) 0) |
| [2] |
Brady N C, Weil R R. Li B G, Xu J M, et al. trans. The nature and properties of soils[M]. 14th ed. Beijing: Science Press, 2019: 153-154.[尼尔·布鲁迪, 雷·韦尔. 李保国, 徐建明, 等. 译. 土壤学与生活[M]. 第十四版. 北京: 科学出版社, 2019: 153-154.]
(  0) 0) |
| [3] |
Li B G, Ren T S, Zhang J B. Current status, challenges and missions in soil physics (In Chinese)[J]. Acta Pedologica Sinica, 2008, 45(5): 810-816. [李保国, 任图生, 张佳宝. 土壤物理学研究的现状、挑战与任务[J]. 土壤学报, 2008, 45(5): 810-816.]
(  0) 0) |
| [4] |
Li B G, Ren T S, Liu G, et al. Soil physics: Present and future (In Chinese)[J]. Bulletin of Chinese Academy of Sciences, 2015, 30(3): 257-269. [李保国, 任图生, 刘刚, 等. 土壤物理学发展现状与展望[J]. 中国科学院院刊, 2015, 30(3): 257-269.]
(  0) 0) |
| [5] |
Zhu X Y, Shen C Y, Chen G W, et al. Advancement in research on bacterial chemotaxis in soil (In Chinese)[J]. Acta Pedologica Sinica, 2019, 56(2): 259-275. [朱晓艳, 沈重阳, 陈国炜, 等. 土壤细菌趋化性研究进展[J]. 土壤学报, 2019, 56(2): 259-275.]
(  0) 0) |
| [6] |
Zhou H, Li B G, Lü Y Z, et al. Multifractal characteristics of soil pore structure under different tillage systems (In Chinese)[J]. Acta Pedologica Sinica, 2010, 47(6): 1094-1100. [周虎, 李保国, 吕贻忠, 等. 不同耕作措施下土壤孔隙的多重分形特征[J]. 土壤学报, 2010, 47(6): 1094-1100.]
(  0) 0) |
| [7] |
Mitchell J K, Soga K. Fundamentals of soil behavior . 3rd ed[M]. Hoboken, NJ: John Wiley & Sons, 2005.
(  0) 0) |
| [8] |
Tuller M, Or D, Dudley L M. Adsorption and capillary condensation in porous media: Liquid retention and interfacial configurations in angular pores[J]. Water Resources Research, 1999, 35(7): 1949-1964. DOI:10.1029/1999WR900098
(  0) 0) |
| [9] |
Zhou H, Lü Y Z, Li B G. Advancement in the study on quantification of soil structure (In Chinese)[J]. Acta Pedologica Sinica, 2009, 46(3): 501-506. DOI:10.3321/j.issn:0564-3929.2009.03.018 [周虎, 吕贻忠, 李保国. 土壤结构定量化研究进展[J]. 土壤学报, 2009, 46(3): 501-506.]
(  0) 0) |
| [10] |
Zhou H, Li W Z, Zhang Z B, et al. Characterization of multi-scale soil structure with X-ray computed tomography (In Chinese)[J]. Acta Pedologica Sinica, 2013, 50(6): 1226-1230. [周虎, 李文昭, 张中彬, 等. 利用X射线CT研究多尺度土壤结构[J]. 土壤学报, 2013, 50(6): 1226-1230.]
(  0) 0) |
| [11] |
Helliwell J R, Sturrock C J, Grayling K M, et al. Applications of X-ray computed tomography for examining biophysical interactions and structural development in soil systems: A review[J]. European Journal of Soil Science, 2013, 64(3): 279-297. DOI:10.1111/ejss.12028
(  0) 0) |
| [12] |
Liu G, Li B G, Hu K L, et al. Simulating the gas diffusion coefficient in macropore network images: Influence of soil pore morphology[J]. Soil Science Society of America Journal, 2006, 70(4): 1252-1261. DOI:10.2136/sssaj2005.0199
(  0) 0) |
| [13] |
Ramstad T, Berg C F, Thompson K. Pore-scale simulations of single-and two-phase flow in porous media: Approaches and applications[J]. Transport in Porous Media, 2019, 130(1): 77-104. DOI:10.1007/s11242-019-01289-9
(  0) 0) |
| [14] |
Alvarez-Ramírez J, Nieves-Mendoza S, González-Trejo J. Calculation of the effective diffusivity of heterogeneous media using the lattice-Boltzmann method[J]. Physical Review E, 1996, 53(3): 2298-2303. DOI:10.1103/PhysRevE.53.2298
(  0) 0) |
| [15] |
Weerts A H, Kandhai D, Bouten W, et al. Tortuosity of an unsaturated sandy soil estimated using gas diffusion and bulk soil electrical conductivity[J]. Soil Science Society of America Journal, 2001, 65(6): 1577-1584. DOI:10.2136/sssaj2001.1577
(  0) 0) |
| [16] |
Zhang X X, Johnson S N, Gregory P J, et al. Modelling the movement and survival of the root-feeding clover weevil, Sitona lepidus, in the root-zone of white clover[J]. Ecological Modelling, 2006, 190(1/2): 133-146.
(  0) 0) |
| [17] |
Zhang X X, Crawford J W, Young I M. A Lattice Boltzmann model for simulating water flow at pore scale in unsaturated soils[J]. Journal of Hydrology, 2016, 538: 152-160. DOI:10.1016/j.jhydrol.2016.04.013
(  0) 0) |
| [18] |
Hu W L, Liu G F, Zhang X X. A pore-scale model for simulating water flow in unsaturated soil[J]. Microfluidics and Nanofluidics, 2018, 22(7): 1-12.
(  0) 0) |
| [19] |
Xiao X, Liu G, Li B G. Finite element analysis of effect of soil pores on measurement of specific heat with the dual-probe heat-pulse method (In Chinese)[J]. Acta Pedologica Sinica, 2013, 50(6): 1138-1142. [肖潇, 刘刚, 李保国. 有限元模拟土壤孔隙对双针热脉冲法测量比热的影响[J]. 土壤学报, 2013, 50(6): 1138-1142.]
(  0) 0) |
| [20] |
Zhang J, Wen N, Sun Q, et al. The effect of macropore morphology of actual anecic earthworm burrows on water infiltration: A COMSOL simulation[J]. Journal of Hydrology, 2023, 618: 129261. DOI:10.1016/j.jhydrol.2023.129261
(  0) 0) |
| [21] |
Zhu K, Ye X, Ran H Y, et al. Contrasting effects of straw and biochar on microscale heterogeneity of soil O2 and pH: Implication for N2O emissions[J]. Soil Biology and Biochemistry, 2022, 166: 108564. DOI:10.1016/j.soilbio.2022.108564
(  0) 0) |
| [22] |
Negassa W C, Guber A K, Kravchenko A N, et al. Properties of soil pore space regulate pathways of plant residue decomposition and community structure of associated bacteria[J]. PLoS One, 2015, 10(4): e0123999. DOI:10.1371/journal.pone.0123999
(  0) 0) |
| [23] |
Toosi E R, Kravchenko A N, Guber A K, et al. Pore characteristics regulate priming and fate of carbon from plant residue[J]. Soil Biology and Biochemistry, 2017, 113: 219-230. DOI:10.1016/j.soilbio.2017.06.014
(  0) 0) |
| [24] |
Or D, Smets B F, Wraith J M, et al. Physical constraints affecting bacterial habitats and activity in unsaturated porous media–A review[J]. Advances in Water Resources, 2007, 30(6/7): 1505-1527.
(  0) 0) |
| [25] |
Ruamps L S, Nunan N, Pouteau V, et al. Regulation of soil organic C mineralisation at the pore scale[J]. FEMS Microbiology Ecology, 2013, 86(1): 26-35. DOI:10.1111/1574-6941.12078
(  0) 0) |
| [26] |
Hsiao T C, Bradford K J. Physiological consequences of cellular water deficits//Taylor H M. Limitations to efficient water use in crop production[M]. ASA, Madison, WI, 1983: 227-265.
(  0) 0) |
| [27] |
Gao W, Hodgkinson L, Jin K, et al. Deep roots and soil structure[J]. Plant, Cell & Environment, 2016, 39(8): 1662-1668.
(  0) 0) |
| [28] |
Xiong P, Zhang Z B, Peng X H. Root and root-derived biopore interactions in soils: A review[J]. Journal of Plant Nutrition and Soil Science, 2022, 185(5): 643-655. DOI:10.1002/jpln.202200003
(  0) 0) |
| [29] |
Colombi T, Braun S, Keller T, et al. Artificial macropores attract crop roots and enhance plant productivity on compacted soils[J]. Science of the Total Environment, 2017, 574: 1283-1293. DOI:10.1016/j.scitotenv.2016.07.194
(  0) 0) |
| [30] |
Zhou H, Whalley W R, Hawkesford M J, et al. The interaction between wheat roots and soil pores in structured field soil[J]. Journal of Experimental Botany, 2021, 72(2): 747-756. DOI:10.1093/jxb/eraa475
(  0) 0) |
| [31] |
Xiong P, Zhang Z B, Guo Z C, et al. Macropores in a compacted soil impact maize growth at the seedling stage: Effects of pore diameter and density[J]. Soil and Tillage Research, 2022, 220: 105370. DOI:10.1016/j.still.2022.105370
(  0) 0) |
| [32] |
Atkinson J A, Hawkesford M J, Whalley W R, et al. Soil strength influences wheat root interactions with soil macropores[J]. Plant, Cell & Environment, 2020, 43(1): 235-245.
(  0) 0) |
| [33] |
Dexter A R. Model experiments on the behaviour of roots at the interface between a tilled seed-bed and a compacted sub-soil[J]. Plant and Soil, 1986, 95(1): 149-161. DOI:10.1007/BF02378860
(  0) 0) |
| [34] |
Nakamoto T. The distribution of maize roots as influenced by artificial vertical macropores[J]. Japanese Journal of Crop Science, 1997, 66(2): 331-332.
(  0) 0) |
| [35] |
Phalempin M, Landl M, Wu G M, et al. Maize root-induced biopores do not influence root growth of subsequently grown maize plants in well aerated, fertilized and repacked soil columns[J]. Soil and Tillage Research, 2022, 221: 105398.
(  0) 0) |
| [36] |
Fang H, Zhou H, Norton G J, et al. Interaction between contrasting rice genotypes and soil physical conditions induced by hydraulic stresses typical of alternate wetting and drying irrigation of soil[J]. Plant and Soil, 2018, 430(1): 233-243.
(  0) 0) |
| [37] |
Zhang Z B, Peng X H. Bio-tillage: A new perspective for sustainable agriculture[J]. Soil and Tillage Research, 2021, 206: 104844.
(  0) 0) |
| [38] |
Benard P, Schepers J R, Crosta M, et al. Physics of viscous bridges in soil biological hotspots[J]. Water Resources Research, 2021, 57(11): e2021WR030052.
(  0) 0) |
| [39] |
Zhang W P, Li B G. Simulation of spatial distribution and parameter analysis of maize root system in homogeneous loam soil (In Chinese)[J]. Acta Pedologica Sinica, 2007, 44(5): 949-955. [张吴平, 李保国. 均质壤土下玉米根系三维空间分布的模拟与参数分析[J]. 土壤学报, 2007, 44(5): 949-955.]
(  0) 0) |
| [40] |
Rabbi S M F, Tighe M K, Flavel R J, et al. Plant roots redesign the rhizosphere to alter the three-dimensional physical architecture and water dynamics[J]. New Phytologist, 2018, 219(2): 542-550.
(  0) 0) |
| [41] |
Nielsen U N. Global to local scales . Cambridge, United Kingdom: Cambridge University Press, 2019.
(  0) 0) |
| [42] |
Bottinelli N, Zhou H, Capowiez Y, et al. Earthworm burrowing activity of two non-Lumbricidae earthworm species incubated in soils with contrasting organic carbon content(Vertisol vs. Ultisol)[J]. Biology and Fertility of Soils, 2017, 53(8): 951-955.
(  0) 0) |
| [43] |
Wang G, Or D. Hydration dynamics promote bacterial coexistence on rough surfaces[J]. The ISME Journal, 2013, 7(2): 395-404.
(  0) 0) |
| [44] |
Paez-Espino D, Eloe-Fadrosh E A, Pavlopoulos G A, et al. Uncovering earth's virome[J]. Nature, 2016, 536(7617): 425-430.
(  0) 0) |
| [45] |
Hampton H G, Watson B N J, Fineran P C. The arms race between bacteria and their phage foes[J]. Nature, 2020, 577(7790): 327-336.
(  0) 0) |
| [46] |
Kortright K E, Chan B K, Turner P E. High-throughput discovery of phage receptors using transposon insertion sequencing of bacteria[J]. Proceedings of the National Academy of Sciences of the United States of America, 2020, 117(31): 18670-18679.
(  0) 0) |
| [47] |
Sokol N W, Slessarev E, Marschmann G L, et al. Life and death in the soil microbiome: How ecological processes influence biogeochemistry[J]. Nature Reviews Microbiology, 2022, 20(7): 415-430.
(  0) 0) |
| [48] |
Jin M, Guo X, Zhang R, et al. Diversities and potential biogeochemical impacts of mangrove soil viruses[J]. Microbiome, 2019, 7(1): 1-15.
(  0) 0) |
| [49] |
Bi L, Yu D T, Du S, et al. Diversity and potential biogeochemical impacts of viruses in bulk and rhizosphere soils[J]. Environmental Microbiology, 2021, 23(2): 588-599.
(  0) 0) |
| [50] |
Chen Z Y, Zhang W, Wang G, et al. Bioavailability of soil-sorbed tetracycline to Escherichia coli under unsaturated conditions[J]. Environmental Science & Technology, 2017, 51(11): 6165-6173.
(  0) 0) |
| [51] |
Wang Y, Ruan C J, Xie W L, et al. Effects of microscopic water and nutrient conditions on the host lysis process of Pseudomonas aeruginosa phage (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(3): 835-845. [王燕, 阮楚晋, 谢文琳, 等. 微观水分和养分条件对铜绿假单胞菌的噬菌体裂解宿主过程的影响[J]. 土壤学报, 2023, 60(3): 835-845.]
(  0) 0) |
| [52] |
Ruan C J, Ramoneda J, Chen G W, et al. Evaporation- induced hydrodynamics promote conjugation-mediated plasmid transfer in microbial populations[J]. ISME Communications, 2021, 1: 54.
(  0) 0) |
| [53] |
Ruan C J, Ramoneda J, Gogia G, et al. Fungal hyphae regulate bacterial diversity and plasmid-mediated functional novelty during range expansion[J]. Current Biology, 2022, 32(24): 5285-5294.e4.
(  0) 0) |
| [54] |
Ebrahimi A, Or D. Mechanistic modeling of microbial interactions at pore to profile scale resolve methane emission dynamics from permafrost soil[J]. Journal of Geophysical Research: Biogeosciences, 2017, 122(5): 1216-1238.
(  0) 0) |
 2023, Vol. 60
2023, Vol. 60

