2. 重庆市农业资源与环境研究重点实验室, 重庆 400716;
3. 重庆市长寿经济技术开发区开发投资集团有限公司, 重庆 401220;
4. 四川省绵阳市涪城区住房和城乡建设局, 四川绵阳 621000
2. Chongqing Key Laboratory of Agricultural Resources and Environment Research, Chongqing 400716, China;
3. Chongqing Changshou Economic and Technological Development Zone Development and Investment Group Co., Ltd., Chongqing 401220, China;
4. Housing and Urban Rural Development Bureau of Fucheng District, Mianyang City, Mianyang, Sichuan 621000, China
随着大量含重金属污染物的废水排放到环境中,我国废水重金属污染日趋严重[1]。此外农药化肥过度使用、资源开发不合理等问题频出,导致土壤生态环境也受到严峻的挑战。其中,重金属铅,具有不可降解性和强致毒性,已经广泛存在于水体和土壤中[2],严重威胁人类健康和生态安全[3]。因此,高效、快速、经济地进行铅污染废水和土壤修复具有重要的现实意义。目前,去除水中的重金属经常采用的方法包括化学沉淀[4]、吸附法[5]等,其中,吸附法被视为经济、高效的方法之一。在众多吸附材料中,磁性纳米材料具有高比表面积、易功能化及可回收等优点[6]。通常采用官能团修饰来解决磁性材料化学稳定性较差的缺点,这种方法已广泛用于重金属离子的去除中[7],例如,蒲生彦等[8]采用原位共沉淀法和交联法将壳聚糖与四氧化三铁Fe3O4合成复合材料CS-EGDE/Fe3O4凝胶微球,使其具有磁性多孔的特点。此外,还有通过柠檬酸改性的甘蔗渣与Fe3O4合成复合材料[9];膨润土和Fe3O4合成磁性Fe3O4/膨润土纳米颗粒[10]。
纳米羟基磷灰石(Ca10(PO4)6(OH)2,HAP)具有独特的多孔结构和较强的吸附能力,对铅具有较高的吸附能力[11]。将HAP与Fe3O4合成复合材料后,不仅能改善复合材料粒径,还能实现材料与介质的快速磁性分离,从而将重金属离子从污染环境中吸附去除,是一种新型环境友好的功能材料[11]。例如,Dong等[12]采用原位沉淀法将Fe3O4与羟基磷灰石结合得到复合材料,研究其对溶液中Pb2+的吸附过程,认为溶解-沉淀和表面络合是复合材料吸附铅的主要吸附机理。但总体上磁性纳米材料对重金属的吸附上仍然存在一些亟待解决的问题,例如如何提高材料的磁响应强度,满足从土壤介质中回收要求,如何提高材料的循环使用次数,实现绿色环保等。基于此,本研究以X射线衍射(XRD)、扫描电镜(SEM)、比表面积测定(BET)等技术为手段,研究MFH材料对污染土壤和废水中Pb2+的去除修复效果,并探讨了重金属活化剂对土壤修复的影响和材料回收再生性能,以期为重金属离子废水处理领域和土壤中重金属的原位处理提供理论参考。
1 材料与方法 1.1 供试材料供试土壤取自重庆大渡口铅污染农田和工业园区,分别记为铅污染土A(农田污染土壤)和铅污染土B(工业园区污染土壤)。供试土壤的pH、有机质、阳离子交换量以及重金属全量的测定分别采用pH电极测定法、重铬酸钾容量法—外加热法、醋酸铵法、土壤消化—火焰原子吸收分光光度法,测定结果如表 1所示。
|
|
表 1 供试铅污染土壤基本理化性质 Table 1 Basic physical and chemical properties of the tested lead-contaminated soil |
根据《土壤环境质量农用地土壤污染风险管控标准》(试行)(GB15618—2018)[13]和《土壤环境质量建设用地土壤污染风险管控标准》(试行)(GB36600—2018)[14],两种土壤中铅含量均高于筛选值,低于管制值。
超顺磁性纳米Fe3O4–磷酸盐功能化材料(MFH)按照方丹丹等[15]的方法合成,其结构表征参见2.8。
1.2 超顺磁性微纳米MFH对溶液中Pb2+的吸附 1.2.1 等温吸附热力学特征及其影响因子称取一定质量的MFH于含有50 mL Pb(NO3)2溶液的离心管中,设置投加量、Pb2+浓度、pH等影响因子,在220 r·min–1的转速下震荡一定时间后,利用磁铁将材料吸附在离心管底部,倾倒出上清液,用火焰原子分光光度计测定溶液中Pb2+剩余浓度。
MFH投加量的影响:分别称取0、0.05、0.10、0.15、0.20、0.30 g MFH,溶液初始Pb2+浓度为625.63 μg·mL–1,pH为5.00,体系温度设置15℃。
溶液初始Pb2+浓度的影响:以硝酸铅配制浓度为0、50、100、200、500、750、1 000 μg·mL–1的Pb2+溶液,称取0.10 g MFH。
pH的影响:设置溶液初始pH为2.00、3.00、4.00、5.00,溶液初始Pb2+浓度为625.63 μg·mL–1。
离子强度的影响:以NaNO3作为支持电解质来调节反应体系离子强度,设置离子浓度为0、0.02、0.10、0.30、0.50、0.70、1.2 mol·L–1。
有机质浓度的影响:在溶液中添加腐殖酸(Q/JFC043-2004标准,上海巨枫化学科技有限公司),以反映有机质对溶液体系中MFH吸附Pb2+的影响。设置腐殖酸浓度为0、10、20、50、100、200 mg·L–1。
1.2.2 反应时间的影响(动力学)设置震荡时间为0、5、10、20、60、120 min,称取0.10 g MFH于含有50 mL 625.63 μg·mL–1 Pb2+溶液的离心管中,溶液pH为5.00,体系温度设置15℃。
1.3 材料的表征用X射线衍射仪XRD(BRUCKER D8 ADVANCE,德国布鲁克)、扫描电子显微镜SEM(SU8020,日本日立)、振动样品磁强计VSM(VSM-Versalab,美国Quantum Design)、比表面积分析BET(ASAP2060,上海麦克默瑞提克)对制得的MFH、吸附Pb2+后的复合材料(A-MFH)以及再生后的复合材料(R-MFH)进行形态、粒径分布、比表面积以及磁性能等参数进行表征。采用电位滴定法测定材料的零电荷pH(pHPZC)。
1.4 MFH对污染土壤铅的去除修复称取1.6 kg的农田铅污染土壤A和工业园区铅污染土壤B于1 000 mL烧杯中,模拟15 cm耕作层土壤厚度,以水土比1︰1做淹水处理,使上覆水层约为5 cm,搅拌10 min,使水土混均。以料土比为0.9%比例加入MFH材料,间歇搅拌20 min,静置2 h,待材料与土壤中的铅充分接触并相互作用后,用磁棒插入土壤并进行搅拌,磁选回收MFH,重复3次。将剩余土壤溶液离心,用火焰原子分光光度计测上清液Pb2+残余浓度,处理后的土壤风干后用BCR法[16]测定土壤铅形态的变化,其中上清液Pb2+浓度算作酸可溶态铅的一部分。根据土壤被处理前后铅形态的变化计算MFH材料对污染土壤中铅的去除效果。
重金属活化剂对土壤铅去除率的影响:考察污染土壤中添加EDTA活化剂对MFH去除土壤铅的影响,称取污染土壤A、B,设置2个处理:①不施EDTA;②称取适量EDTA,溶解于水做淹水处理,使土壤中EDTA含量为3 mmol·kg–1。
1.5 MFH回收与再生MFH回收率测定:将土壤中回收的MFH在清水中反复进行磁吸-解磁操作,以尽量洗脱杂质后,用少量稀酸洗涤,再干燥,去除干燥物中夹带的土壤和弱磁性的铁氧化合物,称重并计算其回收率。
磁场强度对土壤中材料回收率的影响:分别用磁场强度为3 600、4 000、4 500、5 200 G的磁棒按以上方法进行试验,探讨磁场强度对土壤中材料回收率的影响。
MFH再生性能测定:取适量MFH,在20℃、220 r·min–1震荡2 h条件下,处理625.63 μg·mL–1的Pb2+溶液,使MFH饱和吸附Pb2+,用磁铁将材料与溶液分离,测溶液中剩余Pb2+浓度,将材料冷冻干燥,称重。将达到饱和吸附Pb2+离子的MFH材料(A-MFH),进行如下再生处理:将A-MFH加入pH为4.50的稀硝酸溶液(固液比1︰2),在25℃条件下震荡洗脱1 h,过滤,干燥,获得再生产品R-MFH,同上处理,测R-MFH吸附后溶液中剩余Pb2+浓度。
上述试验均设置3个重复,每个重复3个平行,经离群值检验取舍后,以平均值计算MFH对Pb2+的吸附量或去除率。
1.6 数据处理MFH质量损耗率(S)和性能恢复率(H)由下式求得:
| $ S = \frac{{{m_2}}}{{{m_1}}} $ | (1) |
| $ H = \frac{{{f_2}}}{{{f_1}}} $ | (2) |
式中,m1为吸附了Pb2+的R-MFH质量减去吸附了Pb2+的MFH质量(g),m2为吸附了Pb2+的MFH质量(g),f1为MFH对Pb2+的去除率,f2为R-MFH对Pb2+的去除率。
Pb2+的去除率X和吸附容量Q由下式求得:
| $ X = \frac{{\left( {{C_0} - {C_{\text{m}}}} \right)}}{{{C_0}}} $ | (3) |
| $ Q = \frac{{\left( {{C_0} - {C_{\text{m}}}} \right)V}}{m} $ | (4) |
式中,C0为溶液的初始浓度(μg·mL–1),Cm为吸附后溶液的Pb2+浓度(μg·mL–1),V为溶液的体积(L),m为材料MFH投放质量(g)。
采用Microsoft Office Excel 2010进行数据处理,Origin 9对处理后的数据作图分析。
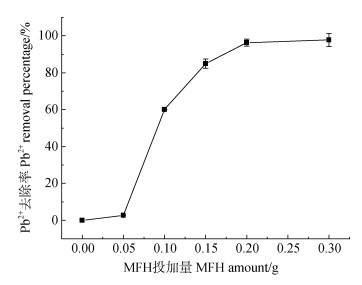
2 结果与讨论 2.1 MFH投加量对吸附溶液中Pb2+的影响通过研究投加量对Pb2+的吸附影响,可以确定材料的最佳投加剂量,有利于实现材料的高效利用。在吸附时间为2 h条件下,MFH投加量对Pb2+去除率的影响曲线见图 1。由图可知,MFH对Pb2+的去除率随投加量的增加逐步增大,表明较高用量的吸附剂为Pb2+提供了更多活性反应位点,Pb2+可有更高机率与MFH的活性基团结合[17]。在投加量达到0.20 g时,MFH对Pb2+的去除量达152.6 mg·g–1,去除率达到97.59%,随着投加量继续增加,去除率不再增加。这是由于随着投加量的进一步增加,可能会发生吸附剂的聚集和活性中心的重叠,吸附过程在该条件下达到平衡,因此去除率没有显著变化[10]。
|
注:图中误差线为数据的标准偏差。下同。 Note:The error bars in the figure are the standard deviation of the data. The same below. 图 1 MFH投加量对溶液中Pb2+的吸附影响 Fig. 1 Effect of MFH dosage on the adsorption of Pb2+ in solution |
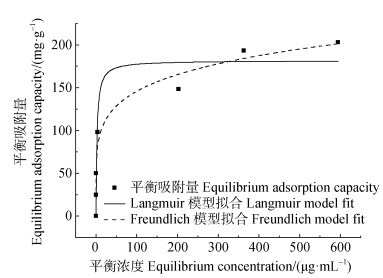
Pb2+在MFH上的等温吸附曲线见图 2。MFH对溶液中Pb2+的吸附量随着Pb2+初始浓度的增加而增大,当Pb2+初始溶液浓度小于200 μg·mL–1时,去除率均达到98%以上,Pb2+几乎完全被MFH吸附;当初始浓度大于200 μg·mL–1时,吸附量增幅明显减缓,吸附逐渐趋于饱和。这是由于Pb2+浓度的增大,使吸附量明显增加;但材料的吸附位点数量一定,阳离子数量增加到一定程度使吸附位点几乎被完全利用,因此吸附量增长缓慢逐渐达到平衡[18]。
|
图 2 MFH对溶液中Pb2+的等温吸附模型 Fig. 2 Isothermal adsorption model of Pb2+ in solution by MFH |
采用吸附等温模型对MFH对Pb2+的吸附过程进行拟合,分析吸附剂的表面结构和吸附机理。由表 2可知,Freundlich方程拟合的决定系数R2达到0.969,可以判定Freundlich吸附等温模型能较合理地描述了MFH对Pb2+吸附过程中的热力学过程,属于多层吸附类型[19]。此外,吸附强度常数n > 1,说明MFH对Pb2+易发生吸附,吸附过程有利且不均匀。拟合得出的MFH对Pb(Ⅱ)的最大吸附能力为181.6 mg·g–1,且与其他磁性吸附剂相比(见表 3)相比具有较大的竞争力。
|
|
表 2 MFH对Pb2+的等温吸附模型拟合 Table 2 Fitting results of isothermal adsorption model of Pb2+ by MFH |
|
|
表 3 不同磁性吸附剂对Pb的吸附能力 Table 3 Comparison of adsorption capacity of different magnetic adsorbents for Pb |
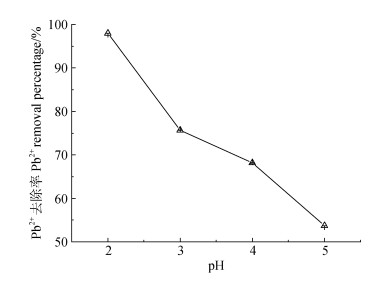
在pH > 6.00时,高浓度的Pb2+溶液(625.63 μg·mL–1)水解产生白色悬浊物,形成Pb(OH)2沉淀,而pH < 2.00时,复合材料中Fe3O4发生明显酸溶解反应使溶液体系变黄,破坏材料结构[17]。故只考虑弱酸性pH 2.00~5.00范围内,pH对MFH吸附性能的影响。从图 3可以看出,低pH范围内MFH对Pb2+的去除率随溶液pH的增加而下降,由pH为2.00时去除率98.02%降至pH为5.00时去除率53.69%。这是由于pH条件可显著改变MFH颗粒表面的荷电状态[24]。
|
图 3 pH对MFH吸附溶液中Pb2+的影响 Fig. 3 Effect of pH on Pb2+ in MFH adsorption solution |
Pb(Ⅱ)在磁性羟基磷灰石上的吸附主要包括表面络合、离子交换、溶解沉淀和静电吸附等机制[17]。首先,是Pb2+发生在Fe3O4和羟基磷灰石表面的吸附,式(5)、式(6)展示了表面络合物的形成,其中,S代表Fe3O4和羟基磷灰石的表面,H+与Pb2+交换形成表面络合物,这一步骤被认为是最开始的快速吸附机制[25]。其次,在酸性条件下,羟基磷灰石发生溶解,溶解出的磷酸盐与Pb2+反应并沉淀,同时,吸附在纳米羟基磷灰石表面的Pb2+,与Ca2+进行离子交换[17](式(7)),使得MFH对Pb2+吸附量显著增加。此外,静电吸附机制也存在于羟基磷灰石对Pb的吸附过程中,式(8)—式(11)展示了磁性羟基磷灰石的表面活性位点在溶液中表现出的缓冲特性。
MFH等电点为pHPZC为8.3,实验条件下,MFH颗粒表面均带正电荷,随着pH的升高,使MFH表面正电荷减少,一方面有利于Pb2+的吸附;另一方面水溶液中Pb2+的存在形态也会随之改变,随着pH的升高,OH–浓度逐渐增加,与Pb2+发生配位反应,形成Pb(OH)+~Pb(OH)42–等多羟基配位化合物或配位离子。OH–的配位竞争不仅减少了MFH对Pb2+的吸附,而且多羟基铅配位化合物的形成,增加了Pb(Ⅱ)的负电荷,使得带负电的MFH与Pb2+吸附力降低,从而使得MFH可吸附的Pb2+量减少[26]。因此,MFH作为吸附剂用于溶液中Pb的去除,适用于较低pH范围。而且pH低于5范围内发生了明显的吸附作用,暗示带正电的吸附剂与正电吸附质(Pb2+)之间不仅仅是简单的静电物理吸附,否则两者吸附作用理应很弱。
| $ {\text{S - OH}} + {\text{P}}{{\text{b}}^{2 + }} \to {\text{S - O - P}}{{\text{b}}^ + } + {{\text{H}}^ + } $ | (5) |
| $ {\text{S - OH}} + {\text{P}}{{\text{b}}^{2 + }} \to {\left( {{\text{S - O}}} \right)_{\text{2}}}{\text{ - Pb}} + 2{{\text{H}}^ + } $ | (6) |
| $ \begin{array}{l} {\text{C}}{{\text{a}}_{10}}{\left( {{\text{P}}{{\text{O}}_4}} \right)_6}{\left( {{\text{OH}}} \right)_2} + {\text{xP}}{{\text{b}}^{2 + }} \to \hfill \\ {\text{C}}{{\text{a}}_{10{\text{ - x}}}}{\text{P}}{{\text{b}}^{2 + }}{\text{x}}{\left( {{\text{P}}{{\text{O}}_4}} \right)_6}{\left( {{\text{OH}}} \right)_2} + {\text{xC}}{{\text{a}}^{2 + }} \hfill \\ \end{array} $ | (7) |
| $ \equiv {\text{FeOH}} + {{\text{H}}^ + } \leftrightarrow \equiv {\text{FeOH}}_2^ + $ | (8) |
| $ \equiv {\text{FeOH}} \leftrightarrow \equiv {\text{Fe}}{{\text{O}}^ - } + {{\text{H}}^ + } $ | (9) |
| $ \equiv {\text{P}}{{\text{O}}^ - } + {{\text{H}}^ + } \leftrightarrow \equiv {\text{PO}}{{\text{H}}^0} $ | (10) |
| $ \equiv {\text{CaOH}}_2^ + \leftrightarrow \equiv {\text{CaO}}{{\text{H}}^0} + {{\text{H}}^ + } $ | (11) |
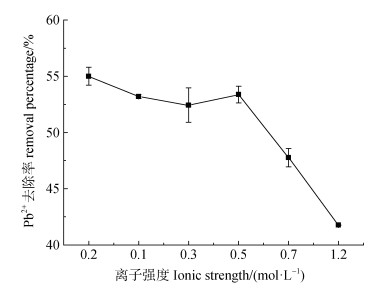
在温度为15℃、吸附时间为2 h、pH为5.00、初始Pb2+浓度625.63 μg·mL–1条件下,离子强度对Pb2+去除率的影响见图 4。可以看出,随着溶液体系中NaNO3浓度的增大,MFH对Pb2+的去除率明显降低。NaNO3浓度由0增到1.2 mol·L–1时,去除率由57.96%降至41.75%。可能原因有:(1)随溶液离子强度增加,Pb2+活度系数降低,从而阻碍了Pb2+从溶液体系扩散到MFH表面。(2)Pb2+被吸附后可能与MFH的活性位点形成外层表面配合物,而外加Na+能够吸附到外层表面活性位点,对MFH吸附Pb2+具有较大的抑制作用[21]。(3)随溶液离子强度增加,外加电解质离子压缩MFH扩散双电层厚度,削弱了MFH微粒间的静电排斥作用,使之发生团聚,从而使有效吸附位点数量减少。(4)MFH与Pb2+在水溶液中表现为静电吸引作用,随溶液离子强度增加,外加电解质离子逐渐包围MFH表面带相反电荷的吸附位点,部分中和吸附位点的电荷,造成吸附位点与Pb2+间的静电吸引作用削弱,不利于MFH吸附Pb2+[7]。
|
图 4 离子强度对MFH吸附溶液中Pb2+的影响 Fig. 4 Effect of ionic strength on Pb2+ adsorption in MFH solution |
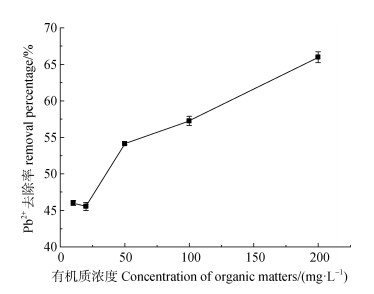
在天然水体系中,颗粒物质含有各种可以影响金属离子迁移和归宿的天然有机质(NOM),主要是腐殖质(HS),包括腐殖酸(HA)、富里酸(FA)等。有机质浓度对Pb2+去除率的影响见图 5,随腐殖酸浓度的增加,MFH对Pb2+的去除率呈上升趋势。腐殖酸浓度由0增至200 mg·L–1时,去除率由47.35%增至65.97%。由于HA结构既含有疏水基团又含有亲水基团[27],所以既能与疏水性物质结合,又能对重金属离子具有键合能力,从而HA与水环境中Pb2+络合,且自身吸附到MFH表面,从而增加了MFH对Pb2+的吸附量。此外,在HA存在时,MFH对Pb2+的键合程度在低pH时会上升,在高pH时会下降,本试验溶液体系为低pH=5.17,一定程度上能增强MFH对Pb2+的吸附作用。综上,有机质能增加溶液体系中MFH吸附Pb2+的量。
|
图 5 有机质浓度对MFH吸附溶液中Pb2+的影响 Fig. 5 Effect of organic matter concentration on Pb2+ in MFH adsorption solution |
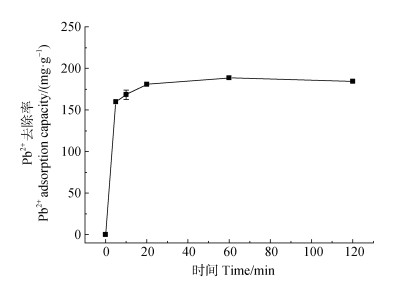
Pb2+在MFH上的动力吸附曲线见图 6。由图可知,MFH对Pb2+的吸附是快速反应过程,反应在前10 min吸附量随时间的增加快速增加,达168.26 mg·g–1,当反应时间超过10 min,吸附量几乎不再增加,达到了吸附平衡。在开始阶段,MFH表面的结合位点较多,其吸附速率较快;反应一段时间后由于Pb(Ⅱ)离子逐渐占据位置,结合位点减少使其吸附速率迅速降低,最后达到吸附平衡[23]。
|
图 6 MFH对溶液中Pb2+的动力学吸附模型 Fig. 6 Kinetic adsorption model of Pb2+ in solution by MFH |
为描述MFH对Pb2+的吸附动力学过程,采用准一级和准二级动力学模型对动力学数据进行拟合,分析吸附过程的机理和潜在的速率控制步骤。表 4中给出准一级动力学和准二级动力学拟合曲线的决定系数以及参数,其决定系数均大于0.993,其中准二级动力学拟合效果更好。准二级动力学方程是基于化学吸附,化学键是联系吸附剂与吸附质之间的桥梁,吸附剂的吸附能力取决于其表面的活性点位数量和性质,决定吸附过程的速率[24]。进一步证实Pb2+与MFH的相互作用主要是化学机制,而非简单的物理作用。
|
|
表 4 MFH对Pb2+的吸附动力学模型拟合 Table 4 Fitting results of kinetic adsorption model of Pb2+ by MFH |
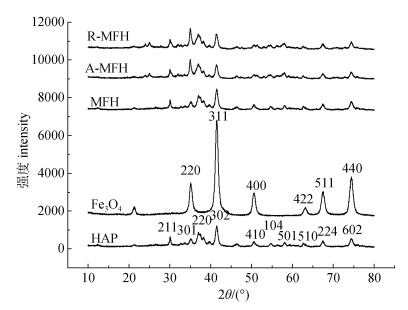
图 7显示了Fe3O4、HAP两种单体、复合材料MFH、吸附Pb2+的复合材料料A-MFH及其再生复合材料R-MFH的XRD光谱图,可以看出,Fe3O4和HAP的晶面与各自的标准谱图峰位一致,没有其他杂质峰,各个主峰强度均较高,表明试验制备得到的Fe3O4和HAP纯度较高且结晶性好[12]。将A-MFH衍射峰与标准卡片对比发现中含有Pb元素峰,且A-MFH所有的衍射峰均能与MFH的衍射峰相对应,说明MFH有效吸附了Pb。再生材料R-MFH的衍射特征峰与A-MFH一致,但铅元素的衍生峰降低,说明再生处理稀硝酸洗脱了大部分Pb2+,同时并未改变MFH的结构,因此再生材料R-MFH的性质稳定。
|
图 7 Fe3O4、HAP、MFH、A-MFH和R-MFH的X射线衍射光谱 Fig. 7 XRD spectrum of Fe3O4, HAP, MFH, A-MFH and R-MFH |
图 8分别为MFH、A-MFH以及R-MFH的SEM表征图片。从图 8a可以看出,经过共沉淀反应,MFH结构中球形Fe3O4与长条形HAP互相紧密附着,形成了粒径约为9 μm的团聚体。从图 8b可以看出,A-MFH有明显团聚现象,可能是MFH颗粒表面带有电荷,且电荷易集中在颗粒的尖角处,导致不同MFH颗粒共同结合Pb2+,而且吸附固定Pb2+后MFH颗粒间存在氢键产生桥接作用,也能够使颗粒发生团聚;从图 8c看,再生后R-MFH,团聚现象减弱,能清晰分辨出粒子形貌,表明经过再生MFH的性能有所恢复[7]。

|
图 8 MFH、A-MFH和R-MFH的扫描电镜图 Fig. 8 SEM micrographs of MFH, A-MFH and R-MFH |
磁性粒子的磁感应强度越大越容易从介质中被磁铁吸出,越有利于污染物质的去除修复[23]。经振动样品磁强计分析得到MFH、A-MFH以及R-MFH三种材料的饱和磁感应强度分别为33.36 emu·g–1、26.41 emu·g–1、27.45 emu·g–1,MFH在吸附Pb2+后,A-MFH饱和磁感应强度降低,再生后的R-MFH磁感应强度有小幅回升。MFH以及A-MFH和R-MFH的磁感应强度均高于目前研究的大部分超顺磁性材料[17,28],具有很好的磁响应能力和实际应用的潜力[7]。
通过对复合材料比表面积进行表征,得到MFH、A-MFH和R-MFH的比表面积分别为83.06 m2·g–1、71.87 m2·g–1与76.83 m2·g–1,对比目前研究的磁性材料,MFH及其再生材料均具有较大的比表面积[19,28],能提供给溶液中Pb2+更多的吸附位点,有利于Pb2+的吸附[26]和后续的循环利用。
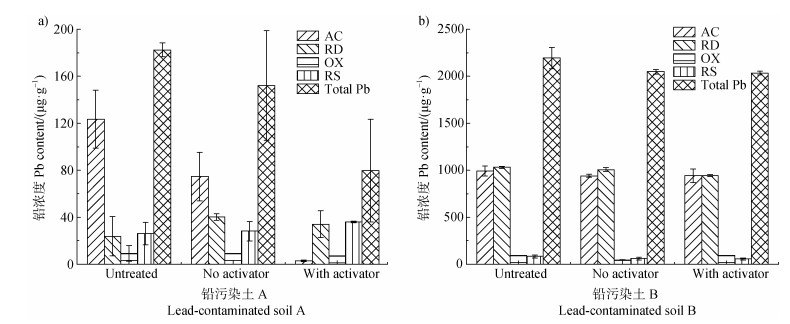
2.8 MFH对铅污染土壤的修复及活化剂的强化效果施用活化剂能打破重金属各形态的化学平衡,使重金属向有效态、水溶态转化,更易被修复剂去除,其中EDTA是土壤重金属修复中提取效率和使用率最高的一种螯合剂[29]。从图 9、表 5可以看出,MFH对农田铅污染土A和工业园区铅污染土B中的铅均有一定去除效果,去除量分别为30.43、145.60 μg·g–1;但MFH处理后的两类铅污染土中铅的含量均不满足铅污染风险筛选值限值。在添加EDTA的试验组中,污染土A、B中总铅去除量明显提高,分别提高至102.74、160.53 μg·g–1。污染土A中总铅含量从182.50 μg·g–1减至79.76μg·g–1,低于铅污染风险筛选值,重金属铅总量能够满足土壤质量标准要求。
|
图 9 铅污染土A、B在MFH处理前后铅形态含量 Fig. 9 Lead form content of lead-contaminated soils A and B before and after MFH treatment |
|
|
表 5 MFH对铅污染土壤的修复及活化剂的强化效果 Table 5 Remediation of lead-contaminated soil by MFH and strengthening effect of activator |
形态分析表明,污染土A中原始酸可溶态铅(AC)含量最高,污染土B中,AC和可还原态铅(RD)含量占比较高。修复过程中添加EDTA活化对形态含量影响较大,污染土A中AC铅含量从对照不加EDTA的74.64 μg·g–1降低至2.814 μg·g–1,污染土B中AC铅含量从对照的942.1 μg·g–1降低至939.42 μg·g–1,RD铅含量从对照的1 006.7 μg·g–1降低至945.1 μg·g–1(图 9)。在铅污染土中施用的EDTA能有效螯合交换态、碳酸盐结合态和氧化物结合态铅,显著增加土壤铅的有效态含量,而对移动能力和生物有效性、环境风险较低的有机态和残余态土壤铅的作用效果不明显[30]。与EDTA结合的铅离子主要通过与MFH发生配位体竞争吸附转变为MFH-Pb结合态,因而使土壤中的铅含量降低,两种理化性质不同的铅污染土在EDTA处理前后,MFH对铅的各形态处理效果有差异。
2.9 MFH的回收与再生不同磁场强度的磁棒条件下,MFH回收率如表 6。磁棒磁场强度越大,材料回收率越大,当磁场强度为4 000 G时,应用于污染土A和B中的MFH材料回收率分别为92.91%和96.23%。当磁棒磁场强度超过4 500 G时,MFH回收量超过施用量,原因是磁棒从土壤中吸附出的磁性物质除了吸附固定铅的MFH外,还有少量土壤中原有的磁性较强的原有磁性矿物,以及附着了MFH使得其可被吸出的磁性较弱的经磁性矿物化学风化产生的次生磁性矿物。综上,在外加磁场强度下,MFH的回收率高,同时根据再生性能试验以及表征结果得出MFH的重复利用率高,这有利于实现土壤中材料和重金属Pb2+的回收利用。
|
|
表 6 不同磁场强度对土壤中MFH回收率的影响 Table 6 Effects of different magnetic field strengths on the recovery of MFH in soil |
再生后的MFH质量损耗率(S)和性能恢复率(H)分别为2.70%和89.49%,S值越低,说明MFH的再生质量损失越小。H值越高,说明MFH的吸附能力恢复越好。稀硝酸洗脱液加入后,H+的存在,能将MFH上固定的Pb2+置换出来,但同时也可能破坏部分分子间稳定化学键结构以及导致Fe元素流失,造成MFH吸附性能略有减弱和质量损失。试验说明经硝酸洗脱液再生的MFH再生效果可观。
3 结论MFH材料对溶液中Pb2+的去除修复效果明显,在0~1 000 μg·mL–1铅含量范围内,MFH能有效、快速地去除溶液中的Pb2+。MFH对Pb2+是快速、多层的吸附过程,反应在10 min左右达到吸附平衡,平衡吸附量181.6 mg·g–1,MFH与Pb2+之间的相互作用主要是化学机制。MFH去除Pb2+适用于较低pH 2.00~5.00范围,溶液中有机质增加能有效提高MFH对Pb2+的吸附量,离子强度增大会抑制MFH对Pb2+的去除率。MFH纯度较高,结晶性较好,具有较大的比表面积,且MFH具有超顺磁性,利于回收,对于轻度铅污染土壤的修复具有较好的修复效果。添加EDTA活化剂后,MFH对土壤中总铅的吸附量明显提升。如何将取得的研究成果应用于实际修复体系中至关重要,对于MFH应用于污染土壤的原位修复仍然是研究的重点,需要后期不断的完善与探索。
| [1] |
Bao X C, Ma J Y, Xu W M, et al. Human bioavailability and health risk assessment of heavy metals in soils from a mining area of southwest China (In Chinese)[J]. Acta Pedologica Sinica, 2022. DOI:10.11766/trxb202107200287 [保欣晨, 马娇阳, 徐武美, 等. 西南某矿区土壤重金属的人体生物有效性及健康风险评估[J]. 土壤学报, 2022.]
(  0) 0) |
| [2] |
Abdolali A, Ngo H H, Guo W S, et al. A breakthrough biosorbent in removing heavy metals: Equilibrium, kinetic, thermodynamic and mechanism analyses in a lab-scale study[J]. Science of the Total Environment, 2016, 542: 603-611. DOI:10.1016/j.scitotenv.2015.10.095
(  0) 0) |
| [3] |
Yuan S J, Zhang P, Yang Z Y, et al. Successive grafting of poly(hydroxyethyl methacrylate)brushes and melamine onto chitosan microspheres for effective Cu(Ⅱ)uptake[J]. International Journal of Biological Macromolecules, 2018, 109: 287-302. DOI:10.1016/j.ijbiomac.2017.12.063
(  0) 0) |
| [4] |
Tan X P, He J H, Guo Z M, et al. Research progresses on soil enzymes as indicators of soil health and their responses to heavy metal pollution (In Chinese)[J]. Acta Pedologica Sinica, 2022. DOI:10.11766/trxb202107240275 [谭向平, 何金红, 郭志明, 等. 土壤酶对重金属污染的响应及指示研究进展[J]. 土壤学报, 2022.]
(  0) 0) |
| [5] |
Albadarin A B, Mangwandi C, Al-Muhtaseb A H, et al. Kinetic and thermodynamics of chromium ions adsorption onto low-cost dolomite adsorbent[J]. Chemical Engineering Journal, 2012, 179: 193-202. DOI:10.1016/j.cej.2011.10.080
(  0) 0) |
| [6] |
Lin A H, Wan T, Ding Y, et al. Structure and heavy metal ion adsorptions of Fe3O4/MLS composite polymer adsorbents (In Chinese)[J]. China Plastics Industry, 2022, 50(3): 44-48. [林安鸿, 万涛, 丁毅, 等. Fe3O4/MLS复合聚合物吸附树脂的结构及其重金属离子吸附性能[J]. 塑料工业, 2022, 50(3): 44-48.]
(  0) 0) |
| [7] |
Zhang L Z, Yi P, Fang D D, et al. Adsorption mechanism of cadmium by superparamagnetic nano-Fe3O4@SiO2 functionalized materials (In Chinese)[J]. Environmental Science, 2021, 42(6): 2917-2927. [张立志, 易平, 方丹丹, 等. 超顺磁性纳米Fe3O4@SiO2功能化材料对镉的吸附机制[J]. 环境科学, 2021, 42(6): 2917-2927.]
(  0) 0) |
| [8] |
Pu S Y, Xiao Y T, Ma H, et al. Adsorption behavior and mechanism of heavy metal ions in water by CS-EGDE/Fe3O4 gel microspheres (In Chinese)[J]. Acta Scientiae Circumstantiae, 2019, 39(7): 2172-2181. [蒲生彦, 肖雨婷, 马慧, 等. CS-EGDE/Fe3O4凝胶微球对水中重金属离子的吸附性能及机理研究[J]. 环境科学学报, 2019, 39(7): 2172-2181.]
(  0) 0) |
| [9] |
Liu G F, Liao L, Dai Z M, et al. Organic adsorbents modified with citric acid and Fe3O4 enhance the removal of Cd and Pb in contaminated solutions[J]. Chemical Engineering Journal, 2020, 395: 125108. DOI:10.1016/j.cej.2020.125108
(  0) 0) |
| [10] |
Shabani E, Salimi F, Jahangiri A. Removal of arsenic and copper from water solution using magnetic iron/bentonite nanoparticles(Fe3O4/bentonite)[J]. Silicon, 2019, 11(2): 961-971. DOI:10.1007/s12633-018-9895-z
(  0) 0) |
| [11] |
Feng J Y, Zhang J, Song W F, et al. An environmental-friendly magnetic bio-adsorbent for high-efficiency Pb(Ⅱ)removal: Preparation, characterization and its adsorption performance[J]. Ecotoxicology and Environmental Safety, 2020, 203: 111002. DOI:10.1016/j.ecoenv.2020.111002
(  0) 0) |
| [12] |
Dong L J, Zhu Z L, Qiu Y L, et al. Removal of lead from aqueous solution by hydroxyapatite/magnetite composite adsorbent[J]. Chemical Engineering Journal, 2010, 165(3): 827-834. DOI:10.1016/j.cej.2010.10.027
(  0) 0) |
| [13] |
Ministry of Ecology and Environment of the People's Republic of China, State Administration for Market Regulation. Soil environmental quality Risk control standard for soil contamination of agricultural land: GB 15618—2018[S]. Beijing: Standards Press of China, 2018: 13.[生态环境部, 国家市场监督管理总局. 土壤环境质量农用地土壤污染风险管控标准: GB 15618—2018[S]. 北京: 中国标准出版社, 2018: 13.]
(  0) 0) |
| [14] |
Ministry of Ecology and Environment of the People's Republic of China, State Administration for Market Regulation. Soil environmental quality Risk control standard for soil contamination of development land: GB 36600—2018[S]. Beijing: Standards Press of China, 2018: 13.[生态环境部, 国家市场监督管理总局. 土壤环境质量建设用地土壤污染风险管控标准: GB 36600—2018[S]. 北京: 中国标准出版社, 2018: 13.]
(  0) 0) |
| [15] |
Fang D D, Zhang L Z, Wang Q. Effects of superparamagnetic nanomaterials on soil microorganisms and enzymes in cadmium-contaminated paddy fields (In Chinese)[J]. Environmental Science, 2021, 42(3): 1523-1534. [方丹丹, 张立志, 王强. 超顺磁性纳米材料对镉污染稻田土壤微生物和酶的影响[J]. 环境科学, 2021, 42(3): 1523-1534.]
(  0) 0) |
| [16] |
Qureshi A A, Kazi T G, Baig J A, et al. Exposure of heavy metals in coal gangue soil, in and outside the mining area using BCR conventional and vortex assisted and single step extraction methods. Impact on orchard grass[J]. Chemosphere, 2020, 255: 126960. DOI:10.1016/j.chemosphere.2020.126960
(  0) 0) |
| [17] |
Li R F, Liu Y Q, Lan G H, et al. Pb(Ⅱ)adsorption characteristics of magnetic GO-hydroxyapatite and the contribution of GO to enhance its acid resistance[J]. Journal of Environmental Chemical Engineering, 2021, 9(4): 105310. DOI:10.1016/j.jece.2021.105310
(  0) 0) |
| [18] |
Liu J Y, Hu C W, Huang Q G. Adsorption of Cu2+, Pb2+, and Cd2+ onto oiltea shell from water[J]. Bioresource Technology, 2019, 271: 487-491. DOI:10.1016/j.biortech.2018.09.040
(  0) 0) |
| [19] |
Fan S L, Huang Z Q, Zhang Y J, et al. Magnetic chitosan-hydroxyapatite composite microspheres: Preparation, characterization, and application for the adsorption of phenolic substances[J]. Bioresource Technology, 2019, 274: 48-55. DOI:10.1016/j.biortech.2018.11.078
(  0) 0) |
| [20] |
Saravanan P, Vinod V T P, Sreedhar B, et al. Gum kondagogu modified magnetic nano-adsorbent: An efficient protocol for removal of various toxic metal ions[J]. Materials Science & Engineering: C, 2012, 32(3): 581-586.
(  0) 0) |
| [21] |
Badruddoza A Z M, Shawon Z B Z, Tay W J D, et al. Fe3O4/cyclodextrin polymer nanocomposites for selective heavy metals removal from industrial wastewater[J]. Carbohydrate Polymers, 2013, 91(1): 322-332. DOI:10.1016/j.carbpol.2012.08.030
(  0) 0) |
| [22] |
Liu J F, Zhao Z S, Jiang G B. Coating Fe3O4 magnetic nanoparticles with humic acid for high efficient removal of heavy metals in water[J]. Environmental Science & Technology, 2008, 42(18): 6949-6954.
(  0) 0) |
| [23] |
Tang Y L, Liang S, Wang J T, et al. Amino-functionalized core-shell magnetic mesoporous composite microspheres for Pb(Ⅱ)and Cd(Ⅱ)removal[J]. Journal of Environmental Sciences, 2013, 25(4): 830-837. DOI:10.1016/S1001-0742(12)60141-7
(  0) 0) |
| [24] |
Khawar A, Aslam Z, Zahir A, et al. Synthesis of Femur extracted hydroxyapatite reinforced nanocomposite and its application for Pb(Ⅱ)ions abatement from aqueous phase[J]. International Journal of Biological Macromolecules, 2019, 122: 667-676. DOI:10.1016/j.ijbiomac.2018.10.223
(  0) 0) |
| [25] |
Thanh D N, Novák P, Vejpravova J, et al. Removal of copper and nickel from water using nanocomposite of magnetic hydroxyapatite nanorods[J]. Journal of Magnetism and Magnetic Materials, 2018, 456: 451-460. DOI:10.1016/j.jmmm.2017.11.064
(  0) 0) |
| [26] |
Song S, Liu Z, Zhang J, et al. Synthesis and adsorption properties of novel bacterial cellulose/graphene oxide/attapulgite materials for Cu and Pb ions in aqueous solutions[J]. Materials, 2020, 13(17): 3703. DOI:10.3390/ma13173703
(  0) 0) |
| [27] |
Shen S Y, Huang Y, Wang W Q, et al. Study on adsorption behavior of Sb(Ⅴ)by ferrihydrite and its humic acid complex (In Chinese)[J]. Acta Scientiae Circumstantiae, 2019, 39(12): 4015-4021. [申思月, 黄阳, 王维清, 等. 水铁矿及其腐殖酸复合体对Sb(Ⅴ)的吸附行为研究[J]. 环境科学学报, 2019, 39(12): 4015-4021.]
(  0) 0) |
| [28] |
Gómez-Pastora J, Bringas E, Ortiz I. Recent progress and future challenges on the use of high performance magnetic nano-adsorbents in environmental applications[J]. Chemical Engineering Journal, 2014, 256: 187-204. DOI:10.1016/j.cej.2014.06.119
(  0) 0) |
| [29] |
Wu J M, Guo S R, Zhu M Y, et al. Application research progress of EDTA in the ecological restoration of heavy metals in soil (In Chinese)[J]. Inner Mongolia Forestry Investigation and Design, 2016, 39(5): 137—140, 15. [吴佳美, 郭实荣, 朱梦银, 等. EDTA在土壤重金属生态修复中应用研究进展[J]. 内蒙古林业调查设计, 2016, 39(5): 137—140, 15.]
(  0) 0) |
| [30] |
Feng J, Zhang Z Q, Li N, et al. Washing of heavy metal contaminated soil around a lead-zinc smelter by several chelating agents and the leached soil utilization (In Chinese)[J]. Chinese Journal of Environmental Engineering, 2015, 9(11): 5617-5625. [冯静, 张增强, 李念, 等. 铅锌厂重金属污染土壤的螯合剂淋洗修复及其应用[J]. 环境工程学报, 2015, 9(11): 5617-5625.]
(  0) 0) |
 2023, Vol. 60
2023, Vol. 60


