2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
砖红壤是在热带季风气候条件下经历高度富铁铝化过程形成的一类土壤,主要分布在我国广东雷州半岛和海南岛北部[1]。由于风化过程中形成大量的铁铝氧化物,对阴阳离子有较强的吸附和富集能力,因此砖红壤中Cr、Cu、Co、Ni等重金属含量普遍高于其他类型土壤[2]。Cr是一种有致畸致癌作用的污染物,土壤中Cr含量通常在15~100 mg·kg–1之间[3]。但在广东雷州半岛玄武岩发育的砖红壤中,Cr的含量可高达430 mg·kg–1 [4]。有研究表明这类土壤中Cr主要存在于矿物中,活性很低,如使用电子探针(Electron probe micro-analysis,EPMA)对采集的玄武岩岩石和砖红壤进行扫描,可观察到铬铁矿等含铬矿物[4]。然而,土壤发生酸化、氧化还原和有机酸的络合作用等可能会破坏矿物结构,导致Cr等重金属的活化和溶出,引发生态和环境风险[5]。因此,有必要研究Cr背景值较高的砖红壤中Cr与土壤组分的结合状态和溶出情况。
土壤中的Cr主要以Cr(Ⅲ)和Cr(Ⅵ)存在,Cr(Ⅲ)在pH > 4的环境中开始沉淀,中性条件几乎完全沉淀[6],在土壤中活性较低。Cr(Ⅵ)的活性较高,在土壤中以含氧酸根阴离子的形态存在,如CrO42–,酸性富铁铝土壤中易被吸附,碱性土壤中保持高度活性[7]。Cr(Ⅲ)不能穿过细胞膜,生物对其利用率低,因此一般认为Cr(Ⅲ)的环境风险较低[8]。然而,一旦Cr(Ⅲ)被氧化为Cr(Ⅵ),其毒性将增加100倍[9-10]。研究发现,Cr(Ⅲ)能吸附到高价锰氧化物的表面,然后被氧化为Cr(Ⅵ)并释放到溶液中,该过程受到锰氧化物含量、溶液pH等因素的影响[11]。砖红壤中含有较多的高价锰氧化物,如水钠锰矿、锂硬锰矿等[12],可将Cr(Ⅲ)氧化为Cr(Ⅵ),增加Cr的环境风险。然而,目前的研究主要集中于锰氧化物矿物对Cr(Ⅲ)的氧化作用,对实际土壤体系中氧化锰与Cr(Ⅲ)反应的研究报道较少。
为了解Cr在砖红壤中的溶出和转化,本文研究了不同浓度的盐酸和柠檬酸对砖红壤中Cr的溶解作用,利用电子探针技术进一步观察Cr的结合形态,并采用染毒老化法研究外源Cr(Ⅲ)在砖红壤中的氧化。研究结果可为砖红壤中的Cr的风险评估提供参考。
1 材料与方法 1.1 土壤的采集和理化性质分析供试的17种砖红壤均由玄武岩发育,其中1种采自云南昆明,6种采自海南岛北部,10种采自广东雷州半岛,均为农田土壤。海南岛北部和雷州半岛是我国玄武岩发育砖红壤的主要分布区域。除去土壤表面的覆盖物后,取0~20 cm的表层土壤,自然风干,磨碎过60目筛备用。
按1︰2.5的土水比制备土壤悬液,振荡30 min后使用pH计测定土壤pH。使用重铬酸钾氧化法测定土壤有机质含量。连二亚硫酸钠-柠檬酸钠-重碳酸钠提取法(Dithionite–citrate–bicarbonate,DCB)用于提取土壤游离铁、铝、锰氧化物,电感耦合等离子体发射光谱仪测定提取液中铁、铝、锰的含量。采用醋酸铵法测定土壤阳离子交换量(Cation exchange capacity,CEC)[13]。称取5.0 g风干土于500 mL三角瓶中,加入200 mL含1 mol·L–1醋酸铵和0.2%氢醌(pH 5.5)的混合溶液提取土壤易还原性锰[14]。将悬液在室温下振动5 h,离心、过滤,用火焰原子吸收光谱法测定提取液中的锰。使用HF- HClO4-HNO3消煮提取土壤总Cr[13],碱性消解法提取土壤Cr(Ⅵ)[15],火焰原子吸收光谱法测定提取液中Cr和Cr(Ⅵ)的含量。
1.2 Cr的溶出实验选择海南3和广东9两种砖红壤进行Cr的溶出实验。称取0.5 g土壤样品于50 mL的离心管中,按土/水比1︰20分别加入不同浓度的盐酸溶液(0.002、0.004、0.1、0.2、0.4、0.6、0.8、1.0 mol·L–1)和柠檬酸溶液(1、5、10、50、100 mmol·L–1)。在25℃下恒温振荡24 h,振荡结束后测定悬液pH。混合物以4 500 r·min–1的速度离心,上清液过0.45 µm滤膜,用火焰原子吸收光谱法测定溶液中的Cr。所用处理均设置2次重复,根据2次重复的结果计算平均值和标准差。
1.3 铁铝氧化物结合态Cr和有机结合态Cr的提取用DCB法溶解土壤铁铝氧化物,提取与铁铝氧化物结合态Cr。具体步骤如下:称取0.5 g土壤样品于50 mL离心管中,加0.3 mol L–1柠檬酸钠20 mL、1 mol·L–1重碳酸钠2.5 mL,水浴加热至80℃,加0.5 g连二亚硫酸钠,不断搅拌15 min;土壤悬液离心、过滤,滤液收集于100 mL的容量瓶中,在残渣中加入10 mL 1 mol·L–1 NaCl,搅拌均匀后再次离心过滤,滤液合并至容量瓶中,该步骤重复三次,最终定容至100 mL。用火焰原子吸收光谱法测定提取液中的Cr。
参考Tessier等五步提取法[16]中有机结合态Cr的提取方法提取土壤有机结合态Cr,在上述DCB处理的残渣中加入5 mL 30% H2O2溶液(pH 2.0),在水浴锅中加热至85℃并维持2 h;再加入5 mL 30% H2O2溶液,继续在85℃水浴锅中加热至蒸干,冷却后,加入5 mL 3.2 mol·L–1醋酸铵,添加20%(V/V)的硝酸溶液使总体积为20 mL,振荡30 min。混合物离心、过滤,滤液收集于25 mL容量瓶中并定容。用火焰原子吸收光谱法测定溶液中的Cr。
1.4 扫描电镜与微区能谱分析用扫描电镜和电子探针微区分析法分别观测广东6砖红壤的形貌并分析土壤元素组成。样品经过Gatan G2树脂包埋处理后抛光,表面喷碳提高导电性。使用JEOL扫描电镜(JXA-8530F PLUS,日本),加速电压15 kV,探针电流为15~20 nA,探针直径为1 μm,面扫描停留时间15 s,Kα线用作所有确定元素的分析线。
1.5 砖红壤中外源Cr(Ⅲ)氧化实验分别称取广东6和广东10砖红壤样品90 g于烧杯中,添加9 mL 200 mmol·L–1的Cr(NO3)3溶液,使外源Cr(Ⅲ)浓度达到20 mmol·kg–1。以不加Cr(Ⅲ)的处理为对照,用去离子水调节土壤含水量至30%,混匀后在25℃下恒温培养。分别在1、3、7、14、28、42 d取土样,用碱式消解法提取Cr(Ⅵ),0.1 mol·L–1 CaCl2提取Mn(Ⅱ)。用二苯碳酰二肼比色法测定提取液中Cr(Ⅵ)含量,火焰原子吸收光谱法测定提取液中Mn(Ⅱ)含量。
对广东6和广东10砖红壤进行去除有机质处理,称取约50 g土样,加入约100 mL的30% H2O2,在水浴锅中加热至85℃并维持至蒸干,该步骤重复3次。将H2O2处理过的土壤在烘箱中低温(40℃)烘干、磨细、过60目筛。此时广东6和广东10砖红壤有机质含量分别由23.75和30.51 g·kg–1降为5.73和4.84 g·kg–1。
采用一次平衡法研究Cr(Ⅲ)在去有机质砖红壤中的氧化转化。准确称取上述土壤0.5 g,按土液比1︰40加入1 mmol·L–1的Cr(NO3)3溶液,其中含有0.05 mol·L–1的NaAc作为pH缓冲剂以维持反应过程中pH基本恒定[17]。使用HNO3和NaOH溶液分别将悬液的pH调节至4.0、4.5、5.0、5.5和6.0。置于25℃的环境中恒温振荡12 h后测定pH,与初始pH值差异控制在±0.1以内。将土壤悬液以4 500 r·min–1的速度离心,过滤后滤液收集于容量瓶中。残渣中加入P浓度为0.1 mol·L–1的K2HPO4-KH2PO4(pH 6.5)提取液,继续振荡12 h,解吸土壤固相上吸附的Cr(Ⅵ)和Mn(Ⅱ)。悬液离心后过0.45 µm滤膜,滤液合并于上述容量瓶中。分别用二苯碳酰二肼比色法和火焰原子吸收光谱法测定溶液中Cr(Ⅵ)和Mn(Ⅱ)的含量。另取一份土壤样品做空白实验,将Cr(NO3)3溶液更换为去离子水,其余步骤相同。上述添加Cr(Ⅲ)处理的结果扣除空白处理的结果即为Cr(Ⅵ)和Mn(Ⅱ)净产生量。
向去除有机质的广东6和广东10砖红壤中分别添加0、0.2、0.4、0.8和1.0 g·kg–1无定形MnO2(国药集团,上海),研究添加外源氧化锰对土壤中Cr(Ⅲ)氧化转化的影响。实验步骤与上述去有机质砖红壤中Cr(Ⅲ)氧化转化步骤相同,悬液pH设定为4.5。
所有实验处理均设置2次重复,并加入一种标准样品(GBW07405)进行质量控制,计算2次重复处理的平均值及标准差。
1.6 统计分析利用SPSS 26.0和EXCEL 2016进行数据分析和图表绘制。
2 结果与讨论 2.1 砖红壤理化性质采集的17种砖红壤基本性质列于表 1中。土壤pH为4.77~6.73,整体呈酸性。土壤有机质含量为10.39~33.06 g·kg–1,CEC含量为62.70~168.56 mmol·kg–1。土壤游离氧化铁、游离氧化铝和游离氧化锰的含量分别在91.04~170.59、10.11~24.19、0.93~7.95 g·kg–1范围内。砖红壤易还原性锰的含量在0.15~4.36 g·kg–1之间,相比于其他类型土壤砖红壤易还原锰含量较高[17-18]。供试的17种砖红壤总Cr含量在1.56~13.17 mmol·kg–1范围内(表 1)。除云南砖红壤外,广东和海南的16种砖红壤总Cr含量均超过土壤环境质量农用地土壤污染风险管控标准(GB15618—2018)中规定的风险筛选值(2.88 mmol·kg–1),说明这16种砖红壤中Cr的背景含量高。在17种砖红壤中Cr(Ⅵ)和水溶性Cr均未检出,说明土壤中的Cr主要以Cr(Ⅲ)存在,并且几乎不以游离态存在。
|
|
表 1 17种玄武岩发育砖红壤的基本性质 Table 1 Basic physicochemical properties of 17 latosols |
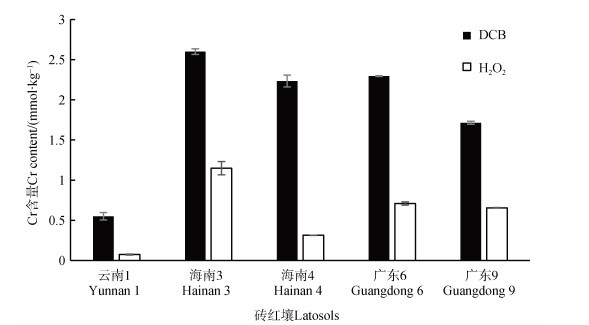
为研究砖红壤中Cr的结合形态,选择了5种总Cr含量不同的砖红壤(云南1、海南3、海南4、广东6和广东9),使用DCB法和H2O2法分别提取与土壤铁铝锰氧化物和有机物结合的Cr,结果如图 1所示。5种土壤中DCB提取Cr含量分别占土壤总Cr含量的35.30%、26.04%、37.04%、17.43%和42.98%,与土壤总Cr含量显著相关(r = 0.65,P < 0.05)。有机结合态Cr分别占总Cr含量的4.76%、11.51%、5.20%、5.38%和16.42%,与土壤总Cr含量相关性不显著。
|
图 1 云南1、海南3、海南4、广东6和广东9砖红壤中可被DCB法和H2O2法提取的Cr含量 Fig. 1 Contents of Cr in latosols of Yunnan 1, Hainan 3, Hainan 4, Guangdong 6 and Guangdong 9 extracted by DCB and H2O2 |
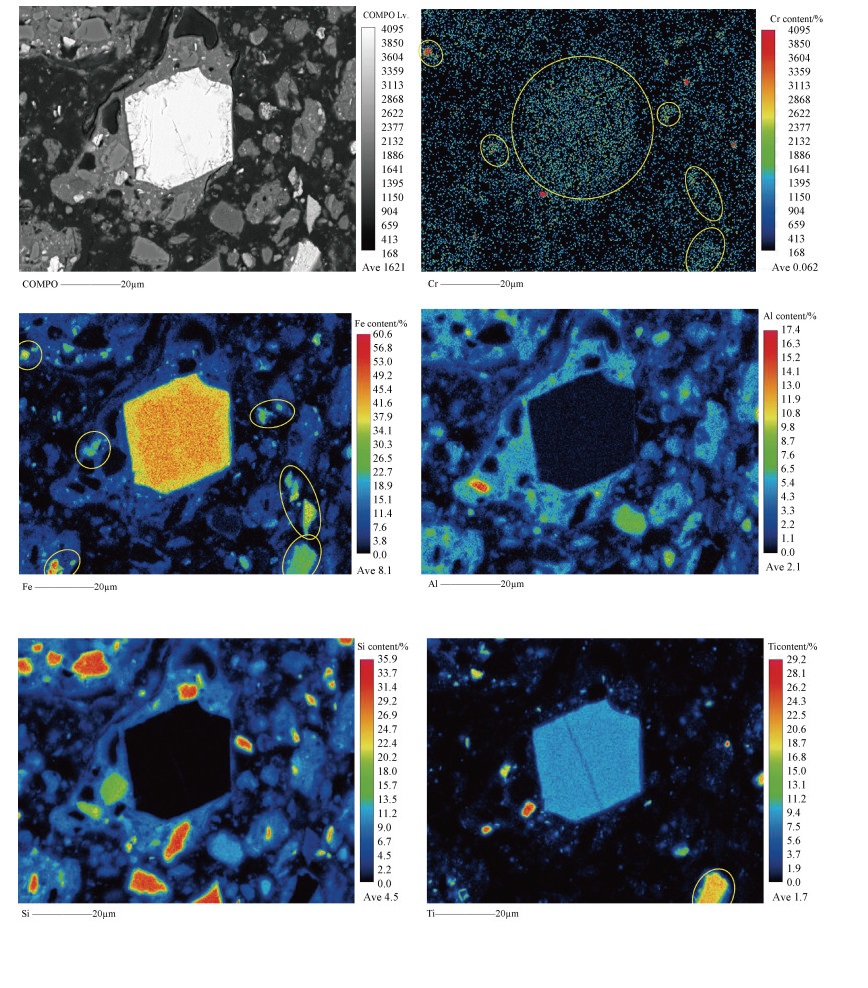
图 1结果表明砖红壤中与氧化物和有机物结合态Cr是Cr的重要存在形态。选择Cr含量最高的广东6砖红壤进行电子探针分析,结果显示,Cr与Fe的相关性良好(图 2),表明砖红壤中的Cr与Fe结合紧密。前人研究发现,铬铁矿(铬尖晶石)和铬磁铁矿是广东砖红壤中Cr的主要存在形态[4]。Cr3+与Fe3+半径相近,在土壤风化过程中Cr3+可与铁氧化物矿物晶格中的Fe3+发生同晶替换,进入铁氧化物矿物中。图 2结果还表明,砖红壤中含有一定量的与铁氧化物结合的Ti,部分Cr与含钛矿物相结合。这与Soubrand-Colin等[19]的研究类似,其扫描电子探针结果显示玄武岩发育的安第斯土壤中钛磁铁矿与Cr的分布重合,也可能是Cr的载体之一。此外,在蛇纹石发育的土壤和玄武岩发育的砖红壤中观察到一部分Cr3+替换硅酸盐矿物中的Al3+,进入该类矿物晶格中,橄榄石和绿泥石也是砖红壤中Cr的重要宿主[4,20]。
|
图 2 电子探针(EPMA)面扫描范围内广东6砖红壤Cr、Fe等元素的分布情况(COMPO:背散射,Ave:平均值) Fig. 2 Mappings of interesting elements obtained by EPMA in the latosol of Guangdong 6(COMPO: backscattered component, Ave: average) |
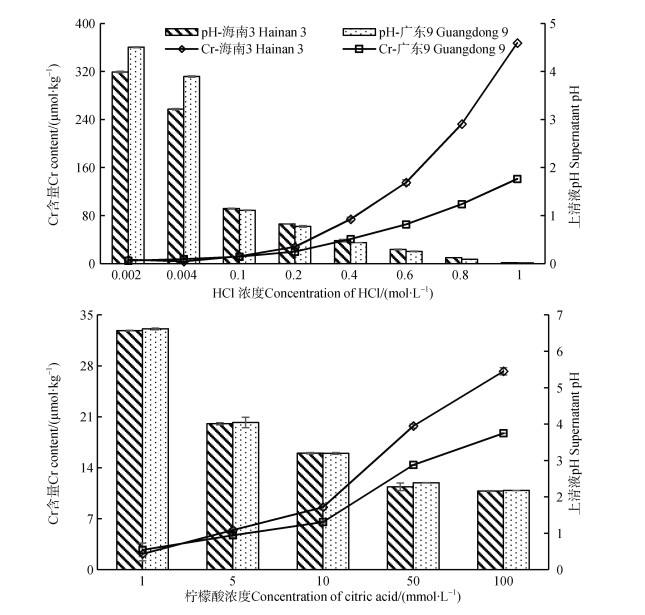
选择海南3和广东9两种Cr含量差异较大的砖红壤研究其在不同浓度的盐酸和柠檬酸中的溶解反应,探讨Cr的溶出风险,结果如图 3所示。海南3的总Cr含量较高,溶解的Cr含量总体上高于广东9。随着盐酸浓度的增加,两种土壤中Cr的溶解量由4.82和6.67 µmol·kg–1分别上升至367.63和141.22 µmol·kg–1,Cr溶解量的增加主要由于Cr的酸溶解作用所致。虽然土壤总Cr含量较高,但即使1 mol·L–1 HCl与土壤反应24 h,Cr的溶解量也仅占土壤总Cr含量的3.68%和3.54%。自然环境中,土壤pH通常在4.0以上,从图中结果可以看出在这一pH条件下,2种土壤中Cr的溶出量仅分别为4.82和7.50 µmol·kg–1,占总Cr含量的0.05%和0.19%。
|
图 3 不同浓度盐酸和柠檬酸处理后海南3和广东9砖红壤中Cr的溶出量和上清液pH Fig. 3 Content of Cr and supernatant pH in latosols of Hainan 3 and Guangdong 9 extracted by hydrochloric acid and citric acid with various concentrations |
不同浓度的柠檬酸与海南3和广东9砖红壤作用后Cr的溶解量由2.16和2.72 µmol·kg–1上升至27.25和18.73 µmol·kg–1(图 3)。在柠檬酸体系中土壤Cr的溶液作用是酸溶解与络合溶解共同作用的结果,当柠檬酸初始浓度为5 mmol·L–1时,土壤溶液pH约为4.0,此时海南3和广东9两种砖红壤Cr的溶出量分别为5.43和4.71 µmol·kg–1,其溶出量也非常低。土壤有机酸主要来源于植物根系分泌、土壤有机物分解和微生物代谢,其浓度通常很低,在0~1 mmol·L–1范围内[21]。
土壤Cr在无机酸和有机酸中的溶解结果说明砖红壤中背景Cr的溶出风险很低,主要原因是这些Cr主要以Cr(Ⅲ)存在于土壤固相中,与土壤铁铝氧化物和矿物牢固地结合在一起,呈非活化状态。
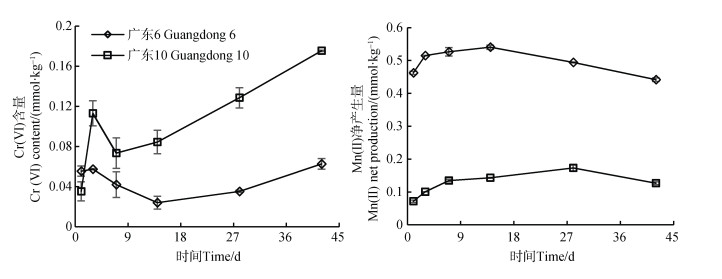
2.4 外源Cr(Ⅲ)在砖红壤中的氧化转化砖红壤锰氧化物含量较高,存在对Cr(Ⅲ)的氧化并使其转化为活性较高的Cr(Ⅵ)的风险。选择了两种易还原性锰含量差异较大的广东6和广东10砖红壤研究Cr(Ⅲ)在土壤中的氧化转化。添加Cr(Ⅲ)染毒并培养42 d期间Cr的转化量和Mn(Ⅱ)的净生成量如图 4所示。Cr(Ⅵ)的生成量随着培养时间的增加而增加,说明外源添加的Cr(Ⅲ)在土壤中发生了氧化反应,Mn(Ⅱ)的生成说明土壤氧化锰是导致Cr(Ⅲ)氧化转化的主要氧化剂。但Cr(Ⅵ)在广东6和广东10砖红壤中最高Cr(Ⅵ)净产生量仅占Cr(Ⅲ)添加量的0.31%和0.87%,说明Cr(Ⅲ)在砖红壤中的氧化转化很难发生。
|
图 4 两种砖红壤中Cr(Ⅵ)含量和Mn(Ⅱ)净产生量随时间的变化 Fig. 4 Contents of Cr(Ⅵ)and net production of Mn(Ⅱ)in latosols during a 42-day incubation |
比较2种砖红壤中Cr(Ⅲ)的氧化转化,总体上广东10砖红壤中产生的Cr(Ⅵ)高于广东6砖红壤,与这2种土壤易还原锰含量大小相反(表 1),也与土壤中Mn(Ⅱ)的产生量的大小顺序相反。主要原因是广东10砖红壤有机质含量(30.51 g·kg–1)高于广东6砖红壤(23.75 g·kg–1),可使部分氧化产生的Cr(Ⅵ)重新还原成Cr(Ⅲ)并固定在土壤中。
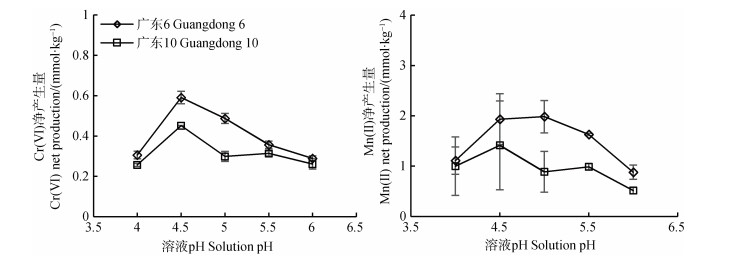
为消除土壤有机质对Cr(Ⅲ)氧化的影响,对土壤进行了去除有机质处理,然后采用一次平衡法研究了Cr(Ⅲ)在土壤中的氧化。一次平衡法的结果如图 5所示。整体上,广东6砖红壤中Cr(Ⅵ)和Mn(Ⅱ)的净产生量高于广东10,与土壤中易还原锰的含量大小一致。这一结果也进一步说明,土壤有机质可以将氧化生成的Cr(Ⅵ)再还原为Cr(Ⅲ)。随着反应pH的上升,Cr(Ⅲ)的氧化量先增加后下降。Cr(Ⅲ)氧化为Cr(Ⅵ)是一个产生H+的过程:
| $ \mathrm{Cr}^{3+}+1.5 \mathrm{MnO}_2(\mathrm{~s})+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{HCrO}_4^{-}+1.5 \mathrm{Mn}^{2+}+\mathrm{H}^{+} \\ \mathrm{Cr}^{3+}+1.5 \mathrm{MnO}_2(\mathrm{~s})+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{CrO}_4^{2-}+1.5 \mathrm{Mn}^{2+}+2 \mathrm{H}^{+} $ |
|
图 5 平衡溶液pH对去有机质砖红壤氧化Cr(Ⅲ)的影响 Fig. 5 Effect of equilibrium solution pH on oxidation of Cr(Ⅲ)in latosols with organic matters removed |
理论上,pH上升有利于该氧化反应的正向进行。然而,Cr(Ⅲ)在pH≈3时开始逐渐沉淀,随着pH上升至5,Cr(Ⅲ)几乎完全沉淀在土壤表面,活性较低[22],不易与同为固体的锰氧化物反应,因此氧化产生的Cr(Ⅵ)随体系pH的进一步升高呈现下降趋势[23]。
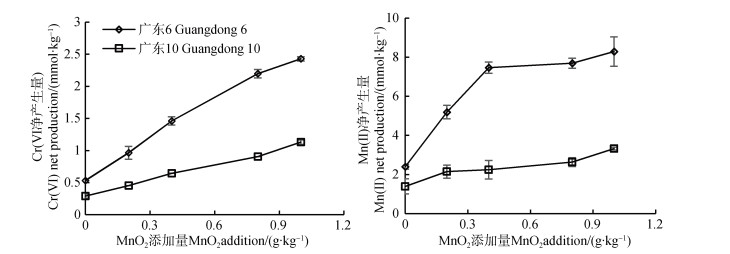
向去除有机质的2种砖红壤中添加人工合成的MnO2,然后再进行Cr(Ⅲ)氧化转化实验,结果如图 6所示。2种土壤中Cr(Ⅵ)和Mn(Ⅱ)的产生量与均与外源添加的MnO2量呈显著正相关(P < 0.05),进一步证明土壤易还原锰是Cr(Ⅲ)的主要氧化剂。外源Cr(Ⅲ)的添加量为40 mmol·kg–1,添加1 g·kg–1的MnO2时,两种砖红壤中由Cr(Ⅲ)氧化生成的Cr(Ⅵ)分别为2.42和1.13 mmol·kg–1,Cr(Ⅲ)氧化量仅占Cr(Ⅲ)添加量的6.05%和2.83%,进一步说明砖红壤中Cr(Ⅲ)不易发生氧化转化。因此,MnO2和Cr(Ⅲ)的含量不是影响Cr(Ⅲ)氧化转化的主要因素,Cr(Ⅲ)的氧化转化主要决定于Cr(Ⅲ)在土壤中的活性[11]。
|
图 6 添加MnO2对去有机质砖红壤氧化Cr(Ⅲ)的影响 Fig. 6 Effect of adding MnO2 on oxidation of Cr(Ⅲ)in latosols with organic matters removed |
虽然在一次平衡法和42 d的染毒老化实验中均观察到了Cr(Ⅲ)的氧化,但Cr(Ⅲ)的氧化转化量在总Cr(Ⅲ)添加量中的占比很小。砖红壤有机质通常较高,对Cr(Ⅵ)有强烈的还原和固定作用,因此砖红壤中外源Cr(Ⅲ)的实际氧化量可能更少。此外,以溶液形式添加到土壤中的Cr(Ⅲ)较砖红壤中与矿物结合的Cr(Ⅲ)更易利用,土壤中原有的Cr(Ⅲ)较外源添加的Cr(Ⅲ)更难氧化转化。因此,虽然砖红壤中Cr的背景值较高,但其主要以Cr(Ⅲ)存在于土壤固相中,很难溶解并发生氧化转化,其潜在风险较低。
3 结论本文研究了砖红壤中Cr的结合形态和溶出规律,探讨了外源添加Cr(Ⅲ)在砖红壤中的氧化转化,分析了砖红壤中Cr释放和氧化转化可能引起的潜在环境风险,主要结论如下:(1)砖红壤中的Cr主要与铁氧化物和硅酸盐矿物结合,酸化和络合作用虽能促进Cr的溶解,但在自然环境条件下的溶解量很低,溶出风险很小;(2)外源Cr(Ⅲ)在砖红壤中可氧化为Cr(Ⅵ),随着溶液pH的增加先上升后下降,氧化量在pH 4.5时达到最高,但Cr(Ⅲ)的氧化转化量在Cr(Ⅲ)添加量中的占比很小,外源Cr(Ⅲ)在土壤中氧化转化的风险也很低;(3)Cr(Ⅲ)在砖红壤中的氧化量随着培养时间的增加略有上升,Cr(Ⅵ)的生成量受土壤易还原锰和有机质含量的影响,土壤有机质可将Cr(Ⅲ)氧化生成的Cr(Ⅵ)再次还原为Cr(Ⅲ)。
| [1] |
Chen Z C, Zhao W J. Attribution of latosol in soil systematic classification (In Chinese)[J]. Soils, 1999, 31(2): 90-96. [陈志诚, 赵文君. 砖红壤在土壤系统分类中的归属[J]. 土壤, 1999, 31(2): 90-96.]
(  0) 0) |
| [2] |
Zeng S Q. The forming process of iron lateritic soil in Hainan Island (In Chinese)[J]. Tropical Geography, 1987, 7(4): 382-389. [曾水泉. 海南岛铁质砖红壤的形成过程[J]. 热带地理, 1987, 7(4): 382-389.]
(  0) 0) |
| [3] |
Shahid M, Shamshad S, Rafiq M, et al. Chromium speciation, bioavailability, uptake, toxicity and detoxification in soil-plant system: A review[J]. Chemosphere, 2017, 178: 513-533. DOI:10.1016/j.chemosphere.2017.03.074
(  0) 0) |
| [4] |
Sun S S, Ao M, Geng K R, et al. Enrichment and speciation of chromium during basalt weathering: Insights from variably weathered profiles in the Leizhou Peninsula, South China[J]. Science of the Total Environment, 2022, 822: 153304. DOI:10.1016/j.scitotenv.2022.153304
(  0) 0) |
| [5] |
[5] Rajkumar M, Vara Prasad M N, Freitas H, et al. Biotechnological applications of serpentine soil bacteria for phytoremediation of trace metals[J]. Critical Reviews in Biotechnology, 2009, 29(2): 120-130. DOI:10.1080/07388550902913772
(  0) 0) |
| [6] |
Charlet L, Manceau A A. X-ray absorption spectroscopic study of the sorption of Cr(Ⅲ)at the oxide-water interface: II. Adsorption, coprecipitation, and surface precipitation on hydrous ferric oxide[J]. Journal of Colloid and Interface Science, 1992, 148(2): 443-458. DOI:10.1016/0021-9797(92)90182-L
(  0) 0) |
| [7] |
Shi Z Q, Peng S M, Lin X F, et al. Predicting Cr(Ⅵ)adsorption on soils: The role of the competition of soil organic matter[J]. Environmental Science Processes & Impacts, 2020, 22(1): 95-104.
(  0) 0) |
| [8] |
Doisy R J, Streeten D H P, Freiberg J M, et al. Chromium metabolism in man and biochemical effects[M]//Prasad A S. Essential and Toxic Element. Pittsburgh, USA: Academic Press, 1976: 79—104.
(  0) 0) |
| [9] |
De Flora S, Camoirano A, Bagnasco M, et al. Estimates of the chromium(Ⅵ)reducing capacity in human body compartments as a mechanism for attenuating its potential toxicity and carcinogenicity[J]. Carcinogenesis, 1997, 18(3): 531-537. DOI:10.1093/carcin/18.3.531
(  0) 0) |
| [10] |
Tandon S K, Saxena D K, Gaur J S, et al. Comparative toxicity of trivalent and hexavalent chromium. Alterations in blood and liver[J]. Environmental Research, 1978, 15(1): 90-99. DOI:10.1016/0013-9351(78)90082-8
(  0) 0) |
| [11] |
Apte A D, Tare V, Bose P. Extent of oxidation of Cr(Ⅲ)to Cr(Ⅵ)under various conditions pertaining to natural environment[J]. Journal of Hazardous Materials, 2006, 128(2/3): 164-174.
(  0) 0) |
| [12] |
Li Y, Gu X Y. Soil manganese oxides and its extraction methods: A review (In Chinese)[J]. Environmental Chemistry, 2022, 41(1): 9-21. [李颖, 顾雪元. 土壤中锰氧化物的形态及其化学提取方法综述[J]. 环境化学, 2022, 41(1): 9-21.]
(  0) 0) |
| [13] |
Lu R K. Analytical methods for soil and agro- chemistry (In Chinese). Beijing: China Agricultural Science and Technology Press, 2000. [鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000.]
(  0) 0) |
| [14] |
Ding C P, Xu R K, et al. Oxidation-reduction processes of soils and their research methods (In Chinese). Beijing: Science Press, 2011. [丁昌璞, 徐仁扣, 等. 土壤的氧化还原过程及其研究法[M]. 北京: 科学出版社, 2011.]
(  0) 0) |
| [15] |
U. S. Environmental Protection Agency. EPA 3060A-1996. Alkaline digestion for hexavalent chromium[S]. Washington DC, USA: Environmental Protection Agency, 1996.
(  0) 0) |
| [16] |
Tessier A, Campbell P, Bisson M. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 1979, 51: 844-851. DOI:10.1021/ac50043a017
(  0) 0) |
| [17] |
Liu Y, Xu R K. Reductive dissolution of MnO2 and manganese oxides in soils by low-molecular-weight organic compounds (In Chinese)[J]. Environmental Chemistry, 2015, 34(6): 1037-1042. [刘源, 徐仁扣. 低分子量有机化合物对MnO2和土壤氧化锰的还原溶解作用[J]. 环境化学, 2015, 34(6): 1037-1042.]
(  0) 0) |
| [18] |
Chen Y X, Zhu Z X, He Z Y. Mechanism of Cr(Ⅲ)oxidation by Mn oxides (In Chinese)[J]. Acta Scientiae Circumstantiae, 1993, 13(1): 45-50. [陈英旭, 朱祖祥, 何增耀. 环境中氧化锰对Cr(Ⅲ)氧化机理的研究[J]. 环境科学学报, 1993, 13(1): 45-50.]
(  0) 0) |
| [19] |
Soubrand-Colin M, Horen H, Courtin-Nomade A. Mineralogical and magnetic characterisation of iron titanium oxides in soils developed on two various basaltic rocks under temperate climate[J]. Geoderma, 2009, 149(1/2): 27-32.
(  0) 0) |
| [20] |
Oze C J P. Chromium geochemistry of serpentinites and serpentine soils[D]. Stanford, California, USA: Stanford University, 2003.
(  0) 0) |
| [21] |
Strobel B W. Influence of vegetation on low-molecular- weight carboxylic acids in soil solution—A review[J]. Geoderma, 2001, 99(3/4): 169-198.
(  0) 0) |
| [22] |
Dai R N, Liu J, Yu C Y, et al. A comparative study of oxidation of Cr(Ⅲ)in aqueous ions, complex ions and insoluble compounds by manganese-bearing mineral(birnessite)[J]. Chemosphere, 2009, 76(4): 536-541.
(  0) 0) |
| [23] |
Pan C, Liu H, Catalano J G, et al. Understanding the roles of dissolution and diffusion in Cr(OH)3 oxidation by δ-MnO2[J]. ACS Earth and Space Chemistry, 2019, 3(3): 357-365.
(  0) 0) |
 2024, Vol. 61
2024, Vol. 61


