氧化亚氮(N2O)的产生和转化是自然界氮循环的重要组成部分,具有很高的全球变暖潜力和平流层臭氧消耗潜力[1]。在百年尺度上,N2O的全球变暖潜力为CO2的298倍[2]。农业生产过程中氮肥施入量大,导致全球农田土壤N2O排放量激增[3]。根据粮农组织发布的统计数据库(FAOSTAT),全球无机氮肥诱导的N2O排放量从1961年的0.2 Tg增加至2021年的2.3 Tg[4]。而我国集约化蔬菜生产土壤N2O的排放系数高达2%~5%,远高于其他旱地农业生态系统[5]。土壤N2O排放主要受硝化和反硝化过程调控,硝化过程中氨氧化细菌(AOB)、氨氧化古菌(AOA)和全程氨氧化菌(Comammox,com2)调控氨氧化过程中间产物的化学分解。反硝化过程中nirK型和nirS型反硝化细菌调控亚硝酸盐的还原过程,产生N2O,而nosZ型反硝化细菌将N2O还原为N2,即消耗N2O[6]。此外,温度升高已被广泛报道为刺激土壤N2O排放的关键变量。大量研究表明,温度可改变硝化菌和反硝化菌群落,从而调节N2O的排放[7-8]。在21世纪,全球表面温度可能上升近5℃[9],这会导致N2O排放量增加150%[10],而N2O排放量增加会引发全球变暖的正反馈效应[11]。因此,探究陆地温室气体排放和持续气候变化之间的反馈,对于预测陆地生态系统中的氮循环变化至关重要。
微塑料(Microplastic,MP)指的是直径小于5 mm的塑料颗粒[12],被视为新兴的全球污染物。农田土壤中微塑料主要来源包括塑料大棚与地膜残留物、有机肥料施用、灌溉水和大气沉降等[13]。我国集约化蔬菜种植具有氮肥施用量大、农事操作频繁和复种指数高的特点[14],同时由于地膜具有保温保墒、减少水分蒸发的作用,在蔬菜种植过程中应用比较普遍[15],这极大地增加了微塑料在菜地土壤内富集的可能性。一般地,由于微塑料中的氮含量可忽略不计,其对氮循环的直接影响可能很小[16]。然而,作为外源性物质,微塑料在土壤中的存在能够影响参与土壤氮循环的微生物群落及其功能基因,不可避免地干扰土壤氮的转化和生物利用度[17]。国内外研究表明,由于微塑料特性(特别是大小和含量)、土壤类型和气候等条件差异,微塑料对N2O排放的影响也有很大不同。当塑料在土壤中积累时,由于紫外线辐射、高温、生物降解和耕作的机械力,塑料可破碎为较小的碎片[18],由此产生的微塑料浓度增加和尺寸减小可能对土壤碳氮循环构成长期挑战。较小尺寸的微塑料可能更易缠绕土壤颗粒,形成土块或破坏土壤结构的完整性[19]。此外,有研究发现,高浓度的微塑料大大提高了溶解有机物(DOM)溶液的养分含量,DOM是微生物的底物和最重要的碳源[20]。还有研究表明,微塑料的添加会导致土壤C/N比值升高,而较高的C/N会限制微生物所需的养分[21],上述因素均有可能影响不同氮素转化过程的速率和方向,对气候变化条件下土壤元素的生物地球化学循环产生深远影响。
我国华南地区高温多雨,土壤保肥性差,水旱轮作系统土壤经常处于干湿交替状态,是我国重要的N2O排放源。目前,关于微塑料富集对土壤氮素循环以及土壤N2O排放影响的研究非常有限,且其对温度升高的响应仍未确定。因此,本文以华南地区集约化菜地土壤为研究对象,通过室内培养试验,探究N2O对温度变化和不同尺寸、浓度微塑料添加的响应及其微生物机制。本研究假设:(1)微塑料在耕作土壤中的富集能够影响氮素循环过程,进而造成土壤N2O排放规律和关键驱动因素的变化。(2)不同温度条件下,微塑料富集对耕作土壤N2O排放规律的影响存在差异。研究结果以期为气候变化条件下微塑料对农田土壤N2O的排放机理探究以及风险评估提供科学依据。
1 材料与方法 1.1 供试土壤及微塑料试验土壤采自广东省广州市花都区京塘荷塘路狮前村集约化模式蔬菜地(23°04′ N,113°04′ E),该地种植蔬菜年限大于20年。该地区位于亚热带季风气候区,平均相对湿度为68%~77%,年均降水量1 689 mm~1 876 mm,年均温21.4℃~21.9℃。采用“S”型五点混合法采集表层土壤(0~20 cm)[22],同时去除可见的砾石和植物残体,过2 mm筛后将新鲜土壤混匀,一部分储存于4℃冰箱以供后续实验,另一部分自然风干,用于测定土壤基础理化性质。土壤的初始性质为:pH 5.35,土壤有机碳0.339 g·kg–1,全氮1.79 g·kg–1,有效磷6.29 g·kg–1,阳离子交换量24.37 cmol·kg–1,微生物生物量碳0.217 g·kg–1。供试微塑料为74 μm和25 μm聚苯乙烯微球,购自上海麦克林生化有限公司(http://www.macklin.cn/)。
1.2 研究方法通过室内培养试验,设置五个不同处理:(1)不添加微塑料(CK);(2)添加质量浓度为0.1%、粒径为74 μm的微塑料(Nlp-0.1%);(3)添加质量浓度为0.5%、粒径为74 μm的微塑料(Nlp-0.5%);(4)添加质量浓度为0.1%、粒径为25 μm的微塑料(Nsp-0.1%);(5)添加质量浓度为0.5%、粒径为25 μm的微塑料(Nsp-0.5%),每个样品设置三个重复。
首先将聚苯乙烯微球用去离子水清洗,紫外线灭菌后备用。然后将每份干物质量20 g的土壤样品放入血清瓶(120 mL)中,各处理按照实验设计加入相应的微塑料并均匀混合。培养期间通过称重法向玻璃瓶中加入适量去离子水,调节土壤水分至保持在最大田间持水量(WHC)的60%,用橡胶和铝盖密封瓶子。将所有土壤样品分别放置在10、20和30 ℃三个温度的恒温培养箱中,在黑暗条件下进行8 d的预培养,以消除干湿效应并激活微生物。预培养结束后,在三个温度下开始正式培养128 h。每份样品中加入相当于田间施肥量240 kg·hm–2(以N计)的氮肥,在开始培养的第0、6、18、48和128小时采集气体样品测定。使用注射器从瓶内采集20 mL气体样品进行测定,同时补充20 mL空气。培养结束后,取出各血清瓶中的土壤样品并混匀,用于测定不同处理的土壤微生物基因丰度、铵态氮(NH4+-N)、硝态氮(NO3–-N)和亚硝态氮(NO2–-N)含量。
1.3 土壤N2O排放量及化学性质测定 1.3.1 土壤N2O排放量测定采集的气体由气相色谱仪(Agilent 7890A,Agilent Ltd,上海)分析,N2O检测器为电子捕获检测器(ECD),载气为氩甲烷,检测器温度300℃。计算累积排放量公式如下:
| $ {E_{{{\text{N}}_2}{\text{O}}}} = \sum\nolimits_{i = 1}^n {\frac{{{F_i} + {F_{i + 1}}}}{2}} \left( {{t_{i + 1}} - {t_i}} \right) \times 1000 $ | (1) |
式中,
破坏性采样完成后,过2 mm筛,称取2.0 g土壤样品于聚乙烯瓶中,加入50 mL 2 mol·L–1的氯化钾溶液浸提,滤液中NH4+含量采用靛酚蓝比色法测定,NO3–-N含量和NO2–-N含量采用紫外分光光度法测定。具体操作参考《土壤农化分析》[23]。
1.3.3 土壤微生物总DNA提取按照Fast DNA SPIN Kit for Soil(MP Biomedicals,美国)试剂盒操作手册,从每个土壤样本中提取DNA。通过qPCR分析目标微生物基因丰度,使用TaqMan系统对累积的荧光实时检测(BioRad,Laboratories Inc.,Hercules,CA,美国)。定量PCR扩增反应体系为20.0 μL,包括:2×qPCR mix 10.0 μL,DNA模板1.5 μL,上下游引物各0.4 μL,灭菌双蒸水7.7 μL。每种基因对应的引物分别为Arch-amoA-26F/Arch-amoA-417R(AOA)、1F/2R(AOB)、nirK876C/ nirK1040(nirK)、cd3af/R3cd(nirS)、nosZ2F/nosZ2R(nosZ)及COM-F2/COM-R2(com2)。每次试验均设置严格的阴性对照,采用灭菌双蒸水代替DNA作为反应模板。
1.4 数据处理与分析使用EXCEL 2019进行数据整理,使用SPSS 21.0进行单因素方差分析和多因素方差分析,显著水平为α=0.05。采用Origin 2021软件进行图件的绘制,并使用Origin中的“Correlation Plot”插件绘制相关性热图,“Principal Component Analysis”插件绘制主成分分析(PCoA)图。用R 4.2.3的“randomForest”包进行随机森林分析。随机森林分析即计算每棵树的精度重要性,并在森林(500棵树)上取平均值。变量的均方误差(MSE)增加百分比用于估计这些预测变量的重要性,MSE越高表示预测变量越重要。所有的数据在分析之前进行正态分布和方差齐性检验,所有试验数据均为平均值±标准差(n=3)。
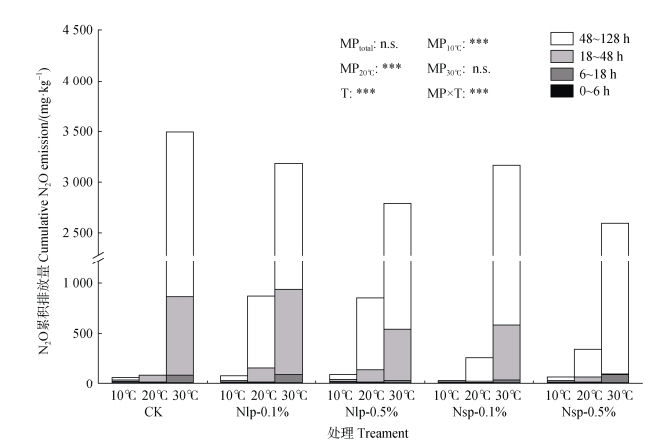
2 结果 2.1 不同温度下微塑料对土壤N2O排放的影响如图 1所示,不同温度条件下,培养期间N2O累积排放量范围为70.3~3 046.3 mg·kg–1,所有微塑料处理土壤N2O排放量均随温度升高而显著增加(P<0.001)。与10℃条件相比,培养温度升高至30℃,土壤N2O累积排放量增加了42.3倍,且排放峰大都集中在培养18 h之后。此外,温度与微塑料存在交互效应,在不同培养温度下各微塑料处理的土壤N2O排放量存在显著差异(P<0.001)。与CK处理相比,大尺寸微塑料的添加在低温(10℃和20℃)下显著增加了土壤N2O排放量。其中在10℃下,Nlp-0.1%处理和Nlp-0.5%处理的N2O排放量相比CK显著提高了29.9%和45.2%,而小尺寸微塑料添加在0.1%浓度处理(Nsp-0.1%)相比CK显著降低了45.9%(P<0.05)。在20℃下仅有大尺寸微塑料的添加显著影响了土壤N2O排放量。具体而言,20℃下Nlp-0.1%处理和Nlp-0.5%处理的N2O排放量相比CK分别显著提高了8.5倍和8.3倍,而小尺寸微塑料(Nsp)处理与CK处理的排放量无显著差异。此外,在30℃下各微塑料处理的N2O排放量均无显著差异。
|
注:CK—不添加微塑料;Nlp-0.1%—添加质量浓度为0.1%、粒径为74 μm的微塑料;Nlp-0.5%—添加质量浓度为0.5%、粒径为74 μm的微塑料;Nsp-0.1%—添加质量浓度为0.1%、粒径为25 μm的微塑料;Nsp-0.5%—添加质量浓度为0.5%、粒径为25 μm的微塑料。方柱上不同大写字母代表同一微塑料处理不同温度之间显著性差异(P < 0.05),不同小写字母代表同一温度下不同微塑料处理之间显著性差异(P < 0.05)。*、**和***分别代表 0.05、0.01和0.001水平效应显著,n.s. 代表无显著差异。双重因素分析中,T、MP分别表示温度效应和微塑料效应,MP×T表示微塑料与温度交互作用,下同。 Note: CK—no microplastics; Nlp-0.1%—addition of microplastics with a mass concentration of 0.1% and a particle size of 74 μm; Nlp-0.5%—added microplastics with a mass concentration of 0.5% and a particle size of 74 μm; Nsp-0.1%—addition of microplastics with a mass concentration of 0.1%, microplastic with 25 μm particle size; Nsp-0.5%—addition of microplastic with 0.5% mass concentration and 25 μm particle size. Different capital letters on the square columns represent significant differences between different temperatures for the same microplastic treatment (P < 0.05), and different lowercase letters represent significant differences between different microplastic treatments at the same temperature (P < 0.05). *, **, and *** represent significant effects at 0.05, 0.01, and 0.001 levels, respectively, and n.s. represents no significant effect. In the two-way factor analysis, T and MP denote the temperature effect and microplastic effect, respectively, and MP×T denotes the interaction effect of microplastic and temperature. The same as below. 图 1 不同温度条件下各微塑料处理N2O累积排放量 Fig. 1 Cumulative N2O emissions under different temperatures for different microplastics (MP) treatments |
培养期间,土壤NO2–-N含量范围为8.8~15.4 mg·kg–1,土壤NH4+-N含量范围为13.0~85.8 mg·kg–1,而土壤NO3–-N含量相对较高,其范围为344.5~592.1 mg·kg–1(表 1)。温度显著改变了NO3–-N含量和NH4+-N含量(P<0.001),土壤NO3–-N含量随着培养温度的升高逐渐增加,CK处理、Nlp-0.1%处理和Nsp-0.5%处理的土壤NH4+-N含量随着培养温度的升高逐渐降低,而Nlp-0.5%处理和Nsp-0.1%处理的土壤NH4+-N含量随着培养温度的升高先减少再增加。在30℃下的土壤NO3–-N含量分别是10℃的1.3倍和20℃下的1.1倍。微塑料显著改变了土壤NO3–-N、NO2–-N和NH4+-N含量(P<0.001)。与CK处理相比,Nlp-0.5%处理和Nsp-0.5%处理的NO3–-N含量显著降低了19.8%和21.7%,Nsp-0.1%处理和Nsp-0.5%处理的NH4+-N含量显著降低了45.1%和43.7%,Nlp-0.1%处理的NO2–-N含量显著提高了33.1%。此外,温度与微塑料对NO3–-N含量和NH4+-N含量均存在显著的交互作用(P<0.001)。在20℃和30℃时,Nsp-0.1%处理的NO3–-N含量显著低于CK处理。在低温(10℃)下,微塑料的添加均显著降低土壤NH4+-N含量,而在高温(30℃)下微塑料处理使土壤NH4+-N含量增加(Nsp-0.5%处理除外)。
|
|
表 1 不同温度条件下各微塑料处理的土壤无机氮含量 Table 1 Soil mineral N content under different temperature conditions for different MP treatments |
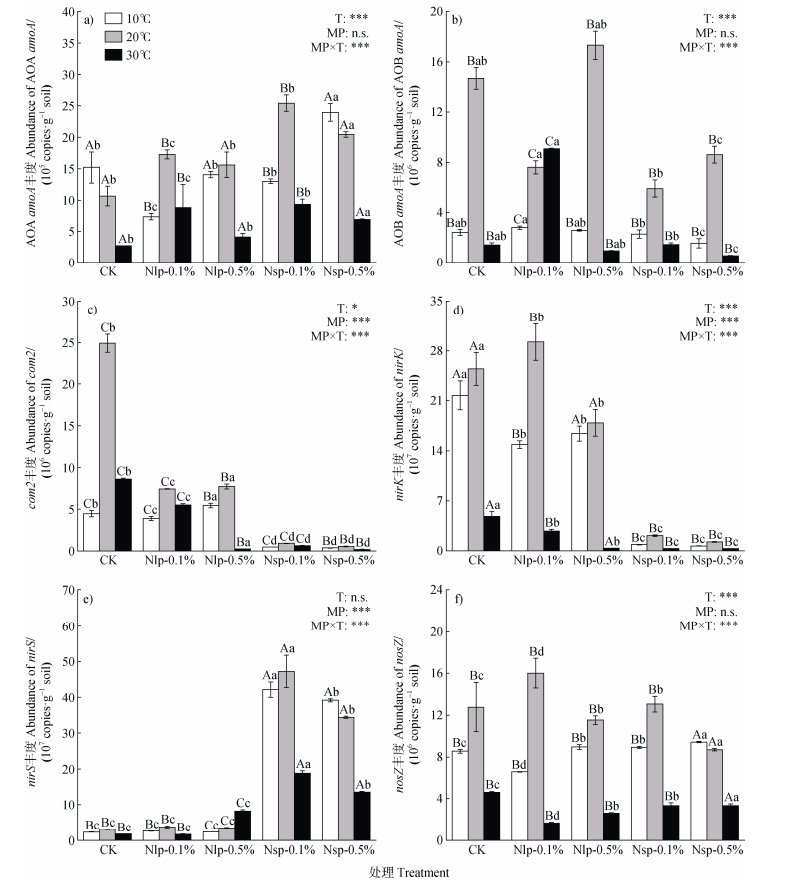
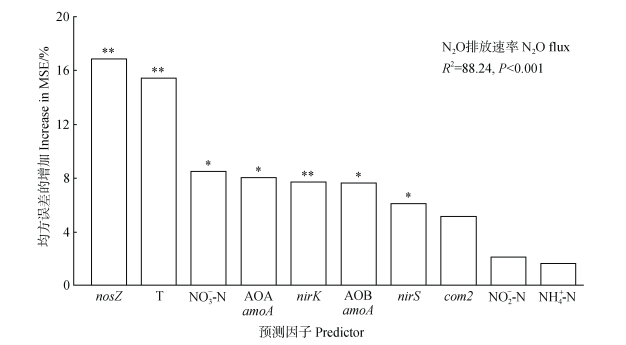
温度显著影响除nirS外的土壤氮循环相关功能基因丰度(图 2)。AOA amoA、AOB amoA、nirS、nirK、nosZ和Comammox(com2)功能基因均在20℃时丰度最高,30℃时丰度最低,表明硝化反硝化微生物群落在此温度变化范围内有较高的敏感性,在20℃下适应性最高。相关性分析表明,温度与AOA amoA、nirK和nosZ功能基因丰度存在负相关关系(图 3)。添加微塑料对nirK、nirS和com2功能基因丰度存在显著影响(P<0.001),且主要是微塑料不同粒径间差异较大。与CK相比,nirK功能基因丰度在Nsp处理下显著降低,nirS功能基因丰度在Nsp处理下显著升高,com2功能基因丰度在Nlp和Nsp处理下均显著降低。此外,温度与微塑料存在交互作用(P<0.001),不同温度处理下氮循环相关功能基因丰度存在显著差异。在20℃和30℃时,添加MP处理的AOA amoA功能基因丰度显著高于CK处理,而nosZ功能基因丰度在30℃时显著降低。主成分分析PCoA1和PCoA2的贡献率分别为47.1%和34.5%,累积贡献率为81.6%(图 4)。在不同温度下,不同浓度和粒径的微塑料添加对土壤氮循环相关功能基因丰度可明显区分开来。随机森林分析进一步确定了土壤氮循环功能基因对N2O排放的影响强度(图 5),分析结果表明nosZ功能基因是影响土壤N2O排放的主要因素,其均方误差(MSE)的增加达到了16.86%,其次是温度,其MSE的增加为15.44%。NO3–-N、AOA amoA功能基因、nirK基因、AOB amoA基因、nirS功能基因的MSE的增加分别为8.51%、8.06%、7.73%、7.64%和6.12%。
|
注:AOA amoA—氨氧化古菌调控基因,AOB amoA—氨氧化细菌调控基因、com2—全程氨氧化菌调控基因,nirS—亚硝酸盐还原酶调控基因,nirK—亚硝酸盐还原酶调控基因,nosZ—N2O还原酶调控基因,方柱上不同大写字母代表同一微塑料处理不同温度之间显著性差异(P < 0.05),不同小写字母代表同一温度下不同微塑料处理之间的显著性差异(P < 0.05)。 Note: AOA amoA—ammonia-oxidizing archaea regulatory gene, AOB amoA—ammonia-oxidizing bacteria regulatory gene, com2—complete ammonia oxidization regulatory gene, nirS—nitrite reductase regulatory gene, nirK—nitrite reductase regulatory gene, nosZ—N2O reductase regulatory gene. Different capital letters on the square columns represent significant differences between different temperatures for the same microplastic treatment (P < 0.05), and different lowercase letters represent significant differences between different microplastic treatments at the same temperature (P < 0.05). 图 2 不同温度下各微塑料处理土壤中相关氮循环功能基因丰度 Fig. 2 Abundance of N cycling functional genes under different temperature conditions for different Mp treatments |
|
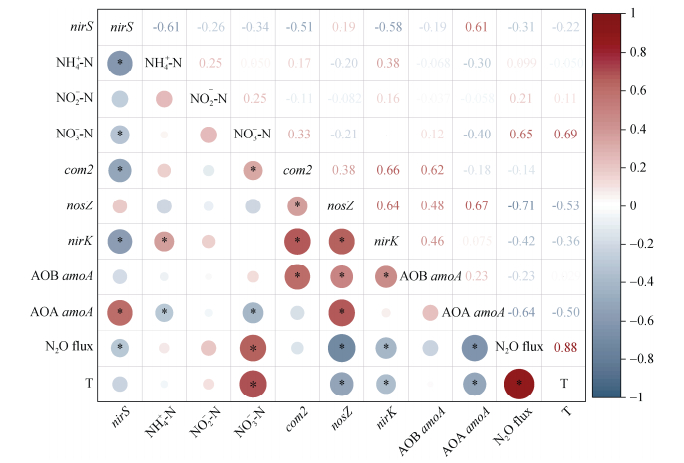
注:N2O flux—N2O排放通量。 Note: N2O flux—N2O emission rate. 图 3 N2O排放速率相关影响因子相关性分析 Fig. 3 Correlation analysis between N2O rate and related parameters |
|
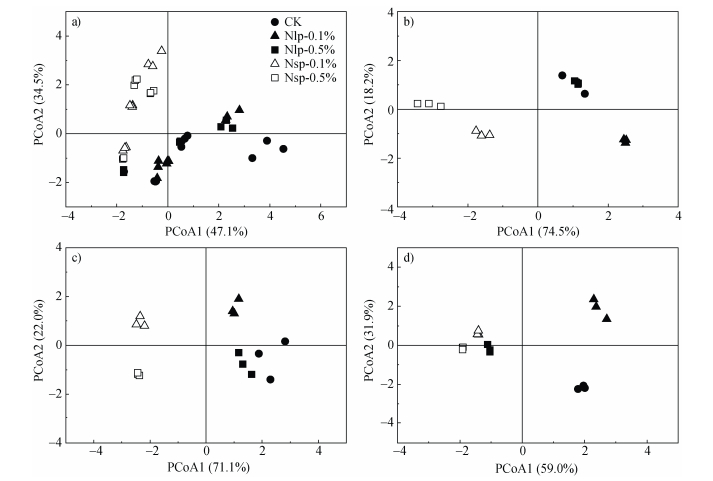
图 4 不同温度下(a. 总体上,b. 10℃,c. 20℃,d. 30℃)微塑料处理对土壤氮循环相关功能基因丰度的主成分分析(PCoA) Fig. 4 Principal componentanalysis (PCoA) of MP treatments on the abundance of N cycling functional genes under different temperatures (a. In total, b. 10℃, c. 20℃, d. 30℃) |
|
图 5 影响土壤N2O排放因素的随机森林分析 Fig. 5 Random forest analysis of factors affecting soil N2O emission rate |
本研究表明,温度升高显著增加了土壤N2O排放(图 1,P<0.001),这与诸多现有报告的研究结果[9,10,24]一致。在土壤氮素循环过程中,N2O主要通过硝化作用和反硝化作用过程产生。随着温度的上升,会催化出更多的硝酸盐矿物和可利用氮量,从而让更多的“好氧”硝化和“厌氧”反硝化过程得以进行,最终导致N2O的排放量增加[6]。本研究中从10℃至30℃,土壤NO3–-N含量随着培养温度的升高逐渐增加,且相关性分析表明土壤NO3–-N含量与温度和N2O排放速率显著正相关(表 1和图 3),进一步表明温度升高为硝化和反硝化作用增加底物。Wang等[25]也发现短期培养条件下,增温显著增加了硝态氮和铵态氮的含量。由于硝化和反硝化通常是微生物过程,因此探索相关微生物对温度的反应对于解释N2O排放量的变化至关重要[26]。此外,本研究中氮素循环功能基因AOA amoA、AOB amoA、nirK、nosZ和com2均受温度影响显著(图 2)。随机森林分析表明,nosZ功能基因的平均预测重要性最高,即含nosZ的反硝化菌与土壤N2O排放量相关性较强(图 5)。当温度从20℃升至30℃时,nosZ功能基因丰度显著降低(图 2),nosZ反硝化细菌可通过N2O还原酶将N2O还原为N2,在N2O消耗中发挥着重要作用[6]。而此温度区间nosZ功能基因丰度的降低,导致N2O难以向N2的转化,可能是高温下N2O排放量增加的主要原因。此外,温度与AOA amoA和nirK功能基因存在显著负相关关系(图 3),这与之前研究结果[27]并不一致。本研究中温度对nirS功能基因无显著影响(图 2),而Xing等[10]的水稻田土壤升温实验发现,含nirS的反硝化细菌对温度变化很敏感,从而增加了土壤中N2O的排放,这进一步佐证在本实验中,微塑料主要是通过介导nosZ调控反硝化作用来影响土壤N2O排放。然而,不同土壤类型和试验条件设置导致结果有很大差异,在今后的研究中,尚需进一步探究全球范围内微生物氮循环过程和基因丰度对温度升高的响应,以明确温度升高条件下微塑料在农田土壤中不断富集对氮素排放的潜在影响。
3.2 微塑料添加对土壤N2O排放的影响虽然本研究中微塑料的添加对土壤N2O的排放总体上无显著影响,但在不同温度条件下,微塑料的添加对土壤N2O排放的影响并不一致(图 1)。在10 ℃和20 ℃下,Nlp处理与CK和Nsp处理相比显著增加了土壤N2O排放量(图 1),表明微塑料的粒径对N2O排放存在影响。Yu等[28]研究发现添加MP(1%质量比,粒径小于187.5 µm)使土壤中nirS功能基因丰度增加,从而使N2O排放量增加了3.7倍;Chen等[29]的研究也表明微塑料添加导致N2O排放量增加,但由于高浓度的微塑料添加会增加嗜热菌的丰度,降低氮的可用性,在0.25%MP处理下N2O排放量达到峰值,然后随着MP浓度的增加而降低[29-30]。此外,本研究中10 ℃下小粒径低浓度的微塑料(Nsp-0.1%)添加与CK相比显著降低了土壤N2O排放量(图 1)。10 ℃时,N2O排放与nirK、com2、NH4+-N呈正相关,与nirS、NO3–-N呈负相关(表 2)。同样也有研究指出MP的添加使N2O排放量减少或无显著影响[31-32],这可能是由于不同的土壤类型、微塑料和实验条件的控制对N2O产生或还原途径的影响不同。nirK和nirS功能基因控制NO2–-N向NO的转化,且相关性分析表明其与N2O排放量均存在显著相关关系(图 3)。本研究中添加小粒径微塑料(Nsp)并未使土壤N2O排放增加,可能是由于Nsp处理使nirK功能基因丰度显著降低(图 2),抵消了部分由于nirS功能基因丰度显著增加导致的N2O排放量增加。Gao等[31]发现,添加MP可通过提高氮的矿化度来增加硝化所需的底物,但会通过减少编码硝化(AOB amoA)和反硝化(nirS)相关酶的微生物功能基因的数量来抑制N2O的产生,因此添加MP后N2O排放量无显著变化。
|
|
表 2 不同温度条件下N2O排放速率与各因素的相关关系 Table 2 Correlation analysis of N2O rate and various factors under different temperature conditions |
本研究中,微塑料对土壤无机氮含量有显著影响,且随浓度和粒径的不同而改变。高浓度微塑料处理显著降低了NO3–-N含量,小粒径微塑料处理显著降低了NH4+-N含量,大粒径低浓度微塑料处理显著提高了NO2–-N含量(表 1)。Zhang等[33]发现,聚乙烯MP浓度从0.01%增加至1.0%,可持续减少土壤中的NO3–-N含量。Su等[34]通过荟萃分析发现在微塑料的添加下,NH4+-N和NO3–-N含量分别降低了6.7%和22.4%,NO2–-N增加了38.8%。NH4+-N浓度降低可能是由于微塑料增加了几种可消耗NH4+-N的微生物丰度,NH4+-N的减少又在一定程度上限制了硝化细菌的生长以及硝化速率。添加微塑料处理使com2功能基因丰度显著降低(图 2),表明硝化速率降低,这可能是NO3–-N含量降低的原因。土壤团聚体是土壤全氮的固存库[35]。有研究表明加入粒径较小的MP颗粒(35 μm)会使土壤团聚体破裂,但粒径较大的MP颗粒(125 μm和500 μm)则未影响土壤团聚体[36]。可能是由于MP加入引入了断裂点,团聚体破裂。随着MP粒径的减小,单位质量的MP数量也随之增加,更多的断裂点可能被引入团聚体中,从而导致团聚体强度下降,减少土壤全氮的存储量,对土壤氮循环产生影响。然而,也有一些研究报道MP对土壤矿质氮含量无显著影响[37-38],可能不会通过调节氮底物的供应而影响N2O的产生。
温度与微塑料添加对土壤N2O存在显著的交互效应(P<0.001),在30 ℃下微塑料的添加对N2O排放量无显著影响,而在10 ℃和20 ℃时,74 μm粒径的微塑料的添加使N2O排放显著增加(图 1,P<0.001)。Iqbal等[21]的研究表明温度升高使添加MP的土壤pH下降幅度更高,而较低的pH(≤ 5.8)会抑制N2O还原酶的活性并导致更高的N2O排放[39]。Shi等[40]的研究表明在15 ℃下,微塑料的存在对土壤氮转化和生物利用率的影响很小,但在25 ℃下,微塑料显著降低了NO3–-N、矿物氮(MN)、总溶解氮(TDN)、净累积氮硝化(Nn)和净累积氮矿化(Nm),表明微塑料降低了高温下土壤的氮生物利用率。因此,温度与微塑料相互作用影响了氮循环相关功能基因的丰度和微生物活性,从而影响了土壤N2O排放。
4 结论温度升高显著增加了菜地土壤的N2O排放量,提高了土壤NO3–-N含量。AOB amoA、com2、nirS、nirK和nosZ功能基因丰度在20℃最高,30℃最低。不同粒径微塑料添加对土壤N2O排放量和相关氮循环功能基因的影响差异较大。微塑料的添加对土壤N2O的排放总体上无显著影响,但是Nlp处理在10 ℃和20 ℃时使菜地土壤N2O排放量显著增加了37.5%、838.7%,表明在不同温度下微塑料对N2O排放影响存在差异。此外,Nsp处理显著降低com2和nirK功能基因丰度、显著提高nirS功能基因丰度。在微塑料添加情况下,土壤N2O排放与温度和NO3–-N含量存在显著正相关关系,与AOA amoA、nirK、nirS和nosZ功能基因丰度存在显著负相关关系(P<0.05),且nosZ功能基因和温度是影响土壤N2O排放的主要因素。研究结果表明,微塑料添加对土壤氮过程有深远影响并与气候变暖存在正反馈效应,采取切实可行的措施降低微塑料污染是减缓全球增温条件下氮素损失的重要举措。
| [1] |
Ravishankara A R, Daniel J S, Portmann R W. Nitrous oxide (N2O): The dominant ozone-depleting substance emitted in the 21st century[J]. Science, 2009, 326(5949): 123-125. DOI:10.1126/science.1176985
(  0) 0) |
| [2] |
Kleinen T, Gromov S, Steil B, et al. Atmospheric methane underestimated in future climate projections[J]. Environmental Research Letters, 2021, 16(9): 094006. DOI:10.1088/1748-9326/ac1814
(  0) 0) |
| [3] |
Menegat S, Ledo A, Tirado R. Greenhouse gas emissions from global production and use of nitrogen synthetic fertilizers in agriculture[J]. Scientific Reports, 2022, 12(1): 14490. DOI:10.1038/s41598-022-18773-w
(  0) 0) |
| [4] |
Li L D, Hong M, Zhang Y, et al. Soil N2O emissions from specialty crop systems: A global estimation and meta‐analysis[J]. Global Change Biology, 2024, 30(3): e17233. DOI:10.1111/gcb.17233
(  0) 0) |
| [5] |
Li B, Huang W H, Elsgaard L, et al. Optimal biochar amendment rate reduced the yield-scaled N2O emissions from Ultisols in an intensive vegetable field in South China[J]. Science of the Total Environment, 2020, 723: 138161. DOI:10.1016/j.scitotenv.2020.138161
(  0) 0) |
| [6] |
Liu X H, Li Y Y, Zheng N G, et al. Effects of global environmental change on soil N2O emission: A review (In Chinese)[J]. Chinese Journal of Soil Science, 2023, 54(1): 213-222. [刘鑫慧, 李雅颖, 郑宁国, 等. 全球环境变化对土壤N2O排放影响的研究进展[J]. 土壤通报, 2023, 54(1): 213-222.]
(  0) 0) |
| [7] |
Cui P Y, Fan F L, Yin C, et al. Long-term organic and inorganic fertilization alters temperature sensitivity of potential N2O emissions and associated microbes[J]. Soil Biology and Biochemistry, 2016, 93: 131-141. DOI:10.1016/j.soilbio.2015.11.005
(  0) 0) |
| [8] |
Sun L F, Sang C P, Wang C, et al. N2O production in the organic and mineral horizons of soil had different responses to increasing temperature[J]. Journal of Soils and Sediments, 2019, 19(10): 3499-3511. DOI:10.1007/s11368-019-02316-4
(  0) 0) |
| [9] |
Dai Z, Yu M, Chen H, et al. Elevated temperature shifts soil N cycling from microbial immobilization to enhanced mineralization, nitrification and denitrification across global terrestrial ecosystems[J]. Global Change Biology, 2020, 26(9): 5267-5276. DOI:10.1111/gcb.15211
(  0) 0) |
| [10] |
Xing X Y, Tang Y F, Xu H F, et al. Warming shapes nirS- and nosZ -type denitrifier communities and stimulates N2O emission in acidic paddy soil[J]. Applied and Environmental Microbiology, 2021, 87(12): e02965-20.
(  0) 0) |
| [11] |
Gineyts R, Niboyet A. Nitrification, denitrification, and related functional genes under elevated CO2: A meta-analysis in terrestrial ecosystems[J]. Global Change Biology, 2023, 29(7): 1839-1853. DOI:10.1111/gcb.16568
(  0) 0) |
| [12] |
Thompson R C, Olsen Y, Mitchell R P, et al. Lost at sea: Where is all the plastic?[J]. Science, 2004, 304(5672): 838. DOI:10.1126/science.1094559
(  0) 0) |
| [13] |
Bläsing M, Amelung W. Plastics in soil: Analytical methods and possible sources[J]. Science of the Total Environment, 2018, 612: 422-435. DOI:10.1016/j.scitotenv.2017.08.086
(  0) 0) |
| [14] |
Li B, Bi Z, Xiong Z. Dynamic responses of nitrous oxide emission and nitrogen use efficiency to nitrogen and biochar amendment in an intensified vegetable field in southeastern China[J]. Global Change Biology Bioenergy, 2017, 9(2): 400-413. DOI:10.1111/gcbb.12356
(  0) 0) |
| [15] |
Xu G R, Yang L, Xu L, et al. Soil microplastic pollution under different land uses in tropics, southwestern China[J]. Chemosphere, 2022, 289: 133176. DOI:10.1016/j.chemosphere.2021.133176
(  0) 0) |
| [16] |
de Souza Machado A A, Kloas W, Zarfl C, et al. Microplastics as an emerging threat to terrestrial ecosystems[J]. Global Change Biology, 2018, 24(4): 1405-1416. DOI:10.1111/gcb.14020
(  0) 0) |
| [17] |
Riveros G, Urrutia H, Araya J, et al. Microplastic pollution on the soil and its consequences on the nitrogen cycle: A review[J]. Environmental Science and Pollution Research, 2022, 29(6): 7997-8011. DOI:10.1007/s11356-021-17681-2
(  0) 0) |
| [18] |
Tian L L, Cheng J J, Ji R, et al. Microplastics in agricultural soils: Sources, effects, and their fate[J]. Current Opinion in Environmental Science & Health, 2022, 25: 100311.
(  0) 0) |
| [19] |
Zhang G S, Zhang F X, Li X T. Effects of polyester microfibers on soil physical properties: Perception from a field and a pot experiment[J]. Science of the Total Environment, 2019, 670: 1-7.
(  0) 0) |
| [20] |
Liu H F, Yang X M, Liu G B, et al. Response of soil dissolved organic matter to microplastic addition in Chinese loess soil[J]. Chemosphere, 2017, 185: 907-917. DOI:10.1016/j.chemosphere.2017.07.064
(  0) 0) |
| [21] |
Iqbal S, Xu J, Arif M S, et al. Do added microplastics, native soil properties, and prevailing climatic conditions have consequences for carbon and nitrogen contents in soil? A global data synthesis of pot and greenhouse studies[J]. Environmental Science & Technology, 2024, 58(19): 8464-8479.
(  0) 0) |
| [22] |
Zhao X, Liu H L, Yang P, et al. Effects of drip irrigation on bacterial diversity and community structure in rhizosphere soil of alfalfa (In Chinese)[J]. Microbiology China, 2019, 46(10): 2579-2590. [赵祥, 刘红玲, 杨盼, 等. 滴灌对苜蓿根际土壤细菌多样性和群落结构的影响[J]. 微生物学通报, 2019, 46(10): 2579-2590.]
(  0) 0) |
| [23] |
Bao S D. Soil and agricultural chemistry analysis (In Chinese). 3rd ed[M]. Beijing: China Agriculture Press, 2000. [鲍士旦. 土壤农化分析[M]. 3版. 北京: 中国农业出版社, 2000.]
(  0) 0) |
| [24] |
Liu Y G, Hu J S, Wang C, et al. Effects of field-aged biochar on denitrification of vegetable soils under different temperature conditions in South China (In Chinese)[J]. Journal of Plant Nutrition and Fertilizers, 2022, 28(9): 1641-1651. [刘一戈, 胡家帅, 王朝, 等. 不同温度条件下生物质炭陈化对华南集约化菜地土壤反硝化过程的影响[J]. 植物营养与肥料学报, 2022, 28(9): 1641-1651.]
(  0) 0) |
| [25] |
Wang X X, Dong S K, Gao Q Z, et al. Effects of short-term and long-term warming on soil nutrients, microbial biomass and enzyme activities in an alpine meadow on the Qinghai-Tibet Plateau of China[J]. Soil Biology and Biochemistry, 2014, 76: 140-142. DOI:10.1016/j.soilbio.2014.05.014
(  0) 0) |
| [26] |
Song Y Q, Wang L, Li K, et al. The mechanism and research progress of soil microorganism reducing N2O (In Chinese)[J]. Environmental Science & Technology, 2019, 42(9): 82-90. [宋雅琦, 王玲, 李昆, 等. 土壤微生物还原N2O机制及其研究进展[J]. 环境科学与技术, 2019, 42(9): 82-90.]
(  0) 0) |
| [27] |
Xue K, Xie J, Zhou A, et al. Warming alters expressions of microbial functional genes important to ecosystem functioning[J]. Frontiers in Microbiology, 2016, 7: 668.
(  0) 0) |
| [28] |
Yu Y X, Li X, Feng Z Y, et al. Polyethylene microplastics alter the microbial functional gene abundances and increase nitrous oxide emissions from paddy soils[J]. Journal of Hazardous Materials, 2022, 432: 128721. DOI:10.1016/j.jhazmat.2022.128721
(  0) 0) |
| [29] |
Chen X, Xie Y J, Wang J, et al. Presence of different microplastics promotes greenhouse gas emissions and alters the microbial community composition of farmland soil[J]. Science of the Total Environment, 2023, 879: 162967. DOI:10.1016/j.scitotenv.2023.162967
(  0) 0) |
| [30] |
Liu Z Q, Wen J H, Liu Z X, et al. Polyethylene microplastics alter soil microbial community assembly and ecosystem multifunctionality[J]. Environment International, 2024, 183: 108360. DOI:10.1016/j.envint.2023.108360
(  0) 0) |
| [31] |
Gao B, Yao H, Li Y, et al. Microplastic addition alters the microbial community structure and stimulates soil carbon dioxide emissions in vegetable-growing soil[J]. Environmental Toxicology and Chemistry, 2021, 40(2): 352-365.
(  0) 0) |
| [32] |
Greenfield L M, Graf M, Rengaraj S, et al. Field response of N2O emissions, microbial communities, soil biochemical processes and winter barley growth to the addition of conventional and biodegradable microplastics[J]. Agriculture, Ecosystems & Environment, 2022, 336: 108023.
(  0) 0) |
| [33] |
Zhang Y, Li X, Xiao M, et al. Effects of microplastics on soil carbon dioxide emissions and the microbial functional genes involved in organic carbon decomposition in agricultural soil[J]. Science of the Total Environment, 2022, 806: 150714. DOI:10.1016/j.scitotenv.2021.150714
(  0) 0) |
| [34] |
Su P J, Gao C Y, Zhang X J, et al. Microplastics stimulated nitrous oxide emissions primarily through denitrification: A meta-analysis[J]. Journal of Hazardous Materials, 2023, 445: 130500. DOI:10.1016/j.jhazmat.2022.130500
(  0) 0) |
| [35] |
Wang Y L, Wu P N, Qiao Y B, et al. The potential for soil C sequestration and N fixation under different planting patterns depends on the carbon and nitrogen content and stability of soil aggregates[J]. Science of the Total Environment, 2023, 897: 165430. DOI:10.1016/j.scitotenv.2023.165430
(  0) 0) |
| [36] |
Fang Z, Sallach J B, Hodson M E. Size- and concentration-dependent effects of microplastics on soil aggregate formation and properties[J]. Journal of Hazardous Materials, 2024, 465: 133395. DOI:10.1016/j.jhazmat.2023.133395
(  0) 0) |
| [37] |
Meng F R, Yang X M, Riksen M, et al. Effect of different polymers of microplastics on soil organic carbon and nitrogen–A mesocosm experiment[J]. Environmental Research, 2022, 204: 111938. DOI:10.1016/j.envres.2021.111938
(  0) 0) |
| [38] |
Blöcker L, Watson C, Wichern F. Living in the plastic age - Different short-term microbial response to microplastics addition to arable soils with contrasting soil organic matter content and farm management legacy[J]. Environmental Pollution, 2020, 267: 115468. DOI:10.1016/j.envpol.2020.115468
(  0) 0) |
| [39] |
Ha T K T, Maeda M, Fujiwara T, et al. Effects of soil type and nitrate concentration on denitrification products (N2O and N2) under flooded conditions in laboratory microcosms[J]. Soil Science and Plant Nutrition, 2015, 61(6): 999-1004. DOI:10.1080/00380768.2015.1094747
(  0) 0) |
| [40] |
Shi J, Wang J, Lv J F, et al. Microplastic presence significantly alters soil nitrogen transformation and decreases nitrogen bioavailability under contrasting temperatures[J]. Journal of Environmental Management, 2022, 317: 115473. DOI:10.1016/j.jenvman.2022.115473
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


