2. 中国地质大学(武汉)环境学院, 武汉 430074;
3. 农产品产地环境监测北京市重点实验室, 北京 100097
2. School of Environment, China University of Geosciences (Wuhan), Wuhan 430074, China;
3. Beijing Key Laboratory of Environmental Monitoring in Agricultural Product Production Areas, Beijing 100097, China
微塑料(Microplastics,MPs)污染已成为全球性的环境问题,其在农田土壤中的积累尤为严重[1]。这些微小的塑料颗粒不仅广泛分布于农田土壤环境中[2],而且由于其难以降解的特性,对土壤生态系统构成了长期威胁[3]。它们不仅能够改变土壤的物理化学性质,还可能通过食物链对人类健康构成潜在风险[4]。MPs因其高比表面积和疏水性,具有吸附土壤中有机污染物的能力,这使得它们成为农药和其他有机污染物的潜在载体[5]。MPs在土壤中的积累可能导致污染物环境行为的改变,进而影响土壤生态系统健康和农作物安全。
与MPs污染同样令人担忧的是农田土壤中新烟碱类农药的残留问题。新烟碱类农药,作为一类新型高效、低毒、环境友好的杀虫剂,在农业生产中得到了广泛应用[6]。然而,这些农药的过度使用和不当处理导致其在土壤中残留,已有研究表明新烟碱类农药广泛存在于中国农田土壤中[7]。这些农药残留不仅可对非靶标生物产生毒性,还可通过食物链富集,最终对人类健康造成威胁[8]。因此,研究新烟碱类农药在农田土壤中的行为和环境影响,对于保障食品安全和生态平衡具有重要意义。
尽管已有研究关注了MPs和新烟碱类农药的环境行为,但目前的研究多集中于单一污染物的行为,MPs和新烟碱类农药共存于农业环境中,它们之间很可能会发生一些相互作用,对于这种复合污染体系的认识尚显不足。有限的研究揭示了MPs能够吸附新烟碱类农药[9],但目前研究多局限于传统MPs,并且MPs对这些农药的解吸行为和生物有效性的影响尚未得到充分研究。这种相互作用可能对农药的环境归宿及生态风险评估产生深远影响,是一个亟待解决的科学问题。因此,深入研究MPs对新烟碱类农药解吸和生物有效性的影响,对于全面理解复合污染体系下的环境行为和制定相应的风险管理措施具有重要意义。
因此,本研究选取了可降解塑料聚丁二酸丁二醇酯(Poly(butylene succinate),PBS)和噻虫啉(Thiacloprid,THI)作为研究对象,因为PBS是可降解地膜中常用材料[10],THI是一种典型的新烟碱类农药,在很多研究中的检出率高达100%[11]。探讨了THI在PBS上的吸附-解吸行为,以及环境因素如pH、盐度和溶解性有机质(DOM)浓度对吸附行为的影响。此外,本研究还采用梯度扩散薄膜(DGT)技术,评估了MPs对土壤中THI生物有效性的影响,旨在揭示MPs对土壤中新烟碱类农药环境行为的潜在影响。研究结果将为理解MPs与农药相互作用的机制提供科学依据,为农药的环境风险评估和管理提供新视角。
1 材料与方法 1.1 供试材料THI(纯度大于99%)和内标物噻虫啉-d4(纯度大于99%)购自多伦多研究化学公司(加拿大)。乙腈和甲醇购自Fisher Scientific(美国)。盐酸(HCl)、氢氧化钠(NaOH)、氯化钠(NaCl)购自国药集团(中国)。腐殖酸(HA)(纯度大于90%)购自麦克林(中国)。牛磺胆酸钠(纯度为98%)购自上海源叶生物科技有限公司。PBS颗粒购自广州杰诚塑业有限公司,粒径为150~300 μm,接触角为55.3°,比表面积为0.419 3 m2·g–1。红壤和黑土(表 1)分别采集自江西省和黑龙江省,这两种土壤类型因其在中国的普遍性和理化特征的显著差异而被选为研究对象。
|
|
表 1 土壤的基本理化性质 Table 1 Basic physical and chemical properties of soils |
称取100.0 mg MPs加入棕色玻璃瓶中,随后加入10.0 mL(5.0 mg·L–1)THI溶液,在25℃、180 r·min–1条件下充分混合。分别在5、10、20、30、45、60、80、100、120、180、360、720、1 440、2 160 min时,取出对应的样品瓶,用注射器取1.0 mL溶液,使用0.22 μm疏水聚四氟乙烯(PTFE)针头式过滤器(已验证对THI的吸附可忽略)过滤后采用高效液相色谱法(HPLC)检测THI浓度。同时设置不加THI的空白和不加MPs的对照实验,每个取样时间设置三个重复。在吸附等温线实验中,将THI的初始浓度设置为0.5、1.0、2.0、5.0、8.0和10.0 mg·L–1,根据吸附动力学的结果确定取样时间为24 h(吸附达到平衡),其余操作与吸附动力学实验一致。
1.3 吸附影响因素实验使用HCl、NaOH、NaCl、HA调整THI工作液的pH(3.0、5.0、7.0、9.0、11)、盐度(0.5、20、35 g·kg–1)和DOM浓度(1.0、10.0、20.0、30.0、50.0 mg·L–1)来研究影响吸附的环境因素。以上实验中THI的初始浓度均设置为5.0 mg·L–1,取样时间固定为24 h,剩余操作与吸附动力学实验一致。
1.4 解吸动力学和解吸等温线实验研究了吸附THI的PBS在纯水和模拟肠道液(SIF)环境下的解吸情况。SIF的配制参考之前的研究[12]。在吸附动力学相同的实验条件达到吸附平衡后,用注射器小心取出5 mL溶液(尽量避免吸出MPs),随后添加等量的超纯水或SIF。再将玻璃瓶放回恒温摇床上进行解吸,分别在5、10、20、30、45、60、80、100、120、180、360、720、1 440、2 160 min时取样,剩余操作与吸附动力学实验一致。
1.5 生物有效性实验本研究采用DGT技术研究PBS对THI生物有效性的影响。DGT技术是以动力学原理为基础的原位被动采样技术,能准确测量土壤溶液及固相释放的有效态浓度,模拟植物根系吸收,具有操作简便、高效、经济、准确性高等优势。DGT的制备和提取方法参考之前的研究[13]。在实验中,向土壤中加入THI和PBS,使土壤THI浓度达到0.5 mg·kg–1,PBS在土壤中的质量占比分别为1%、5%。然后,用超纯水将土壤湿润至60% 最大持水量(MWHC),在恒温培养箱中放置5 d。再将土壤润湿至100% MWHC,在恒温培养箱中放置24 h。然后称取30.0 ± 0.1 g在玻璃培养皿中,放置DGT采样器,24 h后取出DGT,立即对DGT吸附膜进行提取。同时设置不加MPs的对照,每个实验做三个重复。
1.6 高效液相色谱分析方法吸附–解吸动力学、等温线和环境因素对吸附的影响实验中的样品通过HPLC(安捷伦1260,美国)分析THI的浓度,DGT提取液采用超高效液相色谱串联质谱技术测定THI含量,具体分析参数参考之前的研究[14]。
1.7 数据处理吸附动力学实验采用伪一级动力学[15]、伪二级动力学[16]模型对吸附动力学结果进行分析。采用亨利(Henry)模型[17]、朗缪尔(Langmuir)模型[18]和弗罗因德利希(Freundlich)模型[19]对吸附等温线实验结果进行分析。THI的生物有效性浓度采用式(1)计算[13]:
| $ {{\text{C}}_{{\text{DGT}}}} = \frac{{M\vartriangle g}}{{{D_{\text{e}}}{\text{A}}t}} $ | (1) |
式中,CDGT为THI的生物有效性浓度,μg·L–1;M为DGT中累积的THI的质量,ng;Δg为扩散膜和滤膜的厚度,cm;A为DGT装置的开口面积,cm2;t为DGT装置的放置时间,s;De为待测物在扩散膜里的扩散系数,cm2·s–1。使用Origin 2021绘图,使用SPSS 25.0分析实验数据,使用单因素方差分析分析组间差异性,显著性水平设定为P < 0.05。
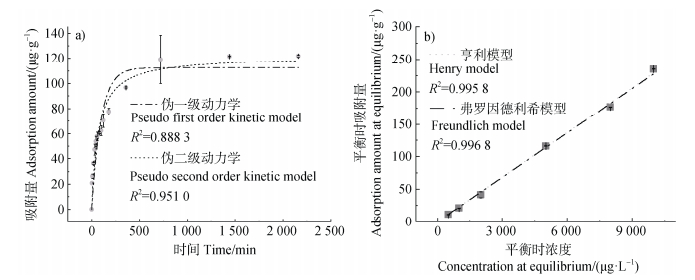
2 结果与讨论 2.1 聚丁二酸丁二醇酯(PBS)对噻虫啉(THI)的吸附动力学和吸附等温线PBS对THI的吸附量在吸附开始2 h内迅速增加,随后吸附速度变缓,在24 h时吸附基本达到平衡(图 1a)。这可能是由于初始固液浓度差异大,促进了THI从溶液向PBS的迁移。此外,PBS表面的大量吸附位点提供了传质驱动力,这在吸附过程中也起到了重要作用。随着时间的推移,PBS和溶液中的THI达到平衡,形成固定的比例,PBS表面的吸附位点趋于饱和[20],导致THI和PBS之间的相互作用减弱。因此,吸附量的增长逐渐减速,最终达到平衡。
|
图 1 聚丁二酸丁二醇酯(PBS)对噻虫啉(THI)的吸附动力学(a)和吸附等温线(b) Fig. 1 Adsorption kinetics (a) and adsorption isotherm (b) of thiacloprid (THI) by poly (butylene succinate) (PBS) |
从吸附动力学的拟合结果(图 1a)可以看出,伪二级动力学模型拟合结果可更好地拟合THI在PBS上的吸附,也说明PBS对于THI的吸附以化学吸附为主。化学吸附不仅包括静电相互作用和氢键,还包括π-π相互作用等多种机制。例如,含有芳香环的有机污染物可通过π-π相互作用与微塑料表面发生强烈的化学吸附[21]。
Henry模型和Freundlich模型均能很好地拟合(R2 > 0.99)PBS对于THI的吸附过程,但是不能用Langmuir模型拟合(图 1 b,表 2)。这表明PBS对于THI的吸附是多层吸附,吸附主要受分配作用影响。此外,PBS对于THI的吸附是高度线性的,说明分布在PBS和相邻水层之间的THI通过范德华力和氢键吸附至MPs上[21]。
|
|
表 2 聚丁二酸丁二醇酯(PBS)对噻虫啉(THI)的吸附动力学和吸附等温线拟合参数 Table 2 Adsorption kinetics and isotherm fitting parameters of poly(butylene succinate)(PBS)for thiacloprid(THI) |
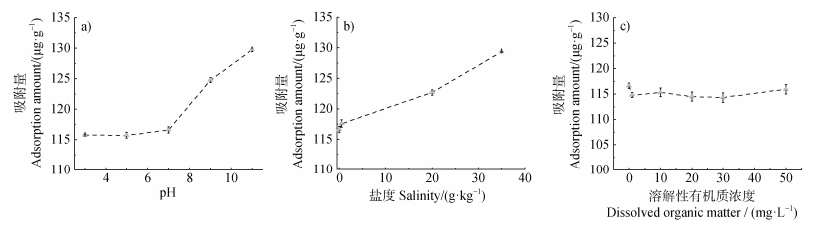
溶液pH对吸附的影响主要表现在两个方面:一方面是污染物的存在形式或溶解度的变化;另一方面是MPs表面电荷的变化,从而影响MPs对污染物的吸附行为。如图 2a所示,随着溶液pH的增加,PBS对于THI的平衡吸附量呈上升趋势。
|
图 2 环境因素(a. pH,b. 盐度,c. 溶解性有机质浓度)对吸附的影响 Fig. 2 The Influence of environmental factors (a. pH, b. Salinity, c. Dissolved organic matter concentration)on adsorption |
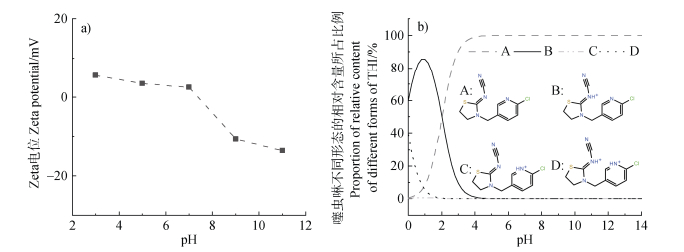
由图 3可以看出,在pH为3.0和5.0时,PBS的Zeta电位均为正电位,而在酸性条件下,部分THI会以阳离子态存在于溶液中。在酸性条件下,PBS表面的正电位会和阳离子态的THI产生静电排斥,从而抑制THI在PBS表面的吸附;而当溶液的pH增加时,PBS表面的Zeta电位逐渐减小甚至变为负电位,THI在溶液中的存在形式也全部变为分子态,PBS与THI之间的静电斥力会减弱,因此PBS对于THI的吸附量也会增加,这也表明静电相互作用是影响THI在PBS上吸附的关键因素。之前的研究表明,对于可电离物质,pH的变化对于吸附量的影响比较大,例如,几项研究表明了pH对四环素[22]在MPs上的吸附有较大的影响;而对于不可电离的物质,pH对其吸附量的影响通常是可忽略的,例如,许佰乐[23]的研究表明pH对聚乙烯(PE)吸附磺胺甲恶唑几乎无影响。
|
注:A:中性形态;B:单质子化形态;C:双质子化形态;D:三质子化形态。 Note: A: neutral form; B: monomeric form; C: biprotonated form; D: triple protonated form. 图 3 不同pH下PBS的Zeta电位(a)和THI不同形态的相对含量所占比例(b) Fig. 3 Zeta potential of PBS (a) and the proportion of relative content of different forms of THI (b) at different pH |
由图 2b可看出,随着盐度的增加,THI在PBS上的吸附量略有增加。随着盐度从0.5 g·kg–1增至35 g·kg–1,PBS对于THI的吸附量增加了10.93%。一方面可能是盐析作用,NaCl的加入可能会产生电解质离子的强烈水合作用,减少溶剂中的有效水体积,并使农药盐析,从而更容易被MPs吸附[9]。还有一些研究表明,NaCl会中和污染物和MPs表面的负电荷,减缓了静电排斥,从而促进吸附[24]。此外,盐度增加时,MPs的双电层可能被压缩以具有更高的堆积密度,并且水合层的厚度可能减小,从而促进吸附[24]。
2.2.3 DOM对吸附的影响随着DOM浓度的增加,THI在PBS上的吸附量变化不明显(图 2 c)。之前也有研究表明,MPs和DOM之间的相互作用可忽略不计。例如,许佰乐[23]发现DOM对PE吸附磺胺甲恶唑的行为几乎无影响,DOM对PE的亲和力低于磺胺甲恶唑。
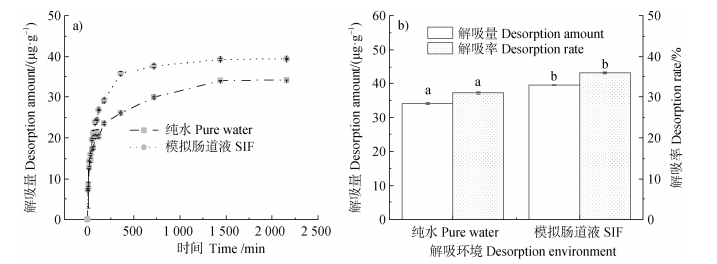
2.3 PBS对THI的解吸PBS上THI的解吸量随时间变化如图 4a所示,纯水和SIF条件下解吸达到平衡所需的时间相同。PBS上THI在SIF中的最大解吸量为39.4 μg·g–1,为纯水中的1.157倍(图 4b)。Xu等[12]的研究表明,SIF中MPs上菲的解吸率(34.6%~60.4%)也显著高于背景溶液中(12.63%~22.21%)。这些现象可解释为由于肠道表面活性剂的存在,其主要通过增加颗粒内孔的扩散速率来提高聚合物的解吸率[25]。另一个可能的原因是在低pH下MPs表面的负电位降低。此外,部分THI可能会以阳离子态存在于溶液中,由于静电排斥导致THI更易发生解吸。因此,当吸附了污染物的MPs被动物摄取后,被MPs吸附了的污染物会在肠道液的条件下进行解吸,而且相对于水环境而言,MPs被动物摄取后将会有更大的潜在风险。
|
注:SIF,模拟肠道液。不同小写字母表示不同解吸条件下的差异,P < 0.01。 Note: SIF, Simulated intestinal fluid. Lowercase letters indicate differences under different desorption conditions, P < 0.01. 图 4 PBS对THI的解吸动力学曲线(a)以及解吸量和解吸率(b) Fig. 4 Desorption kinetics curve (a), and desorption amount and rate (b) of THI by PBS |
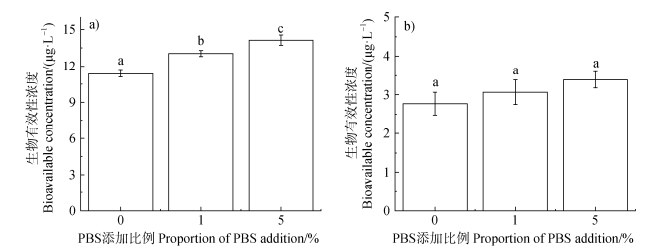
CDGT的变化反映了土壤中THI生物有效性的变化,土壤中CDGT的变化如图 5所示。可以看出红壤和黑土中,添加PBS后CDGT均要高于未添加土壤,并且随着PBS添加比例的增加这种差异继续增大,说明添加PBS后土壤中THI生物有效性增加。目前关于MPs对于土壤中污染物生物有效性的研究还较少,Wang等[26]的研究表明,PE的添加增加了土壤中镉的生物有效性,并且增加的程度随着PE的添加量而增加。Yang等[27]的研究表明,在红壤中添加聚氯乙烯(PVC)21 d后生物有效性Hg2+浓度增加,生物有效性甲基汞减少;而在碱性土中生物有效性Hg2+和甲基汞浓度均减小。MPs改变污染物生物有效性一个原因可能是,MPs可能通过一系列吸附和解吸过程影响污染物在土壤中的迁移和转化,从而导致土壤中污染物有效性变化[26]。另一个原因可能是,MPs会改变土壤自身的理化性质并占据土壤中的吸附位置,使土壤中的污染物变得更加不稳定,从而使污染物更易被动植物摄取[28-29]。
|
注:PBS添加比例为在土壤中的质量百分比。不同小写字母表示不同PBS添加量间的差异,P < 0.01。 Note: The PBS addition ratio is the mass percentage in the soil. Lowercase letters indicate differences in the amount of PBS added, P < 0.01. 图 5 土壤(a. 红壤,b. 黑土)中不同PBS添加量下THI的生物有效性浓度 Fig. 5 Bioavailable concentrations of THI in soils (a. red soil and b. black soil) with different amounts of PBS added |
本研究深入探讨了MPs与新烟碱类农药在农田土壤中的复合污染问题,对于理解土壤生态系统的健康和农作物安全性具有重要意义。通过一系列实验,发现PBS MPs对THI的吸附主要为化学吸附和多层吸附。pH、盐度会影响PBS对THI的吸附行为。在模拟肠道液条件下,PBS对THI的解吸要高于超纯水环境。此外,DGT技术的应用进一步证实了MPs能够增加土壤中THI的生物有效性,这可能对土壤生态系统和农作物安全性构成潜在风险。本研究结论不仅丰富了对MPs与农药相互作用机制的认识,而且为评估农药的环境风险和管理提供了新的视角。然而,本研究也存在一些局限性,例如,对多种MPs和农药共存条件下发生的相互作用的探索不足。此外,研究MPs对土壤微生物群落结构和功能的影响,以及它们如何影响农药的环境归宿和生态毒性,也是未来研究的重要方向。
| [1] |
Zhang Y, Wang K, Chen W Z, et al. Effects of land use and landscape on the occurrence and distribution of microplastics in soil, China[J]. Science of the Total Environment, 2022, 847: 157598. DOI:10.1016/j.scitotenv.2022.157598
(  0) 0) |
| [2] |
Xue Y H, Li J, Jin T, et al. Meso- and microplastic contamination in mulching cultivated soil at a national scale, China[J]. Journal of Cleaner Production, 2023, 418: 138215. DOI:10.1016/j.jclepro.2023.138215
(  0) 0) |
| [3] |
Liu X B, Dong X H, Xie Z H, et al. Ecological effects and biodegradation of microplastics in soils (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(2): 349-363. DOI:10.11766/trxb202102240040 [刘鑫蓓, 董旭晟, 解志红, 等. 土壤中微塑料的生态效应与生物降解[J]. 土壤学报, 2022, 59(2): 349-363.]
(  0) 0) |
| [4] |
Feng X Y, Sun Y H, Zhang S W, et al. Ecological effects of microplastics on soil-plant systems (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 299-313. DOI:10.11766/trxb202007190402 [冯雪莹, 孙玉焕, 张书武, 等. 微塑料对土壤-植物系统的生态效应[J]. 土壤学报, 2021, 58(2): 299-313.]
(  0) 0) |
| [5] |
Kou S Q, Guan Z, Lu X Y, et al. Migration of microplastics in soil and its effect on organic pollutants: A review (In Chinese)[J]. Soils, 2024, 56(3): 457-470. [寇诗棋, 关卓, 鲁旭阳, 等. 土壤中微塑料迁移及其对有机污染物的影响研究进展[J]. 土壤, 2024, 56(3): 457-470.]
(  0) 0) |
| [6] |
Ge L, Wang X, Zhang Y N. Research progress on degradation characteristics of neonicotinoid insecticides (In Chinese)[J]. Soils, 2022, 54(6): 1093-1100. [葛玲, 王新, 张亚楠. 新烟碱类杀虫剂降解特性研究进展[J]. 土壤, 2022, 54(6): 1093-1100.]
(  0) 0) |
| [7] |
Hou J, Wang L X, Wang J Z, et al. A comprehensive evaluation of influencing factors of neonicotinoid insecticides (NEOs) in farmland soils across China: First focus on film mulching[J]. Journal of Hazardous Materials, 2024, 470: 134284. DOI:10.1016/j.jhazmat.2024.134284
(  0) 0) |
| [8] |
Zhang J, Wang Y Y, Wurjihu S, et al. Comprehensive analysis of neonicotinoids in Chinese commercial honey and pollen: A corresponding health risk assessment for non-targeted organisms[J]. Science of the Total Environment, 2024, 919: 170937. DOI:10.1016/j.scitotenv.2024.170937
(  0) 0) |
| [9] |
Li H, Wang F H, Li J N, et al. Adsorption of three pesticides on polyethylene microplastics in aqueous solutions: Kinetics, isotherms, thermodynamics, and molecular dynamics simulation[J]. Chemosphere, 2021, 264: 128556. DOI:10.1016/j.chemosphere.2020.128556
(  0) 0) |
| [10] |
Rajgond V, Mohite A, More N, et al. Biodegradable polyester-polybutylene succinate (PBS): A review[J]. Polymer Bulletin, 2024, 81(7): 5703-5752. DOI:10.1007/s00289-023-04998-w
(  0) 0) |
| [11] |
Mahai G G, Wan Y J, Xia W, et al. Neonicotinoid insecticides in surface water from the central Yangtze River, China[J]. Chemosphere, 2019, 229: 452-460. DOI:10.1016/j.chemosphere.2019.05.040
(  0) 0) |
| [12] |
Xu J P, Zhang K, Wang L, et al. Strong but reversible sorption on polar microplastics enhanced earthworm bioaccumulation of associated organic compounds[J]. Journal of Hazardous Materials, 2022, 423: 127079. DOI:10.1016/j.jhazmat.2021.127079
(  0) 0) |
| [13] |
Xiong J W, Pu C, Qian Z, et al. Diffusive gradients in thin-films (DGT) for in situ measurement of neonicotinoid insecticides (NNIs) in waters[J]. Water Research, 2025, 269: 122772. DOI:10.1016/j.watres.2024.122772
(  0) 0) |
| [14] |
Wang K, Li C, Li H F, et al. Interactions of traditional and biodegradable microplastics with neonicotinoid pesticides[J]. Science of the Total Environment, 2024, 947: 174512. DOI:10.1016/j.scitotenv.2024.174512
(  0) 0) |
| [15] |
Ho Y S, McKay G. Sorption of dye from aqueous solution by peat[J]. Chemical Engineering Journal, 1998, 70(2): 115-124. DOI:10.1016/S0923-0467(98)00076-1
(  0) 0) |
| [16] |
Ho Y S, McKay G. Kinetic models for the sorption of dye from aqueous solution by wood[J]. Process Safety and Environmental Protection, 1998, 76(2): 183-191. DOI:10.1205/095758298529326
(  0) 0) |
| [17] |
Jiang M Y, Hu L Y, Lu A X, et al. Strong sorption of two fungicides onto biodegradable microplastics with emphasis on the negligible role of environmental factors[J]. Environmental Pollution, 2020, 267: 115496. DOI:10.1016/j.envpol.2020.115496
(  0) 0) |
| [18] |
Langmuir I. The adsorption of gases on plane surfaces of glass, mica and platinum[J]. Journal of the American Chemical Society, 1918, 40(9): 1361-1403. DOI:10.1021/ja02242a004
(  0) 0) |
| [19] |
Freundlich H. Über die adsorption in lösungen[J]. Zeitschrift für Physikalische Chemie, 1907, 57(1): 385-470.
(  0) 0) |
| [20] |
Moog D, Schmitt J, Senger J, et al. Using a marine microalga as a chassis for polyethylene terephthalate (PET) degradation[J]. Scientific Reports, 2019, 18(1): 171.
(  0) 0) |
| [21] |
Lončarski M, Gvoić V, Prica M, et al. Sorption behavior of polycyclic aromatic hydrocarbons on biodegradable polylactic acid and various nondegradable microplastics: Model fitting and mechanism analysis[J]. Science of the Total Environment, 2021, 785: 147289. DOI:10.1016/j.scitotenv.2021.147289
(  0) 0) |
| [22] |
Xu B L, Liu F, Brookes P C, et al. Microplastics play a minor role in tetracycline sorption in the presence of dissolved organic matter[J]. Environmental Pollution, 2018, 240: 87-94. DOI:10.1016/j.envpol.2018.04.113
(  0) 0) |
| [23] |
Xu B L. Adsorption behavior and mechanism of microplastics on organic pollutants in soil water environment[D]. Hangzhou: Zhejiang University, 2020.[许佰乐. 土水环境中微塑料对有机污染物的吸附行为及机理[D]. 杭州: 浙江大学, 2020.]
(  0) 0) |
| [24] |
Ma J, Zhao J H, Zhu Z L, et al. Effect of microplastic size on the adsorption behavior and mechanism of triclosan on polyvinyl chloride[J]. Environmental Pollution, 2019, 254: 113104. DOI:10.1016/j.envpol.2019.113104
(  0) 0) |
| [25] |
Kang K H, Kim H U, Lim K H. Effect of temperature on critical micelle concentration and thermodynamic potentials of micellization of anionic ammonium dodecyl sulfate and cationic octadecyl trimethyl ammonium chloride[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2001, 189(1/2/3): 113-121.
(  0) 0) |
| [26] |
Wang F L, Wang X X, Song N N. Polyethylene microplastics increase cadmium uptake in lettuce (Lactuca sativa L.) by altering the soil microenvironment[J]. Science of the Total Environment, 2021, 784: 147133. DOI:10.1016/j.scitotenv.2021.147133
(  0) 0) |
| [27] |
Yang X, Li Z H, Ma C, et al. Microplastics influence on Hg methylation in diverse paddy soils[J]. Journal of Hazardous Materials, 2022, 423: 126895. DOI:10.1016/j.jhazmat.2021.126895
(  0) 0) |
| [28] |
Zhang S W, Han B, Sun Y H, et al. Microplastics influence the adsorption and desorption characteristics of Cd in an agricultural soil[J]. Journal of Hazardous Materials, 2020, 388: 121775. DOI:10.1016/j.jhazmat.2019.121775
(  0) 0) |
| [29] |
de Souza Machado A A, Lau C W, Kloas W, et al. Microplastics can change soil properties and affect plant performance[J]. Environmental Science & Technology, 2019, 53(10): 6044-6052.
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


