塑料污染已成为全球性重大环境问题。2022年,全球塑料产量高达4亿吨,约占全球固体废弃物总量的12%[1]。中国作为塑料的主要生产国和消费国,2022年塑料产量占全球总量的32%,消费量约占全球的30%[2]。大量塑料垃圾因管理不善流入环境,在物理、化学和生物作用下逐渐破碎化[3],成为陆地和海洋生态系统中微/纳米塑料(MNPs)污染的主要来源。研究表明,MNPs不仅能吸附环境中的有害物质,而且易被生物摄入,通过食物链在生态系统中富集,对生物多样性和生态平衡构成潜在威胁[4-6]。MNPs已被发现广泛存在于人体组织、血液甚至胎盘中,可能通过引发炎症反应、氧化应激等机制,对人体健康造成潜在危害[7-9]。鉴于MNPs对生态环境和人类健康的严重威胁,迫切需要深入研究其来源、归宿、生态效应和毒性机制。
近年来,陆地生态系统中MNPs污染及其对环境健康和食品安全的潜在威胁日益受到关注。MNPs主要通过农用地膜破碎、有机肥施用、污水灌溉、污泥农用、轮胎磨损、大气沉降以及地表径流等途径进入土壤并不断累积[10-14]。已有研究报道食用蔬菜[15]、作物[16]能吸收和积累亚微米级甚至微米级球形塑料颗粒,并初步揭示了其进入植物体的通道和机制[17-18]。然而,真实环境中存在的MNPs形态多样,尤其是纤维微塑料在大气、海洋和土壤中被大量检出[13,19-20]。纤维微塑料的主要来源包括纺织品(如地毯、衣物等)[21]、渔业活动中使用的渔网和绳索[22],以及塑料制品的生产和使用过程[23]。纤维微塑料通过多种途径进入环境,例如通过污水排放进入水体,进而通过灌溉等方式进入农业土壤[24]。有研究估计,陆地环境中纤维微塑料的累积量甚至超过了水体中的含量[25],凸显了陆地环境,特别是土壤环境受纤维微塑料污染的严重性。值得注意的是,纤维微塑料显著影响土壤性质、微生物群落和植物生长。例如,其线性缠结特性可能改变土壤团聚体的形态,进而影响土壤的通气性和排水性[26-27]。此外,纤维微塑料还可能影响土壤微生物群落的结构和功能,例如改变微生物多样性、影响养分循环过程[28]。更重要的是,多项研究表明纤维微塑料可能通过诱导氧化应激等机制对植物生长产生负面影响,例如抑制种子萌发、降低生物量、影响根系发育等[29-30],这些影响可能最终破坏土壤生态系统的平衡。
尽管已有研究揭示了球形MNPs的环境行为,但纤维微塑料由于其独特的形状和特性,可能表现出不同的生态效应。形状对微/纳米塑料在生物体内的滞留和穿透生物屏障的能力具有显著影响[31-32],纤维微塑料的形状使其更容易穿透生物组织,并在生物体内滞留,从而可能引起一系列健康问题,如炎症反应、免疫系统紊乱等[32]。因此,深入研究纤维微塑料的生物积累性,不仅有助于拓展对不同形态微/纳米塑料生态风险的科学认知,也为制定相应环境管理策略提供科学依据。
为深入探究纤维微塑料在高等植物中的行为,本研究以玉米(Zea mays L.)为模型植物,选择聚丙烯腈(Polyacrylonitrile,PAN)纤维微塑料作为研究对象。PAN是一种具有较强环境持久性的合成纤维[33],也是环境中常见的纤维微塑料类型[13]。本研究采用特异性荧光染料标记PAN纤维微塑料的方法,利用激光共聚焦显微镜(CLSM)和扫描电子显微镜(SEM)观察其在玉米幼苗体内的积累和分布,旨在探究PAN纤维微塑料在玉米体内的吸收、迁移转化规律。
1 材料与方法 1.1 PAN纤维微塑料制备与表征为了准确追踪PAN纤维微塑料在玉米体内的吸收和迁移,采用荧光标记法对PAN纤维进行标记。将PAN粉末与荧光染料按质量比1:100混合均匀,分散于N,N-二甲基甲酰胺(DMF)中,超声分散30 min,制备得到纺丝液。采用静电纺丝技术,在15 kV电压、1.0 mL·h–1流速、15 cm收集距离的条件下,将纺丝液通过直径为0.9 mm的针头纺丝,得到荧光标记的PAN纳米纤维膜。将纳米纤维膜裁剪成1 cm×1 cm的小块,包埋于OCT包埋剂中,并进行冷冻切片(厚度为10 μm)。经水和酒精反复清洗和过滤后,得到纯净的荧光标记PAN纤维微塑料(NB-PAN和NBD-Cl-PAN)。PAN纤维微塑料分别用扫描电子显微镜(S-4800,日立,日本)和荧光显微镜(Ni-E,尼康,日本)对其尺寸、形貌和荧光特性进行观察。将制备好的荧光标记PAN纤维分散于超纯水中,配制成浓度为2 mg·mL–1的储备液,用于后续实验。
1.2 供试玉米幼苗及生长条件玉米种子(郑单958)由山东寿禾种业提供。挑选饱满大小一致的种子,先用0.5% NaClO(分析纯,国药)溶液浸泡处理10 min,进行表面灭菌。随后用去离子水将种子洗涤三次,以洗去残留的NaClO溶液。将种子置于湿润的无菌纱布上,在27 ℃下,避光催芽4天。种子萌发后在纯净水中生长5天。然后将玉米幼苗取出洗净,转移至Hoagland营养液中,在人工气候室25±2 ℃,12:12 h光照:黑暗和70±5% 相对湿度条件,继续培养生长7天。Hoagland营养液组成为:2.5 mmol·L–1 CaNO3和KNO3,10 μmol·L–1 FeEDTANa2,0.1 mmol·L–1 K2HPO4,75 μmol·L–1 KCl,10 μmol·L–1 H3BO3,1 mmol·L–1 MgSO4,4 μmol·L–1 MnCl2·4H2O,0.5 μmol·L–1 CuSO4·5H2O,1 μmol·L–1 ZnSO4·7H2O和0.2 μmol·L–1 Na2MoO4 · 2H2O.
1.3 植物吸收富集将NB-PAN和NBD-Cl-PAN纤维微塑料储备液超声分散3 min后,与Hoagland营养液混合,配制成浓度分别为10 mg·L–1的PAN纤维微塑料暴露液。试验同时设置不添加PAN纤维微塑料的Hoagland营养液作为对照处理组。所有组别均使用相同批次的Hoagland营养液,并在相同的环境条件下(包括光照、温度、湿度等)进行培养。确保除微塑料这一变量外,所有其他实验条件均保持一致。每个处理六个重复,每个盆钵(1 L)移入两株玉米苗。移栽后的幼苗在人工气候室继续生长。培养过程中,人工气候室条件设置为:温度25±2℃,相对湿度70±5%,光周期12 h /12 h。每隔3天更换一次暴露液。培养14天后,取样分析。利用激光共聚焦显微镜(FluoView FV1000,奥林巴斯,日本)和扫描电子显微镜(S-4800,日立,日本)对玉米根、茎、叶等组织中的PAN纤维微塑料进行观察和定位。CLSM可以实现对荧光标记的PAN纤维微塑料在植物组织内的成像,SEM则可以观察PAN纤维微塑料在植物组织中的形态特征和分布情况。
1.4 激光共聚焦显微镜观察收集吸收富集实验后新鲜的玉米根、茎、叶,用超纯水冲洗干净,根部超声清洗备用。选取根基部、侧根和根尖部位,地上部切取茎和叶,分别包埋于4%低熔点琼脂糖中。利用半自动振动切片机(VT1200S,徕卡,德国)切取100 μm厚的半薄切片,置于载玻片上,用10%浓度的磷酸缓冲盐溶液(PBS)缓冲液封片。使用激光共聚焦显微镜(FluoView FV1000,奥林巴斯,日本),在激发/发射波长分别为488 / 515 nm和635 / 680 nm对茎叶和根部进行观察。每个样品重复观察三次,并使用Fluoview FV1000软件进行图像处理。
1.5 扫描电子显微镜观察将吸收富集实验后的玉米根系、茎和叶用超纯水冲洗干净,取与激光共聚焦显微镜观察相同的部位,切成小块后置于液氮中快速冷冻。随后进行冷冻干燥(10A,信仪,中国)处理,并利用溅射镀膜仪(Cressington model 108,Ted Pella Inc.,美国)以金靶材对样品进行60s的溅射镀膜,以增加样品的导电性。在高真空模式下,使用扫描电子显微镜,以20 kV的加速电压对样品进行观察,并获取不同放大倍数的图像。每个样品重复观察3次。
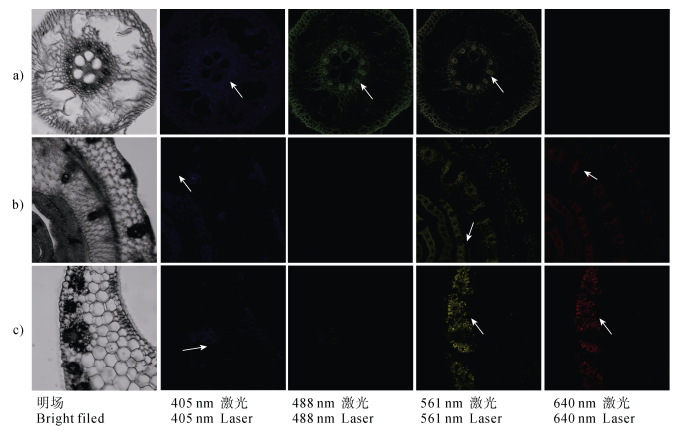
2 结果与讨论 2.1 荧光标记纤维微塑料的表征为探究纤维微塑料在植物体内的吸收和转运过程,本研究首先制备了荧光标记的PAN纤维微塑料,并对其进行了表征。采用静电纺丝技术制备了亚微米级聚丙烯腈(PAN)纤维,以模拟环境中常见的纤维微塑料污染。为有效示踪纤维微塑料在植物组织中的分布,采用高分辨共聚焦显微镜(Axio-Imager LSM-800,蔡司,德国)检测了玉米幼苗根、茎、叶的自发荧光(图 1)。结果表明,根部切片在405 nm(蓝色)、488 nm(绿色)和561 nm(橙色)激发波长下均存在一定程度的自发荧光,而在640 nm附近激发波长下背景荧光较弱(图 1a)。因此,选择激发/发射波长分别为620/680 nm的氯化耐尔蓝(Nile Blue chloride,NB)作为标记根部纤维微塑料的染料。NB是一种具有良好光稳定性和生物相容性的近红外荧光染料[34],其最大发射波长位于近红外区域(638 nm),可有效避开根部组织的主要自发荧光波段。玉米幼苗茎和叶(图 1b,图 1c)在488/561 nm波长附近自发荧光较弱,因此选择激发/发射波长分别为488/518 nm的4-氯-7-硝基-1,2,3-苯并氧杂恶二唑(4-Chloro-7-nitro-1,2,3-benzoxadiazole,NBD-Cl)作为标记茎和叶部纤维微塑料的染料。NBD-Cl是一种小分子荧光探针[35],具有较高的荧光量子产率和较长的发光寿命,其最大发射波长为467 nm,与茎叶组织的自发荧光光谱差异明显。综上,本研究选用NB和NBD-Cl两种荧光染料,分别标记PAN纤维,以区分其在植物不同组织中的分布。
|
图 1 不同激发波长下玉米幼苗根(a)、茎(b)和叶(c)组织的激光共聚焦显微成像图 Fig. 1 Confocal images of the cross section of corn seedlings root (a), stem (b), and leaf (c) under different excitation wavelengths |
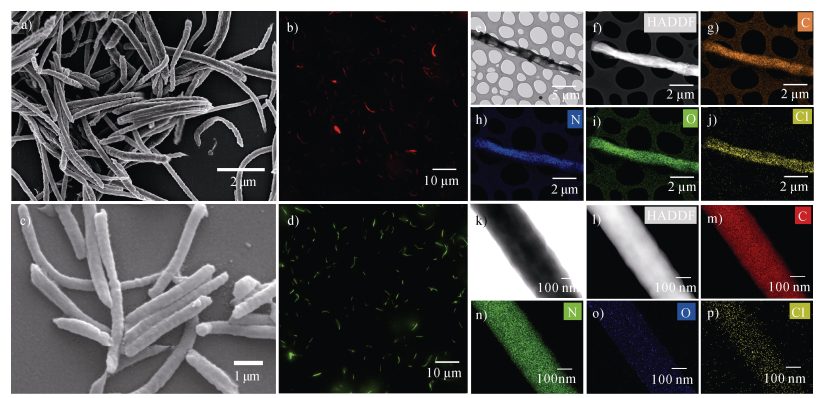
为表征制备的荧光标记PAN纤维微塑料,对其进行了形貌、尺寸和元素组成分析。SEM图像显示(图 2a,图 2c),PAN纤维呈现出均匀的纤维状形态,平均直径约为200 nm,长度主要分布在3~5 μm之间,长径比为15~25。荧光显微镜观察结果(图 2b,图 2d)表明,NB-PAN纤维在Cy5.5通道呈现出强烈的红色荧光,NBD-Cl-PAN纤维在FITC通道呈现出强烈的绿色荧光,表明所选用的荧光染料已成功结合到PAN纤维中。TEM结合元素映射分析(图 2e-图 2p)进一步证实了上述结果。高分辨TEM图像清晰地显示了PAN纤维的纤维状结构,元素映射分析结果表明,NB-PAN和NBD-Cl-PAN纤维主要由碳、氮、氧和氯元素组成。其中,氯元素的检出进一步证明了荧光染料已成功标记在PAN纤维上。通过对PAN纤维长度进行测量,结果表明47.37%的纤维长度分布在3~4 μm之间,36.84%的纤维长度分布在4~5 μm之间。与以往研究多采用球形聚苯乙烯微珠模拟微塑料不同[16,36],本研究选用长径比为20±5的PAN微塑料,更接近环境中常见纤维形态。这些表征结果为后续研究纤维微塑料在植物体内的吸收和转运过程提供了可靠的实验基础。
|
注:a. 氯化耐尔蓝荧光标记纤维微塑料SEM图;b. 氯化耐尔蓝荧光标记纤维微塑料荧光显微镜图;c. 4-氯-7-硝基-1,2,3-苯并氧杂恶二唑荧光标记纤维微塑料SEM图;d. 4-氯-7-硝基-1,2,3-苯并氧杂恶二唑荧光标记纤维微塑料荧光显微镜图;e. 氯化耐尔蓝荧光标记纤维微塑料的透射电镜图;f. 氯化耐尔蓝荧光标记纤维微塑料的高角环形暗场成像;g-j. 分别为氯化耐尔蓝荧光标记纤维微塑料的元素映射分析:C(橙)、N(蓝)、O(绿)、Cl(黄);k. 4-氯-7-硝基-1,2,3-苯并氧杂恶二唑荧光标记纤维微塑料的透射电镜图;l. 4-氯-7-硝基-1,2,3-苯并氧杂恶二唑荧光标记纤维微塑料的高角环形暗场成像;m-p. 4-氯-7-硝基-1,2,3-苯并氧杂恶二唑荧光标记纤维微塑料的元素映射分析:C(红)、N(绿)、O(蓝)Cl(黄)。 Note: a. Scanning electron microscopy (SEM) image of fiber microplastics fluorescently labeled with Nile blue chloride (NB-PAN); b. Fluorescence microscopy image of NB-PAN; c. SEM image of fiber microplastics fluorescently labeled with 4-chloro-7-nitro-1, 2, 3-benzoxadiazole (NBD-Cl-PAN); d. Fluorescence microscopy image of NBD-Cl-PAN; e. Transmission electron microscopy (TEM) image of NB-PAN; f. High-angle annular dark dark-field imaging of NB-PAN; g-j. Elemental mapping analysis of NB-PAN: C (orange), N (blue), O (green), Cl (yellow); k. TEM images of NBD-Cl-PAN; l. High-angle annular dark-field imaging of NBD-Cl-PAN; m-p. Elemental mapping analysis of NBD-Cl-PAN: C (red), N (green), O (blue), Cl (yellow). 图 2 荧光标记聚丙烯腈纤维微塑料表征 Fig. 2 Characterization of fluorescently labeled polyacrylonitrile (PAN) microfibers |
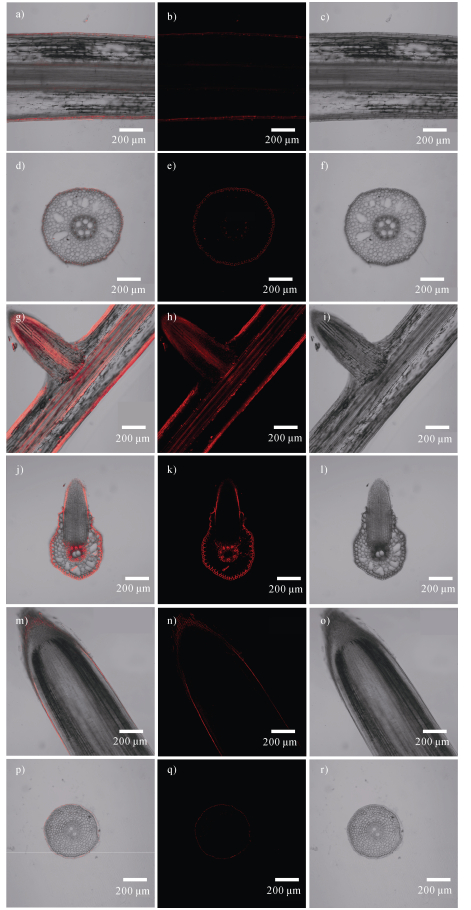
为探究纤维微塑料在玉米根部的吸收和分布特征,本研究采用激光共聚焦显微镜观察了NB-PAN纤维微塑料在根部的分布情况(图 3,图 4)。对照组玉米根的横切面和纵切面均未检测到荧光信号(图 3a-图 3f),表明实验体系无背景干扰。处理组玉米根的观察结果显示,NB-PAN纤维微塑料主要分布在根的根冠表面、新生侧根以及主根与侧根的连接处(图 4a-f)。其中,根冠和新生侧根的外表皮以及主根与侧根之间的间隙处荧光信号最为强烈,表明NB-PAN纤维微塑料主要通过这些部位进入根部。此外,还观察到部分NB-PAN纤维微塑料已经到达了中柱,即植物根部的维管束组织。

|
图 3 对照组(未添加氯化耐尔蓝标记聚丙烯腈纤维微塑料)超纯水处理7 d后玉米根基部横切(a)、纵切(d)的激光共聚焦显微成像图。其中,图a,d分别为b-c,e-f的合成图。在玉米根部横切和纵切片中未观察到红色荧光,指示在根组织中没有聚丙烯腈纤维微塑料积累 Fig. 3 Confocal images of cross and longitudinal section of corn root treated for 7 d without Nile blue fluorescently labeled polyacrylonitrile microplastics fibers. Images a, and d are the corresponding merged images of images b and c, e and f. No red fluorescence was observed in corn root transverse and longitudinal sections, indicating no accumulation of polyacrylonitrile microplastics in the root tissue |
|
图 4 氯化耐尔蓝荧光标记聚丙烯腈纤维微塑料(直径200 nm,长3~5 μm,10 mg·L–1)处理7 d后玉米根基部纵切(a)和横切(d)、侧根部纵切(g)和横切(j)、根尖部纵切(m)和横切(p)的激光共聚焦显微成像明暗场叠加的合成图。其中,图b、e、h、k、n分别为图a、d、g、j、m和p的暗场照片,图c、f、i、l、r分别为图a、d、g、j、m和p的明场照片。在玉米根部横切和纵切片中均观察到红色荧光,指示在根组织中存在聚丙烯腈纤维微塑料积累 Fig. 4 Composite images of laser confocal microscopy of the longitudinal section (a) and cross section (d) of the corn root base, the longitudinal section (g) and cross section (j) of the lateral root, and the longitudinal section (m) and cross section (p) of the root tip after 7 days of treatment with NBD-Cl-PAN (200 nm in diameter, 3-5 μm in length, 10 mg·L–1). Images b, e, h, k, and n are dark-field images, and images c, f, i, l, and r are bright field images. Red fluorescence was observed in both the cross section and longitudinal section of the corn root, indicating the accumulation of polyacrylonitrile microfibers in the root tissue |
试验结果表明,NB-PAN纤维微塑料的传输与亚微米级微球的吸收途径有所类似[17]。PAN纤维微塑料的尺寸和形态直接影响其穿透植物组织的能力。由于尺寸较大,NB-PAN纤维微塑料无法直接穿透根尖的表皮和皮层[17],而是主要通过新生侧根的间隙进入根部。侧根裂隙的存在为纤维微塑料提供了进入植物的便捷通道。此外,根部的其他损伤,如老化或机械损伤,也可能为纤维微塑料提供进入点[37]。一旦进入根部,这些纤维微塑料可能会随着根的生长而被包裹在新的细胞层中。值得注意的是,维管束附近的纤维微塑料存在纵向运输,木质部作为植物体内的运输系统,将纤维微塑料随水分和养分一起向上输送[38],甚至最终到达茎叶等地上部分。这一发现揭示了纤维微塑料在植物体内的独特运输途径,为评估其生态风险提供了重要依据。
为确认玉米根部荧光信号来源于荧光标记的PAN纤维而非植物自身,本研究采用SEM观察了玉米根部组织切片。SEM图像显示(图 5a-图 5c),NB-PAN纤维微塑料主要分布在玉米根部的表皮细胞和细胞间隙中。在木质部导管的细胞壁上也发现了纤维微塑料(图 5d-图 5g)。此外,在主根和新生侧根表皮组织之间的裂隙中,清晰可见纤维微塑料的存在(图 5h-图 5j),表明其可能通过细胞间隙等胞外运输系统进入根部组织。对比SEM图像与激光共聚焦显微镜图像,发现纤维微塑料在根部中的分布位置高度一致,进一步证实了荧光信号来源于NB-PAN纤维微塑料。值得注意的是,与以往研究中塑料微球在植物根部常以聚集状存在的现象不同[17],观察到的NB-PAN纤维微塑料在玉米根部中呈现出无序分布且多以单个存在的特点。这种区别可能是由于PAN纤维本身的特有形态引起的[39],较大的长径比使其在植物体内的存在形态与微球不同,更易于分散在植物组织中。此外,不同作物物种对纤维微塑料的吸收、积累和运输可能存在差异[40],随着暴露周期的延长其在植物体内也可能进一步发生生物转化过程。这些发现揭示了纤维微塑料在植物体内的独特行为,为深入研究其生态效应提供了重要依据。

|
图 5 氯化耐尔蓝荧光标记聚丙烯腈纤维微塑料(直径200 nm,长3~5 μm,10 mg·L–1)处理8 d后玉米的根基横切面中柱(a)和根基纵切面中柱处(d)以及根基的裂隙处纵切面(g)的扫描电镜照片。其中,图a、d、g分别为根基和侧根的全局图,图c、f、i分别为图b、e、h中红色方框处的放大图 Fig. 5 Scanning electron micrographs of root transverse section at mid-column (a) and root longitudinal section at mid-column (d) and root longitudinal section at cleft (g) of maize after 8 d of treatment with NB-PAN (200 nm in diameter, 3-5 μm in length, 10 mg·L–1). Among them, Figures a, d, and g are the global views of the base and lateral roots respectively, and Figures c, f, and i are the enlarged views of the red boxes in Figures b, e, and h, respectively |
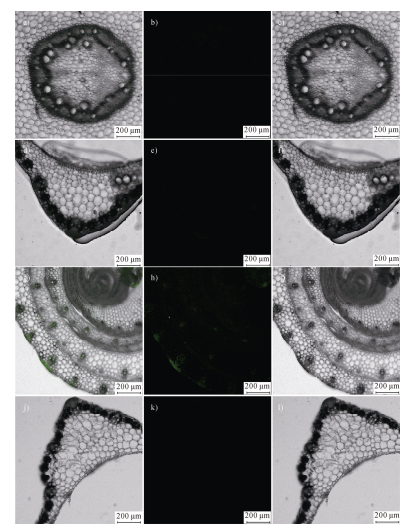
为探究纤维微塑料在玉米植株中的传输特征,本研究采用NBD-Cl标记的PAN纤维微塑料进行暴露实验。激光共聚焦显微镜观察结果显示,对照组玉米茎(图 6a)和叶(图 6d)均未检测到荧光信号,而处理组玉米根部积累的NBD-Cl-PAN纤维微塑料可以通过维管束(植物体内运输水分和养分的管道)向上运输,并在茎的木质部检测到荧光信号(图 6g)。木质部是植物体内运输水分的主要管道。这一结果表明,纤维微塑料能够随着水分的运输向上移动。然而,在两周暴露实验条件下,并未在玉米叶片的脉管组织中检测到纤维微塑料(图 6j)。PAN纤维微塑料的长径比和尺寸可能影响其在木质部导管中的移动效率[17],具有较大长径比的纤维微塑料更容易在蒸腾流的推动下发生旋转和弯曲,并频繁地与导管壁发生碰撞和摩擦。木质部导管内壁的纹孔膜等微观结构进一步增加了移动的复杂性[41]。特别是当植物蒸腾作用驱动的水分流量不足以克服纤维微塑料较大的尺寸阻碍时,其独特的形状不仅增加了在导管中的运动障碍,还可能通过穿透生物组织和植物细胞造成空间位阻。此外,植物在代谢过程中可能产生与微塑料相互作用的木质素或多糖[41],这些生物分子可能增强纤维微塑料的滞留效果。
|
图 6 对照组(未添加NBD-Cl标记聚丙烯腈纤维微塑料)超纯水处理14 d后玉米茎部切片(a)、叶片切片(d)的激光共聚焦显微成像图。在玉米茎和叶片中均未观察到绿色荧光,指示其中没有目标纤维微塑料积累。NBD-Cl荧光标记聚丙烯腈纤维微塑料(10 mg·L–1)处理14 d后玉米茎部切片(g)、叶片切片(j)的激光共聚焦显微成像明暗场叠加的合成图。其中,图a,d,g,j分别为b-c,e-f,h-i,k-l的合成图。图b、e、h、k分别为图a、d、g、j的暗场照片,图c、f、i、l分别为图a、d、g、j的明场照片。在玉米茎中观察到微弱绿色荧光,叶片中未观察到荧光信号,指示目标纤维未继续向上传输至叶片组织积累 Fig. 6 Laser confocal micrographs of corn stem sections (a) and leaf sections (d) after 14 d of ultrapure water treatment with control (no NBD-Cl-PAN). No green fluorescence was observed in either stems or leaves, indicating no accumulation of the target microfibers. Composite images of laser confocal microimaging bright and dark field superimpositions of corn stem sections (g) and leaf sections (j) after 14 d of treatment with NBD-Cl fluorescently labeled Polyacrylonitrile microfibers (10 mg·L–1). Among them, Figures a, d, g, and j are composite images of b-c, e-f, h-i, and k-l, respectively. Figures b, e, h, and k are dark-field photographs of Figures a, d, g, and j, respectively, and Figures c, f, i, and l are bright-field photographs of Figures a, d, g, and j, respectively. Faint green fluorescence was observed in the corn stems, and no fluorescent signal was observed in the leaves, indicating that the target fibers did not continue to transport upward to accumulate in the leaf tissues |
本研究证实了纤维微塑料可在玉米幼苗体内积累,这一发现引发了对其潜在影响的关注。虽然本研究主要关注纤维微塑料在植物体内的吸收和迁移过程,尚未直接考察其对植物生长的影响,但已有研究表明,纤维微塑料在植物体内积累可能通过多种机制对植物产生不利影响。例如,纤维微塑料可能通过物理阻碍作用影响植物根系对水分和养分的吸收[29,42],诱导氧化应激,损害细胞结构和功能,进而影响光合作用和叶绿素含量[43]。这些影响最终可能导致植物生长发育受阻,甚至降低作物产量。需要指出的是,纤维微塑料独特的纤维状结构可能导致其与植物组织相互作用的方式与其他类型微塑料有所不同,例如更容易缠绕在根系表面,影响根系的正常功能[44-45]。因此,针对纤维微塑料的特有影响机制还需要进一步深入研究。更重要的是,纤维微塑料在食用植物中的积累也引发了食品安全方面的担忧。虽然目前关于纤维微塑料通过食物链进入人体并造成直接健康危害的研究还相对有限,但已有研究表明,微塑料可以从植物转移到食用组织[15]。因此应高度关注包括纤维微塑料在内的不同形貌的微塑料可能通过食物链对人类健康造成的潜在风险。未来的研究需要进一步考察纤维微塑料在不同作物中的积累规律,以及长期暴露对人类健康的潜在影响,以制定有效的风险评估和管理策略。
3 结论本研究初步探明了纤维微塑料在玉米体内的吸收和转运机制,为评估其生态风险和食品安全影响提供了重要依据。通过制备长径比为20±5的亚微米级聚丙烯腈(PAN)纤维作为纤维微塑料模型,研究发现,暴露于10 mg·L–1的均匀分散PAN纤维微塑料溶液中时,纤维微塑料主要分布在根部的外表皮及维管柱。玉米根部新生侧根裂隙成为PAN纤维微塑料进入植物体内的主要通道,而根部的其他损伤(如老化或机械损伤)也可能为其提供便捷通道。此外,木质部作为连接植物地下部与地上部物质运输的通道,可将积累在根部的纤维微塑料随水分和养分一起向上输送至茎部。这些发现为进一步研究长期暴露和不同生长基质条件下纤维微塑料的迁移转化行为提供了重要的实验证据和方法学参考。然而,在14d的实验条件下,PAN纤维微塑料未被检测到到达叶片脉管系统,表明其迁移行为可能受到植物内部的物理滞留和微塑料自身物理特性的限制。此外,实验所用的营养液水培与真实土壤环境不同,农田土壤环境更为复杂,短期暴露条件下纤维微塑料在水培体系中的行为,不能直接外推至长期、复杂的土壤环境。值得注意的是,微塑料一旦被玉米吸收累积,其表面吸附的天然有机质、无机离子以及矿物胶质甚至病原微生物等,均有可能随着微塑料的吸收而在植物体内积累,并通过食物链进入人体,从而同步提高其食品安全及人体健康风险。未来研究应重点关注不同类型纤维微塑料在植物体内的长期积累、代谢和降解过程,研究不同植物对纤维微塑料的吸收、转运和积累的差异性。同时,需进一步探讨纤维微塑料对植物生长、发育、生理生化过程的影响,以及对农产品产量和品质的影响。通过深入研究,可为全面评估纤维微塑料对陆地生态系统和人类健康的潜在影响提供科学依据,为制定相应的环境保护策略提供理论支撑。
| [1] |
Geyer R, Jambeck J R, Law K L. Production, use, and fate of all plastics ever made[J]. Science Advances, 2017, 3(7): e1700782. DOI:10.1126/sciadv.1700782
(  0) 0) |
| [2] |
Wang F Y, Wang Q L, Adams C A, et al. Effects of microplastics on soil properties: Current knowledge and future perspectives[J]. Journal of Hazardous Materials, 2022, 424: 127531. DOI:10.1016/j.jhazmat.2021.127531
(  0) 0) |
| [3] |
Zurier H S, Goddard J M. Biodegradation of microplastics in food and agriculture[J]. Current Opinion in Food Science, 2021, 37: 37-44. DOI:10.1016/j.cofs.2020.09.001
(  0) 0) |
| [4] |
Li K, Luo X Y, Rony M W, et al. Low-frequency noise and border traps in irradiated nMOS and pMOS bulk Si FinFETs with SiO2/HfO2 gate dielectrics[J]. IEEE Transactions on Nuclear Science, 2023, 70(4): 442-448. DOI:10.1109/TNS.2023.3239844
(  0) 0) |
| [5] |
Allen S, Allen D, Phoenix V R, et al. Atmospheric transport and deposition of microplastics in a remote mountain catchment[J]. Nature Geoscience, 2019, 12(5): 339-344. DOI:10.1038/s41561-019-0335-5
(  0) 0) |
| [6] |
Dris R, Imhof H, Sanchez W, et al. Beyond the ocean: Contamination of freshwater ecosystems with (micro-) plastic particles[J]. Environmental Chemistry, 2015, 12(5): 539-550. DOI:10.1071/EN14172
(  0) 0) |
| [7] |
American Chemical Society. Methods for microplastics, nanoplastics and plastic monomer detection and reporting in human tissues[OL]. https://www.eurekalert.org/news-releases/478209. [2020-10-21].
(  0) 0) |
| [8] |
Leslie H A, van Velzen M J M, Brandsma S H, et al. Discovery and quantification of plastic particle pollution in human blood[J]. Environment International, 2022, 163: 107199. DOI:10.1016/j.envint.2022.107199
(  0) 0) |
| [9] |
Ragusa A, Svelato A, Santacroce C, et al. Plasticenta: First evidence of microplastics in human placenta[J]. Environment International, 2021, 146: 106274. DOI:10.1016/j.envint.2020.106274
(  0) 0) |
| [10] |
Ren S Y, Wang K, Zhang J R, et al. Potential sources and occurrence of macro-plastics and microplastics pollution in farmland soils: A typical case of China[J]. Critical Reviews in Environmental Science and Technology, 2024, 54(7): 533-556. DOI:10.1080/10643389.2023.2259275
(  0) 0) |
| [11] |
Kole P J, Löhr A J, Van Belleghem F G A J, et al. Wear and tear of tyres: A stealthy source of microplastics in the environment[J]. International Journal of Environmental Research and Public Health, 2017, 14(10): 1265. DOI:10.3390/ijerph14101265
(  0) 0) |
| [12] |
Zhang L S, Xie Y S, Liu J Y, et al. An overlooked entry pathway of microplastics into agricultural soils from application of sludge-based fertilizers[J]. Environmental Science & Technology, 2020, 54(7): 4248-4255.
(  0) 0) |
| [13] |
Zhou Q, Tian C G, Luo Y M. Various forms and deposition fluxes of microplastics identified in the coastal urban atmosphere (In Chinese)[J]. Chinese Science Bulletin, 2017, 62(33): 3902-3909. [周倩, 田崇国, 骆永明. 滨海城市大气环境中发现多种微塑料及其沉降通量差异[J]. 科学通报, 2017, 62(33): 3902-3909.]
(  0) 0) |
| [14] |
Liu M T, Lu S B, Song Y, et al. Microplastic and mesoplastic pollution in farmland soils in suburbs of Shanghai, China[J]. Environmental Pollution, 2018, 242: 855-862. DOI:10.1016/j.envpol.2018.07.051
(  0) 0) |
| [15] |
Li L Z, Zhou Q, Yin N, et al. Uptake and accumulation of microplastics in an edible plant (In Chinese)[J]. Chinese Science Bulletin, 2019, 64(9): 928-934. [李连祯, 周倩, 尹娜, 等. 食用蔬菜能吸收和积累微塑料[J]. 科学通报, 2019, 64(9): 928-934.]
(  0) 0) |
| [16] |
Li R J, Li L Z, Zhang Y C, et al. Uptake and accumulation of microplastics in a cereal plant wheat (In Chinese)[J]. Chinese Science Bulletin, 2020, 65(20): 2120-2127. [李瑞杰, 李连祯, 张云超, 等. 禾本科作物小麦能吸收和积累聚苯乙烯塑料微球[J]. 科学通报, 2020, 65(20): 2120-2127.]
(  0) 0) |
| [17] |
Li L Z, Luo Y M, Li R J, et al. Effective uptake of submicrometre plastics by crop plants via a crack-entry mode[J]. Nature Sustainability, 2020, 3(11): 929-937. DOI:10.1038/s41893-020-0567-9
(  0) 0) |
| [18] |
Luo Y M, Li L Z, Feng Y D, et al. Quantitative tracing of uptake and transport of submicrometre plastics in crop plants using lanthanide chelates as a dual-functional tracer[J]. Nature Nanotechnology, 2022, 17(4): 424-431. DOI:10.1038/s41565-021-01063-3
(  0) 0) |
| [19] |
Barrows A W, Cathey S E, Petersen C W. Marine environment microfiber contamination: Global patterns and the diversity of microparticle origins[J]. Environmental Pollution, 2018, 237: 275-284. DOI:10.1016/j.envpol.2018.02.062
(  0) 0) |
| [20] |
Chen R Z, Zhao X L, Wu X W, et al. Research progress on occurrence characteristics and source analysis of microfibers in the marine environment[J]. Marine Pollution Bulletin, 2024, 198: 115834. DOI:10.1016/j.marpolbul.2023.115834
(  0) 0) |
| [21] |
Napper I E, Thompson R C. Release of synthetic microplastic plastic fibres from domestic washing machines: Effects of fabric type and washing conditions[J]. Marine Pollution Bulletin, 2016, 112(1/2): 39-45.
(  0) 0) |
| [22] |
Liu S C, Liu S Z, Liu L, et al. Photodegradation of bisphenol A (BPA) in coastal aquaculture waters: Influencing factors, products, and pathways[J]. Chemosphere, 2024, 363: 142708. DOI:10.1016/j.chemosphere.2024.142708
(  0) 0) |
| [23] |
Aldalbahi A, El-Naggar M, El-Newehy M, et al. Effects of technical textiles and synthetic nanofibers on environmental pollution[J]. Polymers, 2021, 13(1): 155. DOI:10.3390/polym13010155
(  0) 0) |
| [24] |
Bao R Q, Wang Z Z, Qi H Y, et al. Occurrence and distribution of microplastics in wastewater treatment plant in a tropical region of China[J]. Journal of Cleaner Production, 2022, 349: 131454. DOI:10.1016/j.jclepro.2022.131454
(  0) 0) |
| [25] |
Gavigan J, Kefela T, Macadam-Somer I, et al. Synthetic microfiber emissions to land rival those to waterbodies and are growing[J]. PLoS One, 2020, 15(9): e0237839. DOI:10.1371/journal.pone.0237839
(  0) 0) |
| [26] |
de Souza Machado A A, Lau C W, Till J, et al. Impacts of microplastics on the soil biophysical environment[J]. Environmental Science & Technology, 2018, 52(17): 9656-9665.
(  0) 0) |
| [27] |
Liu S C, Liu S Z, Xiao X Y, et al. Fibrous microplastics in the environment: Sources, occurrence, impacts, and mitigation strategies[J]. Aquatic Toxicology, 2024, 276: 107119. DOI:10.1016/j.aquatox.2024.107119
(  0) 0) |
| [28] |
Rillig M C. Microplastic in terrestrial ecosystems and the soil?[J]. Environmental Science & Technology, 2012, 46(12): 6453-6454.
(  0) 0) |
| [29] |
de Souza Machado A A, Lau C W, Kloas W, et al. Microplastics can change soil properties and affect plant performance[J]. Environmental Science & Technology, 2019, 53(10): 6044-6052.
(  0) 0) |
| [30] |
Singh N, Abdullah M M, Ma X M, et al. Microplastics and nanoplastics in the soil-plant nexus: Sources, uptake, and toxicity[J]. Critical Reviews in Environmental Science and Technology, 2023, 53(18): 1613-1642. DOI:10.1080/10643389.2023.2196230
(  0) 0) |
| [31] |
Gray A D, Weinstein J E. Size- and shape-dependent effects of microplastic particles on adult daggerblade grass shrimp (Palaemonetes pugio)[J]. Environmental Toxicology and Chemistry, 2017, 36(11): 3074-3080. DOI:10.1002/etc.3881
(  0) 0) |
| [32] |
Qiao R X, Deng Y F, Zhang S H, et al. Accumulation of different shapes of microplastics initiates intestinal injury and gut microbiota dysbiosis in the gut of zebrafish[J]. Chemosphere, 2019, 236: 124334. DOI:10.1016/j.chemosphere.2019.07.065
(  0) 0) |
| [33] |
Sait S T L, Sørensen L, Kubowicz S, et al. Microplastic fibres from synthetic textiles: Environmental degradation and additive chemical content[J]. Environmental Pollution, 2021, 268: 115745. DOI:10.1016/j.envpol.2020.115745
(  0) 0) |
| [34] |
Martinez V, Henary M. Nile red and Nile blue: Applications and syntheses of structural analogues[J]. Chemistry, 2016, 22(39): 13764-13782. DOI:10.1002/chem.201601570
(  0) 0) |
| [35] |
Li L Z, Luo Y M, Peijnenburg W J G M, et al. Confocal measurement of microplastics uptake by plants[J]. MethodsX, 2020, 7: 100750. DOI:10.1016/j.mex.2019.11.023
(  0) 0) |
| [36] |
Sun X D, Yuan X Z, Jia Y B, et al. Differentially charged nanoplastics demonstrate distinct accumulation in Arabidopsis thaliana[J]. Nature Nanotechnology, 2020, 15(9): 755-760. DOI:10.1038/s41565-020-0707-4
(  0) 0) |
| [37] |
Rillig M C. Plastic and plants[J]. Nature Sustainability, 2020, 3(11): 887-888. DOI:10.1038/s41893-020-0583-9
(  0) 0) |
| [38] |
Wang Z Y, Xie X Y, Zhao J, et al. Xylem- and phloem-based transport of CuO nanoparticles in maize (Zea mays L.)[J]. Environmental Science & Technology, 2012, 46(8): 4434-4441.
(  0) 0) |
| [39] |
Qin Y, Yang H, Xu Z L, et al. Surface modification of polyacrylonitrile membrane by chemical reaction and physical coating: Comparison between static and pore-flowing procedures[J]. ACS Omega, 2018, 3(4): 4231-4241. DOI:10.1021/acsomega.7b02094
(  0) 0) |
| [40] |
Cifuentes Z, Custardoy L, de la Fuente J M, et al. Absorption and translocation to the aerial part of magnetic carbon-coated nanoparticles through the root of different crop plants[J]. Journal of Nanobiotechnology, 2010, 8: 26. DOI:10.1186/1477-3155-8-26
(  0) 0) |
| [41] |
Ma W L. Botany (In Chinese). 2nd ed[M]. Beijing: Higher Education Press, 2015. [马炜梁. 植物学[M]. 2版. 北京: 高等教育出版社, 2015.]
(  0) 0) |
| [42] |
Tumwet F C, Richter A, Kleint T, et al. Vertical movement of microplastics by roots of wheat plant (Triticum aestivum) and the plant response in sandy soil[J]. Microplastics and Nanoplastics, 2024, 4(1): 15-34. DOI:10.1186/s43591-024-00092-8
(  0) 0) |
| [43] |
Boots B, Russell C W, Green D S. Effects of microplastics in soil ecosystems: Above and below ground[J]. Environmental Science & Technology, 2019, 53(19): 11496-11506.
(  0) 0) |
| [44] |
Rillig M C, Ingraffia R, de Souza Machado A A. Microplastic incorporation into soil in agroecosystems[J]. Frontiers in Plant Science, 2017, 8: 1805-1809. DOI:10.3389/fpls.2017.01805
(  0) 0) |
| [45] |
Dong S N, Xia J H, Sheng L T, et al. Transport characteristics of fragmental polyethylene glycol terephthalate (PET) microplastics in porous media under various chemical conditions[J]. Chemosphere, 2021, 276: 130214. DOI:10.1016/j.chemosphere.2021.130214
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


