2. 中国科学院大学, 北京 100049;
3. 中国科学院大学南京学院, 南京 211135;
4. 南京林业大学生态与环境学院, 南方现代林业协同创新中心, 南京 210037
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. University of Chinese Academy of Sciences, Nanjing, Nanjing 211135, China;
4. Co-Innovation Center for Sustainable Forestry in Southern China, College of Ecology and the Environment, Nanjing Forestry University, Nanjing 210037, China
微塑料是全球广泛关注的新污染物,土壤是陆地生态系统微塑料的主要汇[1]。微塑料具有高碳含量和颗粒态等特性,可改变土壤孔隙度、碳组分占比等基本理化性质,进而影响土壤碳循环过程。有研究报道微塑料污染显著增加土壤可溶性有机质(DOM)的含量、酶活性以及微生物生物量,促进土壤二氧化碳(CO2)的排放[2]。DOM作为土壤有机质中枢纽和动态的成分之一,对环境变化高度敏感[3]。可生物降解塑料被认为是传统不可降解塑料的替代品,其每年的使用量和产能均在不断增加[4]。与传统的石化基难降解微塑料相比,可生物降解的微塑料可对土壤DOM的组分与含量产生更大的影响,导致土壤碳损失[5]。聚乳酸(PLA)作为一种新型可降解塑料,被广泛运用于食品包装和农业环保等领域[6]。Shi等[7]的研究表明PLA微塑料可通过改变氧气微环境和电子传递能力来促进土壤有机质矿化。Sun等[8]亦发现PLA等微塑料可以改变土壤DOM的稳定性和含量,进而影响土壤碳的赋存状态。因此,研究可降解微塑料与土壤DOM的相互作用对土壤碳循环至关重要。
除草剂作为使用量最大的农药类别,极大地提升了农业生产效率。我国每年除草剂的使用量超过数十万吨,施用面积逐年扩增[9]。然而,除草剂的大量使用会导致其在土壤中的高残留,对后茬作物以及土壤生态健康造成复杂影响[10]。氟磺胺草醚是一种二苯醚类除草剂,广泛用于豆科作物田间杂草控制[11]。研究发现氟磺胺草醚能改变土壤微生物群落结构与功能,降低微生物活性,对土壤微生物生态平衡产生负面影响[12-13]。除草剂残留还可通过土壤微生物影响土壤有机质分解和温室气体排放[14-15]。因此,由环境污染所介导的土壤碳循环是关系碳达峰、碳中和战略的重要科学问题。
目前,土壤微塑料与除草剂复合污染已成为不可回避的环境问题。但是,鲜有研究报道微塑料除草剂复合污染对土壤碳循环关键过程的影响。因此,本研究选择氟磺胺草醚和PLA微塑料为模式污染物,通过土壤呼吸试验和光谱特征表征来探究微塑料除草剂复合污染对土壤CO2排放以及土壤DOM组分特征的影响,以期为微塑料除草剂复合环境风险评估提供科学指导。
1 材料与方法 1.1 供试材料供试黑土和红壤分别采自黑龙江省佳木斯市林地和湖南省岳阳市汨罗市白塘乡。采集0~20 cm表层土壤,充分混合封装于采样袋中。风干前移除土壤样品内混杂的植物残留物与大块杂质,所有土壤样品自然风干后过2 mm网筛,保存备用。聚乳酸微塑料(4032D)购自Nature Works(美国),粒径为50~100 μm。氟磺胺草醚标准样品(纯度≥97%)购自北京普西唐生物科技有限公司。
1.2 试验设计参考相关文献,本研究设置0.1%和1%(w:w)两个PLA微塑料添加水平、1 mg·kg−1和5 mg·kg−1两个氟磺胺草醚浓度[12-13,16]。试验共设计9个处理,分别为空白对照(CK)、1 mg·kg−1氟磺胺草醚低污染土壤(Fl)、5 mg·kg−1氟磺胺草醚高污染土壤(Fh)、0.1%PLA(w:w)微塑料低添加土壤(Pl)、1%PLA微塑料高添加土壤(Ph)、1 mg·kg−1氟磺胺草醚与0.1%微塑料复合污染土壤(Fl+Pl)、1 mg·kg−1氟磺胺草醚与1%微塑料复合污染土壤(Fl+Ph)、5 mg·kg−1氟磺胺草醚与0.1%微塑料复合污染土壤(Fh+Pl)和5 mg·kg−1氟磺胺草醚与1%微塑料复合污染土壤(Fh+Ph)。首先,称取95 g土壤样品,添加超纯水调节其含水率至60%~70%田间持水量,在25℃的黑暗条件下预培养7 d。称取5 g土壤样品,加入丙酮浸没土壤表面,分别加入1 mL或5 mL 100 mg·L−1的氟磺胺草醚标准溶液,充分搅匀后放置于通风橱中待丙酮挥发。挥发完成后,将其与预培养的土壤混合、充分搅拌均匀,得到初始浓度为1 mg·kg−1或5 mg·kg−1氟磺胺草醚污染土样。添加微塑料的处理组分别加入0.1 g或1 g PLA微塑料,再次充分搅拌均匀,完成0.1%和1%PLA微塑料污染土的制备。所有样品转移至棕色玻璃瓶中,加入超纯水将土壤含水率调节至60%~70%田间持水量,并用防菌透气膜封住瓶口。将培养瓶放置在人工气候培养箱中,在25℃的黑暗条件下进行培养,每两天通过称重法补充水分。每个处理包含三个重复。
1.3 样品采集与分析土壤基本理化性质的测定[17]:土壤pH采用梅特勒FE20酸度计(德国)在土水比1:5下测定。土壤总有机碳含量采用重铬酸钾氧化—容量法测定。土壤阳离子交换量(CEC)采用醋酸铵法(pH = 7.0)测定。土壤全氮含量采用凯氏定氮法测定。土壤全磷和全钾含量分别采用钼锑抗比色法和火焰光度计(FP640,Huayan,中国)测定。用激光衍射法测定土壤的粒径分布(Malvern Instruments,Malvern,英国)并计算砂粒(2~0.02 mm)、粉粒(0.02~0.002 mm)和黏粒(< 0.002 mm)占比。供试土壤基本理化性质见表 1。
|
|
表 1 供试土壤基本理化性质 Table 1 Basic physicochemical properties of the soils in this study |
CO2的采集与测定:在培养第3、7、14、30、45、60天时采集气体。首先将培养瓶放在通风橱通风处理5 min,以清除瓶内残留气体。随后用注射器从培养瓶中抽取30 mL气体样本,并转移至提前抽真空的labco采气瓶中。然后用带有三通阀的盖子密封培养瓶,培养2 h。培养结束后,再次采集30 mL气体于抽真空的labco采气瓶中,使用气相色谱仪(GC-7890B,Agilent Technologies,美国)测定CO2浓度。CO2排放通量的计算公式如下[18]:
| $ {\text{F}} = \frac{{{\text{273}}}}{{{\text{273 + T}}}} \times \frac{{{\text{(}}{{\text{C}}_{\text{1}}} - {{\text{C}}_{\text{0}}}{\text{)}} \times {\text{V}} \times {\text{M}} \times {\text{1}}{{\text{0}}^{ - 3}}}}{{{\text{24}}{\text{.4}} \times {\text{m}} \times {\text{h}}}} $ | (1) |
式中,F为CO2排放通量(mg·kg−1·h−1);T为采样时的稳定温度(℃);C1为采样时的CO2浓度(μmol·mol−1);C0为初始时的CO2浓度(μmol·mol−1);V为采样时的气体体积(L);M为CO2的摩尔质量(44 g·mol−1);24.4为培养温度下CO2气体的摩尔体积(L·mol−1);m为试验所用的干土质量(kg);h为两次采气间隔的时间(h)。
DOM的提取和紫外光谱表征:在培养的第60天采集土壤样品,取5 g土样于25 mL超纯水中,在25℃条件下以180 r·min−1振荡1 h后,过0.45 μm滤膜,使用总有机碳/总氮分析仪(Analytik Jena,Multi N/C 3100 TOC/TN,德国)测定滤液中的可溶性有机碳(DOC)含量。使用紫外可见光分光光度计(LabTech,UV 8100 B,中国)在波长254 nm和260 nm处测定滤液的吸光度,并除以样品的DOC浓度计算出SUVA254和SUVA260来表征DOM芳香性组分和疏水性组分含量。
DOM三维荧光光谱分析:使用三维荧光扫描光谱仪(Aqualog,HORIBA Instruments Inc.,美国)分析DOM特征。以氙气灯为光源,信噪比 > 20000:1,激发波长为211~618 nm,发射波长为240~600 nm。使用超纯水去除拉曼散射和瑞丽散射,进一步使用SOLO+MIA 8.6.1软件(Eigenvector Research,Inc.,美国)进行平行因子分析,识别荧光组分。黑土中DOM含量较高,使用如下公式进行数据的校正,以消除内滤效应[19]。使用拆半分析和残差分析进行验证,确保结果可靠性。
| $ \text{Fcor}=\text{Fobs}\times {\text{10}}^{\frac{{\text{(A}}_{\text{Ex}}{\text{+A}}_{\text{Em}})}{\text{2}}} $ | (2) |
式中Fobs和Fcor分别为测量和校正的荧光强度,AEx和AEm分别表示激发波长和发射波长。
进一步根据紫外-三维荧光光谱数据计算SUVA254、SUVA260、荧光指数(FI)、自生源指数(BIX)和腐殖化指数(HIX)。SUVA254表示DOM的芳香性,计算方法是DOM在254 nm处的吸光系数除以DOC浓度[20]。SUVA260代表疏水成分含量,计算方法为DOM在260 nm处的吸光系数除以DOC浓度。FI表示微生物代谢活动的强度,计算方法为:在370 nm激发波长处获得的450 nm处与500 nm处发射强度的比值[8]。BIX表示DOM的自生源特征,计算方法为:激发波长为310 nm时,发射波长在380 nm和430 nm处发射强度的比值。HIX是描述腐殖化的指标,计算方法为:激发波长为254 nm时,发射波长在435~480 nm范围与300~345 nm范围的区域积分值的比值。
土壤中氟磺胺草醚的测定:在培养的第60天采集土壤样品,取10 g土壤样品于40 mL玻璃瓶中,加入10 mL含1%甲酸的乙腈溶液。在25℃条件下以220 r·min−1振荡1 h。振荡后,加入4 g MgSO4和1 g NaCl,再次以相同条件振荡15 min。最后,吸取1 mL上清液并过0.22 μm滤膜。使用高效液相色谱仪(Agilent,1260 InfinityII,美国)测定氟磺胺草醚,所用检测装置和色谱柱分别为紫外检测器和C18柱(5 μm × 4.6 mm × 250 mm)。以乙腈和1%磷酸(6:4,v/v)为流动相,进样量为20 µL,柱温设定为30℃,流速为1.2 mL·min−1。
1.4 数据处理使用Excel和SPSS 25.0进行试验数据的处理和分析。采用单因素方差分析中的Duncan多重比较检验数据之间差异的显著性(P < 0.05),使用Origin 2021绘制数据图。
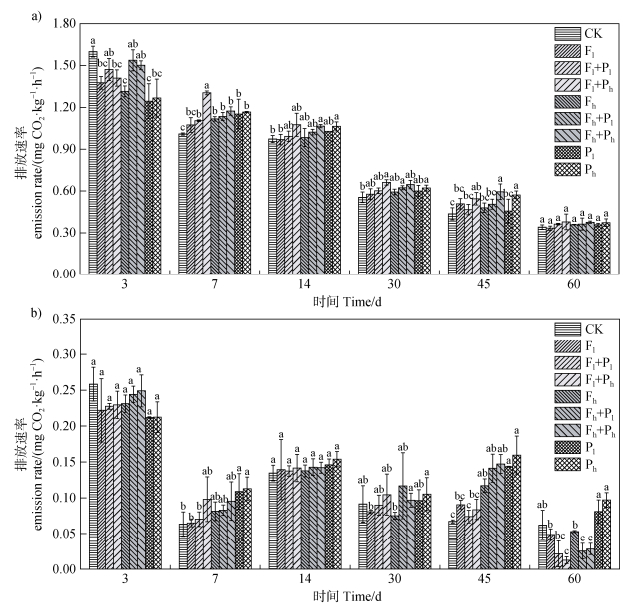
2 结果与讨论 2.1 氟磺胺草醚和PLA微塑料对土壤CO2排放速率的影响黑土CO2的排放速率整体上随着时间的增加而降低(图 1a)。试验初期(0~3天)氟磺胺草醚和PLA微塑料的添加会抑制黑土中CO2的排放速率,但在第7~45天,氟磺胺草醚和PLA微塑料会促进CO2的排放,到第60天各处理组的排放速率趋于平稳。其中氟磺胺草醚-PLA微塑料复合污染的刺激作用相较于其他处理更强。这是因为氟磺胺草醚和微塑料能为土壤微生物提供额外的碳源,同时氟磺胺草醚可刺激微生物代谢活动,进一步促进CO2的排放。一些研究表明PLA等可降解微塑料含有不稳定有机碳,可以通过共代谢促进R策略型细菌的增殖,激发土壤有机质的分解和矿化[21-22]。Yu等[23]的研究表明PLA微塑料显著影响了土壤微生物群落结构,增强了其网络结构的复杂性,同时提升了与有机质分解及矿化相关的基因丰度(如cbbL、cbhI、abfA及Lac等)。Zhang等[24]发现氟磺胺草醚能提高土壤(酸/碱性)磷酸酶、脱氢酶、脲酶活性以及细菌数量,促进CO2的排放。王峰等[25]研究发现四种除草剂均促进了茶园土壤CO2的排放,累积排放量增幅为6.05%~65.46%。
|
注:CK,空白对照;Fl,1 mg·kg−1氟磺胺草醚低污染处理;Fh,5 mg·kg−1氟磺胺草醚低污染处理;Pl,0.1%PLA微塑料低添加处理;Ph,1%PLA微塑料高添加处理;Fl+Pl,1 mg·kg−1氟磺胺草醚与0.1%微塑料复合污染处理;Fl+Ph,1 mg·kg−1氟磺胺草醚与1%微塑料复合污染处理;Fh+Pl,5 mg·kg−1氟磺胺草醚与0.1%微塑料复合污染处理;Fh+Ph,5 mg·kg−1氟磺胺草醚与1%微塑料复合污染处理;不同小写字母表示同一土壤同一采样时间不同处理CO2排放速率差异显著(P < 0.05)。下同。 Note: CK, blank control; Fl, 1 mg·kg−1 fomesafen low-pollution treatment; Fh, 5 mg·kg−1 fomesafen low-pollution treatment; Pl, 0.1% PLA microplastics low addition treatment; Ph, 1% PLA microplastics high addition treatment; Fl+Pl, combined pollution treatment of 1 mg·kg−¹ fomesafen and 0.1% PLA microplastics; Fl+Ph, combined pollution treatment of 1 mg·kg−¹ fomesafen and 1% PLA microplastics; Fh+Pl, combined pollution treatment of 5 mg·kg−¹ fomesafen and 0.1% PLA microplastics; Fh+Ph, combined pollution treatment of 5 mg·kg−¹ fomesafen and 1% PLA microplastics; different lowercase letters indicate the significance of differences in CO2 emission rates between treatments for the same soil at the same sampling time (P < 0.05). The same as below. 图 1 不同处理中土壤CO2排放速率动态变化(a:黑土,b:红壤) Fig. 1 Dynamics of soil CO2 emission rate in different treatments (a: Mollisols, b: Red soil) |
与黑土类似,试验初期红壤CO2的排放速率会受到氟磺胺草醚和微塑料的抑制,试验中期(7~45天)氟磺胺草醚和微塑料会刺激土壤CO2的排放(图 1b)。在第60天,单一低浓度和高浓度氟磺胺草醚污染土壤的呼吸速率与对照相比分别降低了14.8%和21.6%,PLA微塑料的添加会进一步抑制CO2的排放速率,抑制率范围为54.3%~79.7%。在试验末期黑土和红壤的CO2排放速率出现截然不同的结果,由于红壤中有机质含量远低于黑土(表 1),前中期除草剂和PLA微塑料对微生物的刺激作用加速了红壤中不稳定有机质的分解,过度消耗有限的不稳定碳导致试验后期污染红壤CO2排放速率远低于对照。此外,微塑料和除草剂可能会对微生物群落产生毒性效应,抑制微生物代谢活性,减少红壤中CO2的排放。Chen等[26]的研究揭示PLA微塑料会向土壤中持续释放有害物质(增塑剂、抗氧化剂等),对微生物的生长与活性产生毒性效应,降低其生物量和多样性。Wu等[13]的研究表明,长期施用氟磺胺草醚会对土壤微生物群落产生毒害作用,抑制土壤微生物的生长和活性,降低土壤呼吸作用。单一PLA微塑料处理组缺少除草剂对微生物的刺激作用,在试验后期CO2排放速率保持稳定。
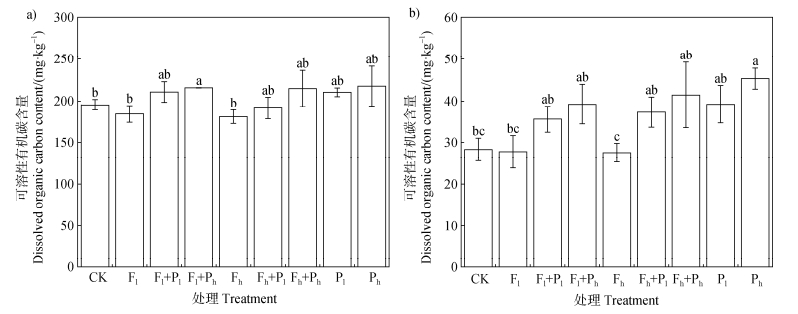
2.2 氟磺胺草醚和PLA微塑料对DOM含量和紫外-可见光光谱指数的影响单一氟磺胺草醚污染对黑土和红壤中DOM含量未产生显著影响(图 2)。单一PLA微塑料或氟磺胺草醚-PLA微塑料复合污染显著提高土壤DOM含量。0.1%PLA微塑料处理土壤中,黑土和红壤DOM含量分别增加了15.06 mg·kg−1和9.07 mg·kg−1;1%PLA微塑料处理土壤中,黑土和红壤DOM含量分别增加了20.54 mg·kg−1和13.69 mg·kg−1。黑土中DOM的增量高于红壤,一方面因为在黑土中PLA分解更快,能释放出更多的DOM,另一方面与土壤本底碳的分解有关。一般而言,聚合物的生物降解过程涵盖微生物在塑料表面的定殖、通过酶促作用分解为低分子量化合物,以及这些低分子量化合物进一步被微生物同化或转化为CO2排放至大气的三个阶段[27]。Yu等[28]研究发现PLA的生物降解量随着土壤碳氮比(C/N)的增加而增加。本研究中,黑土的C/N(18.49)略高于红壤(18.35),这会导致黑土中PLA微塑料的分解速度更快。但是,相较于0.1%PLA微塑料添加,1%PLA微塑料添加处理中DOM的含量并没有呈倍数增长,表明PLA没有直接主导土壤DOM增加。He等[29]研究发现低密度聚乙烯微塑料能够通过改变微生物群落和功能,提高黑土和红壤中的DOC,且降低不稳定碳的占比。与红壤相比,黑土本底有机质含量更高,除草剂和PLA微塑料的添加可能通过激发效应加速微生物对土壤本底有机质的分解,使得黑土DOM的增量高于红壤。
|
图 2 不同处理中土壤可溶性有机碳含量(a:黑土,b:红壤) Fig. 2 Soil dissolved organic carbon content in different treatments (a: Mollisols, b: Red soil) |
根据紫外-三维荧光光谱进一步计算相关指数来表征DOM在形成与转化过程中的差异(表 2)。SUVA254和SUVA260分别表示DOM的芳香性和疏水性成分含量。结果表明添加PLA微塑料后黑土中DOM的芳香性有所提高,但红壤各处理DOM的芳香性略有降低。FI可表征DOM的来源,FI > 1.9代表以微生物源为主,FI < 1.4则以外源输入(植物源)为主[8]。本研究中,黑土和红壤的FI分别介于1.62~1.67和1.19~1.53之间,表明黑土中既有植物源的DOM,也有微生物代谢产物源的DOM,红壤中的DOM以植物源为主(表 2)。BIX可表征DOM的自生源特征,BIX > 0.8表示DOM的分解程度较高[8]。黑土DOM的BIX均小于0.8且处理之间变化不明显,而红壤DOM的BIX均大于0.8,表明红壤中DOM的分解程度相较于黑土更高。红壤中,高添加氟磺胺草醚-微塑料复合污染处理土壤的BIX指数最大,表明高添加氟磺胺草醚-微塑料复合污染会通过刺激微生物,加快对有机质的分解,这与前面的试验结果相符。HIX是描述腐殖化的指标,HIX值越高,腐殖化程度越大[8]。黑土和红壤DOM的HIX值分别为4.10~4.58和1.01~0.71。结果表明黑土的DOM腐殖化程度较高,其中高浓度PLA微塑料显著提高了土壤DOM的腐殖化程度。微塑料可以通过刺激微生物分解木质素等,消耗有机残体,从而促进土壤的腐殖化[30]。同时,有研究表明微塑料会导致土壤中芳香性较低的易降解成分(酚类或蛋白类)被分解和转化,增加腐殖酸类化合物,提高土壤DOM的芳香程度[31]。腐殖化程度的提高增强了土壤有机碳稳定性,这会降低土壤呼吸速率。同时,腐殖质作为胶结剂促进土壤有机质与矿物质结合,增强团聚体结构稳定性,并构建物理屏障阻隔有机质分解[32-33]。红壤DOM的HIX指数均小于1.5,并且微塑料和除草剂的添加会降低其HIX指数,表明微塑料和除草剂不利于红壤DOM的腐殖化。这可能是由于红壤中有机质含量较少,氟磺胺草醚和微塑料刺激了微生物对腐殖质的分解,降低土壤腐殖化程度。例如,在碳源有限的情况下,微生物能够分解腐殖质以获取所需的营养物质[34]。以上结果与SUVA254和SUVA260的分析结果相一致。
|
|
表 2 不同处理中土壤可溶性有机质紫外-荧光指数 Table 2 Ultraviolet-fluorescence index of soil dissolved organic matter in different treatments |
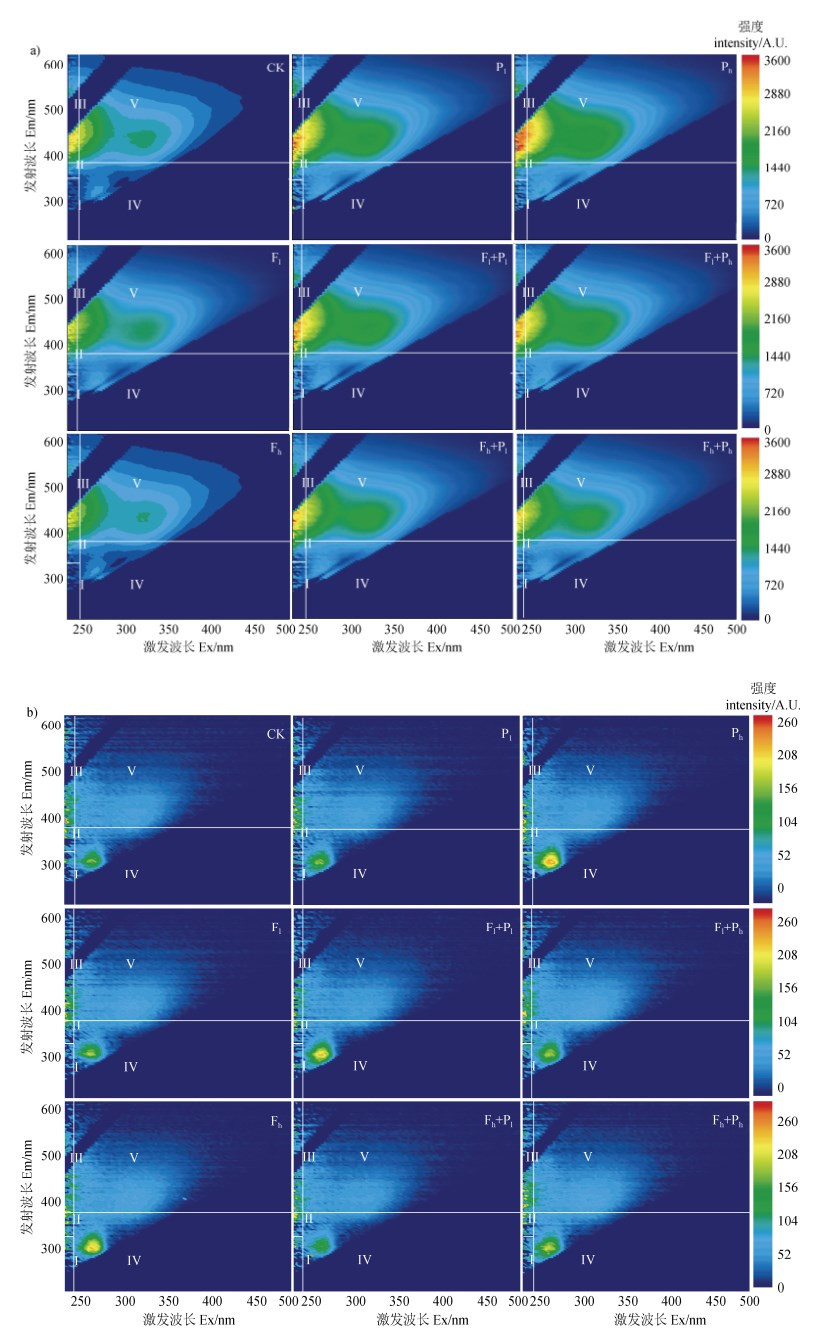
三维荧光光谱根据不同波长分为5个区域,分别代表不同的物质:Ⅰ(Ex/Em,220~250 nm/280~330 nm)代表酪氨酸;Ⅱ(Ex/Em,220~250 nm/330~380 nm)代表色氨酸;Ⅲ(Ex/Em,220~250 nm/380~450 nm)代表类富里酸物质;Ⅳ(Ex/Em,250~400 nm/280~380 nm)代表可溶性微生物副产物;Ⅴ(Ex/Em,250~400 nm/380~500 nm)代表类胡敏酸物质[35]。由图 3可知,与复合污染相比,黑土中单独添加PLA微塑料显著增强了Ⅲ区和Ⅴ区的荧光强度。红壤中单独添加PLA微塑料增强了Ⅳ区的荧光强度,而氟磺胺草醚-PLA微塑料复合污染未显著增强Ⅳ区荧光的强度。
|
图 3 不同处理土壤可溶性有机质的三维荧光光谱组成状况(a:黑土,b:红壤) Fig. 3 Three-dimensional fluorescence spectral composition of soil dissolved organic matter in different treatments (a: Mollisols, b: Red soil) |
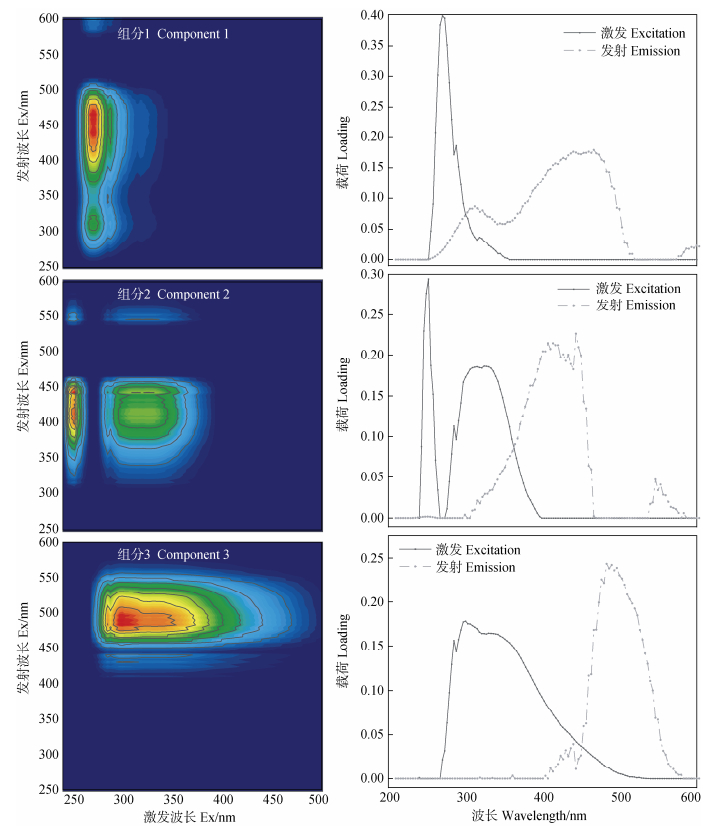
为了更准确地分析DOM组成变化,对三维荧光数据进行平行因子分析,确定了三种DOM荧光组分(C1、C2、C3),结果如图 4所示。其中C1(Ex=270 nm/Em=466 nm)为分子量较大的陆生类腐殖酸,具有相对较高的芳香性和腐殖化程度[36];C2(Ex=252 nm/Em=456 nm,Ex=324 nm/Em=443 nm)是一种与C1类似的短波段腐殖酸组分,分子量较大,主要来源于陆生植物[37];C3(Ex=300 nm/Em=492 nm)为常见的长波段腐殖酸物质,荧光特征类似于富里酸,是一种相对分子量较小的腐殖质,广泛分布于农田和湿地等环境介质[8]。
|
图 4 基于平行因子法分析的可溶性有机质中三种荧光组分 Fig. 4 Three fluorescent components in dissolved organic matter were identified based on PARAFAC |
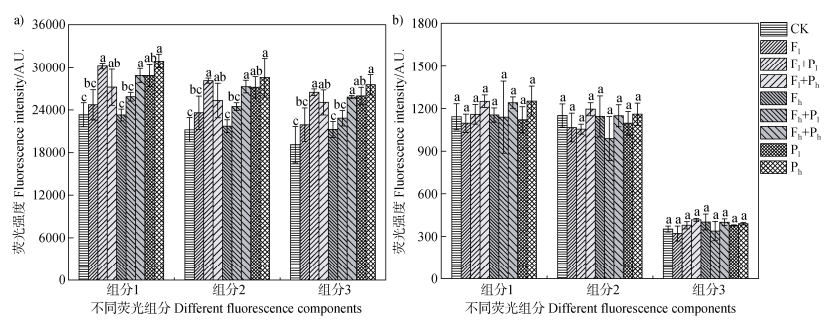
对不同处理土壤中DOM各组分荧光强度进行比较(图 5a),发现单一氟磺胺草醚不会明显改变黑土中三种组分的含量,PLA微塑料显著增加三种组分的含量,且单一高添加PLA微塑料略高于高浓度复合污染。红壤中C3组分的荧光强度远低于C1和C2组分(图 5b),这可能是由于红壤中小分子腐殖酸(如富里酸)分子量较低和溶解性较高,更容易被微生物通过摄取和分解来获取能量[38]。单一氟磺胺草醚、单一PLA微塑料和复合污染处理均未显著改变红壤三种组分的含量(图 5b)。土壤微生物通过合成与分解代谢活动,在土壤有机质的循环过程中扮演着至关重要的角色。Zhou等[39]的研究表明,可降解塑料能在其周围诱导形成β-葡萄糖苷酶的活性热点区域,这一效应加速了酶促反应动力学,促进了纤维素的降解过程。可降解塑料部分降解后形成富碳环境,微塑料源有机碳不稳定性和生物可利用性较高,能刺激微生物代谢,提升酶活性[40]。本研究表明,PLA微塑料主要引起了富含有机质的黑土中DOM的组分变化,对有机质含量较低的红壤而言,除草剂和微塑料污染并不会显著改变DOM不同组分的含量。
|
图 5 不同处理中土壤可溶性有机质三种荧光组分的强度(a:黑土,b:红壤) Fig. 5 Intensity of three fluorescent components of soil dissolved organic matter in different treatments (a: Mollisols, b: Red soil) |
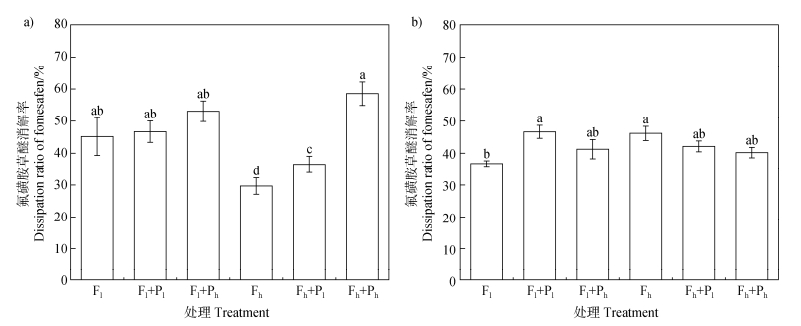
PLA微塑料不仅会改变土壤碳的转化过程,还可以通过干扰微生物群落来影响土壤中氟磺胺草醚的消解。经过60天的培养,在黑土中,0.1%和1%PLA微塑料添加未对低污染氟磺胺草醚消解率产生显著影响,但对高氟磺胺草醚污染处理,0.1%和1%PLA微塑料添加下其消解率分别显著提高了22.9%和97.1%(图 6a)。相比而言,在红壤中,对于低氟磺胺草醚污染处理,0.1%和1%PLA微塑料添加下其消解率提高了27.0%和12.3%,但针对高氟磺胺草醚污染的红壤,两个添加浓度的微塑料均未对其消解率产生显著影响(图 6b)。微塑料可通过改变污染物生物有效性、土壤理化性质和微生物群落来影响有机污染物的消解过程。王康等[41]研究表明可降解微塑料可通过影响杀虫剂在土壤中的吸附和解吸来提高杀虫剂的生物有效性。本试验中土壤的DOM与氟磺胺草醚竞争微塑料上的吸附位点,增加氟磺胺草醚的解吸,提高其生物有效性,同时PLA微塑料可能有利于微生物群落中氟磺胺草醚降解菌的生长,进而促进除草剂的消解。Seeley等[42]的研究表明PLA水解产生的乳酸可成为微生物优势碳源,促进微生物群落演变,提高微生物的代谢功能。Wang等[43]发现PLA微塑料际的微生物α多样性和活性明显高于背景土壤,变形菌门和拟杆菌门的丰度更高,并对外源污染物、碳水化合物和氨基酸表现出更强的降解和代谢能力。Guo等[44]曾报道PLA微塑料显著提升了土壤微生物多样性与代谢活性,且PLA降解产物能与除草剂产生协同降解作用,加速除草剂降解。
|
图 6 不同处理土壤中氟磺胺草醚消解率(a:黑土,b:红壤) Fig. 6 Dissipation ratio of fomesafen in soils of different treatments (a: Mollisols, b: Red soil) |
本研究通过土壤/PLA微塑料/氟磺胺草醚共培养试验,探究了除草剂和微塑料复合污染对短期土壤CO2排放速率和土壤DOM组分的影响。主要结论如下:(1)除草剂氟磺胺草醚和微塑料PLA均会在试验中期(7~45天)促进黑土和红壤CO2排放速率,但在后期除草剂-微塑料复合污染显著抑制红壤的呼吸速率。(2)PLA微塑料能显著提高黑土DOM含量、腐殖化程度和芳香性,高浓度氟磺胺草醚-PLA微塑料复合污染会加快红壤中DOM的分解。(3)单一PLA微塑料和氟磺胺草醚-PLA微塑料复合污染均提高了黑土中陆源类腐殖酸、短波段腐殖酸和类富里酸三种组分的含量,但除草剂和PLA微塑料对红壤DOM组分无显著影响。(4)PLA微塑料能促进黑土和红壤中氟磺胺草醚的消解。
| [1] |
MacLeod M, Arp H P H, Tekman M B, et al. The global threat from plastic pollution[J]. Science, 2021, 373(6550): 61-65. DOI:10.1126/science.abg5433
(  0) 0) |
| [2] |
Zhao S L, Rillig M C, Bing H J, et al. Microplastic pollution promotes soil respiration: A global-scale meta-analysis[J]. Global Change Biology, 2024, 30(7): e17415. DOI:10.1111/gcb.17415
(  0) 0) |
| [3] |
Li R F, Xi B D, Tan W B, et al. Spatiotemporal heterogeneous effects of microplastics input on soil dissolved organic matter (DOM) under field conditions[J]. Science of the Total Environment, 2022, 847: 157605. DOI:10.1016/j.scitotenv.2022.157605
(  0) 0) |
| [4] |
Moshood T D, Nawanir G, Mahmud F, et al. Sustainability of biodegradable plastics: New problem or solution to solve the global plastic pollution?[J]. Current Research in Green and Sustainable Chemistry, 2022, 5: 100273. DOI:10.1016/j.crgsc.2022.100273
(  0) 0) |
| [5] |
Jia K T, Nie S M, Tian M F, et al. Biodegradable microplastics can cause more serious loss of soil organic carbon by priming effect than conventional microplastics in farmland shelterbelts[J]. Functional Ecology, 2024, 38(11): 2447-2458. DOI:10.1111/1365-2435.14662
(  0) 0) |
| [6] |
Karamanlioglu M, Preziosi R, Robson G D. Abiotic and biotic environmental degradation of the bioplastic polymer poly (lactic acid): A review[J]. Polymer Degradation and Stability, 2017, 137: 122-130. DOI:10.1016/j.polymdegradstab.2017.01.009
(  0) 0) |
| [7] |
Shi J, Wang Z, Peng Y M, et al. Effects of microplastics on soil carbon mineralization: The crucial role of oxygen dynamics and electron transfer[J]. Environmental Science & Technology, 2023, 57(36): 13588-13600.
(  0) 0) |
| [8] |
Sun Y Z, Li X F, Li X M, et al. Deciphering the fingerprint of dissolved organic matter in the soil amended with biodegradable and conventional microplastics based on optical and molecular signatures[J]. Environmental Science & Technology, 2022, 56(22): 15746-15759.
(  0) 0) |
| [9] |
Sharma A, Kumar V, Shahzad B, et al. Worldwide pesticide usage and its impacts on ecosystem[J]. SN Applied Sciences, 2019, 1(11): 1446. DOI:10.1007/s42452-019-1485-1
(  0) 0) |
| [10] |
Riedo J, Wettstein F E, Rösch A, et al. Widespread occurrence of pesticides in organically managed agricultural soils-the ghost of a conventional agricultural past?[J]. Environmental Science & Technology, 2021, 55(5): 2919-2928.
(  0) 0) |
| [11] |
Zheng J Y, Wang B H, Yue Z H, et al. Effects of fomesafen on microorganism quantity and enzyme activities in black soil (In Chinese)[J]. Journal of Plant Protection, 2013, 40(5): 468-472. [郑景瑶, 王百慧, 岳中辉, 等. 氟磺胺草醚对黑土微生物数量及酶活性的影响[J]. 植物保护学报, 2013, 40(5): 468-472.]
(  0) 0) |
| [12] |
Hu H Y, Zhou H, Zhou S X, et al. Fomesafen impacts bacterial communities and enzyme activities in the rhizosphere[J]. Environmental Pollution, 2019, 253: 302-311. DOI:10.1016/j.envpol.2019.07.018
(  0) 0) |
| [13] |
Wu X H, Zhang Y, Du P Q, et al. Impact of fomesafen on the soil microbial communities in soybean fields in Northeastern China[J]. Ecotoxicology and Environmental Safety, 2018, 148: 169-176. DOI:10.1016/j.ecoenv.2017.10.003
(  0) 0) |
| [14] |
Cornish C M, Johnson O F, Bansal S, et al. Common use herbicides increase wetland greenhouse gas emissions[J]. Science of the Total Environment, 2024, 933: 172881. DOI:10.1016/j.scitotenv.2024.172881
(  0) 0) |
| [15] |
Sándor Z, Kincses I, Tállai M, et al. Effect of herbicides on soil respiration: A case study conducted at Debrecen-látókép plant cultivation experimental station[J]. F1000Research, 2020, 9: 1348. DOI:10.12688/f1000research.27057.1
(  0) 0) |
| [16] |
Shi W S, Wu N, Zhang Z L, et al. A global review on the abundance and threats of microplastics in soils to terrestrial ecosystem and human health[J]. Science of the Total Environment, 2024, 912: 169469. DOI:10.1016/j.scitotenv.2023.169469
(  0) 0) |
| [17] |
Lu R K. Methods of soil agrochemical analysis (In Chinese). Beijing: China Agricultural Science and Technology Press, 2000. [鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000.]
(  0) 0) |
| [18] |
Hao Y Q, Min J, Ju S R, et al. Possible hazards from biodegradation of soil plastic mulch: Increases in microplastics and CO2 emissions[J]. Journal of Hazardous Materials, 2024, 467: 133680. DOI:10.1016/j.jhazmat.2024.133680
(  0) 0) |
| [19] |
Ji R T, Yang Y T, Wu Y D, et al. Capturing differences in the release potential of dissolved organic matter from biochar and hydrochar: Insights from component characterization and molecular identification[J]. Science of the Total Environment, 2024, 955: 177209. DOI:10.1016/j.scitotenv.2024.177209
(  0) 0) |
| [20] |
Cheng H, Wu Y D, Guo Y H, et al. Spectral characteristics of dissolved organic matter in soils with diverse vegetation cover in the river-lake confluence area of Hongze Lake (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(5): 1309-1319. DOI:10.11766/trxb202408070322 [程虎, 吴玉东, 郭俨辉, 等. 洪泽湖河湖交汇区不同植被覆盖土壤溶解性有机质光谱特征研究[J]. 土壤学报, 2025, 62(5): 1309-1319.]
(  0) 0) |
| [21] |
Zhang G H, Liu D, Lin J J, et al. Priming effects induced by degradable microplastics in agricultural soils[J]. Soil Biology & Biochemistry, 2023, 180: 109006.
(  0) 0) |
| [22] |
Huo Y X, Dijkstra F A, Possell M, et al. Mineralisation and priming effects of a biodegradable plastic mulch film in soils: Influence of soil type, temperature and plastic particle size[J]. Soil Biology & Biochemistry, 2024, 189: 109257.
(  0) 0) |
| [23] |
Yu H, Liu X, Qiu X G, et al. Discrepant soil microbial community and C cycling function responses to conventional and biodegradable microplastics[J]. Journal of Hazardous Materials, 2024, 470: 134176. DOI:10.1016/j.jhazmat.2024.134176
(  0) 0) |
| [24] |
Zhang Q M, Zhu L S, Wang J, et al. Effects of fomesafen on soil enzyme activity, microbial population, and bacterial community composition[J]. Environmental Monitoring and Assessment, 2014, 186(5): 2801-2812. DOI:10.1007/s10661-013-3581-9
(  0) 0) |
| [25] |
Wang F, Chen Y Z, Wu Z D, et al. Effects of herbicides on urea nitrogen transformation and greenhouse gas emission from tea garden soil (In Chinese)[J]. Journal of Agro-Environment Science, 2017, 36(8): 1649-1657. [王峰, 陈玉真, 吴志丹, 等. 除草剂对茶园土壤尿素态氮转化和温室气体排放的影响[J]. 农业环境科学学报, 2017, 36(8): 1649-1657.]
(  0) 0) |
| [26] |
Chen L Y, Han L F, Wang F Y, et al. Polylactic acid microplastics induced negative priming and improved carbon sequestration via microbial processes in different paddy soils[J]. Soil Biology & Biochemistry, 2025, 201: 109653.
(  0) 0) |
| [27] |
Zumstein M T, Schintlmeister A, Nelson T F, et al. Biodegradation of synthetic polymers in soils: Tracking carbon into CO2 and microbial biomass[J]. Science Advances, 2018, 4(7): eaas9024. DOI:10.1126/sciadv.aas9024
(  0) 0) |
| [28] |
Yu Y X, Lin S Y, Sarkar B, et al. Mineralization and microbial utilization of poly (lactic acid) microplastic in soil[J]. Journal of Hazardous Materials, 2024, 476: 135080. DOI:10.1016/j.jhazmat.2024.135080
(  0) 0) |
| [29] |
He Z B, Hou Y R, Li Y, et al. Increased methane production associated with community shifts towards Methanocella in paddy soils with the presence of nanoplastics[J]. Microbiome, 2024, 12(1): 259. DOI:10.1186/s40168-024-01974-y
(  0) 0) |
| [30] |
Zhou Y T, Sun Y, Liu J L, et al. Effects of microplastics on humification and fungal community during cow manure composting[J]. Science of the Total Environment, 2022, 803: 150029. DOI:10.1016/j.scitotenv.2021.150029
(  0) 0) |
| [31] |
Qiu X R, Ma S R, Pan J R, et al. Microbial metabolism influences microplastic perturbation of dissolved organic matter in agricultural soils[J]. The ISME Journal, 2024, 18(1): wrad017. DOI:10.1093/ismejo/wrad017
(  0) 0) |
| [32] |
Tiwari J, Ramanathan A, Bauddh K, et al. Humic substances: Structure, function and benefits for agroecosystems—A review[J]. Pedosphere, 2023, 33(2): 237-249. DOI:10.1016/j.pedsph.2022.07.008
(  0) 0) |
| [33] |
Zhu Y C, Zhang M, Han X Z, et al. Evaluation of the soil aggregate stability under long term manure and chemical fertilizer applications: Insights from organic carbon and humic acid structure in aggregates[J]. Agriculture, Ecosystems & Environment, 2024, 376: 109217.
(  0) 0) |
| [34] |
Mishra B, Srivastava L L. Degradation of humic acid of a forest soil by some fungal isolates[J]. Plant and Soil, 1986, 96(3): 413-416. DOI:10.1007/BF02375145
(  0) 0) |
| [35] |
Li H M, Liu C Q, Ni J Q, et al. Impact of cellulolytic nitrogen-fixing composite inoculants on humification pathways and nitrogen cycling in kitchen waste composting[J]. Bioresource Technology, 2025, 416: 131819. DOI:10.1016/j.biortech.2024.131819
(  0) 0) |
| [36] |
Lei W Y, Teng P J, Sheng M, et al. Characteristics of dissolved organic matter under decomposition of different organic materials in the black soil region of Northeast China (In Chinese)[J]. Chinese Journal of Applied Ecology, 2025, 36(2): 513-525. [雷琬莹, 滕培基, 盛明, 等. 黑土区不同种类有机物料腐解过程中的溶解性有机质特征[J]. 应用生态学报, 2025, 36(2): 513-525.]
(  0) 0) |
| [37] |
Gao J K, Liang C L, Shen G Z, et al. Spectral characteristics of dissolved organic matter in various agricultural soils throughout China[J]. Chemosphere, 2017, 176: 108-116. DOI:10.1016/j.chemosphere.2017.02.104
(  0) 0) |
| [38] |
Lehmann J, Kleber M. The contentious nature of soil organic matter[J]. Nature, 2015, 528(7580): 60-68. DOI:10.1038/nature16069
(  0) 0) |
| [39] |
Zhou J, Gui H, Banfield C C, et al. The microplastisphere: Biodegradable microplastics addition alters soil microbial community structure and function[J]. Soil Biology & Biochemistry, 2021, 156: 108211.
(  0) 0) |
| [40] |
Shi J, Wang X, Wang J. Soil carbon cycling mediated by microplastics: Formation, mineralization, and sequestration (In Chinese)[J]. Scientia Sinica: Technologica, 2024, 54(10): 1854-1867. [石佳, 王祥, 汪杰. 微塑料介导的土壤碳循环: 微塑料对土壤有机碳的形成、矿化和稳定过程的影响[J]. 中国科学(技术科学), 2024, 54(10): 1854-1867.]
(  0) 0) |
| [41] |
Wang K, Chen W, Tian J Y, et al. Study on the composite pollution of degradable microplastics and thiacloprid (In Chinese)[J]. Acta Pedologica Sinica, 2026, 63(2): 628-635. DOI:10.11766/trxb202409150367 [王康, 陈伟, 田佳宇, 等. 典型可降解微塑料与噻虫啉的复合污染研究[J]. 土壤学报, 2026, 63(2): 628-635.]
(  0) 0) |
| [42] |
Seeley M E, Song B, Passie R, et al. Microplastics affect sedimentary microbial communities and nitrogen cycling[J]. Nature Communications, 2020, 11(1): 2372. DOI:10.1038/s41467-020-16235-3
(  0) 0) |
| [43] |
Wang K, Yang S D, Yu X, et al. Effect of microplastics on the degradation of tetracycline in a soil microbial electric field[J]. Journal of Hazardous Materials, 2023, 460: 132313. DOI:10.1016/j.jhazmat.2023.132313
(  0) 0) |
| [44] |
Guo J T, Du Y H, Yang L Y, et al. Effects of microplastics on the environmental behaviors of the herbicide atrazine in soil: Dissipation, adsorption, and bioconcentration[J]. Journal of Hazardous Materials, 2024, 465: 133085. DOI:10.1016/j.jhazmat.2023.133085
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


