2. 农业农村部西北植物营养与农业环境重点实验室, 陕西杨凌 712100
2. Key Laboratory of Plant Nutrition and Agri-environment in Northwest China, Ministry of Agriculture and Rural Affairs, Yangling, Shaanxi 712100, China
现代农业生产中,塑料材料因其优异的机械性能与经济性被广泛应用于地膜覆盖、灌溉系统等领域[1]。目前全球塑料产量已攀升至4.0003亿吨,其中,农用塑料消耗量占比26.8%,且逐年以4.1%的速度增长[2]。聚乙烯(PE)因其高结晶度、强疏水性和化学惰性,占据农膜市场份额的68.3%以上,但其光氧化裂解产生的聚乙烯微塑料(PE-MP)在土壤中表现出超百年尺度的持久性(环境半衰期t1/2=110 ± 15年)[3]。同时,以聚乳酸(PLA)为代表的可降解塑料因政策扶持快速推广,年消费量可达97万吨[4],但其在土壤中的的不完全降解会释放表面电荷极化的次生聚乳酸微塑料(PLA-MP),次生PLA-MP因高表面反应活性而显著区别于传统PE-MP的环境行为[5]。因此,探明不同类型微塑料(MPs)的环境行为对农田生态系统的可持续发展具有极为重要的意义。
土壤动物是陆地生态系统中的活跃生物群体,在土壤发育、能量流动和物质循环过程中发挥着至关重要的作用[6],但MPs的存在对土壤动物造成了显著的负面影响。一方面,粒径较小的MPs可以被土壤动物摄食,并在进入机体后参与生理生化反应,发生生物累积,导致机体功能受损、活动能力下降,生长繁殖能力减弱[7];另一方面,MPs表面粗糙,作为载体可以为污染物提供附着点位,携带污染物进入动物体内,进一步加剧对土壤动物的生物效应[8]。此外,Ding等[9]研究证实MPs在土壤中的老化程度不同,其对土壤动物的生物效应也会发生改变。
蚯蚓作为土壤生态系统中常见的土壤动物,对土壤环境变化极为敏感,因此被视为研究土壤污染物毒性效应的理想模式生物[10]。其中,赤子爱胜蚓因其广泛的分布、对各类实验条件的高度适应以及在生态毒理学研究中的独特价值,常被用作指示生物,以评估污染物对土壤动物的毒性效应[11]。
尽管MPs的土壤生态效应研究已取得阶段性进展,但仍存在以下维度的局限性。首先,现有研究体系多基于传统石油基MPs,对可降解MPs在土壤中的老化特征及生态风险缺乏系统认知;其次,既往研究多采用急性暴露模式(≤28天),时间尺度存在缺陷,难以揭示自然老化过程中MPs性质改变对生物体的累积效应;再者,MPs在环境中的自然老化与生物毒性效应的动态关联机制尚未建立完整的理论框架。基于此,本研究通过微宇宙实验探究不同暴露时间下传统与可降解MPs对蚯蚓产生的毒性效应,拟建立“老化时间-物理化学性质-生物响应”三者的关联模型,明确不同类型MPs在土壤中的老化特征,系统评估MPs暴露下蚯蚓的氧化应激反应、组织病理变化及体内生物累积过程,以期揭示MPs对土壤生态系统潜在风险的生态毒理学机制,为农田微塑料污染的风险评估和可降解农膜的合理应用提供科学依据。
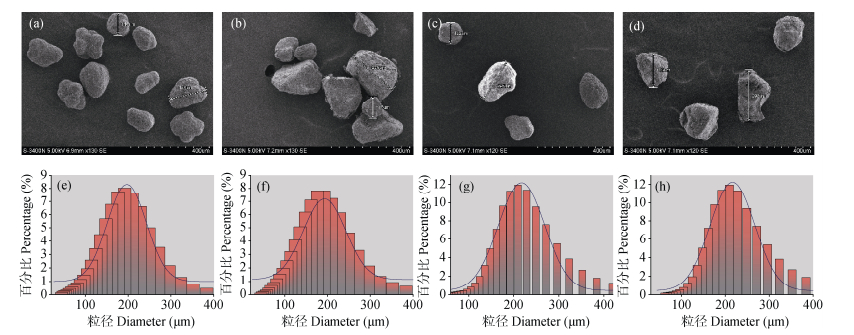
1 材料与方法 1.1 供试材料基于农田MPs污染特征,选用PE-MP和PLA-MP为模式污染物。实验材料分为两类,荧光标记型MPs(λEx/λEm=538 /580 nm,天津倍思乐色谱技术开发中心)用于动态追踪蚯蚓肠道内MPs的积累量;未标记型MPs(广东恒发塑化公司)用于老化特征表征和毒性机制研究。未荧光标记型MPs与乙醇(95%)按照1︰10(m/V)比例,混匀仪60 r·min–1漂洗2 h,TGL-18R高速离心机3 500 r·min–1离心、过滤,然后用去离子水代替乙醇,两试剂交替清洗3个循环,洗涤后的MPs于真空干燥箱(40 ℃)干燥至恒重,密封避光保存。通过扫描电子显微镜(SEM)和激光粒度仪对两类MPs形态(未标记型MPs:图 1a和图 1b;荧光标记型MPs:图 1c和图 1d)和粒径(未标记型MPs:图 1e和图 1f;标记型MPs:图 1g和图 1h)表征,确保两类材料具有生物学行为可比性。
|
图 1 不同类型MPs的SEM图像(PE-MP:a,c;PLA-MP:b,d)及粒径分布(PE-MP:e,g;PLA-MP:f,h) Fig. 1 SEM images (PE-MP: a, c;PLA-MP: b, d) and particle size distribution (PE-MP: e, g;PLA-MP: f, h) of different types of microplastics |
本研究中受试蚯蚓选择赤子爱胜蚓(Eisenia fetida,寡毛纲,正蚓科),购买自陕西省杨凌区正和生物公司。优先选择生殖带清晰、体型均匀、活动水平相近、体重在300~500 mg之间的个体,以减少蚯蚓个体差异引起的实验误差。
供试土壤采集于陕西省西北农林科技大学实验田(34°17′N,108°01′E),采集0~20 cm的表层土壤作为实验用土,清除根系等杂质后室温风干,过2 mm筛备用。已知实验田附近无已知点源污染。通过密度浮选(ZnCl2溶液,ρ=1.50 g/cm3),0.45 μm滤膜收集,体视显微镜(SZX16,Olympus,日本)定量统计[12],得到单位采样土壤中MPs含量为0.008%,与实验设置MPs浓度相比,影响可忽略不计。供试土壤基本理化性质如表 1所示。
|
|
表 1 供试土壤基本理化性质 Table 1 Basic physico-chemical properties of soil samples |
实验设置3组处理:仅蚯蚓组(Q),聚乙烯暴露组(PE+Q)和聚乳酸暴露组(PLA+Q)。每组设置5个生物学重复。微塑料暴露浓度设置为1.5%(w/w),此浓度设置是基于我国大棚种植区农膜微塑料的富集特性,连续覆膜5年后表层土壤MPs丰度可高达12 000~15 000 mg·kg–1[13],该剂量能反映污染区的生物效应特征。
供试蚯蚓在无污染土壤中培养一周,培养环境湿度设置为30%,温度控制在22 ± 2℃[14]。培养结束后,冲洗蚯蚓,放置在铺有湿润滤纸的培养皿中,室温条件下避光清肠48 h。然后随机选择20条蚯蚓转移至聚丙烯树脂花盆中(高14 cm,底部直径10 cm,顶部直径15 cm,容积约1.8 L),每个花盆装有1 kg土和对应比例重量的MPs,土壤表面平铺3 g枯落物(1 cm×1 cm大小)作为蚯蚓的食物,实验周期内不再补充食物。花盆上口和底部排水孔用1.5 mm孔隙的双层纱布缚紧,防止蚯蚓逃逸。环境设置同培养条件,实验周期60天,分别在第30天,60天取样,筛选提取土壤中MPs,同期测定蚯蚓及MPs相关指标。
(1)土壤中MPs提取。采用密度浮选结合氧化消解法进行土壤中微塑料的提取。具体操作步骤如下:首先将风干土样经研磨后过1 mm不锈钢筛网,然后按固液比1︰10(m/V)加入密度为1.50 g·cm–3的ZnCl2溶液,超声波辅助震荡(40 kHz,10 min)后静置24 h浮选,再通过真空抽滤收集上清液中悬浮颗粒;将滤膜收集物转移至锥形瓶,按1:10(m/V)比例加入30% 过氧化氢溶液(H2O2),60 ℃恒温振荡(150 r·min–1)72 h去除有机质,再次抽滤后转移残余物至玻璃培养皿,于真空干燥箱(60 ℃)烘干至恒重,收集样品密封保存于干燥器中,供后续SEM及衰减全反射傅里叶红外光谱(ATR-FTIR)表征分析。
(2)抗氧化酶系统指标测定。清水冲洗蚯蚓表皮泥土和分泌物,黑暗条件下清肠24 h后,擦除蚯蚓体表水分并称重(精确到0.000 1 g)。按照1︰9(m/V)比例加入0.1 mol·L–1磷酸盐缓冲液(PBS,pH = 7.4),冰水浴条件下机械匀浆,2 500 r·min–1离心10 min,得到的上清液用于测定活性氧(ROS)、蛋白总量(TP)、丙二醛(MDA)、过氧化氢酶(CAT)、过氧化物酶(POD)、谷胱甘肽-S转氨酶(GSH-ST)和总超氧化物歧化酶(T-SOD)活力,测定步骤参考文献进行[15]。
(3)蚯蚓肠道MPs浓度的测定。清肠24 h后,沿着蚯蚓的身体轴线横向切开,转移肠组织至玻璃离心管中,加入1 mL硝酸消化2 h(70℃),然后用超纯水定容至5 mL。使用荧光分光光度计在538 nm和580 nm的激发和发射波长下测定蚯蚓肠道中MPs浓度。通过连续稀释荧光MPs悬浮液建立标准曲线,测量处理组蚯蚓肠道中的背景荧光。
(4)病理分析。将已完成清肠且体表干净的蚯蚓放置在玻璃离心管中,加入10%乙醇溶液进行麻醉,待蚯蚓无反应时取出,在戊二醛固定液(2.5%,Gluta固定液)中固定4 h后,用0.1 mol·L–1 PBS冲洗蚯蚓并擦干体表,放至玻璃离心管中,依次加入30%、50%、70%浓度梯度的乙醇溶液进行脱水,风干2 h,在SEM下观察蚯蚓体表损伤。蚯蚓在4%多聚甲醛溶液中固定24 h后,在熔融石蜡中浸泡包埋,用切片机横向切割得到4 μm厚的切片,经苏木精-伊红染色(H&E)后,用生物显微镜观察体壁、肠道和细胞病理。
1.3 数据分析所有数据均以平均值±标准误差的形式列出。数据的统计分析采用SPSS 26.0软件进行,使用单因素方差分析(ANOVA)处理对照组与处理组之间的差异进行显著性检验,设定P < 0.05为显著水平。此外,图表均使用Origin 2021软件绘制。
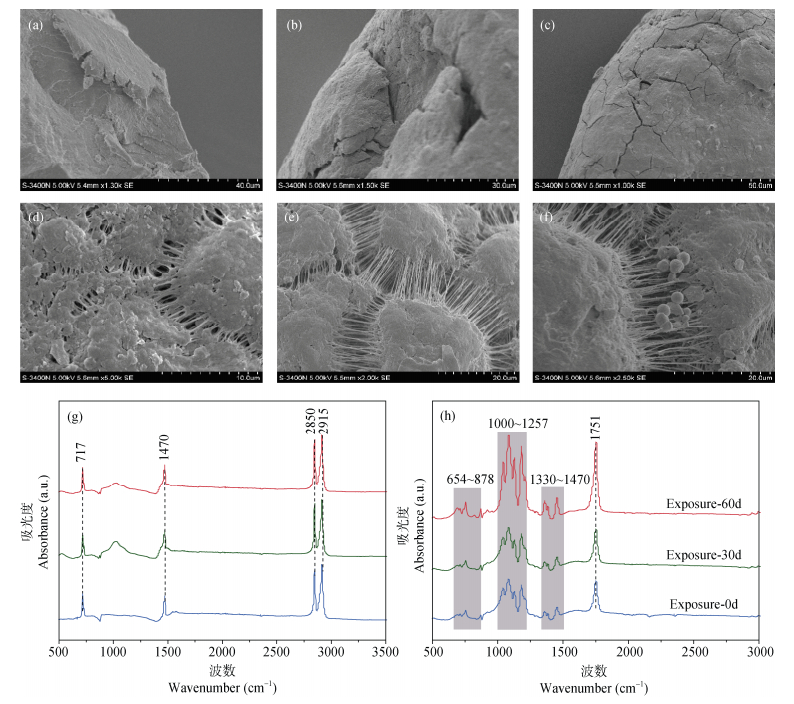
2 结果与分析 2.1 老化过程中MPs表面特征的变化不同老化时间下MPs表面特性如图 2所示。初始状态下,PLA-MP表面平滑且无裂缝(图 2a);老化30天后,其表层泛起,并出现少量细微裂缝(图 2b);当老化时间延长至60天时,PLA-MP表面出现大裂缝与密集小裂缝共存的复杂网络结构(图 2c)。对于PE-MP而言,其原始形态表现为短粗的纤维状连接线(图 2d),随着老化时间的延长,连接线逐渐拉伸,部分出现断裂,且层间结构趋向薄片化(图 2e),特别是在老化60天时,观察到单位结构颗粒发生氧化脱落,表现出明显的降解迹象(图 2f)。
|
图 2 不同暴露时间下MPs表面形态(PLA-MP:a,b,c;PE-MP:d,e,f)和特征峰(PE-MP:g;PLA-MP:h)变化 Fig. 2 Changes in surface morphology (PLA-MP: a, b, c;PE-MP: d, e, f) and characteristic peaks (PE-MP: g; PLA-MP: h) of microplastics at different exposure times |
利用ATR-FTIR分析,观察到PE-MP在717 cm–1、1 470 cm–1、2 850 cm–1和2 915 cm–1处峰强发生变化(图 2g),这主要归因于C-H弯曲振动。PLA-MP在654~878 cm–1处的峰强变化与C-H弯曲振动相关(图 2 h),C-O伸缩振动影响了1 000~1 257 cm–1处的峰强,而-CH的C-H弯曲振动影响了1 330 cm–1~1 470 cm–1处的峰强。酯基(-COO-)氧化导致的C=O伸缩振动影响了1 751 cm–1处的峰强。进一步计算1 750 cm–1与1 450 cm–1两处波长的透过率比值,发现MPs的羰基指数(Carbonyl Index,CI)随暴露时间的延长而增加,其中PE-MP的CI值从0.26增加至0.72,而PLA-MP的CI值则从3.23提升至3.35。
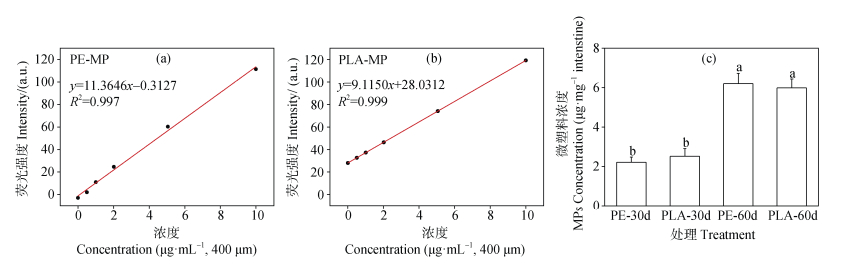
2.2 蚯蚓肠道中MPs浓度的变化将蚯蚓暴露于粒径小于400 μm的MPs环境后,观测不同暴露时间蚯蚓肠道内MPs的摄取与积累情况。发现至第60天,蚯蚓肠道内MPs浓度从初始的2.5 ± 0.28 μg·mg–1增加至6.17 ± 0.13 μg·mg–1(图 3c),且第60天肠道内MPs浓度显著高于第30天(P < 0.05)。同时,相关性分析表明暴露时间与蚯蚓肠道内MPs累积量之间呈正相关关系(图 3a和图 3b)。
|
图 3 浓度标准曲线(a,b)及蚯蚓肠道MPs累积变化(c) Fig. 3 Standard curve (a, b) and changes in microplastic concentration in the earthworm gut (c) |
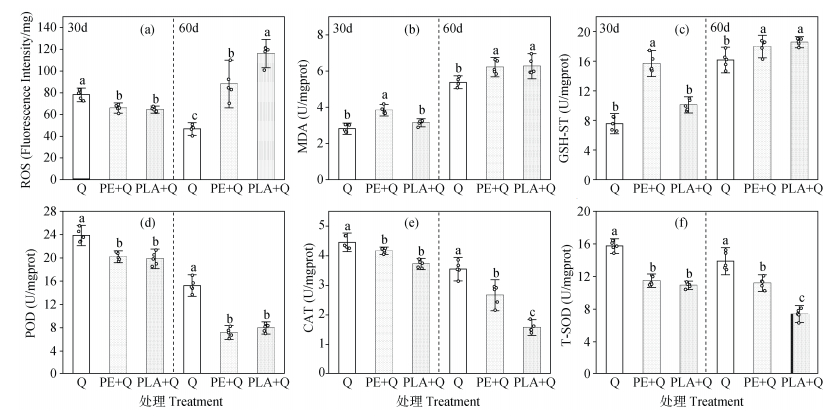
MPs暴露会破坏蚯蚓体内的氧化-抗氧化系统平衡,并引发氧化应激反应。研究表明,暴露30天时,各处理组活性氧(Reactive Oxygen Species,ROS)荧光强度较对照组均呈下降趋势(P < 0.05),表明短期暴露可能通过激活初期抗氧化防御系统降低ROS水平,而延长至60天时,发生明显的氧化应激逆转现象,其中PE+Q组(88.06 ± 12.60 Fluorescence intensity·mg–1 prot)与PLA+Q组(116.1 ± 8.62 Fluorescence intensity·mg–1 prot)的ROS水平较对照组分别提升了1.88倍和2.28倍(图 4a)。ROS异常累积显著加剧了脂质过氧化反应(P < 0.05),表现为MPs暴露组蚯蚓体内MDA含量升高。暴露60天时,PE+Q处理MDA含量为6.21 ± 0.36 U·mg–1 prot,略低于PLA+Q组的6.27 ± 0.41 U·mg–1 prot,但不同暴露处理间差异不显著(图 4b,P > 0.05)。在抗氧化酶活性方面,MPs暴露显著抑制了蚯蚓体内T-SOD、CAT和POD活性,相较于Q处理,酶活性的降低呈现PLA+Q > PE+Q > Q的趋势,同时,暴露时间的延长进一步加剧了这种抑制效应(图 4d-图 4f)。此外,GSH-ST作为参与机体解毒过程的关键酶,其活性在MPs暴露处理中同样表现出上升趋势,与MDA含量的变化规律相吻合,均显著高于对照处理(图 4c)。
|
图 4 MPs暴露下蚯蚓体内抗氧化酶活性水平(a:ROS,b:MDA,c:GSH-ST,d:POD,e:CAT,f:T-SOD) Fig. 4 Levels of antioxidant enzyme activities in earthworms exposed to microplastics (a: ROS, b: MDA, c: GSH-ST, d: POD, e: CAT, f: T-SOD) |
MPs暴露下蚯蚓表皮损伤如图 5所示。Q处理中蚯蚓表皮光滑、刚毛完整、无明显物理损伤(图 5a和图 5d)。PE-MP暴露下,蚯蚓的刚毛出现明显的折裂现象,且随着暴露时间延长,节间处表皮缺失,导致部分组织暴露(图 5b和图 5e)。PLA-MP处理中,蚯蚓节间沟处分泌了大量黏性物质,随着暴露时间延长,表皮黏液细胞出现空泡化现象(图 5c和图 5f)。

|
注:a、b、c表示培养30天的损伤程度,d、e、f表示培养60天的损伤程度。 Note: a, b, and c are the levels of damage after 30 days of cultivation, while d, e and f are the levels of damage after 60 days of cultivation. 图 5 不同MPs暴露时间蚯蚓表皮损伤程度(Q:a,d;PE+Q:b,e;PLA+Q:c,f) Fig. 5 Extent of epidermal damage in earthworms with different microplastic exposure times (Q: a, d;PE+Q: b, e;PLA+Q: c, f) |
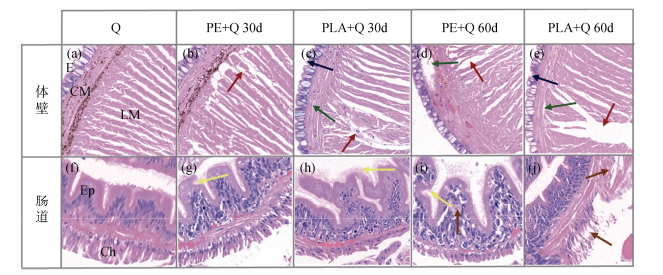
MPs暴露对蚯蚓组织产生了显著影响。Q处理蚯蚓呈现出典型的健康状态,其环肌与纵肌排列井然有序,肠上皮细胞表面光滑无损,整体组织结构保持完好(图 6a和图 6f)。PE-MP暴露30天后,蚯蚓组织结构出现初步损伤,环肌区域充血,纵肌发生纤维化(图 6b和图 6g),暴露时间延长至60天,损伤进一步加剧,肠上皮区域黄色细胞发生病变(图 6d和图 6i)。PLA-MP暴露组中,蚯蚓前期损伤程度相对较低,但仍可观察到环肌有少量充血,纵肌同样出现纤维化趋势(图 6c和图 6h)。然而,随着暴露时间的推移,肠上皮明显肿胀(图 6j),且肌肉组织逐渐松散,甚至在某些区域出现瓦解现象(图 6e)。
|
注:E:表皮,CM:环肌,LM:纵肌,Ep:肠上皮,Ch:黄色细胞。红色箭头表示纵肌纤维化,绿色箭头表示环肌损伤,蓝色箭头表示表皮皮层缺失,黄色箭头表示肠上皮损伤,棕色箭头表示黄色细胞病变。 Note: epidermis (E), circular muscle (CM), longitudinal muscle (LM), epithelium (Ep) and chloragogenous tissue (Ch). Red, green, blue, yellow and brown arrows represent longitudinal muscle fibrosis, circular muscle necrosis, epidermal damage, intestinal epithelium damage, and chloragogenous tissue Pathological changes. 图 6 蚯蚓组织病理学 Fig. 6 Histopathology of earthworms |
通过对比不同类型MPs在土壤环境中的老化行为,发现PLA-MP较PE-MP更易发生老化降解。相同暴露条件下,PLA-MP表现出更显著的老化特征,这种差异可能归因于材料自身的化学组成和结构特性。具体而言,PLA-MP由生物降解聚合物与扩链剂、成核剂等功能性添加剂复合制成,更易被环境中的微生物和酶系统识别和降解[16]-[17];从分子水平分析,构成MPs的聚合物单体结构差异是导致PE-MP和PLA-MP老化程度不同的根本原因。PE-MP具有高度稳定的饱和碳链结构,而PLA-MP的主链中含有易水解的-COO-基团。大部分细菌和真菌能在PLA-MP表面定殖并富集,其分泌的胞外水解酶可以催化PLA-MP中-COO-断裂,生成分子量较低,降解较快的低聚物和单体,形成“老化-降解-毒性”的正反馈循环,同时,老化产物作为碳源刺激微生物增殖,而增殖的微生物群落进一步加速MPs老化[18]。
3.2 不同老化时间下微塑料存在对蚯蚓氧化应激响应的差异分析在生物体生长代谢过程中,外界因素的刺激会导致机体ROS水平失衡,产生氧化胁迫[19]。为应对此类胁迫,生物体通过一系列抗氧化机制,如调控CAT、POD、T-SOD及GSH-ST水平等,以恢复ROS稳态,进而抵御外界损伤并减轻细胞氧化压力。本研究聚焦于MPs暴露下蚯蚓的生理响应,揭示了抗氧化酶系统的独特变化特征。暴露初期,蚯蚓体内ROS水平下降,至第60天时,PLA-MP暴露组ROS水平高达116.14 Fluoe intensity/mg,此现象伴随着脂质过氧化反应的加剧和GSH-ST活性的诱导上调,以及T-SOD、CAT和POD等关键抗氧化酶活性的显著下调。值得注意的是,第60天ROS含量显著升高,抗氧化酶活性普遍降低,且低于第30天,其中PLA-MP处理组的酶活性下降尤为显著(P < 0.05),这表明MPs暴露触发了蚯蚓体内的氧化应激反应,激活了抗氧化酶系统,促使蚯蚓通过调整代谢途径以缓解外界压力。同时,ROS水平上升与MPs在蚯蚓体内的累积效应密切相关。随着暴露时间延长,MPs进一步老化,其亲水性增强,含氧官能团增加[19][20],粒径变小[21],更易被蚯蚓摄食,MPs结构的复杂变化加剧了其对生物体的负面影响。然而,部分研究发现当蚯蚓暴露于500 mg·kg–1的PE-MP 7天后,其ROS和抗氧化酶水平降低;而持续暴露至28天时,ROS浓度显著升高至对照组的1.8倍(P < 0.01),并伴随CAT(+35.2%)、SOD(+28.9%)等关键抗氧化酶的代偿性激活[22],并将此归因于阶段性的解毒调控机制,即短期暴露阶段生物体通过降低基础代谢水平减少ROS产生,而长期暴露导致抗氧化酶系统清除能力饱和,引发了氧化损伤的链式反应。这与本研究中观测到抗氧化酶活性持续下降的现象存在差异,可能是由于本研究仅设定单一MPs浓度,未能充分反映不同浓度梯度下抗氧化酶活性的动态变化特征。此外,MPs一旦进入蚯蚓肠道,不仅作为外源性物质存在,还会在肠道微生物群落(如变形菌门Proteobacteria和科曼氏菌科Comamonadaceae)的作用下发生碎裂与轻微降解。这一过程不仅释放了MPs基质中的添加剂,还可能生成新的有毒副产物,通过增强毒性效应,对蚯蚓造成更为严重的损伤。因此,第60天时ROS的过量累积可能已经导致抗氧化防御系统的功能失衡,进而引发抗氧化酶活性的进一步下降[23]。同时,本研究仅着重探讨了抗氧化酶防御系统,而最新研究表明,联合污染物暴露可能激活其他解毒途径。例如,杨晓霞等[24]发现,PE-MP与镉的联合暴露可诱导蚯蚓细胞色素P450酶活性升高3.2倍,该团队随后发现PE-MP单独暴露60天时细胞色素P450酶活性下低49.3%~53.6%,这说明MPs的毒性机制存在显著的环境条件依赖[24]。鉴于此,后续研究将构建涵盖氧化防御系统、解毒代谢系统、免疫应激反应和肠道微生物组的多维度评价体系,以系统揭示其生物毒理学效应。
3.3 不同老化时间下MPs对蚯蚓组织病理学变化的影响MPs以其高度的疏水特性和显著的吸附能力,对生物体构成了复杂且多样的损伤机制。SEM结果表明随着MPs暴露时间的持续延长,蚯蚓自身的物理损伤并未减弱。PE-MP暴露环境下,初期蚯蚓刚毛发生折裂,随后表现为表皮严重缺失和组织裸露;而在PLA-MP胁迫下,蚯蚓在暴露初期通过表皮的大黏液腺分泌高酸性的硫酸粘多糖作为防御,随着暴露时间延长,其表皮的黏液细胞出现了空泡化的病理变化。组织切片分析进一步揭示了MPs暴露对蚯蚓造成的显著影响,研究结果显示,蚯蚓的肌肉及上皮细胞均遭受了显著的损伤与病变,且不同暴露条件损伤程度具有差异。主要病理特征包括:(1)随着MPs暴露时间的延长,蚯蚓肠上皮萎缩,甚至脱落,并伴有颗粒状的脂褐素样沉积物出现。这是因为MPs老化后含氧官能团数量增加,导致其亲水性、极性和表面电荷增加[26],更易与土壤有机质(SOM)发生共价结合,促使蚯蚓摄食过程中MPs-有机复合体的生物可给性提高,进而加剧对肠道的损伤[27];(2)PLA-MP暴露对蚯蚓的毒害尤为严重,不仅引发了明显的炎症反应,还破坏了盲肠结构。这一发现与Ding等[28]的研究结果相契合,即相较于PE-MP,PLA-MP表现出更为强烈的生理毒性,材料的性质差异是造成毒性差异的主要因素。具体而言,PE-MP因其体积小、形状不规则且边缘锋利,更易于被生物体摄食或粘附于体表,从而引发机械性损伤[29][30];PLA-MP则更易与生物膜及细胞器发生相互作用[31],诱导机体发生氧化应激并触发炎症反应[30]。此外,在生物体内,PLA-MP在肠道微生物的作用下更易解聚为低聚物和单体,该生物降解过程伴随添加剂的持续浸出,进一步加剧了其毒性效应[32][33]。同时,研究还发现长期MPs暴露下蚯蚓体表组织已遭受严重损伤,其并未表现出对MPs胁迫环境的适应,而是通过分泌警报信息素来参与解毒过程,进一步表明MPs对生物体的作用机制极为复杂,涵盖了组织损伤、氧化应激、神经毒性以及肠道微生物群失调等多方面,这些病理过程相互诱导、相互影响[34][35]。
4 结论传统PE-MP和可降解PLA-MP在土壤中的老化过程均会对赤子爱胜蚓造成显著的生理损伤,并诱导机体发生氧化应激反应。相较于PE-MP,PLA-MP更易老化且表现出更强烈的生理毒性;长期MPs暴露实验进一步揭示,MPs会在蚯蚓体内累积,不仅加剧了其对蚯蚓的生理损伤,还可能促使由MPs引起的物理损伤向更为复杂的化学损伤转变。本研究揭示了生物降解塑料的剂量和时间双因素叠加效应,为生物降解塑料产品的环境准入标准提供了新的科学依据。
| [1] |
Sahai H, García V M, Murcia M M, et al. Exploring sorption of pesticides and PAHs in microplastics derived from plastic mulch films used in modern agriculture[J]. Chemosphere, 2023, 333: 138959. DOI:10.1016/j.chemosphere.2023.138959
(  0) 0) |
| [2] |
Zhang F, Deng Z, Ma L, et al. Pollution characteristics and prospective risk of microplastics in the Zhengzhou section of Yellow River, China[J]. Science of the Total Environment, 2024, 931: 172717. DOI:10.1016/j.scitotenv.2024.172717
(  0) 0) |
| [3] |
Zhao Y, Chen X G, Wen H J, et al. Research status and prospect of control technology for residual plastic film pollution in farmland (In Chinese)[J]. Transactions of the Chinese Society for Agricultural Machinery, 2017, 48(6): 1-14. [赵岩, 陈学庚, 温浩军, 等. 农田残膜污染治理技术研究现状与展望[J]. 农业机械学报, 2017, 48(6): 1-14.]
(  0) 0) |
| [4] |
Xie B, Bai R R, Sun H S, et al. Synthesis, biodegradation and waste disposal of polylactic acid plastics: A review (In Chinese)[J]. Chinese Journal of Biotechnology, 2023, 39(5): 1912-1929. [谢彬, 白茸茸, 孙华山, 等. 聚乳酸塑料合成、生物降解及其废弃物处置的研究进展[J]. 生物工程学报, 2023, 39(5): 1912-1929.]
(  0) 0) |
| [5] |
Wang S R, Gao P, Han Q, et al. Insights into photoaging behaviors and mechanisms of biodegradable and conventional microplastics in soil[J]. Journal of Hazardous Materials, 2024, 480: 136418. DOI:10.1016/j.jhazmat.2024.136418
(  0) 0) |
| [6] |
Feng X Y, Sun Y H, Zhang S W, et al. Ecological effects of microplastics on soil-plant systems (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 299-313. DOI:10.11766/trxb202007190402 [冯雪莹, 孙玉焕, 张书武, 等. 微塑料对土壤–植物系统的生态效应[J]. 土壤学报, 2021, 58(2): 299-313.]
(  0) 0) |
| [7] |
Wu X, Zhang Z, Guo X. A systematic review of the mechanisms underlying the interactions between microplastics and microorganism in the environment[J]. Trends in Analytical Chemistry, 2024, 172: 117543. DOI:10.1016/j.trac.2024.117543
(  0) 0) |
| [8] |
Wang F, Wang Q, Adams C A, et al. Effects of microplastics on soil properties: Current knowledge and future perspectives[J]. Journal of Hazardous Materials, 2022, 424: 127531. DOI:10.1016/j.jhazmat.2021.127531
(  0) 0) |
| [9] |
Ding J, Liang Z, Lv M, et al. Aging in soil increases the disturbance of microplastics to the gut microbiota of soil fauna[J]. Journal of Hazardous Materials, 2024, 461: 132611. DOI:10.1016/j.jhazmat.2023.132611
(  0) 0) |
| [10] |
Liang X, Zhou D, Wang J, et al. Evaluation of the toxicity effects of microplastics and cadmium on earthworms[J]. Science of the Total Environment, 2022, 836: 155747. DOI:10.1016/j.scitotenv.2022.155747
(  0) 0) |
| [11] |
Gao Y, Luo Y M. Earthworms as bioindicators of soil pollution and their potential for remediation of contaminated soils (In Chinese)[J]. Acta Pedologica Sinica, 2005, 42(1): 140-148. DOI:10.11766/trxb200402300122 [高岩, 骆永明. 蚯蚓对土壤污染的指示作用及其强化修复的潜力[J]. 土壤学报, 2005, 42(1): 140-148.]
(  0) 0) |
| [12] |
Zhang L, Sun D, Zhang J Q, et al. Research progress on the migration of agricultural film microplastics and phthalates in soil (In Chinese)[J]. Soils, 2024, 56(5): 938-947. [张蕾, 孙东, 张建强, 等. 农膜微塑料与酞酸酯在土壤中迁移的研究进展[J]. 土壤, 2024, 56(5): 938-947.]
(  0) 0) |
| [13] |
Zhang Q Q, Ma Z R, Cai Y Y, et al. Agricultural plastic pollution in China: generation of plastic debris and emission of phthalic acid esters from agricultural films[J]. Environmental Science & Technology, 2021, 55(18): 12459-12470.
(  0) 0) |
| [14] |
Miao H, Xu J M, Yu Y, et al. Toxic effects of atrazine on earthworms in three forest soils (In Chinese)[J]. Soils, 2023, 55(6): 1316-1322. [苗桓, 许加明, 虞悦, 等. 三种森林土壤中莠去津对蚯蚓的毒性效应[J]. 土壤, 2023, 55(6): 1316-1322.]
(  0) 0) |
| [15] |
Cao X, Liang Y, Jiang J, et al. Organic additives in agricultural plastics and their impacts on soil ecosystems: Compared with conventional and biodegradable plastics[J]. Trends in Analytical Chemistry, 2023, 166: 117212. DOI:10.1016/j.trac.2023.117212
(  0) 0) |
| [16] |
Pooja N, Chakraborty I, Rahman M H, et al. An insight on sources and biodegradation of bioplastics: A review[J]. 3 Biotech, 2023, 13(7): 220. DOI:10.1007/s13205-023-03638-4
(  0) 0) |
| [17] |
Zhang S W, Ren S, Pei L, et al. Toxic effects of polyethylene and polylactic acid microplastics on earthworms (In Chinese)[J]. Journal of Applied and Environmental Biology, 2023, 29(2): 322-327. [张书武, 任珊, 裴磊, 等. 聚乙烯和聚乳酸微塑料对蚯蚓的毒性效应[J]. 应用与环境生物学报, 2023, 29(2): 322-327.]
(  0) 0) |
| [18] |
Yu Y, Lin S, Sarkar B, et al. Mineralization and microbial utilization of poly (lactic acid) microplastic in soil[J]. Journal of Hazardous Materials, 2024, 476: 135080. DOI:10.1016/j.jhazmat.2024.135080
(  0) 0) |
| [19] |
Wang Q, Zhang Y, Wang J, et al. The adsorption behavior of metals in aqueous solution by microplastics effected by UV radiation[J]. Journal of Environmental Sciences, 2020, 87: 272-280. DOI:10.1016/j.jes.2019.07.006
(  0) 0) |
| [20] |
Liu G, Zhu Z, Yang Y, et al. Sorption behavior and mechanism of hydrophilic organic chemicals to virgin and aged microplastics in freshwater and seawater[J]. Environmental Pollution, 2019, 246: 26-33. DOI:10.1016/j.envpol.2018.11.100
(  0) 0) |
| [21] |
Wen X, Du C, Xu P, et al. Microplastic pollution in surface sediments of urban water areas in Changsha, China: Abundance, composition, surface textures[J]. Marine Environmental Research, 2018, 136: 414-423.
(  0) 0) |
| [22] |
Chen Y L, Liu X N, Leng Y F, et al. Defense responses in earthworms (Eisenia fetida) exposed to low-density polyethylene microplastics in soils[J]. Ecotoxicology and Environmental Safety, 2020, 187: 109788. DOI:10.1016/j.ecoenv.2019.109788
(  0) 0) |
| [23] |
Yang J, Li L Z, Zhou Q, et al. Microplastics contamination of soil environment: Sources, processes and risks (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 281-298. DOI:10.11766/trxb202006090286 [杨杰, 李连祯, 周倩, 等. 土壤环境中微塑料污染: 来源、过程及风险[J]. 土壤学报, 2021, 58(2): 281-298.]
(  0) 0) |
| [24] |
Yang X X, Zhang X M, Shu X, et al. Toxic effects and interaction evaluation of polyethylene microplastics and cadmium combined exposure on earthworm Eisenia fetida (In Chinese)[J]. Acta Scientiae Circumstantiae, 2024, 44(7): 482-496. [杨晓霞, 张雪梅, 舒晓, 等. 聚乙烯微塑料与镉联合暴露对赤子爱胜蚓的毒性效应及交互作用评估[J]. 环境科学学报, 2024, 44(7): 482-496.]
(  0) 0) |
| [25] |
Yang X, Zhang X, Shu X, et al. The effects of polyethylene microplastics on the growth, reproduction, metabolic enzymes, and metabolomics of earthworms Eisenia fetida[J]. Ecotoxicology and Environmental Safety, 2023, 263: 115390. DOI:10.1016/j.ecoenv.2023.115390
(  0) 0) |
| [26] |
Kong Y, Zuo X Z, Yi P, et al. Research progress on analysis of the properties of natural organic matter and its interaction with soil minerals and exogenous pollutants (In Chinese)[J]. Environmental Chemistry, 2021, 40(9): 2715-2726. [孔颖, 左翔之, 易鹏, 等. 天然有机质的性质分析及其与土壤矿物和外源污染物相互作用研究进展[J]. 环境化学, 2021, 40(9): 2715-2726.]
(  0) 0) |
| [27] |
Ma S R, Li S X, Guo X T. A review on aging characteristics, mechanism of microplastics and their effects on the adsorption behaviors of pollutants (In Chinese)[J]. China Environmental Science, 2020, 40(9): 3992-4003. [马思睿, 李舒行, 郭学涛. 微塑料的老化特性、机制及其对污染物吸附影响的研究进展[J]. 中国环境科学, 2020, 40(9): 3992-4003.]
(  0) 0) |
| [28] |
Ding W, Li Z, Qi R, et al. Effect thresholds for the earthworm Eisenia fetida: Toxicity comparison between conventional and biodegradable microplastics[J]. Science of the Total Environment, 2021, 781: 146884. DOI:10.1016/j.scitotenv.2021.146884
(  0) 0) |
| [29] |
Guo X, Wang J. The chemical behaviors of microplastics in marine environment: A review[J]. Marine Pollution Bulletin, 2019, 142: 1-14.
(  0) 0) |
| [30] |
Lei L, Wu S, Lu S, et al. Microplastic particles cause intestinal damage and other adverse effects in zebrafish Danio rerio and nematode Caenorhabditis elegans[J]. Science of the Total Environment, 2018, 619/620: 1-8.
(  0) 0) |
| [31] |
Jeong C B, Won E J, Kang H M, et al. Microplastic size-dependent toxicity, oxidative stress induction, and p-JNK and p-p38 activation in the monogonont rotifer (Brachionus koreanus)[J]. Environment Science & Technology, 2016, 50(16): 8849-8857.
(  0) 0) |
| [32] |
Zhang J H, Meng H, Kong X C, et al. Combined effects of polyethylene and organic contaminant on zebrafish (Danio rerio): Accumulation of 9-nitroanthracene, biomarkers and intestinal microbiota[J]. Environmental Pollution, 2021, 277: 116767. DOI:10.1016/j.envpol.2021.116767
(  0) 0) |
| [33] |
Yu H, Shi L L, Fan P, et al. Effects of conventional versus biodegradable microplastic exposure on oxidative stress and gut microorganisms in earthworms: A comparison with two different soils[J]. Chemosphere, 2022, 307: 135940. DOI:10.1016/j.chemosphere.2022.135940
(  0) 0) |
| [34] |
Zhang L J, Chen J, Ao R X, et al. Degradation processes of biodegradable plastics in soil and their effects on soil animals (In Chinese)[J]. Environmental Science, 2025, 46(2): 1145-1154. [张莉娟, 陈洁, 敖瑞雪, 等. 土壤中生物降解塑料的降解过程及其对土壤动物的影响[J]. 环境科学, 2025, 46(2): 1145-1154.]
(  0) 0) |
| [35] |
Tousoulis D, Andreou I, Antoniades C, et al. Role of inflammation and oxidative stress in endothelial progenitor cell function and mobilization: Therapeutic implications for cardiovascular diseases[J]. Atherosclerosis, 2008, 201(2): 236-247. DOI:10.1016/j.atherosclerosis.2008.05.034
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


