2. 西南大学资源环境学院, 重庆 400716;
3. 西南交通大学环境科学与工程学院, 成都 611756
2. College of Resources and Environment, Southwest University, Chongqing 400716, China;
3. School of Environmental Science and Engineering, Southwest Jiaotong University, Chengdu 611756, China
微塑料作为一种全球性新污染物,其环境归趋与生态风险已成为环境科学领域的研究热点。近年来,农田土壤已成为微塑料重要的汇集区,其年输入量可能远超海洋环境[1]。地膜残留、有机肥施用及污水灌溉等农业活动是土壤微塑料污染的主要来源[2]。微塑料进入土壤后可改变土壤孔隙结构、通气性及养分循环,并干扰微生物群落,进而影响土壤有机质的稳定性与转化过程[3-4]。
土壤溶解性有机质(DOM)是土壤有机质中最活跃的组分,在维持微生物代谢、驱动碳氮转化过程及影响污染物迁移等方面具有重要作用,其芳香性、分子量及疏水性及组成结构等特征易受环境影响[5]。已有研究表明,微塑料可通过改变土壤孔隙结构、有机质分布和微生物代谢活动,间接调控DOM的浓度与化学组成[6-7],但相关研究多集中于单一微塑料或单一土壤类型,或聚焦于微塑料含量变化对DOM浓度的影响[8-9]。对于不同类型微塑料作用下,典型农田土壤中DOM多维结构特征(如芳香性、分子量及其荧光组分)响应的系统性比较研究仍较为有限。
另一方面,微塑料本身的聚合物类型对其环境行为和生态效应具有重要影响。研究表明残留在环境中的微塑料逐渐老化、降解并进一步持续释放出添加剂、聚合物单体、降解产物等溶解性物质,即塑料源溶解性有机质(MPs-DOM)[10],且不同聚合物类型微塑料释放的MPs-DOM组成特征存在显著差异[11]。与传统石油基不可生物降解微塑料相比,生物可降解材质的MPs-DOM通常含有更多不稳定DOM,如脂质类、蛋白质/氨基糖类或碳水化合物类 [12]。MPs-DOM释放到土壤环境中直接成为土壤DOM的一部分,这可能会影响原有DOM的组成、转化与稳定性[13]。此外,土壤理化性质如pH、质地等在影响DOM特征上发挥重要作用[14]。例如,土壤pH下降会导致脂肪族、高度不饱和化合物及酚类化合物等不稳定组分的丰度增加[14-15]。然而,微塑料释放的MPs-DOM是否会在不同土壤背景下诱发DOM结构与组成的差异化变化,以及这种扰动是否受土壤类型调节,仍缺乏系统实验依据。
基于此,本研究以两种典型南方水稻土—发育于红壤母质的酸性金华水稻土(JH)和滨海相沉积母质碱性慈溪水稻土(CX)为供试土壤,分别选取环境中广泛检出的三类代表性微塑料(传统石油基微塑料:聚乙烯PE和聚氯乙烯PVC;生物可降解微塑料:聚乳酸-对苯二甲酸丁二醇酯共混物PLA+PBAT,Bio),开展室内微宇宙培养试验,系统探讨不同类型微塑料对两种土壤基础理化性质、微生物生物量碳氮、DOM紫外光谱结构参数以及三维荧光光谱荧光组分组成的影响。研究旨在揭示“微塑料类型-土壤类型”交互作用对DOM特性的影响机制,为微塑料的环境风险评估与农田碳循环调控策略提供科学依据。
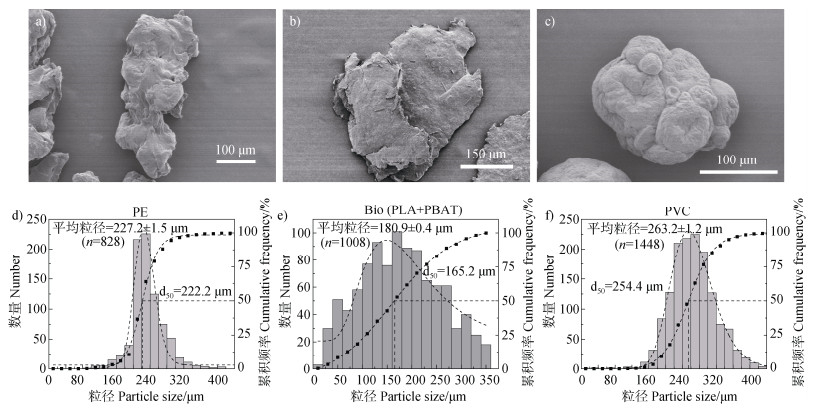
1 材料与方法 1.1 供试材料供试微塑料选用三种聚合物类型:聚乙烯(PE)、聚乳酸/聚己二酸-对苯二甲酸丁二醇酯共混物(PLA+PBAT,以下简称Bio)和聚氯乙烯(PVC)。其中,PE和PVC微塑料为市售商品微塑料,购自于冠步科技有限公司;Bio微塑料由PLA+PBAT材质的购物袋经冷冻球磨法制备获得。三种微塑料颗粒经扫描电子显微镜(SEM)观察其表面形貌,并使用Nano Measure 1.2软件进行粒径统计(图 1)。PE颗粒呈椭球状,表面粗糙;Bio颗粒为不规则片状,存在裂痕,表面较粗糙;PVC颗粒多为球形,表面附有小颗粒聚集。三种微塑料的粒径均呈正态分布,平均粒径分别为PE:(227.2±1.5)μm(n=828)、Bio:(180.9±0.4)μm(n=1 008)和PVC:(263.2±1.2)μm(n=1 448)。
|
注:a)PE的扫描电镜图;b)Bio的扫描电镜图;c)PVC的扫描电镜图;d)PE的粒径分布组成;e)Bio的粒径分布组成;f)PVC的粒径分布组成。 Note: a) SEM of PE MPs; b) SEM of Bio MPs; c) SEM of PVC MPs; d) Particle size of PE; e) Particle size of Bio; f) Particle size of PVC. 图 1 不同聚合物类型微塑料的扫描电镜观测及粒径分布图 Fig. 1 SEM images and particle size distributions of MPs with different polymer types |
供试土壤为两种成土母质的水稻土:发育于红壤母质的金华水稻土(JH)和发育于滨海相沉积母质的慈溪水稻土(CX)。土壤基础理化性质见表 1,JH水稻土为强酸性土壤(pH5.03),CX水稻土为碱性土壤(pH8.26);CX水稻土的有机碳(SOC)和全碳(TC)均高于JH。根据国际土壤质地分类标准,JH水稻土为黏壤土,CX水稻土为粉砂质黏壤土。
|
|
表 1 供试土壤基础理化性质 Table 1 The physico-chemical properties of the tested soil |
采用室内微宇宙培养法探究微塑料对两种水稻土的影响。称取风干过2 mm筛的土样220 g置于250 mL聚丙烯烧杯中,按质量分数0.5%分别添加PE、Bio和PVC微塑料,并设无添加对照(CK)。混匀后覆盖带孔保鲜膜以维持通气,每2天补加超纯水保持60%田间持水量,于25 ℃恒温培养箱中避光培养。分别于培养15、30、45和60 d采样,冻干后–20 ℃保存待测。各处理均设置3个重复,4个取样时间点累积样本量96个。
1.3 土壤样品分析分别对培养15、30、45和60 d的土壤样品进行基础理化性质分析[16]:土壤pH采用电极法测定(土水比1∶2.5),SOC采用重铬酸钾法测定,TC和TN采用元素分析仪测定,土壤机械组成采用激光粒度仪测定。采用氯仿熏蒸浸提法分别对培养30和60 d的土壤样品进行微生物生物量碳(MBC)和微生物生物量氮(MBN)的测定,检测分析由栢晖生物有限公司完成。
土壤DOM样品提取参考Huang等[17]研究:采用TOC分析仪(MultiN/C 3100)测定1∶5(w/v)的土壤∶水悬浮液中溶解性有机碳(DOC)和溶解性有机氮(DON)浓度。土壤DOM光谱测定:使用UV-Vis分光光度计(Mapada,UV-6100S)对土壤DOM溶液进行紫外-可间光谱全波长扫描(190~700 nm,增量为1 nm),并以去离子水作为空白参比[18]。为减少內滤效应,将样品DOC浓度稀释至10 mg·L–1后进行三维荧光光谱分析(日立,F-7000)。检测参数为:发射波长(λEm)范围200~600 nm,激发波长(λEx)范围200~500 nm,Ex和Em的增量为5 nm,带宽设置为2 nm,扫描速度为12 000 nm·min–1,扫描电压为700 V[19]。测定时以超纯水作为空白,用于扣除水拉曼散射背景,并去除瑞利散射,得到三维荧光数据矩阵。
1.4 数据处理紫外-可见光谱参数的计算参考He等[18]研究。SUVA254、SUVA260、SUVA280为波长为254、260和280 nm下单位DOC浓度的吸光度系数,其中SUVA254反映DOM的芳香性,与芳香族碳含量和腐殖化程度呈正相关[20];SUVA260用来表征DOM分子的疏水性[21];SUVA280与分子量成正相关关系[20];光谱斜率SR(S275-295/S350-400)常用于衡量DOM分子量和结构复杂度,通常与DOM分子量成反比[22]。
三维荧光数据的分析参考Lee等[21]:使用MATLAB对DOM荧光数据进行预处理,依次去除拉曼散射、一、二级瑞利散射,并结合常规矫正和非负约束方法剔除异常样本与数据。经预处理后的荧光矩阵用于参数提取和光谱绘图,绘图工作在OriginPro 2021中完成。随后,利用MATLAB中DOMFluor工具箱进行平行因子分析(PARAFAC),并通过半分法验证模型可靠性。最终将提取的激发-发射波长(Ex-Em)与在线Openfluor数据库(http://www.openfluor.org)进行比对,以识别组分类型。
统计分析采用SPSS 22.0软件进行,结果以“均值±标准差”表示,多重比较采用Tukey’s HSD检验法;图像由OriginPro 2021软件绘制,并经Adobe Illustrator CS6软件排版组合。
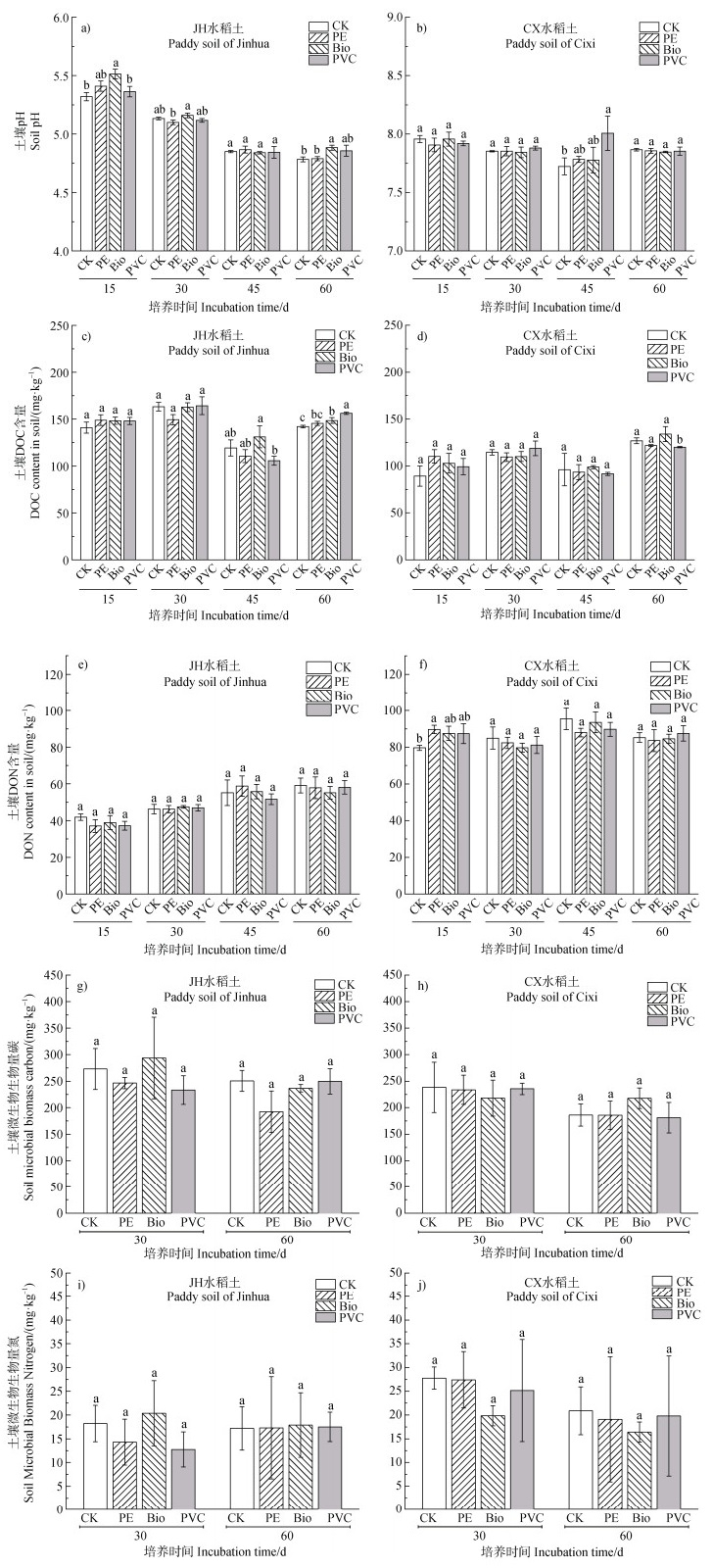
2 结果 2.1 培养期间不同微塑料对土壤基础理化性质的影响微塑料处理对两种水稻土壤pH的影响不同(图 2a,图 2b)。酸性JH水稻土pH整体随时间呈下降趋势,但Bio处理使土壤pH呈增加趋势,培养15 d时Bio处理显著提高pH至5.51(P < 0.05),60 d时相对于CK升高约2.09%;而PE与PVC对JH水稻土pH的影响较小。碱性CX水稻土pH总体稳定(7.73~8.01),仅培养45 d时PVC处理显著升高至8.01(P < 0.05)。表明微塑料对酸性土壤pH的干扰更显著,而对碱性土pH则影响较小。
|
注:CK代表对照处理,PE、Bio和PVC分别代表 05%的PE、Bio和PVC微塑料添加;图中不同小写字母表示在特定处理时间下各微塑料处理间存在显著差异(P < 0.05)。 Note: CK represents the control treatment. PE, Bio, and PVC represent 0.5% addition of PE, Bio, and PVC microplastics, respectively. Different lowercase letters in the figure indicate significant differences among MPs treatments at the same incubation time (P < 0.05). 图 2 不同处理下土壤中基础理化性质、微生物生物量碳氮的动态变化 Fig. 2 Dynamic changes in basic physico-chemical properties, soil microbial biomass carbon (MBC) and microbial biomass nitrogen (MBN) of soil under different treatments |
总体而言,微塑料处理对JH水稻土中DOC含量的影响显著高于CX水稻土(图 2)。在酸性JH水稻土中,各处理下DOC浓度整体在105.7~164.3 mg·kg–1内。在培养初期(15 d和30 d)各处理下DOC浓度无显著性差异(P > 0.05);在45 d时Bio处理下DOC含量最高(131.1 mg·kg–1);在60 d时Bio和PVC处理下DOC浓度为148.5 mg·kg–1和156.3 mg·kg–1,均显著高于CK处理(142.0 mg·kg–1)。土壤DON含量表现为随时间逐渐升高,但不同微塑料处理间无显著性差异(P > 0.05)。在碱性CX水稻土中,DOC含量在整个培养期内波动较小,且处理间差异不明显(P > 0.05),仅在培养60 d时PVC微塑料使DOC含量略有下降(图 2c)。CX水稻土中DON浓度整体水平高于JH水稻土,且PE微塑料在培养15 d时DON浓度显著高于CK处理,但随培养时间增加微塑料对DON含量的影响逐渐减弱,在培养30~60 d时各处理间无显著性差异(P > 0.05)。从图 2g-图 2j可以看出,PE、Bio和PVC三种微塑料对两种水稻土中MBC和MBN均未产生显著性影响;同时,培养时间对上述两个指标的影响亦不显著(P > 0.05)。
2.2 培养期间不同微塑料对土壤DOM紫外光谱参数的影响微塑料处理对土壤DOM紫外光谱特征参数的影响如表 2所示。在酸性JH水稻土中,SUVA254随培养时间显著下降,培养后期(45 d和60 d)降幅最大,约56.5%~67.0%,表明土壤DOM芳香性逐渐减弱。培养30 d时,PE(29.3%)、PLA(28.6%)和PVC(29.9%)处理的SUVA254降幅远高于CK(17.2%),说明微塑料在培养初期加速了DOM中芳香性物质的转化或降解;但随着培养时间延长,各处理间差异逐渐减弱,在培养45~60 d时SUVA254无显著性差异(P > 0.05)。酸性JH水稻土中SUVA260和SUVA280呈类似变化趋势。在培养60 d时,SUVA260降幅为64.6%~67.6%;SUVA280降幅为66.5%~69.2%;但在同一时间点,不同微塑料处理间差异不显著(P > 0.05)。SR则在培养60d时显著升高,CK、PE、Bio和PVC处理较培养15 d分别增加了14.2%、15.7%、23.5%和15.3%,表明土壤DOM分子量明显降低;此外,在培养60 d时,PE、PVC和Bio处理的SR均相对于CK处理呈增加趋势,但仅Bio处理产生了显著性差异(P < 0.05,增幅约8.26%)。
|
|
表 2 不同处理下土壤DOM的紫外光谱特征参数变化 Table 2 UV spectral characteristics of soil DOM under different treatments |
相比之下,碱性CX水稻土中SUVA254、SUVA260和SUVA280整体高于JH水稻土,表明碱性CX水稻土壤DOM芳香性更强。此外,上述SUVA参数随培养时间波动较小(P > 0.05),但SR在培养60 d时显著升高,各处理较培养15 d增长了1.31倍~1.35倍(表 2)。微塑料对碱性CX水稻土DOM紫外特征参数的影响整体较弱,仅在培养15 d时PE处理SUVA254和SUVA260较CK分别下降约20.53%和20.51%(P < 0.05),而Bio和PVC处理下降幅未达显著性水平(P > 0.05)。总体而言,微塑料在酸性JH水稻土中对DOM光谱特征的干扰更明显,Bio处理效应最强;而在碱性CX水稻土中,DOM结构对微塑料扰动响应较弱,表现出更高的稳定性。
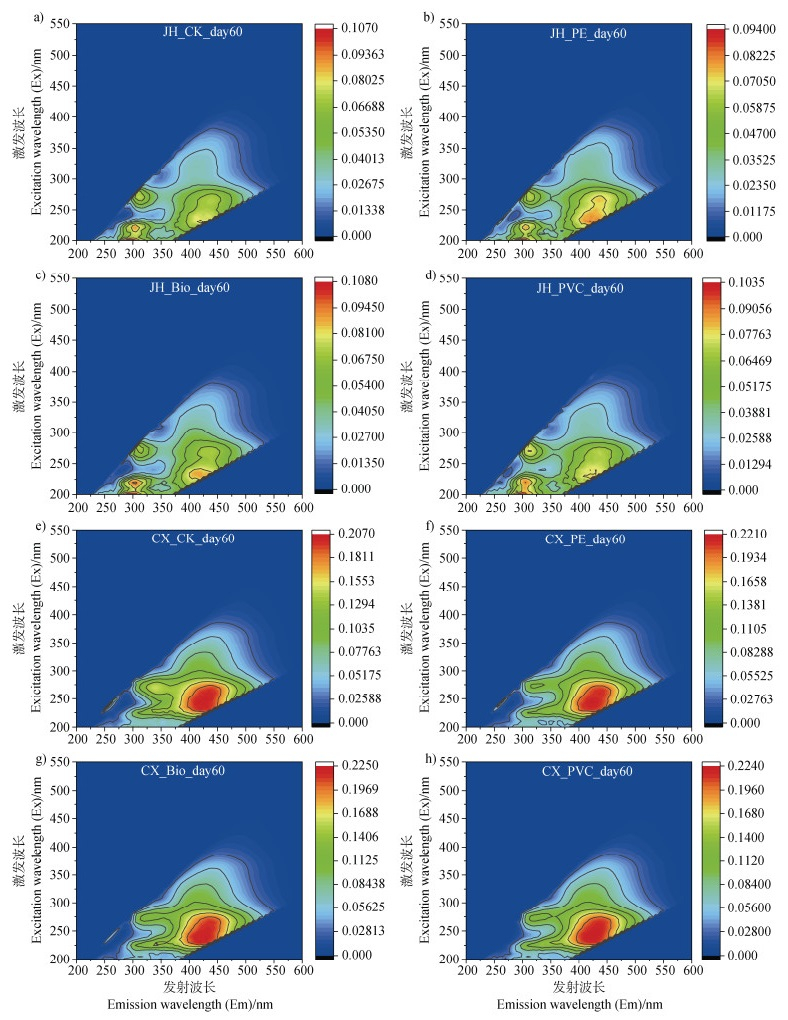
2.3 培养期间不同微塑料对土壤DOM三维荧光光谱光谱及平行因子分析的影响以培养60 d数据为例,各处理土壤DOM的三维荧光等高线谱图如图 3所示。进一步对金华水稻土和慈溪水稻土DOM样品的三维荧光光谱进行平行因子分析,其中,JH水稻土得到2个组分:组分C1(λEx/λEm = 220 nm/335 nm)属于类色氨酸/可溶性微生物副产物(Tryptophan-like/Soluble microbial products),通常与微生物代谢活动或新鲜有机质(如胞外分泌物)相关[23];组分C2(λEx/λEm = 240 nm/430 nm)归类为类腐殖酸组分(Humic-like,HA),对应长波长腐殖化产物,可能来源于植物残体的长期降解或土壤稳定有机质的积累[24];而CX水稻土解析出3个荧光组分:组分C1(λEx/λEm = 235 nm/410 nm)和C2(λEx/λEm = 265 nm/470 nm)属于类腐殖物质[25],C3(λEx/λEm = 225 nm/335 nm)为类色氨酸/蛋白类物质[23]。
|
注:等高线图为三个重复的均值。 Note: The contour spectrum was the mean value of three replicates. 图 3 培养60 d时各处理土壤DOM三维荧光等高线谱图 Fig. 3 Three-dimensional fluorescence contour spectrum of soil DOM in each treatment at 60 days of cultivation |
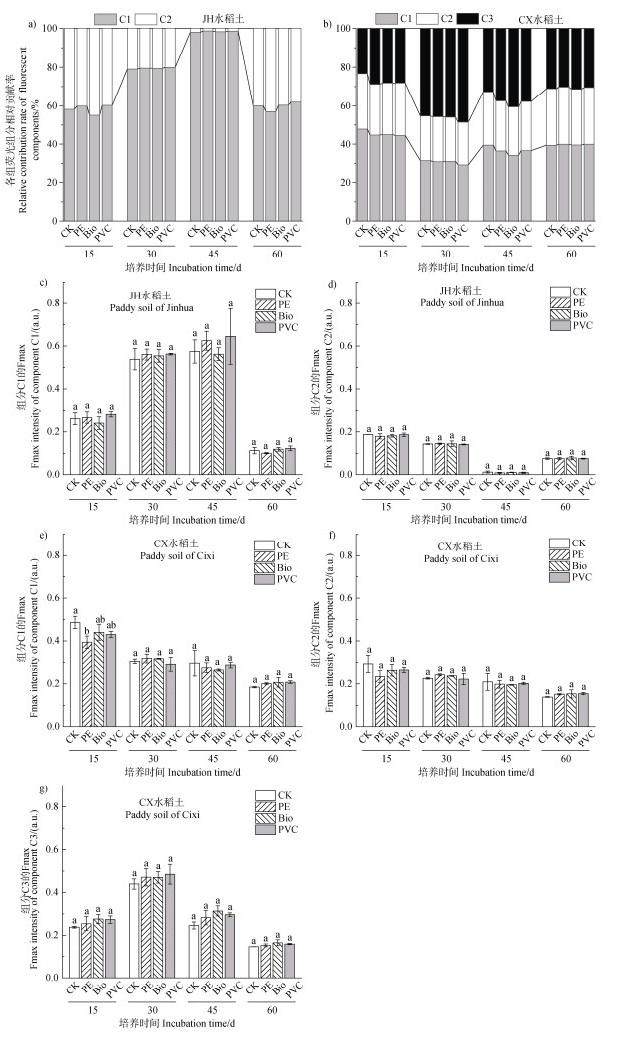
荧光强度贡献率可反映DOM中各个组分的相对含量比例。如图 4所示,在酸性JH水稻土中,组分C1的相对贡献率整体高于C2,说明类色氨酸/可溶性微生物副产物是该土壤DOM的主要荧光成分。各处理间组分相对贡献率无显著性差异(P > 0.05)。组分C1的相对贡献率随培养时间上升,在培养45 d达到最高(约为98%),但在培养60 d时显著下降至57%~62%,其变化趋势与最大荧光强度Fmax一致(图 4c,图 4d)。在碱性CX水稻土中,组分C1和C3的荧光强度相对贡献率和Fmax整体略高于组分C2;组分C1和C2的Fmax值随培养时间的增加而显著下降,而组分C3的Fmax值则表现为“先升高后降低”趋势,并在培养30 d时达到峰值(图 4g)。微塑料对土壤DOM组分荧光强度的影响较小,仅CX水稻土在培养15 d时,PE微塑料使组分C1的Fmax较CK下降约18.9%(图 4e)。
|
注:图中不同小写字母表示在特定处理时间下各微塑料处理间存在显著差异(P < 0.05)。 Note: Different lowercase letters in the figure indicate significant differences among MPs treatments at the same incubation time (P < 0.05). 图 4 不同处理下土壤DOM各组分荧光强度相对贡献率和最大荧光强度Fmax Fig. 4 Relative contribution rate of fluorescent components and maximum fluorescence intensity Fmax of soil DOM under different treatments |
整体上看,Bio微塑料产生的影响相对较高,尤其是在酸性JH水稻土中引起了较为显著的干扰效应。在pH方面,0.5%添加量的Bio处理使土壤pH显著提高(P < 0.05)(图 2a),这可能与Bio微塑料释放出弱碱性物质(如CaCO3)有关。该Bio微塑料由PLA+PBAT共混制成的购物袋冷冻球磨制得,常添加CaCO3以增强韧性、热稳定性并降低成本[26-27],在土壤中可逐步释放Ca2+导致pH升高。我们前期研究也发现PLA+PBAT微塑料(粒径 < 335 μm)可释放2.297 mg·L–1的Ca2+[18]。类似地,不少研究发现也发现PLA和PBAT的存在会使土壤pH升高[28-30]。此外,微塑料还可能通过抑制硝化活性或增强硝酸盐还原活性减少H+释放[29];或通过改变土壤阳离子交换量和土壤水中质子的自由交换进而影响土壤pH[28]。
在DOC方面,Bio微塑料在培养中后期(45 d和60 d)逐渐表现出使JH水稻土DOC浓度增加趋势,且在培养60 d时达到显著水平。类似地,5%和10%的PBAT微塑料可显著提高砖红壤中DOC含量及缩合芳烃类物质、碳水化合物含量[8];1.5%PLA微塑料会显著增加土壤DOC含量,并导致土壤腐殖化增加[31]。已有研究表明生物降解微塑料(如PLA或PBAT)会在微生物或胞外酶的作用下水解、生物降解形成低分子量化合物(如低聚物、二聚体和单体等),显著提高土壤DOM含量[8,32]。在土壤团聚体尺度下,PLA可压缩微生物生态位(如降低Proteobacteria丰度)抑制细菌参与DOM转化过程,转而促进非生物转化,导致小粒径团聚体中DOM的积累和转化[33]。但这些低分子量化合物在后期易被矿化,从而导致DOM浓度下降[32]。本研究中Bio处理虽未显著改变SUVA参数,但60 d时SR显著升高,反映土壤DOM由高分子向低分子转化。与本研究结果类似,Chen等[32]利用ESI FT-ICR-MS技术发现PLA微塑料输入显著减少土壤中DOM分子的数量,且土壤DOM组分多样性(Shannon指数)、分子量(MW)及双键当量(DBE)等指标均低于对照组。本研究中Bio微塑料属于全生物降解塑料,在环境中更容易发生生物降解或水解,生成水溶性低分子量低聚物[34]。Bio的强扰动还可归因于其在土壤中引发的“激发效应”,即外源碳输入引发有机质加速矿化。Sun等[34]指出,源自塑料的碳分子比来自土壤的碳分子更加不稳定,易被微生物利用,更容易提高DOM的不稳定性。Chen等[32]也发现,在营养贫乏的土壤中,MPs-DOM的输入会刺激微生物活性,并增强其对CHONS类化合物的依赖性,进而加速天然有机质(SOM)的矿化。相比之下,传统微塑料如PE和PVC总体扰动效应较弱。本研究中,PE处理对上述指标几乎无显著性影响(P > 0.05),PVC微塑料在JH水稻土中引起DOC升高而在CX水稻土中DOC下降,总体呈现一定的差异性(图 2c,d)。已研究指出,相比于PE和PS微塑料,PVC微塑料对土壤DOM组成的影响更大[35],可能与其含氯结构及氯元素溶出有关,氯元素的溶出可能对微生物产生影响,但在低剂量下效果有限。有研究指出,较高水平的微塑料添加量(28%)能激发土壤酶活性,进而增加DOM溶液中C、N和P的积累;但较低浓度(< 1%~7%)的微塑料添加量对DOM溶液中营养元素物质含量、不稳定有机碳含量及微生物群落结构影响较小[30,33,36]。本研究中微塑料添加量为0.5%,更接近实际农田土壤中暴露水平[37],对土壤微生物生物量碳、氮等指标的扰动能力有限(图 2g-图 2j)。但也有研究指出,微塑料对土壤DOM组成的影响具有一定的滞后性[38],低剂量效应可能需要长期观测验证。
总体而言,微塑料类型在一定程度上会影响土壤理化性质和DOM特征:可降解微塑料(Bio)可通过释放可利用碳源、碱性填料(如CaCO3)等影响土壤DOM;而PE和PVC等传统石油基微塑料影响相对有限。
3.2 土壤理化性质及DOM特性的扰动具有土壤类型依赖性除微塑料聚合物类型外,土壤性质也显著调控微塑料对DOM的影响。本研究中,酸性JH水稻土在pH、SUVA参数及SR等指标上对微塑料与培养时间变化更为敏感,而碱性CX水稻土整体波动较小(图 2、图 4、表 2)。随培养时间延长,酸性JH水稻土中pH和SUVA参数(包括SUVA254、SUVA260和SUVA280)显著下降与SR升高(图 2、表 2),表明随着培养时间增加其DOM芳香性减弱、分子量降低、结构趋于简单;而碱性CX水稻土壤中相关指标的变幅较小,表明其DOM结构较为稳定(图 2、表 2)。这表明DOM结构在酸性JH水稻土中更容易受到外界的扰动。
光谱斜率SR在整个培养内JH水稻土均显著高于CX水稻土(表 2),进一步表明JH水稻土DOM以分子量较小、结构更简单的小分子代谢物为主,结构稳定性较差,更容易受到微塑料的扰动和降解作用的影响。平行因子分析显示,酸性JH水稻土DOM以类色氨酸/可溶性微生物代谢产物(C1)为主。研究表明蛋白质样成分与土壤发色溶解性有机物的生物有效性和微生物活性密切相关[39],更容易受到环境变化的扰动;相比之下,碱性CX水稻土以类腐殖物质(C1和C2)为主,相对稳定。土壤质地也是影响DOM结构的重要因素。根据国际质地分类系统,CX水稻土为粉砂质黏壤土,黏粒含量为31.5%,且粉粒比例高达51.1%,整体质地细腻,有利于对DOM的保留能力更强,吸附稳定性更高[32];而JH水稻土属于黏壤土,黏粒含量为24.5%,砂粒含量为28.4%,空隙较大,结构相对于CX水稻土更为松散,DOM更易溶出或迁移,受外源扰动时更容易发生组分重构。Chen等[32]也发现相比于松软土,铁铝土和淋溶土具有较高的粉粒和黏粒含量,增加了对PLA微塑料衍生物的吸附和保护。此外,Feng等[39]也发现土壤利用类型也会显著影响DOM的组成,林地和农田土壤中DOC含量、自生源指数(BIX)等参数对PE微塑料的响应存在相反趋势。
综上所述,酸性、质地松散的JH水稻土对微塑料扰动及培养时间变化更为敏感,其DOM更容易发生分子量下降、芳香性降低等变化;而碱性、质地细腻的CX水稻土则表现出更强的DOM稳定性。
4 结论微塑料对DOM的干扰效应具有显著的聚合物类型差异,并依赖于土壤pH、质地及DOM组成类型等性质。生物可降解微塑料(Bio)在酸性JH水稻土中显著影响提高pH、DOC及SR,在培养初期显著降低SUVA254值,表明其促进芳香类化合物的转化或降解,且效应随时间逐渐减弱;而传统石油基微塑料(PE与PVC)整体扰动作用较弱。酸性、质地松散的JH水稻土以类色氨酸组分为主,响应更为敏感,在培养过程中DOM芳香性降低、分子量减小、结构趋于简单;相较而言,碱性、质地细腻的CX水稻土以类腐殖物质为主,DOM结构更为稳定性,对微塑料扰动展现出较强的抗扰动能力。本研究揭示了聚合物类型与土壤性质共同调控微塑料扰动DOM的机制,为农田微塑料污染风险评估与DOM调控提供理论依据。
| [1] |
Nizzetto L, Futter M, Langaas S. Are agricultural soils dumps for microplastics of urban origin?[J]. Environmental Science & Technology, 2016, 50(20): 10777-10779.
(  0) 0) |
| [2] |
Yang J, Li L Z, Zhou Q, et al. Microplastics contamination of soil environment: Sources, processes and risks (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 281-298. DOI:10.11766/trxb202006090286 [杨杰, 李连祯, 周倩, 等. 土壤环境中微塑料污染: 来源、过程及风险[J]. 土壤学报, 2021, 58(2): 281-298.]
(  0) 0) |
| [3] |
de Souza Machado A A, Kloas W, Zarfl C, et al. Microplastics as an emerging threat to terrestrial ecosystems[J]. Global Change Biology, 2018, 24(4): 1405-1416. DOI:10.1111/gcb.14020
(  0) 0) |
| [4] |
Qi Y L, Ossowicki A, Yang X M, et al. Effects of plastic mulch film residues on wheat rhizosphere and soil properties[J]. Journal of Hazardous Materials, 2020, 387: 121711. DOI:10.1016/j.jhazmat.2019.121711
(  0) 0) |
| [5] |
Gmach M R, Cherubin M R, Kaiser K, et al. Processes that influence dissolved organic matter in the soil: A review[J]. Scientia Agricola, 2020, 77(3): e20180164. DOI:10.1590/1678-992x-2018-0164
(  0) 0) |
| [6] |
Xiao J N, Zhang Z M. Sources, occurrence characteristics and potential risks of microplastics in farmland soils: A review (In Chinese)[J]. China Plastics, 2024, 38(9): 137-144. [肖进男, 张珍明. 农田土壤中微塑料的来源、赋存特征及其潜在风险[J]. 中国塑料, 2024, 38(9): 137-144.]
(  0) 0) |
| [7] |
Yang J, Tu C, Yuan X Z, et al. Environmental processes and ecological effects of micro-and nano-plastics in soil-plant systems (In Chinese)[J]. Progress in Chemistry, 2025, 37(1): 89-102. [杨杰, 涂晨, 袁宪正, 等. 土壤-植物系统中微/纳塑料的环境过程和生态效应[J]. 化学进展, 2025, 37(1): 89-102.]
(  0) 0) |
| [8] |
Chen M, Zhao X W, Wu D M, et al. Addition of biodegradable microplastics alters the quantity and chemodiversity of dissolved organic matter in latosol[J]. Science of the Total Environment, 2022, 816: 151960. DOI:10.1016/j.scitotenv.2021.151960
(  0) 0) |
| [9] |
Guo Z Q, Li P, Yang X M, et al. Effects of microplastics on the transport of soil dissolved organic matter in the Loess Plateau of China[J]. Environmental Science & Technology, 2023, 57(48): 20138-20147.
(  0) 0) |
| [10] |
Liu X G, Fang L P, Gardea-Torresdey J L, et al. Microplastic-derived dissolved organic matter: Generation, characterization, and environmental behaviors[J]. Science of the Total Environment, 2024, 948: 174811. DOI:10.1016/j.scitotenv.2024.174811
(  0) 0) |
| [11] |
Choi N E, Lee Y K, Oh H, et al. Photo-induced leaching behaviors and biodegradability of dissolved organic matter from microplastics and terrestrial-sourced particles[J]. Chemosphere, 2024, 355: 141826. DOI:10.1016/j.chemosphere.2024.141826
(  0) 0) |
| [12] |
Liu S S, Qiu Y, He Z Q, et al. Microplastic-derived dissolved organic matter and its biogeochemical behaviors in aquatic environments: A review[J]. Critical Reviews in Environmental Science and Technology, 2024, 54(11): 865-882. DOI:10.1080/10643389.2024.2303294
(  0) 0) |
| [13] |
Shi J, Wang X, Wang J. Soil carbon cycling mediated by microplastics: Formation, mineralization, and sequestration (In Chinese)[J]. Scientia Sinica: Technologica, 2024, 54(10): 1854-1867. [石佳, 王祥, 汪杰. 微塑料介导的土壤碳循环: 微塑料对土壤有机碳的形成、矿化和稳定过程的影响[J]. 中国科学: 技术科学, 2024, 54(10): 1854-1867.]
(  0) 0) |
| [14] |
Ding Y, Shi Z Q, Ye Q T, et al. Chemodiversity of soil dissolved organic matter[J]. Environmental Science & Technology, 2020, 54(10): 6174-6184.
(  0) 0) |
| [15] |
Li X M, Sun G X, Chen S C, et al. Molecular chemodiversity of dissolved organic matter in paddy soils[J]. Environmental Science & Technology, 2018, 52(3): 963-971.
(  0) 0) |
| [16] |
Lu R K
. Analytical methods for soil and agrochemistry (In Chinese). Beijing: China Agricultural Science and Technology Press, 2000. [鲁如坤
. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000.]
(  0) 0) |
| [17] |
Huang S Y, Guo T, Feng Z, et al. Polyethylene and polyvinyl chloride microplastics promote soil nitrification and alter the composition of key nitrogen functional bacterial groups[J]. Journal of Hazardous Materials, 2023, 453: 131391. DOI:10.1016/j.jhazmat.2023.131391
(  0) 0) |
| [18] |
He M, Feng Z, Xu Y Y, et al. Macro- and microplastic leachates show a slightly toxic effect on seed germination of cotton[J]. Chemosphere, 2023, 335: 139081. DOI:10.1016/j.chemosphere.2023.139081
(  0) 0) |
| [19] |
Luo H W, Xiang Y H, He D Q, et al. Leaching behavior of fluorescent additives from microplastics and the toxicity of leachate to Chlorella vulgaris[J]. Science of the Total Environment, 2019, 678: 1-9.
(  0) 0) |
| [20] |
Wang L Y, Wu F C, Zhang R Y, et al. Characterization of dissolved organic matter fractions from Lake Hongfeng, Southwestern China Plateau[J]. Journal of Environmental Sciences, 2009, 21(5): 581-588. DOI:10.1016/S1001-0742(08)62311-6
(  0) 0) |
| [21] |
Lee Y K, Murphy K R, Hur J. Fluorescence signatures of dissolved organic matter leached from microplastics: Polymers and additives[J]. Environmental Science & Technology, 2020, 54(19): 11905-11914.
(  0) 0) |
| [22] |
Weishaar J L, Aiken G R, Bergamaschi B A, et al. Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon[J]. Environmental Science & Technology, 2003, 37(20): 4702-4708.
(  0) 0) |
| [23] |
Wang J, Jia M H, Zhang L, et al. Biodegradable microplastics pose greater risks than conventional microplastics to soil properties, microbial community and plant growth, especially under flooded conditions[J]. Science of the Total Environment, 2024, 931: 172949. DOI:10.1016/j.scitotenv.2024.172949
(  0) 0) |
| [24] |
Jia F X, Yang Q, Liu X H, et al. Stratification of extracellular polymeric substances (EPS) for aggregated anammox microorganisms[J]. Environmental Science & Technology, 2017, 51(6): 3260-3268.
(  0) 0) |
| [25] |
Du Y X, Zhang Q Y, Liu Z W, et al. Composition of dissolved organic matter controls interactions with La and Al ions: Implications for phosphorus immobilization in Eutrophic Lakes[J]. Environmental Pollution, 2019, 248: 36-47. DOI:10.1016/j.envpol.2019.02.002
(  0) 0) |
| [26] |
Thenepalli T, Jun A Y, Han C, et al. A strategy of precipitated calcium carbonate (CaCO3) fillers for enhancing the mechanical properties of polypropylene polymers[J]. Korean Journal of Chemical Engineering, 2015, 32(6): 1009-1022. DOI:10.1007/s11814-015-0057-3
(  0) 0) |
| [27] |
Luo S J, Pan S N. Numerical study on the effect of CaCO3 ratio on the mechanical properties of CaCO3/PVC composites[J]. Journal of Physics: Conference Series, 2021, 1820(1): 012140. DOI:10.1088/1742-6596/1820/1/012140
(  0) 0) |
| [28] |
Wang F Y, Wang Q L, Adams C A, et al. Effects of microplastics on soil properties: Current knowledge and future perspectives[J]. Journal of Hazardous Materials, 2022, 424: 127531. DOI:10.1016/j.jhazmat.2021.127531
(  0) 0) |
| [29] |
Wang C L, Bian J J, Min W H, et al. Effects of two PBAT/PLA biodegradable mulch film fragments on soil dissolved organic carbon and nitrogen and their phytotoxicity (In Chinese)[J]. Asian Journal of Ecotoxicology, 2022, 17(5): 465-474. [王春丽, 卞京军, 闵文豪, 等. 2种PBAT/PLA生物降解地膜碎片对土壤溶解性有机碳氮的影响及其植物毒性[J]. 生态毒理学报, 2022, 17(5): 465-474.]
(  0) 0) |
| [30] |
Zhou A Y, Ji Q S, Kong X C, et al. Response of soil property and microbial community to biodegradable microplastics, conventional microplastics and straw residue[J]. Applied Soil Ecology, 2024, 196: 105302. DOI:10.1016/j.apsoil.2024.105302
(  0) 0) |
| [31] |
Qiu X R, Ma S R, Pan J R, et al. Microbial metabolism influences microplastic perturbation of dissolved organic matter in agricultural soils[J]. The ISME Journal, 2024, 18(1): wrad017. DOI:10.1093/ismejo/wrad017
(  0) 0) |
| [32] |
Chen L Y, Huang H K, Han L F, et al. Effects of polylactic acid microplastics on dissolved organic matter across soil types: Insights into molecular composition[J]. Journal of Hazardous Materials, 2025, 488: 137356. DOI:10.1016/j.jhazmat.2025.137356
(  0) 0) |
| [33] |
Qiu X R, Ma S R, Liu Z Y, et al. Microplastics influence dissolved organic matter transformation mediated by microbiomes in soil aggregates[J]. Environmental Science & Technology, 2025, 59(26): 13385-13397.
(  0) 0) |
| [34] |
Sun Y Z, Li X F, Li X M, et al. Deciphering the fingerprint of dissolved organic matter in the soil amended with biodegradable and conventional microplastics based on optical and molecular signatures[J]. Environmental Science & Technology, 2022, 56(22): 15746-15759.
(  0) 0) |
| [35] |
Yu H, Xi B D, Shi L L, et al. Chemodiversity of soil dissolved organic matter affected by contrasting microplastics from different types of polymers[J]. Frontiers of Environmental Science & Engineering, 2023, 17(12): 153.
(  0) 0) |
| [36] |
Liu H F, Yang X M, Liu G B, et al. Response of soil dissolved organic matter to microplastic addition in Chinese loess soil[J]. Chemosphere, 2017, 185: 907-917. DOI:10.1016/j.chemosphere.2017.07.064
(  0) 0) |
| [37] |
Fuller S, Gautam A. A procedure for measuring microplastics using pressurized fluid extraction[J]. Environmental Science & Technology, 2016, 50(11): 5774-5780.
(  0) 0) |
| [38] |
Li R F, Xi B D, Tan W B, et al. Spatiotemporal heterogeneous effects of microplastics input on soil dissolved organic matter (DOM) under field conditions[J]. Science of the Total Environment, 2022, 847: 157605. DOI:10.1016/j.scitotenv.2022.157605
(  0) 0) |
| [39] |
Feng Z W, Zhu N Y, Wu H Z, et al. Microplastic coupled with soil dissolved organic matter mediated changes in the soil chemical and microbial characteristics[J]. Chemosphere, 2024, 359: 142361. DOI:10.1016/j.chemosphere.2024.142361
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


