2. 安徽省生态环境科学研究院, 合肥 230061;
3. 土壤与农业可持续发展全国重点实验室(中国科学院南京土壤研究所), 南京 211135;
4. 精密大地测量与定位全国重点实验室, 中国科学技术大学地球和空间科学学院, 合肥 230026
2. Anhui Academy of Ecological and Environmental Sciences, Hefei 230061, China;
3. State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 211135, China;
4. State Key Laboratory of Precision Geodesy, School of Earth and Space Sciences, University of Science and Technology of China, Hefei 230026, China
生物塑料通过减少化石资源依赖、降低碳足迹和提供堆肥回收途径,展现了显著的可持续潜力[1]。作为传统石化塑料的替代方案,生物塑料已形成以纤维素基、淀粉基、聚酯类(如PLA)等为代表的技术体系,通过微生物发酵、化学合成等工艺实现规模化生产,并渗透至包装、农业地膜、医疗器械等核心领域[2-3],也因其可再生原料来源和可降解特性被广泛视为解决白色污染的关键路径。
然而,需要注意的是,生物塑料不等于生物可降解,其环境风险与传统塑料类似[4]。此外,生物塑料由于本身结构的特性,如淀粉基塑料含大量易断裂的糖苷键,在环境中更容易受到风化作用和紫外线的影响,从而释放有害物质。现有研究多聚焦于材料的表观降解性能,对其在真实环境中的次生污染风险关注不足[5]。生物塑料在环境条件(如光照、水分)作用下可能加速崩解,释放微塑料(MPs)及添加剂(如邻苯二甲酸酯类,PAEs),并通过溶解性有机质(DOM)的协同作用加剧生态毒性[6-7]。
目前,针对生物塑料薄膜降解行为的研究仍然存在空白:其一,光降解过程中材料物理化学性质的动态变化规律尚未系统阐明;其二,次生污染物的生成机制及其环境归趋缺乏定量评估。因此,本文通过模拟太阳光加速降解实验,研究目前主流生物塑料,结合多尺度表征手段,揭示其光降解过程中MPs的生成规律、DOM组分演化及PAEs释放特征,旨在解析生物塑料薄膜“快速分解”与“潜在污染”的双重属性,为完善其环境风险评估框架与标准化管控提供理论依据。
1 材料与方法 1.1 供试材料本研究聚乳酸(PLA)、纤维素基(C)塑料薄膜购买自美国Natural Works公司,淀粉基(S)以及聚乙烯(PE)塑料薄膜购买自金华市威固包装有限公司。
1.2 样品制备将聚乳酸(PLA)、纤维素基(C)、淀粉基(S)以及聚乙烯(PE)塑料薄膜切割成长5 cm、宽2 cm的矩形片,用超纯水反复清洗3遍,再放入超声波清洗30 min,去除塑料薄膜片表面附着的杂质和灰尘,随后将每片薄膜用干净的镊子取出,均匀平铺于干净的培养皿中。每份培养皿中放入三个薄膜条作为平行样,作为对照使用。
使用紫外线灯模拟阳光紫外线,并将其安装在洁净的工作台上,每种样品放置6份,均固定在紫外线加速老化工作台上,用40 W·m–2的UVA-340(紫外光)以及黑暗条件(用锡箔纸包裹)下对生物塑料进行试验,测试不同降解时间(5 d、15 d、30 d)失重率及理化性质变化。在预先设定的陈化时间之后,移除该膜,用去离子水洗涤,再置于真空烘箱室中在室温下进行48 h的干燥,然后将该样本移除以作测试。
1.3 样品表征本研究采用失重率、X射线衍射(XRD)、X射线光电子能谱(XPS)、扫描电镜(SEM)对塑料薄膜紫外光降解前后进行表征,分析塑料薄膜表观形态以及官能团变化。
1.4 微塑料的释放将装有样品的培养皿加入5 mL超纯水,按每次5 mL超纯水进行润洗,共润洗5次,使用过滤装置,通过玻璃纤维膜(孔径0.22 μm)进行过滤,将滤液转移到总有机碳(TOC)测量瓶中,测量滤膜与滤液中的TOC。
利用Sun等[8]提出的膜过滤和总有机碳测定(MF-TOCD)方法,量化微塑料。使用无碳玻璃纤维膜过滤器(孔径0.22 μm)进行膜过滤,将降解产物分为两组:大于0.22 μm的(MPs)和小于0.22 μm的(包括纳米塑料和可溶性分子)。由于玻璃纤维膜的孔径为0.22 μm,所有纳米塑料和可溶性分子均通过过滤器并进入滤液。而膜表面则残留有粒径≥0.22 μm的MPs。分别测量滤膜和滤液中的TOC作为C1和C2。用TOC分析仪三次测定的塑料原料的有机碳比率用R(聚乳酸:80.25%,纤维素基:96.97%,淀粉基:73.79%,聚乙烯:85.57%)表示[9]。
此外,通过图像法分析塑料薄膜释放的微塑料情况,选取20 μm尺度的扫描电镜照片,利用ImageJ软件进行计数,分析微塑料释放情况。
1.5 添加剂及金属元素释放实验(1)生物塑料元素含量测定采用土壤中金属元素含量测定方法,电感耦合等离子体质谱法,通微波消解后进行上机测定。
(2)原塑料中邻苯二甲酸酯(PAEs)的检测:在液氮中冷冻30 s后,将其切成小块,经过2 mm筛(事先用丙酮、甲苯、正己烷清洗)。所有样本均用铝箔纸包好,然后放入干燥机中进行分析。在50 mL离心管中,加入10 mL正己烷,超声波20 min,筛分10 min,再以400 r·min–1离心10 min,将上清液转入琥珀色玻璃罐中。用正己烷5 mL连续提取3次。将萃取液(25 mL)混合后,取出1 mL上清液(过滤机,0.20 µm,13 mm)置于2 mL琥珀色玻璃瓶内,采用气相色谱-质谱联用仪(GC-MS)测定其含量。
(3)浸出实验:在玻璃培养皿中加入3片按前述方法得到的长5cm、宽2cm的塑料薄膜长条,加入20 mL去离子水作为浸出液使薄膜完全浸入其中,密封后置于紫外线老化台上。间隔一定时间(30 d)取样,用0.45 μm玻璃纤维膜过滤后在4℃条件下避光保存。
(4)提取液中含有邻苯二甲酸基团的含量测定:过滤后的提取液进入50 mL液体漏斗中,用二氯甲烷10 mL提取3次。将提取物混合后,用旋转蒸发器将其浓缩至2 mL以下,然后向烧瓶内添加7 mL二氯甲烷,将其清洗3次,然后用一只小漏斗将其输送至氮气吹瓶中,使之接近干燥。再用正己烷再次溶解1 mL试样,用过滤器(0.20 mL,13 mm)滤入2 mL琥珀色玻璃瓶,于–18℃贮存。建立了邻苯二甲酸酯在气相色谱-质谱法中的分析方法。
1.6 数据处理使用Microsoft Excel 2019、Origin2021进行数据处理、统计分析和绘图。
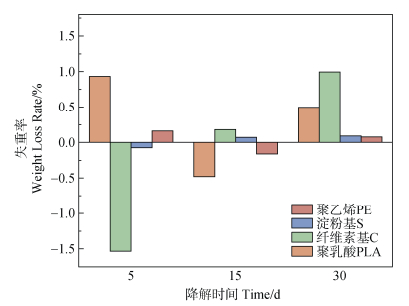
2 结果与讨论 2.1 失重率基于图 1所示质量变化数据,结合材料吸湿特性和降解动力学分析可知:在光降解初期(0~15 d),所有塑料薄膜的质量变化率均未超过±1.5%,其中纤维素基塑料甚至出现–0.8%~–1.5%的负质量损失,这与其表面特性和降解阶段密切相关。
|
图 1 四种塑料薄膜光降解不同时间后的失重率 Fig. 1 Weight loss rates of four types of plastic films after photodegradation at different times |
具体机制可能涉及:1)材料表面吸湿膨胀,特别是淀粉基塑料(吸水性>3%)和纤维素基材料(含水率2%~4%)在紫外辐照过程中因表面氧化产生羟基等亲水基团,引发水分吸附导致表观质量增加,具体反应方程式为(C6H10O5)· + O2 + H2O+hv →(C6H10O5)n–1+ C6H10O7(葡萄糖醛酸)+ 2·OH(自由基)[10];2)光氧化产生的低分子量碎片(如PLA的乳酸低聚物)仍附着于材料表面,尚未达到溶解脱落阈值[11];3)实验环境中大气颗粒物在材料粗糙化表面的物理吸附。当降解进入30天阶段,质量损失率转为正值(生物塑料0.2%~1.2%,PE < 0.2),这与材料本体发生实质性破坏相关。淀粉基材料中多糖链断裂生成葡萄糖单元溶解,RCOOR’→RCOO’+R’,该过程产生羧酸端基(如乙酸),进一步催化水解,而PE仅通过Norrish Ⅱ型断裂产生不溶性烷烃碎片(碳链长度C20-C50)[12],首先PE氧化生成的酮羰基(如R-CO-R')吸收紫外光(hv),经n→π跃迁形成三线态激发态,其次激发态羰基氧夺取γ-碳上的氢,形成1,4-双自由基中间体,最终1,4-双自由基经β-碳断裂(即α与β碳间键断裂),形成烯烃以及烯醇同时生成烷烃碎片[13]。该现象验证了生物塑料的“自催化降解”特性:其主链中的酯基(键能326 kJ·mol–1)和糖苷键(键能268 kJ·mol–1)在光-热协同作用下优先断裂,相较于PE的C-C键(键能345 kJ/mol)具有更低的断裂能垒[14]。
2.2 表观形态变化在对聚乳酸(PLA)、纤维素基(C)、淀粉基(S)以及聚乙烯(PE)塑料薄膜进行15 d、30 d的UV处理后,用SEM对其表面进行了观察(图 2)。四种塑料的扫描电镜图在初始状态下均是光滑的。随着降解的进行,紫外光提供能量可引起聚合物主链的断裂,在15 d时出现较为细小的孔洞,并有少许皱褶产生。在30 d左右,空洞的形成更加明显,并且表面更加的粗糙,紫外线会使原有的缺陷更加严重,从而使得空洞更加频繁地出现。

|
图 2 四种塑料薄膜光降解不同时间后的扫描电镜图 Fig. 2 Scanning Electron Microscope (SEM) images of four types of bioplastic films after different durations of photo-degradation |
但总体而言,生物塑料降解到达30 d时,均未出现较为明显的裂隙,可能是由于降解时间不足的原因。此外,可以发现相较于聚乳酸、纤维素基以及淀粉基而言,聚乙烯塑料表面形态的变化最不明显。相反,淀粉基塑料可能由于其本身材料的缺陷,生产过程中不够紧密,可以发现经过30 d的紫外线照射后,表面出现密集的碎片产生。
值得注意的是,生物塑料与聚乙烯呈现显著差异:聚乳酸和纤维素基塑料在30 d时仍保持相对平滑的结构,未观察到宏观裂隙(裂隙宽度 < 1 μm),可能与其半结晶结构中非晶区的优先降解特性相关;而淀粉基塑料由于加工过程中分子链缠结度较低(自由体积分数 > 0.15),在30天UV暴露后表面产生密集碎片化现象(碎片尺寸5~20 μm),这与淀粉颗粒与基质界面处的应力集中和光氧化产物的积累直接相关。相比之下,聚乙烯薄膜的表面形貌变化最微弱,仅检测到局部微裂纹,这归因于其全碳链结构的化学惰性以及缺乏光敏基团[15]。总体而言,紫外线对生物塑料的降解有着较明显的作用,较显著地改变了塑料的表面形态。
2.3 官能团变化在光降解时,会有新含氧基团被导入,所以可以通过XPS分析的C/O比率来判定不同条件下可生物塑料薄膜的老化状况。随着C/O的降低,薄膜中的氧气含量增加。为此,本实验将利用XPS等手段对其进行探测与分析。
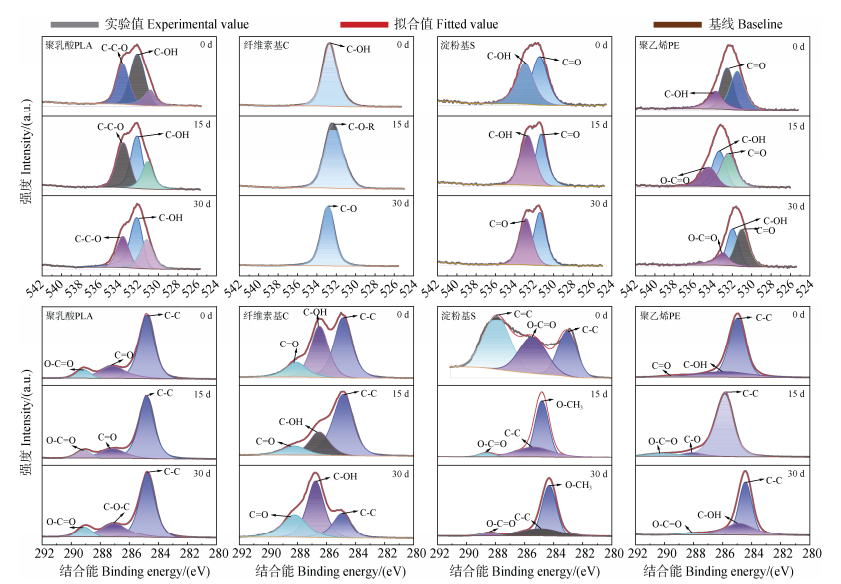
塑料的光降解通常伴随着光氧化过程,导致化学键的变化。因此,为评估紫外线对生物塑料光降解的影响,本研究采用X射线光电子能谱(XPS)分析了化学键的演变(图 3)。紫外线的存在使前后生物塑料的XPS谱图呈现差异。通过对聚乳酸、纤维素基、淀粉基、聚乙烯等材料的界面结合、化学形态等参数的测定,对其进行校正与拟合,得到的数据如图 3所示。将PLA初始图谱和光降解后谱图进行比较,可见在降解过程中,有新的C=O基团加入,这意味着C=O的产生很有可能是由于酯键的断裂所致,这也说明了紫外光对PLA的降解作用[16];对于淀粉基塑料O-C=O键在紫外线作用下发生断裂,O-CH3、C-O是在分子断裂之后生成的,而自由基则是与氧气结合而生成的[17]。同时,在C-OH上C= C断裂,在C-OH上的束缚能从532.3 eV增加至532.9 eV,说明在C-OH上存在着得失电子,O1s光谱进一步证实了这一现象[18]。
|
图 3 四种塑料薄膜光降解不同时间后的XPS拟合图(上方为O1s,下方为C1s) Fig. 3 XPS spectra of four types of plastic films after photodegradation at different times (upper: O1s, lower: C1s.) |
纤维素基塑料在光降解前后官能团没有明显变化,O1s峰的位置由532.6 eV转移至532.3 eV,表明C-OH断裂形成C-O-R以及C-O,说明纤维素基塑料在紫外线下发生了降解。聚乙烯塑料,经紫外线降解后,C-OH断裂形成C-O-R,表明紫外光照射会导致PE进行断链反应。此外,从531.5 eV到531.3 eV的C=O键改变,电子传递过程揭示了在光降解过程中,分子链的断裂和新的链的形成[19]。上述结果表明,在光照条件下,生物塑料均会对其产生老化效应,此外石油基塑料也发生了明显的变化。
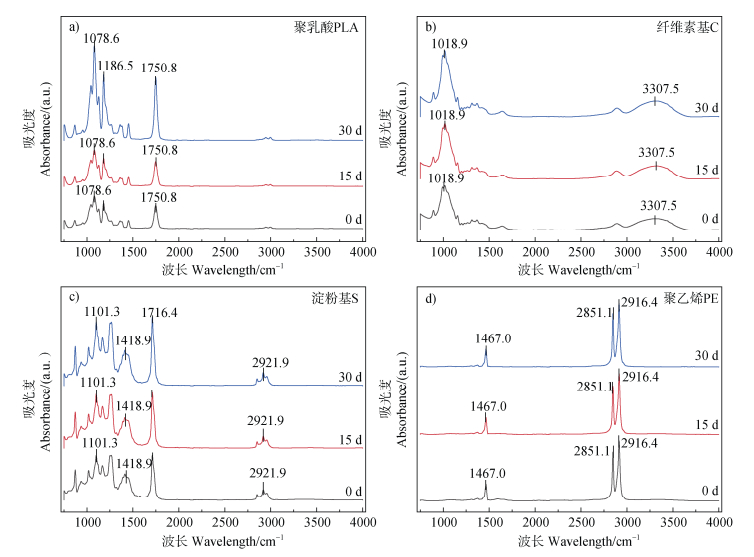
通过傅里叶红外光谱技术(FTIR)研究了生物塑料在光照条件下的降解特性(图 4)。图 4a中纤维素基塑料中在1018.9 cm–1处为C-O键伸缩振动,C-O峰强度随光降解时间延长而增大的现象,主要源于光化学反应引发的有机物氧化与结构重组[20]。当材料暴露于光照时,高能光子或光生自由基会优先攻击分子中的不饱和键(如C=O、C=C)或弱键位点(如C-H),导致羰基(C=O)断裂或脱羧,转化为羧酸(-COOH)、醚(C-O-C)或醇(C-OH)等含C-O键的产物。图 4b中淀粉基塑料1716.4 cm–1处酯键中C=O的特征吸收峰变强,在1716.4 cm–1处的峰面积变大,原因是降解过程中产生了醛、酮、羧酸等混合物。
|
图 4 四种塑料薄膜光降解不同时间后的FTIR图 Fig. 4 FTIR spectra of four types of plastic films after photodegradation at different times |
图 4c中PLA 1750 cm–1处羰基(C=O)峰面积的持续增大通常表明材料发生了显著的光氧化反应。紫外光导致大分子链断裂如碳-氢键或碳-碳键断裂,产生烃基自由基(R•),再与氧作用生成过氧自由基(ROO•)和过氧化氢(ROOH)[21]。这些中间体进一步分解为稳定的羰基化合物(如酮、羧酸或酯类),导致C=O基团含量增加。此外,若材料本身含有酯基或酸酐结构,光降解可能通过水解或氧化产生新的羰基片段(如小分子羧酸),而共轭效应或环状结构的形成(如α,β-不饱和酮或张力环酮)也可能使羰基振动峰向1750 cm–1偏移并增强信号。对于图 4d中PE而言,2916.4 cm–1处C-H(甲基/亚甲基)伸缩振动峰面积的增大可能源于光化学反应诱导的链断裂与结构重组。当高分子材料(如聚酯、聚烯烃)暴露于光照时,紫外光子或光生自由基(如·OH)优先攻击主链中的C-C键或弱C-H键,导致长链断裂并生成短链烷烃片段(如-CH2-、-CH3末端),这些短链的自由度增加会增强C-H振动响应,这些均说明生物塑料在光照的作用下,发生了老化[22]。
生物塑料表面的亲水基团(如羟基、羧基)吸水后,在紫外光激发下引发电子跃迁,促使水分子或基团自身发生化学键均裂(如O-H、C-H键断裂),生成羟基自由基(·OH)等活性氧物种(ROS)。这些自由基通过链式反应(如·OH氧化H2O2产生超氧自由基)加剧材料老化:一方面氧化表面官能团(FTIR/XPS检测到羰基/羟基增加),导致微裂纹扩展和脆化(SEM显示粗糙度提升);另一方面驱动次生污染物的释放与转化,如增塑剂被氧化为醌类毒性产物,或与共存污染物(多环芳烃、重金属)相互作用生成卤代副产物等。该过程受基团敏感性(羟基/羧基>氨基)、水分形态(结合水塑化效应)及环境介质(离子、光催化剂)共同调控,需通过可控亲水改性与抗氧化策略平衡材料的生物降解性与环境风险。
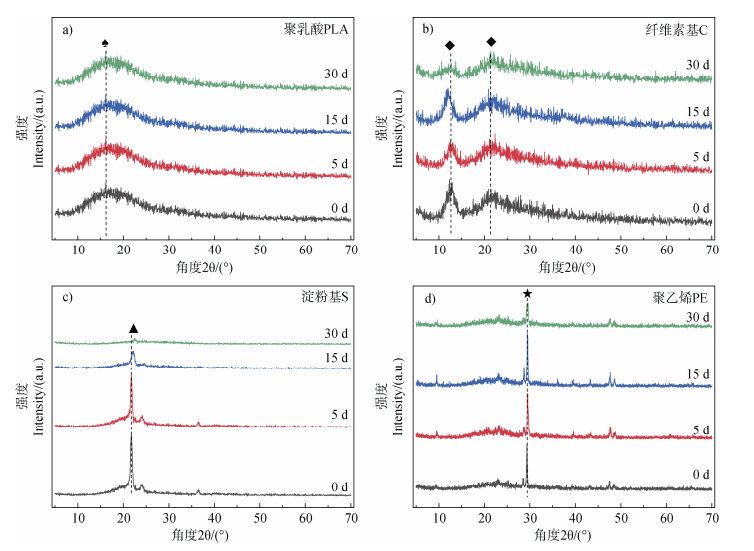
2.4 结晶度变化为了比较生物塑料处理前后结晶度的变化(图 5),对各实验组在0 d、5 d、15 d、30 d采集的样品进行了XRD分析,比较不同试剂处理前后薄膜结晶度变化,并分析可能的原因。通过聚乳酸、纤维素基、淀粉基和聚乙烯塑料的XRD分析,研究不同光组合条件下材料自身性能的变化规律。
|
图 5 四种塑料薄膜光降解不同时间后的XRD图 Fig. 5 XRD patterns of four types of plastic films after photodegradation at different times |
由图 5可知,在光降解前后,生物塑料的特征绕射峰以15°~30°为主,且有更多细小且尖锐的晶体相绕射峰出现。从PLA的结晶性可知,PLA分子链多集中在18°左右,这是聚乳酸的常见峰值,衍射峰分布不均一,说明PLA为半结晶型高分子,其分子链中含有CH3手性碳,导致其主链活性下降60%。纤维素基塑料,可以发现结晶度也有较明显的下降。对于聚乙烯塑料,在20°~23°之间出现明显的特征峰,且结晶度明显下降。由以上表征可以发现,生物塑料薄膜均发生了明显的降解过程。
2.5 微塑料的形成由扫描电镜结果可知,聚乳酸、纤维素基以及聚乙烯在降解至30 d时表面尚未出现大量碎料碎片,因此仅对淀粉基塑料的碎片产生情况进行分析。可以发现,淀粉基塑料的大多数颗粒均小于10 μm,利用ImageJ软件分析淀粉基塑料光降解后微塑料释放情况。
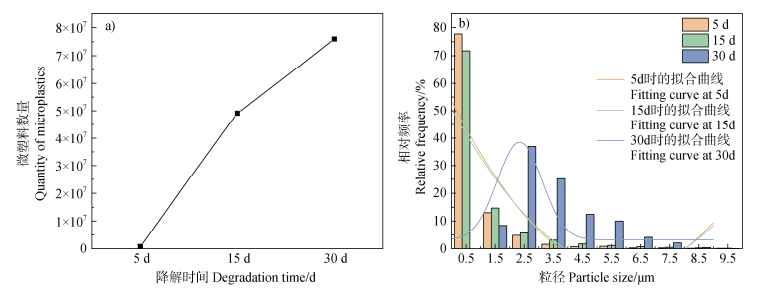
图 6为淀粉基塑料光降解不同时间后的微塑料释放数量与粒径分布。可以发现在紫外光照射下,0~5 μm内的粒子所占比例为87%,而在5~10 μm处仅占一小部分。目前,对微塑料进行定量分析的主要手段主要是通过目视的方式,通过显微镜下的可视化分析,得到的微塑料颗粒大小一般在50 μm以上。因此,大多数研究集中于大于20 μm的微塑料。然而,在本研究中观察到,在UV条件下,产生了大量小于5 μm的微塑料。在实际应用中或废弃的塑料,均会受到紫外线的影响,这是一个无法避免的过程。在此基础上,本文拟通过对不同粒径(< 2 μm)的微塑料及其可溶有机物进行深入研究。
|
图 6 淀粉基塑料光降解不同时间后的微塑料释放数量与粒径分布 Fig. 6 The number and size distribution of microplastics released from starch-based plastics after different periods of photodegradation |
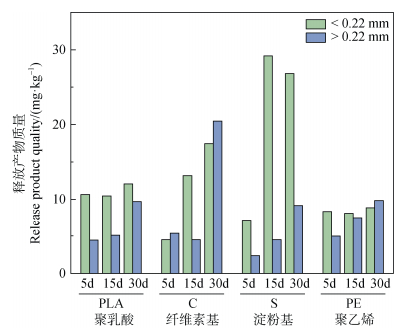
此外,通过膜过滤和总有机碳测定(MF-TOCD)法分析了微塑料释放情况(图 7)。结果表明,PE在15天后释放产物的质量为7.53 mg·g–1,30 d后逐渐增加至9.83 mg·g–1。此外,可以发现淀粉基生物塑料释放的产物中,粒径大于0.22 μm的部分在15 d时达到29.17 mg·kg–1,在30 d时达到26.83 mg·kg–1,而小于0.22 μm的部分含量相对较低,在30 d时仅达到9.15 mg·kg–1,在四类塑料中均呈现最大值。此外,可以发现PE释放的微塑料在5 d、15 d及30 d时均呈现较低的含量水平。PLA薄膜放大于0.22 μm的部分在30 d时达到12.07 mg·kg–1,而小于0.22 μm的部分在30 d时达到9.7 mg·kg–1。综上,总体而言大于0.22 μm部分的产物含量要高于小于0.22 μm的部分。
|
图 7 四种塑料薄膜光降解不同时间后的微塑料释放产物的质量 Fig. 7 The mass and particle size distribution of microplastics released from four types of plastic films after different durations of photo-degradation |
淀粉基塑料薄膜相比于其他三类塑料薄膜而言透明度相对较差,可能是生产过程中不太紧密,因此释放较多的原因。PLA由于其生产工艺的成熟,透光率相对达到较高水平。此外,三类生物塑料薄膜释放的两部分粒径相比于传统石油基塑料均呈现较小值,说明生物塑料在生产过程中由于其本身材料的缺陷,因此在释放过程中相较于PE释放的微塑料含量更高,在使用过程中仍需考虑其生态风险。
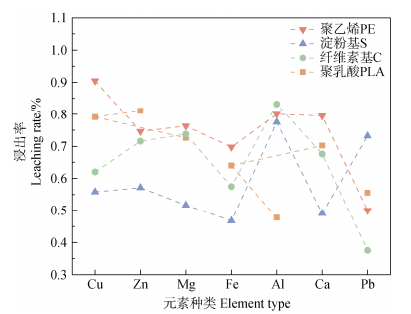
2.6 释放成分化学表征在紫外光条件下,针对聚乳酸、纤维素基、淀粉基及聚乙烯塑料的30 d降解实验研究表明,不同生物塑料的元素迁移特性存在显著差异(图 8)。其中,淀粉基塑料表现出最高的重金属浸出率,其Zn和Cu的累计浸出量分别达1.36 mg·kg–1和2.56 mg·kg–1,迁移率超过30%。这一现象与其光致多孔结构密切相关:微波、超声等物理处理或糖化酶与α-淀粉酶的协同作用可破坏淀粉颗粒的无定形区,形成贯通孔洞和离子扩散通道[23]。例如,复合酶解法中糖化酶优先降解颗粒表面不规则部分,随后α-淀粉酶通过内切作用扩大孔隙,最终形成中空结构,加速了内部重金属的溶出。羟基氧化反应进一步增强了孔隙的连通性,Zn2+和Cu2+的迁移提供了物理通道[24]。此外,生物塑料均未检测出Hg的释放,说明本身材料中均不含有。
|
图 8 四种生物塑料光降解30 d时无机添加剂浸出率 Fig. 8 Leaching rate of inorganic additives during 30-day photodegradation of bioplastics |
相比之下,聚乙烯(PE)因化学稳定性高且结晶度较大,元素浸出速率显著较低。PE的分子链结构致密,非晶区比例低,阻碍了重金属的扩散;但需注意的是,其光氧化降解产物(如羰基化合物)仍可能通过自由基链式反应缓慢释放Pb等元素。而PLA的降解机理则涉及紫外诱导的Norrish Ⅰ/Ⅱ反应,导致酯键断裂并生成小分子化合物,其释放的溶解有机质(DOM)中类蛋白组分可能络合金属离子,间接影响迁移行为。例如,PLA光降解后表面含氧官能团增加,亲水性提升,可能促进Cu的氧化态(如Cu2O)向渗滤液转移。
2.7 添加剂的浸出在表 1中列出了初始塑料中6种邻苯二甲酸酯类添加剂的含量,包括邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二(2-乙基己基)酯(DEHP)、邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二正辛酯(DNOP)、邻苯二甲酸丁苄酯(BBP)、以及邻苯二甲酸二乙酯(DEP)。从表 1可以看出,初始生物塑料中最常见的3种添加剂是DBP(265.93 µg·g–1)、DEHP(171.2 µg g–1)、DEP(100.19 µg g–1),共占邻苯二甲酸酯的36.54%、23.52%、14.11%,其余添加剂的含量总和小于15%,未检出DNOP、DMP。
|
|
表 1 四种初始生物塑料中邻苯二甲酸酯类添加剂的含量 Table 1 The content of phthalate additives in original bioplastic |
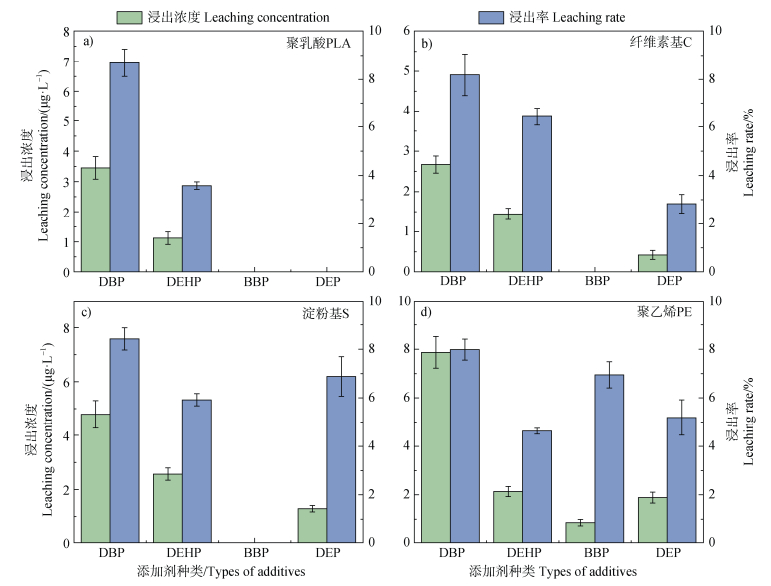
三种邻苯二甲酸酯添加剂在原塑料中的含量很少,但由于原料中三种添加剂的含量很少,很难被检测到。塑料中含量较高的4种添加剂DBP、BBP、DEP和DEHP在去离子水中的浸出浓度与浸出率如图 9所示。由图 9可知,光照30 d后,淀粉基塑料添加剂浸出浓度的大小顺序为DBP(4.79 μg·L–1) > DEHP(2.57 μg·L–1) > DEP(1.29 μg·L–1);纤维素基塑料的浸出浓度的大小顺序DBP(4.91 μg·L–1) > DEHP(3.86 μg·L–1) > DEP(1.7 μg·L–1);至于聚乙烯塑料,DBP(7.87 μg·L–1) > DEHP(4.94 μg·L–1) > BBP(4.62 μg·L–1) > DEP(1.89 μg·L–1);而对于聚乳酸塑料而言DEP浸出浓度未检出,说明其未释放到环境中。结果表明,添加物在塑料基体中的加入量与浸出物的浓度呈正相关关系,表明添加物在塑料中的质量分数对浸出物的释放有很大的影响。此外,添加剂本身的特性也会影响它的浸出。但是,由于DEHP在塑料中的含量较BBP高得多,使得DEHP在塑料中的溶出量要较BBP大得多。
|
图 9 邻苯二甲酸酯类添加剂30 d时的浸出浓度和浸出率 Fig. 9 Leaching concentration and leaching rate of phthalate ester additives at 30 d |
生物塑料不等于生物可降解,其环境风险与传统塑料类似[4]。经过上述实验可以发现,生物塑料在紫外线降解之后表观形态、结构组成、结晶度均发生了明显的变化。此外,通过添加剂的释放实验可以发现生物塑料均存在相应的释放情况,虽然释放量相较于传统石油基塑料有一定减少,但仍然存在相应的环境风险。微塑料的释放方面,淀粉基塑料相较于传统石油基塑料释放的微塑料数量更多,也表明生物塑料具有“分解-污染”双面效应,需要后续加深相关研究。生物塑料的降解过程可能涉及光降解、生物降解和化学降解等多种机制,但其降解速度和效率因材料类型和环境条件而异。尽管生物塑料在某些方面具有可再生和可降解的优势,但其在实际应用中仍面临诸多挑战,如生产成本高、性能不稳定、环境影响复杂等。因此,未来的研究应该集中于生产过程中,研究环境友好和毒性低的添加剂,此外应进一步探索更可持续的塑料替代材料和降解技术,以减少塑料污染和环境风险。
3 结论本研究证实,生物塑料薄膜在光降解过程中呈现出显著的“分解-污染”双面效应:尽管其表观分解速率与结晶度下降幅度高于传统PE膜,但快速崩解导致微塑料的释放。邻苯二甲酸酯类添加剂(如DBP)的迁移量(1.5~8 µg·kg–1)未超出国家标准限值,但仍有可能造成生态毒性风险。这些结果表明,现有生物塑料的“环境友好”属性存在局限性,其光降解衍生的次生污染物(微米塑料、DOM及PAEs)可能形成复合污染链,对农业生态系统构成长期威胁。因此,亟需在材料改性中优化降解可控性,限制添加剂使用,并建立覆盖全生命周期的环境风险评价体系,以实现生物塑料“高效降解”与“低环境负荷”的协同目标。
| [1] |
Gong J Q, Dong Y N, Xu S H, et al. The effect and mechanism of polystyrene on the cotransport of soil colloids and copper in saturated porous media (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(2): 436-447. DOI:10.11766/trxb202401150028 [龚佳琪, 董亚楠, 徐绍辉, 等. 聚苯乙烯对饱和多孔介质中土壤胶体与铜共运移的影响及机制[J]. 土壤学报, 2025, 62(2): 436-447.]
(  0) 0) |
| [2] |
Ardra N, Jo-Ann C, Kumar S, et al. Bioplastics: A boon or bane?[J]. Renewable and Sustainable Energy Reviews, 2021, 29(3): 147-151.
(  0) 0) |
| [3] |
Emadian M S, Onay T T, Demirel B, et al. Biodegradation of bioplastics in natural environments[J]. Waste Management, 2017, 59(13): 526-536.
(  0) 0) |
| [4] |
Han Y J, Teng Y. Research progress on ecological effects and microbial degradation of biodegradable plastics in soils (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(6): 1585-1597. DOI:10.11766/trxb202405270210 [韩玉娟, 滕应. 土壤中生物可降解塑料的生态效应及微生物降解研究进展[J]. 土壤学报, 2025, 62(6): 1585-1597.]
(  0) 0) |
| [5] |
Ghada A, Abanoub M, Parrish C C, et al. Environmental impact of bioplastic use: A review[J]. Heliyon, 2021, 7(9): e07918. DOI:10.1016/j.heliyon.2021.e07918
(  0) 0) |
| [6] |
Scott L, Martin W. Environmental performance of bio-based and biodegradable plastics: The road ahead[J]. Chemical Society Reviews, 2017, 46(22): 6855-6871. DOI:10.1039/C7CS00149E
(  0) 0) |
| [7] |
Polman M E, Gruter M G, Parsons R J, et al. Comparison of the aerobic biodegradation of biopolymers and the corresponding bioplastics: A review[J]. Science of the Total Environment, 2021, 753: 141953. DOI:10.1016/j.scitotenv.2020.141953
(  0) 0) |
| [8] |
Sun J X, Wang X, Zheng H Y, et al. Characterization of the degradation products of biodegradable and traditional plastics on UV irradiation and mechanical abrasion[J]. Science of the Total Environment, 2023, 909: 168618.
(  0) 0) |
| [9] |
Berit G, Merle P, Oskar S, et al. Identification of chain scission products released to water by plastic exposed to ultraviolet light[J]. Environmental Science & Technology Letters, 2018, 5(5): 272-276.
(  0) 0) |
| [10] |
Skopinska-Wisniewska J, Tuszynska M, Olewnik-Kruszkowska E. Comparative study of gelatin hydrogels modified by various cross linking agents[J]. Materials, 2021, 14(2): 396. DOI:10.3390/ma14020396
(  0) 0) |
| [11] |
Liu X P, Hua X D, Wu H. Degradation behavior of poly (lactic acid) during accelerated photo-oxidation: insights into structural evolution and mechanical properties[J]. Journal of Polymers and the Environment, 2024, 32(8): 3810-3821. DOI:10.1007/s10924-024-03211-x
(  0) 0) |
| [12] |
Marchetti B, Karsili T N V, Ashfold M N R. Exploring Norrish type I and type II reactions: An ab initio mechanistic study highlighting singlet-state mediated chemistry[J]. Physical Chemistry Chemical Physics, 2019, 21(26): 14418-14428. DOI:10.1039/C8CP07292B
(  0) 0) |
| [13] |
Li Z, He W Q, Liu E K, et al. Research progress on degradation process and mechanism of polyethylene film (In Chinese)[J]. Journal of Agro-Environment Science, 2019, 38(2): 268-275. [李真, 何文清, 刘恩科, 等. 聚乙烯地膜降解过程与机理研究进展[J]. 农业环境科学学报, 2019, 38(2): 268-275.]
(  0) 0) |
| [14] |
Feghali E, Tauk L, Ortiz P, et al. Catalytic chemical recycling of biodegradable polyesters[J]. Polymer Degradation and Stability, 2020, 179: 24-27.
(  0) 0) |
| [15] |
Jeon H J, Kim M N. Degradation of linear low density polyethylene (LLDPE) exposed to UV-irradiation[J]. European Polymer Journal, 2014, 52: 146-153. DOI:10.1016/j.eurpolymj.2014.01.007
(  0) 0) |
| [16] |
Wang F, Nan Z, Sun X, et al. Characterization of degradation behaviors of PLA biodegradable plastics by infrared spectroscopy[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2022, 279: 121376-121376. DOI:10.1016/j.saa.2022.121376
(  0) 0) |
| [17] |
Ahrens A, Bonde A, Sun H, et al. Catalytic disconnection of C–O bonds in epoxy resins and composites[J]. Nature, 2023, 617(7962): 730-732. DOI:10.1038/s41586-023-05944-6
(  0) 0) |
| [18] |
Lykhach Y, Johanek V, Neitzel A, et al. Redox-mediated C–C bond scission in alcohols adsorbed on CeO2−xthin films[J]. Journal of Physics: Condensed Matter, 2022, 34(19): 79-84.
(  0) 0) |
| [19] |
Idriss H. On the wrong assignment of the XPS O1s signal at 531–532 eV attributed to oxygen vacancies in photo- and electro-catalysts for water splitting and other materials applications[J]. Surface Science, 2021, 712: 121894. DOI:10.1016/j.susc.2021.121894
(  0) 0) |
| [20] |
Li X, Wan C, Tao T, et al. An overview of the development status and applications of cellulose-based functional materials[J]. Cellulose, 2023, 31(1): 61-99.
(  0) 0) |
| [21] |
Wu J Q, Chen J, Wang L, et al. Bronsted acid-catalysed aerobic photo-oxygenation of benzylic C–H bonds[J]. Green Chemistry, 2023, 25(3): 940-945. DOI:10.1039/D2GC04223A
(  0) 0) |
| [22] |
Gelebart A H, Mulder D J, Varga M, et al. Making waves in a photoactive polymer film[J]. Nature, 2017, 546(7660): 632-636. DOI:10.1038/nature22987
(  0) 0) |
| [23] |
Surana D, Vinay C, Patel P, et al. Microplastic fibers in different environmental matrices from synthetic textiles: ecotoxicological risk, mitigation strategies, and policy perspective[J]. Journal of Environmental Chemical Engineering, 2024, 12(2): 112333. DOI:10.1016/j.jece.2024.112333
(  0) 0) |
| [24] |
Saravanan P, Saravanan V, Rajeshkannan R, et al. Comprehensive review on toxic heavy metals in the aquatic system: Sources, identification, treatment strategies, and health risk assessment[J]. Environmental Research, 2024, 258: 119440. DOI:10.1016/j.envres.2024.119440
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


