2. 水污染控制与资源绿色循环全国重点实验室, 南京大学环境学院, 南京 210023
2. State Key Laboratory of Water Pollution Control and Green Resource Recycling, School of the Environment, Nanjing University, Nanjing 210023, China
微塑料(Microplastics,MPs)污染正通过多种途径侵入土壤环境[1-2]。这些颗粒既可直接来源于制造的初级MPs,也可由使用中的塑料制品和管理不善的塑料垃圾因老化、磨损及生物作用形成的次级MPs[3-4]。农业活动(如地膜更换、污水污泥施用)、工业与生活区的废弃物排放、地表径流及大气沉降是主要污染源[5-6]。现有监测数据显示,从高山苔原到工业区土壤中普遍存在聚苯乙烯(Polystyrene,PS)、聚乙烯等多种类型的MPs[7-8],其丰度呈现显著空间异质性,含量范围为每千克土壤几毫克至几万毫克[5,9]。随着MPs的持续排放和逐渐破碎,土壤中纳米塑料(Nanoplastics,NPs)的数量预计会显著增加[10]。MPs向NPs的长期转化过程将伴随有毒化合物(增塑剂、阻燃剂等添加剂及吸附污染物)的不断释放和积累[11-12],从而加剧塑料污染的“毒性债务”效应[13]。
相较于大尺寸MPs,纳米级尺寸(< 100 nm)赋予NPs独特的长距离迁移潜力和跨膜渗透能力,生物有效性高而有更高的生态风险[14-15]。作为土壤生态系统的"工程师",蚯蚓通过消化道机械破碎作用促进MPs纳米化[16-17],并通过其生物扰动行为驱动NPs的垂向迁移[18],从而改变NPs在土壤中的赋存分布及环境行为。此外,蚯蚓是评估土壤污染的重要指示生物,在毒理学研究中显示出对NPs的高度敏感性。研究表明,土壤中低浓度(30 mg·kg−1)NPs暴露即可通过体腔细胞的内吞作用诱发抗氧化酶活性降低和活性氧积累[19];而高浓度(200 mg·kg−1)暴露则进一步加剧蚯蚓消化和免疫系统的损害[19]。更值得关注的是,由于NPs具有高比表面积,其对多环芳烃等污染物的吸附能力增强。实验证实NPs作为载体可显著提高蚯蚓体内芘的积累浓度[20-21],并延长相关生物毒性的持续时间[22]。
目前,关于NPs与蚯蚓相互作用机制的研究仍不清楚,尤其是NPs通过不同途径进入和排出蚯蚓体内的动态过程尚未阐明。传统研究方法将蚯蚓暴露于含NPs的土壤中进行培养,但这种方法难以量化区分摄食与皮肤吸收对NPs内化的相对贡献,也无法明确肛门排泄和体表分泌在NPs排出过程中的差异。生理结构上,蚯蚓体壁具有类似于哺乳动物肺泡膜的气体交换功能:其角质层分布着密集的微小孔隙(主要为表皮腺和皮肾管的开口处),允许氧气渗入表皮下的毛细血管网络,同时实现二氧化碳的排出。理论上,NPs可经角质层孔隙进入表皮,并进一步通过毛细血管系统转运至其他器官或组织。然而,现有研究对蚯蚓皮肤途径的实验验证不足,主要是因为复杂环境基质(如土壤)中NPs的分离提取存在困难,且常规MPs检测方法在NPs分析方面存在局限性[23]。例如,光谱技术受分辨率限制难以识别纳米级颗粒,而热分析法则对低浓度NPs的定量精度不足[24-25]。近期发展起来的稀有金属标记法(如钯、铕标记)因其高灵敏度(检测限可达10–9级)和标记物稳定性(溶出率小于0.1%),已在活性污泥系统、土壤-植物或土壤-蚯蚓体系等复杂介质中成功追踪了NPs的迁移规律和归趋[18,26-27]。该方法为揭示NPs在土壤-蚯蚓界面转移机制提供了技术支撑。
本研究旨在初步量化蚯蚓对NPs的跨膜转运过程,重点揭示非摄食途径(皮肤吸收/排出)在NPs生物累积中的关键作用。以典型表层土壤生物指示种威廉腔环蚓(Metaphire guillelmi)作为模式生物,研究其对土壤表层(污染热点区域)NPs的皮肤吸收和排出过程。采用铕(Eu)标记的PS纳米颗粒作为模型NPs,并结合电感耦合等离子体质谱(ICP-MS)技术,实现对生物基质中NPs的痕量分析。首先,通过皮肤暴露实验,建立NPs浓度、暴露时间与组织分布之间的三维定量关系;其次,通过体腔暴露实验监测皮肤渗出率,解析NPs经皮排出的动力学特征;最后,通过土壤微宇宙实验,比较封口与未封口处理条件下蚯蚓体内NPs的分布差异,定量区分经皮吸收和经口摄入对NPs生物累积的相对贡献。
1 材料与方法 1.1 聚苯乙烯纳米塑料(PS NPs)的表征与定量分析方法采用去离子水对Eu标记的PS NPs分散液(上海百渝流体设备有限公司)进行稀释。随后,利用扫描电子显微镜(SEM,Zeiss-Supra55,蔡司,德国)对沉积于硅片上并经喷金处理的NPs微观形貌和粒径分布进行表征。借助高角环形暗场扫描透射电子显微镜(HAADF-STEM,Tecnai G2 F20,菲达康,美国)与X射线能谱仪(EDS,AZtec X-Max 80T,牛津,英国),分析沉积于铜网碳膜表面的NPs内部元素分布情况。通过ICP-MS仪(NexION 300X,珀金埃尔默,美国)测定NPs中Eu的含量。在进行ICP-MS分析前,将1 mL梯度稀释的NPs分散液(1 mg·L−1~1 g·L−1)与3 mL浓硝酸和2 mL 30%过氧化氢(均为分析纯,购自国药集团化学试剂有限公司)混合,并置于微波加速消解仪(Ethos UP,麦尔斯通,意大利)中进行消解。消解程序设定为:温度从20 ℃上升至160 ℃,耗时20 min,随后保持160 ℃恒温10 min,再冷却至25 ℃。取出样品后,用去离子水定容至50 mL,并经0.22 μm滤膜(直径13 mm,上海安谱科技股份有限公司)过滤后于4 ℃保存。该方法可实现NPs的完全分解,使Eu充分溶出。此外,将Eu标准溶液(购自国家有色金属及电子材料分析测试中心)梯度稀释后进行ICP-MS测定,并根据Eu标准曲线(1~50 μg·L−1)分析不同浓度NPs对应的Eu元素浓度,以计算NPs中Eu的质量分数。将NPs分散液(50 mg·L−1)在室温下静置10 d后,采用1 000 Da超滤膜进行过滤。再使用4 mL硝酸和硫酸混合液(体积比为8:1)对滤膜上的NPs进行消解,消解方法同前述步骤。通过ICP-MS分别测定超滤液和消解液中Eu的含量,并与未超滤处理的NPs消解液中Eu的含量进行对比,计算出Eu的回收率和溶出率。
1.2 供试土壤和动物以采自中国科学院常熟农业生态实验站的乌栅土(属于脱潜水稻土)为基质培养蚯蚓。将采集的土壤样品自然风干后,通过2 mm筛孔进行筛分,并储存备用。在使用前两周,向土壤样品中加入去离子水,调节其含水率至30 g·kg−1,以活化土壤性质。将180 mL浓度为100 mg·L−1的NPs分散液滴加至600 g土壤中,经自然晾干后研磨混匀,并重新加入去离子水恢复其含水率,制备出NPs添加量为30 mg·kg−1的土壤样品。实验所用威廉腔环蚓(M. guillelmi)购自句容蚯蚓养殖场。挑选健康成年个体,并在未添加NPs的土壤中驯养至少14 d。在NPs暴露实验开始前,将蚯蚓取出并清洗体表,随后置于湿润滤纸上,在20 ℃黑暗环境中进行48 h的清肠处理,期间清理排泄物以确保实验条件的一致性。
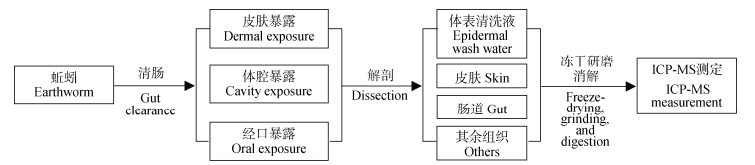
1.3 蚯蚓暴露实验随机选取已完成清肠处理且体重相近的蚯蚓,分别采用三种方式进行暴露。实验流程如图 1所示,具体操作如下:
|
图 1 纳米塑料对蚯蚓的皮肤暴露、体腔暴露及经口暴露实验流程简图 Fig. 1 Schematic workflow for dermal exposure, body cavity exposure, and oral exposure of earthworms to nanoplastics |
将蚯蚓单独转入垫有湿润滤纸的培养皿中(每皿1条),向不同培养皿中蚯蚓体表(背部避开口部)缓慢滴加200 μL不同浓度的NPs分散液(100和1 000 mg·L−1),对应暴露剂量分别为20和200 μg。确保NPs分散液被蚯蚓充分吸收后,将其置于22 ℃黑暗环境中进行培养。暴露3、6、12和24 h后取出蚯蚓,每个处理组包含1条蚯蚓,并设置四个平行样本。
1.3.2 体腔暴露实验将蚯蚓置于–20 ℃冷冻15 min使其麻醉,采用微量注射器(50 μL,汉密尔顿,德国)分别抽取50 μL不同浓度的NPs分散液(400和4 000 mg·L−1),横向轻轻刺入蚯蚓环带后1~2体节的表皮内,对其进行体腔注射,注射剂量(20和200 μg)与皮肤暴露剂量保持一致。注射完成后,立即用医用组织胶水(3M,美国)封闭针孔,以防止液体渗出导致NPs损失。随后将蚯蚓放入垫有湿润滤纸的培养皿中(每皿1条),并在22 ℃黑暗环境中培养。暴露3、6、12和24 h后取出蚯蚓,每个处理组包含1条蚯蚓,并设置四个平行样本。
1.3.3 经口暴露实验将蚯蚓口器侵入组织胶水(博朗,德国)中30 s后取出,待胶水凝固后,其口器被封闭,从而阻断土壤NPs的经口暴露途径。将5条封口处理和5条未封口处理的蚯蚓共同放入添加了18 mg NPs的600 g土壤中,在22 ℃黑暗环境中培养3、6、12、18和24 h后取出,每个处理组包含10条蚯蚓,并设置四个平行样本。
1.4 蚯蚓样品中NPs的定量分析经NPs暴露不同时间后,将蚯蚓取出并用去离子水清洗体表,之后将蚯蚓置于无水乙醇中处死,并进行解剖操作。分别收集蚯蚓的皮肤、肠道及其余组织(口、咽、食管、砂囊和胃等样品合并),并对各部分进行冻干处理及称重。对于同一处理组的相同器官组织样品,将其合并;针对生物量较高的皮肤样品,进一步进行研磨混匀。称取小于0.1 g样本,采用王水(含6 mL体积分数为38%的盐酸和2 mL体积分数为69%的硝酸)并借助微波加速消解仪进行消解处理。具体消解程序设定为:在20 min内将温度从20 ℃升至175 ℃,保持175 ℃恒温10 min,随后冷却至少50 min或直至温度降至25 ℃以下,取出样品并定容至40 mL。最后,利用ICP-MS分别测定各样品中Eu元素的含量,并根据NPs中Eu的质量分数换算各器官组织内NPs的含量。对于皮肤和体腔暴露的蚯蚓,收集其体表清洗水。按照1.1节所述方法对清洗水进行消解处理,测定其中Eu元素的含量,换算为蚯蚓体表NPs的残留量或排出量,并除以暴露剂量得到皮肤渗透率(渗入率或渗出率)。
1.5 蚯蚓皮肤吸收NPs的原位观察对于经皮肤暴露(200 μg)处理的蚯蚓,在完成清肠操作后,清洗其体表并将其置于无水乙醇中处死。随后对蚯蚓进行解剖,剥离皮肤组织,并将组织放入2.5%戊二醛溶液中固定30 min。之后依次使用体积分数为30%、50%、70%、80%、90%和100%的乙醇溶液各处理15 min,以完成梯度脱水。待乙醇完全挥发后,将样品粘附于导电胶上并进行喷金处理,最后利用SEM观察皮肤内侧是否存在NPs。
1.6 数据统计分析采用单因素方差分析结合Tukey检验,比较不同处理组中蚯蚓各器官组织内NPs含量的显著性差异,统计学意义标准为P < 0.05。统计分析通过SPSS 17.0完成。除非另有说明,数据均以四个重复样本计算所得的平均值±标准偏差的形式表示。
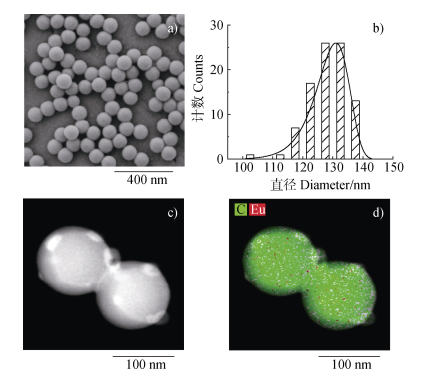
2 结果与讨论 2.1 Eu标记PS NPs的微观结构组成本研究首先对购买的PS NPs进行了系统的表征分析,结果如图 2所示。从SEM图像(图 2a)中可看出,NPs呈现规则的球形结构,其平均直径为128 ± 6 nm(n = 91,图 2b)。较低的标准偏差及多分散指数(0.08)表明粒径分布具有良好的均匀性。HAADF-STEM成像结果(图 2c)进一步验证了纳米颗粒的球形特征,且粒径大小与SEM成像结果一致。此外,通过EDS成像分析(图 2d),发现碳(C)元素在整个纳米颗粒中均匀分布,而Eu元素呈散落分布状态。该结果表明Eu元素是以掺杂的形式引入PS基体中,从而实现标记功能。通过消解处理并结合ICP-MS分析,发现NPs与其所含Eu元素的质量浓度之间呈现出正相关线性关系(y = 0.02 x – 3.6,R2 = 0.999 4)。基于此结果,进一步计算出NPs中Eu元素的掺杂比例为1.7% ± 0.2%。因此,通过测定样品中Eu元素的含量,可实现对NPs含量的准确推算。此外,通过对以去离子水为背景溶液的NPs分散液进行超滤处理,测定得到Eu的溶出率为0.03%,表明Eu标记具有良好的稳定性。
|
图 2 铕(Eu)标记聚苯乙烯纳米塑料的扫描电镜图像(a)、粒径分布(b)、高角环形暗场扫描透射电镜图像(c)及X射线能谱元素(C和Eu)分布图像(d) Fig. 2 Scanning electron microscopic image (a), particle size distribution (b), and high-angle annular dark-field scanning transmission electron microscopic image (c) of Eu-labeled polystyrene nanoplastics and elemental mapping for C and Eu by energy dispersive X-ray spectroscopy (d) |
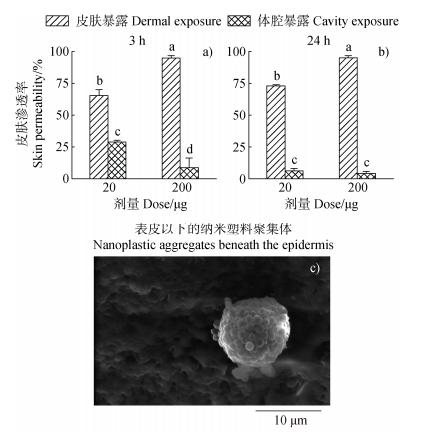
通过在蚯蚓体表滴加NPs分散液,并监测不同时间点体表清洗水中NPs的含量,研究了NPs在蚯蚓皮肤上的吸收动力学特性。如图 3a、图 3b所示,NPs的皮肤渗入率在3 h内迅速提高至65.4% ± 4.7%(20 μg)和94.7% ± 2.1%(200 μg),随后在24 h时缓慢增加至73.0% ± 0.9%(20 μg)和95.0 %± 1.6%(200 μg)。上述结果表明,蚯蚓皮肤能够吸收大部分NPs,且吸收率随着暴露剂量的增加而显著提高。为进一步验证NPs的表皮穿透行为,对蚯蚓皮肤样品进行了SEM表征。由图 3c可看出,在表皮下方可观察到NPs,表明其已穿透表皮屏障。基于上述实验数据推测,蚯蚓皮肤对NPs的吸收呈现快速和慢速两阶段特征,这种吸收行为可能与NPs在皮肤表面赋存形态的变化密切相关。在初期(< 3 h),当NPs分散液滴加于蚯蚓体表时,浓度梯度驱动的被动扩散机制占主导地位,大多数颗粒可随水流迅速跨越表皮屏障,表现为快速吸收。在后期(3~24 h),由于表皮分泌的黏液形成黏滞阻力,以及NPs发生聚集现象,显著抑制了扩散速率和跨膜转运效率,从而导致吸收速率减缓。SEM图像中,表皮下方存在微米尺度的NPs聚集体,揭示了黏液介导的聚集效应。值得注意的是,NPs虽聚集但保持球形,表明其未发生化学降解。因此,蚯蚓皮肤对NPs的吸收过程受到物理扩散机制及黏液介导的聚集效应的共同调控。
|
注:柱状图上不同字母代表显著性差异。下同。 Note: Different letters indicate significant differences (P < 0.05). The same below. 图 3 蚯蚓皮肤或体腔暴露3 h(a)和24 h(b)后纳米塑料的皮肤渗透率及皮肤暴露3 h后的扫描电镜图像(c) Fig. 3 Skin permeability of nanoplastics in earthworms after exposure of the skin or body cavity for 3 h (a) and 24 h (b), and scanning electron microscopic image of the skin following 3 h of exposure (c) |
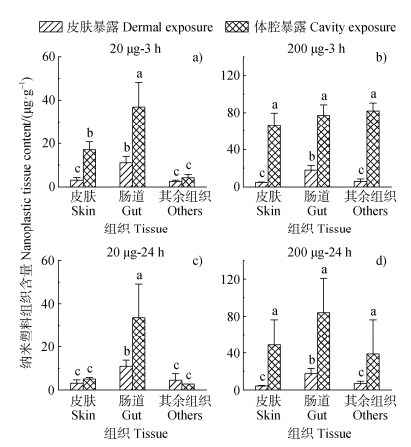
通过系统分析NPs经皮肤暴露后在蚯蚓体内的动态分布特征,发现其转运过程呈现明显的剂量依赖性。在低剂量(20 μg)暴露3 h的情况下,可在蚯蚓的皮肤、肠道及其余组织中检测到NPs(图 4a),说明NPs已突破皮肤屏障进入循环系统。其中,肠道中NPs的积累量(11.0 ± 2.9 μg·g−1)显著高于皮肤(3.1 ± 1.2 μg·g−1)和其余组织(2.5 ± 0.6 μg·g−1)。随着皮肤暴露剂量增至200 μg,各组织中NPs的含量分别提高了1.5倍(皮肤:4.8 ± 0.4 μg·g−1)、1.6倍(肠道:17.9 ± 4.8 μg·g−1)和2.3倍(其余组织:5.8 ± 2.7 μg·g−1)(图 4b)。该增幅差异反映了不同器官对NPs的蓄积能力存在差异。与低剂量相比,高剂量下NPs组织含量的平均增幅(1.8倍)与其皮肤渗透率的增幅(1.4倍)接近(图 3a),表明NPs在蚯蚓体内的转运主要受皮肤渗透效率的调控。然而,当暴露时间延长至24 h,各组织中NPs的含量并未出现显著变化(图 4c,图 4d),可能与皮肤对NPs的慢速吸收以及机体对NPs的缓慢清除机制有关。值得注意的是,NPs在蚯蚓体内的分布表现出显著的器官选择性,其中肠道是主要的积累器官。该特性可能与肠道具有较大的表面积、富含消化液和微生物群落密切相关[28]。消化液中的蛋白质和微生物胞外聚合物可能通过促进NPs的聚集[29-30],进一步增强其在肠道中的吸附和滞留能力。
|
图 4 蚯蚓皮肤或体腔暴露3 h(a,b)和24 h(c,d)后各组织中纳米塑料的含量 Fig. 4 Tissue content of nanoplastics in earthworms after exposure of the skin or body cavity for 3 h (a, b) and 24 h (c, d) |
通过向蚯蚓体腔注射NPs分散液,系统监测了体表清洗水中NPs含量随时间的变化规律,研究了NPs通过蚯蚓皮肤排出的动力学特征。如图 3a、图 3b所示,NPs在3 h内的皮肤渗出率呈现出显著的剂量依赖性差异:低剂量组(20 μg)的渗出率为28.7% ± 1.4%,而高剂量组(200 μg)仅为8.6 % ± 7.6%。至24 h时,两组的渗出率分别降至6.2% ± 1.7%和4.3% ± 1.4%。上述结果表明,NPs皮肤排泄呈现初期快速响应和后期持续衰减的双相动力学特征。NPs可能通过两条途径排出:体壁背孔直接渗出和小肾管(其排泄管直接连通体腔)过滤排泄。值得注意的是,NPs通过皮肤的渗入率显著高于渗出率,这表明皮肤在NPs代谢中的主要功能是吸收而非排泄。皮肤渗出率随体腔暴露时间降低的现象,可能与排出的NPs被重新吸收有关。此外,在体腔暴露条件下,NPs的皮肤渗出率与剂量呈负相关关系,而该趋势与皮肤暴露时观察到的正相关关系形成鲜明对比。这种逆转可能源于NPs的不同分配模式,在皮肤暴露条件下,NPs仅与皮肤相互作用;而在体腔暴露条件下,NPs需在肠道、皮肤及其他器官间动态分配,显著降低了皮肤排泄占比。
蚯蚓经体腔暴露后NPs的组织分布结果(图 4)显示,低剂量组(20 μg)中NPs呈现器官选择性分布特征。肠道中的NPs含量(3 h:36.9 ± 11.3 μg·g−1;24 h:33.6 ± 15.5 μg·g−1)显著高于皮肤(3 h:16.9 ± 3.7 μg·g−1;24 h:5.1 ± 0.7 μg·g−1)及其余组织(3 h:4.2 ± 1.6 μg·g−1;24 h:2.8 ± 0.01 μg·g−1)。当暴露剂量提升至200 μg时,各组织中的NPs含量均显著增加,且分布趋于均质化。此时,肠道(3 h:77.0 ± 11.6 μg·g−1;24 h:84.0 ± 36.8 μg·g−1)、皮肤(3 h:65.7 ± 13.8 μg·g−1;24 h:48.7 ± 27.6 μg·g−1)及其他组织(3 h:82.0 ± 8.6 μg·g−1;24 h:38.7 ± 37.4 μg·g−1)中的NPs含量差异逐渐缩小。值得注意的是,体腔注射3 h内即可在各组织中检测到NPs,表明其能通过体腔液快速转运至全身,并可能通过肠上皮细胞的内吞作用突破肠道屏障后而排出体外。除20 μg暴露24 h的皮肤和其余组织外,所有组织中的NPs含量均显著高于皮肤暴露组(图 4),该结果与体腔暴露组中较低的皮肤渗出率(图 3)形成互证。
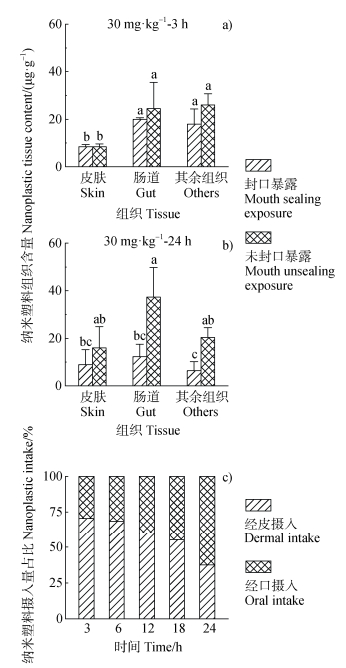
2.4 皮肤吸收是蚯蚓摄入土壤NPs的重要途径为了探究皮肤吸收在蚯蚓摄入土壤NPs中的贡献,通过组织胶水对蚯蚓进行封口处理,构建单一皮肤暴露模型,并与未封口的蚯蚓(皮肤+摄食暴露)共同置于同一土壤环境中24 h,监测各组织中NPs含量分布的变化。结果显示,组织胶水能够在暴露期间有效保持蚯蚓口部闭合状态,同时其运动行为与未经封口处理的蚯蚓无显著差异。NPs在蚯蚓各器官组织中的分布结果如图 5a、图 5b所示。在土壤中暴露3 h后,封口蚯蚓(或未封口蚯蚓)皮肤、肠道和其余组织中NPs的含量分别为8.4 ± 0.8 μg·g−1(或8.5 ± 1.1 μg·g−1)、19.9 ± 0.7 μg·g−1(或24.5 ± 11.1 μg·g−1)和17.9 ± 6.4 μg·g−1(或26.0 ± 4.7 μg·g−1)。由此可见,封口处理并未显著影响蚯蚓对NPs的摄入量。即使蚯蚓不能摄食,其皮肤仍暴露于土壤中的NPs,这些纳米颗粒能够通过皮肤渗入蚯蚓体内。随着暴露时间延长至24 h,未封口蚯蚓皮肤和肠道中NPs的含量分别增加了1.9倍(15.9 ± 8.9 μg·g−1)和1.5倍(37.3 ± 12.5 μg·g−1),而其余组织中NPs的含量则降低了21.9%(20.3 ± 4.1 μg·g−1)。相比之下,封口蚯蚓除皮肤外的组织中NPs含量显著低于未封口蚯蚓,其中肠道含量减少了67%(12.3 ± 5.2 μg·g−1)。该现象与未封口蚯蚓具有额外的摄食功能直接相关。进一步比较封口与未封口蚯蚓全身积累量的差异,计算得出皮肤吸收和摄食两种途径对NPs累积的相对贡献。如图 5c所示,当暴露时间从3 h延长至24 h时,经口摄入量占比从29.4%升至62.5%,而经皮摄入量占比则从70.3%降至37.4%。这些结果表明NPs摄入机制具有时间依赖性特征,初期(< 3 h)以皮肤渗透为主导,后期则转为摄食主导。这种转化可能与表皮接触的NPs饱和效应及肠道持续富集能力有关。由于表皮外暴露剂量始终高于肠道内暴露剂量,导致皮肤吸收途径在早期暴露中的主导作用。
|
图 5 封口与未封口蚯蚓暴露于土壤3 h(a)和24 h(b)后各组织中纳米塑料的含量以及经口和经皮摄入的相对贡献(c) Fig. 5 Tissue content of nanoplastics in earthworms(with or without mouth sealing treatment)exposed to soil for 3 h (a) and 24 h (b), and the relative contribution of oral and dermal intake (c) |
蚯蚓在评估土壤NPs生态风险方面具有重要指示作用,而精准的定量分析方法对于揭示NPs对蚯蚓的暴露途径至关重要。本研究创新性地采用Eu标记结合痕量金属分析技术,突破了传统检测方法的局限性,实现了对蚯蚓通过皮肤、体腔和摄食三种方式暴露后NPs残留量的精确定量分析,并揭示了NPs在土壤-蚯蚓界面的传输机制。皮肤暴露结果表明,NPs能够穿透蚯蚓表皮屏障,皮肤吸收动力学呈现双相模式:初期(0~3 h)快速吸收阶段,主要由浓度梯度驱动的被动扩散主导;后期(3~24 h)则进入慢速吸收阶段,受到表皮黏液层阻力和NPs聚集效应的显著抑制。体腔暴露研究发现,NPs通过皮肤排泄的过程同样表现出双相特征,即快速清除(3 h内达28.7%±1.4%)和缓慢衰减。NPs的皮肤渗出率显著低于皮肤渗入率,这表明皮肤在NPs代谢过程中主要发挥吸收功能。综合封口实验结果,进一步明确了NPs摄入途径的时间依赖性转变规律:暴露初期(< 3 h)以皮肤渗透为主(占比70.3%),而24 h后则转为摄食主导(占比62.5%)。值得注意的是,NPs的皮肤渗透效率表现出明显的剂量依赖性,其在蚯蚓体内呈现器官特异性蓄积特征,其中肠道是最主要的靶器官。上述发现为深入理解纳米污染物在土壤生态系统中的生物地球化学循环提供了重要的理论依据。
| [1] |
He L Y, Li Z B, Jia Q, et al. Soil microplastics pollution in agriculture[J]. Science, 2023, 379(6632): 547-547. DOI:10.1126/science.adf6098
(  0) 0) |
| [2] |
Rillig M C, Lehmann A. Microplastic in terrestrial ecosystems[J]. Science, 2020, 368(6498): 1430-1431. DOI:10.1126/science.abb5979
(  0) 0) |
| [3] |
Su Y, Hu X, Tang H J, et al. Steam disinfection releases micro(nano)plastics from silicone-rubber baby teats as examined by optical photothermal infrared microspectroscopy[J]. Nature Nanotechnology, 2022, 17(1): 76-85. DOI:10.1038/s41565-021-00998-x
(  0) 0) |
| [4] |
Guo J J, Huang X P, Xiang L, et al. Source, migration and toxicology of microplastics in soil[J]. Environment International, 2020, 137: 105263. DOI:10.1016/j.envint.2019.105263
(  0) 0) |
| [5] |
Liu R H, Wang Y H, Zhao J, et al. Microplastics pollution in soil and the potential ecological health risks (In Chinese)[J]. Environmental Chemistry, 2022, 41(10): 3214-3230. [刘锐涵, 王艳华, 赵建, 等. 土壤微塑料污染与生态健康风险[J]. 环境化学, 2022, 41(10): 3214-3230.]
(  0) 0) |
| [6] |
Yang J, Li L Z, Zhou Q, et al. Microplastics contamination of soil environment: Sources, processes and risks (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 281-298. [杨杰, 李连祯, 周倩, 等. 土壤环境中微塑料污染: 来源、过程及风险[J]. 土壤学报, 2021, 58(2): 281-298.]
(  0) 0) |
| [7] |
Scheurer M, Bigalke M. Microplastics in Swiss floodplain soils[J]. Environmental Science & Technology, 2018, 52(6): 3591-3598.
(  0) 0) |
| [8] |
Fuller S, Gautam A. A procedure for measuring microplastics using pressurized fluid extraction[J]. Environmental Science & Technology, 2016, 50(11): 5774-5780.
(  0) 0) |
| [9] |
Yu L, Zhang J D, Liu Y, et al. Distribution characteristics of microplastics in agricultural soils from the largest vegetable production base in China[J]. Science of the Total Environment, 2021, 756: 143860. DOI:10.1016/j.scitotenv.2020.143860
(  0) 0) |
| [10] |
Mitrano D M, Wick P, Nowack B. Placing nanoplastics in the context of global plastic pollution[J]. Nature Nanotechnology, 2021, 16(5): 491-500. DOI:10.1038/s41565-021-00888-2
(  0) 0) |
| [11] |
Kou S Q, Guan Z, Lu X Y, et al. Migration of microplastics in soil and its effect on organic pollutants: A review (In Chinese)[J]. Soils, 2024, 56(3): 457-470. [寇诗棋, 关卓, 鲁旭阳, 等. 土壤中微塑料迁移及其对有机污染物的影响研究进展[J]. 土壤, 2024, 56(3): 457-470.]
(  0) 0) |
| [12] |
Zhang L, Sun D, Zhang J Q, et al. Research progress on the migration of agricultural film microplastics and phthalates in soil (In Chinese)[J]. Soils, 2024, 56(5): 938-947. [张蕾, 孙东, 张建强, 等. 农膜微塑料与酞酸酯在土壤中迁移的研究进展[J]. 土壤, 2024, 56(5): 938-947.]
(  0) 0) |
| [13] |
Rillig M C, Kim S W, Kim T Y, et al. The global plastic toxicity debt[J]. Environmental Science & Technology, 2021, 55(5): 2717-2719.
(  0) 0) |
| [14] |
Gigault J, El Hadri H, Nguyen B, et al. Nanoplastics are neither microplastics nor engineered nanoparticles[J]. Nature Nanotechnology, 2021, 16(5): 501-507. DOI:10.1038/s41565-021-00886-4
(  0) 0) |
| [15] |
Liu X B, Dong X S, Xie Z H, et al. Ecological effects and biodegradation of microplastics in soils (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(2): 349-363. DOI:10.11766/trxb202102240040 [刘鑫蓓, 董旭晟, 解志红, 等. 土壤中微塑料的生态效应与生物降解[J]. 土壤学报, 2022, 59(2): 349-363.]
(  0) 0) |
| [16] |
Kwak J I, An Y J. Microplastic digestion generates fragmented nanoplastics in soils and damages earthworm spermatogenesis and coelomocyte viability[J]. Journal of Hazardous Materials, 2021, 402: 124034. DOI:10.1016/j.jhazmat.2020.124034
(  0) 0) |
| [17] |
Wang L, Peng Y W, Xu Y L, et al. Earthworms' degradable bioplastic diet of polylactic acid: Easy to break down and slow to excrete[J]. Environmental Science & Technology, 2022, 56(8): 5020-5028.
(  0) 0) |
| [18] |
Heinze W M, Mitrano D M, Lahive E, et al. Nanoplastic transport in soil via bioturbation by Lumbricus terrestris[J]. Environmental Science & Technology, 2021, 55(24): 16423-16433.
(  0) 0) |
| [19] |
Tang R G, Zhu D, Luo Y M, et al. Nanoplastics induce molecular toxicity in earthworm: Integrated multi-omics, morphological, and intestinal microorganism analyses[J]. Journal of Hazardous Materials, 2023, 442: 130034. DOI:10.1016/j.jhazmat.2022.130034
(  0) 0) |
| [20] |
Liu Y, Xu G H, Yu Y. Effects of polystyrene microplastics on accumulation of pyrene by earthworms[J]. Chemosphere, 2022, 296: 134059. DOI:10.1016/j.chemosphere.2022.134059
(  0) 0) |
| [21] |
Wang J, Li J, Wang Q, et al. Microplastics as a vector for HOC bioaccumulation in earthworm Eisenia fetida in soil: Importance of chemical diffusion and particle size[J]. Environmental Science & Technology, 2020, 54(19): 12154-12163.
(  0) 0) |
| [22] |
Sun N, Hu S Y, Zhao X C, et al. Amplification of benzo[a]pyrene toxicity persistence in earthworms by polystyrene nanoplastics: From organismal health to molecular responses[J]. Journal of Hazardous Materials, 2025, 487: 137091. DOI:10.1016/j.jhazmat.2025.137091
(  0) 0) |
| [23] |
Blancho F, Davranche M, Hadri H E, et al. Nanoplastics identification in complex environmental matrices: Strategies for polystyrene and polypropylene[J]. Environmental Science & Technology, 2021, 55(13): 8753-8759.
(  0) 0) |
| [24] |
Ivleva N P. Chemical analysis of microplastics and nanoplastics: Challenges, advanced methods, and perspectives[J]. Chemical Reviews, 2021, 121(19): 11886-11936. DOI:10.1021/acs.chemrev.1c00178
(  0) 0) |
| [25] |
Chen Y L, Sun K, Han L F, et al. Separation, identification, and quantification methods in soil microplastics analysis: A review (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(2): 364-380. DOI:10.11766/trxb202012070566 [陈雅兰, 孙可, 韩兰芳, 等. 土壤中微塑料的分离及检测方法研究进展[J]. 土壤学报, 2022, 59(2): 364-380.]
(  0) 0) |
| [26] |
Mitrano D M, Beltzung A, Frehland S, et al. Synthesis of metal-doped nanoplastics and their utility to investigate fate and behaviour in complex environmental systems[J]. Nature Nanotechnology, 2019, 14(4): 362-368. DOI:10.1038/s41565-018-0360-3
(  0) 0) |
| [27] |
Luo Y M, Li L Z, Feng Y D, et al. Quantitative tracing of uptake and transport of submicrometre plastics in crop plants using lanthanide chelates as a dual-functional tracer[J]. Nature Nanotechnology, 2022, 17(4): 424-431. DOI:10.1038/s41565-021-01063-3
(  0) 0) |
| [28] |
Sun M M, Chao H Z, Zheng X X, et al. Ecological role of earthworm intestinal bacteria in terrestrial environments: A review[J]. Science of The Total Environment, 2020, 740: 140008. DOI:10.1016/j.scitotenv.2020.140008
(  0) 0) |
| [29] |
Lee G, Jhang Y J, Jhang Y T, et al. Artificial digestion represents the worst-case scenario for studying nanoplastic fate in gastrointestinal tract[J]. Journal of Hazardous Materials, 2025, 485: 136809. DOI:10.1016/j.jhazmat.2024.136809
(  0) 0) |
| [30] |
Liu Y J, Yue T T, Liu L, et al. Molecular assembly of extracellular polymeric substances regulating aggregation of differently charged nanoplastics and subsequent interactions with bacterial membrane[J]. Journal of Hazardous Materials, 2023, 457: 131825. DOI:10.1016/j.jhazmat.2023.131825
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


