2. 土壤与农业可持续发展全国重点实验室(中国科学院南京土壤研究所), 南京 211135;
3. 南京信息工程大学环境科学与工程学院, 南京 210044;
4. 陕西科技大学环境科学与工程学院, 西安 710021;
5. 南京师范大学环境学院, 南京 210023;
6. 中国科学院大学, 北京 100049
2. State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 211135, China;
3. School of Environmental Science and Engineering, Nanjing University of Information Science & Technology, Nanjing 210044, China;
4. School of Environmental Science and Engineering, Shaanxi University of Science and Technology, Xi'an 710021, China;
5. School of Environment, Nanjing Normal University, Nanjing 210023, China;
6. University of Chinese Academy of Sciences, Beijing 100049, China
塑料已成为现代人类社会不可或缺的材料,其广泛应用带来了前所未有的便利。但与此同时,塑料垃圾所引发的环境污染问题也日益严峻,成为全球面临的重大生态挑战[1]。大量废弃塑料长期滞留于自然环境中,并在物理、化学及生物作用下逐步降解为微塑料(Microplastics,粒径 < 5 mm)和纳米塑料(Nanoplastics,粒径 < 1 μm)。在土壤环境中,微/纳米塑料(Microplastics and Nanoplastics,MNPs)的累积不仅改变了土壤团聚体结构、水分保持能力、总有机碳含量、土壤pH及电导率等理化性质,还可作为有机污染物和重金属的吸附载体,进一步加剧土壤污染的复杂性[2-4]。此外,MNPs对土壤系统中的动植物生长发育也存在直接影响[5-9],进而可对作物安全构成潜在风险,亟需加强关注。
土壤-植物系统是连接土壤、植物及更高营养级生物的重要生态单元,在物质循环和能量流动中扮演核心角色。探究MNPs在土壤-植物系统中的迁移行为及其生态效应已成为环境科学研究的热点方向。要实现对MNPs在土壤-植物系统中行为机制的精准解析,迫切需要依赖可靠的标记与示踪技术。然而,当前有关MNPs的标记技术主要应用于水环境及水生生物体中,对于土壤-植物系统中MNPs的标记研究尚处于起步阶段。本文系统梳理了国内外关于MNPs标记技术的最新研究进展,重点分析了各类标记技术的原理、适用范围、应用现状与优势局限,并探讨了未来MNPs标记技术发展的重点方向,旨在为深入揭示MNPs在土壤-植物系统中的环境行为与生态风险提供理论依据和方法支撑。
1 荧光标记法在现有标记与示踪技术中,荧光标记法被广泛认为是实现MNPs可视化最直接且高效的手段之一。2014年,Desforges等[10]首次将尼罗红(Nile Red)应用于深海微塑料的染色研究,这一研究不仅极大推动了微塑料在环境介质中迁移与归趋研究的进展,也为后续构建可视化追踪体系提供了重要技术支撑。该方法可有效提升在复杂环境基质中对MNPs的识别效率,并为其迁移路径、赋存状态及环境风险评估提供关键技术手段[11-12]。
1.1 荧光标记法的原理荧光标记法的基本原理是将荧光分子与目标物质结合,在特定的波长激发光作用下产生可检测的荧光信号,从而实现对目标的识别、追踪与定量分析。被荧光标记的样品可通过荧光显微镜、流式细胞仪或光谱仪等检测设备进行空间定位、浓度测定及时间动态分析[13]。在MNPs的标记研究中,荧光分子的引入可通过多种技术路径实现。如图 1所示,常见的荧光标记方法包括:物理吸附法[14-15];包埋法[16-18];溶剂溶胀法[19-20],以及化学共聚结合法[21-24]。
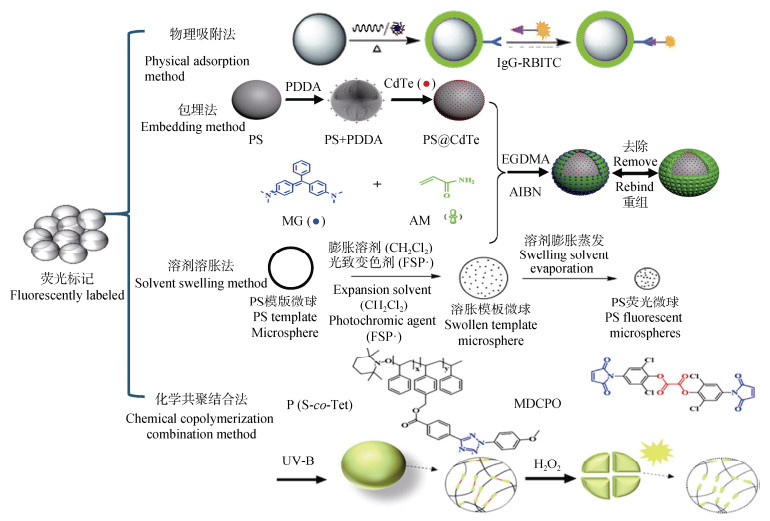
|
图 1 微/纳米塑料荧光标记技术的常见方法[15,18,20-21] Fig. 1 Common methods of fluorescence labeling techniques for MNPs[15, 18, 20-21] |
物理吸附法是一种通过调控MNPs表面物理性质(如表面能、电荷分布或功能位点)以实现荧光染料与被标记塑料非共价结合的标记方法。例如,Sun等[15]利用表面带有磺基的聚对苯乙烯(PPV)微球,通过静电吸附作用将染料吸附于微球表面,从而构建出具有荧光特性的PPV微球体系。然而,物理吸附法中荧光分子裸露于材料表面,易受到介质条件(如pH、离子强度、有机溶剂)的影响,导致标记染料发生解吸或泄漏,进而造成荧光信号的衰减或消失。因此,物理吸附法虽然在操作简便与制备效率方面具有优势,但因在复杂环境中的稳定性和耐久性较差,限制了其在长期示踪研究中的广泛应用。
包埋法是通过将荧光染料分散于聚合体系或载体介质中,借助聚合反应或微胶囊化技术将其包覆形成荧光微球的一种标记策略。该方法能够减少染料因外部环境扰动而发生的泄漏现象。例如,Yang等[18]通过静电自组装方法将量子点(Quantum Dots)分散于PS微球表面,并在其外层进一步结合孔雀石绿染料,形成了典型的核—壳结构,该结构有效防止了荧光染料的泄漏,可显著增强标记体系的荧光稳定性与可追踪性。
溶剂溶胀法则通过调控温度及溶剂环境来诱导MNPs结构发生可逆性膨胀,使荧光染料渗透至聚合物内部,并在冷却或溶剂挥发后“锁定”于塑料微球中,从而实现稳定的荧光标记。该过程通常涉及使用有机溶剂(如甲苯或氯仿)配合温度控制来增强聚合物链段运动性与染料的嵌入效率[25]。例如,Bretler和Marger[20]通过溶胀法将螺吡喃染料嵌入PS微球结构中,实现了染料与塑料之间均匀且紧密的结合,显著提高了其荧光稳定性和抗泄漏性能。
化学共聚结合法是将荧光染料或其前体与高分子单体通过化学反应进行共价结合,在聚合过程中共同构建出荧光微球。这一方法因其结构稳定性高、染料不易脱落,在长期追踪实验中表现出优异的信号保留能力。例如,Liu等[22]将稀土金属铕(Eu)配合物与PS单体进行共聚反应,合成了具有强荧光发射和较长寿命的Eu-PS荧光微球。然而,该方法通常依赖于特定共聚单体、引发剂及复杂反应条件,制备过程较为繁琐且成本较高。
在MNPs荧光标记成功后,通过检测荧光信号可实现MNPs的可视化追踪、空间定位及浓度定量分析[26]。该技术不仅广泛应用于微塑料在环境介质(如水体)及生物组织中的可视化监测,还可结合拉曼光谱和气相色谱-质谱联用技术(GC-MS)等手段,对微塑料的成分进行进一步的定性与定量分析[27]。在成像分析层面,荧光标记的MNPs可通过荧光显微镜或激光共聚焦扫描显微镜进行高分辨率成像与颗粒计数,该方法具有较高的图像处理自动化程度与定量精度[28]。此外,荧光计和荧光光谱仪可用于实现MNPs的半自动定量检测,通过建立荧光强度与浓度之间的标准曲线,可实现对样品中荧光颗粒浓度的快速估算。进一步结合流式细胞仪技术,可实现单颗粒水平的多参数检测,能够高效地识别粒径分布、荧光强度以及颗粒表面特征,实现MNPs在复杂环境或生物样品中的精确识别与定量表征[28]。
1.2 影响荧光标记法效果的主要因素荧光标记法的标记效率受多种因素共同影响,包括所选荧光染料的类型、待标记MNPs的材质特性、染色过程中的温度与时间参数控制,以及样品杂质可能造成的背景干扰等。其中,荧光染料的类型是关键因素。染料与MNPs之间是否具备良好的亲和性及选择性结合能力,以及染料本身的荧光强度和光稳定性,均直接影响标记体系的灵敏度和可靠性。目前应用最广泛的三类荧光染料分别是荧光素及其衍生物(如FITC)、罗丹明类(如Rhodamine B、Rhodamine 6G)和尼罗红[29]。各类荧光染料的特性也决定了其应用的适用性。例如,荧光素类染料对环境中的pH较为敏感,且易发生光漂白;罗丹明类染料的发射波长会发生红移,这有利于与样品背景荧光进行区分,因此在复杂环境样品中表现出更高的信噪比。
在染料与MNPs发生特异性结合(即染色)过程中,标记效率受到多种实验参数的显著影响,影响因素包括染料浓度、染色时间、染色温度以及所选溶剂体系等。通常情况下,适当增加染料浓度与延长染色时间有助于提高荧光标记效果。然而有研究表明该趋势并非无限增长,Lü等[30]发现,当尼罗红浓度从0.1 μg·mL–1增加至25 μg·mL–1时,荧光强度呈递增趋势;但当浓度进一步升高至100 μg·mL–1时,荧光信号反而下降。此外,染料的聚集态荧光信号易被误识别为MNPs颗粒,或在显微成像中被滤光片错误拦截,从而干扰检测结果。并且荧光染料通常具有一定的极性,所以如果选择在非极性或中等极性溶剂(如丙酮、己烷、乙醇)或表面活性剂介质中进行标记,会使得染料更容易均匀分布于微塑料表面。
此外,染色效率还依赖于待标记聚合物的化学性质、几何形态与粒径特征等因素。这些因素直接影响聚合物在染色过程中的溶胀行为与染料渗透性。相同的有机染料对PC、PS的染色效率会较HDPE、PEST和PET的染色效率低,而且随着溶剂极性的增加,染色效率也会有所提升[31]。因为传统有机染料对于某些种类的塑料标记具有局限性,因此需要使用更有效的标记策略来突破局限。Hu等[32]的研究通过使用量子点荧光标记法对PET塑料瓶中释放到水体内的MPs进行标记,实现了对水瓶中MPs浓度的高灵敏度检测(百万分之一)。该研究中所使用的量子点标记手段不仅可以标记一些传统有机染料不容易标记的聚合物类型,还可以避免染色过程中发生的假阳性问题。
除了染料类型、染色条件及聚合物性质等因素外,环境条件在荧光标记法的实际应用中同样起着关键作用,尤其是在对复杂环境基质中的MNPs样品进行标记的情境下。在环境样品中进行荧光标记时,基质中的有机物质常常干扰染料与MNPs之间的特异性结合,显著影响标记的准确性与可靠性。例如,在使用亲脂性的荧光染料尼罗红进行染色时,环境介质中的脂类物质与生物残体可能与染料发生非特异性结合,进而产生假阳性信号。此外,研究发现尼罗红染料在复杂环境中存在显著的泄漏行为,其从已染色的微塑料表面脱附后可进一步吸附于环境中其他疏水性污染物上,从而造成错误标记与信号重叠[33]。正因如此,传统有机荧光染料标记方法在土壤—植物体系中的应用受限。这一体系中不仅存在着大量有机杂质的干扰,还有复杂的环境条件会加速染料的降解或失活,进一步影响染色稳定性与追踪持久性。已经有研究致力于解决这一问题,Feng等[34]评估了PMCN染料标记的微塑料在强酸/碱、冻融循环以及淡水和海水环境中的长期稳定性,并发现该染料在处理60天后仍可保持80%的荧光强度,因此该染料可用于水环境中微塑料的可视化标记,但是否可用于土壤-植物系统还需要进一步探究。
1.3 荧光标记法在MNPs可视化上的应用自尼罗红首次被用于对海洋环境中的微塑料进行直接荧光标记以来,其作为一种高效的荧光染料在MPs研究中的应用已被广泛认可。尤其自2019年起,尼罗红在研究微塑料定性与定量检测方面的使用次数显著增长,成为最常用的荧光染料之一[10]。然而,在实际应用中,尼罗红对环境样品中天然有机物的非特异性染色可能导致微塑料丰度的高估。例如,Shim等[35]研究发现,某些非塑料成分的颗粒在经消化但未完全去除有机物的情况下被尼罗红染色,导致标记过程出现了假阳性信号。为解决这一问题,有研究者引入了多重荧光染色策略以提高标记的特异性与准确性。例如,Tarafdar等[36]将尼罗红与卡尔科弗卢尔白(Calcofluor White)、埃文斯蓝和4',6-二脒基-2-苯基吲哚(DAPI)三种染料按比例混合,开发出一种水溶性复合蓝色染料,通过同时对样品中非塑料有机成分进行标记,可排除部分假阳性信号,提高了荧光标记的准确性。
为了进一步揭示MNPs在土壤—植物系统中的迁移路径、富集机制与空间分布特征,还需要对MNPs进行高效、稳定且尺度可控的标记。然而,传统有机荧光染料的标记分辨率主要集中在微米尺度,对纳米级颗粒的标记能力存在显著局限。针对该问题,已有研究尝试开发更为精准的标记策略。Nguyen和Tufenkji[37]利用被动吸附与热诱导溶胀法,将ATTO 647N染料负载至纳米塑料颗粒表面,使用受激辐射损耗显微镜(Stimulated Emission Depletion Microscopy,STED),将传统有机染料在可视化应用上的灵敏度提高到纳米级别。该研究对所标记的50 nm塑料小球进行了可视化观察,并进一步测试了染料在植物消化液环境(猪笼草)、土壤溶液、酸性条件(pH2.5的HCl溶液)和高温(40 ℃)等环境条件中的稳定性,发现染料在上述条件下的稳定性均可达21天以上。但值得注意的是,该方法仍存在荧光信号易受光漂白影响的问题,限制了其在更长时间追踪中的应用。
为克服这一限制,近年来兴起的聚集诱导发光染料(Aggregation Induced Emission,AIE)因具有高荧光量子产率、良好的光稳定性与低自猝灭特性等特点[38-40],已开始被尝试用于MNPs标记示踪研究。AIE具有在固态或高浓度溶液中强烈发光,而在稀溶液中却不发光的特性。这一特性使其不仅有效避免了荧光淬灭现象的发生,还支持长波长激发及近红外激发条件下的成像应用[40]。Wang和wang[41]基于AIE染料对环境相关浓度(50 μg·L–1)下微/纳米塑料(200 nm和20 μm)在大型水蚤肠道中的富集行为进行了活体成像研究,借助AIE染料优异的组织穿透能力,成功实现了NPs(200 nm)在生物体内的动态可视化和在低至50 μm·L–1NPs暴露浓度下的定量化分析。Yang等[42]进一步将AIE技术应用于斑马鱼模型,探究其体内MNPs的聚集行为,研究表明AIE荧光信号在组织中可穿透达4 mm,展现出优越的活体成像深度。此外,AIE探针在日常光照下连续曝光96 h后还具有优异的光稳定性,这说明AIE技术克服了传统有机染料会发生光漂白的技术难点。综上,AIE技术不仅拥有强大的抗荧光淬灭能力,还有较强的组织穿透性,这为复杂环境生物体系中MNPs的示踪研究提供了新技术。若将AIE染料引入土壤—植物体系,有望实现复杂体系中MNPs的高灵敏度、深穿透标记与成像。
综上,尽管荧光标记法在识别和追踪复杂体系中的MNPs方面已展现出良好的应用前景,但其标记效果受多种因素制约,尤其是在复杂环境条件下的稳定性问题尚未完全解决。该标记法仍在不断发展和优化中。AIE技术标记物所激发的发射波长穿透性强,且具有较强的抗背景干扰能力,因此在动植物活体成像方面具有很大的发展潜力和应用前景。
2 金属标记法金属标记法最初被开发用于定量分析环境中MNPs,尤其是纳米塑料(NPs)的分布行为与迁移路径[43]。借助电感耦合等离子体质谱(ICP-MS)等对金属元素高度敏感的分析技术,可间接实现对MNPs的追踪与定量分析,因此在当前MNPs研究中展现出广阔的应用前景。
2.1 金属标记法的原理金属标记法是一种通过在MNPs表面吸附或在其内部包埋金属元素,实现标记和检测的技术。根据标记方式的不同,金属标记法主要分为三种类型:金属表面标记法、高温掺杂金属法和金属核心标记法(图 2)。
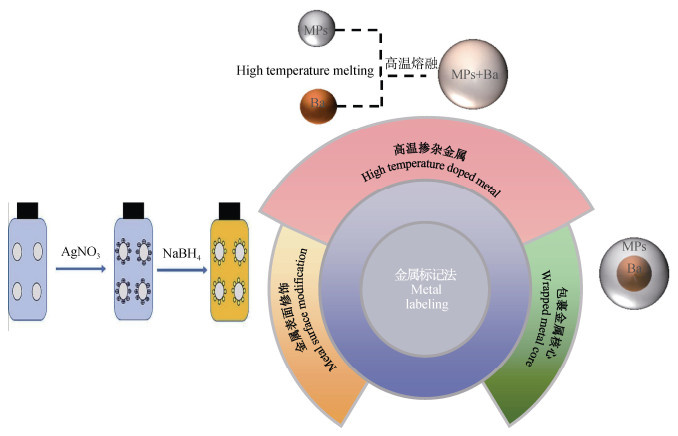
|
图 2 微/纳米塑料的金属标记技术常用方法[44] Fig. 2 Common methods of metal labelling techniques for MNPs |
金属表面标记法通常利用静电相互作用将金属颗粒物理吸附到MNPs表面。为增强MNPs与金属元素的相互作用,研究者通常会对金属颗粒或MNPs表面进行改性处理[28]。其中,银(Ag)纳米颗粒由于其可增强拉曼散射信号的特性而在MNPs表面修饰中的应用备受关注。例如,Zhao等[44]通过在MNPs表面附着Ag+并进行原位还原,成功实现了Ag纳米颗粒对其表面的修饰,并可借助电化学方法对MNPs浓度进行定量表征。但是由于金属表面标记的方法有众多环境因素都会干扰检测,因此在实际应用中需进行前处理,如采用浊点萃取等手段以提升检测的灵敏度和准确性[45]。
金属核心标记法由Mitrano等[43]提出,其核心原理是在单分散体系中首先合成金属核心,随后通过表面交联聚合形成塑料外壳,从而实现标记。另一种方法—高温掺杂金属法,则通过在高温条件下将金属元素均匀掺杂进塑料基体中,实现金属与塑料的稳定结合[46]。目前,钯(Pd,n=10)是最常用于MNPs标记的金属元素,其次依次为铟(In,n=5)、金(Au,n=3)、铕(Eu,n=2)、银(Ag,n=1)、铁(Fe,n=1)以及铂(Pt,n=1)[29]。
如图 3,金属标记法研究MNPs的流程一般包括金属标记MNPs的合成以及金属标记MNPs的检测与表征。其中对MNPs的检测与表征主要依赖于对MNPs所结合金属元素的分析,这一分析过程通常需要对MNPs进行酸消解处理,因此无法保留其原始形貌信息;而借助激光剥蚀电感耦合等离子体质谱仪(LA-ICP-MS)则可实现对金属标记MNPs空间分布的表征[47]。
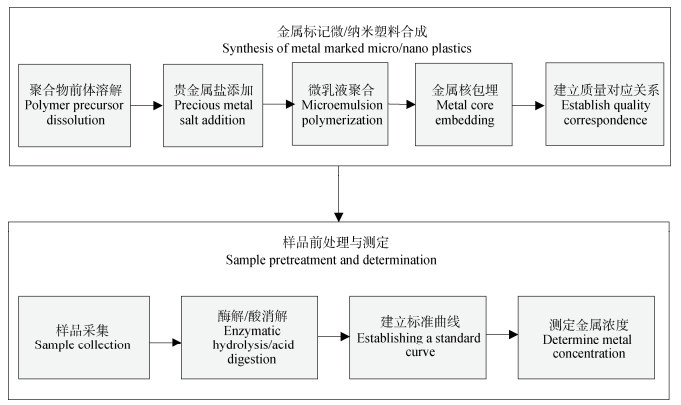
|
图 3 微/纳米塑料金属标记法定量分析流程 Fig. 3 Quantitative analysis flow of micro/nano plastic metal labeling method |
金属标记技术的标记效率受多种因素影响,包括所选金属的种类、粒度、标记浓度以及探测器对金属的响应灵敏度等。因此,为了获得可靠的定量分析结果,需要选择环境中浓度较低、探测器灵敏度高的金属元素作为标记。此外,MNPs的合成温度也是影响标记效果的重要因素。理想情况下,应将合成温度保持在材料玻璃化转变温度(Tg)以下,以确保MNPs的结构完整性。然而,由于具体合成工艺存在差异,实际使用的温度范围可从60℃[43]至300℃[46]不等。
一般而言,基于金属元素表面修饰的标记方法与荧光标记法具有相似的局限性,例如在复杂环境中稳定性差、易受基质干扰等。相比之下,采用金属核心包裹MNPs的标记方法,能够在土壤等复杂环境基质中实现长期稳定存在,并展现出更为可靠的定量分析能力。此外,该方法还可实现对多种MNPs的统一金属标记,从而提升方法的适用性与研究效率[43]。
2.3 金属标记法在MNPs定量研究方面的应用金属标记法已广泛用于定量分析环境中MNPs的浓度。Zhao等[44]研究表明,在AgNO3溶液中使Ag+附着在带负电的PS纳米塑料(100 nm、367 nm、500 nm)上,可通过硼氢化钠将微塑料表面的Ag+还原并产生Ag纳米颗粒。该研究通过这一原理在纯溶液体系中建立了电化学定量分析MNPs浓度的检测方法,并对湖泊和海水等实际水环境中的MNPs样品进行了检测,检测限仅为0.05 mg·mL–1,但并不能满足低浓度MNPs的定量分析需求。这也体现了表面附着金属标记法灵敏度不足的局限性。相较而言,高温掺杂和包裹金属核心(Au、Pd等)的标记方法对MNPs浓度的定量更为精确。例如,Frehland等[46]使用Pd作为金属核心制备了核壳结构的纳米PS小球(100 nm),并利用电感耦合等离子体质谱(ICP-MS)检测标记金属的浓度,从而间接获得污水中MNPs的含量。使用这一方法可精准定量0.05 μg·L–1浓度的纳米PS小球。此外,该研究也对金属标记物的稳定性进行了检测,证实了在去离子水中振荡60天后,所标记的Pd并没有从小球中发生明显的溶出。除了具备较高的稳定性,金属标记法还可用于表征低浓度MNPs在动植物体内的空间分布特征。例如,Du等[48]利用金元素为核心制备的核壳结构纳米塑料,对0.2 mg·L–1浓度NPs(100 nm)暴露下海洋双壳类生物NPs的摄入和分布情况进行了研究,并利用ICP-MS对生物体内低至0.3 μg·L–1的NPs进行了精准的定量分析,为生物体内MNPs研究提供了更具说服力的数据支持,也验证了金属核心标记法更高的灵敏度。Marigliano等[49]比较了金属离子表面吸附、金属有机化合物表面修饰以及纳米金属核心标记3种方法,发现纳米金属核心标记法相较另两种标记方法展现出更高的灵敏度和更强的抗干扰能力。鉴于金属标记法的长期稳定性及与MNPs之间稳定的定量关系,目前主要被应用于污水环境中微/纳米塑料的定量与生物体内微/纳米塑料的示踪分析。金属标记法与荧光标记法等其他标记手段共同标记可同步实现可视化与定量化示踪,这将是金属标记法未来的发展方向之一。
3 同位素标记法同位素标记法是一种通过将化合物中的特定元素替换为其同位素形式,从而实现对目标物质示踪的技术手段。如图 4所示,根据同位素类型的不同,该方法可分为稳定同位素标记法(如13C、15N)和放射性同位素标记法(如14C、64Cu)。
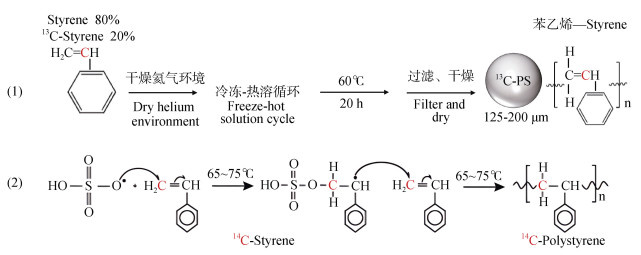
|
图 4 同位素标记PS合成方法 Fig. 4 Isotope-labeled PS synthesis method |
在检测方式上,稳定同位素依赖质谱分析,而放射性同位素则基于放射性信号检测,尽管存在差异,但其核心原理均是通过同位素在质量或放射性特征上的差异实现对MNPs的高特异性追踪[28]。
3.1 稳定同位素标记法稳定同位素标记法是一种通过使用稳定同位素对MNPs进行标记的示踪技术。目前,13C是应用最广泛的稳定同位素,用于标记MNPs,以精确追踪其在环境中的行为[50]。该方法能提供MNPs的空间分布、迁移路径及降解过程的详细信息。由于稳定同位素信号具有高度稳定性和特异性,该方法在揭示MNPs的环境行为及其降解机制方面表现出显著优势。
3.1.1 稳定同位素标记法的原理稳定同位素标记方法是通过在MNPs聚合过程中将聚合物结构中的特定元素替换为其稳定同位素来实现标记。这种替换会引起目标元素的质量变化,从而使标记物能够通过质谱等分析技术与未标记物区分开来,实现对聚合物及其代谢产物的高精准追踪。例如,在聚合反应中,可通过使用含不同丰度的同位素标记单体来代替普通单体,从而合成稳定同位素标记的塑料材料[50]。以碳-13(13C)标记为例,Mauel等[51]通过自由基聚合反应,将80%的普通苯乙烯与20%的13C标记苯乙烯混合,成功合成了13C标记的微塑料(MPs)。随后,可通过同位素比质谱仪获取MNPs中碳元素及其同位素的分布特征,并通过定量检测其降解产物(如13CO2)进一步分析其降解过程。例如,13CO2的释放量可直接反映MNPs的矿化程度,而13C在中间降解产物中的分布特征则有助于解析其降解路径。总体而言,稳定同位素标记技术不仅可提供MNPs降解行为的定量信息,还能深入揭示其所经历的化学过程,为评估其在复杂环境中的归趋和生态风险提供强有力的研究工具。
稳定同位素标记可借助质谱分析技术实现高精度分析表征。在同位素标记的样品中,由于稳定同位素与天然同位素存在质量差异,所形成的离子峰在质谱图中表现为不同的m/z值,从而实现标记物的鉴定与定量分析。对于13C标记的MNPs,其定量分析通常采用以下方法:(1)气相色谱-质谱联用(GC-MS):通过分离并检测标记降解产物(如13CO2),用于评估MNPs的降解程度;(2)元素分析(EA):测定样品中碳元素总量与13C的相对丰度,提供定量信息;(3)同位素比质谱(IRMS):通过测量δ13C值,精确计算13C标记物与天然同位素的比值,进而推算出标记物的浓度[50-52]。
此外,纳米级二次离子质谱法(NanoSIMS)可实现高空间分辨率下元素及同位素分布的可视化,有助于揭示MNPs在微观尺度上的迁移与分布行为[52]。与荧光标记相比,稳定同位素标记在复杂环境中具有显著的长期稳定性,信号不会随时间衰减。例如,通过气相色谱-气体同位素质谱联用仪(GC-IRMS)或13C同位素光腔衰荡光谱(CRDS)技术,可实时监测降解过程中释放的13CO2,从而精确追踪其矿化过程及降解动力学。这些先进手段为MNPs在环境中的归趋及其生态影响研究提供了强有力的技术支撑。
3.1.2 稳定同位素标记法的影响因素在环境样品中,天然有机物常包含一定比例的13C等天然同位素,其背景信号可能干扰13C标记的MNPs的检测,这种干扰的程度受标记丰度及样品中天然同位素浓度的共同影响。因此,在某些复杂基质或天然同位素浓度较高的条件下,为确保定量结果的准确性,需要对实验数据进行一定的校准处理[53]。不仅如此,示踪剂的选择和样品的纯化步骤也是获得可靠数据的重要影响因素[54]。
3.2 放射性同位素标记法早期的研究主要集中于将放射性同位素标记应用于聚合物材料或大塑料(> 5 cm),以探究其生物降解行为。近年来,随着研究重心逐渐转向MNPs,放射性同位素标记技术在该领域的应用也逐渐受到关注[55]。由于其独特的稳定性、高灵敏度、准确性及检测效率,该技术在MNPs环境行为与生态风险评估研究中展现出巨大的潜力。例如,14C标记的PS小球和64Cu标记的PE小球已被成功用于追踪MNPs在环境介质及生物体内的分布与降解过程。这些研究不仅揭示了MNPs的迁移路径和矿化行为,也为其生态风险评估提供了重要数据支持[56]。随着标记技术的不断进步,放射性同位素标记技术有望成为MNPs的环境归趋研究的重要工具。
3.2.1 放射性同位素标记法的原理放射性同位素标记法是通过将MNPs聚合物中的特定元素替换为放射性同位素,实现对其环境行为的高灵敏度追踪。然而,放射性同位素材料的合成、使用及检测需遵循严格的监管规定,且放射性单体价格较高,同时实验操作依赖专用设备(如液体闪烁计数仪、正电子发射断层扫描仪等),因此目前相关研究仍较为有限。已有报道中,14C(n=4)和64Cu(n=2)为常用的标记同位素,分别应用于PS和PE等常见MNPs的研究中[28]。
在合成方面,14C标记MNPs通常通过自由基聚合反应制备,例如使用14C标记的苯乙烯或乙烯单体,可制备出粒径最小达20 nm的纳米塑料[55]。64Cu标记的微塑料(MPs)通常通过化学螯合作用实现:将氨基引入塑料表面后,与1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸(DOTA)形成C–N键,再通过DOTA螯合64Cu,最终合成最小尺寸为10 μm的标记微塑料[56]。
通过检测标记物质的放射性(如液体闪烁计数法或正电子发射断层扫描),可获取MNPs中目标元素及其同位素的空间分布信息,并揭示其降解行为。例如,释放的14CO2量可直接反映MNPs的矿化程度;而64Cu信号可用于追踪MNPs在生物体内的吸收、富集与迁移路径[55-56]。尽管放射性标记法具有极高的灵敏度与特异性,但其推广仍受限于成本、设备条件和辐射安全规范,未来需进一步优化技术体系以降低门槛并扩大研究范围。
放射性同位素标记的样品会发射特定类型的辐射(如β粒子或γ射线),通过检测这些粒子/射线的能量与强度,可精确确定标记物的浓度与空间分布。常用的检测设备包括闪烁计数器、气体电离探测器和半导体探测器,具有较高的灵敏度与定量能力[28]。此外,放射性标记样品还可借助直接成像技术实现空间分布可视化[57]。例如,同位素放射自显像可用于二维平面成像,而正电子发射断层扫描(PET成像)和计算机断层扫描则能够实现三维空间的高分辨率成像。成像完成后,结合ImageJ等图像分析软件计算放射性标记物的浓度,以及合成过程中已知的标记丰度,可将放射性信号转化为MNPs的绝对浓度[58]。这些手段不仅能够提供MNPs的高精度定量数据,还可动态揭示其在复杂环境或生物系统中的行为模式,为评估MNPs的环境归趋及生态影响提供重要支持。
3.2.2 放射性同位素标记法的影响因素放射性同位素的半衰期是决定标记稳定性和适用性的关键物理参数。在选择放射性同位素标记技术时,需综合考虑其衰变特性、半衰期及与之匹配的检测手段。例如,PET成像是一种非侵入性、高灵敏度的成像技术,能够实时、动态监测生物体内放射性示踪剂的行为。PET成像基于β⁺衰变原理,而64Cu的β⁺发射能量(653 keV)显著高于14C(156.5 keV),因此在PET成像中表现出更高的检测灵敏度和空间分辨率,适用于医学诊断和生物体内MNPs的示踪研究[59]。相比之下,14C具有更长的半衰期(约5730年)并可追踪更多土壤—植物系统中的化学过程,因此更适合土壤—植物体系中的研究[60]。在实际应用中应根据研究目标(如短期体内迁移追踪或长期环境稳定性分析)选择合适的放射性同位素及成像技术,以保障标记的稳定性及检测结果的可靠性。
3.3 同位素标记法在MNPs参与的化学过程研究中的应用同位素标记法已成为研究MNPs降解行为的关键技术,可用于揭示底物分解、降解中间体生成、生物量同化及CO2释放等重要过程。目前,多数研究采用13C和14C同位素,使用气相色谱质谱法(GC-MS)以及同位素比质谱仪(IRMS)估算塑料碳的去向及其转化比例[60]。
为进一步阐明聚合物的降解机制,可在单体结构中进行位置选择性标记。例如,Yang等[61]利用全13C标记的PS,研究了黄粉虫对其苯环(α位)和主碳链(β位)的分解与矿化机制。Zumstein等[62]通过分别在PBAT的三个组成单体——丁二醇、己二酸酯和对苯二甲酸酯——中进行13C标记,揭示了各单体的降解路径及微生物代谢转化情况。此外,稳定同位素探测(SIP)技术能够追踪13C标记碳进入微生物生物量并参与代谢,拓展了人们对塑料在真实环境中生物利用机制的理解。
同位素示踪技术还具备空间定位与成像能力。例如,Zumstein等[62]利用NanoSIMS成像,在PBAT膜表面定位检测到13C标记区域,成像面积为45 µm×45 µm至70 µm×70 µm。结果显示,生物定殖区域的13C丰度显著高于背景水平(6 at% vs 1.076 at%),证实了土壤微生物对PBAT的降解活动。然而,NanoSIMS在分析过程中可能因原子混合、溅射或沉积导致空间分布精度下降,从而影响定量结果的准确性。
当前研究多基于实验室条件下未嵌入环境基质的纯标记塑料,背景干扰较小。然而,在自然环境中,MNPs浓度通常较低、降解性弱,且易受复杂基质及环境条件(如土壤、有机质含量、根系分泌物等)的影响,追踪其降解行为面临更大挑战。未来需要在样品的前处理过程中实现突破,以高效排除自然环境中多种复杂因子的干扰,显著提升同位素示踪法在实际土壤—植物系统中的应用潜力。
4 稀土元素标记法稀土元素标记法是一种利用稀土金属元素,如铕(Eu3+)、铽(Tb3+)、钐(Sm3+)等作为示踪剂,通过其独特的荧光性质进行高灵敏度分析的技术[63]。该方法的核心之一在于稀土元素的独特光学特性,如长荧光寿命、窄发射光谱、大斯托克斯位移等,这些特性有效提升了检测的灵敏度和抗背景干扰的能力。此外,稀土元素标记法使用环境中浓度较低的稀土元素作为标记物,可结合ICP-MS对MNPs进行精准定量。作为可同时实现MNPs可视化和精准定量的标记方法,稀土元素标记法在土壤—植物体系下MNPs的研究中具有巨大的应用潜力和价值。
4.1 稀土元素标记法的原理稀土元素的发光主要来源于其4f轨道电子的d-f跃迁,这种跃迁在特定波长下发射特征性光子,形成可被精确探测的荧光信号[64]。在实际应用中,稀土离子通常通过与有机配体形成稳定配合物实现功能化标记。以Eu3+为例,其斯托克斯位移可达290 nm,显著减小了激发光散射对发射信号的干扰;其荧光寿命可达毫秒级,远超传统荧光染料的纳秒级寿命,从而适用于时间分辨荧光技术(TRF),提高检测的时间分辨率与信噪比[65]。
通过将稀土标记探针与目标分子特异性结合,可实现高选择性和高灵敏度的分析。除荧光检测外,稀土元素还可作为金属标记物通过电感耦合等离子体质谱(ICP-MS)进行高灵敏度检测,适用于MNPs的定量分析。在实际操作中,可通过溶胀法将稀土离子有效嵌入MNPs中,实现对其在环境介质中的迁移路径、积累特征及生物可利用性的可视化和定量表征[66]。
4.2 稀土元素标记法的影响因素稀土元素因其独特的光学性质,在生物标记和成像领域中展现出显著优势,但其在实际应用中仍面临一定的挑战。首先,稀土离子的发光特性受激发方式影响较大。稀土离子常见的激发模式包括化学发光、电致发光和光致发光。其中,化学发光和电致发光的量子效率较低,这主要是因为在它们提供和传递能量的过程中会消耗大量能量,而光致发光可为稀土元素精准供能,且具有发光效率高、发射峰窄和寿命长等优势,因此光致发光的激发模式在多种应用中被广泛采用[67]。
其次,标记过程中的pH也会大大影响标记效率,当pH较低时,H+会与稀土离子竞争螯合剂上的配位点,导致标记效率低下。当pH过高时,稀土离子又会发生水解产生沉淀,同样影响标记过程的效率。因此,在使用稀土离子进行标记的过程中,一定要将反应体系的pH控制在弱酸性到中性的范围内,才能达到较好的标记效果[68]。
最后,稀土离子具有较小的摩尔吸光系数(<10 L·mol–1·cm–1=以及4f-4f跃迁的禁阻作用,导致激发能量难以直接作用于稀土中心离子[69-71]。由于发光强度与吸收能力及量子产率正相关,这一弱吸收机制限制了稀土荧光的实际应用。为克服上述问题,“天线效应”或称敏化机制被广泛采用。该机制通过引入强吸收能力的配体(天线分子),增强能量吸收并高效传递给稀土离子,从而显著提升发光强度。早在1942年,Weissman[68]即发现Eu3+与β-二酮配位后,在紫外激发下能显著增强其特征性窄带发射。此后,大量研究围绕稀土–配体复合物展开。例如,Cortecchia等[72]在研究Eu3+掺杂的层状钙钛矿NMA2PbBr4与β—二酮酸配体复合体系中,利用萘基官能化阳离子(NMA=1-萘基甲基铵)实现了Eu3+的直接敏化。配体不仅提供理想的配位几何结构以促进能量转移,还使发光效率提高近30倍。该过程中,配体的吸收能力、配体到金属的能量转移效率及金属中心的辐射效率三者协同决定了发光性能[73]。此外,可通过调整稀土离子种类或其比例实现发射颜色的调控。稀土离子的发光波段覆盖广泛,从紫外区、可见光区(400~800 nm)直至近红外区(NIR,800~1700 nm),其中Eu3+(红光)、Tb3+(绿光)、Sm3+(橙色光)、Tm3+(蓝光)和Dy3+(白光或接近白光)在可见光区域发光,而Pr3+、Nd3+、Sm3+、Dy3+、Ho3+、Er+、Tm3+、Yb3+等则能发射近红外光[74-77]。因此,稀土元素可根据发射波长设计为多色荧光探针,为多重成像与多参数检测提供丰富支持[78]。同时,如果改变配体的结构或电子特性,也可调节荧光强度和波长,实现在不同功能场景下的定制化发光性能[71,79-80]。
4.3 稀土元素标记法在土壤—植物体系中MNPs定量化示踪研究中的应用近年来,利用稀土元素标记法在土壤—植物系统中开展MNPs的示踪与量化研究取得了突破性进展。Luo等[81]使用稀土元素镧系螯合物Eu(TTA)3(噻吩甲酰三氟丙酮)作为双功能示踪剂,成功标记了0.2 μm粒径的PS塑料。该实验在模拟植物细胞环境(2.5 mM CaNO3、1 mM MgSO4、2.5 mM KNO3、0.1 mM K2HPO4、5 mM NaCl、50 μM葡萄糖、25 μM草酸、12.5 μM丝氨酸、5 μM铁叶绿酸钠)下进行了Eu-PS稳定性实验,在6天的实验周期中,Eu(TTA)3未从被标记的PS微球向溶液中产生明显的溶出。该研究利用稀土配合物的时间分辨荧光特性实现了对植物(小麦和生菜)中吸收积累的PS-Eu颗粒的准确可视化追踪,并进一步通过ICP-MS检测了5 μg·L–1浓度PS小球暴露下蔬菜和作物体内的Eu含量,间接量化分析了生菜和小麦对PS-Eu颗粒的吸收和转运量。通过此方法,可对接近微/纳米塑料环境浓度暴露下植物吸收积累量进行量化分析。基于稀土配合物掺杂标记的方法克服了微/纳米塑料颗粒传统荧光标记方法存在的背景荧光干扰、染料易泄漏、难以同时进行精确定量等缺点,为微/纳米塑料颗粒在复杂生物介质中积累、传输和分布提供了一种崭新、简便、通用的研究方法。这将有助于全面理解和认识微/纳米塑料在生物体内的吸收过程与机制,也可为定量评估微/纳米塑料的生态和食物链传递风险奠定方法学基础并提供科学依据。Li等[82]采用Eu3+标记30 nm的PS微球,通过可视化手段成功揭示了其通过叶片气孔进入植物体内,并沿质外体通道向维管组织迁移,最终在毛状体中富集的叶面吸收转移路径。这进一步拓展了稀土标记法在真实环境暴露条件下的应用场景。
表 1对稀土标记及其他几种标记技术的一系列特点进行了比较。荧光标记法主要适用于微纳塑料的可视化研究,可视化的灵敏度可达50 nm粒径,如果选用较为稳定的染料,也可使荧光标记的稳定性达到21天以上[37];金属标记法则在定量研究和稳定性上有所突破,能够实现0.3 μg·L–1微塑料的定量化分析,并在水环境中稳定存在2个月以上[43];同位素标记法则在特异性上尤为突出,能够追踪微纳塑料的降解行为,稳定同位素标记法在环境中也十分稳定;而稀土标记法不仅可同时实现微/纳米塑料的可视化和定量分析,而且定量的灵敏度可达到5 μg·L–1,也能够在细胞环境中稳定存在6天以上[81]。
|
|
表 1 各种标记方法的优缺点比较 Table 1 Comparison of advantages and disadvantages of various marking methods |
综合比较下,稀土元素标记法在土壤-植物系统中微/纳米塑料的示踪与定量研究方面展现出显著的优势,包括高灵敏度可视化能力、定量分析的高准确性、优异的环境稳定性,以及良好的多功能性与适应性,是未来土壤-植物系统中MNPs环境行为与生态效应研究中值得重视和发展的关键技术。
5 结论与展望本文系统总结了荧光标记法、金属标记法、稳定同位素标记法、放射性同位素标记法和稀土元素标记法等几种主要的MNPs标记方法的主要原理、适用范围和应用案例。目前,这些标记技术在应用于土壤—植物系统中的MNPs研究时,往往是通过预先标记MNPs来实现的。但无论何种标记方式,往往都可能对MNPs的理化性质产生影响,进而使研究结果与环境中真实MNPs所产生的效应存在一定的差异。因此,未来土壤—植物系统中MNPs的标记技术发展应重点关注以下几个方面:
(1)研发新型标记物:探索更多多功能的新型标记物,让被标记的MNPs能够提供更多维度的信息,推进土壤—植物体系中MNPs研究的进一步深入。(2)发展多标记物混合标记技术:多种标记物混合标记可提高标记的特异性,降低假阳性的干扰,在荧光标记中使用合适的多种标记物共同标记可提高标记效率。(3)降低标记物泄漏风险:荧光标记、金属标记和稀土标记技术都具有易在环境和生物体内风化降解时产生标记物泄漏的风险,未来可通过筛选结构更稳定的标记物、研发键合更牢固的标记技术,以降低标记物的泄漏风险,提高标记技术的精准性和高效性。(4)建立真实环境中MNPs标记效果的评估体系:建立一套科学有效的评估体系,对真实环境中的MNPs经标记后的理化性质进行系统科学的评估,以确保标记技术在土壤-植物系统中迁移转化和生态效应研究的精准、高效、灵敏和便捷。
| [1] |
Plastic Europe. "Plastics-the facts 2024. " [R/OL]. (2024-11-18)[2025-08-20]. https://plasticseurope.org/knowledge-hub/plastics-the-fast-facts-2024/.
(  0) 0) |
| [2] |
de Souza Machado A A, Kloas W, Zarfl C, et al. Microplastics as an emerging threat to terrestrial ecosystems[J]. Global Change Biology, 2018, 24(4): 1405-1416. DOI:10.1111/gcb.14020
(  0) 0) |
| [3] |
Wang J, Zhu Z Y, Sun L J, et al. The bridging role of soil organic carbon in regulating bacterial community by microplastic pollution: Evidence from different microplastic additions[J]. Journal of Hazardous Materials, 2025, 490: 137761. DOI:10.1016/j.jhazmat.2025.137761
(  0) 0) |
| [4] |
Yang J, Li L Z, Zhou Q, et al. Microplastics contamination of soil environment: Sources, processes and risks (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 281-298. DOI:10.11766/trxb202006090286 [杨杰, 李连祯, 周倩, 等. 土壤环境中微塑料污染: 来源、过程及风险[J]. 土壤学报, 2021, 58(2): 281-298.]
(  0) 0) |
| [5] |
Jiang X F, Chen H, Liao Y C, et al. Ecotoxicity and genotoxicity of polystyrene microplastics on higher plant Vicia faba[J]. Environmental Pollution, 2019, 250: 831-838. DOI:10.1016/j.envpol.2019.04.055
(  0) 0) |
| [6] |
Chen C C, Zheng N, Zhu H C, et al. Polylactic acid microplastics and earthworms drive cadmium bioaccumulation and toxicity in the soil–radish health community[J]. Journal of Hazardous Materials, 2025, 493: 138391. DOI:10.1016/j.jhazmat.2025.138391
(  0) 0) |
| [7] |
Hong W T, Li Z Y, Wu F, et al. Toxicology of nanoplastics to aquatic and terrestrial organism: A critical review (In Chinese)[J]. Environmental Science, 2025, 46(3): 1868-1884. [洪文涛, 李振宇, 吴帆, 等. 纳米塑料对水生与陆生生物的毒理研究进展[J]. 环境科学, 2025, 46(3): 1868-1884.]
(  0) 0) |
| [8] |
Li Z X, Li Q F, Li R J, et al. The distribution and impact of polystyrene nanoplastics on cucumber plants[J]. Environmental Science and Pollution Research, 2021, 28(13): 16042-16053. DOI:10.1007/s11356-020-11702-2
(  0) 0) |
| [9] |
Yang X X, Zhang X M, Shu X, et al. Toxic effects and interaction evaluation of polyethylene microplastics and cadmium combined exposure on earthworm Eisenia fetida (In Chinese)[J]. Acta Scientiae Circumstantiae, 2024, 44(7): 482-496. [杨晓霞, 张雪梅, 舒晓, 等. 聚乙烯微塑料与镉联合暴露对赤子爱胜蚓的毒性效应及交互作用评估[J]. 环境科学学报, 2024, 44(7): 482-496.]
(  0) 0) |
| [10] |
Desforges J W, Galbraith M, Dangerfield N, et al. Widespread distribution of microplastics in subsurface seawater in the NE Pacific Ocean[J]. Marine Pollution Bulletin, 2014, 79(1/2): 94-99.
(  0) 0) |
| [11] |
Liu L, Li L Z, Chen Z K, et al. Corn seedlings can absorb and accumulate fiber microplastics (In Chinese)[J]. Acta Pedologica Sinica, 2026, 63(2). DOI:10.11766/trxb202412200497 [刘璐, 李连祯, 陈浙宽, 等. 玉米幼苗能吸收和积累纤维微塑料[J]. 土壤学报, 2026, 63(2).]
(  0) 0) |
| [12] |
Xu X Y, Hou Z A, Ye J. Effect of organic fertilizers on enrichment of polystyrene nanoplastics in cotton plants [J/OL]. Environmental Science, https://doi.org/10.13227/j.hjkx.202501276.[许晓雨, 侯振安, 冶军, 等. 有机肥对聚苯乙烯纳塑料在棉花植株体内富集的影响[J/OL]. 环境科学, https://doi.org/10.13227/j.hjkx.202501276.]
(  0) 0) |
| [13] |
Batel A, Borchert F, Reinwald H, et al. Microplastic accumulation patterns and transfer of benzo [a] Pyrene to adult zebrafish(Danio rerio)gills and zebrafish embryos[J]. Environmental Pollution, 2018, 235: 918-930. DOI:10.1016/j.envpol.2018.01.028
(  0) 0) |
| [14] |
Zhang X Y, Ren S M, Han T W, et al. New organic–inorganic hybrid polymers as Pickering emulsion stabilizers[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2018, 542: 42-51.
(  0) 0) |
| [15] |
Sun L J, Qiu T, Liu J X, et al. Layer-by-layer fabrication of fluorescent microspheres using micelles as a spacer: Simultaneously realizing fluorescence enhancement and introduction of bioconjugation sites[J]. Journal of Materials Chemistry B, 2018, 6(5): 789-796. DOI:10.1039/C7TB02881D
(  0) 0) |
| [16] |
Li W, Jiang C, Lu S, et al. A hydrogel microsphere-based sensor for dual and highly selective detection of Al3+ and Hg2+[J]. Sensors and Actuators B: Chemical, 2020, 321: 128490. DOI:10.1016/j.snb.2020.128490
(  0) 0) |
| [17] |
Bian Y F, Leng X F, Wei Z Y, et al. End-chain fluorescent highly branched poly(L-lactide)s: Synthesis, architecture-dependence, and fluorescent visible paclitaxel-loaded microspheres[J]. Biomacromolecules, 2019, 20(10): 3952-3968. DOI:10.1021/acs.biomac.9b01020
(  0) 0) |
| [18] |
Yang J, Lin Z Z, Huang Z Y. Rapid detection of trace malachite green using a fluorescence probe based on signal amplification through electrostatic self-assembly of CdTe QDs and polystyrene microsphere[J]. Marine Pollution Bulletin, 2020, 151: 110812. DOI:10.1016/j.marpolbul.2019.110812
(  0) 0) |
| [19] |
Jiang X B, Yan S Q, Sun H, et al. Preparation of fluorescent polyurethane microspheres and their applications as reusable sensor for 4-nitrophenol detection and as microplastics model for visualizing polyurethane in cells and zebrafish[J]. Journal of Colloid and Interface Science, 2024, 673: 550-563. DOI:10.1016/j.jcis.2024.06.070
(  0) 0) |
| [20] |
Bretler S, Marger S. Synthesis and characterization of new spiropyran micrometer-sized photochromic fluorescent polymeric particles of narrow size distribution by a swelling process[J]. Polymer, 2015, 61: 68-74. DOI:10.1016/j.polymer.2015.01.068
(  0) 0) |
| [21] |
Delafresnaye L, Hooker J P, Schmitt C W, et al. Chemiluminescent read-out of degradable fluorescent polymer particles[J]. Macromolecules, 2020, 53(14): 5826-5832. DOI:10.1021/acs.macromol.0c00722
(  0) 0) |
| [22] |
Liu M, Cai Z E, Xu Y, et al. Europium(Ⅲ)-based fluorescent microspheres with styrene copolymerization toward an enhanced photoluminescence performance[J]. ACS Applied Polymer Materials, 2022, 4(11): 8109-8117. DOI:10.1021/acsapm.2c01075
(  0) 0) |
| [23] |
Zhang L J, Mehreen T, Liu X Y, et al. Wide-gamut blended conjugated polymer microspheres[J]. Advanced Optical Materials, 2021, 9(24): 2101788. DOI:10.1002/adom.202101788
(  0) 0) |
| [24] |
Wang G, Zhou L Y, Zhang P F, et al. Fluorescence self-reporting precipitation polymerization based on aggregation-induced emission for constructing optical nanoagents[J]. Angewandte Chemie: International ed, 2020, 59(25): 10122-10128. DOI:10.1002/anie.201913847
(  0) 0) |
| [25] |
Liu S D, Shang E X, Liu J N, et al. What have we known so far for fluorescence staining and quantification A tutorial review[J]. Frontiers of Environmental Science & Engineering, 2022, 16(1): 8.
(  0) 0) |
| [26] |
Zhang L, Xue M Y, Xin Q, et al. Cellular uptake of polystyrene nanoplastics with surface Functionalization: An AIE-based quantitative approach[J]. Analytica Chimica Acta, 2025, 1362: 344184. DOI:10.1016/j.aca.2025.344184
(  0) 0) |
| [27] |
El Hayany B, El Fels L, Quénéa K, et al. Microplastics from lagooning sludge to composts as revealed by fluorescent staining- image analysis, Raman spectroscopy and pyrolysis-GC/MS[J]. Journal of Environmental Management, 2020, 275: 111249. DOI:10.1016/j.jenvman.2020.111249
(  0) 0) |
| [28] |
Liu Y, Li J, Parakhonskiy B V, et al. Labelling of micro- and nanoplastics for environmental studies: State-of-the-art and future challenges[J]. Journal of Hazardous Materials, 2024, 462: 132785. DOI:10.1016/j.jhazmat.2023.132785
(  0) 0) |
| [29] |
Bauten W, Nöth M, Kurkina T, et al. Plastibodies for multiplexed detection and sorting of microplastic particles in high-throughput[J]. Science of the Total Environment, 2023, 860: 160450. DOI:10.1016/j.scitotenv.2022.160450
(  0) 0) |
| [30] |
Lü L L, Qu J H, Yu Z H, et al. A simple method for detecting and quantifying microplastics utilizing fluorescent dyes – Safranine T, fluorescein isophosphate, Nile red based on thermal expansion and contraction property[J]. Environmental Pollution, 2019, 255: 113283. DOI:10.1016/j.envpol.2019.113283
(  0) 0) |
| [31] |
Gao Z Q, Wontor K, Cizdziel J V. Labeling microplastics with fluorescent dyes for detection, recovery, and degradation experiments[J]. Molecules, 2022, 27(21): 7415. DOI:10.3390/molecules27217415
(  0) 0) |
| [32] |
Hu J Y, Wu Y H, Wang J L, et al. Unraveling microplastics release in bottled water under in-vehicle conditions using carbon quantum dots[J]. Journal of Hazardous Materials, 2025, 496: 139200. DOI:10.1016/j.jhazmat.2025.139200
(  0) 0) |
| [33] |
Ho D, Prabhakar P, Karthikeyan K G, et al. Shedding light on the polymer's identity: Microplastic detection and identification through Nile red staining and multispectral imaging(FIMAP)[J]. Journal of Environmental Chemical Engineering, 2025, 13(5): 117944. DOI:10.1016/j.jece.2025.117944
(  0) 0) |
| [34] |
Feng Q C, Cui M, Chen J R, et al. Enhanced long-term stability of stained microplastics with carbon nitride fluorescent polymer for tracking[J]. Environmental Technology & Innovation, 2024, 34: 103593.
(  0) 0) |
| [35] |
Shim W J, Song Y K, Hong S H, et al. Identification and quantification of microplastics using Nile Red staining[J]. Marine Pollution Bulletin, 2016, 113(1/2): 469-476.
(  0) 0) |
| [36] |
Tarafdar A, Choi S H, Kwon J H. Differential staining lowers the false positive detection in a novel volumetric measurement technique of microplastics[J]. Journal of Hazardous Materials, 2022, 432: 128755. DOI:10.1016/j.jhazmat.2022.128755
(  0) 0) |
| [37] |
Nguyen B, Tufenkji N. Single-particle resolution fluorescence microscopy of nanoplastics[J]. Environmental Science & Technology, 2022, 56(10): 6426-6435.
(  0) 0) |
| [38] |
Peng B Y, Wang W X. In Vivo visualization of microplastic degradability and intestinal functional responses in a plastivore insect[J]. Journal of Hazardous Materials, 2025, 486: 137109. DOI:10.1016/j.jhazmat.2025.137109
(  0) 0) |
| [39] |
Song C, Lee J J, Lee S, et al. An AIE-based fluorescent dye for selective staining of polyamide microplastics without pretreatment: Applications to environmental samples and zebrafish[J]. Journal of Hazardous Materials, 2025, 483: 136680. DOI:10.1016/j.jhazmat.2024.136680
(  0) 0) |
| [40] |
Luo J D, Xie Z L, Lam J W Y, et al. Aggregation-induced emission of 1-methyl-1, 2, 3, 4, 5-pentaphenylsilole[J]. Chemical Communications, 2001(18): 1740-1741. DOI:10.1039/b105159h
(  0) 0) |
| [41] |
Wang M J, Wang W X. Accumulation kinetics and gut microenvironment responses to environmentally relevant doses of micro/nanoplastics by zooplankton Daphnia magna[J]. Environmental Science & Technology, 2023, 57(14): 5611-5620.
(  0) 0) |
| [42] |
Yang L P, Tang B Z, Wang W X. Near-infrared-Ⅱ in vivo visualization and quantitative tracking of micro/nanoplastics in fish[J]. ACS Nano, 2023, 17(19): 19410-19420. DOI:10.1021/acsnano.3c07571
(  0) 0) |
| [43] |
Mitrano D M, Beltzung A, Frehland S, et al. Synthesis of metal-doped nanoplastics and their utility to investigate fate and behaviour in complex environmental systems[J]. Nature Nanotechnology, 2019, 14(4): 362-368. DOI:10.1038/s41565-018-0360-3
(  0) 0) |
| [44] |
Zhao Z X, Zhao X, Shan J J, et al. Concentration analysis of metal-labeled nanoplastics in different water samples using electrochemistry[J]. Science of the Total Environment, 2024, 907: 168013. DOI:10.1016/j.scitotenv.2023.168013
(  0) 0) |
| [45] |
Lai Y J, Dong L J, Li Q C, et al. Counting nanoplastics in environmental waters by single particle inductively coupled plasma mass spectroscopy after cloud-point extraction and In situ labeling of gold nanoparticles[J]. Environmental Science & Technology, 2021, 55(8): 4783-4791.
(  0) 0) |
| [46] |
Frehland S, Kaegi R, Hufenus R, et al. Long-term assessment of nanoplastic particle and microplastic fiber flux through a pilot wastewater treatment plant using metal-doped plastics[J]. Water Research, 2020, 182: 115860. DOI:10.1016/j.watres.2020.115860
(  0) 0) |
| [47] |
Smith C, Brown S, Malone N, et al. Nanoplastics prepared with uniformly distributed metal-tags: A novel approach to quantify size distribution and particle number concentration of polydisperse nanoplastics by single particle ICP-MS[J]. Environmental Science: Nano, 2024, 11(3): 911-923. DOI:10.1039/D3EN00342F
(  0) 0) |
| [48] |
Du H Y, Wang Y Q, Zhang P P, et al. Quantitative assessment of in vivo distribution of nanoplastics in bivalve Ruditapes philippinarum using reliable SERS tag-labeled nanoplastic models[J]. Nanoscale, 2022, 14(21): 7807-7816. DOI:10.1039/D2NR00157H
(  0) 0) |
| [49] |
Marigliano L, Grassl B, Szpunar J, et al. Nanoplastic labelling with metal probes: Analytical strategies for their sensitive detection and quantification by ICP mass spectrometry[J]. Molecules, 2021, 26(23): 7093. DOI:10.3390/molecules26237093
(  0) 0) |
| [50] |
Huang W, Wang X H, Chen D Y, et al. Toxicity mechanisms of polystyrene microplastics in marine mussels revealed by high-coverage quantitative metabolomics using chemical isotope labeling liquid chromatography mass spectrometry[J]. Journal of Hazardous Materials, 2021, 417: 126003. DOI:10.1016/j.jhazmat.2021.126003
(  0) 0) |
| [51] |
Mauel A, Pötzschner B, Meides N, et al. Quantification of photooxidative defects in weathered microplastics using 13C multiCP NMR spectroscopy[J]. RSC Advances, 2022, 12(18): 10875-10885. DOI:10.1039/D2RA00470D
(  0) 0) |
| [52] |
Zhou Q, Tu C, Liu Y, et al. Biofilm enhances the copper(Ⅱ)adsorption on microplastic surfaces in coastal seawater: Simultaneous evidence from visualization and quantification[J]. Science of the Total Environment, 2022, 853: 158217. DOI:10.1016/j.scitotenv.2022.158217
(  0) 0) |
| [53] |
Midani F S, Wynn M L, Schnell S. The importance of accurately correcting for the natural abundance of stable isotopes[J]. Analytical Biochemistry, 2017, 520: 27-43. DOI:10.1016/j.ab.2016.12.011
(  0) 0) |
| [54] |
Dueker S R, Jones A D, Clifford A J. Protocol development for biological tracer studies[J]. Advances in Experimental Medicine and Biology, 1998, 445: 363-378.
(  0) 0) |
| [55] |
Al-Sid-Cheikh M, Rowland S J, Kaegi R, et al. Synthesis of 14C-labelled polystyrene nanoplastics for environmental studies[J]. Communications Materials, 2020, 1: 97. DOI:10.1038/s43246-020-00097-9
(  0) 0) |
| [56] |
Kim H, Zaheer J, Choi E J, et al. Enhanced ASGR2 by microplastic exposure leads to resistance to therapy in gastric cancer[J]. Theranostics, 2022, 12(7): 3217-3236. DOI:10.7150/thno.73226
(  0) 0) |
| [57] |
Fan Y L, Pan D H, Yang M, et al. Radiolabelling and in vivo radionuclide imaging tracking of emerging pollutants in environmental toxicology: A review[J]. Science of the Total Environment, 2023, 866: 161412. DOI:10.1016/j.scitotenv.2023.161412
(  0) 0) |
| [58] |
Kręcisz P, Stefańska K, Studziński J, et al. Radiocopper in radiopharmacy and medical use: Current status and perspective[J]. Journal of Medicinal Chemistry, 2025, 68(3): 2356-2376. DOI:10.1021/acs.jmedchem.4c02885
(  0) 0) |
| [59] |
Buchanan C J, Fry S C, Eastwood M A. The use of 14C-labelled substrates to study plant cell wall breakdown in the gastrointestinal tract[J]. Proceedings of the Nutrition Society, 1996, 55(3): 927-936. DOI:10.1079/PNS19960089
(  0) 0) |
| [60] |
Vesamäki J S, Nissinen R, Kainz M J, et al. Decomposition rate and biochemical fate of carbon from natural polymers and microplastics in boreal lakes[J]. Frontiers in Microbiology, 2022, 13: 1041242. DOI:10.3389/fmicb.2022.1041242
(  0) 0) |
| [61] |
Yang Y, Yang J, Wu W M, et al. Biodegradation and mineralization of polystyrene by plastic-eating mealworms: Part 2. role of gut microorganisms[J]. Environmental Science & Technology, 2015, 49(20): 12087-12093.
(  0) 0) |
| [62] |
Zumstein M T, Schintlmeister A, Nelson T F, et al. Biodegradation of synthetic polymers in soils: Tracking carbon into CO2 and microbial biomass[J]. Science Advances, 2018, 4(7): eaas9024. DOI:10.1126/sciadv.aas9024
(  0) 0) |
| [63] |
Hemmilä I. Luminescent lanthanide chelates—A way to more sensitive diagnostic methods[J]. Journal of Alloys and Compounds, 1995, 225(1/2): 480-485.
(  0) 0) |
| [64] |
Hemmilä I, Mukkala V M, Takalo H. Development of luminescent lanthanide chelate labels for diagnostic assays[J]. Journal of Alloys and Compounds, 1997, 249(1/2): 158-162.
(  0) 0) |
| [65] |
Eliseeva S V, Bünzli J G. Lanthanide luminescence for functional materials and bio-sciences[J]. Chemical Society Reviews, 2010, 39(1): 189-227. DOI:10.1039/B905604C
(  0) 0) |
| [66] |
Sun H F, Lei C L, Xu J H, et al. Foliar uptake and leaf-to-root translocation of nanoplastics with different coating charge in maize plants[J]. Journal of Hazardous Materials, 2021, 416: 125854. DOI:10.1016/j.jhazmat.2021.125854
(  0) 0) |
| [67] |
Yuan W K, Xu E G, Li L Z, et al. Tracing and trapping micro- and nanoplastics: Untapped mitigation potential of aquatic plants[J]. Water Research, 2023, 242: 120249. DOI:10.1016/j.watres.2023.120249
(  0) 0) |
| [68] |
Weissman S I. Intramolecular energy transfer the fluorescence of complexes of europium[J]. The Journal of Chemical Physics, 1942, 10(4): 214-217. DOI:10.1063/1.1723709
(  0) 0) |
| [69] |
Feng J, Zhang H J. Hybrid materials based on lanthanide organic complexes: A review[J]. Chemical Society Reviews, 2013, 42(1): 387-410. DOI:10.1039/C2CS35069F
(  0) 0) |
| [70] |
Kido J, Okamoto Y. Organo lanthanide metal complexes for electroluminescent materials[J]. Chemical Reviews, 2002, 102(6): 2357-2368. DOI:10.1021/cr010448y
(  0) 0) |
| [71] |
Kłonkowski A M, Szałkowska I, Pietraszkiewicz M, et al. Influence of xerogel matrices and co-ligands on luminescence parameters in materials with an europium(Ⅲ)cryptate[J]. Journal of Non-Crystalline Solids, 2005, 351(24/25/26): 2047-2056.
(  0) 0) |
| [72] |
Cortecchia D, Mróz W, Folpini G, et al. Layered perovskite doping with Eu3+ and β-diketonate Eu3+ complex[J]. Chemistry of Materials, 2021, 33(7): 2289-2297. DOI:10.1021/acs.chemmater.0c04097
(  0) 0) |
| [73] |
Hasegawa Y, Kitagawa Y, Nakanishi T. Effective photosensitized, electrosensitized, and mechanosensitized luminescence of lanthanide complexes[J]. NPG Asia Materials, 2018, 10(4): 52-70. DOI:10.1038/s41427-018-0012-y
(  0) 0) |
| [74] |
Bünzli J G. Benefiting from the unique properties of lanthanide ions[J]. Accounts of Chemical Research, 2006, 39(1): 53-61. DOI:10.1021/ar0400894
(  0) 0) |
| [75] |
Zhou W L, Chen Y, Lin W J, et al. Luminescent lanthanide–macrocycle supramolecular assembly[J]. Chemical Communications, 2021, 57(87): 11443-11456. DOI:10.1039/D1CC04672A
(  0) 0) |
| [76] |
Binnemans K. Lanthanide-based luminescent hybrid materials[J]. Chemical Reviews, 2009, 109(9): 4283-4374. DOI:10.1021/cr8003983
(  0) 0) |
| [77] |
Zhang Y, Yang X W, Zhao S N, et al. Recent developments of microscopic study for lanthanide and manganese doped luminescent materials[J]. Small, 2022, 18(50): e2205014. DOI:10.1002/smll.202205014
(  0) 0) |
| [78] |
Wang Y, Lu G L, Qiu Y, et al. Synthesis and optical properties of novel apatite-type NaCa3Bi(PO4)3F: Dy3+ yellow-emitting fluorophosphate phosphors for white LEDs[J]. Journal of Rare Earths, 2022, 40(12): 1827-1836. DOI:10.1016/j.jre.2021.11.006
(  0) 0) |
| [79] |
Dang P P, Liang S S, Li G G, et al. Full color luminescence tuning in Bi3+/Eu3+-doped LiCa3MgV3O12 garnet phosphors based on local lattice distortion and multiple energy transfers[J]. Inorganic Chemistry, 2018, 57(15): 9251-9259. DOI:10.1021/acs.inorgchem.8b01271
(  0) 0) |
| [80] |
Zheng B Z, Fan J Y, Chen B, et al. Rare-earth doping in nanostructured inorganic materials[J]. Chemical Reviews, 2022, 122(6): 5519-5603. DOI:10.1021/acs.chemrev.1c00644
(  0) 0) |
| [81] |
Luo Y M, Li L Z, Feng Y D, et al. Quantitative tracing of uptake and transport of submicrometre plastics in crop plants using lanthanide chelates as a dual-functional tracer[J]. Nature Nanotechnology, 2022, 17(4): 424-431. DOI:10.1038/s41565-021-01063-3
(  0) 0) |
| [82] |
Li Y, Zhang J J, Xu L, et al. Leaf absorption contributes to accumulation of microplastics in plants[J]. Nature, 2025, 641(8063): 666-673. DOI:10.1038/s41586-025-08831-4
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


