2. 柏林自由大学生物研究所, 德国柏林 14195
2. Institute of Biology, Freie Universität Berlin, Berlin 14195, Germany
塑料因具有多功能性且价格低廉,已成为现代生活中不可或缺的一部分[1]。自20世纪以来,塑料产量的激增导致了不断累积的塑料垃圾。预计到2050年,塑料废弃物的总量将达到惊人的120亿吨[2]。在紫外线辐射、物理磨损和生物降解等因素的作用下,这些塑料废弃物会逐渐破碎形成“微塑料(< 5 mm)”[3]。当前,微塑料在全球各地均被检测到,从珠穆朗玛峰的顶端到马里亚纳海沟的深处,均有其踪迹[4]。作为一种普遍存在的人为污染物,微塑料对环境和人体健康产生严重威胁,且最近研究表明微塑料可能会对全球碳库产生影响[5]。
土壤有机质是全球最大的陆地有机碳库,其在调节全球气候方面发挥着关键作用,其微小的变化均有可能减缓或加速陆地二氧化碳排放速率以及由此引发的气候变化[6]。同时,土壤环境是微塑料最大的聚集汇,微塑料可通过多种途径进入土壤,包括农资物质使用、大气沉降、径流或灌溉等。已有研究表明,微塑料在土壤中的质量浓度可高达67 000 mg·kg–1[7]。因此,理解微塑料这一新污染物对土壤有机质的影响正逐渐成为研究的热点。土壤溶解性有机质(dissolved organic matter,DOM)是土壤有机质中活性最高的组分,其组成和结构特征对土壤肥力、污染物的环境行为和植物生长等具有重要意义[8]。已有研究表明,微塑料进入土壤之后会释放溶解性有机碳,从而影响土壤DOM的组分特征[9]。研究表明在PE和PAN处理的土壤中,土壤DOM腐殖化指数显著升高[10],但也有研究指出微塑料会降低土壤DOM的腐殖化程度[9]。目前对于微塑料扰动土壤DOM的相关研究仍较少,且多数是在土壤体系中进行的,较少涉及土壤-作物种植体系。
为缓解塑料以及微塑料带来的环境污染问题,世界各国倡导使用可生物降解塑料作为传统石油基塑料的绿色替代品[11]。可生物降解塑料,如聚己二酸对苯二甲酸丁二醇酯、聚乳酸、聚丁二酸丁二醇酯等已被应用于农业、食品、工业和医疗领域[12]。然而,可生物降解塑料的降解条件十分苛刻,在自然条件下很难完全降解,导致在相同条件下可生物降解塑料会形成更多微塑料颗粒[13]。目前,对种植体系中可生物降解微塑料扰动土壤DOM的效应了解较少。
因此,本研究选择玉米(Zea mays L.)种植体系,开展盆栽试验,并首次结合三维荧光-平行因子分析(EEM-PARAFAC)和傅里叶变换离子回旋共振质谱(FT-ICR-MS)等高分辨率技术,系统比较传统难降解微塑料与多种可生物降解微塑料对玉米种植体系中土壤DOM组分和分子特征的影响。本研究的创新之处在于,从分子层面揭示了不同降解特性的微塑料对土壤DOM化学多样性的差异化影响,这对于深入理解微塑料的环境效应,特别是评估可生物降解塑料作为传统塑料替代品的长期生态风险和其在土壤碳循环中的作用,具有重要的理论与现实意义。
1 材料与方法 1.1 土壤与微塑料受试所用土壤采集自中国农业大学上庄试验站(40°14′40.91”N,116°19' 17.94"E),受试土壤无覆膜等塑料使用史。从采样点0~15 cm处收集5份副样方的土壤样品,混合为1份复合样品,对收集到的土壤样品进行风干处理,并过2 mm筛去除其中的石头和根残留物,混合均匀。土壤基本理化性质如下:总有机碳13.8 ± 0.2 mg·g–1,全氮1.64 ± 0.12 mg·g–1,pH 7.93 ± 0.12,黏粒18.4%,粉粒28.8%,砂粒52.8%。所使用的微塑料为传统PE(密度:0.92 g·cm–3)和PS(密度:1.05 g·cm–3),购自阿拉丁(上海,中国);可生物降解PBAT(密度:1.18 g·cm–3)、PLA(密度:1.20 g·cm–3)和PBS(密度:1.26 g·cm–3)购自兴旺塑料(东莞,中国)。购入的微塑料首先过80~100目筛,选择粒径为150~180 μm的微塑料颗粒,之后用甲醇清洗,在40℃下烘干,并储存于4℃备用。
1.2 盆栽试验供试种子为玉米(Zea mays L.),品种为先玉335,购自新芽种业。挑选籽粒饱满的玉米种子,用去离子水清洗后,在5%(w/w)次氯酸钠溶液中浸泡5 min,再用去离子水冲洗干净。本研究设置微塑料污染浓度为0.1%,共设置7个处理组:(1)KB:不添加MPs、不种植玉米;(2)CK:不添加MPs、种植玉米;(3)添加0.1%(w/w)PBAT;(4)添加0.1%(w/w)PBS;(5)添加0.1%(w/w)PLA;(6)添加0.1%(w/w)PE;(7)添加0.1%(w/w)PS。使用2 kg受试土壤,分别加入2 g对应的MPs,充分混匀后放入2.5 L的塑料花盆中。已有研究表明土壤微塑料质量浓度在20~67 500 mg·kg–1范围内[7],但通常情况下,受人类影响的土壤中微塑料的含量一般不超过土壤质量的0.1%[14]。因此选择0.1%(w/w)作为受试浓度,来模拟当前和未来可能达到的、与真实环境相关的微塑料污染水平,旨在研究不同聚合物类型的影响而非剂量效应。保持土壤湿度为20%左右,平衡一周。将清洗后的种子播种,待玉米正常生长约一周后,间苗至每盆2株。在培养阶段,每周使用2~3次超纯水调整土壤湿度,使土壤湿度保持在20%左右。整个培养过程在中国农业大学资源与环境学院的温室进行,室内温度保持在19.5~27.8℃,室内湿度为12%左右,光照时长为10 h·d–1。盆栽试验为期60天,并在第3、7、15、30、60天进行破坏性取样,收集盆栽土壤样品,进行土壤理化性质和DOM特性的测定,以揭示培养过程中土壤DOM的动态变化。
1.3 土壤理化性质测定冻干球磨后的土壤样品使用元素分析仪(Ftash2000,Thermo Fisher,美国)测定土壤总有机碳(total organic carbon,TOC)和全氮(total nitrogen,TN);土壤pH以1:5的土水比用pH计(PHSJ-6L,雷磁,上海)测定;土壤电导率以1︰5的土水比采用电导率仪(PHSJ-6L,雷磁,上海)测定;有效磷采用钼锑抗比色法测定[15];铵态氮和硝态氮采用分光光度计(UV-1900i,SHIMADZU,日本)测定[16]。
1.4 土壤DOM测定(1)土壤DOC测定。DOM浓度通常由DOC定义。使用新鲜土样,以土水比1︰5加入超纯水,室温下振荡1 h后离心,取上清液经0.45 μm乙酸纤维素膜过滤器过滤,使用TOC分析仪(vario TOC,Elementar,德国)测定。
(2)三维荧光光谱测定。使用步骤(1)的方法获得土壤浸提液,将其保存在离心管中并用铝箔包裹,避光保存。土壤DOM的三维荧光光谱使用Aqualog同步分析仪(HORIBA Scientific,美国)测定,测定前对样品进行稀释,以消除内滤效应,使用超纯水对仪器进行空白校正。三维荧光光谱的测试中,激发光波长(Ex)范围250 nm~500 nm,检测步进5 nm;发射光(Em)检测波长范围280 nm~600 nm,检测步长2 nm。测量在室温下进行,仪器偏差用制造商提供的校准文件进行校准。测定后的三维荧光光谱数据参照Murphy等[17]提出的三维荧光数据标准分析流程,使用staRdom包进行空白扣除、一级和二级瑞利峰和拉曼峰去除和拉曼标准化。
(3)FT-ICR-MS测定和分子识别。将土壤样品以土水比1︰25加入超纯水,在25 ℃下恒温振荡8 h,然后离心20 min并将上清液过0.22 μm滤膜。测定上清液的DOC后进行SPE固相萃取(萃取柱型号为Agilent Bond Elut PPL(500 mg,6 mL))。SPE固相萃取的具体操作步骤如下:(1)用1 mol·L–1盐酸调节样品pH至2.0;(2)在固相萃取装置上安装好PPL柱,先后用12 mL甲醇(色谱纯)和12 mL 0.01 mol·L–1盐酸淋洗活化柱子;(3)往PPL柱缓慢加入一定量样品,让样品自然流下,流速保持约2 mL·min–1,考虑样品流过柱子时DOC的损失率为50%,使得最后浓缩得到的DOM有机碳含量约为100 mg·L–1;(4)样品流完后加入18 mL 0.01 mol·L–1盐酸淋洗柱子,以除去盐分;(5)氮吹干燥柱子,然后用12 mL甲醇洗脱,收集洗脱液;(6)氮吹至甲醇完全挥发,样品保存在–20℃冰箱中,FT-ICR-MS测定前用1 mL甲醇溶解[18-20]。
DOM的质谱信息使用SolariX XR FT-ICR-MS(Bruker Daltonik GmbH,Bremen,德国)的负离子模式测定,该仪器配备15.0 T冷却主动屏蔽超导磁体和电喷雾离子源。使用如下设置进行测定:注射速率为120 μL·h–1,注射针电压为-3.8 kV,离子积累时间为0.06 s。测定的质谱在负离子模式下利用10 mmol·L–1的甲酸钠进行校准,检测质量范围设置为m/z 100~1600 Da,去除在空白样品(去离子水和甲醇)和DOM样品中共有的峰。将获得的DOM质谱峰转换为m/z值列表,信噪比 > 3,默认强度阈值为100,为了减少累积误差,整个数据集的所有样本峰彼此对齐,以消除可能的质量偏移。用Formula Calculator软件获得质谱峰的化学式。给定化学式的测量质量与理论质量之间的误差应小于0.35×10–6,且分子式应在O/C≤1.2和0.2 < H/C≤2.2的元素比限制范围内。
1.5 土壤DOM特征表征土壤DOM荧光光谱指标,包括,荧光指数(fluorescence index,FI)、腐殖化指数(humification index,HIX)和新鲜度指数(index of recent autochthonous contribution,BIX)进行计算,以表征DOM特征。同时使用PARAFAC用于对荧光数据进行组分识别和定量。
使用解谱后的DOM质谱数据,将各分子式的信号强度与所有分子信号强度之和进行标准化计算,以获得各分子式的相对信号强度。使用O/C比和H/C比构建van Krevelen(VK)图,根据分子的O/C比和H/C比将其划分为7种不同的分子类型:(1)脂肪类(O/C,0~0.3;H/C,1.5~2.3),(2)蛋白质类(O/C,0.3~0.55;H/C,1.5~2.2),(3)氨基糖类(O/C,0.55~0. 7;H/C,1.5~2.2),(4)碳水化合物类(O/C,0.7~1.2;H/C,1.5~2.2),(5)木质素类(O/C,0.1~0.67;H/C,0.8~1.5),(6)单宁类(O/C,0.67~1.2;H/C,0.8~1.5),(7)稠环烃类(O/C,0~1.0;H/C,0.25~0.8)。此外,并计算分子的双键指数(double-bond equivalent,DBE)、芳香度指数(aromaticity index,AI)、碳标准氧化态(nominal oxidation state of carbon,NOSC),分子不稳定性边界(molecular lability boundary,MLB),以及每个分子的碳氧化半反应的吉布斯自由能(ΔG0)。
1.6 统计分析使用R “staRdom”包对DOM荧光组分进行PARAFAC分析;使用R “ftmsRanalysis”包将DOM分子划分为不同类别并计算分子特性。使用R中的“stats”包进行Kruskal-Wallis检验,评估不同处理间DOM化合物的显著性差异。使用R包“corrplot”进行DOM组分和指数之间的Pearson相关性分析,并进行可视化。将土壤DOM光谱参数归一化,合并成一个矩阵,利用R中的“vegan”包进行主成分分析。使用R“UpSetR”绘制UpSet韦恩图。不同处理之间的差异性使用Kruskal-Wallis test检验其是否具有显著性。
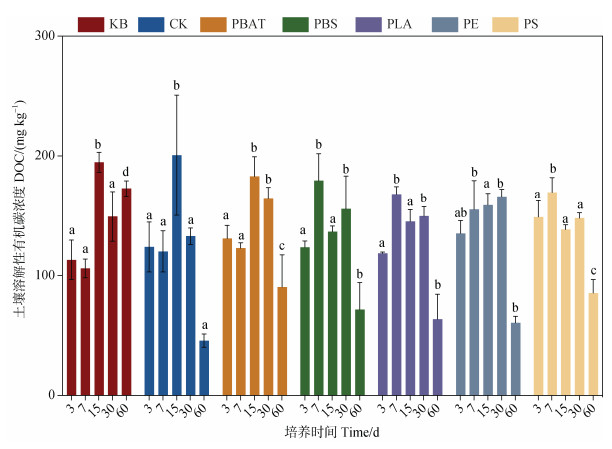
2 结果 2.1 土壤DOC浓度和DOM荧光特征的变化与不种植玉米的KB组相比,种植玉米的处理组在60天的盆栽试验后,土壤DOC含量明显下降(图 1)。整体而言,在种植玉米的处理组中,土壤DOC含量呈现先升高后降低的趋势。与对照相比,微塑料处理并没有显著提高土壤平均DOC的含量,但微塑料处理组中土壤DOC含量在第60天相比于CK组有所提高。如在培养60天后,CK组中DOC的浓度为46.04 mg·kg–1,而在微塑料处理组中DOC浓度为56.23~93.08 mg·kg–1(图 1)。可降解塑料处理与不可降解塑料处理相比,整个培养期的平均浓度并没有显著差异。BIX是反映DOM生物来源相对贡献的指标,在本研究中,BIX指数均低于0.8,表明微生物来源的DOM占比较低;而种植玉米的处理组BIX指数逐渐降低,在微塑料处理组中,BIX相较于CK组变化不明显(图 2a)。各处理组HIX指数的变化较小,但种植玉米的处理组HIX指数逐渐降低,与KB组表现出相反的趋势(图 2b)。不同处理组中,表示DOM来源的FI指数表现出与BIX相同的趋势,在本研究中FI指数均小于1.4,表明DOM的来源主要为陆源;在第60天,微塑料处理组的FI指数均小于CK组(图 2c)。值得注意的是,不同的微塑料处理并没有对土壤DOM的荧光指数等参数产生显著影响。
|
注:KB,不添加MPs、不种植玉米;CK,不添加MPs、种植玉米;PBAT,添加0.1%(w/w)PBAT;PBS,添加0.1%(w/w)PBS;PLA,添加0.1%(w/w)PLA;PE,添加0.1%(w/w)PE;PBS,添加0.1%(w/w)PS,以下图片中缩写均表示相同处理。不同小写字母代表不同处理在相同培养时间时的显著差异,Kruskal-Wallis检验,P < 0.05。 Note: KB, no MPs and maize; CK, no MPs only; PBAT, maize with 0.1% PBAT; PBS, maize with 0.1% PBS; PLA, maize with 0.1% PLA; PE, maize with 0.1% PE; PS, maize with 0.1% PS. The abbreviations are the same meanings in the following figures. Different lowercase letters indicate significant differences among different treatments at the same incubating time, Kruskal-Wallis test, P < 0.05. 图 1 不同处理组土壤DOC含量变化 Fig. 1 Concentration of dissolved organic carbon (DOC) in different treatments |
|
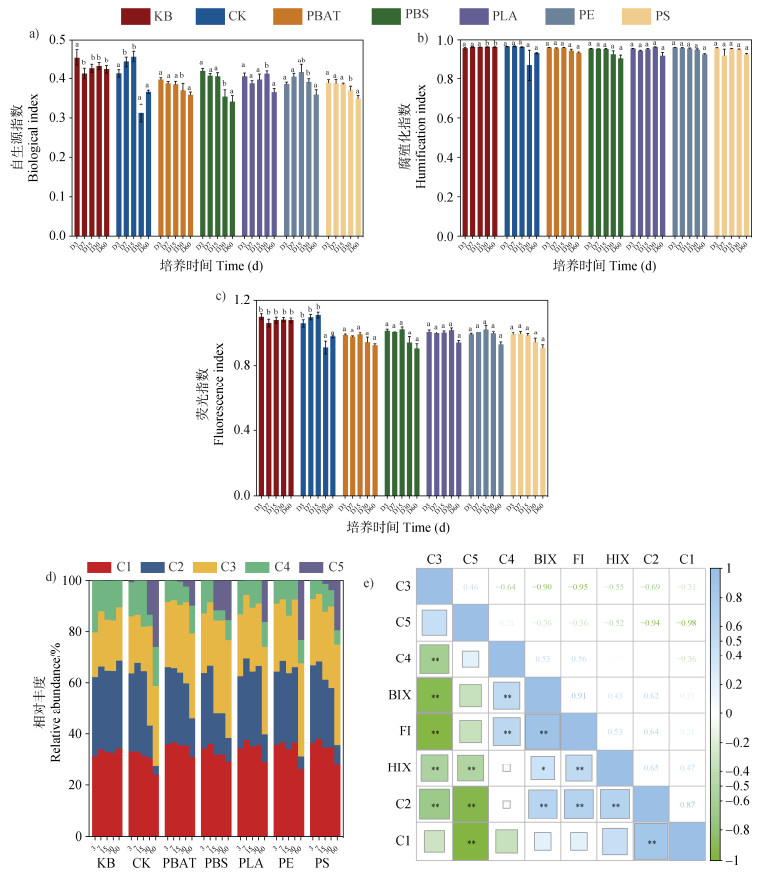
注:BIX,DOM自生源指数;HIX,DOM腐殖化指数;FI,DOM荧光指数;C1,DOM荧光组分1;C2,DOM荧光组分2;C3,DOM荧光组分3;C4,DOM荧光组分4;C5,DOM荧光组分5。不同小写字母代表不同处理在相同培养时间时的显著差异,Kruskal-Wallis检验,P < 0.05。 Note: BIX, biological index of DOM; HIX, humification index of DOM; FI, fluorescence index of DOM; C1, fluorescent component 1 of DOM; C2, fluorescent component 2 of DOM; C3, fluorescent component 3 of DOM; C4, fluorescent component 4 of DOM; C5, fluorescent component 5 of DOM. Different lowercase letters indicate significant differences among different treatments at the same incubating time, Kruskal-Wallis test, P < 0.05. 图 2 土壤DOM荧光特征 Fig. 2 Fluorescence characteristics of soil DOM |
通过EEM-PARAFAC分析,共获得5种荧光组分,分别为2种微生物降解来源的类腐殖质组分(C1和C2)、1种高分子类腐殖质组分(C3)和2种陆源类腐殖质组分(C4和C5),在盆栽试验的初期(第3~15天),两种微生物来源的类腐殖质组分(C1和C2)的占比最高,如在CK和微塑料处理组中为59.37%~65.32%;然而,在种植玉米的处理组,两种组分的相对含量逐渐降低,在第60天占比仅为35.15%~52.83%。高分子类腐殖质组分(C3)和陆源类腐殖质组分(C5)则表现出相反的趋势,随着玉米种植时间的增加,其相对含量逐渐升高(图 2d)。研究进一步分析了不同DOM组分和DOM荧光指数之间的相关关系(图 2e)。微生物降解来源的类腐殖质组分C2和HIX呈显著正相关关系,且与陆源类腐殖质组分C5呈负相关关系;高分子类腐殖质C3与BIX和FI指数呈显著负相关关系,这表明C3是陆源DOM的主要贡献者。
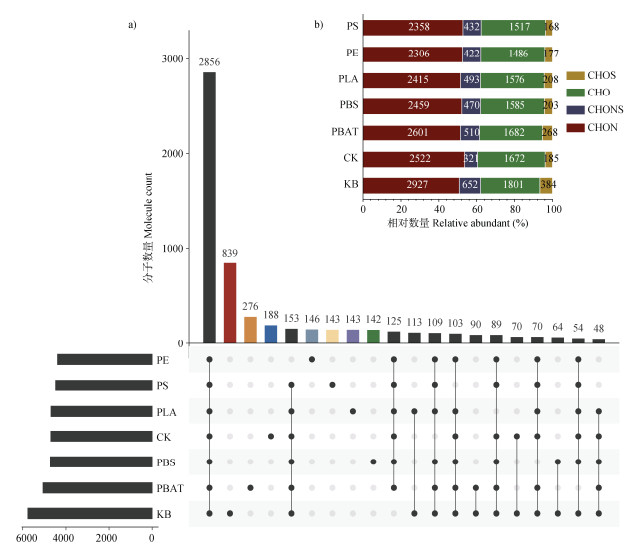
2.2 土壤DOM分子组成及特性变化基于FT-ICR-MS的结果,本研究从分子水平上探究了微塑料对土壤-植物体系中DOM的影响(表 1)。研究计算了DOM的分子特性,结果表明种植玉米显著降低了土壤中DOM的分子数量和M/Z;在微塑料添加的处理组中,DOM分子的NOSC、DBE和AI值升高;H/C和MLBL降低,表明微塑料增加了土壤-植物体系中DOM分子的腐殖化程度。此外,不可降解微塑料PE和PS处理组中,AI、NOSC以及O/C值略高于可降解微塑料处理组,表明相较于可降解塑料而言,不可降解微塑料可能会增加土壤-植物体系中的稳定性。图 3为各个处理组DOM分子组成的异同,以及基于元素组成划分的不同类别DOM分子所占的比例。土壤-植物体系中的DOM分子与不种植玉米的DOM分子存在较大差异。与CK和微塑料处理组相比,KB组中特有的DOM分子数量最多。可生物降解的PBAT处理组中特有的DOM分子最多,有276个。从DOM分子的元素组成类别看,玉米增加了土壤-植物体系中DOM分子中CHO类分子的相对比例;与CK组相比,微塑料降低了CHON和CHO类分子的相对比例。从分子组成上看,一个显著的差异是,与CK组及传统微塑料组相比,可降解塑料处理组中含硫和氮的复杂分子(CHONS、CHON和CHOS)数量相对更多,这可能与其降解产物为微生物活动提供了更丰富的底物有关。
|
|
表 1 不同处理组中DOM分子的特性 Table 1 Molecular parameters of DOM in different treatments |
|
注:CHOS,含碳、氢、氧和硫元素的化合物;CHO,含碳、氢和氧元素的化合物;CHONS,含碳、氢、氧、氮和硫元素的化合物;CHON,含碳、氢、氧和氮元素的化合物。下同。 Note: CHOS, compounds containing carbon, hydrogen, oxygen, and sulfur; CHO, compounds containing carbon, hydrogen, and oxygen; CHONS, compounds containing carbon, hydrogen, oxygen, nitrogen, and sulfur; CHON, compounds containing carbon, hydrogen, oxygen, and nitrogen. The same below. 图 3 土壤DOM分子的UpSet图以及不同元素组成的DOM分子类别的数量及其在全部分子中的占比 Fig. 3 UpSet plot showing the temporal change of DOM molecules, and numbers and proportion of DOM molecules with different heteroatoms |
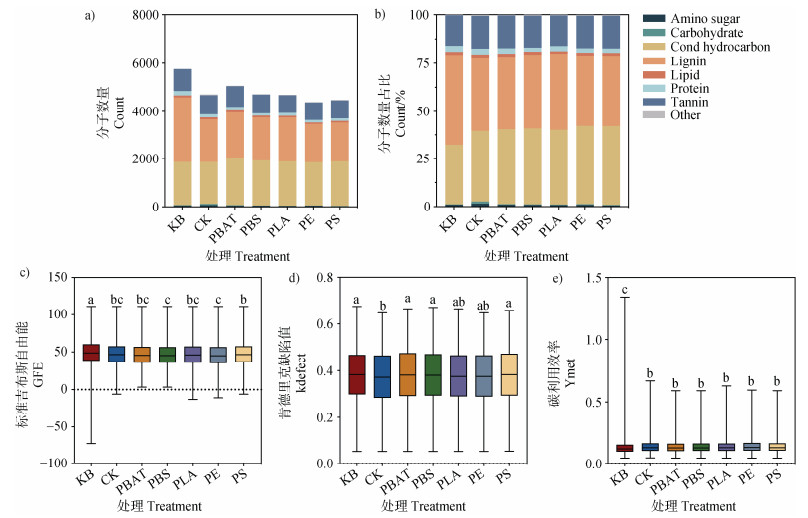
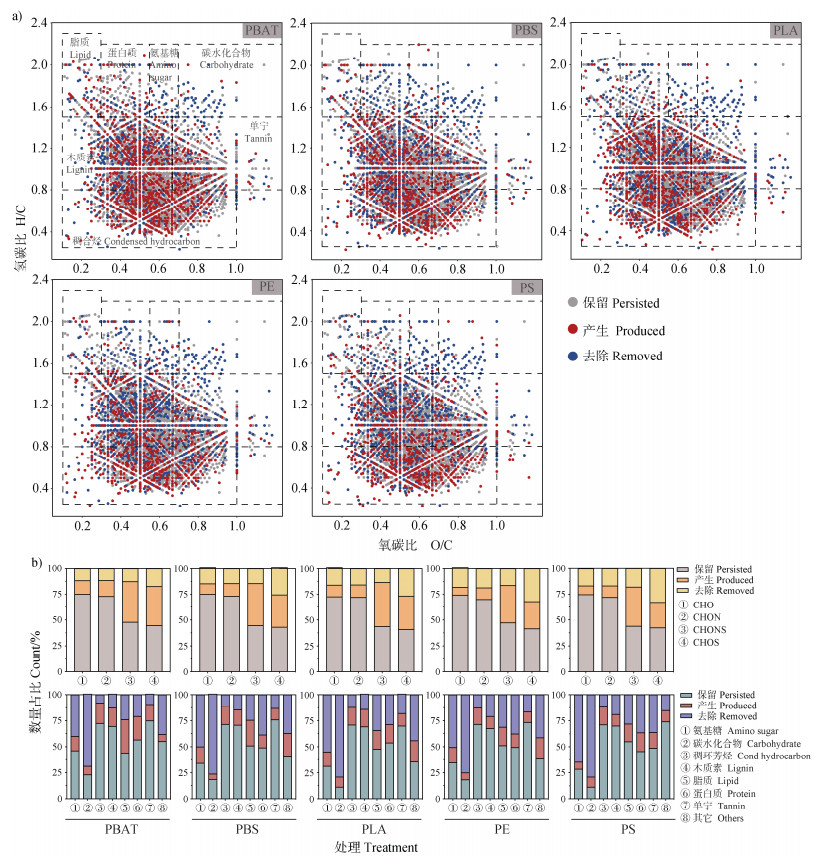
研究根据DOM分子的O/C和H/C将DOM分子分为七大类(图 4a和图 4b)。与KB组相比,种植玉米后,土壤-植物体系中木质素类分子的数量和相对含量降低,稠环芳烃类分子增多;与CK相比,微塑料降低了氨基糖类、碳水化合物类和蛋白质类分子的相对含量,如在CK组中碳水化合物占比为1.19%,在微塑料处理组中,碳水化合物类分子占比为0.28%~0.38%;而微塑料增加了稠环芳烃类分子的相对含量,如在CK组中稠环芳烃类分子占比为36.98%,在微塑料处理组中,稠环芳烃类分子占比为39.19%~41.36%。研究进一步计算了DOM分子的标准吉布斯自由能(ΔG0)、肯德里克缺陷值(Kendrick defect,Kdefect)和碳利用效率(carbon use efficiency,Ymet)。结果表明在微塑料处理组中,PBAT、PLA、PE和PS显著降低了ΔG0和增加了Ymet,表明微塑料处理组中,分子参与代谢反应的热力学效率降低(图 4d,图 4e)。为了进一步比较不同微塑料对土壤-植物体系中不同类型DOM分子的影响,研究比较了不同处理组DOM分子相对于CK的变化情况,并将DOM分子划分为去除、不变和产生三类(图 5)。研究结果表明,微塑料相对于CK组产生最多的是CHONS类分子,去除最多的是CHOS类分子;可生物降解微塑料产生的CHONS类分子占比高于传统MPs,如在PBAT、PBS和PLA处理组中,产生的CHONS类分子占比分别为39.66%、40.78%和42.98%,而在PE、PS处理组中,产生的CHONS类分子占比分别为36.31%和38.03%(图 5)。
|
注:箱体代表 25%至75%分位数,中间线为中位数,上下影线延伸至最大值和最小值。不同小写字母代表不同处理组间分子特征的中位数存在显著差异,Kruskal-Wallis检验,P < 0.05。 Note: The boxplot shows the distribution of values for all molecules within a treatment. The box represents the interquartile range (25th to 75th percentiles), the line inside is the median, and the whiskers extend to the maximum and minimum values. Different lowercase letters indicate significant differences in the median values of molecular characteristics among treatments. Kruskal-Wallis test, P < 0.05. 图 4 不同处理土壤的DOM分子特征 Fig. 4 Molecular characteristics of soil DOM in different treatments |
|
注:将DOM分子分为“保留(Persisted)”、“产生(Produced)”、“去除(Removed)”三类。“保留(Persisted)”表示在微塑料处理与对照处理中均出现的分子;“产生(Produced)”表示在微塑料处理组中出现,但在对照处理中未出现的分子;“去除(Removed)”表示在微塑料处理组中未出现,但在对照处理中出现的分子。 Note: The DOM molecules were categorized into three groups: Persisted, Produced, and Removed. Persisted indicates the molecules showing in the microplastic treatments and control; Produced indicates the molecules showing only in the microplastic treatments; Removed indicates the molecules showing only in the control. 图 5 不同处理组中DOM分子的变化 Fig. 5 Changes in DOM molecules among different treatment groups |
在试验开始初期(D3~D15),土壤DOC含量在种植玉米与未种植玉米的土壤中表现出相同趋势,即随着培养时间的延长而增加。这可能是由于土壤中不稳定SOC的损失,这部分碳转化为DOC和CO2所导致的。在试验后期(D30~D60),未种植玉米的KB组DOC含量逐渐趋于稳定,而CK组的DOC含量降低。在种植植物的处理组中,植物根系分泌物是DOC的来源之一,一方面根系分泌物可以为微生物的活动提供可利用的碳源,从而刺激微生物的活动和胞外酶的活性,增加微生物对本土碳的矿化;而植物也会和微生物竞争土壤养分,从而抑制微生物的矿化作用[21-22]。此外,DOC的产生和组成很大程度上取决于DOC与土壤总SOC的平衡关系,在植物-土壤体系中,新鲜释放的根系分泌物会和稳定的SOC发生交换,该过程可能导致土壤团聚体发生物理破坏,以及原始矿物复合物的解吸,从而增加DOC的浸出和微生物的活性[21]。也有研究表明,CO2的排放和微生物生物量的增加主要来源于近期由植物输入的C(如根系分泌物),而DOC主要来源于SOC;植物根系分泌物会迅速被微生物利用,因此,新输入的C对DOC的贡献较低[23]。总之,土壤-植物体系中DOC的存在是其从SOC中释放、与矿物交换和吸附、被微生物吸收利用以及降解产生CO2的结果[24]。土壤DOC在SOC的稳定和固存中发挥着重要作用,是深层土壤碳的活性中间体和稳定碳的来源[25]。鉴于其在碳循环中的重要作用,未来的研究应进一步关注根系体系中DOC的作用。
与KB相比,种植玉米体系改变了土壤DOM的荧光特性,主要表现在DOM的BIX和FI指数降低,微生物降解来源的类腐殖质组分C1和C2的相对占比显著降低,DOM周转速率更快。这个结果表明种植植物后,DOC的生物活性降低,外源性更强[26]。这在一定程度上反映了植物根系分泌物来源的C对土壤DOM的贡献。两种微生物源类腐殖质DOM组分的减少,表明微生物对该类DOM的转化或分解[27]。从土壤-植物体系DOM的分子变化情况看,种植玉米降低了DOM分子的多样性和DOM的分子量,增加了CHO小分子类物质,以及DOM的不稳定性,降低了木质素类分子的相对含量和碳利用效率(Ymet提高)。这是由于植物根系分泌物多为低分子量碳化合物[28]。结合前述DOC的变化,本研究推测在土壤-植物体系中,由于“根际沉降”效应,微生物利用根际碳快速生长,在短期内吸收、利用和转化易被利用的碳,而快速的消耗过程可能会导致外源碳的“供给不足”,为了弥补新碳输入的不足和持续的碳消耗,微生物可能会通过胞外酶的产生,分解难以利用的碳源(如SOC),以获得养分[29]。因此,DOM中木质素类分子的大量下降,可能是植物根系分泌物所产生的“激发效应”所致[30],而木质素的降低也导致了DOC含量的下降。
3.2 微塑料对土壤-植物体系DOM的影响与CK组相比,在添加微塑料的处理组中,DOC含量在60天的盆栽试验后有所提高,这与Wang等[31]在种植生菜的体系中观察到的PE MPs能提高土壤DOC含量的现象一致。本研究发现,微塑料的加入增加了土壤-植物体系中DOM的腐殖化程度和稳定性(分子的H/C值降低,而NOSC和AI指数增加)。这一结果与部分纯土壤培养研究(如文献[9])提出的微塑料会降低DOM腐殖化程度的结论相反。本研究推测这种差异可能源于本研究中植物根系的存在。“根际激发效应”的引入,使得植物、土壤、微生物与微塑料之间的相互作用更为复杂,它们可能共同促进了DOM向更腐殖化、更稳定的方向转化。
此外,本研究发现传统不可降解微塑料与可生物降解微塑料在影响种植体系土壤DOM上存在一定差异。可生物降解微塑料(PBAT、PBS、PLA)增加了微生物来源的类腐殖质组分(C1和C2)的相对含量,并且在分子水平上产生了更多的CHONS类复杂分子。这有力地表明,这些塑料发生了部分降解,其水解产物可作为微生物的直接碳源。微生物利用这些易于获取的小分子碳源,通过自身代谢活动将其转化为结构更复杂、腐殖化程度更高的大分子物质。DOM分子特征还表明微塑料处理组分子的H/C降低、NOSC和AI指数增加,表明DOM的腐殖化和稳定性增加;DOM分子中氨基酸、碳水化合物和蛋白质类分子的相对含量降低。这可能是由于微塑料增加了微生物对N的需求,使得含N类的分子不断被消耗,最终合成大分子的CHONS类物质。一般而言,低分子量的化合物周转速率更快[32-34],而在本研究观测到的DOM组分均为分子量较大的类腐殖质组分,即可生物降解的微塑料可以提高类腐殖质组分的稳定性。
相比之下,传统难降解微塑料(PE、PS)虽然也增加了DOM的整体腐殖化程度,但其作用机制可能完全不同。由于其化学性质稳定、难以降解,它们无法直接为微生物提供大量碳源。因此,其影响更可能是间接的:一方面,其物理存在可能破坏土壤团聚体,释放被保护的有机质;另一方面,在根系分泌物持续输入环境下,它们可能诱发了更强烈的正向“激发效应”。即微生物在无法利用塑料碳源的情况下,为了获取生长所需养分,会加强对土壤原有有机质(SOC)的分解。因此,本研究推测在土壤-植物体系中,由传统微塑料引发的对原生有机质的“激发效应”可能强于可生物降解微塑料,后者因能提供替代碳源而起到了“稳定剂”的作用。最近的一项研究也表明,微塑料会改变植物光合碳在地下的分配,PVC MPs会提高光合碳在SOC中的比例[35]。
本研究仍存在一些局限性,需要在未来的研究中予以完善。首先,最主要的一点是,本研究未能直接监测和量化实验周期内微塑料自身的降解情况。本研究未能通过测定质量损失、粒径变化、表面形貌或化学结构改变等指标,来直接验证可生物降解塑料(PBAT、PBS、PLA)的实际降解速率和程度,也未能确认传统塑料(PE、PS)在此期间是否发生了老化或微量物质的释放。这一限制使得关于作用机制的讨论主要建立在对DOM分子特征变化的间接推断之上。例如,本研究认为可生物降解微塑料因其降解产物可作为微生物的直接碳源,从而改变了DOM的组分。尽管DOM的分析结果(如微生物源类腐殖质组分C1和C2的增加)为这一假说提供了有力支持,但缺乏微塑料降解的直接数据,使得本研究无法建立降解速率与DOM变化之间的定量关系。因此,未来的研究应将微塑料颗粒的物理化学状态变化与土壤DOM的响应更紧密地结合起来。通过同步监测微塑料的降解动态和土壤DOM的组分演变,将能够更直接、更明确地揭示不同类型微塑料影响土壤碳循环的内在机制。这将有助于本研究更精确地区分由塑料降解产生的直接化学效应和由其物理存在引发的间接效应(如“激发效应”),从而更全面地评估其长期的生态环境风险。
本研究的发现具有重要的环境与政策意义。从分子特征(更高的AI和NOSC值)上看,微塑料的存在似乎增加了DOM的稳定性,这可能对土壤碳汇的长期固存有潜在影响。然而,被视为“绿色”替代品的可生物降解塑料,本研究表明它们能显著改变土壤DOM的分子组成,特别是增加了含氮、硫的复杂有机分子的产生。这对于土壤氮、硫等关键元素的生物地球化学循环可能产生的长远影响,尚不明确。这些发现为全面评估微塑料(包括可生物降解类型)的环境风险,以及制定相关的塑料管控政策,提供了新的科学依据。未来仍需更多研究关注不同类型微塑料对土壤-植物体系中碳氮耦合循环动态变化的影响。
4 结论本研究探讨了土壤-玉米体系下,较低浓度微塑料污染对土壤溶解性有机质的影响。结果表明,与对照组相比,微塑料可增加土壤DOC含量,增加土壤DOM的腐殖化程度和稳定性;可生物降解的微塑料增加微生物来源类腐殖质C1和C2组分的相对含量;同时,微塑料降低土壤-植物体系中DOM分子的H/C值,提高NOSC和AI值,增加土壤DOM腐殖化程度,降低氨基酸、碳水化合物和蛋白质类分子的相对含量。研究为揭示微塑料扰动土壤-植物体系中DOM组成变化提供了分子机制,并为理解微塑料对土壤-植物体系中土壤碳过程的影响提供了理论支持。
| [1] |
Andrady A L, Neal M A. Applications and societal benefits of plastics[J]. Philosophical Transactions of the Royal Society of London Series B, Biological Sciences, 2009, 364(1526): 1977-1984. DOI:10.1098/rstb.2008.0304
(  0) 0) |
| [2] |
Geyer R, Jambeck J R, Law K L. Production, use, and fate of all plastics ever made[J]. Science Advances, 2017, 3(7): e1700782. DOI:10.1126/sciadv.1700782
(  0) 0) |
| [3] |
Thompson R C, Olsen Y, Mitchell R P, et al. Lost at sea: Where is all the plastic[J]. Science, 2004, 304(5672): 838. DOI:10.1126/science.1094559
(  0) 0) |
| [4] |
Peng X, Chen M, Chen S, et al. Microplastics contaminate the deepest part of the world's ocean[J]. Geochemical Perspectives Letters, 2018, 9: 1-5.
(  0) 0) |
| [5] |
Rillig M C, Leifheit E, Lehmann J. Microplastic effects on carbon cycling processes in soils[J]. PLoS Biology, 2021, 19(3): e3001130. DOI:10.1371/journal.pbio.3001130
(  0) 0) |
| [6] |
Whalen E D, Grandy A S, Sokol N W, et al. Clarifying the evidence for microbial- and plant-derived soil organic matter, and the path toward a more quantitative understanding[J]. Global Change Biology, 2022, 28(24): 7167-7185. DOI:10.1111/gcb.16413
(  0) 0) |
| [7] |
Fuller S, Gautam A. A procedure for measuring microplastics using pressurized fluid extraction[J]. Environmental Science & Technology, 2016, 50(11): 5774-5780.
(  0) 0) |
| [8] |
Ding Y, Shi Z Q, Ye Q T, et al. Chemodiversity of soil dissolved organic matter[J]. Environmental Science & Technology, 2020, 54(10): 6174-6184.
(  0) 0) |
| [9] |
Liu H F, Yang X M, Liang C T, et al. Interactive effects of microplastics and glyphosate on the dynamics of soil dissolved organic matter in a Chinese loess soil[J]. Catena, 2019, 182: 104177. DOI:10.1016/j.catena.2019.104177
(  0) 0) |
| [10] |
Shi J, Sun Y Z, Wang X, et al. Microplastics reduce soil microbial network complexity and ecological deterministic selection[J]. Environmental Microbiology, 2022, 24(4): 2157-2169. DOI:10.1111/1462-2920.15955
(  0) 0) |
| [11] |
Peng C, Wang J, Liu X H, et al. Differences in the plastispheres of biodegradable and non-biodegradable plastics: A mini review[J]. Frontiers in Microbiology, 2022, 13: 849147. DOI:10.3389/fmicb.2022.849147
(  0) 0) |
| [12] |
Narancic T, Verstichel S, Chaganti S R, et al. Biodegradable plastic blends create new possibilities for end-of-life management of plastics but they are not a panacea for plastic pollution[J]. Environmental Science & Technology, 2018, 52(18): 10441-10452.
(  0) 0) |
| [13] |
Qin M, Chen C Y, Song B, et al. A review of biodegradable plastics to biodegradable microplastics: Another ecological threat to soil environments[J]. Journal of Cleaner Production, 2021, 312: 127816. DOI:10.1016/j.jclepro.2021.127816
(  0) 0) |
| [14] |
[LinkOut] J, Coffin S, Sun C L, et al. Negligible effects of microplastics on animal fitness and HOC bioaccumulation in earthworm Eisenia fetida in soil[J]. Environmental Pollution, 2019, 249: 776-784. DOI:10.1016/j.envpol.2019.03.102
(  0) 0) |
| [15] |
Bao S D
. Soil and agricultural chemistry analysis (In Chinese). 3rd ed[M]. Beijing: China Agriculture Press, 2000. [鲍士旦
. 土壤农化分析[M]. 3版. 北京: 中国农业出版社, 2000.]
(  0) 0) |
| [16] |
Zhang G L, Gong Z T
. Soil survey laboratory methods (In Chinese). Beijing: Science Press, 2012. [张甘霖, 龚子同
. 土壤调查实验室分析方法[M]. 北京: 科学出版社, 2012.]
(  0) 0) |
| [17] |
Murphy K R, Butler K D, Spencer R G M, et al. Measurement of dissolved organic matter fluorescence in aquatic environments: An interlaboratory comparison[J]. Environmental Science & Technology, 2010, 44(24): 9405-9412.
(  0) 0) |
| [18] |
Wu M, Li P F, Li G L, et al. The chemodiversity of paddy soil dissolved organic matter is shaped and homogenized by bacterial communities that are orchestrated by geographic distance and fertilizations[J]. Soil Biology and Biochemistry, 2021, 161: 108374. DOI:10.1016/j.soilbio.2021.108374
(  0) 0) |
| [19] |
Li Y, Harir M, Lucio M, et al. Proposed guidelines for solid phase extraction of Suwannee River dissolved organic matter[J]. Analytical Chemistry, 2016, 88(13): 6680-6688. DOI:10.1021/acs.analchem.5b04501
(  0) 0) |
| [20] |
Li X M, Sun G X, Chen S C, et al. Molecular chemodiversity of dissolved organic matter in paddy soils[J]. Environmental Science & Technology, 2018, 52(3): 963-971.
(  0) 0) |
| [21] |
He Y H, Cheng W X, Zhou L Y, et al. Soil DOC release and aggregate disruption mediate rhizosphere priming effect on soil C decomposition[J]. Soil Biology and Biochemistry, 2020, 144: 107787. DOI:10.1016/j.soilbio.2020.107787
(  0) 0) |
| [22] |
Finzi A C, Abramoff R Z, Spiller K S, et al. Rhizosphere processes are quantitatively important components of terrestrial carbon and nutrient cycles[J]. Global Change Biology, 2015, 21(5): 2082-2094. DOI:10.1111/gcb.12816
(  0) 0) |
| [23] |
Blagodatskaya E, Yuyukina T, Blagodatsky S, et al. Three-source-partitioning of microbial biomass and of CO2 efflux from soil to evaluate mechanisms of priming effects[J]. Soil Biology and Biochemistry, 2011, 43(4): 778-786. DOI:10.1016/j.soilbio.2010.12.011
(  0) 0) |
| [24] |
Moore T R, Dalva M. Some controls on the release of dissolved organic carbon by plant tissues and soils[J]. Soil Science, 2001, 166(1): 38-47. DOI:10.1097/00010694-200101000-00007
(  0) 0) |
| [25] |
Schmidt M W I, Torn M S, Abiven S, et al. Persistence of soil organic matter as an ecosystem property[J]. Nature, 2011, 478(7367): 49-56. DOI:10.1038/nature10386
(  0) 0) |
| [26] |
Liu J, Chen X F, Li D M, et al. Variation of soil dissolved organic carbon under long-term different fertilizations and its correlation with maize yields[J]. Journal of Soils and Sediments, 2020, 20(7): 2761-2770. DOI:10.1007/s11368-020-02631-1
(  0) 0) |
| [27] |
Stedmon C A, Markager S. Tracing the production and degradation of autochthonous fractions of dissolved organic matter by fluorescence analysis[J]. Limnology and Oceanography, 2005, 50(5): 1415-1426. DOI:10.4319/lo.2005.50.5.1415
(  0) 0) |
| [28] |
Bradford M A, Keiser A D, Davies C A, et al. Empirical evidence that soil carbon formation from plant inputs is positively related to microbial growth[J]. Biogeochemistry, 2013, 113(1): 271-281.
(  0) 0) |
| [29] |
Kuzyakov Y, Xu X L. Competition between roots and microorganisms for nitrogen: Mechanisms and ecological relevance[J]. New Phytologist, 2013, 198(3): 656-669. DOI:10.1111/nph.12235
(  0) 0) |
| [30] |
Kalbitz K, Schwesig D, Schmerwitz J, et al. Changes in properties of soil-derived dissolved organic matter induced by biodegradation[J]. Soil Biology and Biochemistry, 2003, 35(8): 1129-1142. DOI:10.1016/S0038-0717(03)00165-2
(  0) 0) |
| [31] |
Wang F L, Wang X X, Song N N. Polyethylene microplastics increase cadmium uptake in lettuce (Lactuca sativa L.) by altering the soil microenvironment[J]. Science of the Total Environment, 2021, 784: 147133. DOI:10.1016/j.scitotenv.2021.147133
(  0) 0) |
| [32] |
Malik A A, Roth V N, Hébert M, et al. Linking molecular size, composition and carbon turnover of extractable soil microbial compounds[J]. Soil Biology and Biochemistry, 2016, 100: 66-73. DOI:10.1016/j.soilbio.2016.05.019
(  0) 0) |
| [33] |
Textor S R, Wickland K P, Podgorski D C, et al. Dissolved organic carbon turnover in permafrost-influenced watersheds of interior Alaska: Molecular insights and the priming effect[J]. Frontiers in Earth Science, 2019, 7: 275. DOI:10.3389/feart.2019.00275
(  0) 0) |
| [34] |
Qiu Q Y, Wu L F, Ouyang Z, et al. Effects of plant-derived dissolved organic matter (DOM) on soil CO2 and N2O emissions and soil carbon and nitrogen sequestrations[J]. Applied Soil Ecology, 2015, 96: 122-130. DOI:10.1016/j.apsoil.2015.07.016
(  0) 0) |
| [35] |
Hu Z E, Xiao M L, Wu J L, et al. Effects of microplastics on photosynthesized C allocation in a rice-soil system and its utilization by soil microbial groups[J]. Journal of Hazardous Materials, 2024, 466: 133540. DOI:10.1016/j.jhazmat.2024.133540
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


