微纳米塑料污染作为全球性的环境问题,其在海洋、土壤、大气等环境中的生态效应已受到广泛关注,尤其是在陆地生态系统中的赋存状况和负面影响[1]。微纳米塑料主要通过农田地膜覆盖、有机肥或污泥施用、污水灌溉或大气沉降等方式进入土壤环境[2]。土壤中的微纳米塑料不仅会影响土壤结构和性质[3,4],较小粒径的纳米塑料还可以吸附和积累在植物根系的表皮和根毛表面[5],并通过内吞作用或侧根的裂缝进入根系中柱[5,6],在根压和蒸腾拉力的作用下向上运输至茎、叶组织[5,7]。纳米塑料与植物根系的作用引起植物的氧化损伤,诱导脂质过氧化,显著影响植物生长、光合作用和代谢系统等[8,9]。纳米塑料在蔬菜或水果中的积累可能构成严重的食品安全风险,并可能通过饮食和食物链传播,对人类健康构成威胁[10-12]。
烟草作为卷烟的原材料在全国广泛种植,微纳米塑料因覆膜栽培技术的广泛应用、育苗盘等农用塑料制品的使用、污泥堆肥的施用等进入种植土壤,植烟生长过程中根系不可避免地与土壤中的微纳米塑料相互作用。作为嗜好类经济作物,烟草的生长发育与生长代谢对其经济价值至关重要,尤其是烟叶的品质。研究表明,高温、干旱等环境胁迫下烟草碳氮等代谢协调平衡被打破,促进碳氮差异代谢物的产生以提高植物抗逆性,影响烟草生长发育,降低了烟叶的品质和产量[13]。然而,目前针对土壤微纳米塑料对烟草生长、生理及关键代谢物的调控机制研究还不够全面。
因此,本研究以土壤中常见的聚苯乙烯纳米塑料(PS-NPs)为目标污染物,以模式植物本氏烟草(Nicotiana benthamiana)为研究对象,通过盆栽和水培试验综合探究了不同浓度PS-NPs根系暴露对烟草幼苗生长发育、生理代谢的影响,研究结果有助于深入理解土壤生态系统中微纳米塑料所带来的环境和健康风险。
1 材料与方法 1.1 供试材料供试烟草为本氏烟草(Nicotiana benthamiana),来自中国农业科学院烟草研究所。盆栽试验中供试土壤为营养土与蛭石的混合物(1︰3,m/m),土壤pH为5.5,其他性质如表 1所示。
|
|
表 1 盆栽试验中营养土的基本性质 Table 1 Nutrient soil properties in pot experiments |
PS-NPs采用乳液聚合法[14]制备:三口烧瓶中加入0.050 4 g十二烷基硫酸钠(SDS)和85 mL去离子水,混合搅拌,同时加入7.60 g苯乙烯单体。将反应体系在75℃水浴条件下保持5 min后逐滴滴入过硫酸钾(KPS)溶液(称取0.301 9 g KPS溶解于9.43 mL去离子水),最后75℃水浴反应保持5 h,水浴过程中保持搅拌。反应完成后,将反应产物转移至1000 Da分子截留量的透析袋中去除多余的SDS、苯乙烯单体和KPS。产物经冷冻干燥后,根据干燥前后的质量损失计算其质量浓度。采用动态光散射(Zetasizer Nano ZS90,英国)测定PS-NPs的粒径和zeta电位。扫描电子显微镜(Quanta 250 FEG,美国)观察PS-NPs的微观形貌。傅里叶变换红外光谱(Nicolet iS50,美国)表征了PS-NPs的化学组成。
1.2 盆栽试验设计与处理本氏烟草种子经70%酒精清洗1 min,去离子水冲洗3次,风干后采用土培法进行育苗。烟草种子发芽7天后,从育苗盘中选取长势一致的幼苗,小心转移至上口直径为7 cm、高度为7 cm的塑料花盆中。试验共设置4个处理,分别为每千克混合土壤中均匀掺入0、150、500和800 mg PS-NPs。各处理设置15个花盆,各花盆中移入1株烟草幼苗。烟草放置在22 ± 1℃、光照强度为80 μmol·m–2·s–1的生长室中培养35天(烟草幼苗长至11~12片真叶)后收集植物样品。培养期间每5天浇水1次,保持60%~70%的相对湿度,每天光照16 h。
1.3 水培试验设计与处理烟草育苗处理同1.2节。待烟草种子发芽14天后,轻轻将幼苗从土壤中移出,用去离子水仔细清洗根系。随即将每株幼苗转移至含有45 mL 1/4霍格兰营养液(Hoagland nutrient solution,HNS)的50 mL棕色离心管中,置于与1.2节相同条件的生长室中平衡7天。然后将烟草幼苗分别置于PSNPs浓度为0、50、150 μg·mL–1的1/4 HNS中。每个处理设置20个重复,生长30天(烟草幼苗长至11~12片真叶)后进行相关测定。整个处理过程中,每隔6天补充一次营养液,以补充蒸发的水分。
1.4 样品采集与分析用最小刻度为1 mm的钢尺量取盆栽(暴露于PS-NPs 35天)烟草幼苗的株高,以及水培(暴露于PS-NPs 30天)烟草幼苗的株高、根长。用万分之一电子天平(Sartorius,美国)称量水培试验烟草幼苗整株鲜重,在105℃杀青15 min后于80℃烘干至恒重。采集水培试验,烟草从下向上数第6~9片真叶,减去主叶脉后,剪碎混匀,然后使用试剂盒测定烟草叶片与根系中过氧化氢(Hydrogen peroxide,H2O2)、超氧化物歧化酶(Superoxide Dismutase,SOD)及丙二醛(Malondialdehyde,MDA)的含量。盆栽试验(暴露于PS-NPs 35天)烟草第6~9片真叶剪去主叶脉后,置于烘箱40℃烘干。使用试剂盒测定叶片可溶性糖、可溶性蛋白及淀粉含量。
1.5 烟草非靶向代谢组学分析采取盆栽试验中暴露于0和800 mg·kg–1 PS-NPs 35天后的烟草根系和叶片样本。从整个根系中提取样本,用0.01 mol·L–1磷酸盐缓冲液快速洗除土壤。叶片统一选取植株中部的叶片。根系和叶片样品均用锡纸包裹,液氮冷冻15 min,–80℃保存备用。送至奥维森基因科技有限公司(Allwegene,北京)进行非靶向代谢组学分析。采用气相色谱-飞行时间质谱联用(GC-TOF-MS)对样品进行分析。每个处理组包括6个生物重复。
1.6 数据处理采用Origin 2024绘制图形,使用SPSS 22.0统计软件在P<0.05水平上进行单因素方差分析(ANOVA)。
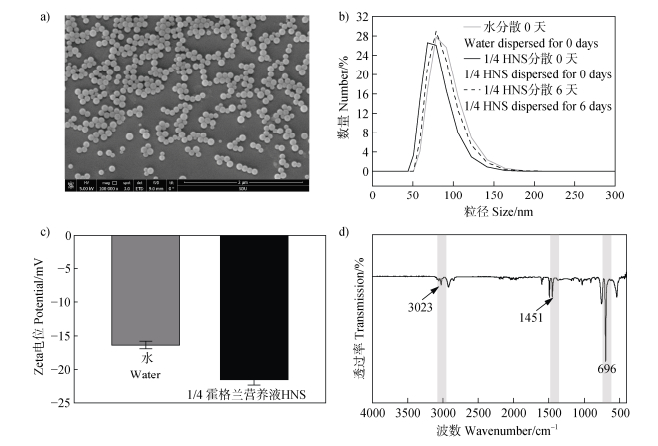
2 结果 2.1 PS-NPs的合成与表征采用乳液聚合法制备PS-NPs。扫描电镜观察(图 1a)显示PS-NPs呈规则的球形颗粒状,粒径约90 nm,分布均匀。由图 1b可知,PS-NPs在水溶液和1/4 HNS中均分散良好,且PS-NPs在1/4 HNS中分散6天后无明显团聚。图 1c的Zeta电位结果表明,PS-NPs在水溶液(pH 6.9)和1/4 HNS(pH 6.8)中的电位分别为–16.37 ± 0.55 mV和-21.63 ± 0.80 mV。图 1d为PS-NPs的傅里叶变换红外光谱。强吸收峰3000~3100 cm–1对应于PS-NPs中苯环的芳香C-H伸缩振动;接近1400 cm–1的强吸收峰为苯环的C-H键变角振动;700 cm–1附近的强吸收峰为单取代苯环上氢原子的面外变角振动。结果进一步证明了分散均匀且带有负电荷的PS-NPs的成功合成。
|
注:a)SEM图像;b)PS-NPs在水中及1/4HNS中分散0天和6天后的水合粒径;c)PS-NPs在水及1/4HNS中的zeta电位;d)傅里叶红外光谱。 Note: a) SEM image; b) the hydrated particle size of PS-NPs in water and after 0 and 6 days of dispersion in 1/4 HNS; c) zeta potential of PS-NPs in water and 1/4 HNS; d) FTIR of PS-NPs. 图 1 PS-NPs的表征 Fig. 1 Characterization of PS-NPs |
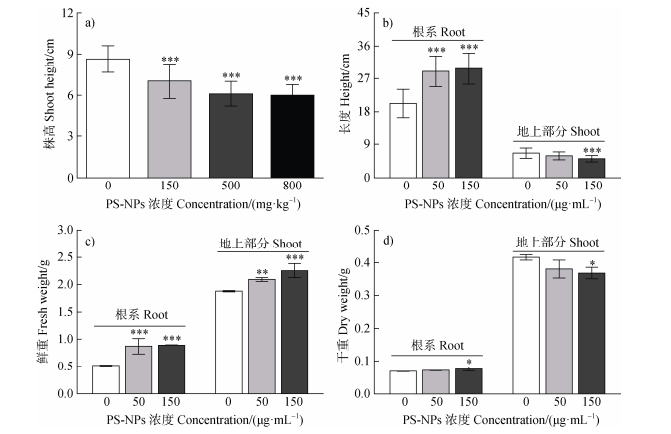
盆栽试验表明,烟草根系暴露于PS-NPs 35天后,150、500和800 mg·kg–1PS-NPs处理组烟草幼苗地上部分的高度较对照组显著降低,降幅分别为18.80%、29.42%和30.67%(图 2a)。水培试验结果表明,与对照组相比,根系暴露于50 μg·mL–1和150 μg·mL–1 PS-NPs 30天后,水培烟草幼苗的根长分别增加了43.52% 和47.20%(P < 0.05,图 2b),烟草幼苗地上部分高度显著降低(图 2b);水培烟草幼苗根系和地上部分的鲜重均显著增加(P < 0.05,图 2c),150 μg·mL–1 PS-NPs处理组水培烟草地上部分的干重显著降低(P < 0.05,图 2d)。
|
注:“*”表示不同处理间差异显著(* P < 0.05;** P < 0.01;*** P < 0.001)。下同。 Note: "*" indicates significant differences among different treatments (* P < 0.05;** P < 0.01;*** P < 0.001).The same below. 图 2 PS-NPs根系暴露对烟草幼苗生长的影响 Fig. 2 Effects of PS-NPs root exposure on the growth of N. benthamiana seedlings |
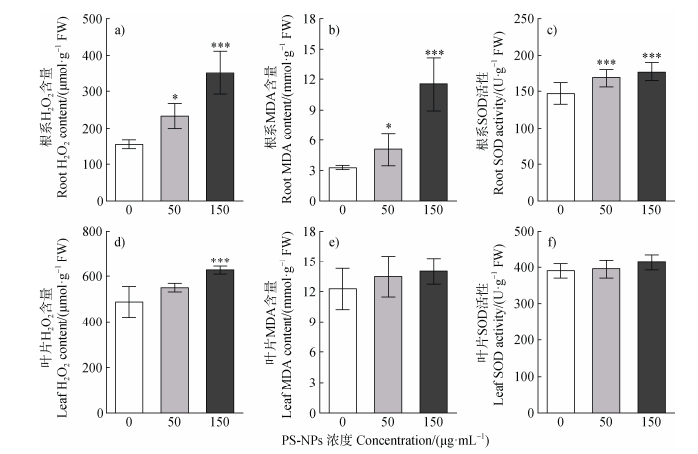
水培试验PS-NPs根系暴露30天后,与对照组相比,PS-NPs显著增加了烟草幼苗根系中H2O2和MDA的含量(P < 0.05,图 3a,图 3b),且50 μg·mL–1和150 μg·mL–1 PS-NPs处理组根系中SOD的活性显著增加,增幅分别为14.48%和20.53%(P < 0.05,图 3c);高浓度150 μg·mL–1 PS-NPs处理下烟草幼苗叶片中H2O2含量较对照组显著增加了15.81%(P < 0.05,图 3d),而MDA的含量及SOD的活性均无显著变化(P > 0.05,图 3e,图 3f)。因此,PS-NPs根系暴露对根系的抗氧化酶系统造成显著损伤,引起根系中H2O2的产生及根系脂质过氧化,且根系防御性地增加了SOD活性以减少氧化损伤。
|
图 3 PS-NPs根系暴露对烟草幼苗的氧化损伤 Fig. 3 Oxidative damage to N. benthamiana seedlings by PS-NPs root exposure |
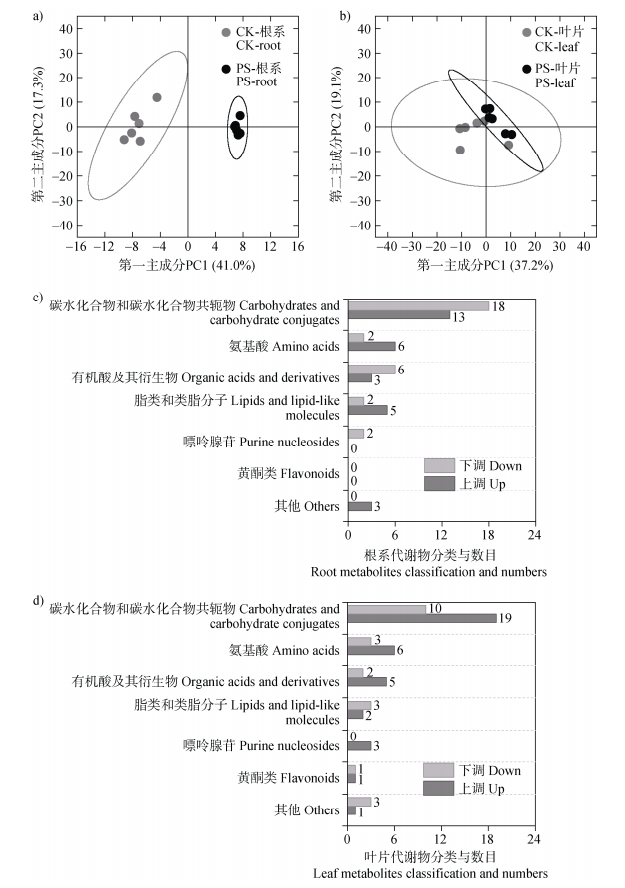
对盆栽试验中暴露于0和800 mg·kg–1 PS-NPs 35天后的烟草根系和叶片进行了非靶向代谢组学测定。通过主成分分析(PCA)图发现,植物根系中对照组与处理组的分离程度(图 4a),相较于叶片更为明显(图 4b),表明PS-NPs对烟草根系代谢物的影响大于对烟草叶片代谢物的影响。分别在烟草根系和叶片中鉴定筛选(VIP > 1)出60种和59种差异代谢产物,差异代谢产物主要包括碳水化合物、氨基酸、有机酸、脂类相关代谢物(图 4c、图 4d)。
|
注:a)对照组与PS-NPs组根系代谢产物的主成分分析;b)对照组与PS-NPs组叶片代谢产物的主成分分析;c)PS-NPs处理下根系中不同种类上调和下调的差异代谢产物的数目;d)PS-NPs处理下叶片中不同种类上调和下调的差异代谢产物的数目。 Note: a) principal component analysis of root metabolites in control and PS-NPs groups; b) Principal component analysis of leaf metabolites in control and PS-NPs groups; c) up-regulated and down-regulated number of different metabolites in root under PS-NPs treatment. d) up-regulated and down-regulated number of different metabolites in leaf under PS-NPs treatment. 图 4 烟草幼苗体内代谢产物的主成分分析和分类 Fig. 4 Principal component analysis and classification of N. benthamiana seedlings' metabolites |
与对照组相比,800 mg·kg–1 PS-NPs处理组根系中苏氨酸、异亮氨酸、脯氨酸、缬氨酸等氨基酸及丁酮酸、草乙酸、3-羟基丙酸等有机酸显著上调(图 5a)。叶片中丙氨酸、N-乙基甘氨酸、N-乙酰-L-亮氨酸等氨基酸及柠檬酸、琥珀酸等有机酸含量显著上调(图 5b)。葡萄糖-6-磷酸、果糖-6-磷酸及果糖-1,6-二磷酸等糖酵解途径相关产物在根系中显著下调,而在叶片中均显著上调。叶片中新橙皮苷、肌醇及根系中核糖醇、肌醇等抗氧化物质显著上调。此外,柠檬酸、α-酮戊二酸是TCA循环中重要的中间产物,对植物的能量代谢有积极作用,它们在根系中显著下调说明PS-NPs影响了烟草体内的能量代谢。

|
注:a)PS-NPs处理下根系中上调和下调的差异代谢产物;b)PS-NPs处理下叶片中上调和下调的差异代谢产物。其中,代谢物颜色表示log2(FC)值的大小,红色表示上调的差异代谢物,蓝色表示下调的差异代谢物,颜色越深,表示差异程度越大。 Note: a) Up-and down-regulated differential metabolites in roots under PS-NPs treatment; b) Up-and down-regulated differential metabolites in leaves under PS-NPs treatment. The color of metabolites indicates the magnitude of log2 (FC) values, with red representing upregulated differential metabolites and blue indicating downregulated differential metabolites. The deeper the color, the higher the extent of differential expression. 图 5 烟草幼苗根系和叶片中主要的差异代谢物 Fig. 5 The main differential metabolites in roots and leaves of N. benthamiana seedlings |
烟草根系和叶片中差异代谢物主要涉及的代谢途径为碳代谢、ABC转运蛋白、TCA循环、乙醛酸和二羧酸代谢、甘油酯代谢、半乳糖代谢、糖酵解及氧化磷酸化途径。PS-NPs也显著扰乱了丙氨酸、天冬氨酸及谷氨酸代谢、抗坏血酸和醛糖代谢、淀粉和蔗糖代谢(图 6a,图 6b)。此外,PS-NPs根系暴露显著干扰了烟草叶片中类黄酮生物合成、丙酮酸和酪氨酸代谢(图 6b)。

|
注:a)烟草根系代谢通路分析;b)烟草叶片代谢通路分析。气泡颜色表示富集分析的P-value,颜色越深表示富集程度越显著,点的大小代表富集到该通路的差异代谢物的个数。 Note: a) analysis of metabolic pathways in N. benthamiana root; b) analysis of metabolic pathways in N. benthamiana leaf. The bubble color indicates the P-value of the enrichment analysis, the darker color indicates the more significant degree of enrichment, and the size of the dot represents the number of differential metabolites enriched to this pathway. 图 6 PS-NPs根系暴露下烟草幼苗体内差异代谢物的KEGG通路富集 Fig. 6 KEGG pathways enriched for differential metabolites in N. benthamiana seedlings under PS-NPs root exposure |
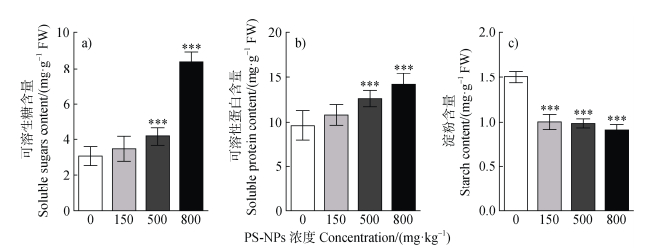
为了探究代谢途径的改变如何影响关键代谢物,本研究对盆栽烟草新鲜叶片中可溶性糖、淀粉和可溶性蛋白含量进行了定量分析。与对照组相比,500和800 mg·kg–1 PS-NPs使烟草新鲜叶片中可溶性糖和可溶性蛋白的含量均显著增加,800 mg·kg–1 PS-NPs处理组可溶性糖和可溶性蛋白含量分别为对照组含量的2.74倍和1.48倍(P < 0.001,图 7a,图 7b);150、500和800 mg·kg–1 PS-NPs处理组烟草叶片中淀粉含量较对照组显著降低,降幅分别为33.46%、34.54%和39.31%(P < 0.001,图 7c)。
|
图 7 PS-NPs根系暴露对烟草幼苗叶片碳氮代谢物的影响 Fig. 7 Effects of PS-NPs root exposure on carbon and nitrogen metabolites in leaves of N. benthamiana seedling |
PS-NPs根系暴露表现出对烟草幼苗地上部分生长的抑制作用(株高降低和干重减小)(图 2a,图 2b,图 2d)。而且,PS-NPs根系暴露促进了根系的伸长(图 2b),对烟草生物量,尤其是根系和地上部分鲜重有显著促进作用(图 2c),这与前人研究结果[15-16]一致。此外,PS-NPs根系暴露诱导烟草体内活性氧的产生,并引起根系中抗氧化酶系统的积极响应(图 3)。根系伸长相对敏感,可能是植物进化中存在胁迫效应或其他非急性毒理学效应的标志[17]。烟草根系在感知到PS-NPs胁迫后,根系的伸长与生物量增加是一种低质量的应激性徒长。根系中葡萄糖-6-磷酸、果糖-6-磷酸等糖酵解产物及柠檬酸、α-酮戊二酸等TCA循环中间产物显著下调(图 5a),表明根系内部实际处于碳饥饿与能量缺乏状态[18],被迫通过积累脯氨酸、苏氨酸、缬氨酸、异亮氨酸等氨基酸维持根系细胞的生存代谢,同时合成多元醇(肌醇显著上调)等物质以被动抵御胁迫(图 5a)。这些代谢紊乱导致根系虽应激性伸长、鲜重增加,但实际上是低质量、低功能的徒长。同时,PS-NPs对根系吸收和运输的影响会抑制地上部的生长[5],导致株高降低。烟草地上部分接收到胁迫信号后,通过渗透调节导致细胞吸水增多和可溶性物质积累(可溶性糖和可溶性蛋白含量显著增加)造成“虚胖”。烟草叶片通过积累葡萄糖-6-磷酸等磷酸己糖与可溶性糖,将氮资源转向可溶性防御蛋白及黄酮类物质(新橙皮苷显著上调)的合成(图 5b)。这必然抑制了叶片中结构性物质(纤维素、蛋白质)的合成,导致株高降低与干重减少。
氨基酸也参与植物体内能量代谢,在植物面临各种胁迫时产生不同程度的累积。根系和叶片中丙氨酸、天冬氨酸及谷氨酸代谢、氨基酸生物合成等途径显著扰动以应对PS-NPs的胁迫(图 6a,图 6b)。PS-NPs引起烟草根系中叶植醇、肌醇含量的显著上调(图 5a)。植醇可用于合成脂溶性抗氧化物质维生素E,可以保护脂质免受氧化损伤[19];肌醇可能通过提高渗透保护物质(如脯氨酸)的积累和改善活性氧清除相关抗氧化酶活性,提高烟草根系对PS-NPs的耐受性[20]。根系丁酮酸、草乙酸、3-羟基丙酸等有机酸的释放也增加了根系对PS-NPs的耐受性(图 5a)。烟草体内碳代谢、淀粉与蔗糖代谢的扰动导致叶片中葡萄糖、蔗糖等代谢物显著上调(图 5b,图 6b)。脂质是生物膜的基本成分,在离子运输、信号传导中起着重要作用,脂质代谢在植物适应非生物胁迫中尤为重要[21]。PS-NPs暴露还刺激了根系和叶片中半乳糖代谢途径的变化(图 6a和图 6b)。先前的研究表明[15],植物可以通过增加体内半乳糖含量来增强对外部胁迫耐受性。因此,暴露于PS-NPs之后,根系和叶片中碳代谢、TCA循环、甘油脂代谢及半乳糖途径的扰动,均与烟草对PS-NPs的耐受性有关。
3.2 PS-NPs对烟草碳氮代谢的影响PS-NPs胁迫彻底扰乱了烟草体内的碳代谢平衡。PS-NPs胁迫下,根系碳代谢呈现高能耗的应激状态:柠檬酸、α-酮戊二酸、磷酸己糖(如葡萄糖-6-磷酸)与纤维二糖醇均显著下调(图 5a),表明碳骨架被大量消耗于基础产能,导致结构性碳水化合物(如纤维素)合成受阻。碳流无法有效用于根系结构建造,而是被引向脯氨酸、肌醇等渗透调节物质的合成,以及通过积累有机酸(如草酰乙酸)以维持衰竭的TCA循环(图 5a)。烟草地上部的叶片则通过分解淀粉、积累磷酸己糖和可溶性糖,将碳源导向用于渗透调节的可溶性糖及黄酮类(如新橙皮苷)等次生防御代谢物的合成(图 5b,图 7a)。
PS-NPs根系暴露同时引发了烟草氮代谢的系统性失衡与防御性转向。根系的氮代谢中丝氨酸、脯氨酸及支链氨基酸(缬氨酸、异亮氨酸等)的显著上调(图 5a),表明PS-NPs可能将氮源固结于渗透调节和氮库中,以应对局部胁迫;而2,4-二氨基丁酸的下调(图 5a),则表明其氮代谢趋于保守,可能限制了特定多胺合成路径的氮消耗。叶片的氮代谢则积极转向主动防御与信号传导,4-氨基丁酸(GABA)与2,4-二氨基丁酸(GABA衍生物)的显著上调(图 5b),标志着GABA支路这一关键应激系统的激活,它不仅参与碳氮平衡的重新调节,更在氧化应激响应和信号传导中发挥核心作用[22]。同时,叶片中丙氨酸、N-乙基甘氨酸等非蛋白氨基酸的积累(图 5b),进一步体现了氮流被重新导向合成应激代谢物,以激活烟草体内对PS-NPs的系统性化学防御。
目前研究主要聚焦于PS-NPs根系暴露对本氏烟草幼苗生长和生理代谢的影响,这种影响可能会因植物种类、栽培方法、NPs类型、处理时间及浓度等不同而有差异。未来需要进一步探究真实土壤环境中,NPs在烟草体内的吸收和转运路径及长期(全生育期甚至多代)低剂量暴露会对烟草生长、产量和品质产生何种慢性、累积性影响。
4 结论PS-NPs根系暴露显著影响了烟草的生长发育,导致烟草根系伸长、株高降低及地上部分干重减少。PS-NPs根系胁迫下诱导了烟草体内活性氧的产生,引起根系抗氧化酶系统的有效防御。烟草的生理代谢对PS-NPs的胁迫做出协调性响应,扰动了碳代谢、氨基酸代谢、乙醛酸和二羧酸代谢、甘油脂代谢、有机酸代谢等代谢通路,碳水化合物、氨基酸、抗氧化物质、有机酸等代谢物含量显著上调。此外,PS-NPs根系胁迫下对烟草体内碳氮代谢的扰乱,显著影响了烟草新鲜叶片中碳氮代谢物的含量,包括可溶性糖和可溶性蛋白含量显著增加,淀粉含量显著降低。本研究系统地揭示了PS-NPs胁迫下烟草碳氮代谢的重编程机制:在碳代谢层面,根系陷入碳饥饿,而叶片通过碳截留将资源转向防御性次生代谢;在氮代谢层面,根系强化渗透调节功能,而叶片则激活系统性防御合成,这种器官特异性的代谢分工驱动植株完成从生长到抗逆的生存策略转换,为理解微纳米塑料的植物效应提供了新的代谢视角。
| [1] |
Liu X B, Dong X S, Xie Z H, et al. Ecological effects and biodegradation of microplastics in soils (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(2): 349-363. DOI:10.11766/trxb202102240040 [刘鑫蓓, 董旭晟, 解志红, 等. 土壤中微塑料的生态效应与生物降解[J]. 土壤学报, 2022, 59(2): 349-363.]
(  0) 0) |
| [2] |
Luo Y M, Zhou Q, Zhang H B, et al. Pay attention to research on microplastic pollution in soil for prevention of ecological and food chain risks (In Chinese)[J]. Bulletin of the Chinese Academy of Sciences, 2018, 33(10): 1021-1030. [骆永明, 周倩, 章海波, 等. 重视土壤中微塑料污染研究防范生态与食物链风险[J]. 中国科学院院刊, 2018, 33(10): 1021-1030.]
(  0) 0) |
| [3] |
Liu S M, Chen F T, Kong F L, et al. Effects of polyethylene microplastics with different particle sizes on characteristics of agricultural soil (In Chinese)[J]. Soils, 2025, 57(2): 387-397. [刘书铭, 陈飞潼, 孔范龙, 等. 不同粒径聚乙烯微塑料对农田土壤特性的影响[J]. 土壤, 2025, 57(2): 387-397.]
(  0) 0) |
| [4] |
Kou S Q, Guan Z, Lu X Y, et al. Migration of microplastics in soil and its effect on organic pollutants: A Review (In Chinese)[J]. Soils, 2024, 56(3): 457-470. [寇诗棋, 关卓, 鲁旭阳, 等. 土壤中微塑料迁移及其对有机污染物的影响研究进展[J]. 土壤, 2024, 56(3): 457-470.]
(  0) 0) |
| [5] |
Sun X D, Yuan X Z, Jia Y B, et al. Differentially charged nanoplastics demonstrate distinct accumulation in Arabidopsis thaliana[J]. Nature Nanotechnology, 2020, 15(9): 755-760. DOI:10.1038/s41565-020-0707-4
(  0) 0) |
| [6] |
Li L Z, Luo Y M, Li R J, et al. Effective uptake of submicrometre plastics by crop plants via a crack-entry mode[J]. Nature Sustainability, 2020, 3(11): 929-937. DOI:10.1038/s41893-020-0567-9
(  0) 0) |
| [7] |
Lu L L, Tian S K, Yang X E, et al. Enhanced root-to-shoot translocation of cadmium in the hyperaccumulating ecotype of Sedum alfredii[J]. Journal of Experimental Botany, 2008, 59(11): 3203-3213. DOI:10.1093/jxb/ern174
(  0) 0) |
| [8] |
Wang Y, Xiang L L, Wang F, et al. Positively charged microplastics induce strong lettuce stress responses from physiological, transcriptomic, and metabolomic perspectives[J]. Environmental Science & Technology, 2022, 56(23): 16907-16918.
(  0) 0) |
| [9] |
Dang F, Wang Q Y, Yan X L, et al. Threats to terrestrial plants from emerging nanoplastics[J]. ACS Nano, 2022, 16(10): 17157-17167. DOI:10.1021/acsnano.2c07627
(  0) 0) |
| [10] |
Jiang M, Wang B Q, Ye R, et al. Evidence and impacts of nanoplastic accumulation on crop grains[J]. Advanced Science, 2022, 9(33): 2202336. DOI:10.1002/advs.202202336
(  0) 0) |
| [11] |
Feng Y D, Yang J, Tu C, et al. Biological health effects and food-chain transfer risks of micro/nano plastics in soil (In Chinese)[J]. Journal of Ecology and Rural Environment, 2023, 39(5): 661-674. [冯裕栋, 杨杰, 涂晨, 等. 土壤中微/纳塑料的生物健康效应和食物链传递风险[J]. 生态与农村环境学报, 2023, 39(5): 661-674.]
(  0) 0) |
| [12] |
Feng X Y, Sun Y H, Zhang S W, et al. Ecological effects of microplastics on soil-plant systems (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(2): 299-313. DOI:10.11766/trxb202007190402 [冯雪莹, 孙玉焕, 张书武, 等. 微塑料对土壤-植物系统的生态效应[J]. 土壤学报, 2021, 58(2): 299-313.]
(  0) 0) |
| [13] |
Zhao H N, Gao S F, Chen P, et al. Research progress in tobacco carbon and nitrogen metabolism and its relationship with quality and stress resistance (In Chinese)[J]. Acta Agriculturae Jiangxi, 2023, 35(6): 10-15. [赵会纳, 高少凡, 陈鹏, 等. 烟草碳氮代谢及其与烟草品质、抗逆性的关系研究进展[J]. 江西农业学报, 2023, 35(6): 10-15.]
(  0) 0) |
| [14] |
Feng L J, Wang J J, Liu S C, et al. Role of extracellular polymeric substances in the acute inhibition of activated sludge by polystyrene nanoparticles[J]. Environmental Pollution, 2018, 238: 859-865. DOI:10.1016/j.envpol.2018.03.101
(  0) 0) |
| [15] |
Lian J P, Wu J N, Xiong H X, et al. Impact of polystyrene nanoplastics (PSNPs) on seed germination and seedling growth of wheat (Triticum aestivum L.)[J]. Journal of Hazardous Materials, 2020, 385: 121620. DOI:10.1016/j.jhazmat.2019.121620
(  0) 0) |
| [16] |
Li S X, Wang T Y, Guo J H, et al. Polystyrene microplastics disturb the redox homeostasis, carbohydrate metabolism and phytohormone regulatory network in barley[J]. Journal of Hazardous Materials, 2021, 415: 125614. DOI:10.1016/j.jhazmat.2021.125614
(  0) 0) |
| [17] |
Barrena R, Casals E, Colón J, et al. Evaluation of the ecotoxicity of model nanoparticles[J]. Chemosphere, 2009, 75(7): 850-857. DOI:10.1016/j.chemosphere.2009.01.078
(  0) 0) |
| [18] |
Zhang J, Yang D S, Li M X, et al. Metabolic profiles reveal changes in wild and cultivated soybean seedling leaves under salt stress[J]. PLoS One, 2016, 11(7): e0159622. DOI:10.1371/journal.pone.0159622
(  0) 0) |
| [19] |
Xie Q J, Michaeli S, Peled-Zehavi H, et al. Chloroplast degradation: One organelle, multiple degradation pathways[J]. Trends in Plant Science, 2015, 20(5): 264-265. DOI:10.1016/j.tplants.2015.03.013
(  0) 0) |
| [20] |
Hu L Y, Yue H, Zhang J Y, et al. Overexpression of MdMIPS1 enhances drought tolerance and water-use efficiency in apple[J]. Journal of Integrative Agriculture, 2022, 21(7): 1968-1981. DOI:10.1016/S2095-3119(21)63822-4
(  0) 0) |
| [21] |
Wang W C, Pang J Y, Zhang F H, et al. Transcriptomic and metabolomics-based analysis of key biological pathways reveals the role of lipid metabolism in response to salt stress in the root system of Brassica napus[J]. Plant Growth Regulation, 2022, 97(1): 127-141. DOI:10.1007/s10725-021-00788-4
(  0) 0) |
| [22] |
Kinnersley A M, Turano F J. Gamma aminobutyric acid (GABA) and plant responses to stress[J]. Critical Reviews in Plant Sciences, 2000, 19(6): 479-509. DOI:10.1080/07352680091139277
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


