近年来,植物与微塑料(MPs)的相互作用机制成为环境科学领域的研究热点,在“十四五”污染防控中备受关注[1]。尤其在植物对微塑料的吸收途径及土壤微塑料对氮素循环的调控作用方面取得显著进展。研究表明,植物可通过叶片[2]和根系吸收微塑料[3-4],且微塑料的类型、粒径等特性通过改变土壤氮转化过程深刻影响植物氮吸收效率[5]。植物叶片可通过气孔主动吸收大气中的微塑料颗粒。南开大学团队2025年研究证实,聚对苯二甲酸乙二醇酯(PET)和聚苯乙烯(PS)等微塑料能通过气孔进入叶片,经质外体途径迁移至维管组织并积累于腺毛中,脱落酸(ABA)处理关闭气孔后,吸收效率可降低86%[2]。野外调查显示,露天种植蔬菜的微塑料浓度显著高于温室蔬菜,且外层叶片浓度高于新生叶片,表明微塑料随暴露时间累积[2]。大气污染水平、叶片生长周期与微塑料积累量呈正相关,巴黎、上海等城市大气中每立方米微塑料颗粒可达数百至数千个,直接影响植物吸收量[2]。土壤中的微塑料可通过根系表皮细胞间隙或质膜进入植物体内。研究[6]发现,纳米级微塑料(< 100 nm)更易穿透根系细胞壁,而微米级颗粒(1~10 μm)主要通过根毛损伤部位入侵。通过使用共聚焦激光扫描显微镜,Liu等[7]能够验证水稻幼苗对MPs的吸收,在水稻幼苗的根、茎和叶中发现了MPs微球。此外,Nizzetto等[8]报道称,苹果中存在2.17 μm大小的MPs,胡萝卜中存在1.51 μm大小的MPs。此外,研究[9]发现不同植物对微塑料的吸收能力存在显著差异,例如,小麦根系对聚乙烯(PE)微塑料的吸收量是玉米的2.3倍,这与根系分泌物(如有机酸)改变微塑料表面电荷有关。
生长在农田土壤中的作物接触微塑料后会富集,国外学者在多种蔬菜和水果中检测到微塑料,人类可能受其影响[10]。有科学家在妇女胎盘和婴儿粪便中发现微塑料[11-12],这表明微塑料已存在于人体内。纳米粒子对植物有毒性作用[13],与纳米颗粒相似,纳米微塑料也可抑制玉米生长等[14]。鉴于MPs对生态环境和人类健康的严重威胁,迫切需要深入研究微塑料的生物积累性,这不仅有助于拓展对微塑料生态风险的科学认知,也为制定相应环境管理策略提供科学依据。因此,本研究采用玉米为实验材料,通过微观组织成像与宏观生理表型,设计种子萌发协同水培暴露实验,系统探究荧光标记PS-MPs在浓度-粒径双因子调控下的植物吸收路径、转运模式及分子机制,系统评估其对种子萌发、幼苗生长发育的抑制作用,并阐明其毒性作用机制。
1 材料与方法 1.1 验材料供试玉米品种为“沈单16”(Zea mays L.),种子源自甘肃省农业科学院;试验采用天津大鹅科技有限公司提供的单分散红色聚苯乙烯荧光微球(PS-MPs),其核心物理化学参数如下:激发/发射波长分别为620 nm/680 nm,粒径梯度涵盖100、500、1 000及5 000 nm,密度1.05 g·cm–3;微球以25 g·kg–1固体含量单分散于去离子水体系,折射率1.60,变异系数(CV)3%~5%,粒子密度达1.46×108 g–1(3.64×107 mL–1),于4℃~8℃暗环境保存有效期大于等于12个月。
1.2 试验方法试验一:以玉米种子为对象,探究不同浓度(0、20、50、100 mg·L–1,粒径固定100 nm)与粒径(100、500、1 000、5 000 nm,浓度固定100 mg·L–1)的PS-MPs荧光微球于种子萌发阶段的吸收、转运规律及调控机制。实验采用标准化流程:均质种子经40 g·kg–1NaClO表面灭菌后,于含5 mL PS-MPs悬浮液的培养皿(25℃黑暗条件)中培养5 d,以对照组发芽率大于90%为终止阈值,同步记录发芽率(GP)、根长及芽长。
试验二:以三叶一心期玉米幼苗为对象,探究不同粒径不同添加方式的PS-MPs荧光微球在100 mg·L–1浓度条件下对幼苗吸收行为及体内转运特征的作用研究。幼苗经珍珠岩预培养后转移至含PS-MPs的霍格兰(Hoagland)营养液,设置不同粒径的不同添加方式(0、100+5 000、100、5 000nm)为变量,每处理3次重复,培养周期14 d(每7天更换营养液),严格控制光照(14 h·d–1,300 μmol·m–2·s–1)、温度(25℃±2℃)及湿度(60%~70%)。
1.3 指标测定方法 1.3.1 PS-MPs荧光微球在玉米种子和幼苗中的吸收与转运完成发芽及水培暴露试验后,依次清洗胚根、玉米根茎叶并干燥。取新鲜胚根根尖及根、茎、叶样本,将经酒精消毒的样品切割为5 mm小段,在60 g·kg–1琼脂中包埋后于4℃冷藏过夜,随后使用振动切片机切制80 μm的半薄切片,封片后使用激光共聚焦电镜(LCSM,TCSSP8,莱卡,德国)观察,设置红光(激发620 nm/发射680 nm)与绿光(激发488 nm/发射518 nm)双通道荧光检测。每个样品重复5次,成像数据经LASAF软件分析处理。
1.3.2 萌发指标玉米种子萌发标准为胚根大于等于2 mm,每日记录各处理发芽数,5 d后终止试验。统计发芽率(GP=发芽数/总数×100%),测定根长、芽长,终止后取出种子铺于吸水纸,吸干表面水分。
1.3.3 抗氧化酶活性及丙二醛含量所有指标均通过试剂盒进行测定,试剂盒购自Solarbio公司。其中,过氧化氢酶(CAT)对应的货号为BC0200,超氧化物歧化酶(SOD)为BC0170,过氧化物酶(POD)为BC0090,丙二醛(MDA)为BC0020。试剂的配制及保存严格遵循试剂盒说明书的要求,且所有试剂的保存条件均为4℃。
1.3.4 叶绿素含量的测定取水培条件下生长的植株,选取生理状态一致的成熟叶片,用蒸馏水冲洗干净后,用滤纸吸干表面水分。准确称取0.1 g鲜样,置于10 mL离心管中,加入10 mL按体积比为2︰1配制的丙酮-乙醇混合提取液,于避光环境中静置24 h,直至叶片完全脱色。以758 g·kg–1丙酮溶液作为空白对照进行调零,使用分光光度计(Lambda 950+Refle,美国)分别测定提取液在663 nm和645 nm波长处的吸光值(A663和A645),按比尔-朗博特(Lambert-Beer)定律计算:
| $ \mathrm{叶}\mathrm{绿}\mathrm{素}\mathrm{a}/\left(\mathrm{m}\mathrm{g}·{\mathrm{g}}^{-1}\right)=\left(12.7\times {{A}}_{663}-2.69\times {{A}}_{645}\right)\times \frac{{v}}{1\;000\times {w}} $ | (1) |
| $ 叶绿素\text{b}/\left(\text{mg}\cdot {\text{g}}^{-1}\right)=\left(22.9\times {A}_{645}-4.68\times {A}_{663}\right)\times \frac{v}{1\;000\times w} $ | (2) |
| $ 总叶绿素/\text{mg}\cdot {\text{g}}^{-1}=\left(8.02\times {A}_{663}+20.21\times {A}_{645}\right)\times \frac{v}{1\;000\times w} $ | (3) |
式中,V为提取液体积(10 mL),W为鲜样质量(0.1 g),单位换算后结果以mg·g–1鲜样质量表示。每处理重复测定,数据经三次验证确保准确性。
1.3.5 可溶性糖含量的测定取水培玉米成熟叶片洗净后称取0.2 g鲜样,剪碎后加入10 mL蒸馏水,密封离心管沸水浴10 min,冷却后5 000 g离心10 min,取上清液重复沸水浴离心步骤。合并上清液定容至10 mL,取1 mL加入1 mL蒽酮乙酸乙酯及5 mL浓硫酸显色,混匀后于485 nm比色,同步以蔗糖标准曲线计算可溶性糖含量(mg·g–1鲜物质量)。步骤包括两次热提取、离心纯化及显色反应,确保数据精确性。
1.3.6 超氧阴离子和过氧化氢测定所有测定均使用Solarbio公司的试剂盒,其中超氧阴离子(O2–)试剂盒货号为BC1290,过氧化氢(H2O2)试剂盒货号为BC3595;试剂的配制与保存均严格按照试剂盒说明书操作,保存温度均为4℃。
1.4 数据统计与分析本研究采用Excel 2017进行数据整理与初步统计;SPSS 20.0软件进行单因素方差分析(One Way-ANOVE)和最小显著差异法(LSD)多重比较分析,检验不同浓度和粒径的PS-MPs荧光微塑料对玉米种子萌发和幼苗生长发育的差异;并使用Origin Pro 2021软件完成图表的制作。
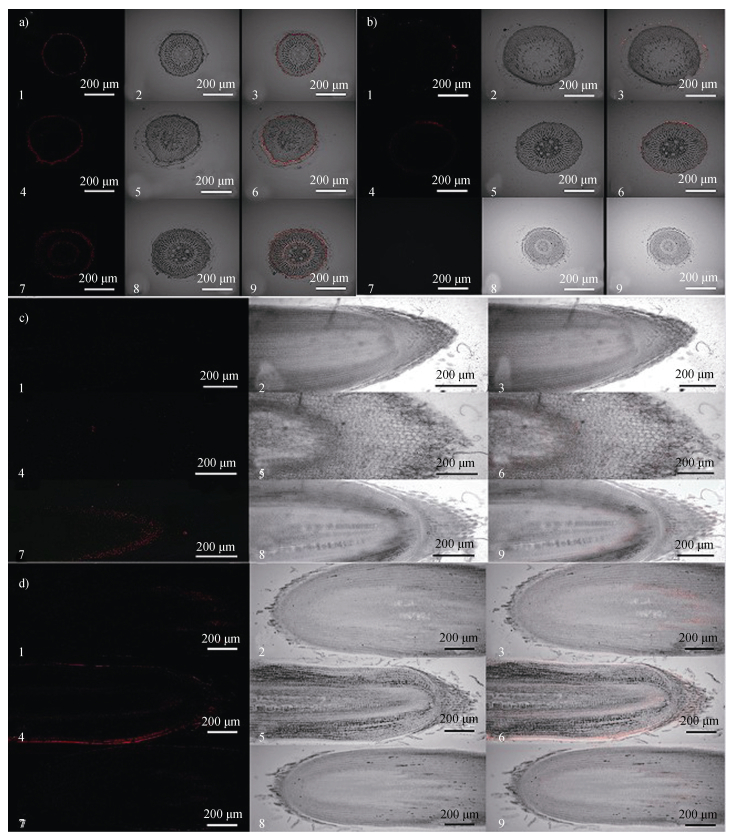
2 结果 2.1 不同浓度和粒径PS-MPs的荧光微球对玉米胚根的影响如图 1a所示,在不同浓度的PS-MPs(100 nm)荧光微球处理下,玉米胚根根尖的横切图显示,随着PS-MPs荧光微球浓度的增加,胚根中的荧光强度逐渐增强。当PS-MPs荧光微球浓度为20 mg·L–1时,荧光信号较弱,且主要分布于皮层和根毛;50 mg·L–1暴露组中,PS-MPs荧光微球呈现皮层薄壁组织与根毛区高密度富集,并发生韧皮部筛管低频侵染;100 mg·L–1暴露组荧光强度达浓度依赖性峰值,至木质部导管。
|
注:图a)、图c)中1~3为20 mg·L–1组的明场显微构象、荧光信号分布及共定位整合视图;4~6为50 mg·L–1组的明场拓扑、荧光强度场及重叠可视化影像;7~ 9为100 mg·L–1组的明场、荧光和重叠图像。图b)、图d)中1~3为500 nm粒径组的明场、荧光和重叠图像;4~6为1 000 nm粒径组的明场、荧光和重叠图像;7~9为5 000 nm粒径组的明场、荧光和重叠图像。 Note: In figures a) and c), images 1-3 show the bright field, fluorescence, and overlap images of the 20 mg·L–1 group, images 4-6 show the bright field, fluorescence, and overlap images of the 50 mg·L–1 group, and images 7-9 show the bright field, fluorescence, and overlap images of the 100 mg·L–1 group. In figures b) and d), 1-3 show the bright field, fluorescence, and overlap images for the 500 nm particle size group, 4-6 show the images for the 1 000 nm group, and 7-9 show the images for the 5 000 nm group. 图 1 在不同浓度(20、50、100 mg·L–1)和不同粒径(500、1 000、5 000 nm)聚苯乙烯微塑料(PS-MPs)荧光微球处理5 d后,胚根根尖横切面和纵切面的激光共聚焦显微镜(LCSM)图像 Fig. 1 Laser confocal scanning microscope (LCSM) images of transverse and longitudinal sections of hypocotyl root tips after five days of treatment with polystyrene microplastics (PS-MPs) fluorescent microspheres at different concentrations (20, 50, and 100 mg·L–1) and sizes (500, 1 000 and 5 000 nm) |
如图 1b所示,在100 mg·L–1浓度条件下,不同粒径的PS-MPs荧光微球被胚根吸收的数量及其荧光强度表现出明显差异:PS-MPs的吸收量和荧光强度随粒径减小而增加,且不同粒径的微球在根部的定位存在空间差异。随着粒径减小,玉米胚根对PS-MPs荧光微球的吸收量增多,对应的荧光信号也更强。其中,500 nm的微球主要富集于根毛区域,而1 000 nm的微球则多分布在根毛与表皮部位。
如图 1c、图 1d所示,纵切面观察显示,不同浓度和粒径的PS-MPs荧光微球在玉米胚根中的分布位置和荧光强度存在差异。PS-MPs荧光微球的根部迁移能力受浓度与粒径协同调控:在20、50 mg·L–1时,PS-MPs局限于皮层;浓度升至100 mg·L–1时,可抵达中柱。在500 nm粒径时可到达表皮并向中柱有限渗透;1 000 nm粒径则主要积累于根冠及表皮,无法深入内部组织。
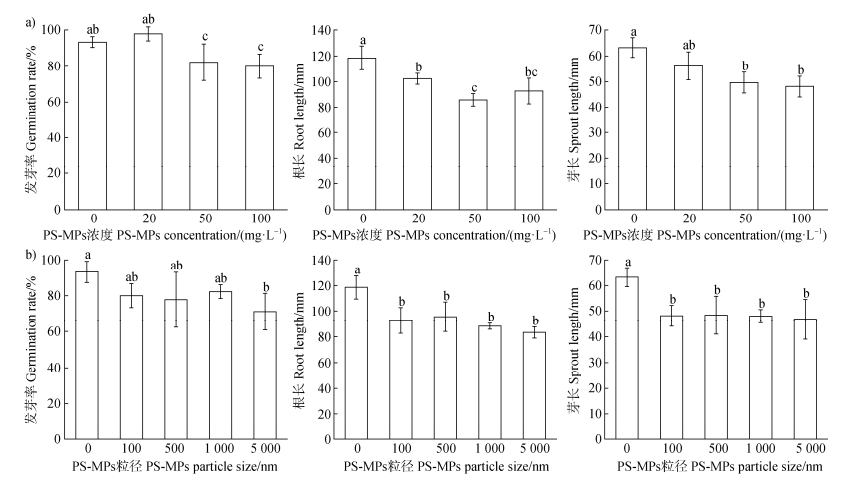
2.2 玉米种子萌发指标在不同浓度与粒径的PS-MPs荧光微球处理下的响应图 2量化了100 nm粒径PS-MPs荧光微球的浓度梯度及100 mg·L–1浓度下不同粒径PS-MPs对玉米种子萌发的影响。如图 2a,20 mg·L–1浓度对发芽率无显著影响,而50和100 mg·L–1浓度显著抑制发芽率。所有浓度处理均显著降低根长,且50 mg·L–1的影响最为显著;在芽长方面,50和100 mg·L–1显著抑制芽长,而20 mg·L–1对芽长无显著影响。
|
注:不同小写字母表示其在P < 0.05水平存在显著差异。下同。 Note: Different lowercase letters indicate significant differences at the 0.05 level of significance. The same below. 图 2 玉米种子萌发阶段对梯度暴露PS-MPs的粒径选择性响应特征(a.PS-MPs剂量梯度对玉米种子萌发的干扰;b.玉米种子对梯度粒径PS-MPs的响应) Fig. 2 Size-selective response characteristics of maize seed germination to a gradient exposure of PS-MPs (a. Disruption of maize seed germination by a gradient of PS-MP doses; b. Response of maize seeds to PS-MPs of different sizes) |
如图 2b,在不同粒径处理下,5 000 nm的PS-MPs荧光微球显著抑制发芽率,其他粒径与对照虽无显著性差异,但整体上发芽率有所下降。此外,各粒径处理均显著降低根长和芽长。
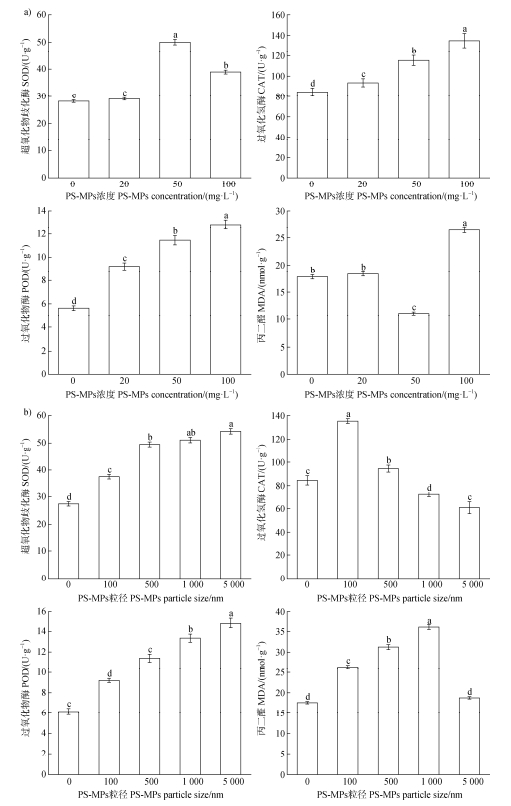
2.3 PS-MPs荧光微球对玉米抗逆性的影响图 3a表征了粒径100 nm的PS-MPs荧光微球在浓度梯度暴露下对玉米种子抗氧化酶系统及丙二醛(MDA)含量的影响。结果表明,CAT与POD活性均呈现显著的浓度依赖性,其强度与PS-MPs处理浓度呈显著正相关。SOD活性方面,20 mg·L–1组与对照组无显著差异,而在50和100 mg·L–1组中,SOD活性分别显著提高了78.26%和38.49%。MDA含量在20 mg·L–1处理下与对照组无显著差异,但在50和100 mg·L–1处理下呈显著变化,其中50 mg·L–1显著降低了MDA含量,而100 mg·L–1则显著提高了MDA含量。
|
图 3 不同浓度PS-MPs(0、20、50、100 mg·L–¹)(a)和不同粒径PS-MPs(0、100、500、1 000和5 000 nm)(b)暴露下对玉米胚根超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、过氧化物酶(POD)活性及丙二醛(MDA)含量的影响 Fig. 3 Effects of different PS-MP concentrations (0, 20, 50, 100 mg·L–1) (a) and different PS-MP particle sizes (0, 100, 500, 1 000, and 5 000 nm) (b) exposure on the activity of superoxide dismutase (SOD), catalase (CAT), and peroxidase (POD) and the content of malondialdehyde (MDA) in maize radicle |
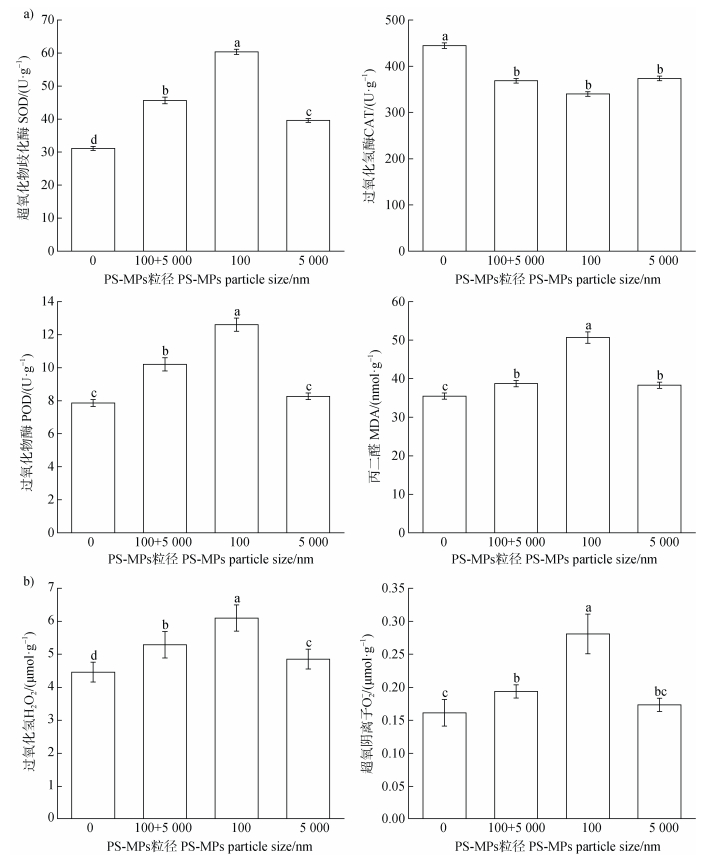
图 3b与图 4a展示了100 mg·L–1剂量下,多粒径PS-MPs荧光颗粒引发的玉米种子萌发期至幼苗生长阶段抗氧化酶协同响应及丙二醛MDA膜脂过氧化表征。其中图 3b显示,大粒径PS-MPs(5 000 nm)激活SOD、POD协同防御机制,而小粒径(100 nm)特异性增强CAT清除效率,较对照组增加61.68%,5 000 nm则瓦解其活性;中小粒径(100、500、1 000 nm)通过膜脂过氧化加剧,导致MDA累积,5 000 nm处理组与对照组无显著差异。图 4a显示对于玉米幼苗,不同添加方式均能显著影响SOD酶活性,其中仅添加100 nm处理时SOD活性最高,较对照组提升94.63%;混合添加100 nm和5 000 nm时,SOD酶活性较仅添加5 000 nm组增加14.77%;所有处理均显著降低了CAT酶活性;POD酶活性在仅添加100 nm组中达到最高值,较对照组增加23.43%;混合添加100 nm和5 000 nm时,POD活性同样显著增强;MDA含量在仅添加100 nm处理下最高,较对照组增加40.82%;混合添加100 nm和5 000 nm时,MDA含量也显著高于对照组。
|
图 4 多粒径PS-MPs(0、100+5 000、100、5 000 nm)暴露对玉米幼苗SOD、CAT、POD活性与MDA含量的影响(a)和过氧化氢(H2O2)与超氧阴离子(O2–)积累水平的影响(b) Fig. 4 Effects of multi-size PS-MPs (0, 100 + 5, 000, 100, and 5, 000 nm) on SOD, CAT, POD activity, and MDA content in maize seedlings (a) and the accumulation levels of hydrogen peroxide (H2O2) and superoxide anion (O2–) (b) |
图 4b分别显示了PS-MPs荧光微球对玉米幼苗叶片超氧阴离子(O2–)和过氧化氢(H2O2)含量的影响。结果表明,除5 000 nm处理外,所有处理均显著诱导玉米幼苗叶片超氧阴离子(O2–)水平升高(P < 0.05),其中仅添加100 nm PS-MPs组诱导O2–累积峰值,较对照组显著增加79.32%;100 nm+ 5 000 nm混合组的O2–含量与5000 nm单一处理组无显著差异。对于H2O2而言,所有处理均使H2O2含量显著升高(P < 0.05),其中仅添加100 nm PS-MPs时,H2O2含量最高,较对照组增加了36.96%;混合添加100 nm+5 000 nm时,H2O2含量相比单独添加5 000 nm PS-MPs组增加了9%。
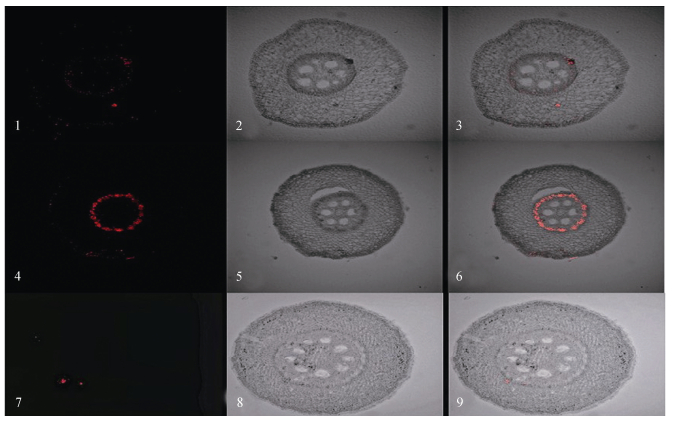
2.4 玉米幼苗对PS-MPs荧光微球的吸收和转运图 5展示了在不同添加方式下,不同粒径PS-MPs荧光微球在玉米幼苗根系横切面的分布情况。在所有处理组中均可观察到红色荧光信号,在100 nm PS-MPs暴露下,荧光强度达到峰值,并特异性聚集在维管束系统的木质部导管中;而100与5 000 nm粒径共暴露处理组中,荧光信号强度仅次于峰值组,扩散至木质部导管与皮层薄壁组织;而5 000 nm组荧光信号最弱,空间分布局限在皮层区域。
|
注:1~3:表征100 nm+5 000 nm混合粒径暴露组的明场显微构象、荧光信号分布及共定位整合视图;4~6:解析100 nm暴露下的明场拓扑、荧光强度场及重叠可视化影像;7~9:呈现5 000 nm暴露的明场、荧光及重叠图谱。 Note: 1-3:Bright-field microscopic configuration, fluorescence signal distribution and colocalisation composite view, characterising the exposure group of mixed particles with sizes ranging 100 nm+5 000 nm; 4-6:Analysis of bright-field topology, fluorescence intensity field and overlay visualisation images, under an exposure of 100 nm; 7-9:Presentation of bright-field, fluorescence and overlay maps, for an exposure of 5 000 nm. 图 5 玉米幼苗暴露于100 mg·L–1不同粒径PS-MPs荧光微球14 d后根尖的LCSM图像 Fig. 5 LCSM images of maize root tips after 14 days of exposure to fluorescent microspheres of 100 mg·L–1 PS-MPs with varying particle sizes |
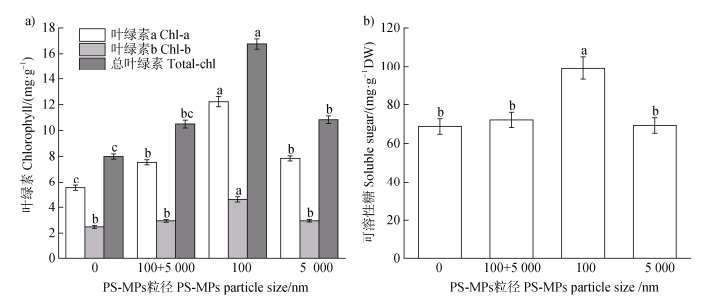
图 6a所示,PS-MPs荧光微球暴露后,玉米幼苗叶片叶绿素a含量在不同添加方式下均呈显著上升(P < 0.05),增幅分别为37.64%、124.44%、43.55%,且组间差异显著;叶绿素b仅于100 nm暴露下特异性激增85.07%(P < 0.05),其余处理无显著波动。叶绿素总量在100 nm与5 000 nm处理下均显著提升(P < 0.05),混合组则维持稳态。图 6b进一步表明,可溶性糖含量于100 nm暴露下显著上升44.81%(P < 0.05)。
|
注:实验结果中同一指标图柱上不同小写字母表示其在P < 0.05水平存在显著差异。 Note: Different lowercase letters on the bars of the same indicator in the experimental results indicate significant differences at the 0.05 level of significance. 图 6 不同粒径PS-MPs(0、100+5 000、100、5 000 nm)暴露下对玉米幼苗叶绿素代谢(a)和可溶性糖含量(b)的影响 Fig. 6 The effects of exposure to PS-MPs of different sizes (0, 100+5 000, 100, 5 000 nm) on the metabolism of chlorophyll (a) and the content of soluble sugars (b) in maize seedlings |
在研究微塑料对植物毒性影响时,常把发芽率作为重要的标志物[15]。也有研究发现,菜心种子发芽率随着PS-MPs荧光微球浓度的增加抑制作用增强,PS-MPs荧光微球粒径越大对种子发芽的抑制作用越强,PS-MPs粒径越小则抑制能力越弱[16]。在对玉米种子萌发的影响方面,本研究发现不同浓度和粒径的PS-MPs荧光微球表现出不同的作用:20 mg·L–1低浓度暴露显著激发萌发,而50与100 mg·L–1中高浓度则抑制发芽(图 2a)。原因可能是中高浓度微球在木质部导管内形成物理性占位屏障,直接阻碍水分及矿质营养输导系统,最终导致萌发动能衰竭[17]。不同粒径的PS-MPs荧光微球对发芽率也有影响,与对照组相比大粒径(5 000 nm)对发芽率有显著抑制作用(图 2b)。这可能是由于大粒径微塑料对种子萌发过程中的生理活动阻碍更大。研究证实,微塑料通过黏液多糖氢键作用优先吸附于种子表皮、胚根及根毛区,形成多重表面覆盖层[18]。本研究揭示了梯度浓度与多粒径PS-MPs荧光颗粒对玉米种子根系伸长生长的速率及胚轴伸长的显著阻滞效应。原因是PS-MPs荧光微球大多数团聚在种子胚根和根毛的表面,影响了水分的吸收[19]。水分是种子萌发和幼苗生长的关键因素,水分吸收受阻必然会抑制种子的萌发和幼苗的生长。
氧化损伤的代谢扰动强度被纳入多污染物生态风险分级体系[20]。植物为了应对微塑料诱导的氧化应激反应,体内SOD、CAT及POD活性增幅与自由基清除效能呈正相关,其酶活性水平可作为量化外界胁迫强度的关键生物标志物[21]。在本研究中发现,20 mg·L–1的PS-MPs荧光微球对玉米胚根SOD活性无显著影响,而50和100 mg·L–1的处理下均显著增加了SOD酶活性,且SOD活性随粒径增大而增强(图 3a,图 3b)。这可能是因为在中高浓度微塑料胁迫下,植物体内产生氧化应激,SOD作为抗氧化防御系统的第一道屏障被激活[22]。在不同浓度处理下,玉米胚根的POD和CAT活性与浓度呈正相关,随着浓度的升高而增强(图 3a);在不同粒径处理下,CAT活性随粒径的增大而下降,POD活性随粒径的增大而增强(图 3b)。这与Zhang等[23]实验结果一致,SOD活性和CAT活性随微塑料浓度梯度升高而增强,MDA含量与活性氧(ROS)水平也显著上升。微塑料粒径梯度差异通过调控H2O2累积过量(图 4b)时,特异性激活POD与CAT的协同清除通路,其活性变异系数直接表征氧化应激强度粒径效应。其结果与Jiang等[24]的结果一致,推测可能是由于抗氧化防御系统衰竭所致,超出了自身调节能力的阈值。
植物代谢能量需求主要由叶绿体光合磷酸化过程驱动,仅小部分源自线粒体呼吸作用;其中叶绿素密度通过调控光系统Ⅱ量子产额,显著影响光能捕获效率,进而成为表征植株生理状态的关键生物标志物[25]。本研究揭示,PS-MPs荧光标记颗粒暴露对玉米幼苗叶绿素代谢通路产生显著干扰:所有暴露组均检测到叶绿素a的累积量明显上升;而叶绿素b的含量仅在100 nm粒径处理中呈现特异性增长;叶绿素总量则在单一添加100 nm或5 000 nm微塑料的条件下显著升高,混合添加100 nm+5 000 nm的处理对其无显著影响(图 6a)。推测微塑料可能通过影响植物的光合作用相关机制,从而改变叶绿素含量。可溶性糖作为渗透调节核心溶质,不仅可保持内稳态的稳定,同时也可维持保护膜的平衡与细胞结构的稳定[26]。本研究证实,仅在100 nm PS-MPs荧光微球暴露条件下,玉米幼苗可溶性糖含量呈现显著波动(图 6b),该现象表明纳米级微球通过非生物胁迫,特异性干扰玉米幼苗生理代谢稳态。可能是特定粒径的微塑料对玉米幼苗的代谢过程产生干扰。高剂量PS-NPs(100 mg·L–1)迫使光合产物向可溶性糖分流,中低剂量导致可溶性糖库容缩减[27]。
4 结论PS-MPs对玉米种子及幼苗生长的毒性效应呈现显著的浓度与粒径依赖性。LCSM分析证实,在玉米种子萌发期,PS-MPs荧光微球特异性定植于胚根根毛区,部分粒径跨表皮迁移至皮层组织,少数进一步侵入木质部导管;该导管作为水分与养分输导的核心通道,其堵塞现象最终引发了萌发受阻及氧化损伤应激。基于水培体系的暴露实验结合LCSM表明,在玉米幼苗阶段,PS-MPs荧光标记微球可经由蒸腾作用产生的拉力驱动,实现由根系向地上组织的主动迁移,在维管组织内形成特异性富集微区,进而构建毒性微环境,最终诱导生长障碍与生理功能失调。综上所述,微塑料对玉米种子及玉米幼苗的影响是多方面的,其原因主要涉及水分和养分输送受阻、氧化应激、影响光合作用相关机制、干扰代谢过程等多个方面。上述影响可能会对玉米的生长和发育产生不利影响,进而影响农业生产。因此,需要更加关注微塑料对农业生态系统的潜在影响,并采取相应的措施来减少微塑料的污染。
| [1] |
Andrady A L. Microplastics in the marine environment[J]. Marine Pollution Bulletin, 2011, 62(8): 1596-1605. DOI:10.1016/j.marpolbul.2011.05.030
(  0) 0) |
| [2] |
Li Y, Zhang J J, Xu L, et al. Leaf absorption contributes to accumulation of microplastics in plants[J]. Nature, 2025, 641(8063): 666-673. DOI:10.1038/s41586-025-08831-4
(  0) 0) |
| [3] |
Bai H H, Yang Y Q, Huang Y. Distribution of microplastics and their effects on nutrient absorption in strawberry plants[J]. Scientia Horticulturae, 2024, 332: 113214. DOI:10.1016/j.scienta.2024.113214
(  0) 0) |
| [4] |
Li L Z, Luo Y M, Li R J, et al. Effective uptake of submicrometre plastics by crop plants via a crack-entry mode[J]. Nature Sustainability, 2020, 3(11): 929-937. DOI:10.1038/s41893-020-0567-9
(  0) 0) |
| [5] |
Dan X Q, He M Q, Wen Y H, et al. The size-variation of microplastics alters plant nitrogen uptake by regulating soil gross nitrogen transformation rates[J]. Soil Biology & Biochemistry, 2025, 210: 109934.
(  0) 0) |
| [6] |
Iqbal S, Li Y J, Xu J C, et al. Smallest microplastics intensify maize yield decline, soil processes and consequent global warming potential[J]. Journal of Hazardous Materials, 2025, 486: 136993. DOI:10.1016/j.jhazmat.2024.136993
(  0) 0) |
| [7] |
Liu Y Y, Guo R, Zhang S W, et al. Uptake and translocation of nano/microplastics by rice seedlings: Evidence from a hydroponic experiment[J]. Journal of Hazardous Materials, 2022, 421: 126700. DOI:10.1016/j.jhazmat.2021.126700
(  0) 0) |
| [8] |
Nizzetto L, Futter M, Langaas S. Are agricultural soils dumps for microplastics of urban origin?[J]. Environmental Science & Technology, 2016, 50(20): 10777-10779.
(  0) 0) |
| [9] |
Liu Y H, Xiao M L, Shahbaz M, et al. Microplastics in soil can increase nutrient uptake by wheat[J]. Journal of Hazardous Materials, 2022, 438: 129547. DOI:10.1016/j.jhazmat.2022.129547
(  0) 0) |
| [10] |
Oliveri Conti G, Ferrante M, Banni M, et al. Micro- and nano-plastics in edible fruit and vegetables. The first diet risks assessment for the general population[J]. Environmental Research, 2020, 187: 109677. DOI:10.1016/j.envres.2020.109677
(  0) 0) |
| [11] |
Ragusa A, Svelato A, Santacroce C, et al. Plasticenta: First evidence of microplastics in human placenta[J]. Environment International, 2021, 146: 106274. DOI:10.1016/j.envint.2020.106274
(  0) 0) |
| [12] |
Yan Z H, Liu Y F, Zhang T, et al. Analysis of microplastics in human feces reveals a correlation between fecal microplastics and inflammatory bowel disease status[J]. Environmental Science & Technology, 2022, 56(1): 414-421.
(  0) 0) |
| [13] |
Ma X M, Geiser-Lee J, Deng Y, et al. Interactions between engineered nanoparticles (ENPs) and plants: Phytotoxicity, uptake and accumulation[J]. Science of the Total Environment, 2010, 408(16): 3053-3061. DOI:10.1016/j.scitotenv.2010.03.031
(  0) 0) |
| [14] |
Asli S, Neumann P M. Colloidal suspensions of clay or titanium dioxide nanoparticles can inhibit leaf growth and transpiration via physical effects on root water transport[J]. Plant, Cell & Environment, 2009, 32(5): 577-584.
(  0) 0) |
| [15] |
Khalid N, Aqeel M, Noman A. Microplastics could be a threat to plants in terrestrial systems directly or indirectly[J]. Environmental Pollution, 2020, 267: 115653. DOI:10.1016/j.envpol.2020.115653
(  0) 0) |
| [16] |
Huang X P, Xiang L, Guo J J, et al. The toxic effects of polystyrene microspheres on Chinese broccoli seeds and seedlings (In Chinese)[J]. Journal of Agricultural and Environmental Sciences, 2021, 40(5): 926-933. [黄献培, 向垒, 郭静婕, 等. 聚苯乙烯微球对菜心种子及幼苗的毒性效应[J]. 农业环境科学学报, 2021, 40(5): 926-933.]
(  0) 0) |
| [17] |
Li R J, Tu C, Li L Z, et al. Visual tracking of label-free microplastics in wheat seedlings and their effects on crop growth and physiology[J]. Journal of Hazardous Materials, 2023, 456: 131675. DOI:10.1016/j.jhazmat.2023.131675
(  0) 0) |
| [18] |
Bosker T, Bouwman L J, Brun N R, et al. Microplastics accumulate on pores in seed capsule and delay germination and root growth of the terrestrial vascular plant Lepidium sativum[J]. Chemosphere, 2019, 226: 774-781. DOI:10.1016/j.chemosphere.2019.03.163
(  0) 0) |
| [19] |
Liang X M, Nie X P, Ying G G, et al. Assessment of toxic effects of triclosan on the swordtail fish (Xiphophorus helleri) by a multi-biomarker approach[J]. Chemosphere, 2013, 90(3): 1281-1288. DOI:10.1016/j.chemosphere.2012.09.087
(  0) 0) |
| [20] |
Sun X D, Yuan X Z, Jia Y B, et al. Differentially charged nanoplastics demonstrate distinct accumulation in Arabidopsis thaliana[J]. Nature Nanotechnology, 2020, 15(9): 755-760. DOI:10.1038/s41565-020-0707-4
(  0) 0) |
| [21] |
Ping L W, Li X X, Zhang C, et al. Oxidative stress and DNA damage induced by DEP exposure in earthworms[J]. Huan Jing Ke Xue, 2018, 39(10): 4825-4833.
(  0) 0) |
| [22] |
Li Y, Zhang S S, Jiang W S, et al. Cadmium accumulation, activities of antioxidant enzymes, and malondialdehyde (MDA) content in Pistia stratiotes L[J]. Environmental Science and Pollution Research, 2013, 20(2): 1117-1123. DOI:10.1007/s11356-012-1054-2
(  0) 0) |
| [23] |
Zhang Y, Yang X, Luo Z X, et al. Effects of polystyrene nanoplastics (PSNPs) on the physiology and molecular metabolism of corn (Zea mays L.) seedlings[J]. Science of the Total Environment, 2022, 806: 150895. DOI:10.1016/j.scitotenv.2021.150895
(  0) 0) |
| [24] |
Jiang X F, Chen H, Liao Y C, et al. Ecotoxicity and genotoxicity of polystyrene microplastics on higher plant Vicia faba[J]. Environmental Pollution, 2019, 250: 831-838. DOI:10.1016/j.envpol.2019.04.055
(  0) 0) |
| [25] |
Li Y H, Huang X Y. The effects of heavy metal pollution on plant photosynthesis (In Chinese)[J]. Introduction and Consultation, 2006(6): 23-24. [李裕红, 黄小瑜. 重金属污染对植物光合作用的影响[J]. 引进与咨询, 2006(6): 23-24.]
(  0) 0) |
| [26] |
Moustakas M, Sperdouli I, Kouna T, et al. Exogenous proline induces soluble sugar accumulation and alleviates drought stress effects on photosystem Ⅱ Functioning of Arabidopsis thaliana leaves[J]. Plant Growth Regulation, 2011, 65(2): 315-325. DOI:10.1007/s10725-011-9604-z
(  0) 0) |
| [27] |
Qiu C C, Li G X, Li Q S, et al. Effects of polystyrene nanoplastics on the physiological growth of garlic (In Chinese)[J]. Environmental Science, 2022, 43(8): 4387-4393. [邱陈陈, 李国新, 李青松, 等. 聚苯乙烯纳米塑料对大蒜生长生理的影响[J]. 环境科学, 2022, 43(8): 4387-4393.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


