2. 浙江省工业污染低碳治理技术重点实验室, 浙江工业大学环境学院, 杭州 310014;
3. 青海盐湖资源综合利用工程技术中心, 中国科学院青海盐湖研究所, 西宁 810008
2. Zhejiang Key Laboratory of Low-carbon Control Technology for Industrial Pollution, College of Environment, Zhejiang University of Technology, Hangzhou 310014, China;
3. Qinghai Engineering and Technology Research Center of Comprehensive Utilization of Salt Lake Resources, Qinghai Institute of Salt Lakes, Chinese Academy of Sciences, Xining 810008, China
西北地区作为中国重要的农耕区域,其土壤现状对农业生产的可持续发展具有重要影响。然而,该地区气候干旱少雨,水资源相对匮乏;且在强烈的物理风化和广泛的风成作用下,土壤基质以黏粒和砂粒为主,土壤质地整体偏轻,结构松散[1]。鉴于此,我国西北农耕区广泛使用塑料地膜,以减少土壤水分蒸发并提高土壤温度,为作物的生长保水保墒。为响应限塑令,作为传统塑料地膜替代品,以聚对苯二甲酸-己二酸丁二醇酯(Polybutylene adipate co-terephthalate,PBAT)为代表材质的生物可降解塑料(Biodegradable plastics,BPs)地膜已越来越多地在农耕地区得到应用[2]。新疆昌吉国家农业高新技术产业示范区内,可生物降解地膜(PBAT、聚乳酸和支化聚碳酸亚丙酯等)已在12 200 hm2的农业生产中使用[3]。
值得注意的是,在老化过程中与传统塑料相比,BPs可能会生成更多的微塑料,甚至纳米塑料(Biodegradable nanoplastics,BNPs)。Zhao等[4]研究发现,在三种低密度聚乙烯残留的土壤中微塑料的丰度约为27 922±1 995 n·kg–1,而三种BPs残留的土壤中,微塑料(MPs)丰度高达约458 725±50 848 n·kg–1。Tong等[5]在模拟实验室机械磨损条件下,对BPs产生的BNPs及其碎片进行观察,发现BPs(PBAT、聚丁二酸丁二酯和聚乳酸)的次生BNPs粒径范围为(31.6±10.0)~(97.9±21.4)nm,与传统塑料(聚乙烯、聚苯乙烯和聚氯乙烯)产生的颗粒粒径((226.0±43.6)~(308.0±61.1)nm)相比,其粒径显著小于传统塑料。由于BPs在物理性质、化学结构以及降解性能方面与传统塑料存在较大差别,其对土壤理化性质的影响可能不同于传统塑料。
首先,相较于生物不可降解塑料,BNPs通常含有更多含氧官能团,可改变塑料表面的极性和电荷,除了增强塑料表面的吸附能力外,还可通过静电吸引、络合和氢键促进BNPs与土壤中的金属阳离子等组分相互作用。因此,BNPs一旦到达土壤表面,通过水分入渗以及其他干扰土壤团聚体结构的过程进入土壤基质,可能同时改变土壤颗粒的团聚行为[6]及土壤中离子的赋存特征[7]。有关土壤团聚体中塑料颗粒丰度和分布的研究表明,约72%的塑料颗粒与土壤团聚体有关联/结合,其余则处于分散状态[8],这意味着土壤中的BNPs可能参与了土壤团聚体的形成。第二,大多数的BPs降解单体是各种有机酸,如PBAT的组成单体,对苯二甲酸(Polycondensation of terephthalic acid,PTA)和己二酸(Adipic acid,AA),其酸度系数分别为3.5[9]和4.4[10],这类含有羧酸基团(−COOH)或酚羟基(−OH)的低聚物接触水后可释放H+,在局部形成酸性环境,可能引起土壤pH的下降,进而对土壤结构和功能产生影响。此外,土壤含水率对BPs地膜的降解速率有显著影响。Wang等[11]发现,在苗期缺乏灌溉导致降解速率较为缓慢,而在频繁灌溉期间降解速率显著加快。可见,土壤的干湿条件可能显著改变BPs,尤其是BNPs,对土壤团聚、离子含量、pH等性质的影响,亟需展开相关研究。
作为粒径在0.002 mm以下的土壤颗粒,黏粒在西北干旱区积盐速度较慢但总量大,易导致土壤板结。黏粒在新疆阿拉尔和石河子土壤中占比分别为115 ±101 g·kg–1和240 ±121 g·kg–1[12]。土壤团聚体的形成过程受黏粒、氧化物、交换性阳离子组成、溶液浓度和pH等多种因素影响,其中,黏粒、交换性阳离子和有机质的共同作用是形成团聚体的主要机制[13]。黏粒的团聚与分散是土壤物理行为中的重要反应,影响着土壤的脆性、入渗速率、可蚀性等特性[14];而其膨胀、离子吸附等行为与土壤团聚体的稳定性以及土壤的盐度、碱度等理化性质密切相关。随着BPs地膜在我国西北农耕区的广泛应用,其纳米颗粒在当地土壤中的赋存日益普遍,但BNPs对盐碱土壤中黏粒团聚、离子吸附和pH等性质的调节作用尚未可知。同时,在西北地区典型的灌溉条件下(作物生育期通常灌溉3~4次,间隔在5~15 d[15]),BNPs对黏粒结构与性质的影响也亟待探索。
基于上述背景,本研究的目的:(1)基于PBAT塑料地膜的使用现状和污染情况,模拟当地复湿条件下环境浓度的PBAT-BNPs对土壤黏粒团聚、盐度和碱度的影响;(2)探索PBAT-BNPs对土壤黏土矿物结构和无机阴阳离子赋存(释放)的影响。研究可为BNPs改善土壤黏粒结构和性质提供新视角。
1 材料与方法 1.1 土样采集与黏粒样品提取方法土壤样品采自中国新疆乌鲁木齐的表层(0~20 cm)土样,根据中国土壤系统分类为潮湿碱积盐成土,属于生态保护区域和盐碱改良区。将采集到的土壤样品充分混匀后过5 mm筛,去除碎石和根系等杂质后进行研磨,过2 mm筛后备用。该土壤的主要理化性质为:pH9.0±0.0,电导率30.4± 0.8 mS·cm–1,含水率43±15 g·kg–1,黏粒含量646.6 g·kg–1。利用激光粒度仪(Mastersizer2000,马尔文帕纳科有限公司,英国)测得原土的平均粒径为3.1±0.0 μm。根据《国际土粒分级标准》(International Society of Soil Science,1930),单独提取黏粒部分(0.002~0.020 mm),其主要理化性质为:pH:8.9±0.0,电导率:6.7±0.0 mS·cm–1。
将通过2 mm筛孔的土样(50.0 g)以土水质量比1︰5的比例制成悬液,振荡1 h后,离心15 min(1 000 r·min–1),弃去上清液。重复上述过程,直至上清液电导率小于40.0 mS·m–1,以去除可溶性盐。在经过上述处理的样品中加入适量盐酸溶液(1 mol·L–1),再加水至250 mL,于80 ℃加热15 min,并不断搅拌。静置过夜后离心15 min(1 000 r·min–1),弃去上清液,重复上述过程直至上清液中电导率小于40.0 mS·m–1,以去除碳酸盐。将预处理后的样品转移至锥形瓶中,加适量水,使溶液体积控制在150~200 mL,再加入25 mL六偏磷酸钠分散剂,于振荡器上振荡18 h(90 r·min–1),以分散土样。将洗筛(63 μm)放在玻璃漏斗里,并将漏斗颈置于量筒中;将分散好的样品转移至洗筛上,用洗瓶冲洗样品直至滤液不再浑浊。向量筒中加水至1 000 mL,制成悬浊液。根据斯托克斯定律,利用土粒在静水中的沉降规律,采用虹吸管法提取黏粒样品,烘干后备用。所有土壤样品均进行灭菌处理以排除微生物作用,土壤在玻璃培养皿中以薄层(1~2 cm)铺开,使用高压灭菌锅(LDZF-75L-Ⅱ,上海申安医疗器械厂)在121 ℃、1.1 atm条件下灭菌60 min。
1.2 BNPs悬浮液的制备及浓度定量方法将购得的PBAT颗粒(中诚塑胶,平均粒径500 μm)装在玻璃培养皿中加盖石英片后置于紫外线老化箱(ZC-80,坤云仪器,浙江绍兴)中,在60 ℃紫外老化过程中,光辐射强度为20 μW·cm–2。每24小时搅拌一次塑料样品,以确保塑料均匀老化,老化时间设置为28 d。将0.1 g老化28 d的PBAT颗粒与10 mL超纯水(用硫酸(0.1 mol·L–1)调节pH至4.0)混匀。混合液在摇床(150 r·min–1)振荡72 h后,经过滤(0.1 μm)得到的滤液即为纳米塑料(BNPs)悬浮液。将过滤得到的膜上物充分冲洗并收集,再次冷冻干燥后称重,通过计算反应前后的质量差确定质量浓度,为0.6±0.0 g·L–1。移取2 μL BNPs悬浮液滴在金片上,使用光学显微镜(BX53,奥林巴斯,日本)确定金片上液滴(2 μL)的覆盖面积(439 471 μm2),随后通过Image J软件对颗粒进行计数,最终换算得到BNPs的颗粒浓度为3.4×109 particles·mL–1。
1.3 PBAT-BNPs与土壤黏粒混合的复湿试验称取15.0 g灭菌处理后的黏粒土样,均匀平铺于直径90 mm玻璃培养皿中,加入15 mL 8.8×109 particles·mL–1的BNPs溶液于培养皿中,使用玻璃棒充分搅拌以确保与土样均匀混合[16]。参考新疆农田生物可降解地膜降解试验数据[11],以质量已知且降解率为70%的PBAT薄膜为基准,根据PBAT密度和本试验测得的BNPs平均粒径,对PBAT-BNPs的颗粒浓度定量。
模拟西北旱区的农田灌溉过程[15],向PBAT-BNPs与黏土的混合样品加去离子水并自然风干,在风干过程中,通过电子天平(FA2004,上海衡平仪器仪表厂)实时监测土壤质量变化以确定含水率变化,直至含水率恢复至原土水平(43 g·kg–1)或更低。在此基础上,参考西北地区典型农田灌溉制度(作物生育期通常灌溉3~4次,间隔在5~15 d[15]),将PBAT-BNPs与黏粒混合样品分别放置0、7、14、28 d后分别进行二次覆水处理(即复湿),待风干后再次测定其理化参数。同时,设置三组对照试验:(1)不加PBAT-BNPs但复湿,(2)加PBAT-BNPs但0 d加水后不复湿,(3)不加PBAT-BNPs且0 d加水后不复湿。每组试验重复三次,以确保数据的可靠性和可重复性。
1.4 黏粒团聚体分析混合样品加水后,分别在0.5、1、2 h三个时间点进行取样。每次取少量黏粒样(0.1 g),加入10 mL超纯水稀释并充分混匀后,移取50 μL样品在显微镜(BX53,奥林巴斯,日本)下(20×)观察团聚体粒径的变化。在复湿试验中,采用激光粒度仪(Mastersizer2000,马尔文帕纳科有限公司,英国)分析0、7、14、28 d试验组和对照组样品的平均粒径(D50)和粒径分布。同时,为探究PBAT-BNPs对团聚体长期稳定性的影响,将在复湿条件下28 d采集的样品于避光条件下干燥保存230 d后,再次复湿,测定团聚体的粒径分布。
1.5 土壤理化性质测定土壤pH的测定参照《HJ962—2018土壤pH值的测定电位法》:原土土壤(过2 mm筛后)和黏粒样品分别以水土质量比2.5:1的比例混合,剧烈搅拌1 min,静置30 min,用pH计(FE-28,梅特勒托利多科技有限公司,上海)在土壤上清液中测定pH。电导率的测定参照《HJ802—2016土壤电导率的测定电极法》:原土土壤(过2 mm筛后)和黏粒样品分别以水土质量比5:1的比例混合,在摇床(200 r·min–1)振荡30 min,取下静置30 min,将上清液经定性滤纸过滤,用电导率仪在滤液中测定电导率。其次,含水率参照《HJ613—2011土壤干物质和水分的测定重量法》:将带盖容器于105 ℃±5 ℃下烘干1 h,稍微冷却后盖好盖子,置于干燥器中至少冷却45 min,测定带盖容器的质量。将10~15 g风干的原土样品转移至已称重的容器中,盖上容器盖,测定总质量。取下容器盖,将容器和风干的原土土壤样品一并放入烘箱中,在105 ℃±5 ℃下烘干至恒重,同时烘干容器盖。盖上容器盖,冷却后立即测定带盖容器和烘干土壤的总质量。此外,阳离子交换量(CEC)参照《HJ889—2017土壤阳离子交换量的测定三氯化六氨合钴浸提—分光光度法》:分别称取3.5 g原土土壤和黏粒样品于离心管中,加入50 mL三氯化六氨合钴(1.7 cmol·L–1)溶液,在20 ℃±2 ℃下振荡60±5 min。以4 000 r·min–1离心10 min,收集上清液,通过紫外分光光度计(UV-1800,岛津仪器(苏州)有限公司,苏州)在波长475 nm处,以水为参比,分别测量吸光度。
1.6 土壤中可溶性盐分离子的测定原土土壤(过2 mm筛后)和黏粒样品分别以水土质量比5:1的比例混合,振荡3 min后立即过滤,滤液作为土壤可溶盐分测定的待测液:钾(K+)、钙(Ca2+)、钠(Na+)等阳离子含量测定[17]的具体方法为在消解烧杯中加土壤滤液和硝酸放置加热板,加盖30 min后去盖,蒸发至溶液为澄清或略带黄色为止。加去离子水至溶液近干后定容至10 mL,通过电感耦合等离子体发射光谱仪(iCAP 7000 Plus Series ICP-OES,赛默飞,德国)进行定量。其次,碳酸根(CO32–)、碳酸氢根(HCO3–)采用双指示剂中和滴定法测定[18]:滤液中加入酚酞指示剂,如有紫红色出现,用硫酸标准溶液滴定至终点;再加溴酚蓝指示剂,用硫酸标准溶液滴定至终点。由标准酸的两次用量可分别求得土壤中CO32–、HCO3–的含量。氯离子(Cl–)采用硝酸银滴定法,参照《GB11896—89水质氯化物的测定硝酸银滴定法》测定:滤液中加入铬酸钾指示剂,用硝酸银滴定至终点,记录所用硝酸银溶液的体积。同法作空白滴定,根据体积差求得土壤中Cl–的含量。硫酸根离子(SO42–)采用氯化钡比浊法,参照《GB/T5750.5—2023生活饮用水标准检验方法第5部分:无机非金属指标》测定:滤液中加入混合稳定剂(氯化钠溶液、丙三醇和乙醇)。沿烧杯壁缓慢加入氯化钡溶液,用磁力搅拌器搅拌。立即将试液倒入吸收皿中,以纯水作为参比,在420 nm处测量吸光度。通过硫酸根标准溶液制备的标准曲线计算土壤中SO42–浓度。最后,硅酸根离子(SiO32–)采用硅钼蓝分光光度法测定,参照《SL91.2—1994二氧化硅(可溶性)的测定(硅钼蓝分光光度法)》:滤液中加盐酸溶液和钼酸铵溶液,放置5 min,加入草酸溶液,1 min后立即加1-氨基-2-萘酚-4-磺酸溶液,放置10 min,以试剂空白为参比,在640 nm处测定其吸光度。通过二氧化硅标准溶液制备的标准曲线计算土壤中SiO32–浓度。
1.7 X射线衍射(XRD)及晶体层间距分析取0.1 g原土土壤(研磨后过0.075 mm的筛子)与复湿处理下添加PBAT-BNPs第7天和第28天样品,用X射线衍射仪(SmartLab SE,Rigaku公司,日本)进行测试。测试靶材为Cu靶,X射线波长为1.5 Å,扫描角度范围在5°~90°之间,扫描速度设置为1(°)·min–1。根据布拉格方程(nλ=2dsinθ),计算晶体层间距(d值)。其中,λ为X射线波长,θ为衍射角,n为衍射级数。
1.8 PTA单体定量方法对复湿处理下添加PBAT-BNPs第7天及原始土壤样品进行密度浮选,取土壤样品加入浮选溶液,静置24 h,吸出上清液,取沉淀物进行消解。在土壤样品中分别加入硝酸、氢氟酸和高氯酸,置于加热板上。加盖持续加热至溶液澄清或略带黄色为止,加入硝酸,加热至近干。加入去离子水至溶液近干后取出,定容至10 mL。取部分消解溶液(7 d)进行对苯二甲酸含量测定[19-20]。对苯二甲酸通过高效液相色谱(High Performance Liquid Chromatography,HPLC,岛津仪器(苏州)有限公司,苏州)检测:波长为240 nm;流动相为6:4(v:v)的甲醇与水混合溶液,用冰乙酸调节其pH为3.0;流速设置为0.8 mL·min–1;柱温为30 ℃。另取部分消解溶液通过电感耦合等离子体发射光谱仪进行Na+浓度测定。
1.9 数据处理对实验组、对照组以及各组不同处理时间的样品数据通过StatView5.0软件进行One-way ANOVA单因素分析,检验是否存在显著性差异(P<0.05)。通过HighScore 3.0.5对XRD数据进行Rietveld精修,以计算矿物比例。XRD数据的处理依次包括背景确定、峰搜索和物相匹配。通过适当调整背景多项式、比例因子、晶胞参数和轮廓变量等参数,直至拟合可靠性(R)因子(期望可靠性因子(Rexp)、图谱可靠性因子(Rp)、加权图谱可靠性因子(Rwp)和拟合优度(G))达到可接受范围(数值越低表示精度越高)。
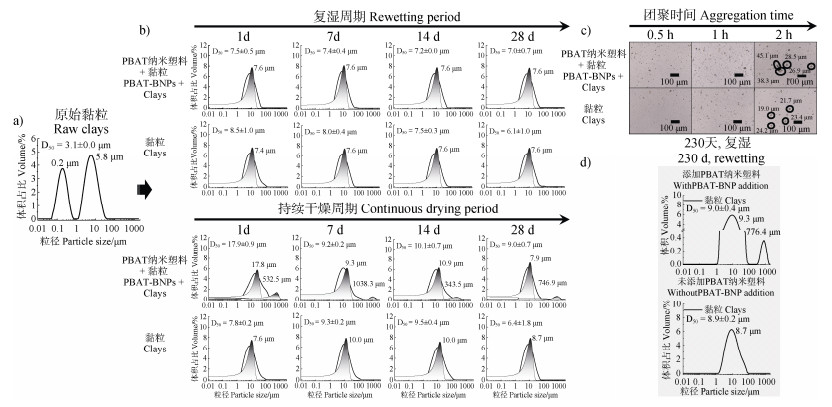
2 结果与讨论 2.1 复湿条件下PBAT-BNPs对土壤黏粒团聚行为的影响复湿是土壤经历多次干燥与湿润循环的过程,是影响土壤颗粒团聚行为的重要环境因子,同时也是影响PBAT-BNPs效应的关键因素。原始土壤的粒径呈现双峰分布(图 1a),其中,小粒径(0.2 μm)处的峰值属于黏粒范畴。在长达28 d的每周复湿处理下,有、无添加PBAT-BNPs的土壤黏粒中,原本分布于0.2 μm处的黏粒全部团聚,粒径分布从双峰分布变为单峰分布,平均粒径从原来的3.1 μm增至7.0 μm以上,且随复湿处理次数增加而保持稳定,整体粒径变化与未加PBAT-BNPs的组别相近(图 1b),说明复湿处理可导致黏粒团聚。相对地,初始土样加水后不再复湿的处理组别,PBAT-BNPs的添加不仅在短期内(1 d)使黏粒出现明显团聚——平均粒径17.9±0.9 μm,还导致黏粒形成532.5 μm的大团聚体;随着干燥处理时间的延长,双峰分布中的小尺寸团聚体粒径减小,而大团粒始终存在。由此可推测,PBAT-BNPs的加入很可能导致土壤黏粒团聚,但该现象在以7 d为周期的复湿处理组中并不显著。
|
注:PBAT为聚对苯二甲酸-己二酸丁二醇酯,D50为中值粒径。下同。 Note: PBAT stands for poly (butylene adipate co-terephthalate), D50 stands for median particle size. The same below. 图 1 原始黏粒的粒径分布(a)、黏粒在复湿和持续干燥条件下第1、7、14和28天的粒径分布变化(b)、黏粒在复湿0.5、1、2 h的显微镜图片(c)及复湿条件下28 d样品在干燥保存230 d后再次复湿的粒径分布(d) Fig. 1 Particle size distribution of raw clays (a), particle size distribution variation of clays at 1, 7, 14 and 28 d under rewetting and continuous drying conditions, respectively (b), microscopic images of clay aggregates at 0.5, 1, and 2 h after rewetting of clays (c), and particle size distribution of clays under rewetting after 230 d dry preservation of 28 d rewetting samples (d) |
进一步,对加入PBAT-BNPs的黏粒加水后2 h内的颗粒团聚情况进行观测(图 1c),发现超过25 μm的团粒;虽然未添加PBAT-BNPs纳米塑料组的黏粒也出现团聚,但粒径大小显著小于PBAT-BNPs处理组。水分的变化通过改变孔隙度,使团聚体收缩和膨胀,影响团聚体的形成、粒径分布和结构稳定性[21]。而PBAT-BNPs会在很短时间(如2 h)内进一步促进团聚,然而,土壤的盐度和离子会抑制其长时间(如7 d)的团聚效果,因此,整体表现为复湿条件下,PBAT-BNPs的存在不会显著强化黏粒团聚。
考虑西北地区非农耕时期干旱少雨的气候条件,本研究还探究了PBAT-BNPs在黏粒中赋存230 d且干燥状态下,黏粒的团聚情况。通过粒径分析发现了776.4 μm大团粒的形成,而该大团聚体并未在未添加PBAT-BNPs的组别出现(图 1d)。这表明,PBAT-BNPs长期赋存和土壤长期干燥后,短暂的复湿有可能诱导黏粒发生明显团聚。
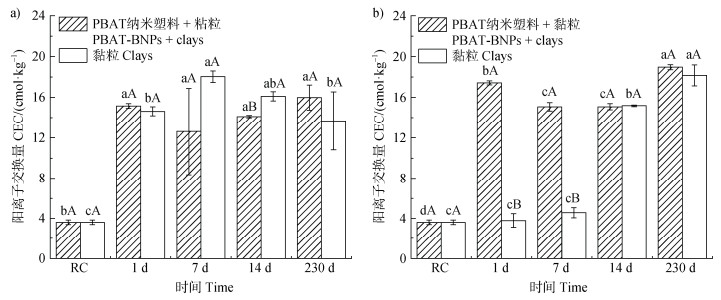
2.2 复湿条件下PBAT-BNPs对黏粒理化性质的影响 2.2.1 阳离子交换量(CEC)变化土壤阳离子交换量是衡量土壤肥力的和理化性质的重要指标[22],CEC与土壤胶体类型、阳离子类型和pH有关。如图 2a显示,与原始黏粒相比,在复湿处理下有无添加PBAT-BNPs的黏粒CEC含量从1 d开始均显著上升,这是由于土壤盐度和碱度下降后土壤中可吸附位点增加,从而提高CEC含量;同时,复湿处理下黏粒团聚体的形成增加了土壤有效吸附的面积。然而,在加水后不复湿(持续干燥)的土壤中(图 2b),仅有添加PBAT-BNPs组的CEC从第1天起就显著增加;未添加PBAT-BNPs组则需要较长时间(14 d)才能达到与添加PBAT-BNPs组的相似水平。这表明在PBAT-BNPs自身的作用下土壤黏粒的CEC可显著提高,而复湿条件也能够促进黏粒CEC的增加。在230 d的长周期下,复湿组和干燥组中添加PBAT-BNPs的CEC含量均显著高于原始黏粒。
|
注:RC为原始黏粒。不同小写字母表示有或无添加PBAT-BNPs组别中不同处理时间的差异显著(P < 0.05),不同大写字母表示相同处理时间下有和无添加PBAT-BNPs的差异显著(P < 0.05)。下同。 Note: RC is raw clay. Different lowercase letters indicate significant difference (P < 0.05) between different treatment times in the group with or without PBAT-BNP addition, and different capital letters indicate significant difference (P < 0.05) between groups with and without PBAT-BNP addition at the same treatment time. The same below. 图 2 复湿(a)和持续干燥条件(b)下黏粒的阳离子交换量变化 Fig. 2 Changes in cation exchange capacity of clays under rewetting (a) and continuous drying conditions (b) |
黏粒含量和CEC是影响地貌过程的重要土壤特性,对土壤肥力至关重要。PBAT-BNPs的强表面络合和吸附能力有助于提高黏粒CEC,且不受土壤复湿的影响。作为形成土壤团聚体的“胶水”,高CEC的黏粒能促进形成良好的团粒结构,使土壤更疏松、透气,有利于根系生长。此外,CEC的高低直接影响土壤中养分的供应和保蓄能力,进而影响植物对养分的吸收利用。本研究中,PBAT-BNPs的存在使土壤CEC提高,利于增强土壤黏粒对pH、盐分和养分等的缓冲性能,为农耕土壤中的作物提供稳定的生长环境,避免极端土壤条件的危害。在以7 d为周期的复湿条件下,PBAT-BNPs的加入会使土壤黏粒吸附和保存更多的营养阳离子,这对盐度、碱度和黏粒含量普遍偏高的西北农耕区土壤有重要意义,例如,肥料随灌溉水流失的情况可一定程度上得到缓解。
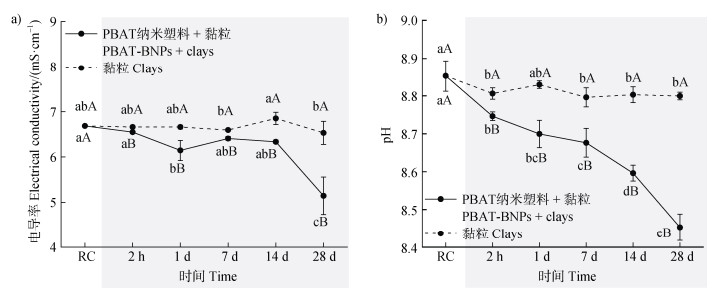
2.2.2 电导率变化如图 3a所示,在复湿处理下添加PBAT-BNPs组黏粒的电导率在试验过程中均呈下降趋势,并且随着频繁复湿操作而愈加明显,黏粒的电导率从原始的6.7 mS·cm–1下降至5.1 mS·cm–1;而未添加PBAT-BNPs的黏粒电导率与原始黏粒相比无显著变化(P>0.05)。PBAT-BNPs可通过静电相互作用、表面络合和离子交换吸附土壤中的阳离子(如,Na+、Ca2+等),从而降低土壤中的游离阳离子浓度,使电导率下降。有研究[23]表明,在NaCl浓度为2.0 g·kg–1的土壤中,聚乙烯、聚乳酸的添加会降低土壤电导率,特别是可生物降解微塑料(聚乳酸)。与可生物降解微塑料类似,PBAT-BNPs也可能通过相似的机制影响土壤电导率。由于PBAT-BNPs具有更大的比表面积和更高的表面活性,其对土壤中离子的吸附能力可能更强。土壤电导率主要受土壤溶液中离子浓度的影响。因此,PBAT-BNPs可能会干扰土壤中的离子平衡,从而直接或间接地影响土壤的电导率。此外,电导率的下降还可能与土壤中团聚体的形成有关。在复湿条件下,添加PBAT-BNPs处理可显著提高土壤CEC,增加土壤中黏粒的含量。黏粒中出现了粒径更大的团聚体,该现象表明,PBAT-BNPs的添加可能通过促进团聚体的形成,土壤结构得以改善,间接降低了土壤中游离离子的浓度。
|
图 3 复湿条件下有、无添加PBAT-BNPs的黏粒电导率(a)和pH(b)的变化 Fig. 3 Changes in clays electrical conductivity (a) and pH(b) under rewetting conditions with and without the addition of PBAT-BNPs |
土壤团聚试验过程中,黏粒在复湿处理下,添加PBAT-BNPs组的pH在试验过程中表现出显著的下降趋势,并且随着复湿次数增加逐渐明显(图 3b),pH从原始的8.8下降至8.5;而未添加PBAT-BNPs黏粒的pH虽有下降,但下降幅度小于PBAT-BNPs处理组。
土壤pH的降低可能是PBAT-BNPs水解释放小分子有机酸导致的。大多数生物可降解塑料在降解过程中会产生多种有机酸单体,这些单体的释放会显著影响土壤的酸碱环境[24]。例如,PBAT的组成单体PTA和AA的酸度系数分别为3.5和4.4。当这些含有羧酸基团(−COOH)或酚羟基(−OH)的降解产物与水接触时,会释放H+,从而形成局部酸性的环境,导致土壤pH降低。综上所述,PBAT-BNPs通过降解产物(有机酸单体)的释放、离子交换性能以及团聚体形成等,显著影响了黏粒的CEC、电导率和pH。从PBAT-BNPs释放有机酸单体的角度,将第7天的样品进行密度浮选分离,分析土壤团聚体中的Na+和PTA浓度在PBAT-BNPs处理条件下的变化(表 1)。PBAT-BNPs处理组的Na+浓度从原始状态6.6上升至7.2 g·kg–1,呈现上升趋势。同时,土壤样品中的PTA浓度从原始状态的1.7×10–3显著增加至6.1 mg·g–1,说明团聚试验过程中PBAT-BNPs释放了大量的有机酸单体。
|
|
表 1 土壤样品中Na+和对苯二甲酸(PTA)浓度 Table 1 Concentrations of Na+ and polycondensation of terephthalic acid (PTA) in soil samples |
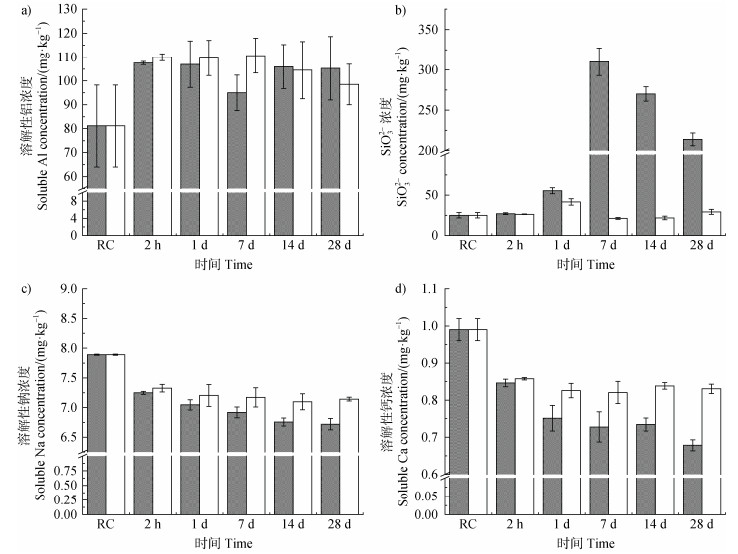
为研究土壤团聚过程中离子浓度的变化,对不同实验条件下土壤浸出液的离子浓度进行了测定。与原始黏粒相比,在28 d复湿处理下添加PBAT-BNPs组的土壤样品中,由于PBAT-BNPs诱导的酸性环境,黏土矿物溶解,溶解性铝和硅酸根离子释放(图 4a,图 4b)。然而在2小时的复湿条件下添加PBAT-BNPs组的土壤样品与未添加PBAT-BNPs组相比,溶解性铝的浓度略有降低(图 4a)。溶解性铝的降低可能是由于土壤CEC的升高导致土壤缓冲作用增加,在较高的CEC情况下能吸附部分铝离子;同时CEC的升高促使黏粒含量增加,铝离子被黏附在黏土颗粒上,在复湿条件下充当混凝剂,参与土壤团聚体的形成。
|
图 4 复湿条件下有、无添加PBAT-BNPs的土壤浸出液离子(a. 溶解性铝,b. 硅酸根,c. 溶解性钠,d. 溶解性钙)浓度变化 Fig. 4 Changes in ion concentration (a. soluble Al, b. SiO32–, c. soluble Na, d. soluble Ca) in soil leachate with and without the addition of PBAT-BNPs under rewetting conditions |
根据Oelkers[25]提出的理论,在酸性条件下,硅酸盐的溶解过程主要由表面质子化反应主导,在本试验中黏粒中的PBAT-BNPs可通过其所释放的单体提供酸性微环境,延长黏土矿物溶解的动力学过程,最终导致硅酸根的累积。在黏土矿物溶解过程中,以铝离子为代表的金属阳离子和硅酸根离子逐步释放至土壤环境中[25]。溶解反应通常遵循酸碱反应机制,pH对溶解过程具有重要影响。在PBAT-BNPs所创造的低pH环境中,氢离子能够与硅酸盐矿物表面发生反应,促进金属阳离子和硅酸根离子的释放,而PBAT-BNPs的表面官能团还能与金属离子形成稳定的配合物[26-27],改变矿物的溶解平衡,进而提高溶解速率。
复湿处理下添加PBAT-BNPs组黏粒中的溶解性钠(图 4c)和钙(图 4d)与原始黏粒相比浓度显著降低。溶解性钠浓度的降低与PBAT-BNPs对Na+的强吸附能力密切相关。有机质可通过表面官能团(如,−COOH和−OH)与土壤中的Na+发生交换反应,从而降低土壤中游离Na+的浓度;基于相同的机理,富含含氧官能团的PBAT-BNPs也表现出类似的Na+固定能力。溶解性钙浓度的降低可能与矿物组成有关。在黏粒中,Ca2+浓度的降低可能归因于PBAT-BNPs与Ca2+的络合或吸附作用。
在添加PBAT-BNPs处理的土壤样品中表现出多价金属离子释放浓度升高的现象。小分子有机酸与土壤金属氧化物之间有较强的相互作用:一方面,金属氧化物通过静电作用等机制吸附小分子有机酸;另一方面,吸附的有机酸能够促进金属氧化物的溶解和金属离子的释放。此外,有机酸还可通过质子攻击矿物表面(如硅酸盐中的≡Si−O−M键,M为金属阳离子),破坏矿物晶格,加速矿物溶解。以上结果表明,PBAT-BNPs的添加对土壤中金属离子的释放以及硅酸矿物溶解具有促进作用。
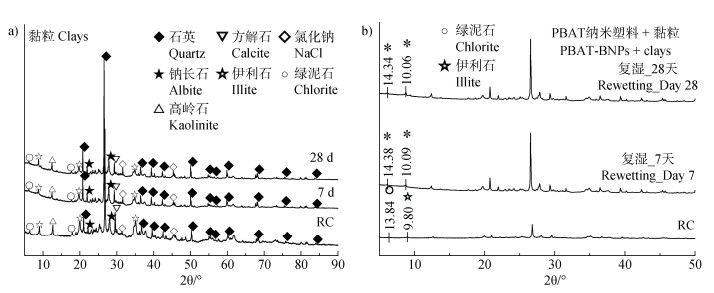
2.4 PBAT-BNPs导致土壤黏粒矿物结构改变对原始状态以及复湿条件第7天和28天添加PBAT-BNPs组的土壤样品进行了XRD分析,以定性分析其中的矿物组分(图 5a)。此外,通过布拉格公式对矿物层间距(以伊利石和绿泥石为例)进行了计算,结果(图 5b)显示,复湿处理下PBAT-BNPs的添加在团聚过程中一定程度上会影响土壤矿物的层间距。绿泥石的层间距从原始的13.8 Å增至第7天的14.4 Å和第28天的14.3 Å,伊利石的层间距从9.8 Å增至10.1 Å(第7天)和10.1 Å(第28天)。矿物层间距的变化可从以下几个方面进行分析:首先,PBAT-BNPs在降解过程中释放的有机酸单体可能进入矿物层间,导致层间距增大[28];其次,有机酸单体进入层间后,其羧酸基团可能吸附外部的阳离子,进而影响层间结构[29]。
|
注:*代表该矿物的(001)晶面间距值(d001值)与原始黏粒相比有所增加。 Note: * indicates that the (001) d-spacing (d001 value) of mineral has increased compared to the raw condition. 图 5 黏粒的X射线衍射(XRD)谱图(a)及矿物层间距(b) Fig. 5 X-ray diffraction (XRD) spectrum of clays (a) and mineral interlayer spacing(b) |
除矿物层间距变化外,还通过HighScore软件对XRD数据进行Rietveld精修,定量分析了团聚试验过程中矿物相对含量的变化(表 2)。根据Rietveld精修结果,发现PBAT-BNPs处理条件下土壤样品中硅铝酸盐矿物(钠长石,Albite;伊利石,Illite;绿泥石,Chlorite)的相对含量与原始黏粒相比均呈现下降趋势。该结果再次印证了PBAT-BNPs的添加可能通过其表面特性促进了矿物的溶解,从而显著影响了土壤中矿物的相对含量分布。
|
|
表 2 复湿下矿物相对含量变化 Table 2 Changes in relative mineral content under rewetting conditions |
本研究主要探讨了PBAT-BNPs对盐碱土中黏粒团聚体形成的促进作用及其对黏粒理化性质的影响。通过周期性复湿模拟西北干旱区土壤的灌溉情景,发现复湿可在短时间内显著促进黏粒团聚,表明水分条件的变化可增强PBAT-BNPs与土壤颗粒之间的相互作用;PBAT-BNPs的添加进一步促进了该效应,但受到黏粒整体高盐碱的限制。土壤黏粒中的PBAT-BNPs使其CEC显著增加,改善了土壤结构;由于PBAT-BNPs对游离阳离子(如Na□)的吸附作用以及土壤中团聚体的形成,土壤的电导率和碱度降低。PBAT-BNPs的添加加速了硅铝酸盐矿物离子组分的溶出(尤其是1个复湿周期后),硅酸根被释放而铝离子可能通过絮凝促进黏粒团聚;同时,矿物离子和纳米塑料单体的释放使矿物层间距增大。复湿条件不会对PBAT-BNPs促进黏粒团聚和脱盐碱产生负面影响。本研究结果为生物可降解纳米塑料对土壤性质的调控作用提供了新视角和科学依据。
| [1] |
Song Q, Gao X, Du H Q, et al. Cultivation impacts on soil texture during oasis expansion in Xinjiang, Northwest China: Wind erosion effects[J]. Aeolian Research, 2021, 50: 100646. DOI:10.1016/j.aeolia.2020.100646
(  0) 0) |
| [2] |
Zheng X R, Gao W C, Xi Y X, et al. Effects of PBAT biodegredable mulching film on soil microbial community, function and metabolic characteristics[J/OL]. Southwest China Journal of Agricultural Sciences, 2025, 38(11): DOI: 51.1213.S.20250925.1256.038.[郑欣蓉, 高维常, 席元肖, 等. PBAT生物降解地膜对土壤微生物群落、功能和代谢物特征的影响[J/OL]. 西南农业学报, 2025, 38(11): DOI: 51.1213.S.20250925.1256.038.]
(  0) 0) |
| [3] |
Liu Q. Changji National Agricultural High-tech Industry Demonstration Zone tackles white pollution with "Triple-Membrane Synergy" [OL]. [2025-04-08]. http://cjxww.cn/xw/cjxw/202504/t20250408_27811412.html.[刘茜. 昌吉国家农高区"三膜联推"破解白色污染[OL]. [2025-04-08]. http://cjxww.cn/xw/cjxw/202504/t20250408_27811412.html.]
(  0) 0) |
| [4] |
Zhao Z Y, Wang P Y, Wang Y B, et al. Fate of plastic film residues in agro-ecosystem and its effects on aggregate-associated soil carbon and nitrogen stocks[J]. Journal of Hazardous Materials, 2021, 416: 125954. DOI:10.1016/j.jhazmat.2021.125954
(  0) 0) |
| [5] |
Tong H Y, Zhong X C, Duan Z H, et al. Micro- and nanoplastics released from biodegradable and conventional plastics during degradation: Formation, aging factors, and toxicity[J]. Science of the Total Environment, 2022, 833: 155275. DOI:10.1016/j.scitotenv.2022.155275
(  0) 0) |
| [6] |
Lian X Q, Zhang S F, Yang X, et al. Effect of polyethylene microplastics on soil physical properties: The interactive effect of particle size and content[J/OL]. Acta Pedologica Sinica, 2026, DOI: 10.11766/trxb202412240508.[练小晴, 张树峰, 杨潇, 等. 聚乙烯微塑料对土壤物理性质的影响: 粒径与含量的交互效应[J/OL]. 土壤学报, 2026, DOI: 10.11766/trxb202412240508.]
(  0) 0) |
| [7] |
Guo Y, Liu L W, Fan Y M, et al. Polyethylene terephthalate nanoplastics affect potassium accumulation in foxtail millet (Setaria italica) seedlings[J]. BMC Plant Biology, 2024, 24: 1253. DOI:10.1186/s12870-024-06007-2
(  0) 0) |
| [8] |
Zhang G S, Liu Y F. The distribution of microplastics in soil aggregate fractions in southwestern China[J]. Science of the Total Environment, 2018, 642: 12-20. DOI:10.1016/j.scitotenv.2018.06.004
(  0) 0) |
| [9] |
Yang W S, Liu R, Li C, et al. Hydrolysis of waste polyethylene terephthalate catalyzed by easily recyclable terephthalic acid[J]. Waste Management, 2021, 135: 267-274. DOI:10.1016/j.wasman.2021.09.009
(  0) 0) |
| [10] |
Das B, Baruah J B. Assemblies of cytosine within H-bonded network of adipic acid and citric acid[J]. Journal of Molecular Structure, 2011, 1001(1/2/3): 134-138.
(  0) 0) |
| [11] |
Wang Z H, Wu Q, Fan B H, et al. Testing biodegradable films as alternatives to plastic films in enhancing cotton (Gossypium hirsutum L.) yield under mulched drip irrigation[J]. Soil and Tillage Research, 2019, 192: 196-205. DOI:10.1016/j.still.2019.05.004
(  0) 0) |
| [12] |
Zhao S Q, Chi D Q, Jia F C, et al. Study on fractal characteristics of soil particles of saline soil in different regions (In Chinese)[J]. Jiangsu Agricultural Sciences, 2021, 49(6): 203-207. [赵守强, 迟大群, 贾付诚, 等. 不同地区盐渍土土壤颗粒的分形特征[J]. 江苏农业科学, 2021, 49(6): 203-207.]
(  0) 0) |
| [13] |
Liu Y L, Wang P, Wang J K. Formation and stability mechanism of soil aggregates: Progress and prospect (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(3): 627-643. DOI:10.11766/trxb202112180686 [刘亚龙, 王萍, 汪景宽. 土壤团聚体的形成和稳定机制: 研究进展与展望[J]. 土壤学报, 2023, 60(3): 627-643.]
(  0) 0) |
| [14] |
Luo X J, Wang Z C, Yang F. Research progress on clay dispersion characteristics of saline-sodic soil (In Chinese)[J]. Soils, 2024, 56(2): 255-263. [罗雪娇, 王志春, 杨帆. 苏打盐碱土壤黏粒分散特征研究进展[J]. 土壤, 2024, 56(2): 255-263.]
(  0) 0) |
| [15] |
Yin J, Yang Y P, Eeswaran R, et al. Irrigation scheduling for potatoes (Solanum tuberosum L.) under drip irrigation in an arid region using AquaCrop model[J]. Frontiers in Plant Science, 2023, 14: 1242074. DOI:10.3389/fpls.2023.1242074
(  0) 0) |
| [16] |
de Souza Machado A A, Lau C W, Till J, et al. Impacts of microplastics on the soil biophysical environment[J]. Environmental Science & Technology, 2018, 52(17): 9656-9665.
(  0) 0) |
| [17] |
Kovács B, Prokisch J, Györi Z, et al. Analytical methods and quality assurance: Studies on soil sample preparation for inductively coupled plasma atomic emission spectrometry analysis[J]. Communications in Soil Science and Plant Analysis, 2000, 31(11/12/13/14): 1949-1963.
(  0) 0) |
| [18] |
Jue W S, Wang Y P, Pu L G, et al. Determination of carbonate and bicarbonate in soil samples by centrifugal separation and dual indicator method (In Chinese)[J]. Yunnan Chemical Technology, 2024, 51(1): 91-94. [角文升, 王应平, 蒲利国, 等. 离心分离-酚酞溴酚蓝双指示剂中和法测定土壤中的碳酸根和碳酸氢根[J]. 云南化工, 2024, 51(1): 91-94.]
(  0) 0) |
| [19] |
Hua Z Y, Li Y, He X, et al. Quantitative analysis of PBAT microplastics and their degradation products in soil by mass spectrometry[J]. Eco-Environment & Health, 2025, 4(3): 100166.
(  0) 0) |
| [20] |
Li Y H, Su C, Hu F H, et al. Transforming poly (butylene adipate-co-terephthalate) into protocatechuic acid via enzymatic degradation and whole-cell catalysis[J]. Biomacromolecules, 2025, 26(3): 1701-1708. DOI:10.1021/acs.biomac.4c01490
(  0) 0) |
| [21] |
Guo Z, Zhang F B, Huang Y, et al. Response of soil aggregate stability changes of typical huangmian soil to vegetation succession (In Chinese)[J]. Soils, 2025, 57(1): 195-203. [郭正, 张风宝, 黄悦, 等. 典型黄绵土团聚体稳定性变化对植被演替的响应[J]. 土壤, 2025, 57(1): 195-203.]
(  0) 0) |
| [22] |
Ma J L, Ma K, Xie T N, et al. Prediction of spatial distribution of cation exchange in agricultural soils based on machine learning (In Chinese)[J]. Environmental Science, 2025, 46(3): 1737-1750. [马纪龙, 马琨, 谢铁娜, 等. 基于机器学习的农田土壤阳离子交换量空间分布预测[J]. 环境科学, 2025, 46(3): 1737-1750.]
(  0) 0) |
| [23] |
Xu S, Zhao R, Sun J, et al. Microplastics change soil properties, plant performance, and bacterial communities in salt-affected soils[J]. Journal of Hazardous Materials, 2024, 471: 134333. DOI:10.1016/j.jhazmat.2024.134333
(  0) 0) |
| [24] |
Hu L L, Zhou Y H, Chen Z, et al. Oligomers and monomers from biodegradable plastics: An important but neglected threat to ecosystems[J]. Environmental Science & Technology, 2023, 57(27): 9895-9897.
(  0) 0) |
| [25] |
Oelkers E H. General kinetic description of multioxide silicate mineral and glass dissolution[J]. Geochimica et Cosmochimica Acta, 2001, 65(21): 3703-3719. DOI:10.1016/S0016-7037(01)00710-4
(  0) 0) |
| [26] |
Zeng L, Peng T J, Sun H J, et al. Dissolution process and mechanism of montmorillonite in oxalic acid and sulfuric acid media at various pH levels[J]. Applied Clay Science, 2024, 261: 107573. DOI:10.1016/j.clay.2024.107573
(  0) 0) |
| [27] |
El Fadili H, Ait-Khouia Y, Ouffa N, et al. Comprehensive review on alkaline dissolution of aluminosilicates and its role in the mechanisms and properties of geopolymers and alkali-activated materials[J]. Case Studies in Construction Materials, 2025, 23: e05330. DOI:10.1016/j.cscm.2025.e05330
(  0) 0) |
| [28] |
Ndzana G M, Zhang Y L, Yao S H, et al. The adsorption capacity of root exudate organic carbon onto clay mineral surface changes depending on clay mineral types and organic carbon composition[J]. Rhizosphere, 2022, 23: 100545. DOI:10.1016/j.rhisph.2022.100545
(  0) 0) |
| [29] |
Yeasmin S, Singh B, Kookana R S, et al. Influence of mineral characteristics on the retention of low molecular weight organic compounds: A batch sorption–desorption and ATR-FTIR study[J]. Journal of Colloid and Interface Science, 2014, 432: 246-257. DOI:10.1016/j.jcis.2014.06.036
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


