2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
土壤有机碳库(SOC)是陆地生态系统中最大的碳库,其碳储量超过了大气和植被碳库的总和,在提高土壤生产力、缓解温室效应以及维持生态系统健康方面至关重要[1]。土壤碳泵理论表明,当新鲜的植物凋落物与根系分泌物进入土壤后,微生物会通过分解代谢和合成代谢将易被利用的碳底物转化为微生物自身的生物量和代谢产物[2-3]。随着微生物的死亡,细胞碎片、胞外聚合物和小分子化合物会在下一代的微生物利用中保留下来,与矿物相结合,并且稳定在土壤中[4]。这类由微生物衍生的土壤碳组分被称为微生物残体碳(Microbial necromass carbon,MNC),Liang等[5]基于温带不同生态系统表层土壤,量化了微生物残体碳占SOC的比例,结果表明在农田、草地、森林生态系统中,微生物残体占SOC的比例分别为55.6%、61.8% 和32.6%。微生物生长、繁殖、死亡是一个连续迭代的过程,在此过程中,微生物通过代谢活动源源不断地产生并在土壤中持续积累微生物残体碳[2]。此外,微生物残体因为自身化学结构相对稳定以及土壤中的物理化学保护作用,使其能够成为土壤稳定碳库的重要组成部分[6]。因此,鉴于微生物残体碳对土壤有机碳库的突出贡献,深入理解微生物残体碳在土壤中的固存机制,对于揭示土壤碳固存过程、优化土壤管理实践以及制定气候变化应对策略具有重要的科学和实践意义。
目前,有关微生物残体的研究主要集中于其对土壤养分、农田管理、气候变化等因素的响应[7],但关于土壤团聚体对微生物残体碳固存影响的研究仍相对较少,其具体机制尚需进一步揭示[8]。土壤团聚体作为土壤的基本结构单元,可以通过形成物理屏障促进微生物残体在土壤中积累转化[9]。土壤团聚体主要通过物理保护减少微生物残体与外界接触,这具体体现在:1)形成的小室能够阻断微生物残体与微生物的接触;2)限制氧气进入与扩散;3)防止土壤酶与其的接触[10]。值得注意的是,由于不同粒径的团聚体周转速度和稳定性不同,结合在其中的微生物残体所受到的保护程度和寿命有差异[11]。例如,Xu等[12]研究结果指出相较于大团聚体,微团聚体中的氨基糖含量更高。
土壤团聚体为微生物残体提供了物理保护,微生物残体反过来也参与了土壤团聚体的形成与稳定过程[12–13]。例如,微生物在新陈代谢过程中分泌的多糖可以作为胶结剂将土壤黏粒粘连起来形成微团聚体[14-16]。Huang等[17]研究发现,在施用有机肥条件下,微生物残体,尤其是真菌残体积累,有助于土壤的团聚过程。Sae-Tun等[18]研究也发现,在减少耕作强度下,真菌残体碳含量的增加有利于提高团聚体稳定性和实现土壤有机碳固存。微生物残体的转化、积累与消耗通常伴随着土壤团聚体的形成、稳定和崩解,鉴于两者的周转过程是相互影响的,因此,探究微生物残体碳与团聚体稳定性之间的关系对于寻找促进微生物残体碳固存的途径至关重要。
本研究结合Meta分析和机器学习方法,基于在全球范围内收集到的1 791对土壤氨基糖(MNC的生物标志物)观测数据和2 264对土壤团聚体(用于计算团聚体稳定性)观测数据,分别通过机器学习模型进行全球预测,并进一步探讨微生物残体碳与土壤团聚体稳定性之间的关系。本研究旨在解决以下2个科学问题:1)微生物残体碳含量与土壤团聚体稳定性是否显著相关?2)土壤团聚体稳定性促进微生物残体碳固存的影响机制是什么?研究结果有助于理解土壤团聚体促进微生物残体碳稳定的机制,为土壤碳库的管理提供物理保护的新方法,同时将为团聚体稳定性这一指标纳入微生物残体预测模型提供重要思路。
1 材料与方法 1.1 收集数据本研究在中国知网(CNKI)、Web of Science、Google Scholar数据库中,以“氨基糖”(amino sugars)、“微生物残体碳”(microbial necromass/ residue carbon)和“团聚体”(aggregate)作为联合关键词,搜索2024年11月前公开发表的文献。为减少发表偏倚,对文章进行了筛选,以确定其符合要求,筛选条件如下:1)文献同时提供微生物残体碳数据(或者能够通过公式转化计算出MNC)以及MWD数据(或者能够通过公式转化计算出MWD);2)选择湿筛法测定团聚体粒级;3)不包括培养实验以及研究干湿交替、冻融、污染实验;4)当相同结果在不同刊物被多次发表时,该数据仅被纳入一次。基于以上标准,筛选获得11篇有效文献,共78组观测数据。
基于同样的方法,将“氨基糖”(amino sugar)、“氨基葡糖糖”(GlcN)和“胞壁酸”(MurA)作为关键词,搜索2023年11月前公开发表的文献。筛选条件如下:1)文献直接提供GlcN和MurA数据,进而能够通过公式换算得到微生物残体含量;2)仅使用表层土(0~30 cm),不考虑底层土数据;3)不包括培养实验、盆栽实验;4)当相同结果在不同刊物被多次发表时,该数据仅被纳入一次。基于以上标准,筛选获得215篇有效文献,共1 791个观测数据。
基于同样的方法,将“团聚体”(aggregate)、“平均重量直径”(mean weight diameter,MWD)作为关键词,共筛选出239篇文献,得到2 264个观测数据。筛选标准如下:1)文献中直接含有MWD值,或提供不同团聚体的粒径范围和比重,最终能够通过MWD计算公式计算出MWD值;2)不包括培养实验以及研究干湿交替、冻融、污染实验;3)只使用表层土(0~30 cm),不考虑底层土数据;4)选择湿筛法测定土壤团聚体粒径;5)当相同结果在不同刊物被多次发表时,该数据仅被纳入一次。
原始数据从文献表格中获取,或者使用GetData Graph Digitizer软件(http://www.getdata-graph-digitizer.com)从文献图形中获取。附加信息包括实验地点(经纬度、海拔),气候条件(年均温MAT、年降雨MAP、年潜在蒸发量PET)、土壤性质(pH、容重BD、土壤有机碳SOC、全氮TN、全磷TP、碳氮比C/N、碳磷比C/P、氮磷比N/P、微生物生物量碳MBC、微生物生物量氮MBN、微生物生物量碳氮比MBC/N、砂粒含量Sand、粉粒含量Silt、黏粒含量Clay)。对于缺失的数据,从以下全球数据库中进行补充:全球土壤数据来自网格化的0.083°空间分辨率的全球土壤数据(http://globalchange.bnu.edu.cn/research/soilw);1970—2000年的气候数据(空间分辨率为30弧秒)来自WorldClim数据(https://www.worldclim.org/data/worldclim21.html)。
1.2 微生物残体碳与团聚体稳定性的计算方法氨基糖分析法是目前最常用的MNC量化方法。其中,土壤中胞壁酸(MurA)的唯一来源是细菌细胞壁,而氨基葡萄糖(GlcN)则主要来源于真菌细胞壁[19]。根据微生物细胞壁的生物标记物:MurA和GlcN,分别估计真菌残体碳(Fungal necromass carbon,FNC)和细菌残体碳(Bacteria necromass carbon,BNC)含量,以此得到MNC,单位为mg·g –1 soil。具体公式如下[20]:
| $ \begin{gathered} \mathrm{FNC}=(\mathrm{GlcN} / 179.17-2 \times \mathrm{MurA} / 251.23) \times \\ 179.17 \times 9 \end{gathered} $ | (1) |
| $ \mathrm{BNC}=\mathrm{MurA} \times 45 $ | (2) |
| $ \mathrm{MNC}=\mathrm{FNC}+\mathrm{BNC} $ | (3) |
式(1)中179.17与251.23分别为GlcN和MurA的摩尔质量,2表示细菌中MurA和GlcN的摩尔系数比为1∶2,9为MurA到FNC的转换系数。式(2)中的45为GlcN到BNC的转换系数。
选择平均重量直径(MWD)[21]来衡量团聚体稳定性,其基于各粒级团聚体的重量和大小而拟定,具体公式如下:
| $ {\text{MWD}} = \sum {({X_i} \times {W_i})} $ |
式中,
为预测MNC全球分布特征的变化情况,分别采用样地水平GlcN和MurA作为标签,选择11个土壤变量(pH、BD、SOC、TN、TP、C/N、C/P、N/P、Sand、Silt、Clay)和3个气候变量(MAT、MAP、PET)作为特征。为确定预测GlcN和MurA全球变化的最佳模型,选择4个常规的机器学习模型(轻量梯度提升模型(Light Gradient Boosting Machine,LightGBM)、极端梯度提升模型(Extreme Gradient Boosting,XGBoost)、类别型提升模型(Categorical Boosting,CatBoost)、随机森林模型(Random Forest))和2个深度学习模型(卷积神经网络模型(Convolutional Neural Networks,CNN)、多重感知机模型(Multilayer Perceptron,MLP)),使用均方误差(Mean Squared Error,MSE)和决定系数(R2)评估模型的预测能力[22-23]。将数据按照7∶3的比例随机分成训练集和验证集。根据模型预测情况,从验证集中选择R2最高的模型作为最优模型。故选择最优模型LightGBM和XGBoost分别预测GlcN与MurA(表 1),并最终根据氨基糖计算公式计算获得MNC的全球预测集,共计32 975对数据。所有机器学习模型在Python中建立运行。
|
|
表 1 不同机器学习模型预测的决定系数(R2) Table 1 R2 predicted by different machine learning models |
基于同样的方法,采用样地水平MWD作为标签预测MWD全球分布特征的变化情况,最终选择最优模型CatBoost来预测MWD的全球变化(表 1)。
1.4 数据处理利用随机森林模型分析MNC对环境变量(如气候条件、土壤性质及MWD)的响应。模型构建和分析通过R软件(版本4.3.2)的RandomForest”包完成。鉴于湿筛法的具体步骤和参数可能对MWD产生影响,通过R软件(版本4.3.2)的“scale”函数对MWD数据进行标准化处理。基于克里金插值法,使用ArcGIS软件绘制了MNC和MWD的全球分布图,空间分辨率为5角分(约10 km)。此外,采用R软件的“corrplot”包进行Pearson相关性分析评估MNC与MWD之间的相关性,采用R软件的“plspm”包进行偏最小二乘路径模型(PLS-PM)分析以进一步探讨MWD调控MNC的影响机制。
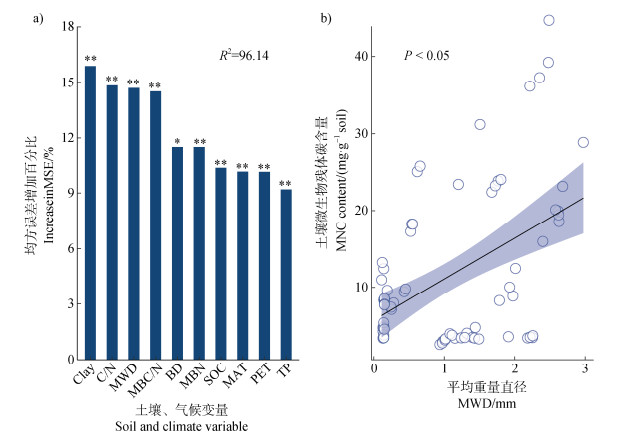
2 结果 2.1 微生物残体碳与团聚体稳定性的相关性对同时包含MNC和MWD测量值的78对观测数据进行随机森林模型分析,结果见图 1a。除Clay、C/N外,MWD是MNC预测中第三重要的变量。此外,线性回归分析显示MNC与MWD之间存在显著的正相关关系(P < 0.05)(图 1b)。
|
注:a),环境因子预测MNC的相对重要性。*、**分别表示变量在0.05、0.01水平上显著,R2表示模型的解释程度。Clay:黏粒含量;MWD:平均重量直径;MBC/N:微生物生物量碳氮比;BD土壤容重;MBN:微生物生物量氮;SOC:土壤有机碳;MAT:年均温;PET:年潜在蒸发量;TP:全磷。b),MNC与MWD的线性回归分析。P值为显著性水平,误差带为回归线的95%置信区间。下同。 Note:a),The relative importance of environmental factors in predicting MNC. * and ** represent variables that are significant at 0.05 and 0.01 level. R2 represents the degree of interpretation of the model. Clay:Clay content;MWD:Mean weight diameter;MBC/N:Microbial biomass carbon-nitrogen ratio;BD:Bulk density;MBN:Microbial biomass nitrogen;SOC:Soil organic carbon;MAT:Mean annual temperature;PET:Potential evapotranspiration;TP:Total phosphorus. b),Linear regression analysis of MNC and MWD:P-value is the significance level,and error band is the 95% confidence interval of the regression line. The same below. 图 1 微生物残体碳与团聚体稳定性之间的关系 Fig. 1 Relationship between microbial residue carbon and aggregate stability |
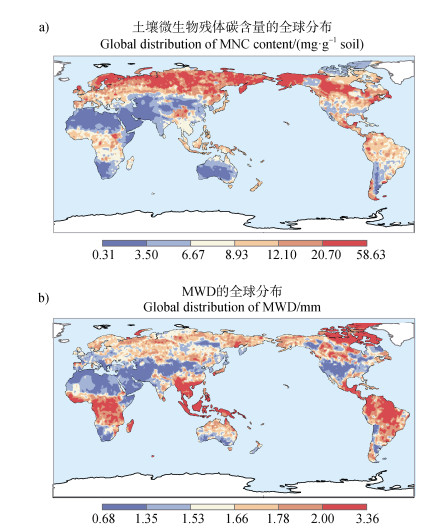
考虑到同时包含MNC与MWD的数据在规模上有所限制,为了扩大分析范围,本文通过机器学习预测了MNC与MWD的全球数据,并绘制了相应的全球分布地图(分辨率:约10 km)。如图 2所示,全球MNC平均值为8.33 mg·g –1土壤,MWD平均值为1.74 mm。地图显示MNC与MWD在空间分布上有类似的规律。例如,在北温带、南美洲及北极地区,这两个指标均呈现较高的数值,而在非洲北部和中亚地区,这些值则相对较低。
|
注:地图的空间分辨率为5角分(约10km),地图上共计38 879个点。底图下载自自然资源部标准地图服务中心,审图号为GS(2016)1566号。 Note:The spatial resolution of the map is 5 arcminutes(~10 km),and there are 38 879 points on this map. The base map is downloaded from the Standard Map Service Center of the Ministry of Natural Resources,and the review number is GS(2016)1566. 图 2 MNC和MWD的全球分布 Fig. 2 Global distribution of MNC and MWD |
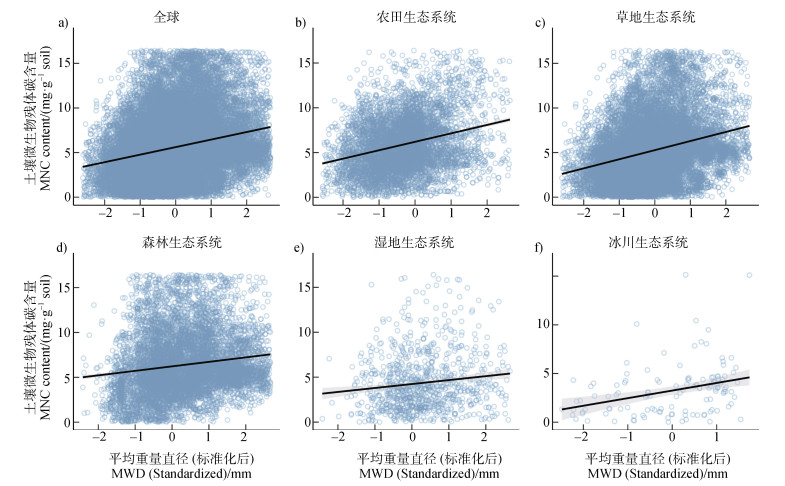
对基于机器学习模型所获得的全球预测数据集进行了相关性分析,结果显示在全球范围内,MNC与MWD之间仍保持显著的正相关性(P < 0.001)(图 3a)。为进一步分析不同生态系统对MNC与MWD关系的潜在影响,将全球预测数据集按照生态系统类型进行细分。结果发现,在农田、草地、森林、湿地和冰川生态系统中,这种显著的正相关关系依然存在(P < 0.001)(图 3 b-图 3f)。
|
注:图a)为全球MNC与MWD的相关性,图b)至图f)分别表示在农田、草地、森林、湿地和冰川生态系统下MNC与MWD的相关性。 Note:Fig. a)shows the correlation between MNC and MWD for global data,while Figs. b)to f)represent the correlation between MNC and MWD in farmland,grassland,forest,wetland,and glacier ecosystems,respectively. 图 3 全球及不同生态系统下MNC与MWD的相关性分析 Fig. 3 Correlation analysis of MNC and MWD in global and different ecosystems |
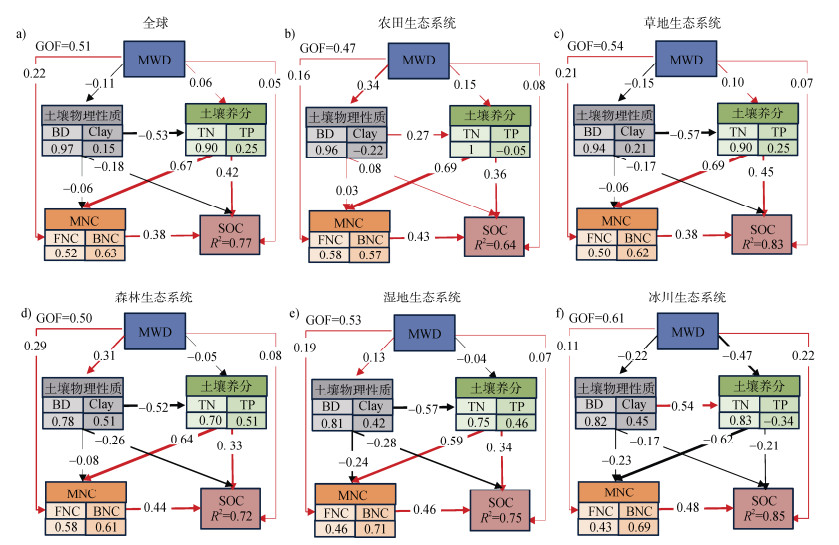
偏最小二乘路径模型(PLS-PM)结果表明在全球范围内,MWD对MNC有直接影响(路径系数0.22,P < 0.05)。此外,MWD还通过影响土壤物理性质(BD、Clay)和土壤养分(TN、TP),从而间接影响MNC的变化(图 4)。值得注意的是,土壤养分对MNC的正向影响最为显著(路径系数0.67,P < 0.05),这表明土壤养分是MWD促进微生物残体碳固存的关键中间变量。此外,MWD对SOC的直接影响较弱(路径系数0.05,P < 0.05),而MWD通过MNC间接促进了SOC的积累(路径系数0.38,P < 0.05)。
|
注:箭头旁边的数字是标准化路径系数,箭头的宽度表示标准化路径系数的强度,黑线表示路径系数为负,红线表示路径系数为正。观察变量下的数值为观察变量所占的权重值,R2表示模型中方差的解释比例。 Note:The number next to the arrow is the standardized path coefficient,the width of the arrow indicates the strength of the standardized path coefficient and the black line indicates the negative path coefficient,the red line indicates the positive path coefficient. The numerical value under the observation variable is the weight value assigned to the observation variable and R2 indicates the explained proportion of the difference in the model. 图 4 偏最小二乘路径模型(PLS-PM)分析揭示MWD影响MNC固存的机制 Fig. 4 Partial least squares path analysis(PLS-PM)reveals the influence mechanism of MWD on MNC retention |
在不同生态系统中,MWD对MNC的影响途径存在显著差异,表现在具体路径的方向和强度有所差异。例如,在农田生态系统中,MWD对MNC的直接贡献(路径系数0.16,P < 0.05)较弱,但通过土壤物理性质和养分的间接路径作用明显,且MWD对土壤物理性质有一个正相关作用。而在森林生态系统中,MWD对MNC的直接作用较为显著(路径系数0.29,P < 0.05)。此外,在湿地和冰川生态系统中,MNC对SOC的贡献作用更为显著。
3 讨论 3.1 微生物残体碳含量与团聚体稳定性显著相关本研究发现,无论是基于在野外测量的78对MWD和MNC观测值,还是依托机器学习技术在全球尺度上预测到的32 975对MWD和MNC数据,结果均一致表明,MNC与MWD之间存在显著的正相关关系。该发现与Luo等[24]和Liu等[25]研究结果相一致,这可能源于微生物残体的积累转化过程与团聚体形成和稳定之间存在相互促进的动态机制。
一方面,微生物残体碳在土壤有机碳库中的稳定化过程与土壤团聚体提供的物理保护密切相关[26]。微生物碳泵理论中的“续埋效应”强调了微生物残体在土壤中源源不断产生并趋于稳定,其中“埋”便是基于微生物残体碳在土壤中的物理保护作用所提出[5]。因为当微生物残体被物理性封闭在团聚体的内部,能够避免其与分解酶和微生物等直接接触,而当团聚体破碎后,这部分有机碳可能被释放并分解[10]。土壤团聚体稳定性越高,其周转率越低,有利于长时间稳定其内部的碳[13]。例如,Liu等[25]的研究结果表明,随着团聚体稳定性增加,大团聚体周转率降低,微生物残体碳含量增加。此外,稳定的团聚体还可以为微生物提供理想的栖息环境,尤其是其内部孔隙结构维持了适宜的水分、养分和气体流通条件,促进了微生物的生长和繁殖,从而间接促进微生物残体碳的积累[13]。
另一方面,微生物残体的胶结作用在团聚体的形成与稳定过程中也发挥着重要作用。团聚体周转过程是一种动态过程,原生矿物风化所形成的土壤矿物颗粒首先与可溶性有机物相互胶结形成有机矿物复合物,并成为微团聚体的结构单元[27]。在微团聚体形成和稳定过程中,微生物残体发挥着重要作用。Oades和Waters[28]研究发现,在微团聚体中,黏土颗粒包裹着微生物及其衍生物(多糖、细菌碎片等)形成的复合结构单元。Tisdall[29]则基于前人电子显微镜的观察结果,提出微生物死亡后的残留物,尤其是多糖物质,能够促进微团聚体的稳定。微团聚体在有机质和金属氧化物等胶结剂的作用下逐步形成大团聚体,在此过程中,微生物分泌物(多糖等)发挥着黏附作用,随着团聚体尺寸的增加,通过进一步的微生物活动与有机质积累,逐渐增强其内部的稳定性[30-31]。
微生物残体可以作为团聚体形成的胶结剂,促进土壤颗粒的结合和稳定,从而增强土壤的结构稳定性。而团聚体作为微生物的“孵化器”,为其生长、繁殖、死亡过程提供场所,所形成的物理屏障也为微生物残体提供了庇护[21]。这种相互促进的动态平衡关系,不仅对土壤结构稳定性至关重要,也为土壤微生物残体碳在土壤趋于稳定提供了重要保障。
3.2 团聚体稳定性促进微生物残体碳固存的影响机制为了探究团聚体稳定性对微生物残体积累转化过程的影响,本研究利用全球数据集进行了偏最小二乘路径模型(PLS-PM)分析。结果表明,土壤团聚体稳定性除了通过形成空间屏障为微生物残体提供直接的物理保护外(路径系数0.22,P < 0.05),还通过改变土壤物理性质和土壤养分状态,间接影响了土壤微生物残体碳含量(图 4)。稳定的土壤团聚体可以改善土壤质量和功能,如降低土壤容重、增加土壤孔隙度等,这可以为微生物的活动和代谢提供更为有利的空间条件[32]。研究表明,微生物数量和群落结构会影响土壤中微生物残体碳的积累动态,并且微生物代谢过程中分泌的胞外多糖等代谢物也会通过增强土壤颗粒间的黏附性进一步稳定微团聚体结构,间接提高了有机碳的保护和固存[33]。此外,土壤物理结构还影响着土壤养分以及水的流通,土壤养分的提高有利于微生物生长和活动,加速微生物残体碳的积累过程,从而促进土壤有机碳的输入和转化[34]。前人研究结果证实,长期施肥等土壤养分管理措施,可以显著提高微生物残体碳含量,并促进微生物残体对团聚体形成的正向贡献[35]。例如外源氮的添加,能够提高团聚体中真菌残体碳含量,而真菌残体通过菌丝网络和其持久性成分(如几丁质)显著影响着土壤团聚体的长期稳定性,这进而提高了土壤对微生物残体碳的物理保护作用[24]。
土壤团聚体稳定性对不同生态系统中微生物残体碳固存的影响过程具有显著差异(图 4),这可能是由于在不同生态系统中,有机质输入的质量与数量、土壤微生物的作用过程、土壤管理措施以及外界的气候因子等因素有所不同所造成的[26]。例如,在农田生态系统中,土壤团聚体通过土壤物理性质和土壤养分的间接路径对微生物残体的影响更强。可能的原因是,在农田生态系统中,覆盖作物、施肥等措施能够增加外源氮磷养分和碳源的输入,进而增加了团聚体中微生物残体碳的积累[36]。而传统耕作和机械压实会扰动土壤的物理结构,破坏大团聚体,加快微团聚体的周转,增加土壤容重,在本研究中表现为土壤团聚体稳定性与土壤物理性质显著正相关(路径系数0.34,P < 0.05)[37]。相比土壤团聚体提供的物理保护,在农田生态系统中矿物保护可能发挥了更重要的作用,因为耕作活动促进了有机质与土壤矿物颗粒的结合[38]。在森林生态系统中,团聚体稳定性对微生物残体的直接作用最强(路径系数0.29,P < 0.05),这可能与在森林生态系统中,输入的植物残体(如木质素、纤维素)占比更高有关[3]。植物残体结构较为复杂,其分解主要以真菌为主,而真菌菌丝对大团聚体的形成稳定起关键作用,反过来这又正向促进了团聚体对微生物残体的固存[39]。
偏最小二乘路径模型(PLS-PM)分析结果表明,土壤团聚体稳定性对土壤有机碳的直接作用较弱(路径系数0.22,P < 0.05),但通过微生物残体碳的间接路径,对土壤有机碳产生显著影响。可能的原因是,微生物残体碳因为自身结构较为稳定以及受到土壤中的物理化学保护,通常被认为是土壤有机碳库中最难分解的部分,其稳定性和长期固存能力使得间接路径对有机碳的影响更为显著[40]。此外,这些结果表明,微生物残体碳是团聚体稳定性调控土壤有机碳积累的关键中间变量,凸显了微生物残体碳作为土壤有机质形成的重要前体物质,在土壤碳循环和长期有机碳储存中发挥的重要作用。
4 结论团聚体稳定性是微生物残体碳含量的重要预测因子。在全球尺度上,微生物残体碳与土壤团聚体稳定性之间呈显著正相关,这一现象可能源于微生物残体的积累转化过程与团聚体形成稳定过程之间相互促进的动态机制。土壤团聚体除了形成空间屏障保护微生物残体不被分解外,还间接地调控了土壤物理性质与土壤养分,共同促进了微生物残体碳的固存。在不同生态系统中,土壤团聚体稳定性影响微生物残体碳固存的具体过程有显著差异。例如,在农田生态系统中,农田管理措施和耕作措施通过调节土壤物理性质和养分状态,增强了土壤团聚体对微生物残体碳积累的间接影响。未来研究可以进一步探讨不同土壤管理措施如何影响微生物残体碳与土壤团聚体间的相互关系,从而为农业可持续发展提供更为深入的科学依据。
| [1] |
Stockmann U, Adams M A, Crawford J W, et al. The knowns, known unknowns and unknowns of sequestration of soil organic carbon[J]. Agriculture, Ecosystems & Environment, 2013, 164: 80-99.
(  0) 0) |
| [2] |
Liang C, Schimel J P, Jastrow J D. The importance of anabolism in microbial control over soil carbon storage[J]. Nature Microbiology, 2017, 2: 17105. DOI:10.1038/nmicrobiol.2017.105
(  0) 0) |
| [3] |
Wang B R, An S S, Liang C, et al. Microbial necromass as the source of soil organic carbon in global ecosystems[J]. Soil Biology & Biochemistry, 2021, 162: 108422.
(  0) 0) |
| [4] |
Kallenbach C M, Grandy A S, Frey S D, et al. Microbial physiology and necromass regulate agricultural soil carbon accumulation[J]. Soil Biology & Biochemistry, 2015, 91: 279-290.
(  0) 0) |
| [5] |
Liang C, Amelung W, Lehmann J, et al. Quantitative assessment of microbial necromass contribution to soil organic matter[J]. Global Change Biology, 2019, 25(11): 3578-3590. DOI:10.1111/gcb.14781
(  0) 0) |
| [6] |
Dungait J A J, Hopkins D W, Gregory A S, et al. Soil organic matter turnover is governed by accessibility not recalcitrance[J]. Global Change Biology, 2012, 18(6): 1781-1796. DOI:10.1111/j.1365-2486.2012.02665.x
(  0) 0) |
| [7] |
Lu X F, Hou E Q, Guo J Y, et al. Nitrogen addition stimulates soil aggregation and enhances carbon storage in terrestrial ecosystems of China: A meta-analysis[J]. Global Change Biology, 2021, 27(12): 2780-2792. DOI:10.1111/gcb.15604
(  0) 0) |
| [8] |
Blackwood C B, Dell C J, Smucker A J M, et al. Eubacterial communities in different soil macroaggregate environments and cropping systems[J]. Soil Biology & Biochemistry, 2006, 38(4): 720-728.
(  0) 0) |
| [9] |
Hontoria C, Gómez-Paccard C, Mariscal-Sancho I, et al. Aggregate size distribution and associated organic C and N under different tillage systems and Ca-amendment in a degraded Ultisol[J]. Soil & Tillage Research, 2016, 160: 42-52.
(  0) 0) |
| [10] |
Lehmann J, Kleber M. The contentious nature of soil organic matter[J]. Nature, 2015, 528(7580): 60-68. DOI:10.1038/nature16069
(  0) 0) |
| [11] |
Puget P, Chenu C, Balesdent J. Dynamics of soil organic matter associated with particle-size fractions of water-stable aggregates[J]. European Journal of Soil Science, 2000, 51(4): 595-605. DOI:10.1111/j.1365-2389.2000.00353.x
(  0) 0) |
| [12] |
Xu Y D, Sun L J, Gao X D, et al. Contrasting response of fungal versus bacterial residue accumulation within soil aggregates to long-term fertilization[J]. Scientific Reports, 2022, 12(1): 17834. DOI:10.1038/s41598-022-22064-9
(  0) 0) |
| [13] |
Liu Z L, Yu W T. Review of researches on soil aggregate and soil organic carbon (In Chinese)[J]. Chinese Journal of Eco-Agriculture, 2011, 19(2): 447-455. [刘中良, 宇万太. 土壤团聚体中有机碳研究进展[J]. 中国生态农业学报, 2011, 19(2): 447-455.]
(  0) 0) |
| [14] |
Rillig M C, Mummey D L. Mycorrhizas and soil structure[J]. New Phytologist, 2006, 171(1): 41-53. DOI:10.1111/j.1469-8137.2006.01750.x
(  0) 0) |
| [15] |
Six J, Bossuyt H, Degryze S, et al. A history of research on the link between(micro)aggregates, soil biota, and soil organic matter dynamics[J]. Soil & Tillage Research, 2004, 79(1): 7-31.
(  0) 0) |
| [16] |
Tan W F, Xu Y, Shi Z H, et al. The formation process and stabilization mechanism of soil aggregates driven by binding materials (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(5): 1297-1308. DOI:10.11766/trxb202308060312 [谭文峰, 许运, 史志华, 等. 胶结物质驱动的土壤团聚体形成过程与稳定机制[J]. 土壤学报, 2023, 60(5): 1297-1308.]
(  0) 0) |
| [17] |
Huang X L, Jia Z X, Wang J S, et al. Linking soil aggregation to organic matter chemistry in a Calcic Cambisol: Evidence from a 33-year field experiment[J]. Biology and Fertility of Soils, 2023, 59(1): 73-85. DOI:10.1007/s00374-022-01684-3
(  0) 0) |
| [18] |
Sae-Tun O, Bodner G, Rosinger C, et al. Fungal biomass and microbial necromass facilitate soil carbon sequestration and aggregate stability under different soil tillage intensities[J]. Applied Soil Ecology, 2022, 179: 104599. DOI:10.1016/j.apsoil.2022.104599
(  0) 0) |
| [19] |
Amelung W. Assessment methods for soil carbon . Boca Raton: Lewis Publishers, 2001: 233-270.
(  0) 0) |
| [20] |
Appuhn A, Joergensen R G. Microbial colonisation of roots as a function of plant species[J]. Soil Biology & Biochemistry, 2006, 38(5): 1040-1051.
(  0) 0) |
| [21] |
Liu Y L, Wang P, Wang J K. Formation and stability mechanism of soil aggregates: Progress and prospect (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(3): 627-643. DOI:10.11766/trxb202112180686 [刘亚龙, 王萍, 汪景宽. 土壤团聚体的形成和稳定机制: 研究进展与展望[J]. 土壤学报, 2023, 60(3): 627-643.]
(  0) 0) |
| [22] |
Hu H, Chen J, Zhou F, et al. Relative increases in CH4 and CO2 emissions from wetlands under global warming dependent on soil carbon substrates[J]. Nature Geoscience, 2024, 17(1): 26-31. DOI:10.1038/s41561-023-01345-6
(  0) 0) |
| [23] |
Hu H, Qian C, Xue K, et al. Reducing the uncertainty in estimating soil microbial- derived carbon storage[J]. Proceedings of the National Academy of Sciences of the United States of America, 2024, 121(35): e2401916121.
(  0) 0) |
| [24] |
Luo R Y, Kuzyakov Y, Liu D Y, et al. Nutrient addition reduces carbon sequestration in a Tibetan grassland soil: Disentangling microbial and physical controls[J]. Soil Biology & Biochemistry, 2020, 144: 107764.
(  0) 0) |
| [25] |
Liu L, Gunina A, Zhang F S, et al. Fungal necromass increases soil aggregation and organic matter chemical stability under improved cropland management and natural restoration[J]. Science of the Total Environment, 2023, 858: 159953. DOI:10.1016/j.scitotenv.2022.159953
(  0) 0) |
| [26] |
Zhang B, Chen Q, Ding X L, et al. Research progress on accumulation, turnover and stabilization of microbial residues in soil (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(6): 1479-1491. DOI:10.11766/trxb202012270705 [张彬, 陈奇, 丁雪丽, 等. 微生物残体在土壤中的积累转化过程与稳定机理研究进展[J]. 土壤学报, 2022, 59(6): 1479-1491.]
(  0) 0) |
| [27] |
Kögel-Knabner I, Guggenberger G, Kleber M, et al. Organo-mineral associations in temperate soils: Integrating biology, mineralogy, and organic matter chemistry[J]. Journal of Plant Nutrition and Soil Science, 2008, 171(1): 61-82. DOI:10.1002/jpln.200700048
(  0) 0) |
| [28] |
Oades J M, Waters A G. Aggregate hierarchy in soils[J]. Soil Research, 1991, 29(6): 815. DOI:10.1071/SR9910815
(  0) 0) |
| [29] |
Tisdall J M. Structure and organic matter storage in agricultural soils . Boca Raton: CRC Press, 1995: 57-96.
(  0) 0) |
| [30] |
Six J, Elliott E T, Paustian K. Soil macroaggregate turnover and microaggregate formation: A mechanism for C sequestration under no-tillage agriculture[J]. Soil Biology & Biochemistry, 2000, 32(14): 2099-2103.
(  0) 0) |
| [31] |
Rillig M C, Muller L A, Lehmann A. Soil aggregates as massively concurrent evolutionary incubators[J]. The ISME Journal, 2017, 11(9): 1943-1948. DOI:10.1038/ismej.2017.56
(  0) 0) |
| [32] |
Vogel H J, Balseiro-Romero M, Kravchenko A, et al. A holistic perspective on soil architecture is needed as a key to soil functions[J]. European Journal of Soil Science, 2022, 73(1): e13152. DOI:10.1111/ejss.13152
(  0) 0) |
| [33] |
Bronick C J, Lal R. Soil structure and management: A review[J]. Geoderma, 2005, 124(1/2): 3-22.
(  0) 0) |
| [34] |
Zhang W X, Hendrix P F, Dame L E, et al. Earthworms facilitate carbon sequestration through unequal amplification of carbon stabilization compared with mineralization[J]. Nature Communications, 2013, 4: 2576. DOI:10.1038/ncomms3576
(  0) 0) |
| [35] |
Xiong L, Drosos M, Wang P, et al. The divergent accumulation mechanisms of microbial necromass C in paddy soil under different long-term fertilization regimes[J]. Geoderma, 2023, 439: 116688. DOI:10.1016/j.geoderma.2023.116688
(  0) 0) |
| [36] |
Zhou R R, Tian J, Cui Z, et al. Microbial necromass within aggregates stabilizes physically-protected c response to cropland management[J]. Frontiers of Agricultural Science and Engineering, 2023, 10(2): 198-209.
(  0) 0) |
| [37] |
Bartlová J, Badalíková B, Pospíšilová L, et al. Water stability of soil aggregates in different systems of tillage[J]. Soil and Water Research, 2015, 10(3): 147-154. DOI:10.17221/132/2014-SWR
(  0) 0) |
| [38] |
Schmidt J, Fester T, Schulz E, et al. Effects of plant-symbiotic relationships on the living soil microbial community and microbial necromass in a long-term agro-ecosystem[J]. Science of the Total Environment, 2017, 581: 756-765.
(  0) 0) |
| [39] |
Cotrufo M F, Soong J L, Horton A J, et al. Formation of soil organic matter via biochemical and physical pathways of litter mass loss[J]. Nature Geoscience, 2015, 8(10): 776-779. DOI:10.1038/ngeo2520
(  0) 0) |
| [40] |
Liang C, Zhu X F. The soil microbial carbon pump as a new concept for terrestrial carbon sequestration (In Chinese)[J]. Scientia Sinica: Terrae, 2021, 51(5): 680-695. [梁超, 朱雪峰. 土壤微生物碳泵储碳机制概论[J]. 中国科学: 地球科学, 2021, 51(5): 680-695.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


