2. 植物干细胞定向育种烟台市工程研究中心/功能作物种质创新与栽培利用山东省工程研究中心/烟台市蚕桑功能物质评价与利用重点实验室, 山东省蚕业研究所, 山东烟台 264002;
3. 国家盐碱地综合利用技术创新中心, 山东东营 257347
2. Yantai Engineering Research Center for Plant Stem Cell Targeted Breeding / Shandong Engineering Research Center of Functional Crop Germplasm Innovation and Cultivation Utilization / Yantai Key Laboratory of Evaluation and Utilization of Silkworm Functional Substances, Shandong Institute of Sericulture, Yantai, Shandong 264002, China;
3. National Center of Technology Innovation for Comprehensive Utilization of Saline-Alkali Land, Dongying, Shandong 257347, China
硝化作用是土壤氮循环的关键环节,直接影响到氮肥利用效率和环境安全[1]。硝化过程的副产物氧化亚氮(N2O)是强效温室气体,不仅加剧全球气候变暖,还会破坏臭氧层[2]。硝化产物硝态氮(NO3–-N)易通过淋溶或径流流失,导致水体污染,并降低氮肥利用率[3]。因此,有效调控土壤硝化过程对于提高氮肥利用效率、减少氮素环境损失具有重要意义。
传统的硝化调控策略主要依赖于硝化抑制剂(如双氰胺、DCD),但长期使用可能导致土壤微生物群落结构改变及抑制效果减弱[4]。因此,探索环境友好且可持续的硝化调控策略成为当前研究的重点。近年来,生物质炭和硅藻土作为新型土壤改良剂引起了广泛关注。生物质炭因其比表面积大、吸附性强,能够显著影响土壤氮循环[5]和微生物活性[6]。硅藻土则以其轻质多孔、化学稳定性高、环境友好等特点,在土壤改良领域展现出广阔的应用潜力[7]。生物质炭和硅藻土可能通过改变土壤理化性质和微生物活性来调控硝化过程[8-9]。然而,现有研究多集中于非盐渍化土壤,关于其在滨海盐渍土中的作用机制和效果,尤其是对氨氧化古菌(AOA)和氨氧化细菌(AOB)群落的影响研究尚不充分。
AOA和AOB是驱动硝化过程的关键微生物类群,二者在生态位和功能上存在显著差异[10]。研究表明,AOA通常在低氨浓度和酸性环境中更具优势[11],而AOB则在高氨浓度和中性至碱性环境中表现出更强的适应性[12]。在滨海盐渍土中,高盐度显著抑制土壤硝化过程,可能与其抑制AOA和AOB的活性并影响群落组成有关[13]。AOA和AOB对盐度的耐受性也存在差异:AOA在较高盐分条件下可能更具优势,而AOB在低盐环境中更为活跃[14]。这种功能分化可能与AOA和AOB的生理特性及其对环境的适应性有关。例如,AOA可能通过更高效的氨摄取机制在低氨环境中占据优势,而AOB则通过更高的氨氧化速率在高氨环境中占据主导地位[15]。此外,AOA和AOB的群落结构对土壤pH、盐度和养分条件的响应也存在差异,这进一步影响了其在硝化过程中的功能角色[16]。
基于上述背景做出如下假设:1)生物质炭和硅藻土通过改变土壤中无机氮的动态变化,对AOA和AOB的丰度及群落结构产生差异化影响;2)生物质炭和硅藻土的添加会改变AOA和AOB的群落结构,进而影响硝化过程。为此,本研究以黄河三角洲滨海盐渍土为对象,结合分子生态学方法,通过对比硅藻土、生物质炭和DCD对土壤无机氮的影响,探明生物质炭和硅藻土如何通过改变无机氮的动态变化,影响AOA和AOB的丰度及群落结构,揭示AOA和AOB对生物质炭和硅藻土添加的响应机制,明确生物质炭和硅藻土对AOA和AOB群落的差异化调控如何影响硝化过程,旨在探究生物质炭和硅藻土对滨海盐渍土中无机氮动态变化的影响,并揭示其对AOA和AOB丰度及群落结构的差异化调控机制。研究结果将为阐明生物质炭和硅藻土在滨海盐渍土中的硝化调控效应及其微生物学机制提供理论依据,并为滨海盐渍土改良和氮肥高效利用提供技术支撑。
1 材料与方法 1.1 供试材料供试土壤采自山东省农业科学院黄河三角洲现代农业试验示范基地(37°17´N,118°36´E)的旱地,该区域位于黄河三角洲典型地带,属暖温带大陆性季风气候,年均降水量552 mm,年均蒸发量2 431 mm,年均气温6.8~18.9 ℃。土壤类型为盐化潮土,质地为黏壤土[17]。采用“S”形采样法采集表层土壤(0~20 cm),将土样充分混匀后于室温下阴凉处风干、压碎过2 mm筛,剔除石砾和动植物残体后保存备用。土壤基本性质为:pH 7.3,电导率(EC)1 827 µS·cm–1,含盐量5.6 g·kg–1,属于重度盐渍土(含盐量范围为4~6 g·kg–1),有机质12.3 g·kg–1,全氮770 mg·kg–1,铵态氮(NH4+-N)6.86 mg·kg–1,亚硝态氮(NO2–-N)0.50 mg·kg–1,NO3–-N101.4 mg·kg–1。
试验所用硅藻土为吉林长白硅藻土,有机质含量0.28 g·kg–1,全氮量极低(1.1 mg·kg–1)。生物质炭为水稻秸秆生物质炭,其含碳量523.9 g·kg–1,含氮量1.8 g·kg–1,碳氮比291.1。硝化抑制剂为DCD,由阿拉丁公司生产,纯度为98%。
1.2 试验设计试验设置5个处理,各处理3次重复:1)不施肥(CK);2)施用250 mg·kg–1干土的尿素(U);3)施用等量尿素并添加施氮量4%的DCD(DCD);4)施用等量尿素并添加相当于干土质量2.5%的硅藻土(DE);5)施用尿素并添加相当于干土质量2.5%的稻壳生物质炭(BC)。
硅藻土和生物质炭与风干土按比例混匀,取相当于20 g烘干土的风干土于250 mL三角瓶中,调节土壤水分至最大持水量(WHC)的40%,封口膜覆盖,在25 ℃恒温培养箱中预先培养一周以激活土壤微生物。预培养7 d后,将尿素和DCD溶液加入土壤中,加入量为2 mL,含氮量均为250 mg·kg–1干土,DCD用量为施氮量4%。同时加入蒸馏水调节水分至65% WHC,封口膜覆盖,扎3孔以保证通气,于25 ℃恒温培养箱中培养42 d,每隔2~3 d称重补水。
于培养0、7、14、28和42 d采集土壤样品。采用破坏性取样方法,各处理随机取3瓶,按土水比1∶5加入2 mol·L–1 KCl溶液,于25 ℃、250 r·min–1振荡1 h,用定量滤纸过滤,收集滤液用于测定NH4+-N、NO2–-N和NO3–-N浓度。此外,取培养7、14和42 d的土壤样品于–20 ℃保存,用于AOA、AOB荧光定量和高通量测序分析。
1.3 测定方法土壤pH和电导率分别按照土水比1∶5浸提后,使用pH计(Mettler S210,美国)和电导率仪(DDS-11A)进行测定。土壤全氮采用凯氏定氮仪(KDY-9830)测定,土壤有机质含量采用重铬酸钾(K2Cr2O7)氧化容量法测定。土壤KCl浸提液中的NH4+-N、NO2–-N和NO3– -N浓度采用全自动间断化学分析仪(Smartchem 200S/N1104238,WESTCO,法国)测定。
DNA提取严格按照Fast DNATM Spin Kit for Soil试剂盒上的说明步骤进行,提取后的DNA样品保存在–20 ℃备用,采用微量紫外分光光度计(NanoDrop 2000c,美国)测定DNA浓度和纯度。采用实时荧光定量PCR技术研究不同处理下滨海盐渍土中AOA和AOB的丰度变化。使用TB Green Premix Ex TaqTM试剂盒在CFX96实时光学检测系统进行定量分析。定量PCR反应体系为20 μL,包括1 μL DNA模板、10 μL TB Green Premix Ex Taq,正反向引物各0.5 μL(10 μmol·L–1),并用无菌水补齐。使用引物Arch-amoA-for/Arch-amoA-rev[18]和amoA-1F/amoA-2R[19]分别对氨氧化微生物AOA和AOB功能基因amoA进行定量分析。实时定量PCR的标准曲线采用arch-amoA、amoA基因的代表性克隆重组质粒进行10倍稀释,稀释梯度为8个。空白样品模板为水,根据标准曲线计算样品基因拷贝数,并以每克干土中的基因拷贝数为单位进行分析。每个样品设3次重复,并设置不加模板的反应管为阴性对照。通过标准曲线确定扩增效率,所有PCR反应的扩增效率均在90%以上,决定系数(R2)均大于98%。
采用高通量测序技术研究不同处理对氨氧化微生物群落结构的影响。针对AOA的arch-amoA基因的特异性引物(Arch-amoAF/Arch-amoAR)[20]和AOB的amoA基因的特异性引物(amoA-1F/ amoA-2R)[19]进行PCR扩增,扩增产物长度分别为635 bp和491 bp。PCR反应体系为20 μL,包含4 μL的5×FastPfu缓冲液、2 μL的2.5 mmol·L–1 dNTPs、0.8 μL的正反向引物(5 μmol·L–1)、0.4 μL的FastPfu聚合酶以及10 ng的DNA模板,每个样品设置3个平行重复。PCR反应参数为:95 ℃预变性5 min,95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s,AOA和AOB引物分别扩增40和35个循环;最后72℃延伸10 min。扩增后的PCR产物通过2%琼脂糖凝胶电泳进行检测和分离,并使用AxyPrep DNA凝胶回收试剂盒(Axygen Biosciences,USA)按照生产商的说明书进行纯化。纯化后的PCR产物使用Illumina PE250平台进行双端测序(上海凌恩生物有限公司)。每个样品的测序深度为34 000~42 000条有效读段(reads)。
1.4 数据处理净硝化速率(Net nitrification rate,NNR)定义为单位培养天数内的净硝化量(mg·kg–1·d–1),计算公式如下:
| $ {\text{NNR = }}\frac{{C{{{\text{[NO}}_{\text{3}}^ - - N{\text{]}}}_t} - C{{{\text{[NO}}_{\text{3}}^ - - N{\text{]}}}_{{t_{\text{0}}}}}}}{{t - {t_0}}} $ | (1) |
式中,C[NO3–-N]t和C[NO3–-N]t0分别为培养时间t和初始时间t0时土壤NO3–-N浓度,mg·kg–1;t为培养时间,d;t0为初始培养时间,d。
净矿化速率(Net mineralization rate,NMR)定义为单位培养天数内的净矿化量,mg·kg–1·d–1,计算公式如下:
| $ {\text{NMR = }}\frac{{C{{{\text{[NH}}_4^ + - {\text{N + NO}}_3^ - - {\text{N]}}}_{{t_{\text{2}}}}} - C{{{\text{[NH}}_4^ + - {\text{N + NO}}_3^ - - {\text{N]}}}_{{t_{\text{1}}}}}}}{{{t_{\text{2}}} - {t_1}}} $ | (2) |
式中,C[NH4+-N+NO3–-N]t□为培养时间t2时土壤NH4+-N和NO3– -N浓度之和,mg·kg–1;C[NH4+-N+NO3– -N]t1为培养时间t1时土壤NH4+-N和NO3–-N浓度之和,mg·kg–1;t2和t1为培养时间,d。
硝化抑制率(Nitrification inhibition ratio,NIR)(%)计算公式如下:
| $ {\text{NIR = }}\left( {\frac{{\Delta C{{{\text{[NO}}_3^ - - {\text{N]}}}_{\text{U}}} - \Delta C{{{\text{[NO}}_3^ - - {\text{N]}}}_{\text{T}}}}}{{\Delta C{{{\text{[NO}}_3^ - - {\text{N]}}}_{\text{U}}}}}} \right) $ | (3) |
式中,
试验数据使用Excel 2010整理后,采用SPSS 16.0软件进行单因素方差分析(one-way ANOVA),并使用最小显著性差异法(LSD)进行差异显著性检验(α= 0.05)。在本研究中,显著性差异水平设定为P < 0.05。若未特别说明,所有比较均基于此显著性水平。相关性分析采用Pearson相关分析,并使用SPSS 16.0软件进行。使用Origin 2021作图。高通量数据分析采用R语言的vegan包进行基于Bray-Curtis距离矩阵的聚类树分析。所有Illumina PE250测序的原始数据已上传至NCBI序列读取档案(SRA)数据库(登录号为:PRJNA1228279)。
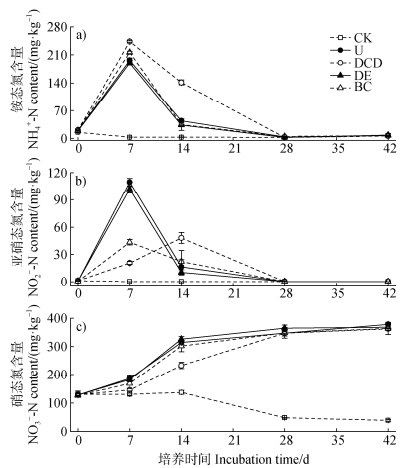
2 结果 2.1 不同处理土壤无机氮含量的变化随着尿素的水解,施氮处理土壤NH4+-N含量于培养7 d时达到峰值,变化范围为190~244 mg·kg–1,其中,DCD处理NH4+-N含量(244 mg·kg–1)最高,其次为BC处理(216 mg·kg–1),二者均显著高于U处理(197 mg·kg–1)和DE处理(190 mg·kg–1),之后随着培养时间的推移逐渐下降(图 1a)。培养14 d时,DCD处理NH4+-N含量分别较U、DE和BC处理高出2.2倍、3.2倍和2.0倍(图 1a)。培养后期,不同处理间NH4+-N含量差异不显著。
|
注:图中误差线为标准误差,n=3。CK:不施肥;U:单施尿素;DCD、DE和BC分别代表施加尿素并添加双氰胺、硅藻土和生物质炭。下同。 Note: Error bars are standard errors, n=3. CK: no fertilizer; U: urea application; DCD, DE, and BC stand for application of urea in combination with DCD, diatomite, and biochar, respectively. The same below. 图 1 不同处理土壤无机氮含量动态变化 Fig. 1 Dynamics of inorganic N contents in soil under different treatments |
除CK外,U、DE和BC处理中NO2–-N含量在培养7 d时达到峰值,U处理NO2–-N含量与DE处理无显著差异,但显著高于DCD和BC处理的4.3倍和1.5倍(图 1b)。DCD处理NO2–-N累积峰值出现在培养14 d(48.0 mg·kg–1),显著低于U和DE处理的峰值,但与BC处理无显著差异。
各施肥处理NO3–-N含量在培养初期逐渐增加,在42 d的观测期内达到约350 mg·kg–1并趋于稳定,且均显著高于CK(图 1c)。培养7 d时,DCD处理中NO3–-N含量最低(145 mg·kg–1),分别较U、DE和BC处理显著低21.8%、20.1%和13.5%(图 1c)。DE处理NO3–-N含量与U处理无显著差异,但BC处理显著低于U处理(图 1c)。培养14 d时,DE和BC处理NO3–-N含量与U处理无显著差异,但DCD处理较U处理显著低约25.9%(图 1c)。培养后期,不同施氮处理土壤NO3–-N含量差异不显著。
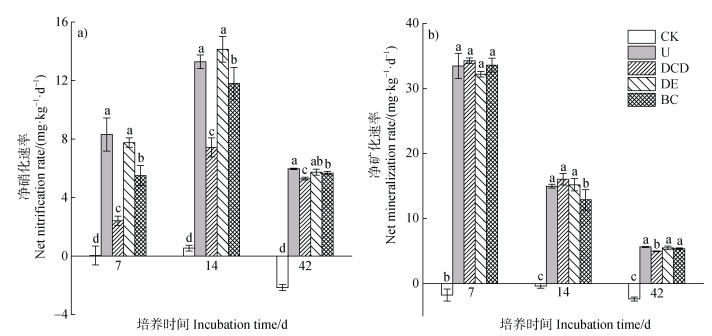
2.2 不同处理对土壤氮转化过程的动态调控效应在不同培养时间,施氮处理土壤的净硝化速率均显著高于对照,土壤净硝化速率随着培养时间的延长呈现先升高后降低的趋势(图 2a)。在培养7 d时,DE处理的净硝化速率与U处理无显著差异,DCD和BC处理的净硝化速率分别较U处理显著低71.0%和33.8%(图 2a)。培养至14、42 d时,各施肥处理间的差异与第7天基本一致,但在培养14 d时,DCD和BC处理的净硝化速率分别较U处理显著降低了44.1%和11.1%(图 2a),至42 d时,DE处理与BC处理的净硝化速率无显著差异(图 2a)。
|
注:同一组柱形图上方不同小写字母表示不同处理间差异显著(P < 0.05)。下同。 Note: Different lowercase letters above the bars within the same group denote significant differences at 0.05 level for different treatments. The same below. 图 2 不同处理培养7、14、42 d土壤净硝化速率和净矿化速率 Fig. 2 Net nitrification rate and net mineralization rate in soil under different treatments at 7, 14, and 42 days after incubation |
施氮处理土壤净矿化速率均显著高于对照,随着培养时间的延长呈逐渐下降的趋势(图 2b)。培养7 d时,各施氮处理间的净矿化速率无显著差异,但均显著高于14、42 d的净矿化速率(图 2b)。培养至14 d时,BC处理的净矿化速率显著低于U、DCD和DE处理,分别降低了14.0%、19.8%和15.3%(图 2b)。培养至42 d时,DCD处理的土壤净矿化速率分别较U、DE和BC处理显著降低了12.0%、9.5%和7.4%(图 2b)。
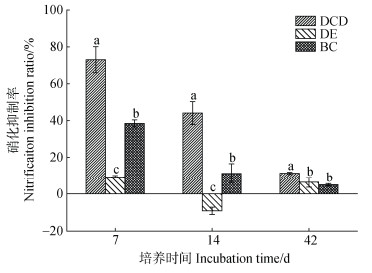
随着培养时间的延长,不同处理的硝化抑制率总体呈逐渐下降趋势(图 3)。在不同培养阶段,DCD处理的硝化抑制率始终最高,培养至7 d时,其硝化抑制率达到最大值(73.1%),随后逐渐下降,至14和42 d时分别降至44.1%和11.2%。BC处理的硝化抑制率在第7天达到最大值(38.5%),显著高于DE处理,但较DCD处理显著低47.3%(图 3)。培养至14 d时,DE处理的硝化抑制率为–9.2%,而BC处理的硝化抑制率为11.2%,显著低于DCD处理(图 3)。培养至42 d时,DE和BC处理的硝化抑制率无显著差异,但二者均显著低于DCD处理(图 3)。
|
图 3 不同施氮处理培养7、14、42 d土壤硝化抑制率 Fig. 3 Nitrification inhibition ratio in soil under different nitrogen treatments at 7, 14, and 42 days after incubation |
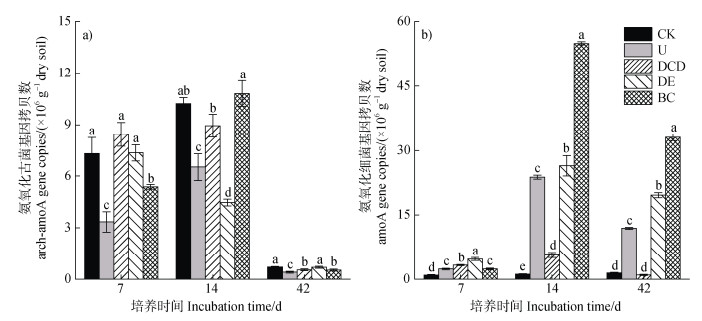
AOA amoA基因丰度整体呈现先升高后降低的趋势(图 4a)。培养初期(7 d),DCD处理AOA amoA基因丰度最高,与对照和DE处理间无显著差异,但显著高于U和BC处理,分别高出1.5倍和0.57倍。培养14 d时,BC处理AOA amoA基因丰度达到最大值,较U、DCD和DE处理分别高出1.7倍、1.2倍和2.4倍,但与CK无显著差异。培养结束时,除CK外,DE处理AOA amoA基因丰度显著高于U、DCD和BC处理。DCD与BC处理间无显著差异,但均显著高于U处理。
|
图 4 不同处理培养7、14和42 d土壤氨氧化古菌(AOA)和氨氧化细菌(AOB)的amoA基因丰度 Fig. 4 Ammonia-oxidizing archaea(AOA)and ammonia-oxidizing bacteria(AOB)amoA gene abundance in soils under different treatments at 7, 14, and 42 days after incubation |
AOB amoA基因丰度的变化趋势与AOA amoA基因丰度随时间的变化趋势一致(图 4b)。除培养42 d时DCD处理中AOB amoA基因丰度与CK无显著差异外,其余施氮处理AOB amoA基因丰度均显著高于CK。培养7 d时,DE处理中AOB amoA基因丰度最高,其次为DCD处理,二者均显著高于U和BC处理。培养14 d时,DCD处理AOB amoA基因丰度最低,较U、DE和BC处理分别显著低76.4%、78.8%和89.8%。培养42 d时,DCD处理AOB amoA基因丰度仍为最低,较U、DE和BC处理分别显著低91.9%、95.1%和97.1%。
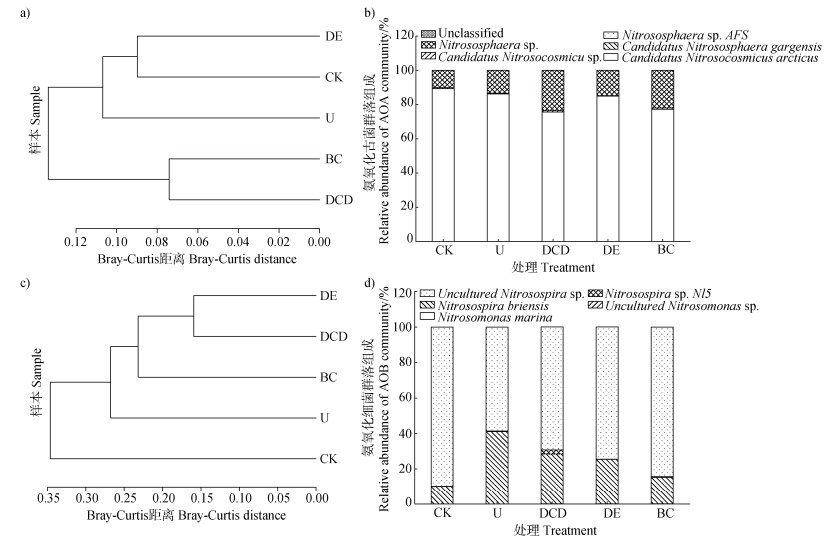
AOA群落结构的相似度树状图如图 5a所示。其中,CK和DE处理归属于第三分支,并与U处理共同归属于第二分支;而DCD和BC处理则归属于第二分支。根据样本在聚类树中的分布位置及枝长分析表明,CK与DE处理间AOA群落结构相似性较高,DCD与BC处理间也具有较高的相似性。在种水平上,各处理中Candidatus Nitrosocosmicus arcticus为优势菌种,相对丰度为75.6%~86.2%;其次为Nitrososphaera sp.(10.2%~23.6%)。值得注意的是,Candidatus Nitrosocosmicus arcticus在U和DE处理的相对丰度高于DCD和BC处理,而Nitrososphaera sp.则在DCD和BC处理表现出更高的相对丰度(图 5b)。
|
a)AOA聚类树Clustering tree of AOA;b)AOA群落组成Community composition of AOA;c)AOB聚类树Clustering tree of AOB;d)AOB群落组成Community composition of AOB。 图 5 培养42 d后不同处理土壤中氨氧化古菌(AOA)和氨氧化细菌(AOB)的聚类树及群落组成 Fig. 5 Clustering trees and community composition of ammonia-oxidizing archaea(AOA)and ammonia-oxidizing bacteria(AOB)in soils under different treatments after 42 days of incubation |
基于AOB群落结构的聚类分析显示(图 5c),第一分支包含CK和第二分支,第二分支包含U处理和第三分支,第三分支包含BC处理和第四分支,第四分支则包含DCD和DE处理,这表明DCD与DE处理间AOB群落结构具有较高的相似性。在种水平上,各处理中Uncultured Nitrosospira sp.为优势菌种,相对丰度为58.6%~89.8%;其次为Nitrosospira briensis(10.0%~41.1%)。除CK外,Uncultured Nitrosospira sp.在BC处理相对丰度最高(84.3%),而Nitrosospira briensis则在U处理达到最高相对丰度(41.1%,图 5d)。
2.4 氨氧化微生物基因丰度与土壤硝化过程关键指标的关系相关性分析结果表明,AOA和AOB的基因丰度变化与硝化过程密切相关(表 1)。AOA amoA基因丰度与NH4+-N含量(r = 0.34)和NIR(r = 0.46)呈显著正相关,而与NO3–-N含量(r = –0.38)呈显著负相关。与AOA相反,AOB amoA基因丰度与NH4+-N含量(r = –0.34)和NIR(r = –0.45)呈显著负相关,而与NO3–-N含量(r = 0.57)呈极显著正相关。通过相关分析,AOB amoA基因丰度与NNR(r = 0.62)呈极显著正相关,而AOA amoA基因丰度与NNR的相关性较弱(r = 0.13)。此外,AOA/AOB比值与NO3–-N含量(r = 0.55)和NIR(r = 0.80)呈极显著正相关,而与NNR(r = –0.53)呈极显著负相关。
|
|
表 1 土壤氨氧化功能基因丰度与氮转化特征之间的相关分析 Table 1 Correlation analysis between soil ammonia-oxidizing functional gene abundance and nitrogen transformation characteristics |
本研究结果表明,DCD在培养初期显著抑制了滨海盐渍土壤的硝化过程,降低了NO3–-N的累积(图 1),这与以往研究结果一致[21]。DCD于预培养7 d后添加,而硅藻土和生物质炭在预培养前加入。此设计旨在区分DCD的靶向抑制效应与改良剂的长期物理化学调控作用。DCD通过抑制氨单加氧酶(AMO)的活性,可有效阻碍NH4+-N向NO2–-N的氧化过程,进而减少NO3–-N的产生[22]。在本研究中,DCD处理的硝化抑制率在培养初期(7 d)达到了最大值(73.1%,图 3),其高效性得益于预培养7 d后稳定的土壤微环境:1)微生物代谢功能恢复。风干土壤经复水后通过预培养恢复原有微生物群落的基础代谢活性。参考同类土壤硝化作用研究[23-24],7 d时长可确保AOB等关键功能菌群完成活性激活,使DCD精准抑制活跃的AOB(图 4b)。2)吸附时效归一化。通过高氮输入(250 mg·kg–1)稀释硅藻土/生物质炭对本底NH4+-N(6.86 mg·kg–1)的初期吸附差异(图 1a),有效规避了对后续硝化抑制率评估的干扰。然而,随着培养时间的延长,DCD的抑制效果逐渐减弱,这可能是由于DCD在土壤中逐渐分解或被微生物代谢所致[25-26],提示其单一应用的局限性,需结合缓释技术或与其他改良剂联用以延长持效性。
与DCD相比,生物质炭在短期内(0~14 d)表现出轻度硝化抑制(抑制率11.2%~33.7%,图 3),其机制可能包括:1)生物质炭具有较大的比表面积和孔隙结构,能够吸附土壤中的NH4+-N[27],在预培养期间(7 d)完成对本底氮的吸附,后续高氮输入削弱了其短期吸附差异(图 1a);2)生物质炭可能通过改变土壤微环境(如pH、养分和透气性)间接影响硝化过程[28],但预培养后稳定的微生物群落削弱了此类间接效应的显著性。值得注意的是,生物质炭的抑制率在42 d后降至4.8%(图 3),可能反映其吸附饱和或微生物群落的适应性增强。此外,生物质炭在培养后期对AOA丰度的促进作用(图 4a)暗示其可能通过长期调控微生物结构影响硝化进程,但需进一步验证。
在氮肥加入后的2 h内DE处理中的NH4+-N浓度显著低于U处理,而BC处理未表现出显著的吸附作用,凸显了二者物理吸附的时效性差异。硅藻土对硝化过程的抑制作用并不显著,NO3–-N累积量持续升高(图 1c),甚至在某些情况下表现出促进硝化的趋势(14 d时抑制率为-9.2%,图 3),可能与以下机制相关[7]:1)多孔结构改善通气性:预培养7 d使硅藻土充分整合至土壤基质,为AOB增殖提供富氧环境(图 4b);2)保水保肥效应:硅藻土的高保水性维持尿素水解产生的NH4+-N持续释放,驱动AOB主导的硝化进程(表 1);3)表面电荷特性:硅藻土(表面负电荷)对NO3–-N的弱吸附性可能加速硝化产物的累积。硅藻土的促硝化特性表明其适用于需加速氮循环的盐渍土改良场景,但需警惕氮素淋失风险。
相关性分析表明,AOB的amoA基因丰度与NO3–-N含量和净硝化速率呈极显著正相关,而AOA的amoA基因丰度与NO3–-N含量呈显著负相关,却与净硝化速率相关性不显著(表 1)。这一结果支持了生物质炭和硅藻土通过调控AOB丰度来影响硝化过程的机制,可能与预培养后稳定的土壤pH密切相关:在中性-弱碱性条件下,AOB对氨氧化过程的主导作用已被广泛证实[29]。因此,通过预培养7 d的设计平衡吸附差异和微生物恢复,本研究不仅更精准地揭示了AOB在滨海盐渍土硝化中的核心地位,也为结果的可靠性提供了关键支撑。尽管预培养期间未直接监测吸附动态及微生物活性恢复参数,可能影响时效性机制的精细解析,但通过高氮输入与文献参照[23-24]间接验证了时间节点的科学性。未来研究建议增设预培养期间的高频动态监测(如每24 h测定吸附量及微生物多样性参数),并结合生物质炭/硅藻土与DCD的协同施用方案,以平衡硝化抑制的即时效应与土壤氮素的长效调控需求。
3.2 硅藻土和生物质炭对滨海盐渍土壤氨氧化微生物丰度及群落的影响氨氧化微生物(AOA和AOB)在土壤氮素循环中发挥着至关重要的作用,二者在功能和生态位上存在差异[10]。本研究中,AOA和AOB的丰度在不同处理下呈现出不同的变化趋势,揭示了不同改良剂对氨氧化微生物群落的差异化影响。在培养初期,DCD处理显著提高了AOA的丰度(图 4a),这可能是因为DCD对AOB的抑制作用更强,从而间接促进了AOA的生长和繁殖。这一结果与一些研究发现DCD对AOB的抑制作用大于AOA的抑制作用一致[30-31]。DCD对AOB丰度的抑制效果持续到42 d,但对NH4+-N和NO3–-N含量的影响在14 d后逐渐减弱,可能原因如下:1)残留的AOB种群通过适应性机制(如酶活性调节或代谢补偿)恢复了部分功能[32];2)其他微生物(如AOA或异养硝化细菌)的活跃补偿了AOB功能活性的下降[10];3)底物(NH4+-N)浓度逐渐降低,减少了AOB的功能压力[11];4)DCD的抑制效果随时间逐渐减弱[33]。
随着培养时间的推移,生物质炭则表现出促进AOB丰度的作用,这与前期研究结果一致[34],可能与生物质炭对土壤微环境(如pH、养分和透气性)的改善更有利于AOB的生长和繁殖有关[35-36]。硅藻土则显著提高了AOB的丰度(图 4b),表明硅藻土为AOB提供了更适宜的生长环境。硅藻土的多孔结构可能增加了土壤的通气性,促进了氧气的供应,从而提高了AOB的活性。此外,硅藻土中的某些成分可能也为AOB的生长提供了必要的营养物质[7]。DCD处理显著抑制了AOB的丰度(图 4b),进一步证实了DCD对AOB的直接抑制作用。这表明,DCD对氨氧化微生物群落的影响具有选择性,不同类型的微生物对其响应存在差异[37]。生物质炭促进AOA丰度,而硅藻土促进AOB丰度的特性,为材料的合理搭配和应用提供了参考。
从群落结构上来看,不同处理对氨氧化微生物群落结构的影响各不相同。CK和DE处理中AOA的群落结构相似,而DCD和BC处理中AOA的群落结构更为相似(图 5a),表明硅藻土对AOA群落结构的影响较小,而DCD和生物质炭可能通过不同的机制影响AOA的群落结构。例如,DCD可能通过抑制氨单加氧酶的活性改变AOA的群落结构,而生物质炭可能通过吸附作用影响底物的释放,从而影响AOA的群落结构。AOB的群落结构也呈现出类似的趋势,DCD和DE处理中AOB的群落结构较为相似,而其他处理的AOB群落结构则相对分散(图 5b),这可能与DCD对AOB的直接抑制作用以及硅藻土对AOB的促进作用有关。此外,AOA的主要优势菌种为Candidatus Nitrosocosmicus arcticus和Nitrososphaera sp.,AOB的主要优势菌种为Uncultured Nitrosospira sp.和Nitrosospira briensis,这些优势菌种在滨海盐渍土氮循环中可能发挥着关键作用[14,38]。这些发现有助于进一步了解滨海盐渍土壤中氨氧化微生物的群落结构和功能特征。
本研究表明,生物质炭和硅藻土在滨海盐渍土中的硝化调控效果存在显著差异,其中生物质炭更适合作为AOA的促进剂,而硅藻土则更有利于AOB的生长。在实际应用中,可根据土壤盐渍化程度和氮素管理目标选择改良剂:对于氮素易流失的盐渍土,可考虑使用生物质炭抑制硝化作用;对于氮素转化缓慢的盐渍土,可考虑使用硅藻土促进硝化作用。此外,生物质炭和硅藻土的混合使用可能达到更好的改良效果。需要注意的是,由于本研究时间较短,可能无法完全反映生物质炭和硅藻土对微生物群落的长期影响,因此,未来研究可结合田间试验,进一步探讨生物质炭和硅藻土的长期效应及其与其他改良措施的协同作用,并综合考虑温度、pH和水分等因素,深入研究通过调控氨氧化微生物群落结构来改善盐渍土壤氮素转化机制,从而为盐渍土壤氮肥高效利用提供更全面的理论支撑。
4 结论DCD、生物质炭和硅藻土对滨海盐渍土壤的硝化过程具有不同的影响效果。DCD在短期内能有效抑制盐渍土的硝化过程,显著降低NO3–-N累积,但其抑制效果会随时间减弱;生物质炭短期内也具有一定的硝化抑制作用,但长期来看,其对AOA的丰度具有促进作用;硅藻土则对硝化过程的抑制作用不显著,反而显著提高了AOB的丰度。AOA丰度与NO3–-N积累显著负相关,AOB丰度与NO3–-N浓度极显著正相关,表明二者功能分化。生物质炭和硅藻土分别通过吸附-缓释和物理吸附机制改变氮素分布,进而调控AOA与AOB的竞争关系,影响硝化进程。
致谢 感谢山东省农业科学院黄河三角洲现代农业试验示范基地为本研究提供的土壤样品。感谢实验室全体成员对本研究的帮助。
| [1] |
Li Z L, Zeng Z Q, Tian D S, et al. Global patterns and controlling factors of soil nitrification rate[J]. Global Change Biology, 2020, 26(7): 4147-4157. DOI:10.1111/gcb.15119
(  0) 0) |
| [2] |
Tian H Q, Xu R T, Canadell J G, et al. A comprehensive quantification of global nitrous oxide sources and sinks[J]. Nature, 2020, 586(7828): 248-256. DOI:10.1038/s41586-020-2780-0
(  0) 0) |
| [3] |
Nouri A, Lukas S, Singh S, et al. When do cover crops reduce nitrate leaching? A global meta-analysis[J]. Global Change Biology, 2022, 28(15): 4736-4749. DOI:10.1111/gcb.16269
(  0) 0) |
| [4] |
Duff A M, Forrestal P, Ikoyi I, et al. Assessing the long-term impact of urease and nitrification inhibitor use on microbial community composition, diversity and function in grassland soil[J]. Soil Biology and Biochemistry, 2022, 170: 108709. DOI:10.1016/j.soilbio.2022.108709
(  0) 0) |
| [5] |
Liu Q, Zhang Y H, Liu B J, et al. How does biochar influence soil N cycle? A meta-analysis[J]. Plant and Soil, 2018, 426(1-2): 211-225. DOI:10.1007/s11104-018-3619-4
(  0) 0) |
| [6] |
Palansooriya K. N, Wong J T F, Hashimoto Y, et al. Response of microbial communities to biochar-amended soils: a critical review[J]. Biochar, 2019, 1(1): 3-22. DOI:10.1007/s42773-019-00009-2
(  0) 0) |
| [7] |
Aksakal E L, Angin I, and Oztas T. Effects of diatomite on soil physical properties[J]. Catena, 2012, 88(1): 1-5.
(  0) 0) |
| [8] |
Ren X N, Wang Q, Chen X, et al. Pathways and mechanisms of nitrogen transformation during co-composting of pig manure and diatomite[J]. Bioresource Technology, 2021, 329: 124914. DOI:10.1016/j.biortech.2021.124914
(  0) 0) |
| [9] |
Liu Q, Wu Y X, Ma J, et al. How does biochar influence soil nitrification and nitrification-induced N2O emissions?[J]. Science of The Total Environment, 2024, 908: 168530. DOI:10.1016/j.scitotenv.2023.168530
(  0) 0) |
| [10] |
Prosser J I and Nicol G W. Archaeal and bacterial ammonia-oxidisers in soil: the quest for niche specialisation and differentiation[J]. Trends in Microbiology, 2012, 20(11): 523-531. DOI:10.1016/j.tim.2012.08.001
(  0) 0) |
| [11] |
Zhang L M, Hu H W, Shen J P, et al. Ammonia-oxidizing archaea have more important role than ammonia-oxidizing bacteria in ammonia oxidation of strongly acidic soils[J]. The ISME Journal, 2012, 6(5): 1032-1045. DOI:10.1038/ismej.2011.168
(  0) 0) |
| [12] |
Yin C, Tan C, Chen H, et al. Insight into the role of competition in niche differentiation between ammonia-oxidizing archaea and bacteria in ammonium-rich alkaline soil: A network-based study[J]. Soil Biology and Biochemistry, 2022, 168: 108638. DOI:10.1016/j.soilbio.2022.108638
(  0) 0) |
| [13] |
Zhu H, Yang J S, Li Y L, et al. Effects of soil salinity on nitrification and ammonia-oxidizing microorganisms in coastal reclaimed farmland soil[J]. Journal of Soil Science and Plant Nutrition, 2022, 22(2): 2743-2754. DOI:10.1007/s42729-022-00841-9
(  0) 0) |
| [14] |
Sun X X, Zhao J, Zhou X, et al. Salt tolerance-based niche differentiation of soil ammonia oxidizers[J]. The ISME Journal, 2022, 16(2): 412-422. DOI:10.1038/s41396-021-01079-6
(  0) 0) |
| [15] |
Martens-Habbena W, Berube P M, Urakawa H, et al. Ammonia oxidation kinetics determine niche separation of nitrifying Archaea and Bacteria[J]. Nature, 2009, 461(7266): 976-979. DOI:10.1038/nature08465
(  0) 0) |
| [16] |
Tao J Y and Liu X Y. The effect of soil salt content and ionic composition on nitrification in a Fluvisol of the Yellow River Delta[J]. Soil and Tillage Research, 2024, 235: 105907. DOI:10.1016/j.still.2023.105907
(  0) 0) |
| [17] |
Liu X Y, Yang J S, Tao J Y, et al. Effects of the combined application of biochar and humic substances on the improvement of saline cropland in the Yellow River Delta of China[J]. Land Degradation and Development, 2023, 34(15): 4793-4809. DOI:10.1002/ldr.4810
(  0) 0) |
| [18] |
Tourna M, Freitag T E, Nicol G W, et al. , Growth, activity and temperature responses of ammonia-oxidizing archaea and bacteria in soil microcosms[J]. Environmental Microbiology, 2008, 10(5): 1357-1364. DOI:10.1111/j.1462-2920.2007.01563.x
(  0) 0) |
| [19] |
Rotthauwe J H, Witzel K. P, and Liesack W. The ammonia monooxygenase structural gene amoA as a functional marker: molecular fine-scale analysis of natural ammonia-oxidizing populations[J]. Applied and Environmental Microbiology, 1997, 63(12): 4704-4712. DOI:10.1128/aem.63.12.4704-4712.1997
(  0) 0) |
| [20] |
Francis C A, Roberts K J, Beman J M, et al. Ubiquity and diversity of ammonia-oxidizing archaea in water columns and sediments of the ocean[J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(41): 14683-14688.
(  0) 0) |
| [21] |
Ma L, Shan J, and Yan X Y. Nitrite behavior accounts for the nitrous oxide peaks following fertilization in a fluvo-aquic soil[J]. Biology and Fertility of Soils, 2015, 51(5): 563-572. DOI:10.1007/s00374-015-1001-8
(  0) 0) |
| [22] |
Wu Z J, Shi Y F, Chen L J. Research progress of the mechanisms of nitrification inhibition (In Chinese)[J]. Chinese Journal of Soil Science, 2008, 39(4): 962-970. [武志杰, 史云峰, 陈利军. 硝化抑制作用机理研究进展[J]. 土壤通报, 2008, 39(4): 962-970.]
(  0) 0) |
| [23] |
Huang J J, He L L, Liu Y X, et al. Effects of biochar combined with nitrification /urease inhibitors on soil active nitrogen emissions from subtropical paddy soils (In Chinese)[J]. Chinese Journal of Applied Ecology, 2022, 33(4): 1027-1036. [黄佳佳, 何莉莉, 刘玉学, 等. 生物炭配施硝化/脲酶抑制剂对亚热带水稻土活性氮气体排放的影响[J]. 应用生态学报, 2022, 33(4): 1027-1036.]
(  0) 0) |
| [24] |
Wang X Q, Jiang C L, Meng L W, et al. Effects of combined application of biochar and nitrification inhibitor on N2O emission from tropical rice-vegetable rotation soils in Hainan region (In Chinese)[J]. Journal of Agro-Environment Science, 2025, 44(6): 1667-1674. [王小淇, 蒋春兰, 孟龙威, 等. 生物炭配施硝化抑制剂对热区稻菜轮作土壤N2O排放的影响[J]. 农业环境科学学报, 2025, 44(6): 1667-1674.]
(  0) 0) |
| [25] |
Sun Z M, Wu Z J, Chen L J, et al. Application effects, affecting factors, and evaluation of nitrification inhibitors: A review (In Chinese)[J]. Chinese Journal of Applied Ecology, 2008, 19(7): 1611-1618. [孙志梅, 武志杰, 陈利军, 等. 硝化抑制剂的施用效果、影响因素及其评价[J]. 应用生态学报, 2008, 19(7): 1611-1618.]
(  0) 0) |
| [26] |
Guardia G, Marsden K A, Vallejo A, et al. Determining the influence of environmental and edaphic factors on the fate of the nitrification inhibitors DCD and DMPP in soil[J]. Science of The Total Environment, 2018, 624: 1202-1212. DOI:10.1016/j.scitotenv.2017.12.250
(  0) 0) |
| [27] |
Xiang J, Sun X, Wang C, et al. Effects of biochar application on nitrogen transformation and N2O emission in a coastal saline-alkali soil (In Chinese)[J]. Chinese Journal of Applied Ecology, 2023, 34(11): 2969-2977. [项剑, 孙禧, 王成, 等. 生物炭对滨海盐碱土氮素转化和N2O排放的影响[J]. 应用生态学报, 2023, 34(11): 2969-2977.]
(  0) 0) |
| [28] |
Wang H K, Wu Y B, Liu J P, et al. A review of research advances in the effects of biochar on soil nitrogen cycling and its functional microorganisms (In Chinese)[J]. Journal of Ecology and Rural Environment, 2022, 38(6): 689-701. [王翰琨, 吴永波, 刘俊萍, 等. 生物炭对土壤氮循环及其功能微生物的影响研究进展[J]. 生态与农村环境学报, 2022, 38(6): 689-701.]
(  0) 0) |
| [29] |
Sun J L, Rengel Z, Zhou Y Z, et al. Ammonia-oxidizing archaea bacteria(AOB)and comammox drive the nitrification in alkaline soil under long-term biochar and N fertilizer applications[J]. Applied Soil Ecology, 2024, 193: 105124. DOI:10.1016/j.apsoil.2023.105124
(  0) 0) |
| [30] |
Zhou X, Wang S W, Ma S T, et al. Effects of commonly used nitrification inhibitors—dicyandiamide(DCD), 3, 4-dimethylpyrazole phosphate(DMPP), and nitrapyrin— on soil nitrogen dynamics and nitrifiers in three typical paddy soils[J]. Geoderma, 2020, 380: 114637. DOI:10.1016/j.geoderma.2020.114637
(  0) 0) |
| [31] |
Shen X Y, Xia W W, Cirenlamu, et al. Effect of allylthiourea on soil nitrification and the underlying microbial mechanism in short-term laboratory microcosms (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(6): 1552-1563. [沈晓忆, 夏围围, 次仁拉姆, 等. 短期培养下抑制剂烯丙基硫脲对土壤硝化作用及微生物的影响[J]. 土壤学报, 2021, 58(6): 1552-1563.]
(  0) 0) |
| [32] |
Di H J and Cameron K C. How does the application of different nitrification inhibitors affect nitrous oxide emissions and nitrate leaching from cow urine in grazed pastures?[J]. Soil Use and Management, 2011, 28(1): 54-61.
(  0) 0) |
| [33] |
Lan T, Han Y, Roelcke M, et al. Effects of the nitrification inhibitor dicyandiamide(DCD)on gross N transformation rates and mitigating N2O emission in paddy soils[J]. Soil Biology and Biochemistry, 2013, 67: 174-182. DOI:10.1016/j.soilbio.2013.08.021
(  0) 0) |
| [34] |
Song Y J, Zhang X L, Ma B, et al. Biochar addition affected the dynamics of ammonia oxidizers and nitrification in microcosms of a coastal alkaline soil[J]. Biology and Fertility of Soils, 2013, 50(2): 321-332.
(  0) 0) |
| [35] |
Xiao Z G, Rasmann S, Yue L, et al. The effect of biochar amendment on N-cycling genes in soils: A meta-analysis[J]. Science of The Total Environment, 2019, 696: 133984. DOI:10.1016/j.scitotenv.2019.133984
(  0) 0) |
| [36] |
Liu X. R, Shi Y L, Zhang Q W, et al. Effects of biochar on nitrification and denitrification-mediated N2O emissions and the associated microbial community in an agricultural soil[J]. Environmental Science and Pollution Research, 2020, 28(6): 6649-6663.
(  0) 0) |
| [37] |
Yin M J, Gao X P, Kuang W N, et al. Meta-analysis of the effect of nitrification inhibitors on the abundance and community structure of N2O-related functional genes in agricultural soils[J]. Science of The Total Environment, 2023, 865: 161215. DOI:10.1016/j.scitotenv.2022.161215
(  0) 0) |
| [38] |
Shi Y L, Liu X R, Zhang Q W, et al. Biochar and organic fertilizer changed the ammonia-oxidizing bacteria and archaea community structure of saline–alkali soil in the North China Plain[J]. Journal of Soils and Sediments, 2019, 20(1): 12-23.
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


