2. 河南大学商学院, 河南开封 475004;
3. 河南大学人工智能学院, 郑州 450046
2. Business School of Henan University, Kaifeng, Henan 475004, China;
3. School of Artificial Intelligence, Henan University, Zhengzhou 450046, China
根际是受植物根系活动影响形成的微域环境[1],是植物与土壤互作的界面。根际土壤中富含拟杆菌、变形菌和其他富营养型微生物[2],植物通过根系分泌物影响土壤微生物群落组成,同时根际微生物通过多种机制影响植物的生长和发育。根系分泌物是指植物正常生长过程中,由根系不同部位向外界环境释放的一系列化学物质,包括氨基酸、糖、酚类和酶类等[3-4],对根际土壤生态环境中的物质循环具有重要的驱动作用[5]。根系分泌物能提供养分和生长调节物质,从而促进植物生长代谢[6];还能参与根际土壤中植物组织和微生物群落的调节,影响植物生长和土壤生态,进而增强植物抗逆性[7-8],在植物生长和生态系统中发挥着重要作用。
根际微生物是与根际相关的微生物的完整集合,通过数亿年的相互作用与共同进化,根际微生物与植物根际之间形成了复杂的关系,例如互利共生、共生、寄生和竞争等[9-11]。根系分泌物与微生物之间存在互作效应,形成植物−微生物的共生网络,这有利于养分循环,提高土壤的肥力。植物根系分泌物通过释放特定的化学信号物质(如酚酸、黄酮类化合物和糖类)主动调控根际微生物的群落组成和功能[12]。例如,拟南芥分泌的芥子油苷衍生物可特异性招募具有硫苷代谢能力的细菌(如假单胞菌属),从而抑制土传病原菌并促进植物健康[13]。水稻中,根系分泌的独脚金内酯不仅吸引丛枝菌根真菌以增强磷吸收,还能诱导根际放线菌分泌抗生素,协同抵御病原菌入侵[14]。此外,在干旱胁迫下,玉米根系分泌的甜菜碱和脯氨酸可富集具有1-氨基环丙烷-1-羧酸(ACC)脱氨酶活性的伯克氏菌属(Burkholderia),通过降低乙烯合成缓解植物胁迫损伤,同时增强土壤持水性[15]。故根系分泌物及根际微生物在调控陆地生态系统根际微环境间的物质、能量和信息交流中具有重要作用[16]。因此,构建准确、适用的根系分泌物收集方法及土壤样品采集方法,是理解植物根系−土壤界面生态过程的关键环节和前提。由于植物根系的生长高度依赖周围土壤环境,且根系形态错乱复杂,在不影响根系生长的同时,避开对根系本身损伤的情况下,实现对根系分泌物及根际土壤的匹配收集存在一定的难度。
鉴于操作便捷性与农业生产实际需求,研究者针对生长周期较短的草本植物,开发出多种室内根系分泌物收集方法。这些方法分为非连续式收集法与连续式收集法两大类。非连续式根系分泌物收集方法主要包括土培收集法、溶液培养收集法及基质培收集法[17]。其中土培收集法是用蒸馏水洗下根际土壤后,通过离心或振动过滤从而获得根系分泌物,但不能完全排除土壤颗粒的影响[18-19]。溶液培养法是将根系放入超纯水中培养一段时间后,收集、浓缩、过滤培养液,用树脂分离营养离子[17]。其液体环境中根系通气性差,且不能准确反映自然条件下植物的生长情况。基质培养法是将植物培养在蛭石和琼脂中,然后将基质浸泡在蒸馏水或有机溶剂中以提取有机物,将得到的液体浓缩、过滤。该方法需要补充额外的营养液以保持基质营养和湿度水平。而现有的连续式根系分泌物收集培养系统一般选用石英砂为培养基质,在外连接收集器直接收集根系分泌物[20]。
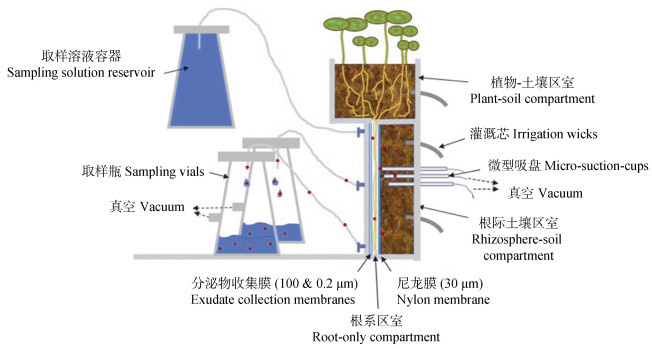
为尽量减少植物根系在收集过程中造成的干扰以及土壤颗粒的潜在影响,研究者已发明了一套用于收集根系分泌物的根箱系统[21]。该装置在植物-土壤隔室的底部有一个垂直缝隙,植物根系通过该缝隙向下伸展和生长,然后可使用真空采样系统以采样液冲洗根垫,实现原位收集根系分泌物(图 1)。Wei等[22]设计了一种非破坏性连续采样根箱装置,用于从单个番茄植株中收集根际土壤样品,他们以青枯病菌为主要病原菌,动态追踪单个番茄植株在多个生长阶段的根际微生物区系特征,这使得探索初始土壤微生物群落、微生物群落功能和植物病害发展之间的关系成为可能(图 2)。
|
注:该图根据已报道的根系分泌物收集方法[21]重新绘制,对原图的布局、配色和字体进行了统一修改。 Note: This figure was redrawn based on the reported methods for collecting root exudates[21], and made uniform modifications to the layout, color scheme, and font of the original image. 图 1 原位收集根系分泌物的根箱装置示意图 Fig. 1 Schematic diagram of the rhizobox device for in-situ collection of root exudates |

|
注:a)根箱由一个高度为136 mm、直径为110 mm的三层圆柱体组成。内层(根室)由50 μm尼龙网制成,可防止根进入中间层,外层由4 mm金属网制成,以支撑根茎盒。b)中间采样层由18个单独的尼龙网袋(150 μm尼龙网,高度136 mm,宽度18~21 mm,厚度1~2 mm)组成,其中包含均质灭菌的田间土壤。因此,中间层尼龙网袋中的土壤与植物根系和根系分泌物紧密接触,并被用作根际细菌群落的代理。该图根据Wei等[22]的成果重新绘制,对原图的布局、配色和字体进行了统一修改。 Note: a)The rhizobox consisted of a three-layer cylinder with a height of 136 mm and a diameter of 110 mm. The inner layer(root compartment)is made of a 50 μm nylon mesh net, which prevents roots from entering the middle layer, and the outer layer is made of a 4 mm metal mesh to support the rhizobox. b)The middle sampling layer consisted of 18 individual nylon mesh bags(150 μm nylon mesh; height, 136 mm; width, 18 to 21 mm; thickness, 1 to 2 mm)containing homogenized and sterilized field soil. The soil in the nylon mesh bags of the middle layer was thus in close contact with plant roots and root exudates and was used as a proxy of the rhizosphere bacterial community. This figure was redrawn based on the results of Wei et al. [22], and made uniform modifications to the layout, color scheme, and font of the original figure. 图 2 非破坏性收集根际土壤的根箱系统示意图 Fig. 2 Schematic diagram of the rhizobox system for non-destructive collection of rhizosphere soil |
然而,上述传统的实验方法和已有装置的土壤采集部分与根系分泌物收集部分相互独立,无法实现根际土壤和根系分泌物的匹配性收集,不能实时观察植物-微生物的相互作用,并且缺乏可视化和操控的能力。为解决上述问题,本研究设计了一种原位动态可视化精准收集根际土壤和根系分泌物的装置及其收集方法。新型装置较图 1装置可进行原位根际土壤的收集;较图 2根箱装置可进行原位动态根系分泌物的收集。近期对分泌物进行了收集和检测,并与已有方法和装置进行比较,结果发现利用本装置收集具有以下优点:根系分泌物在收集过程中对植物根系扰动小,采样回收率高,准确性高;可精确采集距根表面不同距离层次的根际土壤,准确、便捷;根系生长情况可直接观测。
该装置已经申请国家实用新型专利,专利授权号为ZL202322715004.5,下面加以详细介绍。
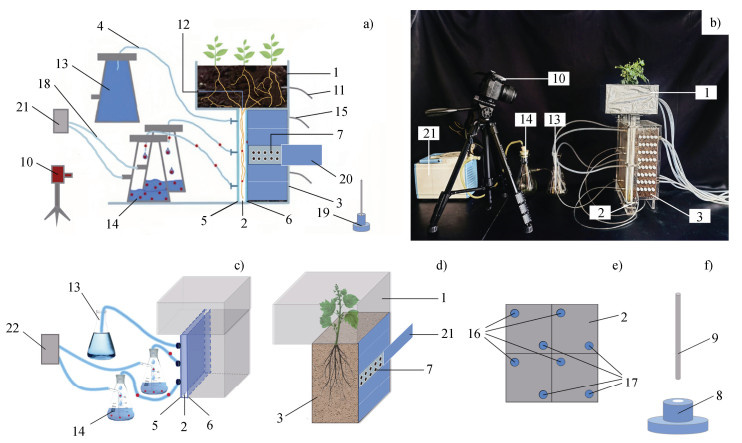
1 材料与方法 1.1 收集根际土壤和根系分泌物的装置一种收集根际土壤和根系分泌物的装置,如图 3a和图 3b所示,包括植物生长区室、根系生长区室、土壤区室、连通于所述根系生长区室的根系分泌物采样装置以及辅助土壤取样的取样管和辅助器。其中,植物生长区室1侧壁连接有第一灌溉管11,植物生长区室1底部并排设置有根系生长区室2和土壤区室3,植物生长区室1和根系生长区室2之间设置有狭缝12,土壤区室3远离根系生长区室2一侧安装有第二灌溉管15。如图 3c所示,根系生长区室2内壁设置有第一滤膜5(孔径:100 μm),以防止颗粒物或根毛等干扰物质进入和堵塞采样管路,根系生长区室2与土壤区室3之间设置有第二滤膜6(孔径:25 μm),根系生长区室2远离土壤区室3一侧安装根系分泌物采样装置18。如图 3e所示,根系生长区室2与根系分泌物采样装置18相连的外壁分为四个相同区域,每个区域上下对侧设置有接口,上侧的接口为淋洗液入口16,下侧的接口为淋洗液出口17,实现对根系分泌物的分区采样。如图 3d所示,土壤区室3前后壁均匀分布有若干取样孔7,取样孔7上安装有取样盖20,取样孔7分别与淋洗液入口16和淋洗液出口17并列设置,收集范围准确集中于同一区域根系及其所对应的土壤环境,确保分泌物和根际土壤匹配性收集。
|
注:1、植物生长区室;2、根系生长区室;3、土壤区室;4、连通管;5、第一滤膜;6、第二滤膜;7、取样孔;8、辅助手柄;9、取样管;10、实时拍摄设备;11、第一灌溉管;12、狭缝;13、储液瓶;14、采样瓶;15、第二灌溉管;16、淋洗液入口;17、淋洗液出口;18、根系分泌物采样装置;19、土壤取样装置;20、取样盖;21、真空泵。 Note: 1. Plant growth compartment, 2. Root growth compartment, 3. Soil compartment, 4. Connecting tubes, 5. First filter membrane, 6. Second filter membrane, 7. Sampling holes, 8. Auxiliary handles, 9. Sampling tubes, 10. Real-time imaging device, 11. The first irrigation pipe, 12. Slit, 13. Reservoir bottles, 14. Sampling bottles, 15. Second irrigation pipe, 16. Eluent inlet, 17. Eluent outlet, 18. Root exudates sampling device, 19. Soil sampling device, 20. Sampling caps, 21. Vacuum pump. 图 3 一种匹配性收集根际土壤和根系分泌物的装置的结构示意图(a)和实物图(b)、根系生长区室和根系分泌物采样装置示意图(c)、植物生长区室和土壤区室的示意图(d)、根系生长区室外壁右视图(e)和土壤取样装置的爆炸图(f) Fig. 3 Schematic diagram(a)and picture(b)of a device for coordinated collection of rhizosphere soil and root exudates, schematic diagram of the root growth compartment and root exudates sampling device(c), schematic diagram of the plant growth compartment, and soil compartment(d), right side view of the outdoor wall of the root growth compartment(e)and exploded diagram of soil sampling device(f) |
如图 3c所示,根系分泌物采样装置18包括真空泵21(GM-0,津腾,天津市津腾实验设备有限公司)、储液瓶13、采样瓶14和连通管4,真空泵21和采样瓶14管路连接,储液瓶13和淋洗液入口16采用连通管4连接,采样瓶14和淋洗液出口17采用连通管4连接,真空泵21由电磁开关和程序自动控制采样时长及间隔,减少了对植物根系的扰动,同时可进行连续取样;根系生长区室2的外壁为透明有机玻璃,根系生长区室2外设置有实时拍摄设备10;土壤区室3外侧设置有土壤取样装置19,如图 3f所示,土壤取样装置19包括取样管9和辅助手柄8,取样管9和辅助手柄8插拔连接。
植物生长区室1顶部为开口,第一灌溉管11和第二灌溉管15分别设置有多个;土壤区室3为可拆卸式,第二灌溉管15设置有两排,上下均匀分布;取样孔7在土壤区室3前后壁上分别设置有8行,每行取样孔7后设置有厘米刻度,代表不同层次的土壤深度,每行取样孔7设置有7个,分别距根系生长区室2一侧2 mm、7 mm处设有根际土样孔;15 mm、30 mm、45 mm、60 mm、75 mm处设有非根际土样孔,每个取样孔7上方设有毫米刻度,代表孔径中心距根系生长区室2的距离;取样管9管壁外设有毫米刻度,取样管9直径小于取样孔7孔径,根据插入深度估计收集土量。
1.2 工作原理使用时,首先在植物生长区室1和土壤区室3填装土壤,将植物种子或幼苗定植于植物生长区室1进行培养,期间,通过植物生长区室1侧壁上的第一灌溉管11为植物输送水分,提供原位生长环境。培养过程中,植物根系通过植物生长区室1底部的狭缝12进入根系生长区室2,在此区室进行根系分泌物的收集。根系生长区室2与土壤区室3之间夹设有第二滤膜6,土壤区室3装有土壤,由于第二滤膜6的阻挡作用,根系无法穿越第二滤膜6进入土壤,土壤颗粒也无法进入根系生长区室2影响根系分泌物的取样,而土壤中的养分和水分可透过第二滤膜6供植物根系利用。根系生长区室2的根系通过夹设于根系生长区室2与土壤区室3之间的第二滤膜6与土壤区室3进行水和溶质的交换,生长形成根垫,位于根系生长区室2外侧的拍摄设备10定时进行拍摄,实时记录根系生长状况及构型。
根系分泌物的收集在根系生长区室2中进行。收集根系分泌物时,由电磁开关和程序控制打开真空泵21开关,每间隔10 min采集根系分泌物一次,每次采样时间为2 min(采样间隔和时间不做要求,可根据实验需要调整)。储液瓶13中的去离子水通过连通管4进入根系生长区室2淋洗根系后,再通过第一滤膜5由连通管4抽入采样瓶14,实现根系分泌物的采样。
土壤样品的收集在土壤区室3中进行。收集非根际土壤时,根据实验需要选择某一深度层次的土壤,接着选择距根垫不同距离处的取样孔7,旋开对应取样孔7的取样盖20,通过辅助手柄8将取样管9垂直插入取样孔7采集土样,根据取样管9上刻度粗略估计收集土样量,之后取出取样管9,去皮称重,倒出土样。收集根际土壤时,可将土壤区室3取下,水平放置使内壁第二滤膜6面朝上,取下第二滤膜6,其上所附着的土壤厚度小于3 mm,为直接与根垫相接触的根际土壤,将土壤抖落,即为根际土壤样品;同时也可通过距离根垫2 mm及4 mm的取样孔7采集根际土壤,其方法与上述非根际土壤的采集方法相同。
1.3 土壤的准备与植物培育方法供试土壤取自河南大学金明校区,自然晾干后研磨,过2 mm标准筛。为了保证植物生长所需营养,实验初期可在土壤区室中预混肥料,后续养分不足可通过灌溉管添加营养液,实现可控的养分输入。栽培前采用60%最大田间持水量对基质进行为期7 d的水分平衡处理。土壤填充的操作流程如下:将土壤区室3取下,水平放置使内壁第二滤膜6面朝上,取下第二滤膜6,用小铁铲逐层填充土壤,每层填充后进行适度压实。组装完成的实验装置固定于定制化支架系统(具体组装流程见视频https://www.bilibili.com/video/BV1mFEHzqEgi/?share_source=copy_web&vd_source=95bc8aefe703cb2ae8343fee61be6678)。
供试小麦种子(品种:周麦26)经3%(w/w)过氧化氢溶液表面灭菌后,使用去离子水彻底冲洗,于珍珠岩基质中进行催芽处理。选择长势均一的健壮幼苗,分别移栽至植物生长区室及对照组盆栽中。已移植小麦幼苗的装置如图 4a所示。幼苗移栽后,自然光下培养,除地上部分外,所有地下装置组件均使用锡箔纸进行避光处理。

|
图 4 小麦生长与收集装置(a)、定时相机拍摄照片(b)和溶液收集法(c) Fig. 4 Growth of wheat in the experiment and collection device(a), timed camera taking photos(b), and solution collection method(c) |
本研究根系分泌物的收集分别用装置收集法和溶液收集法。
装置收集法:预处理阶段将所有收集容器经5%(v/v)硝酸溶液浸泡24 h,用三重去离子水清洗后风干备用。连接根系分泌物收集装置,在小麦灌浆期进行样本采集。每次采样前30 min使用含有微生物抑制剂的去离子水对系统进行预冲洗,冲洗液废弃处理,正式采集时段设定为10:00—16:00。
溶液收集法:在小麦灌浆期,将盆栽中小麦植株完整挖出,剥离根际土壤后使用去离子水充分冲洗根系表面残留物。随后将洁净根系垂直置于250 mL酸洗处理过的烧杯中,注入200 mL去离子水(液面高度低于根茎结合部2 cm),烧杯外壁包裹遮光锡箔纸以避免光干扰,如图 4c所示。收集时段与装置法同步(10:00—16:00),其间保持静态浸提。
将收集到的根系分泌物用C18固相萃取小柱萃取后,用6 mL乙腈洗脱。使用Termovap样品浓缩器将萃取后的根系分泌物浓缩,浓缩后样品过0.22 μm有机膜后装入2 mL棕色进样瓶,置于–20 ℃冰箱中待测。使用高效液相色谱分析仪(Agilent InfinityLab LC系统1260 Infinity Ⅱ,Agilent公司,美国)测定根系分泌物中槲皮素含量,色谱柱为ZORBAX Eclipse Plus C18色谱柱(4.6 mm× 250 mm,5 μm,美国Agilent公司)。流动相:A为0.4%(v/v)磷酸溶液,B为甲醇,梯度洗脱程序为0~10 min,A/B48:52(v/v);10~25 min,A/B65:35(v/v)。流速:1.0 mL·min–1;检测波长:210 nm。以槲皮素为标准品制得标准曲线,计算根系分泌物中槲皮素的含量[23]。
为增强数据可靠性,本研究以大豆为试验材料进行了补充试验,品种为“安豆6263”,分别采用上述两种方法收集根系分泌物,并测定其中大豆苷元的含量。色谱分析条件如下:流动相A为pH 3的磷酸溶液,B为乙腈,梯度洗脱程序(均为体积分数)为:0 min,5% B;0~25 min,B线性升至55%;25~28 min,B由55%快速升至100%;28~29 min内B降至5%;29~31 min,系统平衡。总运行时间为31 min。流速:1.5 mLŸmin–1;检测波长:236 nm。以大豆苷元为标准品制得标准曲线,计算根系分泌物中大豆苷元的含量[24]。
2 结果与讨论 2.1 装置的高效性与准确性本装置在根系分泌物回收效率方面与传统方法(如溶液收集法)具有可比性,可通过小麦和大豆两种作物根系分泌物的检测结果综合验证。如表 1所示,采用本研究装置收集法获得的小麦根系分泌物中槲皮素含量为0.011 28 mg,低于溶液收集法的平均值0.015 97 mg;而在大豆实验中(表 2),装置收集法测定值为0.001 75 mg,与溶液收集法(0.001 64 mg)接近(略高)。
|
|
表 1 不同收集方法中小麦灌浆期根系分泌物中槲皮素的含量 Table 1 Quercetin content in root exudates of wheat at the grain-filling stage collected by different methods |
|
|
表 2 不同收集方法中大豆子叶期根系分泌物中大豆苷元的含量 Table 2 Daidzein content in root exudates of soybean at the cotyledon stage collected by different methods |
装置收集法所测小麦根系分泌物中槲皮素含量偏低,其原因可能包括:首先,溶液收集法将根系离体并置于无菌环境中,分泌物免受土壤微生物降解;而本装置作为一种原位土壤培养方法,根系分泌物在释放后即暴露于包含根际微生物的复杂环境。尽管物理隔离与即时淋洗尽可能降低微生物干扰,但根表附着的微生物对槲皮素的快速利用与降解可能是导致其回收量低于离体溶液收集法的主要原因之一[21]。其次,槲皮素作为酚酸类物质,相较于大豆苷元,可能更易被根表或根际土壤颗粒吸附;此外,小麦根系发达、根毛密布,形成的致密根垫可能在一定程度上阻碍了淋洗液均匀、充分地接触根表,从而降低洗脱效率。相比之下,大豆苷元疏水性较弱,且大豆根系表面蜡质层较厚、根毛稀疏,更利于淋洗,因此装置法与溶液法测定结果较为一致。
综上所述,尽管装置法在测定特定分泌物绝对量时可能存在一定局限,但并不否定装置的价值,反而强调了其在反映真实根际过程方面的独特优势:本装置不破坏根系与土壤间的自然生长状况,也避免传统方法中因频繁取样或根系暴露导致的机械损伤,保证植物根系的完整性,反映了植物在接近自然生长状态下的分泌物释放特征,从而提升了试验数据的准确性。此外,本装置通过优化设计显著简化了操作步骤,实现了更高效率的样本采集。一方面装置收集法避免了传统土培法中根系剥离、反复冲洗等繁琐操作;另一方面,传统非连续式方法(如溶液收集法)需在不同生长阶段进行破坏性取样,单株植物仅能获取单一时段数据。本装置实现了对同一植株分泌物连续、动态的采集,且采样间隔与时长可根据试验需求灵活调整,显著提升了单株植物的研究效率,尤其适用于植物-微生物互作机制的长期动态解析。
2.2 装置的双向性本装置是一种收集根际土壤和根系分泌物的双向装置,在根系分泌物试验领域开辟了全新赛道。装置包括植物生长区室,所述植物生长区室侧壁连接有第一灌溉管,为植物根系生长提供水分;植物生长区室底部并排设置有根系生长区室和土壤区室,植物生长区室和根系生长区室之间设置有狭缝,供根系延伸进入根系生长区室;根系生长区室内壁设置有第一滤膜,可有效减少土壤颗粒对根系分泌物收集的干扰;根系生长区室与土壤区室之间设置有第二滤膜,用于阻隔根毛、颗粒物等杂质进入采样管路,防止堵塞;还包括在根系生长区室远离土壤区室一侧安装的根系分泌物采样装置,实现样品高效收集。
据调查,现仅有一种实验装置可集成根际土壤样品和根系分泌物的双收集,但现有装置具有相应的局限性,其根系分泌物收集在收集箱石英砂介质中进行,由于受材料吸附的影响,回收率较低;其土壤采集部分与根系分泌物收集部分相互独立,无法实现根际土壤和根系分泌物的匹配性收集;且根系生长在箱体内部,难以观测根系的生长状态[25]。而本装置是一种收集根际土壤和根系分泌物的新型装置,将根系分泌物和根际土壤收集技术巧妙结合,可实现二者的原位双收集,且收集范围可准确集中于同一区域的根系及其所在土壤环境,确保分泌物和根际土壤匹配性收集。
2.3 装置抗土壤干扰性现有根系分泌物收集技术种类多样,例如水培收集、基质培养收集及土培收集等[17],但均存在一定的缺陷(表 3)。水培收集将根系浸泡于溶液中易导致其通气不良而影响根系生长,且缺少根际微生物释放的信号分子反馈作用[26];基质培养收集的基质环境与原位根际环境存在差异,需要另外添加营养液来维持养分和湿度[27];传统土培收集难以排除土壤自身成分,使得收集到的分泌物与真实根系分泌物有很大出入[27],且目前几乎没有土培装置可在准确收集根系分泌物的同时实现对根系土壤样品的取样,以更加全面地研究和理解植物根系-土壤微环境。
|
|
表 3 根系分泌物和根际土壤不同收集方法的比较 Table 3 Comparison of different collection methods of root exudates and rhizosphere soil |
本装置可很好地减少土壤对根系分泌物收集造成的干扰,将植物种子或幼苗定植于植物生长区室中,根系通过区室底部狭缝进入根系生长区室,根系生长区室与土壤区室之间隔有第二滤膜,通过尼龙膜精确区分根/土界面,保持根系正常生长环境,由于滤膜的阻挡作用,土壤微粒无法穿越滤膜进入根系区室,而土壤中的养分和水分可透过滤膜供植物根系利用,从而减少了土壤对根系分泌物收集造成的干扰。尽管根系未完全生长于土壤中,但25 μm第二滤膜设计,其孔径显著大于先前研究中使用的膜(如0.65 μm、0.2 μm),确保了分泌物扩散效率。且植物生长区室的设计允许根-土直接接触,进一步保障了生态真实性[28]。植物生长区室和土壤区室连通有灌溉管,为植物根系生长提供水分。根系生长区室外壁为有机玻璃板,其内紧贴有尼龙滤膜,以防止颗粒物或根毛等干扰物质进入和堵塞采样管路。
2.4 装置的连续性与可控性本装置设计巧妙,其根系分泌物采样装置配有真空泵,能够实现对采样时间和间隔的控制,对植物根系扰动小,采样效率高;在根系分泌物收集过程中,由电磁开关和程序控制打开真空泵开关,每间隔10 min采样一次,单次采样时间为2 min(采样间隔和时间可根据试验需要调整)。储液瓶中的淋洗液通过连通管进入根系生长区室淋洗根系后,再通过连通管抽入采样瓶,实现根系分泌物的采样。
2.5 装置的精准定位性对于根际土样的收集,目前多采用田间人工抖土法[29],这种方法快捷简单,但带有强烈的随机性和粗糙性,且仅能用于研究根际和非根际土壤之间的差异[30],不能研究距根表面不同距离和层次的土壤特性,无法精确区分根/土界面。本装置根系生长区室外壁为有机玻璃板,玻璃板上分布有多个接口,通过连通管分别与储液瓶和采样瓶相连,以实现对根系分泌物的分区采样;采集土壤样品时,根据试验需要选择某一深度层次的土壤,接着选择距根系不同距离处的取样孔[28],将取样管垂直插入采集土样,根据取样管上刻度粗略估计收集土样的量,之后取出取样管,去皮称重,倒出土样。实现距根表面不同距离、不同层次土壤的分层精确采集。
2.6 动态监测装置根系生长区室外侧设有可定时拍摄的设备,实现根系生长状况及构型可视化动态监测,该装置外围设置有挡光壁,以避免光照对植物根系生长的影响,取下后可直接观测根系生长状态,实现动态观测。整体而言,植物根系无损伤原位监测法操作简便,能够快速实现植物根系的长期原位无损伤动态监测,并可同步完成根系分泌物中特定成分的连续收集。
2.7 局限性与应用场景当前设计虽实现了根际土壤与分泌物的原位匹配收集,但其制造成本集中于真空泵、滤膜组件及精密加工的多区室结构,且尼龙滤膜需定期更换以维持性能,导致维护费用较高。未来可通过开发低成本复合材料替代现有滤膜,合并灌溉与采样管路以简化结构,引入3D打印技术实现复杂内部结构的一体化制造,从而降低成本。技术拓展方面,尽管现有系统支持分泌物的动态收集,但化学分析仍依赖离线检测;未来结合拉曼光谱技术有望实现分泌物成分的实时在线分析,进一步提升研究效率。在适用性上,本装置适用于生长周期短、根系分布集中的草本植物(如小麦、拟南芥)及旱作作物,其狭缝设计可引导根系进入生长区室,实现整个生长周期的动态监测,但对木本植物或深根系物种需调整区室尺寸与灌溉模式。土壤类型方面,装置对砂质土或壤土适配性较好,而高黏土可能因颗粒堵塞滤膜影响养分交换。
2.8 不同收集方法的优缺点通过对比分析现有的根系分泌物和根际土壤的主要收集方法,本文总结了各自的优缺点(表 3)。
3 结论本装置创新性地集成了植物生长、根系分泌物收集与根际土壤分层与梯度距离采样功能于一体,通过巧妙设计实现了对植物根系分泌物和根际土壤的精准、原位、连续及动态收集。装置中的真空泵采样系统能够智能控制采样时长与间隔,最小化对植物根系的干扰,同时确保根系分泌物样本的高效收集。结合尼龙滤膜与尼龙膜的精准分隔技术,不仅有效维护了根系的正常生长环境,还实现了根/土界面的清晰界定。此外,土壤区室的灵活可拆卸结构及精确标定的取样孔,支持对不同层次、不同距离根表面的根际土壤进行高精度取样。综上所述,该装置以其全面的功能、高效的采样能力及精准的控制机制,为植物生理生态学研究领域提供了强有力的工具,有助于推动根际土壤与根系分泌物研究的深入发展。
| [1] |
He Y, Lin H, Yu G, et al. Spatio-temporal characteristics of O2 in rhizosphere of hyperaccumulator Leersia hexandra Swartz under chromium stress (In Chinese)[J]. Soils, 2022, 54(5): 1024-1031. [贺瑶, 林华, 俞果, 等. 铬处理下超富集植物李氏禾根际溶解氧时空分布特征[J]. 土壤, 2022, 54(5): 1024-1031.]
(  0) 0) |
| [2] |
Ling N, Wang T T, Kuzyakov Y. Rhizosphere bacteriome structure and functions[J]. Nature Communications, 2022, 13(1): 836. DOI:10.1038/s41467-022-28448-9
(  0) 0) |
| [3] |
Yang X H, Wang L Y, Li H X, et al. Effects of root exudates from buckwheat and sorghum on the root border cellsand root growth of maize (In Chinese)[J]. Acta Ecologica Sinica, 2023, 43(9): 3778-3788. [杨小环, 王立印, 李宏鑫, 等. 荞麦、高粱根系分泌物对玉米根边缘细胞和根生长的影响[J]. 生态学报, 2023, 43(9): 3778-3788.]
(  0) 0) |
| [4] |
You C, Yang T J, Zhou X G, et al. Research advances on mechanisms and preventions of soil-borne diseases exacerbated by root exudates in continuous cropping systems (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(5): 1201-1211. DOI:10.11766/trxb202307180281 [游川, 杨天杰, 周新刚, 等. 连作根系分泌物加剧土传病害的机制和缓解措施研究进展[J]. 土壤学报, 2024, 61(5): 1201-1211.]
(  0) 0) |
| [5] |
Ding A F. Introduction and application about a novel tool for sampling plant root exudates (In Chinese)[J]. Chinese Journal of Soil Science, 2016, 47(3): 746-750. [丁爱芳. 新型根系分泌物采样装置的介绍与应用[J]. 土壤通报, 2016, 47(3): 746-750.]
(  0) 0) |
| [6] |
Meng T T. Effects of rhizosphere/endophytic microbial communities and growth-promoting microorganisms on host growth and metabolism of Codonopsis pilosula[D]. Lanzhou: Lanzhou University of Technology, 2023.[孟彤彤. 党参根际/内生微生物群落及促生微生物对宿主生长代谢的影响[D]. 兰州: 兰州理工大学, 2023.]
(  0) 0) |
| [7] |
Niu S Q. Physiological research on growth promotingrhizobacteria from Haloxylon ammodendron regulating perennial ryegrass growth and stress tolerance[D]. Lanzhou: Lanzhou University, 2017.[牛舒琪. 梭梭根际促生细菌调控黑麦草生长和抗逆性的生理研究[D]. 兰州: 兰州大学, 2017.]
(  0) 0) |
| [8] |
Liu Y X, Li X, Cai L T, et al. Identification of phenolic acid in tobacco root exudates and their role in the growth of rhizosphere microorganisms (In Chinese)[J]. Plant Nutrition and Fertilizer Science, 2016, 22(2): 418-428. [刘艳霞, 李想, 蔡刘体, 等. 烟草根系分泌物酚酸类物质的鉴定及其对根际微生物的影响[J]. 植物营养与肥料学报, 2016, 22(2): 418-428.]
(  0) 0) |
| [9] |
Baidullah N, Bratibai E. Research progress on the relationship between plant rhizosphere microorganisms and crop growth and development (In Chinese)[J]. Seed Science and Technology, 2023, 41(22): 142-144. [努兰·拜都拉, 恩特马克·布拉提白. 植物根际微生物与农作物生长发育之间关系的研究进展[J]. 种子科技, 2023, 41(22): 142-144.]
(  0) 0) |
| [10] |
Pu Z T, Wang F, Li C, et al. Research progress of arbuscular mycorrhizal fungi affecting plant nitrogen absorption and transport (In Chinese)[J]. Journal of Agricultural Science and Technology, 2024, 26(11): 171-179. [蒲子天, 王菲, 李畅, 等. 丛枝菌根真菌影响植物氮素吸收和转运的研究进展[J]. 中国农业科技导报, 2024, 26(11): 171-179.]
(  0) 0) |
| [11] |
Zhu J N, Bi Y, Zhang Y, et al. Effects of HH103 effector NopT of rhizobium on nodule fixation and symbiotic early defense response of soybean (In Chinese)[J]. Biotechnology, 2024, 34(4): 517-524. [朱加楠, 毕宇, 张悦, 等. 根瘤菌HH103效应子NopT影响大豆结瘤固氮及共生早期防御反应[J]. 生物技术, 2024, 34(4): 517-524.]
(  0) 0) |
| [12] |
Shi X Y, Zhao Y G, Xu M W, et al. Insights into plant–microbe interactions in the rhizosphere to promote sustainable agriculture in the new crops era[J]. New Crops, 2024, 1: 100004. DOI:10.1016/j.ncrops.2023.11.002
(  0) 0) |
| [13] |
Hu L F, Robert C A M, Cadot S, et al. Root exudate metabolites drive plant-soil feedbacks on growth and defense by shaping the rhizosphere microbiota[J]. Nature Communications, 2018, 9(1): 2738. DOI:10.1038/s41467-018-05122-7
(  0) 0) |
| [14] |
Naz M, Afzal M R, Raza M A, et al. The significant effects of strigolactones on plant growth and microbe interactions: A review[J]. Plant Growth Regulation, 2025, 105(4): 937-957. DOI:10.1007/s10725-025-01325-3
(  0) 0) |
| [15] |
Wang P Q, Wu Y L, Li Y F, et al. Research and prospects of plant root exudates and micro-environment (In Chinese)[J]. Rural Science and Technology, 2021, 12(27): 96-98. [王朋强, 吴义兰, 李永富, 等. 植物根系分泌物及微域环境的研究与展望[J]. 乡村科技, 2021, 12(27): 96-98.]
(  0) 0) |
| [16] |
Li Y L, He H P, Liu J, et al. Analysis of organic acid components in root exudates and their effects on soil nutrients and enzyme activities (In Chinese)[J]. Northern Horticulture, 2024(12): 73-79. [李彦林, 贺怀鹏, 刘菁, 等. 不同根系分泌有机酸组分分析及其对土壤养分、酶活性的影响[J]. 北方园艺, 2024(12): 73-79.]
(  0) 0) |
| [17] |
Guo W J, Zhang Z L, Liu Q, et al. Research progress of root exudates collection technology (In Chinese)[J]. Chinese Journal of Applied Ecology, 2019, 30(11): 3951-3962. [郭婉玑, 张子良, 刘庆, 等. 根系分泌物收集技术研究进展[J]. 应用生态学报, 2019, 30(11): 3951-3962.]
(  0) 0) |
| [18] |
Chen Q B, Peng L X, He L M, et al. Allelopathic substances in root and rhizosphere-soil of eucalyptus 12ABL (In Chinese)[J]. Chinese Journal of Tropical Agriculture, 2002(4): 28-34. [陈秋波, 彭黎旭, 贺利民, 等. 刚果12号桉树根及根际土壤中化感物质的成分分析[J]. 热带农业科学, 2002(4): 28-34.]
(  0) 0) |
| [19] |
Hartmann A, Rothballer M, Schmid M. Lorenz Hiltner, a pioneer in rhizosphere microbial ecology and soil bacteriology research[J]. Plant and Soil, 2008, 312(1/2): 7-14.
(  0) 0) |
| [20] |
Tang C S, Young C C. Collection and identification of allelopathic compounds from the undisturbed root system of bigalta limpograss(Hemarthria altissima)[J]. Plant Physiology, 1982, 69(1): 155-160. DOI:10.1104/pp.69.1.155
(  0) 0) |
| [21] |
Oburger E, Dell'mour M, Hann S, et al. Evaluation of a novel tool for sampling root exudates from soil-grown plants compared to conventional techniques[J]. Environmental and Experimental Botany, 2013, 87: 235-247. DOI:10.1016/j.envexpbot.2012.11.007
(  0) 0) |
| [22] |
Wei Z, Gu Y A, Friman V P, et al. Initial soil microbiome composition and functioning predetermine future plant health[J]. Science Advances, 2019, 5(9): eaaw0759. DOI:10.1126/sciadv.aaw0759
(  0) 0) |
| [23] |
Zhang Z Y. Effects of insect herbivory on mycorrhizal fungi colonization and root-associated microbial community in common ragweed(Ambrosia artemisiifolia)[D]. Kaifeng, Henan: Henan University, 2022.[张钟月. 昆虫取食对豚草菌根真菌定殖及根系微生物群落的影响[D]. 河南开封: 河南大学, 2022.]
(  0) 0) |
| [24] |
Graham T L. Flavonoid and isoflavonoid distribution in developing soybean seedling tissues and in seed and root exudates[J]. Plant Physiology, 1991, 95(2): 594-603. DOI:10.1104/pp.95.2.594
(  0) 0) |
| [25] |
Liao J P, Lin X G, Cao Z H, et al. A new system for continuous trapping of root exudate (In Chinese)[J]. Soils, 2003, 35(4): 311-313. [廖继佩, 林先贵, 曹志洪, 等. 一种新型连续根分泌物收集装置[J]. 土壤, 2003, 35(4): 311-313.]
(  0) 0) |
| [26] |
Ma W M, Tang S H, Dengzeng Z M, et al. Root exudates contribute to belowground ecosystem hotspots: A review[J]. Frontiers in Microbiology, 2022, 13: 937940. DOI:10.3389/fmicb.2022.937940
(  0) 0) |
| [27] |
Luo Y, Chen Y, Ding N, et al. Research progress on the composition, release mechanism and collection technology of plant root exudates (In Chinese)[J]. Rural Science and Technology, 2023, 14(1): 127-131. [罗阳, 陈原, 丁娜, 等. 植物根系分泌物组成、释放机制和收集技术研究进展[J]. 乡村科技, 2023, 14(1): 127-131.]
(  0) 0) |
| [28] |
Wenzel W W, Wieshammer G, Fitz W J, et al. Novel rhizobox design to assess rhizosphere characteristics at high spatial resolution[J]. Plant and Soil, 2001, 237(1): 37-45. DOI:10.1023/A:1013395122730
(  0) 0) |
| [29] |
Han C H, Zhang H Y, Zhao L, et al. Effects of sorbitol-chelated potassium through foliar spraying on wheat yield, potassium availability, and rhizosphere microbiome (In Chinese)[J]. Soils, 2025, 57(2): 290-299. [韩传浩, 张欢洋, 赵立, 等. 叶面喷施山梨醇螯合钾对小麦产量、钾利用率及根际土壤微生物群落的影响[J]. 土壤, 2025, 57(2): 290-299.]
(  0) 0) |
| [30] |
Li Y, Wang Y, Xiong Z Y, et al. Effect of manure with biomass carbon on forms of nutrients and nitrogen in rhizosphere / non-rhizosphere soils (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(2): 495-505. DOI:10.11766/trxb202206200331 [李越, 王颖, 熊子怡, 等. 有机肥配施生物质炭对根际/非根际土壤氮赋存形态的影响[J]. 土壤学报, 2024, 61(2): 495-505.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


