土壤中约含2 344 Pg的有机碳,是地球碳库的重要组成部分,与土壤健康、粮食安全、全球气候变化等息息相关[1]。众多研究针对土壤有机碳(Soil organic carbon,SOC)的结构组成、分布规律以及周转机制进行了深入探索。已有研究证明,铁在SOC固定过程中发挥关键作用,是土壤矿物碳泵(Mineral carbon pump,MnCP)中的重要组成部分,其可以通过吸附、络合和共沉淀等途径固持土壤有机碳,并通过“续埋”效应与微生物碳泵(Microbial carbon pump,MCP)共同发挥作用[2-4]。据估算,全球表层(0~30cm)土壤中铁结合态有机碳(Iron associated organic carbon,FeOC)储量为233 Pg C,占土壤表层总有机碳储量的33%±15%[5]。FeOC与SOC和矿物结合态有机碳(Mineral associated organic carbon,MAOC)呈显著正相关,表明铁氧化物在SOC的积累和保护中发挥着重要作用。然而,有研究指出,FeOC的稳定性受环境因素的影响。在铁的氧化还原循环中,部分有机碳在氧化铁的还原溶解过程中被释放,并经微生物代谢及芬顿反应进一步分解和矿化[6]。此外,有机碳分子与铁氧化物之间的相互作用对铁的形态转化过程有着显著影响。土壤有机碳的存在不仅影响铁的结晶和老化速率,也改变了新生铁氧化物的反应活性及其对有机碳的固持能力[7]。以上研究结果均说明铁碳循环过程的紧密耦合。2015年《联合国气候变化框架公约》第21次缔约方大会通过《巴黎协定》,法国农业部提出“千分之四全球土壤增碳计划”后,铁碳研究工作逐渐向碳汇和碳排放等气候变化关键问题侧重。因此,深入探究铁氧化物在土壤有机碳库动态变化中的核心作用具有重要意义,可为土壤健康管理和碳固持提供科学依据,进而为农业固碳减排策略的制定提供理论支持。
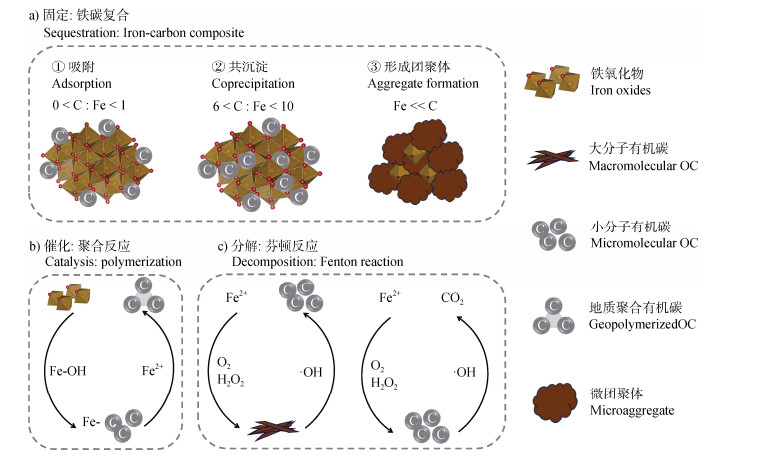
1 铁氧化物对土壤碳组分周转的影响作为土壤中重要的活性矿物,铁氧化物在碳周转过程中扮演着多种角色[8-9]。一方面,铁氧化物通过吸附固定以及催化聚合等过程增强土壤碳库的稳定性。另一方面,铁诱导的芬顿反应又会加快土壤有机碳的周转(图 1)。
|
注:大分子有机碳代表纤维素、木质素等性质较为稳定、分子量较高的自然有机碳。地质聚合有机碳代表小分子有机碳经非生物催化聚合形成的高分子量有机碳。 Note:macromolecular organic carbon refers to organic carbon with relatively stable properties and high molecular weight,such as cellulose and lignin. Geopolymerized organic carbon represents high-molecular-weight organic carbon formed by abiotic catalytic polymerization of small-molecular-weight organic carbon. 图 1 土壤铁对有机碳分子的固定、催化和分解作用 Fig. 1 Sequestration, catalysis and decomposition of organic carbon by iron in soils |
土壤铁氧化物通过静电作用、配体交换、表面络合作用、疏水作用、氢键作用以及阳离子桥联作用等方式与有机碳结合[10]。通过吸附、共沉淀、形成团聚结构等途径,形成较为稳定的FeOC,促进土壤有机碳库的积累(图 1a)。具体的结合机制随碳铁摩尔比(C︰Fe)发生变化:当C︰Fe达到1时,吸附作用发挥主要作用;C︰Fe达到6~10时,共沉淀作用成为主导[11-12]。一般情况下,通过共沉淀机制形成的FeOC性质更为稳定,对于土壤和沉积物中有机碳的积累具有重要意义[13-14]。Gao等[15]研究发现,相较于吸附态的针铁矿-葡萄糖复合物,共沉淀态的铁碳复合物添加进土壤后,葡萄糖的平均驻留时间增加10.8倍,其衍生的CO2释放量降低16.7%。此外,C︰Fe较高时,铁氧化物同时发挥物理胶结和化学吸附作用,促进土壤微团聚体(> 250 μm)的形成,维持土壤有机碳的长期稳定[16-17]。
铁氧化物自身性质也影响其与有机分子的结合能力。有研究发现,厌氧条件下铁碳复合物的稳定性取决于铁氧化物的结晶度,而非铁碳结合机制(吸附、共沉淀)[18]。结晶度较低的铁氧化物(如水铁矿)具有较大的比表面积,且表面的羟基结合位点较多,反应活性较高,更有利于有机碳的附着。但这类铁氧化物稳定性较差,形成的FeOC易受还原溶解影响。然而,结晶度较高的铁氧化物(如赤铁矿)比表面积和表面羟基数量相对较低,能够负载的有机碳数量相对较少,但形成的FeOC稳定性较高,能够持久固持有机碳[19-20]。Duan等[21]研究发现,与2线水铁矿(结晶度偏低)-葡萄糖复合物相比,6线水铁矿(结晶度偏高)-葡萄糖复合物添加进土壤后,葡萄糖的碳矿化降低29%,固碳效率提高51%。同时,铁氧化物的表面缺陷以及同晶替代均会影响其与有机碳的结合能力,这主要归因于矿物的表面缺陷会增加吸附位点,而同晶替代改变了铁氧化物的表面形态和氧化还原电位,从而影响其吸附能力[22]。有研究利用X射线光电子能谱和原子力显微镜表征发现,当水铁矿的铝取代率达到10%时,其表面羟基的相对比例增加9.46%,氧空位增加9.70%,使水铁矿与腐殖酸的结合力增加约100 pN[23]。
由于有机碳的官能团种类以及分子量大小存在差异,铁氧化物对有机碳的固持具有选择性[24]。动态吸附实验表明,铁氧化物表面优先吸附芳香族溶解性有机碳(DOC),随后疏水性更强、分子量较小(< 400 Da)的非芳香族组分通过有机-有机相互作用进一步富集[25]。随着有机碳固定量的增加,部分有机碳的结合强度可能会因静电排斥和/或空间位阻而降低,但总体而言,有机碳羧基数量的增加可显著提高铁碳复合物的结构稳定性[26]。基于有机碳在矿物表面的斑块分布形式,有学者认为亲和度较高的有机碳吸附在铁氧化物表面后,再吸附的有机碳会通过疏水作用堆叠在已有碳分子的外表面形成多层吸附,从而导致铁碳相互作用以及有机碳分子之间的相互作用同时存在[27]。有研究通过碳同位素标记结合纳米二次离子质谱技术(NanoSIMS),发现外源有机碳腐解产生的新碳更多地附着在与金属氧化物表面结合的有机碳上[28]。这表明有机-有机相互作用驱动外源碳在土壤中积累,而非单独通过矿物和有机碳的直接接触。
1.1.2 铁氧化物催化的有机碳聚合反应铁氧化物在有机碳聚合过程中发挥重要作用(图 1b)[29-30]。一方面,铁氧化物可以提供反应界面,提高局部区域中有机分子浓度。另一方面,铁可以充当催化剂,加快有机分子的聚合速率。该过程中,铁氧化物主要通过加速有机分子中羧基和氨基的聚合而促进有机碳的腐殖化过程,也被称为美拉德反应(Maillard reaction)[31-32]。此外,铁氧化物还参与多酚类化合物的缩合反应,进一步影响有机碳的转化过程。
美拉德反应作为地质聚合的关键途径,可以将还原糖和游离氨基酸聚合成复合芳烃,形成具有N-取代环、羰基、羧基和氨基官能团的芳香聚合物[33]。近期研究发现,铁锰氧化物通过离子桥键以及吸附聚集等作用,增加美拉德反应前体物质——席夫碱的产生,从而大幅提升有机碳的聚合效率。与无催化剂条件相比,铁锰氧化物的催化作用可将聚合反应速率提升两个数量级,且孔隙水模型估算结果显示铁锰催化有机碳聚合每年可为海洋沉积物贡献约4.1 Tg C[34]。这一量化结果不仅凸显了金属氧化物及其溶解态离子在非生物有机聚合中的重要性,也表明以往研究低估了其对全球碳循环的贡献。
在土壤和沉积物中,多酚作为另一类重要的有机前体,在金属氧化物催化下氧化产生半醌自由基和羧酸,进而通过缩聚反应逐渐形成腐殖质[35]。然而,在自然腐殖化过程中,美拉德反应作为关键的非生物催化途径,与多酚氧化聚合过程共同驱动腐殖质的形成。研究表明,在铁氧化物催化下,葡萄糖、甘氨酸、儿茶酚能发生缩合反应。其中,甘氨酸和儿茶酚同时存在时,腐殖酸的生成量最高,表明两者存在协同效应;而添加葡萄糖后,这种缩聚反应受到干扰,导致产物中脂肪族结构的比例显著增加[36]。这些发现表明美拉德反应和多酚途径之间存在复杂交互作用,因此,将多酚和美拉德反应连接成一个综合腐殖化途径,有助于进一步理解土壤和沉积物中的自然腐殖化过程。
1.2 铁介导的芬顿/类芬顿反应促进有机碳转化土壤铁的氧化还原过程会驱动土壤有机碳的周转[37]。一方面,铁氧化还原过程伴随着铁碳解耦,使原本负载在铁氧化物表面的有机碳释放,提高土壤有机碳的生物有效性。另一方面,活性铁介导的芬顿及类芬顿反应促进有机碳的非生物矿化过程,加速有机碳的分解(图 1c)[6]。
芬顿和类芬顿反应在铁氧化还原过程中广泛发生,是引起土壤有机碳分解的主要原因之一[38]。土壤中累积的过氧化氢与Fe(Ⅱ)发生反应,产生活性较高的自由基,进而将有机碳氧化为CO2。在芬顿反应中,过氧化氢主要生成羟基自由基(HO•),其反应速率在pH接近3时最高;而类芬顿反应则生成多种自由基,如过氧自由基(HO2•)和超氧阴离子(O2•−)等,并且这种反应可以在pH 2~10范围内发生[39]。在芬顿/类芬顿反应体系中,Fe(Ⅱ)的生成是主要的限速步骤。在氧化还原频繁发生的潮湿土壤和沉积物中(稻田、湿地等),铁氧化物长期维持低结晶度,易还原溶解提供大量Fe(Ⅱ),在自由基生成过程中发挥重要作用,从而促进芬顿和类芬顿反应的持续发生。Chen等[40]通过模拟水稻土的氧化还原波动发现,经过5次氧化还原循环,HO•介导的氧化反应导致SOC矿化损失显著增加,贡献了总CO2排放的15.1%~30.8%,而仅5.2%~7.1%的SOC被铁氧化物稳定。
铁介导的芬顿反应不仅能加速SOC矿化,还能有效降解木质素、纤维素等难降解的大分子有机物,促进外源有机碳向土壤碳库转化[41]。这种降解作用在植物残体富集的区域尤为显著。由于这些区域底物(如植物残体)的可用性高,为芬顿反应提供了充足的反应物,从而形成了反应活性远高于周围土壤的“热区”。研究发现,在紧邻秸秆(0~3 mm)的土壤微域内,Fe(Ⅱ)、H2O2和HO•浓度分别较远离秸秆的土壤高2.1倍~3.0倍、3.0倍~9.0倍和2.6倍~2.8倍[42]。然而,铁诱导的芬顿反应对有机碳的影响并非单一的分解矿化。研究进一步发现,在破坏木质素、纤维素稳定结构的同时,该过程还能促进醌酚循环的电子传递过程,促进土壤腐殖质的形成[43]。例如,堆肥过程中外源添加硫酸铁能够促进腐殖质中羧酸和羰基化合物的形成,提高有机物料的腐殖化程度。与对照组相比,添加硫酸铁处理组的腐殖化程度提高了24.72%,腐殖质含量提升10%[44]。综上所述,土壤铁氧化还原过程一方面通过诱导自由基的产生促进有机碳分解,导致土壤有机碳库损失;另一方面通过促进醌酚循环的电子传递过程,从而有助于难降解的外源有机碳向土壤腐殖质转化,提升土壤碳库的储量和稳定性。
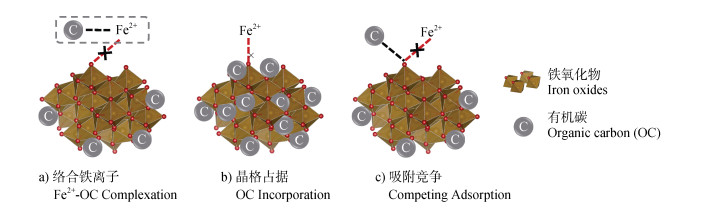
2 有机碳介导的铁氧化物转化过程铁碳结合不仅影响有机碳的固持和分解,还会改变铁氧化物的形态转化过程。研究表明,土壤有机碳通过干扰铁氧化物的聚合和结晶,抑制晶型铁氧化物的形成[7]。这一抑制效应主要归结为两方面原因:一是有机碳抑制Fe(Ⅱ)离子与铁矿物之间的电子传递;二是有机碳阻碍铁矿物结构中Fe(Ⅱ)的释放[45-46]。在土壤环境中,有机碳主要通过络合Fe(Ⅱ)、晶格占据与吸附竞争3种方式阻碍铁氧化物的原子交换和电子传递过程(图 2)。首先,有机碳络合Fe(Ⅱ)形成铁碳复合物,降低土壤溶液中Fe(Ⅱ)离子浓度。其次,有机碳占据铁氧化物的晶格和孔隙,阻碍Fe(Ⅱ)离子接触铁氧化物。此外,有机碳与Fe(Ⅱ)离子之间存在竞争吸附,减弱了铁氧化物对Fe(Ⅱ)的吸附作用。
|
图 2 有机碳分子对铁氧化物再结晶过程的抑制作用(据Hua等[7]修改) Fig. 2 Inhibition of iron oxides recrystallization by organic carbon molecules(modified from Hua et al[7]) |
有机碳对铁氧化物矿相转化的影响程度与有机碳自身的性质紧密相关。有研究利用铁同位素跟踪次生矿物的形成过程,发现胡敏酸-水铁矿复合物在培养过程中有60%~80%的水铁矿向针铁矿转化;而富里酸-水铁矿复合物则未观察到显著的矿相转化,但Fe(Ⅱ)与铁碳复合物之间仍发生电子转移,约85%的结构铁和水相Fe(Ⅱ)发生交换[47]。这可能是因为富里酸具有更高的电荷密度和更丰富的羧基官能团,使其能与水铁矿紧密结合,表现出更强的铁相转化抑制作用[48]。除了有机碳的组分性质,有机碳的负载量也影响铁氧化物的形态转化。在低碳负载条件下(C︰Fe ≤ 0.05),有机碳对铁氧化物矿相转化过程没有明显抑制作用,但随着碳铁摩尔比的增加,有机碳对铁氧化物结晶的抑制作用逐渐增强[49]。除此之外,铁碳结合方式也会影响铁的矿相转化。吸附和共沉淀两种机制可能形成了不同的化学键强度和分子结构[18,50],共沉淀过程中有机碳分子在铁氧化物表面重构,通过分子间的胶结作用形成更为紧密的复合结构,从而显著抑制铁结晶过程[51-52]。
已有研究表明,提高土壤Fe(Ⅱ)离子浓度可以有效缓解有机碳对铁矿相转化的抑制效果。虽然最终反应产物仍以水铁矿为主,但高浓度Fe(Ⅱ)离子提高了赤铁矿、磁铁矿等晶型矿物的产率[53]。在Fe(Ⅱ)离子催化铁氧化物向晶型铁转化过程中,可能影响铁碳复合物中有机碳的稳定性。有研究发现,Fe(Ⅱ)催化水铁矿-自然有机碳复合物的矿相转化过程中,铁碳复合物的碳铁摩尔比从1.8降至0.7,且复合物和溶液中的有机碳保持着动态交换状态[54]。其中,富含羧基官能团的有机碳组分通过多羧基配体交换吸附机制与铁氧化物紧密结合,在铁氧化物矿相转化过程中脱附的概率较低,延长了相关有机碳在土壤中的周转时间[55]。
综上所述,有机碳对铁氧化物形态转化的抑制作用与有机碳性质、铁碳结合方式以及Fe(Ⅱ)离子浓度紧密相关,可以使铁氧化物长期维持低结晶状态。这种抑制作用可能在不同程度上维持着铁氧化物的活性,同时导致FeOC的稳定性降低。
3 有机碳固定与分解过程的关键生物作用 3.1 “酶栓”和“铁门”在土壤环境中,铁氧化物还原形成Fe(Ⅱ)主要由微生物呼吸驱动[36]。Shewanella、Geobacter等铁还原菌通过表面附着或电子穿梭介导电子传递过程,以Fe(Ⅲ)作为电子受体,氧化有机碳产生CO2和Fe(Ⅱ),从而减弱铁对有机碳的保护作用[56-57]。据估算,Fe(Ⅲ)还原贡献了热带森林土壤厌氧呼吸的44%[58],以及北极沿海平原土壤有机碳矿化的40%~63%[59]。因此,还原条件下铁氧化物吸附固定有机碳的稳定作用可能被弱化,“酶栓”和“铁门”等生物活性限制作用逐渐增强,在土壤碳库稳定机制中占据主导地位。
根据“酶栓”理论,还原条件下土壤环境存在氧气限制,微生物代谢速率和酚氧化酶活性降低,导致多酚化合物在土壤中积累[60]。这些酚类化合物会抑制微生物的酶活性,如水解酶、氧化还原酶和裂解酶等,导致土壤有机碳持续积累。因此,“酶栓”保护机制有效弥补了还原条件下铁碳解耦导致的碳库稳定机制缺失,促进了土壤有机碳积累。但是,还原条件下土壤中丰富的Fe(Ⅱ)离子可以通过芬顿/类芬顿反应分解酚类化合物,导致“酶栓”对土壤有机碳的保护作用减弱[61-62]。同时,近期有研究发现,酚氧化酶并不是酚类化合物的唯一“酶栓”,土壤微生物通过多种酶(如过氧化物酶、醌还原酶)在不同氧化还原条件下代谢多酚,削弱了“酶栓”的碳稳定作用[63]。受“酶栓”保护的有机碳组分较为脆弱,一旦脱离还原环境,微生物和酶解除氧气限制,溶解态有机碳就会发生剧烈的矿化损失。
当土壤环境从还原条件向氧化条件转变时,以土壤亚铁氧化过程为核心的“铁门”保护机制逐渐发挥作用[64]。有研究发现,在自然湿地水位下降的条件下,土壤酚氧化酶的活性随Fe(Ⅱ)浓度的降低而降低。该过程中,Fe(Ⅱ)氧化导致羟基自由基产率逐渐降低,且通过释放质子降低土壤pH,进而抑制酚氧化酶活性,减缓湿地氧化过程中有机碳的分解;同时新生铁氧化物逐渐形成,再次发挥对有机碳的固持作用,底土中约40%的木质素酚被弱晶型铁氧化物保护,维持土壤中酚类化合物的持续积累[12]。
“酶栓”和“铁门”反映了铁碳解耦-耦合的动态变化。在还原阶段,微生物以有机碳作为电子供体驱动Fe(Ⅲ)还原,铁碳解耦导致有机碳生物有效性增加,但氧气限制抑制了土壤有机碳的生物矿化;氧化阶段,Fe(Ⅱ)含量逐渐降低,该过程抑制微生物酶活恢复,又通过新生铁氧化物的吸附作用增强有机碳固存。这种阶段性变化在水-旱轮作体系中表现为:水稻季的还原条件激活“酶栓”,减少有机碳损失;小麦季的氧化环境触发“铁门”,促进有机碳与新生铁矿物结合[65]。因此,在铁氧化物氧化-还原过程中,“铁门”和“酶栓”交替发挥作用,实现土壤有机碳的长期固存。
3.2 激发效应外源有机碳的输入能够强烈地改变土壤有机碳的生物分解速率,这种现象被称为激发效应(Priming effect,PE)[66]。铁碳结合能够抑制外源碳诱导的土壤有机碳矿化损失,促进微生物量碳的积累,表现为负激发效应。然而,铁碳解耦过程会释放不稳定有机碳[67],导致土壤有机碳矿化损失加剧,产生正激发效应。
在氧化条件下,铁氧化物能够诱导有机碳的负激发效应。首先,铁碳结合能有效降低有机碳的生物有效性,直接减少微生物的矿化分解。此外,铁氧化物在固持有机碳的同时也会吸附土壤中氮、磷等营养元素,该吸附过程会使土壤养分化学计量失衡,导致微生物的养分限制,从而降低激发效应[68]。结晶度较高的铁氧化物与有机碳结合后稳定性更高,能够在较高程度上诱导负激发效应。在钙积土中外源添加葡萄糖和不同形态铁氧化物的研究表明:相较于单独添加葡萄糖的处理,针铁矿与葡萄糖共同添加使总CO2排放量降低11%~12%,而水铁矿与葡萄糖共同添加处理仅减少7%~8%的碳损失[69]。
铁氧化物的还原过程能够释放其表面结合或吸附的有机碳,增加土壤中可溶性有机碳和低分子量有机碳含量,从而诱导正激发效应。Liu等[70]结合全球数据分析和室内培养实验发现,厌氧条件下土壤有机碳矿化速率较高时(高于好氧条件的有机碳矿化速率),90%的土壤有机碳矿化损失是由铁还原驱动的,且在氧化还原波动频繁、可还原性铁含量较高和脂质丰度较低的表层土壤中更为明显。根际土壤有机碳激发损失(Rhizosphere priming effect,RPE)也与铁还原过程密切相关,RPE释放的CO2与土壤Fe(Ⅱ)含量呈显著正相关关系(R2 = 0.65,P < 0.01)[71]。这可能是由于根际土壤中生物可利用的有机分子含量较高,且草酸、柠檬酸等有机配体能够通过络合和还原作用驱动短程有序矿物(SRO)和有机碳解耦,显著提升根际碳的激发效应,这导致森林生态系统中约1% C·a−1的土壤有机碳矿化损失[72]。
在农业生产中,秸秆还田、畜禽粪便施用存在显著的正激发效应。该过程中较高水平的土壤有机碳损失,直接影响农田土壤的改良、培肥和固碳减排[73]。因此,土壤改良过程可以与铁氧化物含量或活性调控措施相结合,以降低有机碳激发损失,提升土壤有机改良剂的施用效益,增强土壤有机碳库的固持潜力。还有研究表明,正激发效应的强度可能也与土壤对外源碳输入的适应性有关,当土壤在几年到几十年的时间里适应高强度的碳输入时,正激发效应造成的碳损失会降低[74]。这种土壤对碳输入的适应性,可能是由微生物群落及土壤矿物组成共同决定的,铁氧(氢)氧化物等活性矿物在其中发挥的作用还需要进一步明晰。
4 环境因素对铁氧化物-有机碳耦合过程的影响自然土壤环境异质性较强,水分、氧含量、pH等关键环境因素持续变化,显著影响土壤中生物化学反应过程与强度。因此,不同环境条件下土壤有机碳库的核心稳定机制有所区别,铁氧化物在有机碳形态转化过程中发挥的作用也存在差异。
4.1 水分及氧含量水分及氧含量的变化对于调控土壤氧化还原状态具有关键作用。例如,在潮湿的热带土壤、水稻土和根际土壤中,氧气浓度波动频繁,导致铁的氧化还原持续发生,显著影响土壤铁碳耦合过程[75]。Chen等[6]通过铁碳同位素标记的方法,探究氧化还原循环过程中铁对有机碳的保护作用。结果表明:仅在静态有氧条件下及铁和DOC同时添加时才能发挥有机碳保护作用,新生铁氧化物对DOC和SOC的矿化抑制作用分别达到35%和47%;但在低O2浓度条件下,新生成的活性铁氧化物优先被还原,分别使DOC和SOC的矿化增加74%和32%~41%。也有研究表明,与暴露于低O2浓度环境相比,高O2浓度环境会导致更快的Fe(Ⅱ)氧化速率,但形成的铁氧化物结晶度偏低[76]。这可能导致后续经历还原过程时,会发生更高强度的铁氧化物还原和有机碳矿化。
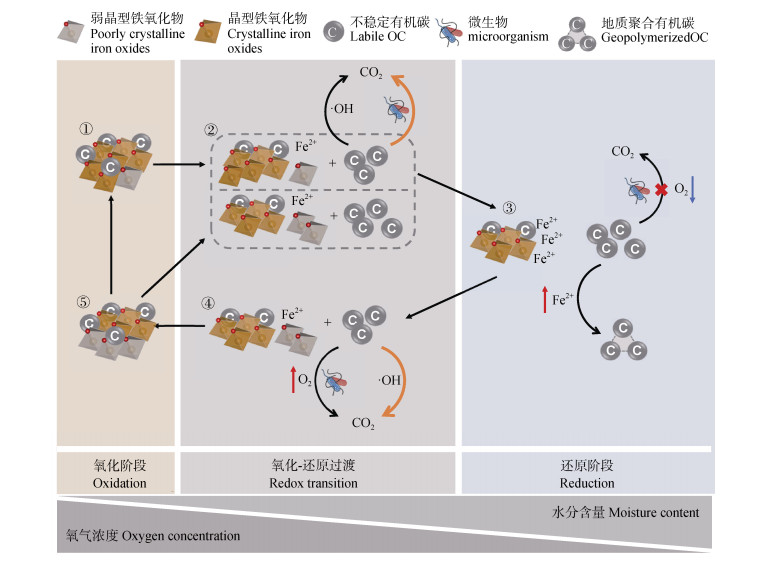
为进一步描述水分、氧含量诱导的土壤环境变化过程对土壤铁碳耦合机制的影响,可以将该过程划分为氧化阶段、氧化还原过渡阶段以及还原阶段。氧化还原过渡阶段又可以区分为氧化向还原过渡阶段、还原向氧化过渡阶段。这种阶段性变化在自然环境降水和蒸发导致的地下水位波动、水稻种植管理的灌排水过程中时常发生。图 3描述了上述5个阶段对应的铁形态动态变化过程,以及土壤有机碳的矿化和保护机制。
|
图 3 土壤水分和氧含量变化诱导的铁碳关系转换 Fig. 3 Transformation of iron-carbon interactions induced by variations in soil moisture and oxygen levels |
(1)氧化阶段:该阶段环境氧含量较高,微生物活性强,碳库保护机制以矿物固定为主[13]。该阶段铁氧化物与有机碳结合,抑制微生物代谢诱导的生物矿化。且铁氧化物在氧化条件下能够维持稳定,芬顿反应诱导的非生物矿化强度也处于较低水平。(2)氧化向还原过渡阶段:该阶段环境氧含量降低,微生物活性逐渐减弱,碳库保护机制以矿物固定为主。其中,晶型铁氧化物结构稳定,可维持铁碳复合状态;而弱晶型铁氧化物的碳保护作用逐渐失效[21]。由于部分铁碳解耦,该阶段存在较强的矿化作用,芬顿反应诱导的非生物矿化与生物矿化过程同时发生。受Fe(Ⅱ)浓度限制,该阶段的非生物矿化作用较弱;而环境氧含量限制还未形成,生物矿化作用可能更为强烈。(3)还原阶段:该阶段Fe(Ⅱ)浓度较高,稳定性较差的小分子有机碳较多;且环境氧含量低,微生物活性弱,碳库保护机制主要是受“酶栓”所主导的生物活性限制,即氧水平降低导致的生物矿化作用减弱[60]。同时,由于热力学限制,该阶段晶型铁氧化物不易还原溶解,其较强的结构稳定性在碳库保护过程中存在优势。由于土壤溶液中Fe(Ⅱ)浓度较高,催化反应诱导的非生物聚合作用可能有所增加。(4)还原向氧化过渡阶段:该阶段Fe(Ⅱ)浓度逐渐降低,环境氧含量升高,微生物活性逐渐恢复。生物活性限制和矿物固定两种碳库保护机制同时发挥作用(铁门机制)。Fe(Ⅱ)浓度降低,酚氧化酶活性受到抑制,且铁氧化物重新结晶,矿物固定作用逐渐恢复[64]。该过程中,Fe(Ⅱ)持续氧化产生Fe(Ⅲ)以及活性氧,以芬顿反应为主导的非生物矿化作用强烈。同时,土壤氧气水平逐渐恢复,但微生物活性恢复存在适应过程,因此生物矿化作用可能较弱。该阶段短程有序铁(SRO)逐渐形成,其具有较强的碳负载能力,可能在生物矿化速率提升前及时恢复有机碳的矿物保护作用。(5)氧化阶段:该阶段环境氧含量重新恢复到较高水平,微生物活性强。碳库保护机制以矿物固定为主,新生铁氧化物中SRO形态占比较高,具有更强的有机碳负载能力,但稳定性相对偏低[76]。因此,在未形成晶型矿物之前,新生铁氧化物可能在下一个还原阶段中产生更为强烈的铁碳解耦过程。
总体而言,矿物吸附固定有机碳在氧化环境中更具优势,而生物活性限制主要在还原条件下发挥作用。当氧气和水分含量变化导致土壤环境从氧化阶段向还原阶段切换时,铁氧化物对有机碳的保护作用相对减弱,而“酶栓”和“铁门”等生物活性限制作用逐渐增强。在土壤环境从还原阶段重新进入氧化阶段时,由于积累了大量Fe(Ⅱ)和不稳定碳组分,有机碳的矿化损失风险最高。该阶段生物活性限制和矿物吸附固定同时发挥作用,其相对重要性可能取决于氧气浓度逐渐提高过程中微生物活性的增长趋势,以及铁氧化物对有机碳保护作用的恢复程度。相对而言,在氧化、还原阶段切换过程中,土壤中铁碳形态的变化更为复杂,催化、聚合等反应可能同时发生。因此,有必要进一步探究氧化还原的过渡阶段、土壤铁形态变化与有机碳周转的相互关系。
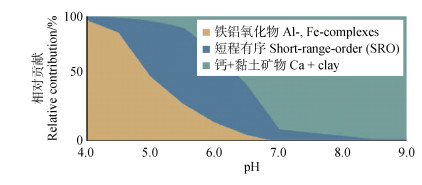
4.2 pH土壤pH通过改变铁的形态和电荷特征影响铁碳结合过程[77]。在低pH条件下,铁的氧化速率显著降低,Fe(Ⅱ)甚至可以在氧化条件下稳定存在;而在高pH条件下,土壤铁会被迅速氧化形成Fe(Ⅲ)矿物,此时Fe(Ⅱ)仅能在缺氧环境中存在[78]。Fe(Ⅱ)浓度和质子浓度直接影响土壤芬顿和类芬顿反应速率。因此,在pH偏低时,铁诱导的有机碳形态转化可能更为剧烈。低pH促进铁氧化物的溶解和再结晶过程,通过吸附、共沉淀促进FeOC的形成。其次,pH改变了铁氧化物表面电荷,当pH低于零点电荷时,铁矿物表面质子化,净正电荷增加,增加其对有机碳的吸附强度。这增强了铁氧化物对土壤有机碳的保护作用,对于正激发效应等有机碳损失过程有显著的抑制作用。有研究表明,pH较低的酸性土壤环境中,相同数量的铁可以通过吸附或共沉淀负载更多的有机碳[79]。但是,当土壤pH达到7.2~7.6时,铁矿物与有机碳的结合优势就会向含钙矿物转变[80]。因此,不同pH条件下土壤铁氧化物对土壤有机碳库稳定性的贡献具有显著差异(图 4)。具体表现为,酸性条件下铁铝金属氧化物的相对贡献偏高,pH 4~5范围内铁铝有机络合物占据主导作用,而在pH 5~6区间内短程有序金属氧化物(SRO)的相对贡献维持在较高水平[81]。
|
图 4 不同pH条件下各类土壤矿物对有机碳稳定的相对贡献(据Rasmussen等[81]修改) Fig. 4 Relative contribution of various soil minerals to SOC stabilization across different pH gradients(modified from Rasmussen et al[81]) |
综上所述,在酸性土壤条件下,铁氧化物对土壤有机碳库的稳定具有关键意义。在农业生产过程中,酸化不仅阻碍土壤健康的维持,而且对农业可持续发展构成了挑战[82]。因此,众多研究致力于提升土壤pH及其抗酸化能力,以实现农田土壤酸化改良。然而,目前鲜有研究深入探讨农田土壤酸化改良过程中,金属氧化物对有机碳固存能力的变化,FeOC的相对含量及其稳定性的变化规律需要通过进一步研究来明确和阐释。
4.3 光照光照可以改变有机碳的化学结构和分子量。光照条件下,有色可溶性有机物发生光化学降解[83],且在铁氧化物的参与下,光化学过程进一步复杂化。铁氧化物在光照下产生光电子和空穴,其表面羟基通过配体-金属电荷转移形成Fe(Ⅲ)-羟基配合物,促进Fe(Ⅱ)和HO•、O2•−的生成[84]。这些活性氧不仅直接提高有机碳的光化学降解速率,还能通过芬顿/类芬顿反应进一步产生羟基自由基,从而促进有机碳的降解。针对针铁矿和DOC的光催化实验研究表明,相较于黑暗处理,光催化形成了HO•、O2•−等活性氧,使Fe(Ⅱ)含量增加了4.75倍~16.66倍,DOC浓度降低约10%[85]。该过程改变了DOC的结构组成,使碳水化合物、脂质和蛋白质化合物氧化损失。此外,铁氧化物可以降低光照条件下土壤有机碳的生物矿化损失。Wen等[86]研究发现,光催化通过促进木质素解聚,增加微生物的底物可用性,促进木质素的生物降解,该过程中生物矿化产生的CO2较非生物矿化多出5倍以上。其中铁氧化物通过与木质素衍生物结合降低光催化影响,减少微生物对木质素的可及性并限制其分解。同时,光照还影响着有机碳分子的聚合过程。有研究发现,与铁结合的溶解态有机碳在模拟太阳光照射下会发生光化学转化,使溶解态有机碳转化为富含新形成的脂肪族和缩合芳香族分子的颗粒态有机碳。同时,DOC络合的Fe(Ⅱ)和Fe(Ⅲ)离子结晶形成铁氧化物,与新形成的有机碳重新结合[87]。该过程被称为光絮凝,促进沉积物中颗粒态有机物的积累。
4.4 温度环境温度变化不会直接改变铁碳结合机制[88],但可以通过影响土壤pH、土壤水分与含氧量、矿物风化情况等因素,调控铁碳耦合过程。在自然环境温度升高时,凋落物和根系分泌物的积累加快,这导致土壤中酸性物质增加,并通过调控土壤pH影响铁碳耦合关系[89]。同时,环境增温会导致土壤含水量降低,提升土壤含氧量,从而提高土壤铁氧化物的结晶度,增强铁碳复合物的稳定性[90]。但需要注意的是,增温诱导铁的结晶度增加会减少有机碳的负载容量,从而降低铁碳复合物的形成效率[91]。因此,环境温度变化虽然没有直接改变铁碳复合机制,但可以通过影响其他环境因素调控铁碳耦合过程。
现有研究中,通常用Q10(土壤温度每升高10 ℃时有机碳分解速率成比例增加的倍数)衡量碳组分的温度敏感性[92]。据估计在全球范围内,未受矿物保护的有机碳较MAOC的气候温度敏感性高28%[93]。有研究发现,有机络合铁是影响MAOC温度敏感性变化的主要因素,增温条件下有机络合铁变化与MAOC Q10的变化呈负相关,表明铁氧化物保护作用是导致MAOC温度敏感性降低的主要原因[94]。全球变暖趋势和极端气候导致的干湿交替频率增加将促进矿物风化。风化过程不仅会增强矿物对有机物的亲和力,而且还会促进铁氧化物等活性矿物的生成[95-96],微生物代谢和矿物风化之间的协同作用可进一步促进铁结合态有机碳的形成。同时,全球变暖使土壤环境经历更强的氧化还原波动和紫外线辐射[97],这种环境变化增强了土壤铁氧化还原与有机碳形态转化的相互联系,直接影响铁氧化物的活性和有机碳的赋存形态。因此,土壤铁氧化物等活性矿物的相对含量提升和形态调控是提升土壤固碳潜力和土壤碳库稳定性的有效途径[98]。
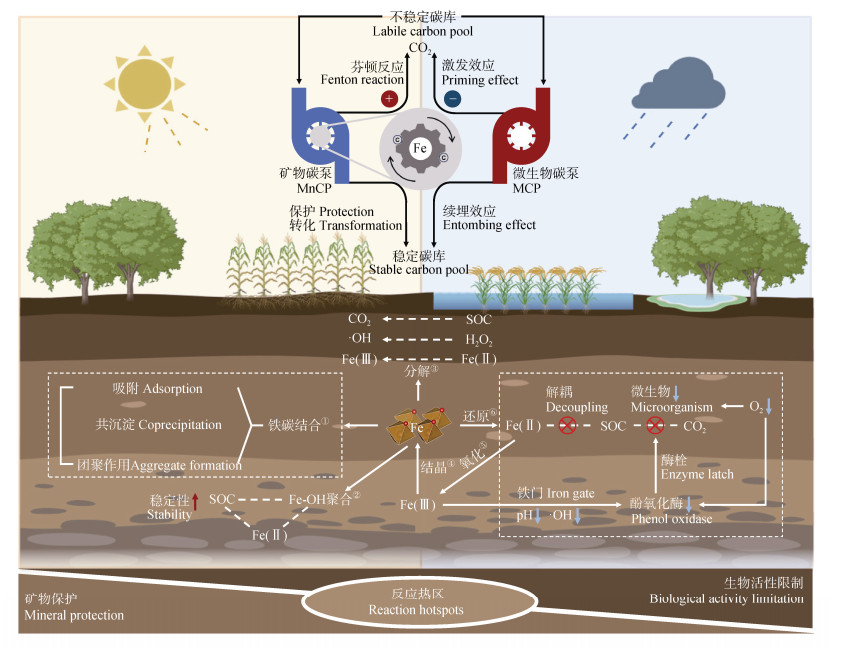
5 结论与展望土壤铁是矿物碳泵的核心组成,是双泵联合固碳的重要桥梁(图 5)。在矿物碳泵理论中,一方面土壤铁氧化物通过吸附固定、催化聚合促进稳定碳库的形成,另一方面铁氧化还原通过芬顿反应加快土壤有机碳的形态转化。在微生物碳泵理论中,铁氧化物能够抑制激发效应导致的有机碳生物代谢损失,并通过吸附固定加快微生物源碳向土壤稳定碳库转化。在环境水氧含量变化时,铁氧化物与有机碳存在解耦-再耦合的动态变化过程,有机碳保护机制在铁氧化物主导的矿物保护和“酶栓”、“铁门”主导的生物活性限制之间切换。
|
图 5 铁在碳泵中的关键作用及其在不同环境条件下与土壤碳周转的相互关系 Fig. 5 The key role of iron in the carbon pump and its relationship with soil carbon turnover under different environmental conditions |
在自然土壤环境中,铁氧化物的赋存形态决定其在碳周转过程中的作用,调控土壤铁循环过程有望成为应对气候变化和土壤固碳的新途径。因此,在农业实践中,可针对不同的土壤环境采取相应措施调控铁氧化物的形态和含量,以实现土壤有机碳库的长期稳定固持。例如,在风化程度较高的旱地土壤中,可以通过施用改良剂提高铁氧化物的有效性,促进有机碳腐解的同时提升土壤固碳潜力。而在水稻种植区域,可通过晒田等方法提高土壤铁氧化物的稳定性,以减少氧化还原波动诱导的土壤有机碳库损失。综上所述,土壤铁氧化物与有机碳的耦合机制较为复杂,对土壤碳固持策略具有重要意义,未来还可在以下几个方面深入研究:(1)土壤有机碳聚合反应的直观验证与量化。虽然金属氧化物在地质聚合反应过程中的催化作用已有研究,但SOC的聚合反应仍缺乏直观证据。这主要受限于土壤复杂的物质组成,以及多种生物化学反应几乎同时发生,导致铁氧化物在聚合反应中发挥的作用难以被观测和量化。SOC聚合反应是腐殖化过程中的关键步骤,因此有必要深入探究土壤活性矿物催化的聚合反应及其对SOC保存的影响。未来可利用同步辐射X射线技术观测SOC聚合过程中的光谱特征变化,明确其反应机理,构建模型并结合数据分析量化其环境效益。(2)土壤微区生物过程对铁碳耦合的调控机制。除了上述“酶栓”、“铁门”机制,微生物本身就是土壤有机碳的主要来源,微生物分泌的有机物质如胞外聚合物(Extracellular polymeric substances,EPS)会直接与铁氧化物作用。此外,微生物还参与电子传递,影响铁碳耦合过程中的氧化还原反应。植物根际土壤有机碳种类丰富,显著增强了生物过程对铁碳耦合的影响。同时,根系活动以及低分子有机酸等根系分泌物也会影响铁碳耦合过程。然而,根系-微生物-铁氧化物的相互作用对有机碳固持的影响尚不明确,未来可通过碳同位素示踪结合原位微区表征技术进一步探究。(3)铁氧化还原过程中有机碳固定与形态转化的权衡机制。在土壤氧化还原过渡阶段,铁氧化物界面存在反应热点,铁结合态有机碳处于吸附-解吸的动态变化过程,且芬顿反应和催化聚合导致的有机碳形态转化频繁发生。但该阶段中,铁氧化物介导的有机碳固定与形态转化的反应贡献有待进一步量化。未来应进一步结合同步辐射、穆斯堡尔谱、傅里叶变换离子回旋共振质谱(FT-ICR MS)等表征技术探究氧化还原波动下铁氧化物对碳固持效率的时空异质性,为农业管理(如稻田水分调控)提供理论依据。(4)铁碳耦合的跨尺度模型整合与碳汇潜力评估。土壤数据的缺失和对生物地球化学过程异质性的理解不足,阻碍了SOC动态模型的构建[99]。将微观尺度的铁碳耦合机制(如吸附、催化)整合至全球碳循环模型中至关重要。人工智能和机器学习发展迅速,推动土壤研究从验证微观机理向量化宏观效益进一步拓展。未来应将表征技术与人工智能进一步结合,开发铁碳交互模块并嵌入SOC模型,实现从分子机制到碳汇效益的跨尺度预测,支撑碳中和目标的科学决策。
综上所述,将新兴表征技术与先进算法相结合,有望进一步解析土壤铁碳耦合的微观机制,并推动SOC固持效益的宏观量化,为应对气候变化和提升土壤碳库及其稳定性提供理论依据和技术支持。
| [1] |
Stockmann U, Adams M A, Crawford J W, et al. The knowns, known unknowns and unknowns of sequestration of soil organic carbon[J]. Agriculture, Ecosystems & Environment, 2013, 164: 80-99.
(  0) 0) |
| [2] |
Xiao K Q, Zhao Y, Liang C, et al. Introducing the soil mineral carbon pump[J]. Nature Reviews Earth & Environment, 2023, 4(3): 135-136.
(  0) 0) |
| [3] |
Xiao K Q, Li X N, Xing W, et al. Mechanisms of organic carbon sequestration and stabilization mediated by the soil "mineral carbon pump(MnCP)" (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(3): 595-609. DOI:10.11766/trxb202404250169 [肖可青, 李心男, 邢稳, 等. 土壤"矿物碳泵(MnCP)"介导有机碳的固存与稳定机制[J]. 土壤学报, 2025, 62(3): 595-609.]
(  0) 0) |
| [4] |
Zhu X F, Kong W D, Huang Y M, et al. Soil microbial carbon pump conceptual framework 2.0 (In Chinese)[J]. Chinese Journal of Applied Ecology, 2024, 35(1): 102-110. [朱雪峰, 孔维栋, 黄懿梅, 等. 土壤微生物碳泵概念体系2.0[J]. 应用生态学报, 2024, 35(1): 102-110.]
(  0) 0) |
| [5] |
Jia N, Li L, Guo H, et al. Important role of Fe oxides in global soil carbon stabilization and stocks[J]. Nature Communications, 2024, 15: 10318. DOI:10.1038/s41467-024-54832-8
(  0) 0) |
| [6] |
Chen C M, Hall S J, Coward E, et al. Iron-mediated organic matter decomposition in humid soils can counteract protection[J]. Nature Communications, 2020, 11: 2255. DOI:10.1038/s41467-020-16071-5
(  0) 0) |
| [7] |
Hua J, Sun J, Chen M J, et al. Aqueous Fe(II)-catalyzed iron oxide recrystallization: Fe redox cycling and atom exchange, mineralogical recrystallization and contributing factor[J]. Reviews in Environmental Science and Bio/Technology, 2023, 22(1): 55-78. DOI:10.1007/s11157-023-09646-3
(  0) 0) |
| [8] |
Liu L H, Zheng N G, Yu Y X, et al. Soil carbon and nitrogen cycles driven by iron redox: A review[J]. Science of the Total Environment, 2024, 918: 170660. DOI:10.1016/j.scitotenv.2024.170660
(  0) 0) |
| [9] |
Dong H L, Zeng Q, Sheng Y Z, et al. Coupled iron cycling and organic matter transformation across redox interfaces[J]. Nature Reviews Earth & Environment, 2023, 4(9): 659-673.
(  0) 0) |
| [10] |
Underwood T R, Bourg I C, Rosso K M. Mineral-associated organic matter is heterogeneous and structured by hydrophobic, charged, and polar interactions[J]. Proceedings of the National Academy of Sciences of the United States of America, 2024, 121(46): e2413216121.
(  0) 0) |
| [11] |
Wagai R, Mayer L M. Sorptive stabilization of organic matter in soils by Hydrous iron oxides[J]. Geochimica et Cosmochimica Acta, 2007, 71(1): 25-35. DOI:10.1016/j.gca.2006.08.047
(  0) 0) |
| [12] |
Wang Y Y, Wang H, He J S, et al. Iron-mediated soil carbon response to water-table decline in an alpine wetland[J]. Nature Communications, 2017, 8: 15972. DOI:10.1038/ncomms15972
(  0) 0) |
| [13] |
Chen C M, Dynes J J, Wang J, et al. Properties of Fe-organic matter associations via coprecipitation versus adsorption[J]. Environmental Science & Technology, 2014, 48(23): 13751-13759.
(  0) 0) |
| [14] |
Han L F, Sun K, Keiluweit M, et al. Mobilization of ferrihydrite-associated organic carbon during Fe reduction: Adsorption versus coprecipitation[J]. Chemical Geology, 2019, 503: 61-68. DOI:10.1016/j.chemgeo.2018.10.028
(  0) 0) |
| [15] |
Gao W, Duan X, Chen X B, et al. Iron-carbon complex types and bonding forms jointly control organic carbon mineralization in paddy soils[J]. Science of the Total Environment, 2024, 953: 176117. DOI:10.1016/j.scitotenv.2024.176117
(  0) 0) |
| [16] |
Silva L C R, Doane T A, Corrêa R S, et al. Iron-mediated stabilization of soil carbon amplifies the benefits of ecological restoration in degraded lands[J]. Ecological Applications, 2015, 25(5): 1226-1234. DOI:10.1890/14-2151.1
(  0) 0) |
| [17] |
Han Z G, Zhou Y C, Guo Y L, et al. Organic carbon sequestration by Fe oxides in aggregates in a Pinus massoniana conifer-broadleaf mixed forest[J]. Soil and Tillage Research, 2024, 240: 106105. DOI:10.1016/j.still.2024.106105
(  0) 0) |
| [18] |
Wang S, Gao W, Ma Z, et al. Iron mineral type controls organic matter stability and priming in paddy soil under anaerobic conditions[J]. Soil Biology and Biochemistry, 2024, 197: 109518. DOI:10.1016/j.soilbio.2024.109518
(  0) 0) |
| [19] |
Li Q, Hu W F, Li L F, et al. Interactions between organic matter and Fe oxides at soil micro-interfaces: Quantification, associations, and influencing factors[J]. Science of the Total Environment, 2023, 855: 158710. DOI:10.1016/j.scitotenv.2022.158710
(  0) 0) |
| [20] |
Lü J T, Zhang S Z, Wang S S, et al. Molecular-scale investigation with ESI-FT-ICR-MS on fractionation of dissolved organic matter induced by adsorption on iron oxyhydroxides[J]. Environmental Science & Technology, 2016, 50(5): 2328-2336.
(  0) 0) |
| [21] |
Duan X, Li Z, Wang S, et al. Stability of iron-carbon complexes determines carbon sequestration efficiency in iron-rich soils[J]. Soil Biology and Biochemistry, 2025, 203: 109718. DOI:10.1016/j.soilbio.2025.109718
(  0) 0) |
| [22] |
Liu F, Ding Z C, Lu Y, et al. Nano-scale investigation of organic C sequestration and distribution on Fe oxides during ferrihydrite transformation: Effect of Al-substitution[J]. Environmental Science: Nano, 2022, 9(10): 4007-4017. DOI:10.1039/D2EN00505K
(  0) 0) |
| [23] |
Fan Y K, Chi J L, Wang L J, et al. Aluminum substitution stabilizes organic matter in ferrihydrite transforming into hematite: A molecular analysis[J]. Science of the Total Environment, 2024, 945: 174035. DOI:10.1016/j.scitotenv.2024.174035
(  0) 0) |
| [24] |
Hu Z, McKenna A M, Wen K, et al. Controls of mineral solubility on adsorption-induced molecular fractionation of dissolved organic matter revealed by 21 T FT-ICR MS[J]. Environmental Science & Technology, 2024, 58(5): 2313-2322.
(  0) 0) |
| [25] |
Zhu X Y, Wang K, Liu Z Z, et al. Probing molecular-level dynamic interactions of dissolved organic matter with iron oxyhydroxide via a coupled microfluidic reactor and an online high-resolution mass spectrometry system[J]. Environmental Science & Technology, 2023, 57(7): 2981-2991.
(  0) 0) |
| [26] |
Curti L, Moore O W, Babakhani P, et al. Carboxyl- richness controls organic carbon preservation during coprecipitation with iron(oxyhydr)oxides in the natural environment[J]. Communications Earth & Environment, 2021, 2: 229.
(  0) 0) |
| [27] |
Ye Y P, Wang Z W, Liu L J, et al. Novel insights into the temporal molecular fractionation of dissolved black carbon at the iron oxyhydroxide - water interface[J]. Water Research, 2023, 229: 119410. DOI:10.1016/j.watres.2022.119410
(  0) 0) |
| [28] |
Kang J, Qu C C, Chen W L, et al. Organo-organic interactions dominantly drive soil organic carbon accrual[J]. Global Change Biology, 2024, 30(1): e17147. DOI:10.1111/gcb.17147
(  0) 0) |
| [29] |
Ruiz-Mirazo K, Briones C, de la Escosura A. Prebiotic systems chemistry: New perspectives for the origins of life[J]. Chemical Reviews, 2014, 114(1): 285-366. DOI:10.1021/cr2004844
(  0) 0) |
| [30] |
Kleber M, Bourg I C, Coward E K, et al. Dynamic interactions at the mineral–organic matter interface[J]. Nature Reviews Earth & Environment, 2021, 2(6): 402-421.
(  0) 0) |
| [31] |
Jokic A, Frenkel A I, Vairavamurthy M A, et al. Birnessite catalysis of the Maillard reaction: Its significance in natural humification[J]. Geophysical Research Letters, 2001, 28(20): 3899-3902. DOI:10.1029/2001GL013839
(  0) 0) |
| [32] |
Wang H Y, Qian H, Yao W R. Melanoidins produced by the Maillard reaction: Structure and biological activity[J]. Food Chemistry, 2011, 128(3): 573-584. DOI:10.1016/j.foodchem.2011.03.075
(  0) 0) |
| [33] |
Hedges J I. The formation and clay mineral reactions of melanoidins[J]. Geochimica et Cosmochimica Acta, 1978, 42(1): 69-76. DOI:10.1016/0016-7037(78)90218-1
(  0) 0) |
| [34] |
Moore O W, Curti L, Woulds C, et al. Long-term organic carbon preservation enhanced by iron and manganese[J]. Nature, 2023, 621(7978): 312-317. DOI:10.1038/s41586-023-06325-9
(  0) 0) |
| [35] |
Ashraf A, Wu H Y, Zhang B J, et al. Exploring abiotic non-catalytic polyphenol-Maillard humification in light-limited environment[J]. Applied Geochemistry, 2025, 184: 106368. DOI:10.1016/j.apgeochem.2025.106368
(  0) 0) |
| [36] |
Jokic A, Wang M C, Liu C, et al. Integration of the polyphenol and Maillard reactions into a unified abiotic pathway for humification in nature the role of δ-MnO2[J]. Organic Geochemistry, 2004, 35(6): 747-762. DOI:10.1016/j.orggeochem.2004.01.021
(  0) 0) |
| [37] |
Huang J Z, Jones A, Waite T D, et al. Fe(II)redox chemistry in the environment[J]. Chemical Reviews, 2021, 121(13): 8161-8233. DOI:10.1021/acs.chemrev.0c01286
(  0) 0) |
| [38] |
Garrido-Ramírez E G, Theng B K G, Mora M L. Clays and oxide minerals as catalysts and nanocatalysts in Fenton-like reactions—A review[J]. Applied Clay Science, 2010, 47(3/4): 182-192.
(  0) 0) |
| [39] |
Yu G H, Kuzyakov Y. Fenton chemistry and reactive oxygen species in soil: Abiotic mechanisms of biotic processes, controls and consequences for carbon and nutrient cycling[J]. Earth-Science Reviews, 2021, 214: 103525. DOI:10.1016/j.earscirev.2021.103525
(  0) 0) |
| [40] |
Chen N, Fu Q L, Wu T L, et al. Active iron phases regulate the abiotic transformation of organic carbon during redox fluctuation cycles of paddy soil[J]. Environmental Science & Technology, 2021, 55(20): 14281-14293.
(  0) 0) |
| [41] |
Hall S J, Silver W L. Iron oxidation stimulates organic matter decomposition in humid tropical forest soils[J]. Global Change Biology, 2013, 19(9): 2804-2813. DOI:10.1111/gcb.12229
(  0) 0) |
| [42] |
Du H Y, Chen C M, Yu G H, et al. An iron-dependent burst of hydroxyl radicals stimulates straw decomposition and CO2 emission from soil hotspots: Consequences of Fenton or Fenton-like reactions[J]. Geoderma, 2020, 375: 114512. DOI:10.1016/j.geoderma.2020.114512
(  0) 0) |
| [43] |
Sun R, Cao Z Y, Wen X L, et al. Quinone redox cycling drives lignocellulose depolymerization and degradation in composting environments based on metagenomics analysis[J]. Science of the Total Environment, 2023, 856: 159009. DOI:10.1016/j.scitotenv.2022.159009
(  0) 0) |
| [44] |
Sun R, Fu M X, Ma L C, et al. Iron reduction in composting environment synergized with quinone redox cycling drives humification and free radical production from humic substances[J]. Bioresource Technology, 2023, 384: 129341. DOI:10.1016/j.biortech.2023.129341
(  0) 0) |
| [45] |
Chen C M, Thompson A. The influence of native soil organic matter and minerals on ferrous iron oxidation[J]. Geochimica et Cosmochimica Acta, 2021, 292: 254-270. DOI:10.1016/j.gca.2020.10.002
(  0) 0) |
| [46] |
ThomasArrigo L K, Mikutta C, Byrne J, et al. Iron(II)- catalyzed iron atom exchange and mineralogical changes in iron-rich organic freshwater flocs: An iron isotope tracer study[J]. Environmental Science & Technology, 2017, 51(12): 6897-6907.
(  0) 0) |
| [47] |
Zhou Z, Latta D E, Noor N, et al. Fe(II)-catalyzed transformation of organic matter-ferrihydrite coprecipitates: A closer look using Fe isotopes[J]. Environmental Science & Technology, 2018, 52(19): 11142-11150.
(  0) 0) |
| [48] |
Vindedahl A M, Stemig M S, Arnold W A, et al. Character of humic substances as a predictor for goethite nanoparticle reactivity and aggregation[J]. Environmental Science & Technology, 2016, 50(3): 1200-1208.
(  0) 0) |
| [49] |
ThomasArrigo L K, Byrne J M, Kappler A, et al. Impact of organic matter on iron(II)-catalyzed mineral transformations in ferrihydrite-organic matter coprecipitates[J]. Environmental Science & Technology, 2018, 52(21): 12316-12326.
(  0) 0) |
| [50] |
Sodano M, Lerda C, Nisticò R, et al. Dissolved organic carbon retention by coprecipitation during the oxidation of ferrous iron[J]. Geoderma, 2017, 307: 19-29. DOI:10.1016/j.geoderma.2017.07.022
(  0) 0) |
| [51] |
Henneberry Y K, Kraus T E C, Nico P S, et al. Structural stability of coprecipitated natural organic matter and ferric iron under reducing conditions[J]. Organic Geochemistry, 2012, 48: 81-89. DOI:10.1016/j.orggeochem.2012.04.005
(  0) 0) |
| [52] |
Siéliéchi J M, Lartiges B S, Kayem G J, et al. Changes in humic acid conformation during coagulation with ferric chloride: Implications for drinking water treatment[J]. Water Research, 2008, 42(8/9): 2111-2123.
(  0) 0) |
| [53] |
Chen C M, Kukkadapu R, Sparks D L. Influence of coprecipitated organic matter on Fe2+(aq)-catalyzed transformation of ferrihydrite: Implications for carbon dynamics[J]. Environmental Science & Technology, 2015, 49(18): 10927-10936.
(  0) 0) |
| [54] |
Noor N, Thompson A. Localized alteration of ferrihydrite natural organic matter coprecipitates following reaction with Fe(II)[J]. Soil Science Society of America Journal, 2022, 86(2): 253-263. DOI:10.1002/saj2.20366
(  0) 0) |
| [55] |
Zhao Y, Moore O W, Xiao K Q, et al. The role and fate of organic carbon during aging of ferrihydrite[J]. Geochimica et Cosmochimica Acta, 2022, 335: 339-355. DOI:10.1016/j.gca.2022.07.003
(  0) 0) |
| [56] |
Patzner M S, Mueller C W, Malusova M, et al. Iron mineral dissolution releases iron and associated organic carbon during permafrost thaw[J]. Nature Communications, 2020, 11: 6329. DOI:10.1038/s41467-020-20102-6
(  0) 0) |
| [57] |
Pan W N, Kan J J, Inamdar S, et al. Dissimilatory microbial iron reduction release DOC(dissolved organic carbon)from carbon-ferrihydrite association[J]. Soil Biology and Biochemistry, 2016, 103: 232-240. DOI:10.1016/j.soilbio.2016.08.026
(  0) 0) |
| [58] |
Dubinsky E A, Silver W L, Firestone M K. Tropical forest soil microbial communities couple iron and carbon biogeochemistry[J]. Ecology, 2010, 91(9): 2604-2612. DOI:10.1890/09-1365.1
(  0) 0) |
| [59] |
Lipson D A, Raab T K, Goria D, et al. The contribution of Fe(III)and humic acid reduction to ecosystem respiration in drained thaw lake basins of the Arctic Coastal Plain[J]. Global Biogeochemical Cycles, 2013, 27(2): 399-409. DOI:10.1002/gbc.20038
(  0) 0) |
| [60] |
Freeman C, Ostle N, Kang H. An enzymic 'latch' on a global carbon store[J]. Nature, 2001, 409(6817): 149.
(  0) 0) |
| [61] |
Yang K J, Jia B, Liu J B, et al. A novel perspective on the role of hydroxyl radicals in soil organic carbon mineralization within the detritusphere: Stimulating C-degrading enzyme activities[J]. Environmental Science & Technology, 2025, 59(10): 5045-5055.
(  0) 0) |
| [62] |
Song W, Clough T, Hou H H, et al. Nitrate-induced hydroxyl radical releases deep soil organic carbon by opening the 'enzyme latch' under micro-aerobic conditions[J]. Soil Biology and Biochemistry, 2024, 192: 109389. DOI:10.1016/j.soilbio.2024.109389
(  0) 0) |
| [63] |
McGivern B B, Cronin D R, Ellenbogen J B, et al. Microbial polyphenol metabolism is part of the thawing permafrost carbon cycle[J]. Nature Microbiology, 2024, 9(6): 1454-1466. DOI:10.1038/s41564-024-01691-0
(  0) 0) |
| [64] |
Wang S M, Liu T, Zhu E X, et al. Potential retention of dissolved organic matter by soil minerals during wetland water-table fluctuations[J]. Water Research, 2024, 254: 121412. DOI:10.1016/j.watres.2024.121412
(  0) 0) |
| [65] |
Jia Z X, Huang X L, Li L N, et al. Rejuvenation of iron oxides enhances carbon sequestration by the 'iron gate' and 'enzyme latch' mechanisms in a rice-wheat cropping system[J]. Science of the Total Environment, 2022, 839: 156209. DOI:10.1016/j.scitotenv.2022.156209
(  0) 0) |
| [66] |
Kuzyakov Y, Friedel J K, Stahr K. Review of mechanisms and quantification of priming effects[J]. Soil Biology and Biochemistry, 2000, 32(11/12): 1485-1498.
(  0) 0) |
| [67] |
Bölscher T, Cardon Z G, Garcia Arredondo M, et al. Vulnerability of mineral-organic associations in the rhizosphere[J]. Nature Communications, 2025, 16: 5527. DOI:10.1038/s41467-025-61273-4
(  0) 0) |
| [68] |
Duan X, Li Z, Li Y H, et al. Iron–organic carbon associations stimulate carbon accumulation in paddy soils by decreasing soil organic carbon priming[J]. Soil Biology and Biochemistry, 2023, 179: 108972. DOI:10.1016/j.soilbio.2023.108972
(  0) 0) |
| [69] |
Fang Y Y, Tavakkoli E, Weng Z, et al. Disentangling carbon stabilization in a Calcisol subsoil amended with iron oxyhydroxides: A dual-13C isotope approach[J]. Soil Biology and Biochemistry, 2022, 170: 108711. DOI:10.1016/j.soilbio.2022.108711
(  0) 0) |
| [70] |
Liu T, Wang X, Wang S M, et al. Iron-driven fast decomposition of soil carbon under periodic Anoxia[J]. Global Change Biology, 2025, 31(4): e70184. DOI:10.1111/gcb.70184
(  0) 0) |
| [71] |
Wu C Y, Huang W, Liu Y X, et al. Physicochemically protected organic carbon release is the rate-limiting step of rhizosphere priming in paddy soils[J]. Science of the Total Environment, 2024, 955: 176859. DOI:10.1016/j.scitotenv.2024.176859
(  0) 0) |
| [72] |
Keiluweit M, Bougoure J J, Nico P S, et al. Mineral protection of soil carbon counteracted by root exudates[J]. Nature Climate Change, 2015, 5(6): 588-595. DOI:10.1038/nclimate2580
(  0) 0) |
| [73] |
Shahbaz M, Kuzyakov Y, Sanaullah M, et al. Microbial decomposition of soil organic matter is mediated by quality and quantity of crop residues: Mechanisms and thresholds[J]. Biology and Fertility of Soils, 2017, 53(3): 287-301. DOI:10.1007/s00374-016-1174-9
(  0) 0) |
| [74] |
Schiedung M, Don A, Beare M H, et al. Soil carbon losses due to priming moderated by adaptation and legacy effects[J]. Nature Geoscience, 2023, 16(10): 909-914. DOI:10.1038/s41561-023-01275-3
(  0) 0) |
| [75] |
Huang W J, Hall S J. Elevated moisture stimulates carbon loss from mineral soils by releasing protected organic matter[J]. Nature Communications, 2017, 8: 1774. DOI:10.1038/s41467-017-01998-z
(  0) 0) |
| [76] |
Chen C M, Thompson A. Ferrous iron oxidation under varying pO2 levels: The effect of Fe(III)/Al(III)oxide minerals and organic matter[J]. Environmental Science & Technology, 2018, 52(2): 597-606.
(  0) 0) |
| [77] |
Handler R M, Frierdich A J, Johnson C M, et al. Fe(II)-catalyzed recrystallization of goethite revisited[J]. Environmental Science & Technology, 2014, 48(19): 11302-11311.
(  0) 0) |
| [78] |
Li X X, Sheng A X, Ding Y F, et al. A model towards understanding stabilities and crystallization pathways of iron(oxyhydr)oxides in redox-dynamic environments[J]. Geochimica et Cosmochimica Acta, 2022, 336: 92-103. DOI:10.1016/j.gca.2022.09.002
(  0) 0) |
| [79] |
Ye C L, Huang W J, Hall S J, et al. Association of organic carbon with reactive iron oxides driven by soil pH at the global scale[J]. Global Biogeochemical Cycles, 2022, 36(1): e2021GB007128. DOI:10.1029/2021GB007128
(  0) 0) |
| [80] |
Wen H Y, Yang F, Sun Z, et al. Asymmetric responses of soil organic carbon stability to shifting dominance of pH-mediated metal-bound organic carbon[J]. Communications Earth & Environment, 2025, 6: 574.
(  0) 0) |
| [81] |
Rasmussen C, Heckman K, Wieder W R, et al. Beyond clay: Towards an improved set of variables for predicting soil organic matter content[J]. Biogeochemistry, 2018, 137(3): 297-306. DOI:10.1007/s10533-018-0424-3
(  0) 0) |
| [82] |
Zhao X Q, Pan X Z, Ma H Y, et al. Scientific issues and strategies of acid soil use in China (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(5): 1248-1263. DOI:10.11766/trxb202307250290 [赵学强, 潘贤章, 马海艺, 等. 中国酸性土壤利用的科学问题与策略[J]. 土壤学报, 2023, 60(5): 1248-1263.]
(  0) 0) |
| [83] |
Fu H Y, Liu H T, Mao J D, et al. Photochemistry of dissolved black carbon released from biochar: Reactive oxygen species generation and phototransformation[J]. Environmental Science & Technology, 2016, 50(3): 1218-1226.
(  0) 0) |
| [84] |
Ma Z P, Cheng H F. Insights into the photochemical mechanism of goethite: Roles of different types of surface hydroxyl groups in reactive oxygen species generation and Fe(III)reduction[J]. Environmental Science & Technology, 2024, 58(33): 14812-14822.
(  0) 0) |
| [85] |
Yang S S, Ge X, Li Y Z, et al. Light-induced coupling process of Fe redox cycling and natural dissolved organic matters oxidative decomposition at goethite surface: Key role of reactive oxidative species[J]. Chemical Geology, 2022, 603: 120928. DOI:10.1016/j.chemgeo.2022.120928
(  0) 0) |
| [86] |
Wen Y L, Wu J L, Wen X T, et al. Exogenous iron mitigates photo-facilitation of soil organic matter[J]. Geochimica et Cosmochimica Acta, 2025, 395: 1-11.
(  0) 0) |
| [87] |
Chen H M, Abdulla H A N, Sanders R L, et al. Production of black carbon-like and aliphatic molecules from terrestrial dissolved organic matter in the presence of sunlight and iron[J]. Environmental Science & Technology Letters, 2014, 1(10): 399-404.
(  0) 0) |
| [88] |
Nguyen M L, Goldfarb J L, Plante A F, et al. Sorption temperature and the stability of iron-bound soil organic matter[J]. Geoderma, 2019, 341: 93-99. DOI:10.1016/j.geoderma.2019.01.040
(  0) 0) |
| [89] |
Ye C L, Chen D M, Hall S J, et al. Reconciling multiple impacts of nitrogen enrichment on soil carbon: Plant, microbial and geochemical controls[J]. Ecology Letters, 2018, 21(8): 1162-1173. DOI:10.1111/ele.13083
(  0) 0) |
| [90] |
Li Y, Chen Z M, Chen J, et al. Oxygen availability regulates the quality of soil dissolved organic matter by mediating microbial metabolism and iron oxidation[J]. Global Change Biology, 2022, 28(24): 7410-7427. DOI:10.1111/gcb.16445
(  0) 0) |
| [91] |
Wu Y T, Peng Z Y, Wang X, et al. Warmer climate reduces the carbon storage, stability and saturation levels in forest soils[J]. Earth's Future, 2025, 13(2): e2024EF004988. DOI:10.1029/2024EF004988
(  0) 0) |
| [92] |
Qin S Q, Chen L Y, Fang K, et al. Temperature sensitivity of SOM decomposition governed by aggregate protection and microbial communities[J]. Science Advances, 2019, 5(7): eaau1218. DOI:10.1126/sciadv.aau1218
(  0) 0) |
| [93] |
Georgiou K, Koven C D, Wieder W R, et al. Emergent temperature sensitivity of soil organic carbon driven by mineral associations[J]. Nature Geoscience, 2024, 17(3): 205-212. DOI:10.1038/s41561-024-01384-7
(  0) 0) |
| [94] |
Zhang Z R, Gao H, Gao X X, et al. Short-term warming supports mineral-associated carbon accrual in abandoned croplands[J]. Nature Communications, 2025, 16: 344. DOI:10.1038/s41467-024-55765-y
(  0) 0) |
| [95] |
Doetterl S, Berhe A A, Arnold C, et al. Links among warming, carbon and microbial dynamics mediated by soil mineral weathering[J]. Nature Geoscience, 2018, 11(8): 589-593. DOI:10.1038/s41561-018-0168-7
(  0) 0) |
| [96] |
Slessarev E W, Chadwick O A, Sokol N W, et al. Rock weathering controls the potential for soil carbon storage at a continental scale[J]. Biogeochemistry, 2022, 157(1): 1-13.
(  0) 0) |
| [97] |
Yang Y, Tilman D, Jin Z N, et al. Climate change exacerbates the environmental impacts of agriculture[J]. Science, 2024, 385(6713): eadn3747. DOI:10.1126/science.adn3747
(  0) 0) |
| [98] |
Wu S L, Konhauser K O, Chen B D, et al. "Reactive Mineral Sink" drives soil organic matter dynamics and stabilization[J]. NPJ Materials Sustainability, 2023, 1: 3. DOI:10.1038/s44296-023-00003-7
(  0) 0) |
| [99] |
Doetterl S, Berhe A A, Heckman K, et al. A landscape-scale view of soil organic matter dynamics[J]. Nature Reviews Earth & Environment, 2025, 6(1): 67-81.
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


