2. 国家林业局水土保持与荒漠化防治重点实验室, 北京 100083;
3. 北京林业大学水土保持学院, 重庆缙云山三峡库区森林生态系统国家定位观测研究站, 北京 100083
2. Key Laboratory of Soil and Water Conservation and Desertification Control, State Forestry Administration, Beijing 100083, China;
3. Jinyun Forest Ecosystem Research Station, School of Soil and Water Conservation, Beijing Forestry University, Beijing 100083, China
土壤有机碳库作为陆地生态系统中最大的活性碳库之一,在全球碳循环中扮演着不可或缺的角色[1]。耕地作为陆地生态系统的组成部分和人类赖以生存的基本自然资源,其土壤有机碳(Soil organic carbon,SOC)动态对于维持生态平衡与推动可持续发展具有关键意义。农业管理实践,如耕作方式、轮作制度及施肥策略等,均会显著影响SOC的积累与分解速率。此外,耕地SOC的变化不仅直接关系到土壤肥力与农业生产效率,还对温室气体排放模式及全球气候变化进程产生重要影响。因此,深入理解耕地SOC的来源、形成转化过程及其固存机制,对于评估陆地生态系统的碳汇功能和制定有效的气候缓解策略至关重要[2]。
传统观点认为,土壤有机碳的累积是植物残体逐级腐化的结果[3-4]。但是基于对土壤微生物代谢及其在土壤有机质转化和积累过程中的作用的分析,Liang等[5]和Angst等[6]提出了微生物碳泵(MCP)的概念体系,即土壤有机碳主要来源于植物残体和微生物代谢产物。土壤中的植物残体(木质素、纤维素和脂肪酸)具有不易分解的特性,会在土壤中不断积累并影响土壤碳库的稳定性[7-8]。随着近年来生物标志物方法的发展,学者们开始使用木质素酚作为土壤中植物源碳的生物标志物[9]。土壤中木质素来源的酚类单体包括香草基类(vanillyl phenols,V)、丁香基类(syringyl phenols,S)和肉桂基类(cinnamyl phenols,C),共8类化合物[10]。土壤微生物作为微生物碳泵概念体系的主体,其完整的生命周期使其在死亡后会生成大量的微生物残体碳并滞留在土壤中,从而增加土壤的碳储量。基于代谢状态可分为活体、休眠和死亡三类,其中死亡微生物遗留的细胞物质贡献了约56%的微生物源碳[11]。土壤微生物残体碳(由细胞膜碎片、酶类等组成)是土壤有机碳库的重要来源,但其直接量化仍面临技术挑战。微生物细胞壁成分的氨基糖因其化学稳定性成为关键生物标志物,其中可检测的氨基葡萄糖(Glucosamine,GlcN)、氨基半乳糖(Galactosamine,GalN)、氨基甘露糖(Mannosamine,ManN)和胞壁酸(Muramic acid,MurA)可特异性区分碳来源:GlcN主要来源于真菌的细胞壁,MurA只存在于细菌细胞壁中,GalN和ManN则是真菌和细菌共有。因此,可以通过GlcN来计算土壤真菌源碳,通过MurA来计算土壤细菌源碳[12]。
分布在山坡上、坡度大于2°的耕地被称为坡耕地,占国内耕地总量的28.35%。紫色土是中国特有的土壤类型,长江上游紫色土区域面积约为18万km2,该区域耕地主要是旱作坡耕地,占总耕地面积的60.8%[13]。紫色土以其独特的母质快速风化、低渗透性和较差的抗侵蚀能力而著称[14],并且由于其显著的破碎化特征,导致了该土壤类型的脆弱性[15]。此外,人类耕作活动进一步加剧了这一地区的水土流失。因此,长江上游坡耕地采取了大量坡改梯以防治水土流失,但该措施与作物类型的协同作用对当地坡耕地有机碳库及其组成的影响尚不明确。因此,本研究选取5种典型坡耕地为研究对象,通过氨基糖和木质素酚双生物标志物体系,比较不同类型坡耕地土壤有机碳库及其组成的差异,揭示坡改梯与作物类型对紫色土区坡耕地土壤有机碳库及其组成的影响,为探究有机碳来源和储存的微生物学机制、进一步完善微生物碳泵理论提供数据支撑。
1 材料与方法 1.1 研究区域研究区位于重庆市渝北区东河小流域(29°54′56.37″N,106°56′10.78″E),该地区属于亚热带湿润气候,年平均气温17.3℃;年平均降水量1 100 mm,主要集中在4—9月;年平均蒸发量864 mm,相对湿度81%。主要地貌类型为条状山脉与宽谷丘陵交互组成的平行岭谷,海拔560—1 034 m。土壤类型以紫色土为主。研究区内植被类型丰富,针叶林主要有杉木(Cunninghamia lanceolata)、马尾松(Pinus massoniana)等,阔叶林主要有木荷(Schima superba)、麻栎(Quercus acutissima)等,经济作物以玉米(Zea mays)和柑橘(Citrus reticulata)为主。
1.2 样品采集与处理2024年5月在东河小流域内选取玉米顺坡(Corn Slope,CoS)、玉米梯田(Corn Terracing,CoT)、柑橘顺坡(Citrus Slope,CiS)、柑橘梯田(Citrus Terracing,CiT)、玉米—柑橘套种梯田(Corn-Citrus Terracing,CoCiT)为研究对象,开展试验。每个研究样地选取三个采样点。采样时,去除地表枯落物,用容积为100 cm3的环刀分别采集0~10 cm和10~20 cm的分层土壤,当日测定土壤容重及含水率。每个取样点“S”形随机采集5点混匀,构成1个混合样本。将样品装入密封袋后置于4℃环境下送至实验室。
抵达实验室后,分离出植物根系和砾石,并用四分法将样品分为两份,一份直接过2 mm筛并冷藏,用于土壤氨基糖含量测定;另一份直接风干,风干后磨碎分别过2 mm、0.15 mm筛,用于测定土壤理化性质和土壤木质素酚含量。
1.3 土壤理化性质测定土壤容重(BD)用环刀法测定;土壤含水量(SWC)通过测定在105℃烘箱中干燥8 h后的质量损失来确定;土壤pH以土水比1︰2.5用pH计测定;土壤粒径采用马尔文激光粒度分析仪测定,根据美国农业部(United States Department of Agriculture,USDA)的土壤分类标准:土壤粒径 < 0.002 mm为黏粒,0.05~0.002mm为粉粒,2~0.05 mm为砂粒。
土壤有机碳(SOC)采用重铬酸钾氧化—外加热法测定;土壤颗粒态有机碳(POC)采用六偏磷酸钠浸提—重铬酸钾外加热法测定;矿质结合态有机碳(MAOC)采用间接法计算,用土壤有机碳量减去颗粒态有机碳量即为矿质结合态有机碳量;土壤微生物生物量碳(MBC)采用氯仿熏蒸—K2SO4提取进行测定,其中未熏蒸部分浸提液中的碳含量为可溶性有机碳(DOC)。
1.4 土壤木质素酚测定取适量样品至离心管中,分别加入1 g氧化铜和0.1 g硫酸亚铁铵,再加入20 mL 2 mol·L–1的氢氧化钠溶液,涡旋混匀5 min,在150℃条件下反应3 h,反应后的溶液转移至50 mL离心管中,加入5 mL去离子水超声清洗,使用6 mol·L–1盐酸将溶液pH调至1,在黑暗环境中静置1 h后离心,取出上清液加入乙酸乙酯溶液萃取3次,将所有上层有机相合并,在常温下使用氮气流吹至接近干燥状态,加入内标物,混合后再次使用氮气流吹干。加入0.1 mL衍生试剂(甲氧胺盐酸盐),在37℃下反应60 min,加入0.1 mL MSTFA溶液,在37℃下反应30 min,常温静置1 h后,取上清液在Agilent气相色谱系统(Agilent 7820,Agilent Technologies,USA)上机检测。SOC中植物来源有机碳的贡献P1根据下式计算:
| $ {P_1} = \frac{{\frac{V}{{33\% }} + \frac{S}{{90\% }} + C}}{{a \times {\text{SOC}}}} \times 100\% $ | (1) |
式中,V、S、C分别代表香草基类(vanillyl)、丁香基类(syringyl)和肉桂基类(cinnamyl)的木质素酚单体含量(mg·kg–1soil);33%、90%分别表示香草基类和丁香基类化合物被CuO的氧化效率,肉桂基类化合物的这一值为100%;a代表不同地块植被残体中木质素的平均含量,耕地中为8%[16]。
1.5 土壤氨基糖测定准确称量适量样品至50 mL离心管中,加入5 mL 6 mol·L–1盐酸溶液,在105℃条件下加热8 h。取500 μL样品在氮气流中吹干,加入1 mL超纯水溶解后离心取上清液,过0.22 μm滤膜过滤至样品瓶中,进行上机检测。采用Thermo ICS5000离子色谱系统(ICS5000,Thermo Fisher Scientific,USA),利用电化学检测器对单糖组分进行分析检测。测定的4种氨基糖,即氨基葡萄糖(GlcN)、氨基半乳糖(GalN)、氨基甘露糖(ManN)和胞壁酸(MurA)的总和为总氨基糖含量。细菌残体碳(BNC)、真菌残体碳(FNC)、微生物残体碳(MNC)的含量(g·kg–1),以及土壤有机碳中微生物来源有机碳的贡献P2计算方式如下:
| $ {\text{BNC}} = MurA \times 45 $ | (2) |
| $ {\text{FNC}} = \left( {\frac{{{\text{GlcN}}}}{{179.17}} - 2 \times \frac{{{\text{MurA}}}}{{251.23}}} \right) \times 179.17 \times 9 $ | (3) |
| $ {\text{MNC}} = {\text{BNC + FNC}} $ | (4) |
| $ {P_2} = \frac{{{\text{MNC}}}}{{{\text{SOC}}}} $ | (5) |
式中,179.17和251.23分别为GlcN和MurA的分子量;45为从MurA到细菌残体碳的转化因子,9为GlcN到真菌残体碳的转化因子[17]。
1.6 数据处理采用Excel、IBM SPSS Statistics 27对数据进行整理、统计和分析,利用R 4.4.1对数据进行作图。
2 结果 2.1 土壤有机碳含量及有机碳形态分布不同类型坡耕地土壤有机碳组分含量如表 2所示。不同类型坡耕地的0~10 cm土层中有机碳含量存在显著差异,柑橘坡改梯的两土层之间存在显著差异(P < 0.05);而10~20 cm土层中以及除柑橘梯田外的坡耕地两土层之间有机碳含量没有显著差异(P > 0.05)。同时,坡改梯均降低了土壤有机碳含量。玉米坡改梯相较于玉米顺坡,有机碳含量降低了45%~73%,而柑橘样地在实施坡改梯后,有机碳含量降低了12%~78%。同一土层中,坡改梯的坡耕地有机碳含量表现为:玉米柑橘套种梯田 > 玉米坡改梯 > 柑橘坡改梯。
|
|
表 1 样地土壤基本理化性质 Table 1 Basic physical and chemical properties of sample soils |
|
|
表 2 样地土壤有机碳含量及形态分布 Table 2 Soil organic carbon content and morphological distribution in sample sites |
不同类型坡耕地土壤中颗粒态有机碳(POC)和矿质结合态有机碳(MAOC)的含量也存在显著差异(P < 0.05),且随着坡改梯的实施而降低。玉米坡改梯相较于玉米顺坡,土壤POC的含量降低了20%~45%,而在柑橘坡改梯样地中,这一值降低了22%~61%;土壤MAOC含量在玉米坡改梯和柑橘坡改梯中,分别降低了53%~90%和18%~91%。在同一土层中,采取坡改梯的坡耕地POC含量表现为:玉米柑橘套种梯田 > 玉米坡改梯 > 柑橘坡改梯,且0~10 cm土层中玉米柑橘套种梯田和柑橘坡改梯之间存在显著差异(P < 0.05);MAOC含量表现为:玉米柑橘套种梯田 > 柑橘坡改梯 > 玉米坡改梯,三者之间不存在显著差异(P > 0.05)。玉米坡改梯10~20 cm土层的土壤微生物量碳(MBC)含量略微增加,但是其与同土层深度玉米顺坡土壤没有显著差异(P > 0.05);其余样地均表现为坡改梯降低了土壤MBC含量,但5个样地同土层之间以及各样地的两土层之间均不存在显著差异(P > 0.05)。
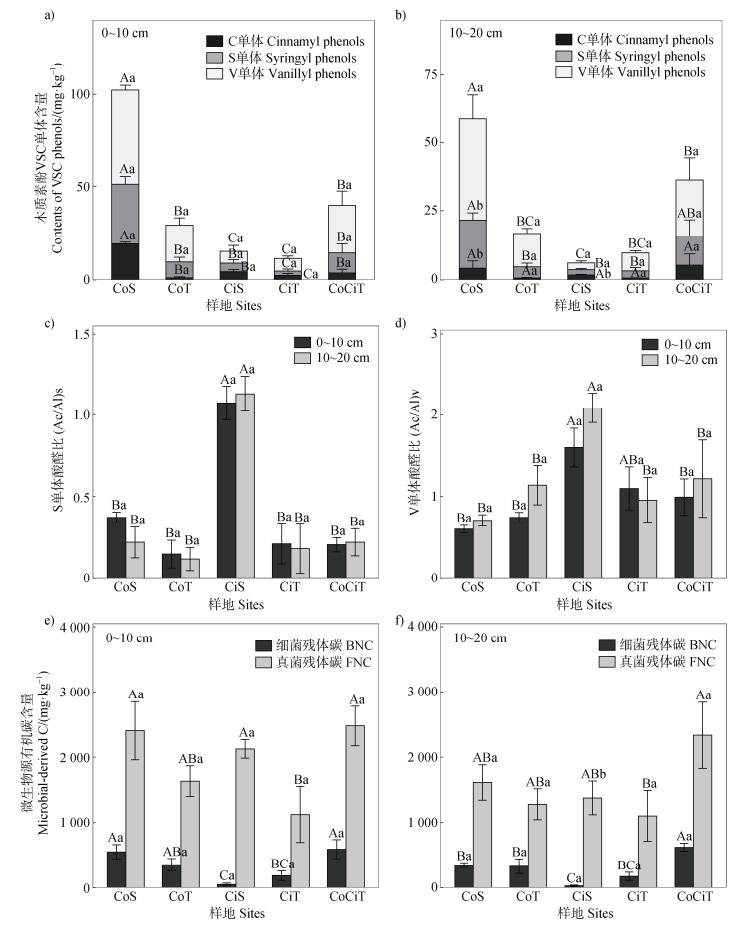
2.2 土壤木质素酚和氨基糖的积累特征不同类型坡耕地土壤木质素酚和氨基糖的积累特征如图 1所示。由图 1可知,不同类型坡耕地之间土壤木质素酚总量存在显著差异,在0~10 cm的土层中表现为玉米顺坡 > 玉米柑橘套种梯田 > 玉米坡改梯 > 柑橘顺坡 > 柑橘坡改梯,而在10~20 cm的土层中则表现为玉米顺坡 > 玉米柑橘套种梯田 > 玉米坡改梯 > 柑橘坡改梯 > 柑橘顺坡,且玉米顺坡显著高于其余样地(P < 0.05)。在各样地的木质素酚组分中,香草基类(V)单体均为主要成分,占木质素酚总量的39%~78%,且不同样地之间V单体的含量存在显著差异(P < 0.05),但是V单体在总木质素酚中的占比不存在显著差异(P > 0.05)。在0~10 cm土层中,玉米顺坡的丁香基类(S)单体和肉桂基类(C)单体含量显著高于其余样地,而其余4个样地之间不存在显著差异;在10~20 cm的土层中,玉米顺坡的S单体含量显著高于玉米坡改梯、柑橘顺坡以及柑橘坡改梯(P < 0.05),而5个样地的C单体含量不存在显著差异(P > 0.05)。木质素酚类化合物的氧化程度方面,S单体和V单体的氧化程度均为柑橘顺坡最高,0~10 cm和10~20 cm土层中,柑橘顺坡的(Ad/Al)s和(Ad/Al)v均显著高于其余样地(P < 0.05),其余样地之间以及各样地的两土层之间木质素酚的氧化程度相近,且无显著差异(P > 0.05)。
|
图 1 不同类型坡耕地木质素酚和氨基糖积累、氧化特征 Fig. 1 Characteristics of lignin phenol and amino sugar accumulation and oxidation in different types of sloping cultivated land |
由图 1可以得出,各样地微生物源有机碳的主要来源均为真菌残体碳,其占比为74.50%~98.88%,同时各样地两土层中真菌残体碳含量均表现为:玉米柑橘套种梯田 > 玉米顺坡 > 柑橘顺坡 > 玉米坡改梯 > 柑橘坡改梯;0~10 cm土层中,柑橘坡改梯的真菌残体碳含量显著低于前三个样地(P < 0.05),而10~20 cm土层中,柑橘坡改梯的真菌残体碳含量显著低于玉米柑橘套种梯田(P < 0.05)。与之相比,各样地两土层中细菌残体碳含量均表现为:玉米柑橘套种梯田 > 玉米顺坡 > 玉米坡改梯 > 柑橘坡改梯 > 柑橘顺坡,且柑橘顺坡的细菌残体碳含量显著低于前三个样地(P < 0.05)。
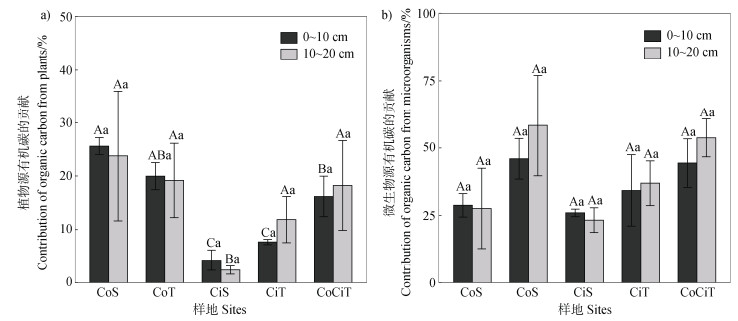
2.3 植物源和微生物源有机碳对土壤有机碳的贡献不同类型坡耕地植物源和微生物源有机碳对土壤有机碳的贡献如图 2所示。样地土壤植物源碳对土壤有机碳的贡献存在显著差异(P < 0.05)。在0~10 cm土层中,两柑橘样地的植物源碳贡献显著低于相同措施的玉米样地,顺坡和坡改梯样地分别较玉米对应样地降低了83.46%和61.61%;在10~20 cm土层中,两柑橘样地的植物源碳贡献也低于相同措施的玉米样地,但是只有柑橘顺坡与其余样地之间存在显著差异(P < 0.05)。微生物源碳方面,两顺坡样地均为0~10 cm土层微生物源碳贡献略高于10~20 cm土层,而其余坡改梯样地则相反;同时,两顺坡样地土壤微生物源碳贡献均低于坡改梯样地;但是不同样地的同一土层之间、同一样地的不同土层之间均不存在显著差异(P > 0.05)。
|
图 2 不同类型坡耕地植物源和微生物源有机碳对土壤有机碳的贡献 Fig. 2 Contribution of organic carbon from plant and microbial sources to soil organic carbon in different types of sloping cultivated land |
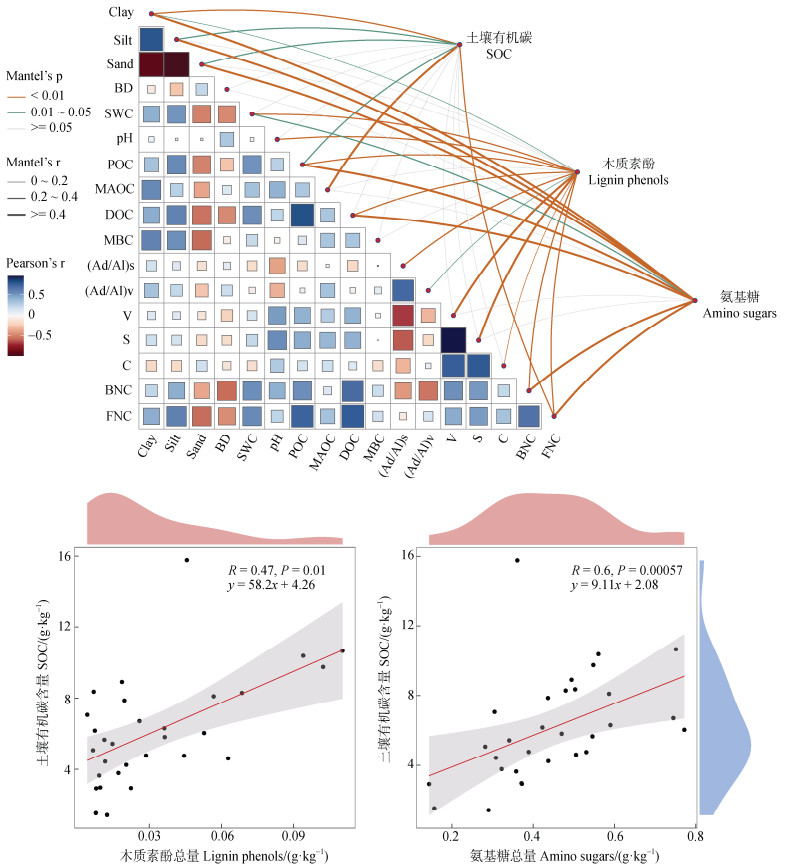
土壤有机碳库及其组成与各影响因子的相关性见图 3。由图 3可知,土壤机械组成、矿质结合态有机碳、真菌残体碳对土壤有机碳含量产生极显著影响(P < 0.01),颗粒态有机碳对土壤有机碳产生显著影响(P < 0.05);土壤含水量、pH、颗粒态有机碳、可溶性有机碳、香草基类单体的氧化程度对土壤木质素酚含量产生极显著影响(P < 0.01),土壤机械组成、丁香基类单体的氧化程度对其产生显著影响(P < 0.05);土壤机械组成、颗粒态有机碳、可溶性有机碳、细菌残体碳、真菌残体碳对土壤氨基糖含量存在极显著影响(P < 0.01),土壤含水量对其存在显著影响(P < 0.05)。同时,土壤总有机碳与土壤木质素酚含量和氨基糖含量分别呈极显著正相关性(P < 0.01)。
|
注:Clay,Silt,Sand分别为土壤黏粒、粉粒、砂粒;BD为土壤容重;SWC为土壤含水量;POC,MAOC,DOC,MBC分别为颗粒态有机碳、矿质结合态有机碳、可溶性有机碳、微生物生物量碳;(Ad/Al)s,(Ad/Al)v分别为木质素酚S和V单体的氧化程度;BNC,FNC分别为细菌残体碳和真菌残体碳含量。 Note:Clay,Silt,Sand are soil clay,silt,and sand contents,respectively;BD is soil bulk density;SWC is soil water content;POC,MAOC,DOC,MBC are particulate organic carbon,mineral-bound organic carbon,soluble organic carbon,and microbial biomass carbon contents,respectively;(Ad/Al)s,(Ad/Al)v are the oxidation degree of lignin phenol S and V monomers,respectively;BNC,FNC are bacterial residual carbon and fungal residual carbon contents,respectively;BNC,FNC are bacterial residual carbon and fungal residual carbon contents,respectively. Oxidation degree:BNC,FNC are the bacterial residue carbon and fungal residue carbon content,respectively. 图 3 土壤有机碳库及其组成与各影响因子相关性 Fig. 3 Correlation of soil organic carbon pools and their composition with various impact factors |
本研究发现,相较于玉米顺坡种植,实施坡改梯后,土壤有机碳(SOC)含量显著下降了45%至73%;而在柑橘样地中,这一降幅范围为12%至78%。进一步分析显示,作为土壤碳库的重要组成部分,颗粒态有机碳(POC)和矿质结合态有机碳(MAOC)的含量同样受到了坡改梯这一措施的显著影响。具体而言,坡改梯导致POC减少了20%~61%,MAOC含量降低了18%~91%。这表明尽管坡改梯是一种有效的水土保持措施,但它对紫色土坡耕地土壤碳储量产生了负面影响。这与张玥等[18]和Chen等[19]的研究结果一致,即修建年限不足5年的梯田固碳效益呈现下降趋势,这段时间内土壤SOC的含量会低于坡耕地。原因在于梯田建设过程中带来的土壤扰动会混合不同土层的土壤,土壤微生物群落因此发生改变,进而增加土壤呼吸,加速SOC的分解。周萍等[20]对我国南方三种水稻田有机碳积累机制的研究指出,SOC含量在粉粒和黏粒中最高;而在本研究中,不同类型坡耕地SOC含量与土壤黏粒占比之间存在极显著正相关关系,说明土壤黏粒的结合保护能力影响紫色土区土壤有机碳的固持。但是在MAOC方面,黏粒和粉粒占比最小的柑橘坡改梯土壤,其MAOC含量高于玉米坡改梯,这一结果与牟凌等[21]的研究结果相符。推测原因为玉米坡改梯样地通常会采取翻耕、清除地被物等方法来维持植物生长,因此直接或间接影响土壤微生物群落组成,而土壤微生物组成,尤其是真菌含量又与MAOC含量息息相关[22]。此外,也有研究指出,南方稻作梯田中影响有机碳固持能力的因素是团聚体的物理保护能力而不是黏粒的结合保护能力[23];同时,匡艳云等[24]指出,团聚体稳定性与微生物残体碳之间呈显著正相关。本研究中并没有对不同类型坡耕地土壤团聚体进行测定,此后的研究可以进行相关试验,进一步补充团聚体对土壤有机碳固持能力的影响。
3.2 坡改梯对土壤植物源碳和微生物源碳积累的影响本研究中土壤木质素酚含量受坡改梯的影响显著,尤其是在0~10 cm土层中,不同作物顺坡样地的木质素酚含量均高于坡改梯样地,推测是由于坡改梯更易于截留坡耕地的叶凋落物,而叶凋落物的积累导致土壤有机碳矿化失稳。Fontaine等[25]和Wang等[26]的研究指出,叶凋落物中含有更多纤维素、多糖等不稳定化合物,是有机质矿化的有效底物,且其有利于微生物合成降解高抗性化合物的胞外酶,刺激微生物生长,从而引发正激发效应。此外,叶凋落物的输入也会破坏团聚体对土壤有机碳的物理保护,进一步加剧正激发效应[27]。
木质素酚不同单体之间的比值,不仅可以表征土壤有机碳的植物来源,也可以表示土壤中木质素的降解程度。被子植物、裸子植物和非维管植物的残体中,V、S、C的单体含量差异较大。被子植物中含有V、S、C三种单体,而裸子植物中没有S单体,所以土壤中的S/V、C/V值会由于植被的不同而有所差异,从而可以推算出土壤有机碳的植物来源[28]。此外,土壤有机碳在降解过程中,降解化合物的氧化反应会使V、S单体中的羧酸含量增加,而醛含量减少,进而导致酸醛比逐渐增加[29]。因此,通过土壤中V和S单体的酸醛比可以得到木质素在土壤中的氧化程度。本研究中柑橘顺坡样地的V和S单体的酸醛比均显著高于其余样地,这说明柑橘顺坡的土壤有机碳降解程度是5个样地中最高的,而其余4个样地的土壤有机碳降解程度相差无几。
本研究中微生物源碳对土壤总有机碳的贡献占比为20.9%~84.6%,这与前人的研究结果类似[30-31],也表明微生物残体碳在土壤有机碳固存和稳定过程中的重要性。同时,本研究发现,真菌残体碳对SOC的贡献(7.8%~70.7%)高于细菌残体碳(0.2%~13.9%),这也与以往的研究结果相似[32-33],其原因可能为:首先,细菌细胞壁主要成分为肽聚糖,相较于真菌细胞壁,肽聚糖更容易被分解,因此细菌残体碳对SOC的贡献率更低[34];其次,真菌的微生物碳利用效率(CUE)普遍高于细菌,因此真菌的生物量会高于细菌,从而导致其残体碳积累高于细菌[35]。同时各样地真菌残体碳含量方面,玉米柑橘套种梯田最高,玉米和柑橘样地均表现为坡改梯样地低于顺坡样地,但细菌残体碳含量略有不同。这表明单一作物种植模式下,坡改梯降低了土壤中真菌含量,其对土壤细菌含量的影响因作物的不同而存在差异,这与胡漫等[36]的研究结果类似;而在坡改梯套种模式下,土壤真菌和细菌含量相较单一作物种植模式均有所提升。
4 结论不同类型坡耕地中SOC、POC、MAOC的含量均会随坡改梯的实施而降低。坡改梯会显著降低玉米样地的总木质素酚含量,也会显著降低柑橘样地木质素酚的氧化程度。各样地微生物源有机碳的主要来源均为真菌残体碳,其占比为74.50%~98.88%,且在单一作物种植模式下,坡改梯会降低土壤中真菌残体碳含量。建议紫色土区后续坡改梯工程实施过程中,采取分层施工的方式,避免扰动不同土层的土壤微生物群落;同时,在梯田边缘或田埂种植深根系植物,修建植物篱,利用根系分泌物和凋落物形成局部碳富集区。
| [1] |
Lal R, Monger C, Nave L, et al. The role of soil in regulation of climate[J]. Philosophical Transactions of the Royal Society of London Series B, Biological Sciences, 2021, 376(1834): 20210084. DOI:10.1098/rstb.2021.0084
(  0) 0) |
| [2] |
Stockmann U, Adams M A, Crawford J W, et al. The knowns, known unknowns and unknowns of sequestration of soil organic carbon[J]. Agriculture, Ecosystems & Environment, 2013, 164: 80-99.
(  0) 0) |
| [3] |
Dou S, Shan J, Song X Y, et al. Are humic substances soil microbial residues or unique synthesized compounds?A perspective on their distinctiveness[J]. Pedosphere, 2020, 30(2): 159-167. DOI:10.1016/S1002-0160(20)60001-7
(  0) 0) |
| [4] |
Simpson A J, Kingery W L, Hayes M H, et al. Molecular structures and associations of humic substances in the terrestrial environment[J]. Naturwissenschaften, 2002, 89(2): 84-88. DOI:10.1007/s00114-001-0293-8
(  0) 0) |
| [5] |
Liang C, Schimel J P, Jastrow J D. The importance of anabolism in microbial control over soil carbon storage[J]. Nature Microbiology, 2017, 2: 17105. DOI:10.1038/nmicrobiol.2017.105
(  0) 0) |
| [6] |
Angst G, Mueller K E, Nierop K G J, et al. Plant- or microbial-derived A review on the molecular composition of stabilized soil organic matter[J]. Soil Biology and Biochemistry, 2021, 156: 108189. DOI:10.1016/j.soilbio.2021.108189
(  0) 0) |
| [7] |
Crow S E, Lajtha K, Filley T R, et al. Sources of plant-derived carbon and stability of organic matter in soil: Implications for global change[J]. Global Change Biology, 2009, 15(8): 2003-2019. DOI:10.1111/j.1365-2486.2009.01850.x
(  0) 0) |
| [8] |
Dai G H, Zhu S S, Cai Y, et al. Plant-derived lipids play a crucial role in forest soil carbon accumulation[J]. Soil Biology and Biochemistry, 2022, 168: 108645. DOI:10.1016/j.soilbio.2022.108645
(  0) 0) |
| [9] |
Ma T, Zhu S S, Wang Z H, et al. Divergent accumulation of microbial necromass and plant lignin components in grassland soils[J]. Nature Communications, 2018, 9: 3480. DOI:10.1038/s41467-018-05891-1
(  0) 0) |
| [10] |
Thevenot M, Dignac M F, Rumpel C. Fate of lignins in soils: A review[J]. Soil Biology and Biochemistry, 2010, 42(8): 1200-1211. DOI:10.1016/j.soilbio.2010.03.017
(  0) 0) |
| [11] |
Cotrufo M F, Wallenstein M D, Boot C M, et al. The Microbial Efficiency-Matrix Stabilization(MEMS)framework integrates plant litter decomposition with soil organic matter stabilization: Do labile plant inputs form stable soil organic matter[J]. Global Change Biology, 2013, 19(4): 988-995. DOI:10.1111/gcb.12113
(  0) 0) |
| [12] |
Zhang B, Chen Q, Ding X L, et al. Research progress on accumulation, turnover and stabilization of microbial residues in soil (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(6): 1479-1491. DOI:10.11766/trxb202012270705 [张彬, 陈奇, 丁雪丽, 等. 微生物残体在土壤中的积累转化过程与稳定机理研究进展[J]. 土壤学报, 2022, 59(6): 1479-1491.]
(  0) 0) |
| [13] |
Gao Y, Xu Y J, Chen W L, et al. Changes and coupling of C and N in hillslope cropland of purple soil and microbial biomass (In Chinese)[J]. Acta Scientiae Circumstantiae, 2014, 34(7): 1794-1800. [高扬, 徐亚娟, 陈维梁, 等. 紫色土坡耕地C、N与微生物C、N变化及其耦合特征[J]. 环境科学学报, 2014, 34(7): 1794-1800.]
(  0) 0) |
| [14] |
Li S, Tian Y, Luo X M, et al. Effects of rainfall on soil erosion, nitrogen and phosphorus loss from sloping cultivated land in the hilly area of central Sichuan (In Chinese)[J]. Environmental Science & Technology, 2024, 47(12): 161-168. [李森, 田耘, 罗雪梅, 等. 降雨对川中丘陵区坡耕地土壤侵蚀和氮磷流失的影响[J]. 环境科学与技术, 2024, 47(12): 161-168.]
(  0) 0) |
| [15] |
He L D, Wu Y, Tian Y, et al. Influence of collapse deposits on nutrient content of purple soil (In Chinese)[J]. Bulletin of Soil and Water Conservation, 2024, 44(4): 66-76. [何林东, 吴勇, 田耘, 等. 崩塌堆积物对紫色土养分含量的影响[J]. 水土保持通报, 2024, 44(4): 66-76.]
(  0) 0) |
| [16] |
Lin Q L, Tian Q X, Liao C, et al. Persistence of soil microbial residuals and lignin phenols in forest ecosystems along the latitude gradient[J]. Journal of Soils and Sediments, 2024, 24(6): 2425-2436. DOI:10.1007/s11368-024-03794-x
(  0) 0) |
| [17] |
Qin Z K, Liu R H, He P, et al. Effects of mixed broadleaved tree species with pure Pinus massoniana plantation on soil microbial necromass carbon and organic carbon fractions (In Chinese)[J]. Chinese Journal of Applied Ecology, 2024, 35(1): 141-152. [覃振凯, 刘润红, 何鹏, 等. 马尾松纯林混交改造对土壤微生物残体碳和有机碳组分的影响[J]. 应用生态学报, 2024, 35(1): 141-152.]
(  0) 0) |
| [18] |
Zhang Y, Guo X F, Han J Q, et al. Preliminary estimation of soil carbon sequestration benefits of terrace construction on the Loess Plateau in the past nearly 40 years (In Chinese)[J]. Journal of Soil and Water Conservation, 2024, 38(4): 190-197. [张玥, 郭学锋, 韩剑桥, 等. 黄土高原近40年梯田建设的土壤固碳效益初步估算[J]. 水土保持学报, 2024, 38(4): 190-197.]
(  0) 0) |
| [19] |
Chen D, Wei W, Daryanto S, et al. Does terracing enhance soil organic carbon sequestration A national-scale data analysis in China[J]. Science of the Total Environment, 2020, 721: 137751. DOI:10.1016/j.scitotenv.2020.137751
(  0) 0) |
| [20] |
Zhou P, Song G H, Pan G X, et al. SOC Accumulation in three major types of paddy soils under long-term agro-ecosystem experiments from south China Ⅰ. Physical protection in soil micro-aggregates (In Chinese)[J]. Acta Pedologica Sinica, 2008, 45(6): 1063-1071. [周萍, 宋国菡, 潘根兴, 等. 南方三种典型水稻土长期试验下有机碳积累机制研究Ⅰ. 团聚体物理保护作用[J]. 土壤学报, 2008, 45(6): 1063-1071.]
(  0) 0) |
| [21] |
Mou L, Wu H L, Gu G J, et al. Soil microbes and enzyme activities in four vegetation types in Yunnan karst faulted basin (In Chinese)[J]. Chinese Journal of Applied and Environmental Biology, 2020, 26(5): 1081-1086. [牟凌, 吴宏蕾, 顾国军, 等. 云南岩溶断陷盆地4种植被类型土壤微生物和酶活性特征[J]. 应用与环境生物学报, 2020, 26(5): 1081-1086.]
(  0) 0) |
| [22] |
Cao Z C, Cheng S L, Fang H J, et al. Responses of soil organic carbon dynamics and microbial community structure to organic nitrogen fertilization in the temperate needlebroadleaved mixed forest (In Chinese)[J]. Acta Pedologica Sinica, 2020, 57(4): 963-974. DOI:10.11766/trxb201908130350 [曹子铖, 程淑兰, 方华军, 等. 温带针阔叶林土壤有机碳动态和微生物群落结构对有机氮添加的响应特征[J]. 土壤学报, 2020, 57(4): 963-974.]
(  0) 0) |
| [23] |
Han Y, Zhao Z, Tian J, et al. Characterization of organic carbon pool and the source of paddy soil from typical rice terraces across southern China (In Chinese)[J]. Journal of Agricultural Resources and Environment, 2025, 42(1): 139-148. [韩玥, 赵正, 田静, 等. 中国南方典型稻作梯田土壤有机碳积累及其来源表征[J]. 农业资源与环境学报, 2025, 42(1): 139-148.]
(  0) 0) |
| [24] |
Kuang Y Y, Hu H, Li S, et al. The relationship between microbial necromass carbon and soil aggregate stability on a global scale (In Chinese)[J]. Acta Pedologica Sinica, 2025. DOI:10.11766/trxb202409030355 [匡艳云, 胡汗, 李森, 等. 全球尺度上微生物残体碳与土壤团聚体稳定性的关系[J]. 土壤学报, 2025.]
(  0) 0) |
| [25] |
Fontaine S, Barot S, Barré P, et al. Stability of organic carbon in deep soil layers controlled by fresh carbon supply[J]. Nature, 2007, 450(7167): 277-280. DOI:10.1038/nature06275
(  0) 0) |
| [26] |
Wang Y B, Hu X D, Yu S X, et al. Soil conservation of sloping farmland in China: History, present, and future[J]. Earth-Science Reviews, 2024, 249: 104655. DOI:10.1016/j.earscirev.2023.104655
(  0) 0) |
| [27] |
Shahbaz M, Kuzyakov Y, Heitkamp F. Decrease of soil organic matter stabilization with increasing inputs: Mechanisms and controls[J]. Geoderma, 2017, 304: 76-82. DOI:10.1016/j.geoderma.2016.05.019
(  0) 0) |
| [28] |
Wan X H, Huang Z Q. Application of plant biomarkers to studying carbon cycling in forest soil systems (In Chinese)[J]. Acta Pedologica Sinica, 2013, 50(6): 1207-1215. DOI:10.11766/trxb201301110023 [万晓华, 黄志群. 植物标志物在森林土壤碳循环研究中的应用[J]. 土壤学报, 2013, 50(6): 1207-1215.]
(  0) 0) |
| [29] |
Jex C N, Pate G H, Blyth A J, et al. Lignin biogeochemistry: From modern processes to Quaternary archives[J]. Quaternary Science Reviews, 2014, 87: 46-59. DOI:10.1016/j.quascirev.2013.12.028
(  0) 0) |
| [30] |
Wang B R, An S S, Liang C, et al. Microbial necromass as the source of soil organic carbon in global ecosystems[J]. Soil Biology and Biochemistry, 2021, 162: 108422. DOI:10.1016/j.soilbio.2021.108422
(  0) 0) |
| [31] |
Shao P S, Liang C, Lynch L, et al. Reforestation accelerates soil organic carbon accumulation: Evidence from microbial biomarkers[J]. Soil Biology and Biochemistry, 2019, 131: 182-190. DOI:10.1016/j.soilbio.2019.01.012
(  0) 0) |
| [32] |
Gao W T, Wang Q T, Zhu X M, et al. The vertical distribution pattern of microbial- and plant-derived carbon in the rhizosphere in alpine coniferous forests[J]. Rhizosphere, 2021, 20: 100436. DOI:10.1016/j.rhisph.2021.100436
(  0) 0) |
| [33] |
Liu X Y, Tao Y L, Wang Y P, et al. Changes in plant- and microbial-derived soil organic carbon in three temperate mature forests (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(6): 1828-1838. [刘新颖, 陶玉兰, 王延平, 等. 三种温带成熟林土壤植物源和微生物源有机碳的变化[J]. 土壤学报, 2025, 62(6): 1828-1838.]
(  0) 0) |
| [34] |
Kögel-Knabner I. The macromolecular organic composition of plant and microbial residues as inputs to soil organic matter[J]. Soil Biology and Biochemistry, 2002, 34(2): 139-162. DOI:10.1016/S0038-0717(01)00158-4
(  0) 0) |
| [35] |
Luo R Y, Kuzyakov Y, Zhu B, et al. Phosphorus addition decreases plant lignin but increases microbial necromass contribution to soil organic carbon in a subalpine forest[J]. Global Change Biology, 2022, 28(13): 4194-4210. DOI:10.1111/gcb.16205
(  0) 0) |
| [36] |
Hu M, Zeng Q C, Zhou Q, et al. Study on the coupling mechanism between soil bacterial community diversityand ecosystem multifunctionality in intensive citrus cultivation systems (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(4): 1197-1209. [胡漫, 曾全超, 周全, 等. 集约化种植柑橘土壤细菌群落多样性与生态系统多功能性的耦合机制研究[J]. 土壤学报, 2025, 62(4): 1197-1209.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


