土壤微生物对生物地球化学循环和生态系统可持续发展至关重要[1],然而土壤微生物组的物种多样性复杂、功能多样性高,这使得利用微生物的功能特征对其进行分类或分组的研究极具挑战性[2]。在植物和动物生态学研究中,生态学家通过生活史策略(Life history strategy)描述资源受限情况下生物个体在生长和繁殖等特征之间进行适应性权衡的对策;而在微生物生态学中,微生物的功能特征以微生物生理代谢为核心,不仅决定了微生物对不同环境的生存和适应性特征,也为利用微生物功能特征预测未来环境变化提供了可能性[3]。因此,针对微生物物种与功能复杂多样的特性,将不同微生物性状分解成为一个或多个维度,捕捉微生物在不同性状维度之间的转换特征,从而进行广泛的微生物“投资策略”比较,对解析微生物的环境适应性特征及预测其对全球生态系统的潜在影响具有重要的意义[4-5]。
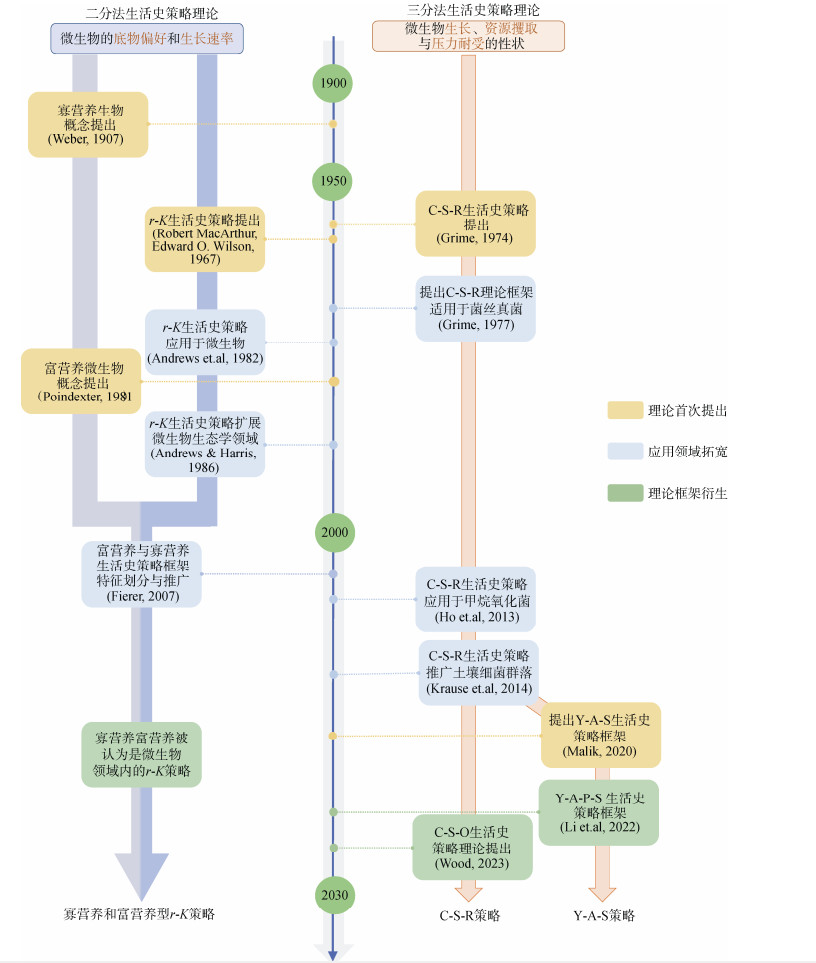
微生物学和生态学等领域的研究人员已经根据微生物个体及群落的不同“投资策略”提出了多种生活史策略理论框架(图 1),主要包括二分法和三分法[6-7]。其中,二分法框架将微生物分为r策略者和K策略者,以及富营养和寡营养微生物;而三分法框架主要包括C-S-R(Competitive,Stress-tolerant,Ruderal)模型[7]与Y-A-S(High yield,Resource acquisition,Stress tolerance)模型[6]及其衍生模型[8-9]。这些分类理论研究不仅填补了微生物行为与生态系统功能之间的理论空白,深化了人们对微生物生态功能的理解,还为农业可持续发展提供了科学依据。
|
图 1 微生物生活史策略分类的重要理论及其发展过程 Fig. 1 Milestones for the development of life history strategy theoretical framework |
然而,目前针对土壤微生物生活史策略的研究仍集中于发展分类理论,对微生物功能性状的研究仍局限于静态观测的识别和分类阶段,缺乏对微生物功能在不同性状维度之间转换的调控机理研究。因此,本文重点梳理了土壤微生物生活史策略理论框架的发展和应用进展,包括:(1)微生物生活史策略的理论发展过程;(2)生活史策略二分法的内涵与应用;(3)生活史策略三分法的内涵与应用。在此基础上,提出需要推动微生物生活史策略研究从“静态观测”向“动态监测”,从“识别分类”向“定向调控”的跨越,进一步优化现有生活史策略理论框架,以期将微生物策略分类从理论工具转化为解决土壤健康和农业可持续性等实际问题的核心手段。
1 微生物生活史策略的发展生活史策略理论框架中最经典的寡营养-富营养微生物分类和r-K生活史策略理论是基于微生物个体底物代谢和生长特征的区分方法(图 1)。其中寡营养微生物(oligotrophy)的概念是1907年提出的[10],该类群的特点是能够在低浓度营养底物下生长,具有较高的底物利用效率,生长速率较为缓慢,对资源可利用性变化的响应较小[11];而富营养微生物(copiotrophy)的概念是1981年提出[12-13],该类群生长更为迅速,对碳源可利用性的变化更加敏感[14]。与寡营养和富营养微生物概念同时发展的r-K生活史策略理论是由MacArthur和Wilson[15]于1967年首次提出的,用于理解岛屿生物多样性形成特征,其中r代表内禀增长率,而K代表环境负载量,是一个二分连续体理论框架。1970年,美国生态学家Pianka[16]在此基础上将r-K生活史策略框架扩展到一切有机体,并进一步提出了r/K策略者的特征,其中r策略者生长在不稳定的环境中,以快速的生长与繁殖为主要特征;而K策略者生活在相对稳定的环境中,在获取资源、竞争能力和生存方面更具优势。该r-K策略理论框架至1982年才被首次应用到微生物学研究中,主要针对植物病原菌的侵染策略[17-18];随后于1986年进一步扩展至微生物生态学领域,用于解释土壤微生物对资源波动的响应[19]。总体而言,尽管微生物富营养-寡营养分类与r-K生活史策略分类的起源不同,其概念也不完全相同,但富营养微生物的“投资策略”与r策略者类似,寡营养微生物的“投资策略”与K策略者类似。Fierer等[20]于2007年通过实验分析结合大尺度调研将土壤细菌的r-K生活史策略与传统的底物偏好性联系起来,用富营养与寡营养的概念来描述典型的r和K生活史策略的微生物,将生活史策略应用于广泛的土壤细菌类群。因此,近年来微生物生态学的许多研究通常将r-K生活史策略微生物与富营养-寡营养微生物作为同一概念[21]。
与生活史策略理论的二分法框架同步发展的还有三分法框架。1974年,Grime[22]以植物的生活史策略权衡为基础提出了最初的C-S-R理论框架,该框架针对植物群落的功能性状进行分类,综合考虑了植物生长、资源竞争与压力耐受等生活策略。虽然三分法框架提出时间较早,但这一理论框架直至2013年才被应用至细菌群落研究中[7],该研究针对甲烷氧化菌群落中的不同类群,将其功能性状归类为C策略者和S策略者。随后Krause等[23]于2014年将这一分类方式推广至土壤微生物群落,其中C策略微生物可以快速占用环境中的可利用资源,S策略微生物可以在不利的环境条件或选择压力下存活,R策略微生物可以在高度干扰的环境促进群落重建。随着基因组学技术进步,基于微生物群落生活史策略的三分法框架也逐渐得到发展。2018年,Wood等[24]基于16S rRNA基因测序数据,将根际微生物群落不同的代谢通路划分为不同的生活史策略,并将微生物的觅食策略(Foragin,F策略)加入C-S-R框架,将该框架拓展为C-S-R-F理论框架。为了更契合微生物在不同非生物胁迫和资源丰富度条件下的能量投资策略,Malik等[6]在C-S-R-F框架的基础上提出了微生物Y-A-S生活史策略框架,其中Y策略微生物可以降低耐受胁迫和资源获取过程中的能量消耗,最大限度地提高生物量积累效率;A策略微生物优先满足资源获取过程的能量投资;S策略微生物优先满足环境压力耐受过程的能量投资。C-S-R策略和Y-A-S策略这两个三分法框架在土壤微生物生态学研究领域均有广泛的应用和发展,并形成了多种衍生理论,例如Wood等[8]以C-S-R框架为基础提出了C-S-O(Competitors,Stress- tolerators,Opportunist)框架,而Li等[9]则对Y-A-S框架进行了补充,增加了细胞生长潜力维持策略(Cellular and high growth potential maintenance strategy,P策略),提出了Y-A-P-S理论框架。
2 生活史策略二分法理论框架的内涵及其应用虽然寡营养与富营养微生物生活史策略普遍被认为是微生物r-K策略的衍生,但其实寡营养微生物的概念诞生远早于富营养微生物以及r-K生活史策略,这可能是在土壤与海洋等生态系统中通常由生长缓慢的寡营养细菌主导,导致环境微生物的早期研究以寡营养类群为主[25–27]。随着富营养微生物概念提出,不同养分条件下截然不同的生长速度成为区分富营养与寡营养细菌的重要指标,这一特征与r-K二分法框架的理念有一定重合。
2.1 二分法框架的内涵及其分类依据微生物r策略者能依靠极高繁殖速率与较短寿命占据干扰较大的生态环境中的生态位优势,而K策略者具有较长寿命与较强的适应性,能在稳定的生态环境中占据优势。因此r-K二分法框架往往以微生物的繁殖速率、微生物的个体大小等特征作为分类依据。近期也有研究表明,微生物基因组中鸟嘌呤与胞嘧啶(GC碱基)含量可能与微生物在r-K策略之间的权衡相关,r策略者较小的细胞体积与较快繁殖的能力与微生物基因组中较高的GC含量有关;而K策略者代谢成本更高、细胞体积更大,其基因组中往往GC含量较低,因此也有研究将基因组中的GC含量作为r/K策略者的分类依据之一[28]。
相比之下,富营养与寡营养二分法框架则更关注微生物的生理性状,通过微生物的底物代谢亲和力与微生物生长特征进行分类,一类为在资源匮乏且底物较难分解环境中缓慢生长的寡营养微生物,另一类则是在资源丰富且具有多种不同可利用的底物环境中占据优势的富营养微生物。研究表明富营养微生物往往富集了易利用碳源代谢相关的基因,而寡营养微生物则富集了难利用碳源代谢相关的基因[29-30]。此外,微生物的基因组大小、rRNA操纵子拷贝数(rrn拷贝数)、微生物信号转导与转录机制等能够反应其获取和利用资源能力的固有特征,这些特征也常被作为富营养与寡营养微生物的分类依据[31-32]。例如富营养微生物往往具有较高的rrn拷贝数,而寡营养微生物的rrn拷贝数通常较低[33]。
与细菌相比,真菌通常能利用复杂的碳源且生长速度较慢,因此具有更多的寡营养/K策略者的特征[34]。然而,真菌群落的不同类群也可以区分为富营养和寡营养真菌[35]。富营养型真菌的孢子会根据环境中资源的可利用性进行萌发或休眠,这些真菌往往生命周期较短,可以通过产生传播性孢子,重新定殖在资源丰富的环境中,或通过产生休眠孢子留在原始环境中,直到资源满足生长条件[36]。寡营养真菌则具有降解复杂聚合物的能力,部分寡营养真菌也可以从空气中获得营养物质,从而在资源较匮乏的环境中生长[37]。
总体而言,r-K策略二分法是以环境容量及环境干扰下微生物的生长速率作为区分微生物生活史策略的方式,而富营养与寡营养二分法则侧重环境中碳源可利用性与微生物的代谢能力。因此,二分法理论框架代表了微生物群落在生长速率与资源利用效率之间的基本权衡[38-39],其中r策略/富营养微生物通常具有较快的生长速度、在资源丰富的条件下占据优势,而K策略/寡营养微生物则更擅长在资源有限的环境中进行高效资源利用和竞争[40]。这两个框架均考虑了不同环境下微生物的生存策略,为描述复杂环境中微生物群落生活史策略提供了理论依据。
最初对于土壤微生物群落生活史策略的研究主要是依据纯培养获得的已知微生物的代谢与繁殖特征,并与土壤环境中微生物群落的16S rRNA基因数据或磷脂脂肪酸分析(Phospholipid Fatty Acids,PLFA)获得的微生物群落组成数据结合对土壤环境状态进行推测[41]。例如,革兰氏阳性菌(Gram Positive,G+)的生长速度通常较革兰氏阴性菌(Gram Negative,G-)缓慢[42]。PLFA中G+的生物量可以用i14︰0,i15︰0,a15︰0,i16︰0,i17︰0,a17︰0等一系列脂肪酸的总量来估算,而G-的生物量可以用16︰1ω5,16︰1ω7t,16︰1ω9,cyl7︰0,18︰1ω5等一系列的脂肪酸总量来估算[43]。因此,计算不同类型脂肪酸的含量比,可以表征土壤中的G+/G-比。此外,酸杆菌门(Acidobacteria)与放线菌门(Actinobacteria)可以在低资源有效性的环境中维持正常生长[44],而变形菌门(Proteobacteria)和拟杆菌门(Bacteroidetes)则在资源丰富的环境中更具优势[45-46]。很多基于16S rRNA基因扩增子测序的研究通过计算土壤中酸杆菌门与变形菌门[47]、放线菌门与拟杆菌门[48]以及富营养微生物(β-变形菌、拟杆菌门)与寡营养微生物(酸杆菌门)相对丰度的比例[42]来表征农田、草地、森林等土壤生态系统中土壤微生物的生活史策略特征。
2.2 二分法框架在土壤微生物群落研究中的应用土壤中的养分状态可能影响环境微生物生活史策略。热带雨林土壤中通过人为控制凋落物的输入提高土壤中有机碳的含量会促进土壤中微生物群落向r策略或富营养策略转变[49]。土壤微生物群落在喀斯特地区森林恢复过程[50]、黄土高原辽东栎林次生演替过程[51]、废弃农田的自然演替过程[52]中均表现出从r策略向K策略转变的过程,其中寡营养或K策略细菌相对丰度和微生物群落rrn拷贝数均显著降低;而在温带草原草地恢复的过程中,土壤微生物群落表现出从K策略向r策略群落转变的过程[29]。出现这种不同结果的原因可能是在植被演替的早期土壤中营养缺乏,导致K策略微生物占据优势[39],而植被恢复后期营养输入增加,导致r策略微生物主导[38,53]。
在农业生态系统中,微生物生活史策略也受到土壤施肥量与肥料类型的影响。研究表明,肥料投入使土壤中细菌与真菌生物量的比值显著高于不施肥的土壤,从而使土壤微生物群落具有更强的r策略特征[54]。长期施用混合有机肥(秸秆、牛粪与绿肥)与施用无机肥料相比,其农田土壤微生物群落中的r策略或富营养类群的丰度更高[55],这有可能是因为长期施用有机肥料有利于土壤有机质积累[56],提高土壤中有机碳源的可利用性,从而促进土壤细菌向r策略或富营养类群为主的群落演替;而仅施用无机肥料的土壤中有机质积累慢甚至逐年下降[57],这导致微生物群落更趋向于K策略或寡营养类群为主的群落[58-59]。添加秸秆也是增加土壤有机碳含量的重要途径,同样能促进形成r策略或富营养微生物群落[60-61]。总体而言,有机质含量较低的农田土壤中寡营养微生物群落的相对丰度较高,而在有机质较高的农田中富营养微生物的相对丰度较高[62]。除了有机质含量外,土壤氮有效性也对微生物生活史策略具有重要影响,土壤中氮含量增加会提高r策略者或富营养细菌的相对丰度[63-64],而在土壤缺氮条件下,即使没有其他环境因子的限制,寡营养微生物仍在环境中占据优势,因为寡营养微生物可以通过分解土壤中的复杂有机质并从中获取氮源用于自身生长[65-66]。例如,深红三叶草改良土壤(富氮环境),其中的微生物以富营养微生物为主,黑麦改良土壤(贫氮环境)则以寡营养微生物为主[67]。与土体土壤相比,根际微生物在根际效应的作用下代谢更活跃,其中快速生长和繁殖的富营养类群丰度更高[68]。
土壤微生物群落的生活史策略除了受到土壤养分有效性调控外还受到酸化、盐碱、干旱等环境胁迫的影响。土壤中绝大部分类群均适宜在接近中性pH的环境下生长[69],而在酸化或盐碱土壤中寡营养微生物的比例均随酸化或盐碱程度提高而增加[70-71]。此外,在全球气候变化影响下,增温与干旱均会导致草地[72]和农田土壤[73]中贫营养或K策略微生物类群的相对丰度增加。以上研究表明与r策略者相比,K策略者能将更多资源投资于个体生存与耐受性,而不是用于驱动养分周转与繁殖,所以对环境胁迫等具有更强的抵抗力[74]。因此,微生物群落的抵抗力与恢复力也可以用r-K生活史策略理论来解释,可以预测微生物群落在全球变化背景下应对一系列环境干扰的稳定性[39]。
2.3 二分法框架的研究瓶颈当前微生物生活史策略的研究多聚焦于特定分类单元或功能群在特定环境条件下的响应规律,而将这些规律推广至群落或生态系统层面,仍面临显著的跨尺度整合挑战。土壤微生物的生活史策略不仅受土壤特征、底物特征、养分有效性等非生物因素调控,更与生物之间复杂的相互关系密切关联[75-76]。例如,在根际环境下,根系分泌物输入提高了碳源可利用性,会导致微生物分解作用增强[77]。此外,较大空间和长时间尺度上物理、化学、生物因素的不均匀分布也会使微生物的生活史策略产生巨大波动[78]。因此生态系统异质性会造成微生物生活史策略选择在空间和时间上的偏移,从而削弱了静态生活史策略理论的预测能力[79]。未来需重点解析微生物群落组装对个体生活策略选择的影响机制,阐明生态系统资源的时空异质性对微生物生活史选择的反馈作用。
目前针对于细菌与真菌群落的二分法策略分析往往从门水平对微生物进行生活史策略分类[80],然而该分类依据需要以微生物个体特征在高分类水平上(如门分类水平)具有代表性,因此其准确性仍需要进一步推敲。基于已有的细菌门水平上的二分法策略研究结果,大多数微生物可以在不同的环境中表现出不同的特征(图 2)[81-82]。例如,放线菌门可以在富营养环境中维持较强的生长能力,在大多数研究中被归类为富营养细菌,然而也有研究表明放线菌门具备寡营养细菌的特征,如在富营养环境中与生物量增长相关的蛋白合成量减少[83]。因此,将细菌从门水平归类为同一种策略的做法是不准确的[84-85]。此外,微生物学家在研究中发现不论是r-K生活史策略还是富营养与寡营养生活史策略微生物的响应特征均可能是连续的,因此不能简单的将某一细菌固定地划分为某一种策略的类群[41]。Philippot等[86]基于陆地微生物基因组分析发现其生态特征的一致性水平与分类学等级之间呈负相关关系,因此微生物生活史策略的二分法分类应在更精细的分类水平(如科、属)上进行估计,才能提高分类精确度[41]。

|
注:基于Web of Science数据库以关键词“soil”与“copiotrophic”/“oligotrophic”进行检索,仅统计2024年10月之前通过实测数据对微生物寡营养/富营养特征进行直接定义的文献(总计18篇),后续通过引用他人定义结果作为分类依据的文献不予考虑。图中百分比为被定义为该菌门被定义为寡营养或富营养的研究数量占总研究数量的比例,括号中的数字为研究数量,上标方括号中为参考文献。由于变形菌在土壤中丰度较高,一些研究将不同变形菌从纲水平与其他细菌门水平共同分析,*代表部分参考文献中将变形菌从纲水平进行生活史策略的划分 Note: Based on a Web of Science database, using the keywords "soil" and "copiotrophic"/"oligotrophic, " a total of 18 studies published prior to October 2024 were included. These studies directly defined microbial copiotrophic or oligotrophic characteristics based on empirical data. Publications that only cited definitions from previous studies without direct measurements were excluded. The percentages in the figure represent the proportion of studies that classified each bacterial phylum as either copiotrophic or oligotrophic, relative to the total number of studies referencing that phylum. The numbers in parentheses indicate the number of relevant studies, while superscript square brackets refer to the corresponding. Given the high abundance of Proteobacteria in soil, many studies treat different classes within Proteobacteria as comparable to phylum-level taxa. * indicates that some studies classified Proteobacteria based on class-level; therefore, a single study may include multiple classes of Proteobacteria, with more than one group identified as either copiotrophic or oligotrophic 图 2 土壤主要细菌类群(门水平)的生活史策略分类 Fig. 2 Classification of microbial life history strategies of soil dominant bacterial phylum |
在土壤环境中,微生物可利用的资源的种类和数量并不是影响微生物生长繁殖的唯一因素,非生物环境的胁迫(如酸性与碱性环境、干旱与淹水条件、高温与低温等)和来自生物因素的干扰(如捕食、竞争等)也会影响微生物生长。在较高胁迫压力下,即使土壤环境具有很高的底物可利用性,微生物也很难正常生长[87],所以仅仅依赖微生物的底物偏好和生长策略对微生物群落进行生活史策略的划分是不充分的,也应当考虑其是否因为环境压力而进入休眠等可逆的代谢不活跃的“投资策略”。与二分法相比,三分法生活史策略框架综合考虑了竞争、生长代谢、资源获取与抗逆等功能性状,这也是二分法框架与三分法框架之间最大的差异[100]。
Lovero和Treseder[101]分析了37株真菌的功能基因和生长速率,发现真菌存在以氨基酸渗透酶基因为特征的快速生长策略和由细胞外酶和营养转运蛋白组成为特征的资源获取策略,这两种策略和胁迫耐受性相关性状组成的三种生活史策略在不同生长条件下存在权衡关系。Piton等[102]分析了128个全球土壤细菌群落宏基因组数据,也发现土壤细菌群落存在由基因组大小、生物代谢能力和响应环境等特征共同决定的生活史策略,证明了土壤细菌群落存在多种生活史策略权衡这一观点。这些研究证实并丰富了微生物C-S-R与Y-A-S框架,为加强对微生物生活史策略的理解提供了支撑。
3.1 三分法框架的分类依据 3.1.1 C-S-R理论及其衍生框架微生物C-S-R理论框架的早期研究是将某一类微生物的功能与C-S-R策略进行匹配,认为微生物在环境干扰与压力均最小时主要投资自身C策略功能,提高自身底物代谢能力、产生高质量后代;随着环境压力的增大,微生物将会将更多能量投资于抵抗环境胁迫,执行S策略功能;而当环境干扰较为频发时,微生物则会大量产生后代,维持种群数量以获得生存优势(表 1)。Ho等[7]在甲烷氧化菌群落的生活史策略研究中将MMO标记基因(如pmoA、mmoX)和基因转录物质(mRNA)的合成,以及在高甲烷浓度环境中代谢活跃的功能性状被归类为C-R策略;将嗜盐、嗜热、嗜碱以及可以在不利条件下利用多种不同底物的性状归类为S-R策略;将菌株通过休眠维持生存和从干扰中恢复代谢能力的功能性状归类为S-C策略。与之类似,Chagnon等[103]也将丛枝菌根真菌群落的功能归到C-S-R理论框架中,促进土壤菌丝密度、提高碳代谢能力和推迟孢子产生等相关功能为C策略;维持较低的生长速率、较长的菌丝体寿命,以及对低温等逆境的抗性等相关功能为S策略;而维持高生长速度、促进孢子产生和菌丝愈合能力等相关功能为R策略。随后,Heuck等[104]在其基础上修改了丛枝菌根真菌的C-S-R理论框架,使之侧重于描述气候变化对农业生态系统中丛枝菌根真菌生活史策略的潜在影响,该框架认为将生物量分配个菌丝生长以获取磷的类群为C策略;生命周期短,能够迅速建立功能性菌丝网络的类群为R策略,而周转率较低并最终导致真菌生物量低的类群为S策略。
|
|
表 1 C-S-R与Y-A-S生活史策略理论框架中不同策略的潜在性状 Table 1 Potential traits of C-S-R and Y-A-S life history strategies theoretical framework |
然而,仅针对某一类微生物的生活史策略研究对理解复杂微生物群落的生活史策略仍远远不够,近年来基因组学技术的发展为微生物群落的三分法生活史策略研究提供了基于功能基因组成特征的研究思路。Krause等[23]在细菌[7]、古菌[112]、真菌[103,113]性状的一系列研究基础上,将微生物不同性状相关的功能基因划分到C-S-R框架中,其中与微生物生长速率、生物量增长与抗生素合成能力相关的功能划分为C策略;与产孢、维持细胞完整性、胞外酶、胞外聚合物的合成以及物质吸收系统划分为S策略;而与呼吸速率、rrn拷贝数,以及微生物的趋化趋避、运动和对环境的响应能力则被划分为R策略。其中,仅有部分功能属于典型的C-S-R生活史策略,例如研究普遍认为抗生素的合成是C策略性状,因为微生物合成抗生素是通过抑制其他种群的资源获取来提高自身的资源竞争能力[114-115];R策略微生物均表现出快速生长的性状(高生长速率、rrn拷贝数)[33,116];而S策略微生物具有耐受环境压力的能力(产孢、休眠和抗逆等功能)[117-118]。此外,微生物运动相关的功能特征(如趋化性等)却很难归类到C-S-R框架中的特定策略中,Krause等[23]认为微生物运动相关的功能是微生物获取环境中可利用资源并增加自身生物量的能力,应归类为R策略;而Thijs和Vangronsveld[114]则认为这些特征在环境压力较大时会使微生物快速利用环境中可利用资源,占据生态位与竞争中的优势,应归类C策略。在随后关于根际微生物生活史策略的特征研究中,Wood等[24]将微生物运动相关的功能(如趋化性和鞭毛产生)定义为与觅食(Foragin)有关的特征,并将其命名为F策略,他认为微生物的觅食特征并不属于原有的理论框架,应当作为单独的策略进行讨论,因此在C-S-R框架基础上提出了C-S-R-F框架。随后,将其进一步修改为C-S-O理论框[8],该理论框架中的微生物性状主要受到环境中资源的限制与多样性的影响,可以更好地描述微生物群落是如何被环境所影响,其中C策略的定义修改为在资源使用不受限制的环境中促进资源垄断的特征,例如抗生素生产、生物膜的形成及高ATP产量代谢;S策略的定义修改为有利于在资源使用受到限制的环境中生存的特征,例如DNA修复、胞外酶的释放、缓慢生长;原有的R策略修改为O策略并加入了微生物运动性的特征,定义为在资源可利用性波动的环境中促进资源垄断的特征,例如快速生长、趋化、孢子的形成及微生物的多底物代谢能力。
3.1.2 Y-A-S理论及其衍生框架Malik等[6]在Wood等[24]提出的C-S-R-F生活史策略框架的基础上对微生物生活史策略进行重新整理和分类后提出了Y-A-S生活史策略理论框架。在Y-A-S框架中,A策略取代了C策略与F策略,因为微生物的竞争主要体现在对资源的竞争,微生物的运动与趋化等觅食相关的性状也是微生物为了获取更多环境中的资源而发挥的功能。而Y策略则被定义为每单位资源消耗所产生的微生物生物量,其与R策略之间最大的区别是Y策略考虑的是微生物最终的生物产量而非其最大生长速率(表 1)[33]。与C-S-R框架相比,Y-A-S框架与土壤碳循环之间的联系更紧密,其中Y策略微生物增加生物量的过程有利于微生物残体碳的生成[119],A策略微生物则通过投资胞外酶的合成来促进元素循环[120],S策略微生物则可能取决于其受到的环境压力类型,例如在干旱条件下产生的胞外多糖等复杂化合物可能对于土壤碳储量的具有更加重要的贡献[121]。2022年,Li等[9]在Y-A-S理论框架上提出了Y-A-S-P理论框架,这是一种针对干旱土壤生态系统的理论框架,其中P策略代表了细胞生长潜力维持策略,该策略可能在更干旱的土壤中占主导地位,代表这些微生物可以对干旱缓解后产生的资源进行快速响应。
3.2 三分法框架的应用近年来,许多研究考虑了土壤养分条件与微生物生活史策略转变的关系。在农田土壤中,适量提高养分可利用性(合理施用氮肥或生物质炭)可以促进微生物将能量投资于自身生长,因此Y策略微生物更占据优势,这些微生物的增殖与周转形成了大量微生物残体,可以促进土壤有机质的形成[122]。同样,在林地[123]和草地[124]生态系统中,添加速效养分也会提高微生物群落投资Y策略的比例,提高土壤微生物碳源利用效率,从而加强微生物碳泵介导的土壤有机碳积累作用[125]。然而,过量施用氮肥则会加剧微生物的化学计量碳需求,使微生物群落策略转向资源获取A策略转变,降低土壤中碳的稳定性[126]。因此在农业生态系统中进行养分管理时,也需要考虑微生物生活史策略转变特征,在优化养分管理的同时促进生态系统有机碳固存。
非生物胁迫也会导致微生物生活史策略转变。例如,土壤中镉污染增加会导致微生物S策略增强[24]。干旱也会导致微生物群落更倾向于投资S策略,降低土壤有机碳周转率[105,127]。但是,随着环境胁迫减弱(如干旱缓解),微生物群会向更强的Y策略与A策略转变[128]。然而,并非所有土壤环境胁迫减弱均会导致类似的变化,有研究表明长期干旱土壤中降水增加时,尽管干旱胁迫降低,但土壤中微生物群落S策略反而增强了[129],可能是由于微生物群落适应了当前的环境条件,当其发生剧烈变动时可能会对微生物群落产生选择压力[130]。
除土壤条件外,植物的根际效应也会对土壤微生物的生活史策略产生影响。在镉污染土壤中,土体微生物的生活史策略随镉污染增加以S策略为主,而在污染土壤中的作物根际微生物群落的生活史策略则由R策略向C策略转变,可能是根系分泌物为微生物提供了大量可利用碳源,在一定程度上缓解了镉污染的胁迫[24,131]。此外,植物的资源获取策略不同也会通过植物-土壤反馈系统对土壤微生物的生活史策略产生不同的影响。研究表明,紫云英、红车轴草和紫花苜蓿等营养获取型植物(Acquisitive plants)可以富集A策略的土壤微生物,增强细菌趋化性、分泌系统及细胞运动性等功能,提高土壤中的氮素有效性,促进土壤养分循环;而多花黑麦草、小麦和芥菜等保守型植物(Conservative plants)则富集Y策略的土壤微生物,增强碳固定、三羧酸循环(TCA)、核糖体及支链氨基酸生物合成等代谢性状,提高了土壤微生物的固碳能力[132]。
3.3 三分法框架的研究瓶颈Y-A-S及C-S-R等生活史策略理论框架对理解和认识不同土壤中的复杂微生物群落功能特征提供了切入点,为预测环境变化或人类活动下的微生物群落功能演替及其生态效应提供了理论支撑。然而,同一微生物类群或群落在不同环境条件下的功能特征及其生活史策略并不是不变的,当前主要基于微生物基因组功能分析的微生物群落生活史策略的分类研究并不能准确体现土壤微生物的投资策略。因此,为进一步理解微生物生活史策略,未来需要重点关注微生物实际发挥的功能及其与环境因素之间的关系,可以利用单菌株或者群落水平的多组学研究解析微生物在不同环境条件下的原位代谢特征,解析关键功能参与的生活史策略转换过程,同时利用机器学习等手段构建微生物生活史策略的动态适应网络。
4 微生物生活史策略的研究展望纵观微生物生活史策略理论框架的发展过程,无论是二分法框架还是三分法框架,均经历了从动植物生态学理论到微生物生态学理论的移植和优化过程,其中二分法框架主要考虑微生物的底物代谢能力和生长繁殖特征,以微生物生长速率与资源利用效率为分类依据;而三分法框架主要考虑微生物在复杂环境下的功能特征,以微生物群落水平的功能基因组聚集特征为分类依据(表 2)。二分法适用于资源梯度驱动的系统,能够快速识别微生物对营养变化的响应,尤其在农业施肥、污染治理等场景中应用广泛。然而,这类模型在复杂环境中往往难以解释多个生态因子的交互作用,其策略划分在门/纲水平下也存在分类比较粗放的局限性。相比之下,三分法模型引入多个生态轴,强调干扰、胁迫与资源获取的多维度权衡。例如,C-S-R模型将微生物群落划分为竞争者、胁迫耐受者与扰动适应者,而Y-A-S模型则进一步提出产量、资源获取与胁迫耐受三类功能谱系。此类模型更适用于群落水平的演替研究与复杂环境响应解析,具备更强的生态解释力与扩展性,尤其在模拟多重胁迫、干扰和异质性环境下的群落动态中展现出优势。尽管三分法模型在理论上更加完善,但其参数化要求高、分类标准尚不统一,导致其在微生物生态学中的应用仍处于探索阶段。微生物生活史策略的理论框架研究仍处于快速发展阶段,未来研究应结合具体研究问题与数据类型,灵活选用或整合不同的策略,然而目前针对土壤微生物群落生活史策略的研究仍局限于静态特征的识别和分类,尚未形成系统化的动态解析与调控体系。为推动微生物生活史策略研究从理论工具向生态解决方案转化,本文对未来的研究方向进行了展望。
|
|
表 2 二分法与三分法生活史策略理论框架特征与应用 Table 2 Characteristics and applications of two-way and three-way life history strategy theoretical frameworks |
当前的土壤微生物群落生活史策略研究主要依赖扩增子测序和宏基因组测序等技术,在此基础上利用基因组功能预测分析,以微生物群落水平的功能基因组聚集特征为分类依据。然而,微生物基因组中存在的功能基因并不都是激活状态,而是在不同环境条件下选择性表达[133]。因此,这些分析手段仅能反映微生物的潜在功能,无法揭示其在动态环境中的实际行为。然而如何实现微生物功能从基因的组成性分析到基因表达的动态监测,仍是当前研究的技术瓶颈。为突破这一局限,亟需构建动态多维解析途径。未来可以整合多组学检测技术,如利用转录组测序明确基因动态表达特征,利用代谢组和蛋白组监测菌株代谢产物组成(如合成生物量、产生胞外酶、合成抗逆代谢物等)特征,利用单细胞拉曼光谱、荧光标记等原位活性监测手段,突破传统生活史策略的离散分类理论。同时,利用人工智能的机器学习与深度学习手段从高维、多源的组学数据中挖掘微生物关键特征,并通过构建预测模型整合环境变化和微生物功能特征的关系,共同建立动态的微生物生活策略转换模型,实现从基因组到生态系统尺度的多层级建模,推动微生物生活史策略研究进入可预测的新阶段。
4.2 揭示土壤微生物生活史策略转换的驱动机制,推动环境响应的特征识别到功能可编程的定向调控研究微生物可以通过功能“重编程(functional reprogramming)”响应周围环境信号实现生活史策略的动态转换[134],然而当前研究多局限于策略相关基因组成的特征识别及其丰度统计的描述性分析,对微生物生活史策略转换的调控机制、关键分子元件、核心调控途径仍不明确,缺乏系统研究。因此,建议在解析微生物在不同环境条件和生物互作条件下的生活史策略动态转换特征基础上,进一步明确微生物生活史策略转换的分子开关,并阐明其作用机制。首先利用环境变化-生物互作-基因表达开关-功能投资策略响应过程分析,建立生活史策略转变的调控网络,明确其中的核心控制模块;然后利用合成生物学和生物合成学等手段,设计环境快速响应和功能高效转化的生活史策略可编程菌株或合成菌群,从而实现微生物生活史策略的按需转换。
4.3 完善农业生态系统服务功能的土壤微生物生活史策略响应框架,利用策略分类理论建立生态功能管理体系微生物生活史策略分类理论研究以微生物为核心,重点探究其与土壤环境变化的关系,很少考虑生物之间的互作关系。而在农业生态系统中,微生物群落不仅与土壤肥力演变相关,还与作物生长之间具有紧密的关联。例如作物根际益生菌具有协助植物抵抗环境胁迫、增强植物抗病性、促进土壤养分循环和植物吸收养分等功能[135],这些功能与现有的三分法生活史策略理论有一定的重合性;此外,微生物还能分泌促进植物生长发育的激素(例如分泌细胞分裂素),然而这部分功能并没有被考虑进现存的生活史策略框架中。因此现存的生活史策略研究缺乏对微生物与植物互作、微生物-微生物互作中策略响应特征的深入剖析,也未明确策略与农业生态系统服务功能的量化关系。因此,未来可以以微生物功能为核心,构建以生态系统服务功能为核心的微生物生活史策略分类框架,支撑生态调控与农业可持续管理。整合土壤-微生物-作物互作网络,明确微生物生活史策略对微生物-植物互作和微生物-微生物互作的响应;在此基础上关联微生物生活史策略与养分利用效率和作物生产力等生态系统服务功能,建立微生物功能和生活史策略驱动生态系统服务功能的协同关系,定量化微生物生活史策略转换对生态系统服务功能的影响。
总之,微生物生活史策略的分类不仅对于描述土壤中微生物群落结构与功能提供了更易识别的方法,也为预测生态系统在环境变化下生态效应提供了理论基础,在促进土壤质量提升和农业绿色转型等方面具有广泛的应用价值和潜力。因此,应在当前以定性的生活史策略特征描述为主的研究基础上,进一步建立以微生物功能表达和动态响应为核心的生态系统服务功能定向调控研究框架,为开发基于微生物生活史策略的调控体系提供科学支撑,为促进土壤质量提升和农业绿色转型提供微生物组角度的解决方案。
| [1] |
Fang L C, Hu Z Y, Cui Q L, et al. Construction and application of synthetic communities: A new strategy to improve soil health (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(5): 1233-1245. [方临川, 胡紫莹, 崔庆亮, 等. 合成菌群构建与应用: 提升土壤健康新策略[J]. 土壤学报, 2025, 62(5): 1233-1245.]
(  0) 0) |
| [2] |
Crowther T W, Hoogen J V D, Wan J, et al. The global soil community and its influence on biogeochemistry[J]. Science, 2019, 365(6455): eaav0550. DOI:10.1126/science.aav0550
(  0) 0) |
| [3] |
Philippot L, Chenu C, Kappler A, et al. The interplay between microbial communities and soil properties[J]. Nature Reviews Microbiology, 2024, 22(4): 226-239. DOI:10.1038/s41579-023-00980-5
(  0) 0) |
| [4] |
Green J L, Bohannan B J M, Whitaker R J. Microbial biogeography: From taxonomy to traits[J]. Science, 2008, 320(5879): 1039-1043. DOI:10.1126/science.1153475
(  0) 0) |
| [5] |
Martiny J B H, Jones S E, Lennon J T, et al. Microbiomes in light of traits: A phylogenetic perspective[J]. Science, 2015, 350(6261): aac9323. DOI:10.1126/science.aac9323
(  0) 0) |
| [6] |
Malik A A, Martiny J B H, Brodie E L, et al. Defining trait-based microbial strategies with consequences for soil carbon cycling under climate change[J]. The ISME Journal, 2020, 14(1): 1-9. DOI:10.1038/s41396-019-0510-0
(  0) 0) |
| [7] |
Ho A, Kerckhof F, Luke C, et al. Conceptualizing functional traits and ecological characteristics of methane‐oxidizing bacteria as life strategies[J]. Environmental Microbiology Reports, 2013, 5(3): 335-345. DOI:10.1111/j.1758-2229.2012.00370.x
(  0) 0) |
| [8] |
Wood J L, Malik A A, Greening C, et al. Rethinking CSR theory to incorporate microbial metabolic diversity and foraging traits[J]. The ISME Journal, 2023, 17(11): 1793-1797. DOI:10.1038/s41396-023-01486-x
(  0) 0) |
| [9] |
Li C, Liao H, Xu L, et al. The adjustment of life history strategies drives the ecological adaptations of soil microbiota to aridity[J]. Molecular Ecology, 2022, 31(10): 2920-2934. DOI:10.1111/mec.16445
(  0) 0) |
| [10] |
Weber C A. Aufbau und vegetation der Moore Norddeutschlands[J]. Botanische Jahrbücher für Systematik, Pflanzengeschichte und Pflanzengeographie, 1907, 90: 19-34.
(  0) 0) |
| [11] |
Roughgarden J. Density‐dependent natural selection[J]. Ecology, 1971, 52(3): 453-468. DOI:10.2307/1937628
(  0) 0) |
| [12] |
Poindexter J S. Oligotrophy: Fast and famine existence. //Advances in microbial ecology[M]. Springer US, 1981: 63—89.
(  0) 0) |
| [13] |
Hirsch P, Bernhard M, Cohen S S, et al. Life under conditions of low nutrient. //Strategies of microbial life in extreme environments[M]. Verlag Chemie, 1979: 357—372.
(  0) 0) |
| [14] |
Anagnostopoulos G D. Microbial life in extreme environments[J]. Nature, 1979, 279(5714): 658-658.
(  0) 0) |
| [15] |
MacArthur R H, Wilson E O. The MacArthur-Wilson equilibrium model: A chronicle of what it said and how it was tested. //The theory of island biogeography[M]. Princeton, Princeton University Press, 1967.
(  0) 0) |
| [16] |
Pianka E R. On r- and K-Selection[J]. The American Naturalist, 1970, 104(940): 592-597. DOI:10.1086/282697
(  0) 0) |
| [17] |
Esch G W, Hazen T C, Aho J M. Parasitism and r- and K-selection. //Regulation of Parasite populations[M]. Elsevier, 1977: 9—62.
(  0) 0) |
| [18] |
Andrews J H, Rouse D I. Plant pathogens and the theory of r- and K-Selection[J]. The American Naturalist, 1982, 120(3): 283-296. DOI:10.1086/283991
(  0) 0) |
| [19] |
Andrews J H, Harris R F. r- and K-selection and microbial ecology. //Advances in microbial ecology[M]. Springer US, 1981: 99—147.
(  0) 0) |
| [20] |
Fierer N, Bradford M A, Jackson R B. Toward an ecological classification of soil bacteria[J]. Ecology, 2007, 88(6): 1354-1364. DOI:10.1890/05-1839
(  0) 0) |
| [21] |
Marshall D J, Cameron H E, Loreau M. Relationships between intrinsic population growth rate, carrying capacity and metabolism in microbial populations[J]. The ISME Journal, 2023, 17(12): 2140-2143. DOI:10.1038/s41396-023-01543-5
(  0) 0) |
| [22] |
Grime J P. Vegetation classification by reference to strategies[J]. Nature, 1974, 250(5461): 26-31. DOI:10.1038/250026a0
(  0) 0) |
| [23] |
Krause S, Le Roux X, Niklaus P A, et al. Trait-based approaches for understanding microbial biodiversity and ecosystem functioning[J]. Frontiers in Microbiology, 2014, 5: 251.
(  0) 0) |
| [24] |
Wood J L, Tang C, Franks A E. Competitive traits are more important than stress-tolerance traits in a cadmium-contaminated rhizosphere: A role for trait theory in microbial ecology[J]. Frontiers in Microbiology, 2018, 9: 121. DOI:10.3389/fmicb.2018.00121
(  0) 0) |
| [25] |
Wang Y, Wilhelm R C, Swenson T L, et al. Substrate utilization and competitive interactions among soil bacteria vary with life-history strategies[J]. Frontiers in Microbiology, 2022, 13: 914472. DOI:10.3389/fmicb.2022.914472
(  0) 0) |
| [26] |
Zhu M, Dai X. Shaping of microbial phenotypes by trade-offs[J]. Nature Communications, 2024, 15(1): 4238. DOI:10.1038/s41467-024-48591-9
(  0) 0) |
| [27] |
López J L, Fourie A, Poppeliers S W M, et al. Growth rate is a dominant factor predicting the rhizosphere effect[J]. The ISME Journal, 2023, 17(9): 1396-1405. DOI:10.1038/s41396-023-01453-6
(  0) 0) |
| [28] |
Aliperti L, Aptekmann A A, Farfañuk G, et al. R/K selection of GC content in prokaryotes[J]. Environmental Microbiology, 2023, 25(12): 3255-3268. DOI:10.1111/1462-2920.16511
(  0) 0) |
| [29] |
Yang Y, Dou Y, Wang B, et al. Deciphering factors driving soil microbial life‐history strategies in restored grasslands[J]. iMeta, 2023, 2(1): e66. DOI:10.1002/imt2.66
(  0) 0) |
| [30] |
Zhang C, Liu G, Xue S, et al. Soil bacterial community dynamics reflect changes in plant community and soil properties during the secondary succession of abandoned farmland in the Loess Plateau[J]. Soil Biology and Biochemistry, 2016, 97: 40-49. DOI:10.1016/j.soilbio.2016.02.013
(  0) 0) |
| [31] |
Klappenbach J A, Dunbar J M, Schmidt T M. rRNA operon copy number reflects ecological strategies of bacteria[J]. Applied and Environmental Microbiology, 2000, 66(4): 1328-1333. DOI:10.1128/AEM.66.4.1328-1333.2000
(  0) 0) |
| [32] |
Wilhelm R C, Amsili J P, Kurtz K S M, et al. Ecological insights into soil health according to the genomic traits and environment-wide associations of bacteria in agricultural soils[J]. ISME Communications, 2023, 3(1): 1. DOI:10.1038/s43705-022-00209-1
(  0) 0) |
| [33] |
Roller B R K, Stoddard S F, Schmidt T M. Exploiting rRNA operon copy number to investigate bacterial reproductive strategies[J]. Nature Microbiology, 2016, 1(11): 16160. DOI:10.1038/nmicrobiol.2016.160
(  0) 0) |
| [34] |
Garcia-Pausas J, Paterson E. Microbial community abundance and structure are determinants of soil organic matter mineralisation in the presence of labile carbon[J]. Soil Biology and Biochemistry, 2011, 43(8): 1705-1713. DOI:10.1016/j.soilbio.2011.04.016
(  0) 0) |
| [35] |
Andrews J H. Fungal life-history strategies[M]//Carroll C G, Wicklow D T. The fungal community: Its organization and role in the ecosystem. 2nd ed. Marcel Dekker, New York, 1992: 119—145.
(  0) 0) |
| [36] |
Ho A, Lonardo D P D, Bodelier P L E. Revisiting life strategy concepts in environmental microbial ecology[J]. FEMS Microbiology Ecology, 2017, 93(3): fix006.
(  0) 0) |
| [37] |
Chen C, Zhang J, Lu M, et al. Microbial communities of an arable soil treated for 8 years with organic and inorganic fertilizers[J]. Biology and Fertility of Soils, 2016, 52(4): 455-467. DOI:10.1007/s00374-016-1089-5
(  0) 0) |
| [38] |
Wang Y, Qu M, Wang J, et al. Recovery of bacterial network complexity and stability after simulated extreme rainfall is mediated by K-/r-strategy dominance[J]. Applied Soil Ecology, 2024, 203: 105657. DOI:10.1016/j.apsoil.2024.105657
(  0) 0) |
| [39] |
Liu J, Peng Z, Tu H, et al. Oligotrophic microbes are recruited to resist multiple global change factors in agricultural subsoils[J]. Environment International, 2024, 183: 108429. DOI:10.1016/j.envint.2024.108429
(  0) 0) |
| [40] |
Allison S D, Martiny J B H. Resistance, resilience, and redundancy in microbial communities[J]. Proceedings of the National Academy of Sciences of the United States of America, 2008, 105(supplement_1): 11512-11519.
(  0) 0) |
| [41] |
Stone B W G, Dijkstra P, Finley B K, et al. Life history strategies among soil bacteria—Dichotomy for few, continuum for many[J]. The ISME Journal, 2023, 17(4): 611-619. DOI:10.1038/s41396-022-01354-0
(  0) 0) |
| [42] |
De Vries F T, Shade A. Controls on soil microbial community stability under climate change[J]. Frontiers in Microbiology, 2013, 4: 265.
(  0) 0) |
| [43] |
Frostegård Å, Tunlid A, Bååth E. Microbial biomass measured as total lipid phosphate in soils of different organic content[J]. Journal of Microbiological Methods, 1991, 14(3): 151-163. DOI:10.1016/0167-7012(91)90018-L
(  0) 0) |
| [44] |
Muazi Alenazi A, Anwar Y, EM Abo-Aba S, et al. A review on Actinomycetes distribution, isolation, and their medical applications[J]. Novel Research in Microbiology Journal, 2023, 7(2): 1918-1931. DOI:10.21608/nrmj.2023.294180
(  0) 0) |
| [45] |
Fierer N, Strickland M S, Liptzin D, et al. Global patterns in belowground communities[J]. Ecology Letters, 2009, 12(11): 1238-1249. DOI:10.1111/j.1461-0248.2009.01360.x
(  0) 0) |
| [46] |
Zechmeister-Boltenstern S, Keiblinger K M, Mooshammer M, et al. The application of ecological stoichiometry to plant-microbial-soil organic matter transformations[J]. Ecological Monographs, 2015, 85(2): 133-155. DOI:10.1890/14-0777.1
(  0) 0) |
| [47] |
Sun Y, Wang C, Yang J, et al. Elevated CO2 shifts soil microbial communities from K‐ to r‐strategists[J]. Global Ecology and Biogeography, 2021, 30(5): 961-972. DOI:10.1111/geb.13281
(  0) 0) |
| [48] |
Zhou Z, Wang C, Luo Y. Effects of forest degradation on microbial communities and soil carbon cycling: A global meta-analysis[J]. Global Ecology and Biogeography, 2018, 27(1): 110-124. DOI:10.1111/geb.12663
(  0) 0) |
| [49] |
Nemergut D R, Cleveland C C, Wieder W R, et al. Plot-scale manipulations of organic matter inputs to soils correlate with shifts in microbial community composition in a lowland tropical rain forest[J]. Soil Biology and Biochemistry, 2010, 42(12): 2153-2160. DOI:10.1016/j.soilbio.2010.08.011
(  0) 0) |
| [50] |
Hu P, Zhang W, Kuzyakov Y, et al. Linking bacterial life strategies with soil organic matter accrual by karst vegetation restoration[J]. Soil Biology and Biochemistry, 2023, 177: 108925. DOI:10.1016/j.soilbio.2022.108925
(  0) 0) |
| [51] |
Yan B, Sun L, Li J, et al. Change in composition and potential functional genes of soil bacterial and fungal communities with secondary succession in Quercus liaotungensis forests of the Loess Plateau, western China[J]. Geoderma, 2020, 364: 114199. DOI:10.1016/j.geoderma.2020.114199
(  0) 0) |
| [52] |
Li J, Shangguan Z, Deng L. Dynamics of soil microbial metabolic activity during grassland succession after farmland abandonment[J]. Geoderma, 2020, 363: 114167. DOI:10.1016/j.geoderma.2019.114167
(  0) 0) |
| [53] |
Chen H, Jing Q, Liu X, et al. Microbial respiratory thermal adaptation is regulated by r‐/K‐strategy dominance[J]. Ecology Letters, 2022, 25(11): 2489-2499. DOI:10.1111/ele.14106
(  0) 0) |
| [54] |
Gordon H, Haygarth P M, Bardgett R D. Drying and rewetting effects on soil microbial community composition and nutrient leaching[J]. Soil Biology and Biochemistry, 2008, 40(2): 302-311. DOI:10.1016/j.soilbio.2007.08.008
(  0) 0) |
| [55] |
Mao X, Sun T, Zhu L, et al. Microbial adaption to stoichiometric imbalances regulated the size of soil mineral-associated organic carbon pool under continuous organic amendments[J]. Geoderma, 2024, 445: 116883. DOI:10.1016/j.geoderma.2024.116883
(  0) 0) |
| [56] |
Xia W J, Liu K L, Zhang L F, et al. Effect of long-term fertilization on soil microbial biomass and enzyme activities in reddish paddy soil (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(3): 628-637. DOI:10.11766/trxb201912050570 [夏文建, 柳开楼, 张丽芳, 等. 长期施肥对红壤稻田土壤微生物生物量和酶活性的影响[J]. 土壤学报, 2021, 58(3): 628-637.]
(  0) 0) |
| [57] |
Wu N X, Wang P, Liu Y L, et al. Response characteristics and influencing factors of soil organic carbon to reduced chemical fertilizers or organic fertilizer substitution[J]. Acta Pedologica Sinica, DOI: 10.11766/trxb202408190332.[吴能祥, 王萍, 刘亚龙, 等. 土壤有机碳对化肥减施或有机肥替代的响应特征及影响因素[J]. 土壤学报, DOI: 10.11766/trxb202408190332.]
(  0) 0) |
| [58] |
Wu X, Liu P, Wegner C E, et al. Deciphering microbial mechanisms underlying soil organic carbon storage in a wheat-maize rotation system[J]. Science of the Total Environment, 2021, 788: 147798. DOI:10.1016/j.scitotenv.2021.147798
(  0) 0) |
| [59] |
Liu M F, Zhou G X, Zhang J B, et al. Effects of long-term straw burying and nitrogen fertilizer application on soil bacterial community characteristics (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(5): 1374-1385. [刘明凤, 周桂香, 张佳宝, 等. 长期秸秆掩埋配施氮肥对土壤细菌群落特征的影响[J]. 土壤学报, 2024, 61(5): 1374-1385.]
(  0) 0) |
| [60] |
Xu R, Zhang Y, Li Y, et al. Linking bacterial life strategies with the distribution pattern of antibiotic resistance genes in soil aggregates after straw addition[J]. Journal of Hazardous Materials, 2024, 471: 134355. DOI:10.1016/j.jhazmat.2024.134355
(  0) 0) |
| [61] |
Yang F, He B, Dong B, et al. Film-straw dual mulching improves soil fertility and maize yield in dryland farming by increasing straw-degrading bacterial abundance and their positive cooperation[J]. Agriculture, Ecosystems & Environment, 2024, 367: 108997.
(  0) 0) |
| [62] |
Senechkin I V, Speksnijder A G C L, Semenov A M, et al. Isolation and partial characterization of bacterial strains on low organic carbon medium from soils fertilized with different organic amendments[J]. Microbial Ecology, 2010, 60(4): 829-839. DOI:10.1007/s00248-010-9670-1
(  0) 0) |
| [63] |
Leff J W, Jones S E, Prober S M, et al. Consistent responses of soil microbial communities to elevated nutrient inputs in grasslands across the globe[J]. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(35): 10967-10972.
(  0) 0) |
| [64] |
Fierer N, Lauber C L, Ramirez K S, et al. Comparative metagenomic, phylogenetic and physiological analyses of soil microbial communities across nitrogen gradients[J]. The ISME Journal, 2012, 6(5): 1007-1017. DOI:10.1038/ismej.2011.159
(  0) 0) |
| [65] |
Fontaine S, Henault C, Aamor A, et al. Fungi mediate long term sequestration of carbon and nitrogen in soil through their priming effect[J]. Soil Biology and Biochemistry, 2011, 43(1): 86-96. DOI:10.1016/j.soilbio.2010.09.017
(  0) 0) |
| [66] |
Chen R, Senbayram M, Blagodatsky S, et al. Soil C and N availability determine the priming effect: microbial N mining and stoichiometric decomposition theories[J]. Global Change Biology, 2014, 20(7): 2356-2367. DOI:10.1111/gcb.12475
(  0) 0) |
| [67] |
Thapa R, Tully K L, Hamovit N, et al. Microbial processes and community structure as influenced by cover crop residue type and placement during repeated dry-wet cycles[J]. Applied Soil Ecology, 2022, 172: 104349. DOI:10.1016/j.apsoil.2021.104349
(  0) 0) |
| [68] |
Ling N, Wang T, Kuzyakov Y. Rhizosphere bacteriome structure and functions[J]. Nature Communications, 2022, 13(1): 836. DOI:10.1038/s41467-022-28448-9
(  0) 0) |
| [69] |
Wang X, Lin J, Peng X, et al. Microbial rrn copy number is associated with soil C: N ratio and pH under long-term fertilization[J]. Science of the Total Environment, 2024, 954: 176675. DOI:10.1016/j.scitotenv.2024.176675
(  0) 0) |
| [70] |
Chen X, Luo M, Liu Y, et al. Linking carbon-degrading enzyme activity to microbial carbon-use trophic strategy under salinization in a subtropical tidal wetland[J]. Applied Soil Ecology, 2022, 174: 104421. DOI:10.1016/j.apsoil.2022.104421
(  0) 0) |
| [71] |
Xun W, Zhao J, Xue C, et al. Significant alteration of soil bacterial communities and organic carbon decomposition by different long‐term fertilization management conditions of extremely low‐productivity arable soil in South China[J]. Environmental Microbiology, 2016, 18(6): 1907-1917. DOI:10.1111/1462-2920.13098
(  0) 0) |
| [72] |
De Vries F T, Liiri M E, Bjørnlund L, et al. Land use alters the resistance and resilience of soil food webs to drought[J]. Nature Climate Change, 2012, 2(4): 276-280. DOI:10.1038/nclimate1368
(  0) 0) |
| [73] |
De Vries F T, Liiri M E, Bjørnlund L, et al. Legacy effects of drought on plant growth and the soil food web[J]. Oecologia, 2012, 170(3): 821-833. DOI:10.1007/s00442-012-2331-y
(  0) 0) |
| [74] |
Schimel J P. Life in dry soils: Effects of drought on soil microbial communities and processes[J]. Annual Review of Ecology, Evolution, and Systematics, 2018, 49(1): 409-432. DOI:10.1146/annurev-ecolsys-110617-062614
(  0) 0) |
| [75] |
Mao Z, Zhao Z, Da J, et al. The selection of copiotrophs may complicate biodiversity-ecosystem functioning relationships in microbial dilution-to-extinction experiments[J]. Environmental Microbiome, 2023, 18(1): 19. DOI:10.1186/s40793-023-00478-w
(  0) 0) |
| [76] |
Dragone N B, Hoffert M, Strickland M S, et al. Taxonomic and genomic attributes of oligotrophic soil bacteria[J]. ISME Communications, 2024, 4(1): ycae081. DOI:10.1093/ismeco/ycae081
(  0) 0) |
| [77] |
Kuzyakov Y, Blagodatskaya E. Microbial hotspots and hot moments in soil: Concept & review[J]. Soil Biology and Biochemistry, 2015, 83: 184-199. DOI:10.1016/j.soilbio.2015.01.025
(  0) 0) |
| [78] |
Nguyen J, Lara-Gutiérrez J, Stocker R. Environmental fluctuations and their effects on microbial communities, populations and individuals[J]. FEMS Microbiology Reviews, 2021, 45(4): fuaa068. DOI:10.1093/femsre/fuaa068
(  0) 0) |
| [79] |
Widder S, Allen R J, Pfeiffer T, et al. Challenges in microbial ecology: Building predictive understanding of community function and dynamics[J]. The ISME Journal, 2016, 10(11): 2557-2568. DOI:10.1038/ismej.2016.45
(  0) 0) |
| [80] |
Domsch K H. Compendium of soil fungi[J]. IHW-Verlag, 1993, 1: 630-643.
(  0) 0) |
| [81] |
Jones R T, Robeson M S, Lauber C L, et al. A comprehensive survey of soil acidobacterial diversity using pyrosequencing and clone library analyses[J]. The ISME Journal, 2009, 3(4): 442-453. DOI:10.1038/ismej.2008.127
(  0) 0) |
| [82] |
Männistö M, Ganzert L, Tiirola M, et al. Do shifts in life strategies explain microbial community responses to increasing nitrogen in tundra soil?[J]. Soil Biology and Biochemistry, 2016, 96: 216-228. DOI:10.1016/j.soilbio.2016.02.012
(  0) 0) |
| [83] |
Bastida F, Selevsek N, Torres I F, et al. Soil restoration with organic amendments: Linking cellular functionality and ecosystem processes[J]. Scientific Reports, 2015, 5(1): 15550. DOI:10.1038/srep15550
(  0) 0) |
| [84] |
Morrissey E M, Mau R L, Schwartz E, et al. Phylogenetic organization of bacterial activity[J]. The ISME Journal, 2016, 10(9): 2336-2340. DOI:10.1038/ismej.2016.28
(  0) 0) |
| [85] |
Papp K, Hungate B A, Schwartz E. Glucose triggers strong taxon‐specific responses in microbial growth and activity: Insights from DNA and RNA qSIP[J]. Ecology, 2020, 101(1): e02887. DOI:10.1002/ecy.2887
(  0) 0) |
| [86] |
Philippot L, Andersson S G E, Battin T J, et al. The ecological coherence of high bacterial taxonomic ranks[J]. Nature Reviews Microbiology, 2010, 8(7): 523-529. DOI:10.1038/nrmicro2367
(  0) 0) |
| [87] |
Cleveland C C, Nemergut D R, Schmidt S K, et al. Increases in soil respiration following labile carbon additions linked to rapid shifts in soil microbial community composition[J]. Biogeochemistry, 2007, 82(3): 229-240. DOI:10.1007/s10533-006-9065-z
(  0) 0) |
| [88] |
Eilers K G, Lauber C L, Knight R, et al. Shifts in bacterial community structure associated with inputs of low molecular weight carbon compounds to soil[J]. Soil Biology and Biochemistry, 2010, 42(6): 896-903. DOI:10.1016/j.soilbio.2010.02.003
(  0) 0) |
| [89] |
Padmanabhan P, Padmanabhan S, DeRito C, et al. Respiration of 13C-labeled substrates added to soil in the field and subsequent 16S rRNA gene analysis of 13C-labeled soil DNA[J]. Applied and Environmental Microbiology, 2003, 69(3): 1614-1622. DOI:10.1128/AEM.69.3.1614-1622.2003
(  0) 0) |
| [90] |
Xie G, Zhang Y, Gong Y, et al. Extreme trophic tales: Deciphering bacterial diversity and potential functions in oligotrophic and hypereutrophic lakes[J]. BMC Microbiology, 2024, 24(1): 348. DOI:10.1186/s12866-024-03488-x
(  0) 0) |
| [91] |
Luo H, Moran M A. How do divergent ecological strategies emerge among marine bacterioplankton lineages?[J]. Trends in Microbiology, 2015, 23(9): 577-584. DOI:10.1016/j.tim.2015.05.004
(  0) 0) |
| [92] |
Jenkins S N, Rushton S P, Lanyon C V, et al. Taxon-specific responses of soil bacteria to the addition of low level C inputs[J]. Soil Biology and Biochemistry, 2010, 42(9): 1624-1631. DOI:10.1016/j.soilbio.2010.06.002
(  0) 0) |
| [93] |
Ramirez K S, Craine J M, Fierer N. Consistent effects of nitrogen amendments on soil microbial communities and processes across biomes[J]. Global Change Biology, 2012, 18(6): 1918-1927. DOI:10.1111/j.1365-2486.2012.02639.x
(  0) 0) |
| [94] |
Hungate B A, Mau R L, Schwartz E, et al. Quantitative microbial ecology through stable isotope probing[J]. Applied and Environmental Microbiology, 2015, 81(21): 7570-7581. DOI:10.1128/AEM.02280-15
(  0) 0) |
| [95] |
Pascault N, Ranjard L, Kaisermann A, et al. Stimulation of different functional groups of bacteria by various plant residues as a driver of soil priming effect[J]. Ecosystems, 2013, 16(5): 810-822. DOI:10.1007/s10021-013-9650-7
(  0) 0) |
| [96] |
Pepe-Ranney C, Campbell A N, Koechli C N, et al. Unearthing the ecology of soil microorganisms using a high resolution DNA-SIP approach to explore cellulose and xylose metabolism in soil[J]. Frontiers in Microbiology, 2016, 7: 703.
(  0) 0) |
| [97] |
Van Kessel M A H J, Speth D R, Albertsen M, et al. Complete nitrification by a single microorganism[J]. Nature, 2015, 528(7583): 555-559. DOI:10.1038/nature16459
(  0) 0) |
| [98] |
Daims H, Lebedeva E V, Pjevac P, et al. Complete nitrification by Nitrospira bacteria[J]. Nature, 2015, 528(7583): 504-509. DOI:10.1038/nature16461
(  0) 0) |
| [99] |
Merino N, Aronson H S, Bojanova D P, et al. Living at the extremes: Extremophiles and the limits of life in a planetary context[J]. Frontiers in Microbiology, 2019, 10: 780. DOI:10.3389/fmicb.2019.00780
(  0) 0) |
| [100] |
Grime J P, Pierce S. The evolutionary strategies that shape ecosystems[M]. John Wiley & Sons, 2012.
(  0) 0) |
| [101] |
Lovero K G, Treseder K K. Trade-offs between growth rate and other fungal traits[J]. Frontiers in Forests and Global Change, 2021, 4: 756650. DOI:10.3389/ffgc.2021.756650
(  0) 0) |
| [102] |
Piton G, Allison S D, Bahram M, et al. Life history strategies of soil bacterial communities across global terrestrial biomes[J]. Nature Microbiology, 2023, 8(11): 2093-2102. DOI:10.1038/s41564-023-01465-0
(  0) 0) |
| [103] |
Chagnon P L, Bradley R L, Maherali H, et al. A trait-based framework to understand life history of mycorrhizal fungi[J]. Trends in Plant Science, 2013, 18(9): 484-491. DOI:10.1016/j.tplants.2013.05.001
(  0) 0) |
| [104] |
Heuck M K, Powell J R, Kath J, et al. Evaluating the usefulness of the C‐S‐R framework for understanding AM fungal responses to climate change in agroecosystems[J]. Global Change Biology, 2024, 30(11): e17566. DOI:10.1111/gcb.17566
(  0) 0) |
| [105] |
Malik A A, Bouskill N J. Drought impacts on microbial trait distribution and feedback to soil carbon cycling[J]. Functional Ecology, 2022, 36(6): 1442-1456. DOI:10.1111/1365-2435.14010
(  0) 0) |
| [106] |
Treseder K K, Lennon J T. Fungal traits that drive ecosystem dynamics on land[J]. Microbiology and Molecular Biology Reviews, 2015, 79(2): 243-262. DOI:10.1128/MMBR.00001-15
(  0) 0) |
| [107] |
Treseder K K. Ecological strategies of microbes: Thinking outside the triangle[J]. Journal of Ecology, 2023, 111(9): 1832-1843. DOI:10.1111/1365-2745.14115
(  0) 0) |
| [108] |
Alster C J, Allison S D, Treseder K K. Trait relationships of fungal decomposers in response to drought using a dual field and laboratory approach[J]. Ecosphere, 2022, 13(6): e4063. DOI:10.1002/ecs2.4063
(  0) 0) |
| [109] |
Lustenhouwer N, Maynard D S, Bradford M A, et al. A trait-based understanding of wood decomposition by fungi[J]. Proceedings of the National Academy of Sciences of the United States of America, 2020, 117(21): 11551-11558.
(  0) 0) |
| [110] |
Westoby M, Nielsen D A, Gillings M R, et al. Strategic traits of bacteria and archaea vary widely within substrate-use groups[J]. FEMS Microbiology Ecology, 2021, 97(11): fiab142. DOI:10.1093/femsec/fiab142
(  0) 0) |
| [111] |
Lipson D A, Monson R K, Schmidt S K, et al. The trade-off between growth rate and yield in microbial communities and the consequences for under-snow soil respiration in a high elevation coniferous forest[J]. Biogeochemistry, 2009, 95(1): 23-35. DOI:10.1007/s10533-008-9252-1
(  0) 0) |
| [112] |
Portillo M C, Leff J W, Lauber C L, et al. Cell size distributions of soil bacterial and archaeal taxa[J]. Applied and Environmental Microbiology, 2013, 79(24): 7610-7617. DOI:10.1128/AEM.02710-13
(  0) 0) |
| [113] |
Crowther T W, Maynard D S, Crowther T R, et al. Untangling the fungal niche: the trait-based approach[J]. Frontiers in Microbiology, 2014, 5: 579.
(  0) 0) |
| [114] |
Thijs S, Vangronsveld J. Towards an enhanced understanding of plant–microbiome interactions to improve phytoremediation: Engineering the metaorganism[J]. Frontiers in Microbiology, 2016, 7: 341.
(  0) 0) |
| [115] |
Fierer N, Leff J W, Adams B J, et al. Cross-biome metagenomic analyses of soil microbial communities and their functional attributes[J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(52): 21390-21395.
(  0) 0) |
| [116] |
Nemergut D R, Knelman J E, Ferrenberg S, et al. Decreases in average bacterial community rRNA operon copy number during succession[J]. The ISME Journal, 2016, 10(5): 1147-1156. DOI:10.1038/ismej.2015.191
(  0) 0) |
| [117] |
Hall E K, Bernhardt E S, Bier R L, et al. Understanding how microbiomes influence the systems they inhabit[J]. Nature Microbiology, 2018, 3(9): 977-982. DOI:10.1038/s41564-018-0201-z
(  0) 0) |
| [118] |
Schimel J, Balser T C, Wallenstein M. Microbial stress-response physiology and its implications for ecosystem function[J]. Ecology, 2007, 88(6): 1386-1394. DOI:10.1890/06-0219
(  0) 0) |
| [119] |
Kallenbach C M, Frey S D, Grandy A S. Direct evidence for microbial-derived soil organic matter formation and its ecophysiological controls[J]. Nature Communications, 2016, 7(1): 13630. DOI:10.1038/ncomms13630
(  0) 0) |
| [120] |
Malik A A, Puissant J, Goodall T, et al. Soil microbial communities with greater investment in resource acquisition have lower growth yield[J]. Soil Biology and Biochemistry, 2019, 132: 36-39. DOI:10.1016/j.soilbio.2019.01.025
(  0) 0) |
| [121] |
Bouskill N J, Wood T E, Baran R, et al. Belowground response to drought in a tropical forest soil. I. changes in microbial functional potential and metabolism[J]. Frontiers in Microbiology, 2016, 7: 525.
(  0) 0) |
| [122] |
Zhang Y, Wang T, Yan C, et al. Microbial life-history strategies and particulate organic carbon mediate formation of microbial necromass carbon and stabilization in response to biochar addition[J]. Science of the Total Environment, 2024, 950: 175041. DOI:10.1016/j.scitotenv.2024.175041
(  0) 0) |
| [123] |
Wang Q, Ding J, Zhang Z, et al. Rhizosphere as a hotspot for microbial necromass deposition into the soil carbon pool[J]. Journal of Ecology, 2025, 113(1): 168-179. DOI:10.1111/1365-2745.14448
(  0) 0) |
| [124] |
Fan Y, Li T, Liu W, et al. Anthropogenic disturbances consistently favor the high-yield strategists of soil bacterial community in the Eurasian steppe[J]. Annals of Microbiology, 2021, 71(1): 45. DOI:10.1186/s13213-021-01658-0
(  0) 0) |
| [125] |
Li X, Leizeaga A, Rousk J, et al. Recovery of soil microbial metabolism after rewetting depends on interacting environmental conditions and changes in functional groups and life history strategies[J]. Global Change Biology, 2024, 30(10): e17522. DOI:10.1111/gcb.17522
(  0) 0) |
| [126] |
Yang L, Canarini A, Zhang W, et al. Microbial life‐history strategies mediate microbial carbon pump efficacy in response to N management depending on stoichiometry of microbial demand[J]. Global Change Biology, 2024, 30(5): e17311. DOI:10.1111/gcb.17311
(  0) 0) |
| [127] |
Allison S D. Microbial drought resistance may destabilize soil carbon[J]. Trends in Microbiology, 2023, 31(8): 780-787. DOI:10.1016/j.tim.2023.03.002
(  0) 0) |
| [128] |
Bittleston L S, Freedman Z B, Bernardin J R, et al. Exploring microbiome functional dynamics through space and time with trait-based theory[J]. mSystems, 2021, 6(4): e00530-21.
(  0) 0) |
| [129] |
Treseder K K, Alster C J, Cat L A, et al. Nutrient and stress tolerance traits linked to fungal responses to global change[J]. Elementa: Science of the Anthropocene, 2021, 9(1): 00144. DOI:10.1525/elementa.2020.00144
(  0) 0) |
| [130] |
Canarini A, Schmidt H, Fuchslueger L, et al. Ecological memory of recurrent drought modifies soil processes via changes in soil microbial community[J]. Nature Communications, 2021, 12(1): 5308. DOI:10.1038/s41467-021-25675-4
(  0) 0) |
| [131] |
Shentu J L, He Z L, Zeng Y Y, et al. Microbial biomass and PLFA profile changes in rhizosphere of Pakchoi(Brassica chinensis L.) as affected by external cadmium loading[J]. Pedosphere, 2014, 24(4): 553-562. DOI:10.1016/S1002-0160(14)60041-2
(  0) 0) |
| [132] |
Cheng S, Xue W, Gong X, et al. Reconciling plant and microbial ecological strategies to elucidate cover crop effects on soil carbon and nitrogen cycling[J]. Journal of Ecology, 2024, 112(12): 2901-2916. DOI:10.1111/1365-2745.14431
(  0) 0) |
| [133] |
López-Maury L, Marguerat S, Bähler J. Tuning gene expression to changing environments: From rapid responses to evolutionary adaptation[J]. Nature Reviews Genetics, 2008, 9(8): 583-593. DOI:10.1038/nrg2398
(  0) 0) |
| [134] |
Feng H, Fu R, Luo J, et al. Listening to plant's Esperanto via root exudates: Reprogramming the functional expression of plant growth-promoting rhizobacteria[J]. New Phytologist, 2023, 239(6): 2307-2319. DOI:10.1111/nph.19086
(  0) 0) |
| [135] |
Kong Y L, Qin H, Zhu C Q, et al. Research progress on the mechanism by which soil microorganisms affect soil health (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(2): 331-347. [孔亚丽, 秦华, 朱春权, 等. 土壤微生物影响土壤健康的作用机制研究进展[J]. 土壤学报, 2024, 61(2): 331-347.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


