土壤团聚体是土壤结构的基本单位,是评价土壤质量的重要指标之一[1]。土壤团聚体为微生物提供不同的微环境,影响微生物群落结构的组成和功能,进而影响土壤碳、氮的含量和循环[2-3]。土壤团聚体变化受多种因素影响,人为管理和农业活动对其影响最为明显[4-5]。目前集约化的农业管理,如过度施用化肥和农药,虽快速提高了作物产量[6],但对土壤健康造成了不同程度的破坏。有研究表明,长期施用化肥对土壤碳氮等元素含量的影响是多方面的,其中既包括对土壤碳氮含量的直接影响,也包括对土壤微生物群落的间接影响[7]。这些影响会进一步作用于土壤的肥力和生态功能,降低土壤的生产力和稳定性。因此,为了改善土壤健康和提高土壤生产力,必须采取可持续的农业管理措施。
生物质炭是由农林废弃物等生物质材料在缺氧条件和700 ℃以下的热解温度下生产的一种富碳材料[8]。由于其丰富的碳含量,在施入土壤后可提供大量的有机碳,这些有机碳在为土壤微生物提供能量的同时,也作为“黏合剂”影响大团聚体的生成。研究发现,生物质炭施用可显著提高2~0.25 mm粒径团聚体在土壤中的占比,且可显著提高土壤碳氮含量,这与团聚体分布密切相关[9]。土壤养分与团聚体关系密切,这与团聚体内的微生物有着重要关系,而不同大小的微生物聚集体对土壤养分含量的影响可能不同[10-11]。有研究表明,通过长期保护性耕作增加土壤大团聚体中微生物群落的丰度,可提高土壤团聚体的有机碳、碳氮比以及含水量[12]。此外,团聚体的大小、养分含量、含水量的不同可显著影响土壤微生物的栖息环境[13-14]。目前,生物质炭施入灌区农田的研究主要集中在其施用短期内对土壤理化性质、酶活性等方面的影响,其中,过氧化氢酶活性反映土壤清除活性氧、维持氧化还原平衡的能力,影响有机质分解和养分循环[15];蔗糖酶活性表征土壤碳转化强度,直接关系有效碳源的供应[16];脲酶活性则主导尿素等有机氮向植物可利用铵态氮的转化效率,是评价土壤氮素供应潜力的重要指标[17]。这些酶活性共同构成了反映土壤肥力生物活性的核心指标。但对生物质炭施入后土壤团聚体分布、团聚体稳定性和土壤团聚体碳氮含量变化及其团粒结构中土壤微生物群落结构的了解仍然有限,因此,开展生物质炭施入对北疆灌区农田土壤团聚体微生物群落、团聚体碳氮含量的影响及其持续效应研究具有重要意义。
本研究基于定位试验,分析在北疆灌区麦田施用不同量生物质炭:不施生物质炭(B0)、生物质炭施用10 t·hm–2(B1)、生物质炭施用20 t·hm–2(B2)三年后土壤团聚体有机碳、全氮、微生物生物量碳氮及其相关酶和微生物群落的变化。利用16S rRNA基因和内转录间隔区(ITS)高通量测序等技术,通过对土壤微生物共生网络和群落组成分析,探讨生物质炭施用后土壤微生物多样性的变化及其对土壤团聚体碳氮组分含量及碳氮转运酶活性的影响。旨在澄清三个问题:(1)不同生物质炭施用量对土壤团聚体有机碳及全氮含量的影响如何?(2)不同生物质炭施用量对土壤团聚体内的微生物群落结构的影响如何?(3)不同生物质炭量对土壤团聚体内微生物网络稳定性有何改变?研究可为评价生物质炭在灌区农田改善土壤结构、提升地力及固碳等方面的长期应用提供可靠的理论和数据支撑。
1 材料与方法 1.1 试验地概况本研究在新疆维吾尔自治区奇台县麦类试验站(42°45′—45°29′N,89°13′—91°22′E,海拔1 760 m)进行。该地区属于温带大陆性气候,年均降水量265.6 mm,年平均最高气温15 ℃,年平均最低气温3 ℃,无霜期153 d。试验地土壤为沙壤土,成土母质为冲积物,在中国土壤系统分类中属于灌淤土,土壤团聚体结构详见表 1,pH 8.25,土壤基础养分含量:全氮1.14 g·kg–1,全磷1.23 g·kg–1,全钾28.16 g·kg–1,有机质20.85 g·kg–1,碱解氮61.02 mg·kg–1,有效磷18.54 mg·kg–1,速效钾147.0 mg·kg–1。
|
|
表 1 土壤团聚体机械分布及稳定性 Table 1 Distribution and stability of soil mechanical aggregates |
研究所用玉米秸秆生物质炭购自金和福农业科技股份有限公司。其制备方法为:将玉米秸秆经风干、粉碎后,于450 ℃的限氧条件下热解炭化4 h,冷却后破碎过筛,获得0.05~2.00 cm的颗粒状产品。所得产物pH9.3,全氮21.8 g·kg–1,碱解氮5.4 mg·kg–1,有效磷200.9 mg·kg–1。固定碳含量为687 g·kg–1,全碳757.6 g·kg–1,挥发分含量为206 g·kg–1,灰分106 g·kg–1。
1.3 试验设计定位试验采用随机区组设计,设3个生物质炭用量:不施生物质炭(B0)、生物质炭10 t·hm–2(B1)、生物质炭20 t·hm–2(B2)。各小区面积为9 m2(3 m× 3 m),三次重复,共9个小区。生物质炭于2021年4月作为基肥通过旋耕机一次性施入试验田,后续再无添加。氮肥用量为258 kg·hm–2(纯N),其中,50%作为基肥施入,剩余50%分别在春小麦拔节期和孕穗期按照6︰4质量比追施。春小麦选用当地主栽品种新春37号,于2023年4月采用20 cm等行距条播,播种量为每公顷450万株。田间管理措施均与大田常规操作保持一致。
1.4 土壤团聚体采集及筛分春小麦成熟期(8月1日),去除取样点上层石块及凋落物后,采用“S”形五点取样法在小区选取5个取样点,在每个取样点使用直径8 cm的土钻在0~30 cm土层钻取土样,并将所取土样混合均匀,放入保温箱带回实验室。通过改良的干筛新鲜土壤方法[14]分离出三种团聚体尺寸(> 2 mm、2~0.25 mm、< 0.25 mm)。土样运至实验室后,立即放在无菌超净工作台上,称量约1 kg新鲜土壤,依次通过2 mm和0.25 mm无菌标准筛,人工筛分,时间为2~3 min,静置1 min,收集各层筛面上的土壤团聚体分别称重,记录并装袋。将不同粒径团聚体分成两部分,一部分放在–80 ℃超低温冰箱中用于随后的微生物DNA提取,另一部分用于测定团聚体中养分指标和酶活性指标。
1.5 土壤化学分析土壤有机碳采用H2SO4-K2Cr2O7外加热法测定;全氮采用半微量凯氏定氮法测定,并使用半自动凯氏定氮仪(KDN-520,KEFEI,上海)进行分析。土壤蔗糖酶和脲酶活性分别采用3,5-二硝基水杨酸比色法和苯酚钠-次氯酸钠比色法测定,其吸光度均使用BIOLOG MicroStation读数仪(GEN Ⅲ型,美国)读取。土壤过氧化氢酶活性采用高锰酸钾滴定法测定。微生物生物量碳(MBC)和微生物生物量氮(MBN)采用氯仿熏蒸—K2SO4提取法提取后,使用可溶性碳氮测定仪(Multi N/C 3000,德国)进行测定。所有测定方法的具体操作步骤均参考《土壤农化分析》[18]。
1.6 土壤微生物测定土壤样本经干冰冷冻运输至北京百迈克生物技术有限公司进行后续分析。使用TGuide® S96磁性土壤/粪便DNA提取试剂盒(天津生物技术(北京)有限公司)提取土壤细菌和真菌总DNA。细菌16S rRNA基因的V3~V4高变区采用引物对338F(5'-ACTCCTACGGGAGGCAGCA-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')进行PCR扩增。真菌内转录间隔区(ITS)rRNA基因区域采用引物ITS1(5'-CTGTCATTAGGGAGAGAGA-3')和ITS2(5'-GCTGCGTTCTTCATCGATGA-3')进行PCR扩增。扩增产物在Illumina MiSeq平台上进行高通量测序,以测定土壤细菌和真菌群落的丰度与多样性。测序完成后,在97%相似度阈值下,利用USEARCH软件将序列聚类为操作分类单元(OTU),并移除了相对丰度低于0.005%的稀有OTU。基于SILVA参考数据库,通过核糖体数据库计划(Ribosomal Database Project,RDP)分类器对OTU代表序列进行比对与分类学注释,从而获得各OTU的物种分类信息。原始序列已上传到国家生物中心(CNCB)阅读序列档案(GSA)数据库,登录号为PRJCA049190。
1.7 数据处理采用SPSS 25.0软件进行数据处理,通过单因素方差分析(one-way ANOVA)与邓肯(Duncan)多重比较法,检验不同改良处理间的差异显著性(P < 0.05)。α多样性分别由QIIME2和Origin 2021软件计算和显示。采用主坐标分析法(PCoA)分析β多样性。采用R中的“igraph”软件包进行斯皮尔曼(Spearman)相关性分析,计算微生物OTU之间的相关性,构建具有显著相关性(| R | > 0.6,P < 0.05)的OTU之间的相关性网络。最后利用R中的“igraph”软件包计算微生物网络拓扑系数。
2 结果 2.1 生物质炭用量对土壤团聚体碳氮和微生物生物量碳氮含量影响由表 2可知,在B0条件下,有机碳主要分布在小于0.25 mm团聚体中,2~0.25 mm团聚体次之,大于2 mm团聚体最少。生物质炭施用可显著提高大于2 mm团聚体和2~0.25 mm团聚体有机碳含量,两种团聚体径粒分别在B2条件下有机碳含量达到最高,与B0相比分别提升了76.60%和41.28%。生物质炭施用对小于0.25 mm团聚体有机碳含量影响不显著,在B1条件下达到最大值。生物质炭施用对土壤团聚体全氮含量的影响不显著,但2~0.25 mm团聚体和小于0.25 mm团聚体全氮含量随着生物质炭的施用呈上升趋势,大于2 mm团聚体全氮含量随着生物质炭施用呈先上升后下降的趋势,在B1达到最高。大于2 mm团聚体碳氮比随生物质炭施用量的增加而增大,其中,B1和B2较B0处理分别显著升高42.07%和127.91%。
|
|
表 2 不同生物质炭施用条件下土壤团聚体OC、TN、MBC、MBN及C/N Table 2 OC, TN, MBC, MBN and C/N of soil aggregates under different biochar application conditions |
大于2 mm团聚体中MBC含量随着生物质炭的施用量增加呈上升趋势,在B2达到最高值,与B0对照组相比,B1和B2处理分别提高7.22%和11.07%;2~0.25 mm团聚体和小于0.25 mm团聚体中MBC含量随着生物质炭的施用呈降低趋势,其中B1生物质炭施用量显著降低了小于0.25 mm团聚体中MBC含量,B1处理相较B0显著降低34.01%。
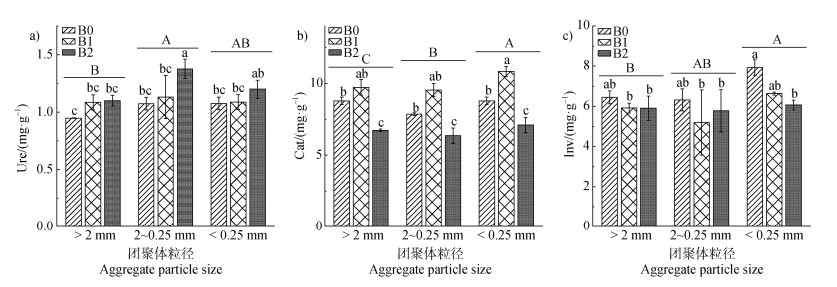
2.2 生物质炭用量对土壤团聚体酶活性的影响在2~0.25 mm土壤团聚体中,脲酶活性随着生物质炭用量的增加显著升高,其中B2处理的脲酶活性高于B0处理28.26%(图 1a)。过氧化氢酶活性随着生物质炭的施用呈先上升后降低的趋势,在B1条件下达到最高,B1处理土壤团聚体3种粒级过氧化氢酶活性分别高于B0处理10.64%、21.43%和23.40%。在生物质炭施用量较高(B2)时,土壤团聚体3种粒级中过氧化氢酶活性会显著降低,与B0相比分别降低23.40%、19.05%和19.15%(图 1b)。蔗糖酶活性随着生物质炭的施用呈下降趋势,生物质炭施用对大于2 mm团聚体和2~0.25 mm团聚体中蔗糖酶活性无显著影响,但小于0.25 mm团聚体中蔗糖酶活性随着生物质炭的施用呈显著下降趋势,其中B2相较B0处理降低23.53%(图 1c)。
|
注:图中大写字母为各团聚体间差异显著(P < 0.05);小写字母为各团聚体和生物质炭处理间差异显著(P < 0.05)。下同。 Note: In the figure, uppercase letters indicate significant differences between aggregates(P < 0.05);Lowercase letters indicate significant differences among biochar and aggregate treatments(P < 0.05). The same below. 图 1 不同生物质炭施用条件下土壤团聚体酶活性差异(a. 脲酶(Ure),b. 过氧化氢酶(Cat),c. 蔗糖酶(Inv)) Fig. 1 Differences in enzyme activity of soil aggregates under different biochar application conditions(a. Urease(Ure), b. Catalase(Cat), c. Invertase(Inv)) |
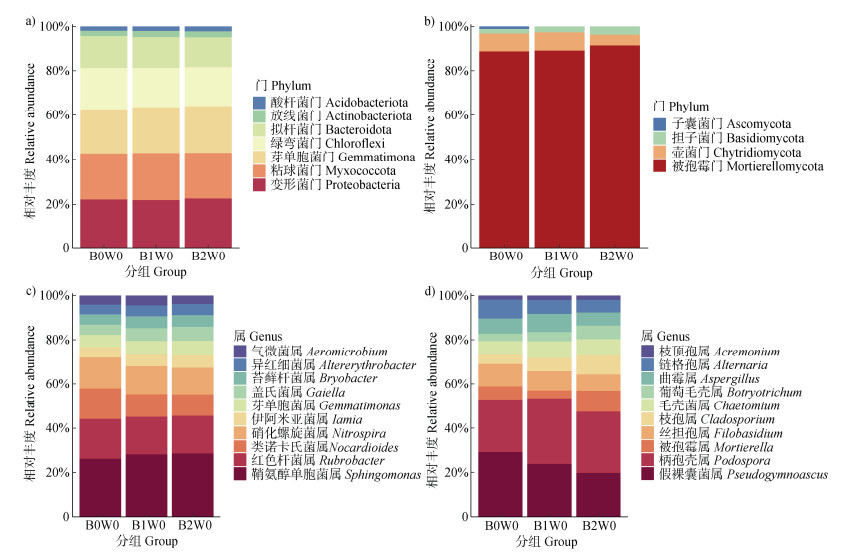
采用Spearman相关性对本研究中土壤团聚体中微生物组成进行分析,并从门和属水平上选择相对丰度前十的细菌和真菌作为优势种(图 2)。土壤团聚体细菌共检测到38门、99纲、292目、604科、1 162属,其中变形菌门(21.21%~21.73%)、放线菌门(19.41%~21.24%)、酸杆菌门(17.22%~18.96%)、芽单胞菌门(12.4%~13.73%)、绿弯菌门(10.59%~11.84%)为优势菌门(平均丰度大于5%)。真菌含17门、56纲、142目、336科、860属。
|
图 2 不同生物质炭施用条件下土壤团聚体微生物群落组成差异(a. 细菌群落门水平组成,b. 真菌群落门水平组成,c. 细菌群落属水平组成,d. 真菌群落属水平组成) Fig. 2 Differences in microbial species composition of soil aggregates under different biochar application conditions(a. The composition of the bacterial community at the phylum level, b. The composition of the fungal community at the phylum level, c. The composition of the bacterial community at the genus level, d. The composition of the fungal community at the genus level) |
与B0相比,施用生物质炭可增加大多数土壤细菌门水平的相对丰度。变形菌门、放线菌门和拟杆菌门随着生物质炭的施用呈先上升后降低的趋势,在B1生物质炭施用量下达到最高,相反绿弯菌门和芽单胞菌门随着生物质炭的施用呈下降趋势。土壤真菌优势真菌门主要为子囊菌门(72.92%~76.26%)、担子菌门(9.59%~14.87%)、被孢霉门(2.58%~3.36%)、壶菌门(1.18%~5.51%)、球囊菌门(1.35%~2.08%),其中,子囊菌门和担子菌门随着生物质炭的施用呈下降的趋势,在B2生物质炭量下达到最低,被孢霉门、壶菌门和球囊菌门随着生物质炭的施用呈先上升后下降的趋势,在B1生物质炭量下达到最高。
就属水平而言,施用生物质炭同样可增加大多数土壤细菌属水平的相对丰度。芽单胞菌属为细菌群的主要菌群,占总丰度的6.30%~10.56%,前十种细菌属中,芽单胞菌属和维西纳米杆菌随着生物质炭的施用呈上升趋势,在B2达到最高,鞘氨醇单胞菌随着生物质炭的施用呈先上升后下降的趋势,在B1达到最高。土壤优势真菌属为柄孢壳菌属(3.14%~14.81%)、枝孢菌属(1.71%~13.30%),土壤真菌群落属水平相对丰度与细菌呈相反的趋势,除枝孢菌属相对丰度随着生物质炭施用增高外,生物质炭对其余真菌群落相对丰度影响不显著。
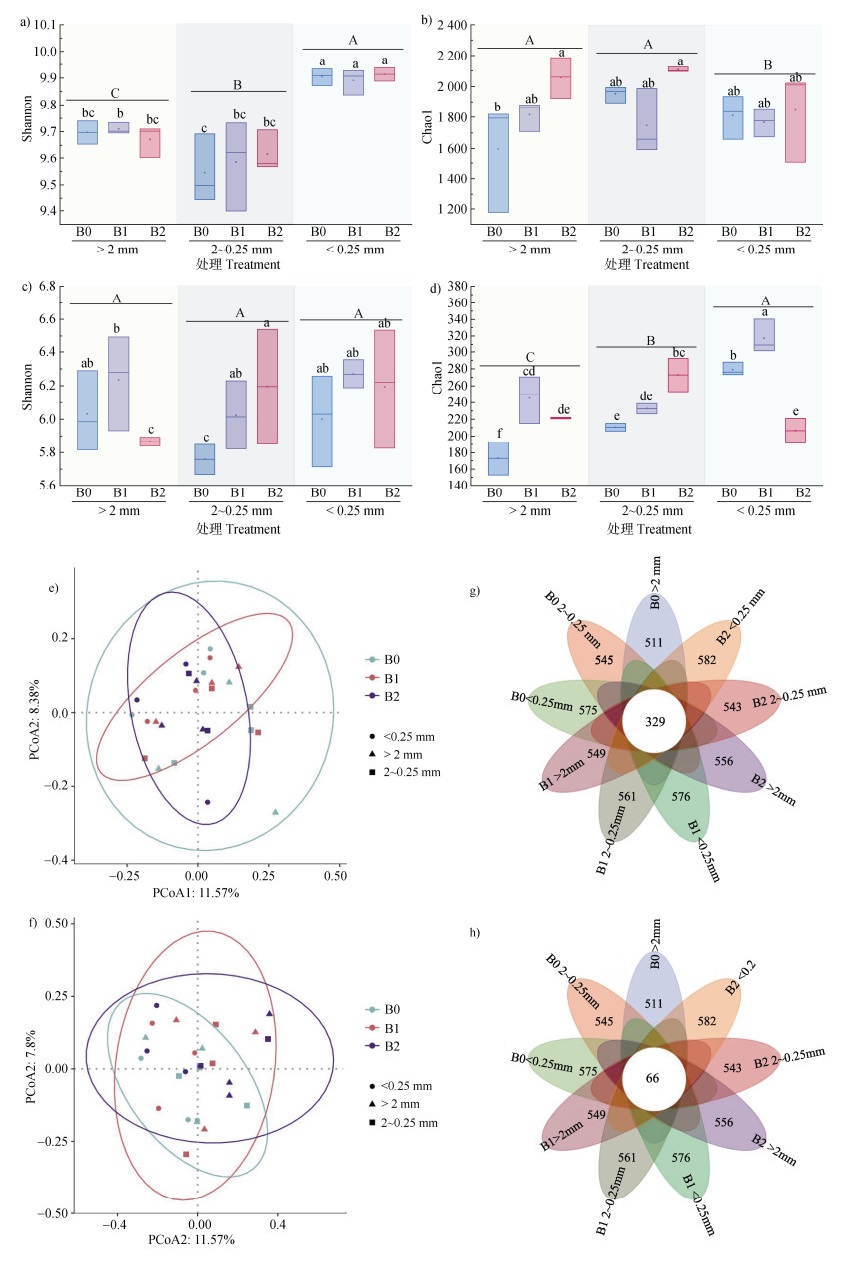
2.4 生物质炭用量对土壤团聚体微生物群落及多样性影响进一步分析土壤团聚体中微生物群落及其多样性(图 3)可知,细菌Shannon指数随着团聚体粒径的减小显著升高,且在大于2 mm团聚体和2~0.25 mm团聚体粒径下,细菌Shannon指数随着生物质炭的施用呈上升趋势。细菌Chao1指数随团聚体粒径的减小呈下降趋势,微团聚体细菌Chao1指数与大团聚体相比显著降低,在大团聚体中,细菌Chao1值随着生物质炭的施用显著提高,且在B2生物质炭施用量下达到最高值。各粒径团聚体之间真菌Shannon指数无显著差异,各粒径团聚体真菌Shannon指数均随着生物质炭的施用呈增加趋势;各粒径团聚体之间真菌Chao1指数随着团聚体粒径的减小显著提高,大于2 mm和小于0.25 mm团聚体真菌Chao1指数随着生物质炭的施用呈先增加后降低的趋势,在B1生物质炭施用量下达到最高,2~0.25 mm团聚体则随着生物质炭的施用显著提高,在B2生物质炭施用条件下达到最高。
|
注:图a)和图b)为不同生物质炭施用条件下细菌α-多样性;图c)和图d)为真菌α-多样性;图e)为土壤细菌群落组成的主成分分析(PCoA);图f)为土壤真菌群落组成d的PCoA分析;基于β-多样性差异细菌群落(g)和真菌群落(h)中常见和独特的OTU数量。 Note: Fig. a)and Fig. b)are bacterial α-diversity under different biochar application conditions; Fig. c)and Fig. d)are fungal α-diversity; Fig. e)is Principal Coordinates Analysis analysis of soil bacterial community composition; Fig. f)is PCoA analysis of soil fungal community composition; Based on β-diversity differences, the number of common and unique OTUs in bacterial communities(g)and fungal communities(h). 图 3 不同生物质炭施用条件下土壤团聚体微生物多样性差异 Fig. 3 Differences in microbial α-diversity of soil aggregates under different biochar application conditions |
OTU水平上的PCoA在不同生物质炭施用量下对不同团聚体的微生物组成并无显著影响(图 3e,图 3f)。但由图 3g和图 3h可知,细菌各粒级团聚体特有OTU数量在生物质炭施用后均呈现增加趋势,并在B2生物质炭施用量下达到最高;真菌各粒级团聚体特有OTU数量随着生物质炭的施用呈下降趋势,并在B2生物质炭施用量下达到最低。
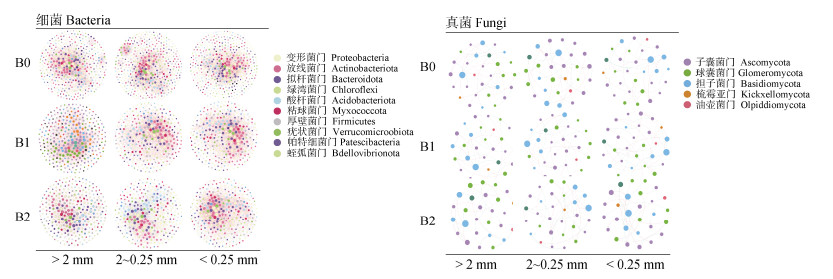
2.5 生物质炭用量对土壤团聚体微生物网络影响通过分析土壤团聚体微生物共生网络图(图 4)可知,细菌的网络OTU较真菌OTU更紧密和丰富,并且存在更多的正相关性。不同团聚体大小的细菌网络在B0生物质炭施用量下相对分散,表明B1生物质炭土壤微生物网络复杂性最高,抗外界环境干扰的稳定性更强。B0的网络复杂性最低,土壤细菌和真菌之间的协同作用可能较弱。在B0条件下,三种粒径团聚体主要以放线菌门起到连接作用,随着生物质炭施用,疣微菌门更多地参与微生物网络连接。
|
注:在门水平上土壤微生物的共生网络,一个连接表示强(Spearman's r > 0.6)和显著(P < 0.05)相关。红边和绿边分别表示正相关和负相关。每个节点的大小与连接数成正比。节点的颜色代表它们在门水平上的分类。 Note: At the phylum level, a symbiotic network of soil microorganisms is strongly(Spearman's r > 0.6)and significantly(P < 0.05)correlated. The red and green edges represent positive and negative correlations, respectively. The size of each node is proportional to the number of connections. The color of the nodes represents their classification at the phylum level. 图 4 不同生物质炭施用条件下土壤团聚体微生物共生网络 Fig. 4 Microbial symbiosis network of soil aggregates under different biochar application conditions |
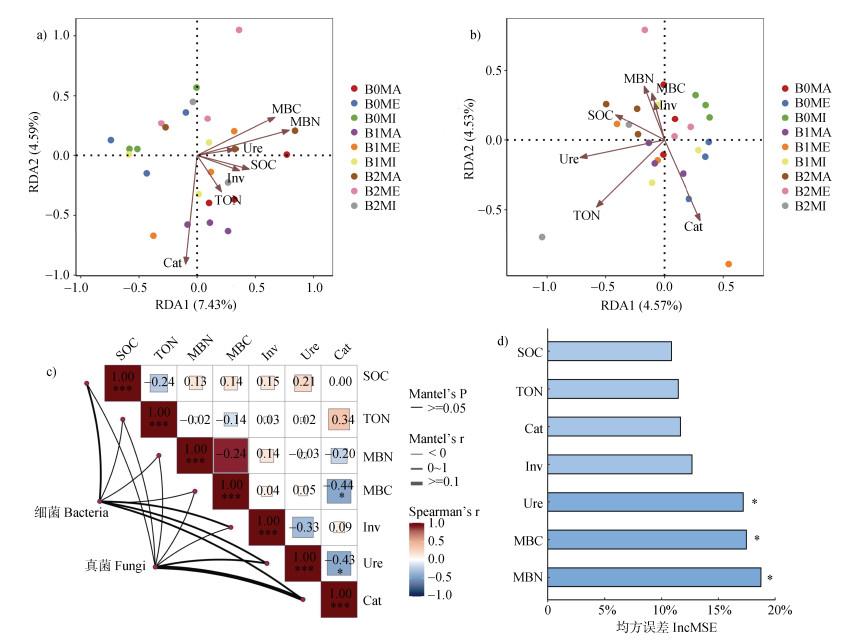
本研究使用冗余分析(RDA)探究土壤团聚体化学因素与土壤团聚体细菌和真菌群落之间的关系(图 5a,图 5b)。RDA的前两个轴分别解释了土壤细菌和真菌群落总变化的12.02%和9.1%。细菌群落和真菌群落的相对丰度与除土壤蔗糖酶外的其他指标均呈正相关。其中,细菌群落与MBC和MBN密切相关,真菌群落与全氮和脲酶的相关性更强。为了进一步探索微生物群落结构对土壤生化特性的影响,本研究进行了曼特尔(Mantel)分析并建立了两者之间的联系(图 5c)。结果表明:土壤团聚体中细菌和真菌群落受土壤团聚体中3种酶的影响大于其他理化因子。其中,细菌群落受过氧化氢酶影响最大,其次是蔗糖酶和脲酶。真菌群落表现出与细菌群落相同的趋势。随机森林算法用于对影响微生物群落丰度的各种因素进行关联和排序。MBN是影响微生物群落丰度的最重要因素,其次是MBC和脲酶(图 5d)。
|
注:a)土壤细菌群落结构和环境因子的冗余分析(RDA),b)土壤真菌群落结构和环境因子的RDA,c)土壤微生物群的水平结构和土壤理化因素的曼特尔(Mantel)分析,d)对微生物活动影响因素的随机森林模型。其中,ME为大于2 mm粒级团聚体;MA为2~0.25 mm粒级团聚体;MI为小于0.25 mm粒级团聚体。具有统计学意义的结果标记为*(P < 0.05)。 Note: a)Redundancy analysis(RDA)of soil bacterial community structure and environmental factors, b)RDA of soil fungal community structure and environmental factors, c)Mantel analysis of the horizontal structure of soil microbial communities and soil physicochemical factors, d)Random forest model of factors affecting microbial activity. Here, ME refers to aggregates larger than 2 mm; MA refers to aggregates of 2-0.25 mm; MI refers to aggregates smaller than 0.25 mm. Results with statistical significance are marked as *(P < 0.05). 图 5 土壤团聚体微生物与环境因子的关系 Fig. 5 Microbial symbiosis network of soil aggregates under different biochar application conditions |
土壤团聚体作为稳定和保护有机碳、氮的载体,其粒径大小的不同也会导致土壤团聚体对有机碳、氮的储存能力不同。本研究显示,三种团聚体有机碳总体主要分布在微团聚体中(< 0.25 mm),团聚体有机碳随着生物质炭的施用显著提高,而团聚体中全氮含量变化不显著(表 2),这与Zhang等[19]的研究结果相似。分析可能原因是,土壤有机碳在不同粒径团聚体中的固定与保存机制存在差异:大团聚体更利于其快速周转,而微团聚体则通过减缓周转速率来实现长期封存[20-22]。因此,小于0.25 mm团聚体对有机碳的保护能力更高,有机碳含量也相对更高。同时,因为生物质炭自身的理化性质,施入土壤后为各粒级团聚体带来大量碳源,而这些外来碳源由于中大型团聚体有更大的可直接接触面积,则优先附着于大于2mm和2~0.25 mm团聚体上[23]。本研究也发现,施用生物质炭后大于2 mm和2~0.25 mm团聚体有机碳增长率高于小于0.25mm团聚体(表 2)。此外,2~0.25 mm团聚体MBC和MBN含量较大于2 mm和2~0.25 mm团聚体更低(表 2),这与赵吉霞等[24]的研究结果不吻合,分析认为,2~0.25 mm团聚体有机碳含量低有两点原因:其一是,大于2 mm团聚体相较2~0.25 mm团聚体体积更大,孔隙结构允许微生物进入,同时,大团聚体外层形成的物理屏障减少了有机质的分解速率[25];其二是,小于0.25 mm团聚体富含矿物结合态有机质(MAOM),通过铁铝氧化物或黏粒表面吸附,形成稳定复合体[26]。土壤团聚体通过控制不同粒级中有机质的可接触性、微生物群落组成、水分等因素直接影响着土壤酶的活性。本研究显示,三种酶在三种团聚体条件下,均表现出小于0.25 mm团聚体最大,2~0.25 mm团聚体次之,大于2 mm团聚体最小的趋势(图 1)。这是因为,土壤酶活性主要来自土壤微生物的代谢活动,而分布在小于0.25 mm团聚体中的微生物由于有机碳含量较其他粒径团聚体高(表 2),这些有机碳为微生物的生长提供更充足的能量,导致酶活性均在小于0.25 mm团聚体更高。此外,脲酶和过氧化氢酶活性随着生物质炭施用后提高(图 1),分析可能原因除了生物质炭可为土壤提供额外碳源,帮助微生物生长繁殖外,生物质炭具有较大的比表面积和吸附能力,可吸附土壤中的酶分子,减少酶的降解,从而保护酶的活性[27]。
本研究中,施用生物质炭对团聚体的微生物群落结构影响较小(图 2),但就细菌群落结构组成而言,变形菌门、放线菌门、酸杆菌门等作为土壤中富营养群类,可通过有效利用生物质炭带来的碳源而快速繁殖和增长(图 2),说明生物质炭对土壤微生物有正向的作用,这与Zhang等[28]研究结果相似。本研究发现,施用生物质炭可提高细菌的多样性(图 3a,图 3b),说明在适度施用生物质炭的水平下细菌多样性最大。施用生物质炭后,土壤养分的增加直接带动微生物多样性的增加,微生物的增加可大幅度改善土壤环境[29]。即,施用生物质炭后,微生物群落结构与土壤环境因子之间存在正反馈关系,两者协同改善土壤质量[28]。这与Bai等[30]的研究结果一致。但生物质炭施用并未显著改变土壤团聚体内的群落组成差异(图 3e,图 3f),分析可能原因有两点;一是由于生物质炭自身具有高化学稳定性和复杂的芳香化结构,这使它在土壤中的分解速度较慢,因此,对微生物群落的直接影响可能不如预期的显著[31]。由于生物质炭的碳含量高且化学惰性,它在土壤中形成了一个相对惰性的碳库,不易被微生物快速利用;二是土壤微生物群落对生物质炭的施用存在一定的适应性,能够在新的环境中重新适应,进而影响微生物的生长繁殖并改变其结构和组成[32],这种变化可能在短时间内并不显著。然而,生物质炭的施用会改变微生物群落中常见和独特的OTU数量,三种团聚体粒级中的细菌特有OTU随着生物质炭施用的增加而增加,真菌则是随着生物质炭施用的增加而减少(图 3g,图 3h)。
通过土壤微生物共生网络图发现,土壤微生物并不能够单独在土壤中生存;它们通过构建复杂的相互作用网络来维持自身的生存和繁衍。网络分析更好地了解微生物之间的复杂关系,微生物群落之间的相互作用可反映土壤养分的固存和分解[33]。有研究发现,施用生物质炭可提高微生物网络的复杂性,提高微生物对碳、氮的代谢效率[34]。本研究结果显示,适量的生物质炭施用(B1)可提高大于2 mm和2~0.25 mm粒径团聚体的网络复杂性(图 4),然而生物质炭施用对真菌的影响较小(图 4),分析可能原因有两点:一是因为土壤真菌种类较少,相对地,不同真菌物种之间的竞争压力较小,每种真菌可更稳定地占据其特定的生态位,获取所需的养分和生存空间,从而在面对环境变化时,能够更好地维持自身的生长和功能[35];二是真菌网络复杂性更低,当环境发生变化时,网络中的某些节点或连接可能受到影响,但由于整体结构简单,其他部分仍能保持稳定,从而维持整个群落的功能[36]。
4 结论从生物质炭施用中长期持续效应考虑,施用10 t·hm–2生物质炭(B1)三年后,可通过优化团聚体碳氮分布、提升细菌多样性及增强大团聚体微生物网络稳定性,更有效改善土壤结构与地力,为北疆灌区农田固碳及可持续土壤管理提供理论依据。
| [1] |
Wang Q K, Wang S L. Forming and stable mechanism of soil aggregate and influencing factors (In Chinese)[J]. Chinese Journal of Soil Sciences, 2005, 36(3): 415-421. [王清奎, 汪思龙. 土壤团聚体形成与稳定机制及影响因素[J]. 土壤通报, 2005, 36(3): 415-421.]
(  0) 0) |
| [2] |
Ji W Y, Guan D R, Mi L F, et al. Effects of different land use patterns on soil aggregate stability and carbon and nitrogen content (In Chinese)[J]. Bulletin of Soil and Water Conservation, 2024, 44(6): 377-386. [季卫英, 管丹蓉, 宓立峰, 等. 不同土地利用方式对土壤团聚体稳定性及碳氮含量的影响[J]. 水土保持通报, 2024, 44(6): 377-386.]
(  0) 0) |
| [3] |
Wang X, Qi J Y, Jing Z H, et al. Effects of long-term conservation tillage on soil aggregate stability and carbon and nitrogen in paddy field (In Chinese)[J]. Transactions of the Chinese Society of Agricultural Engineering, 2019, 35(24): 121-128. [王兴, 祁剑英, 井震寰, 等. 长期保护性耕作对稻田土壤团聚体稳定性和碳氮含量的影响[J]. 农业工程学报, 2019, 35(24): 121-128.]
(  0) 0) |
| [4] |
Liu Y L, Wang P, Wang J K. Formation and stabilization mechanism of soil aggregates: Research progress and prospects (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(3): 627-643. DOI:10.11766/trxb202112180686 [刘亚龙, 王萍, 汪景宽. 土壤团聚体的形成和稳定机制: 研究进展与展望[J]. 土壤学报, 2023, 60(3): 627-643.]
(  0) 0) |
| [5] |
Bai Y H, Hou S S, Zhao Y P, et al. Soil organic carbon accumulation and aggregate stabilization processes and their interactions (In Chinese)[J]. Soil and Fertilizer Sciences in China, 2024(7): 208-220. [白懿杭, 侯赛赛, 赵玉璞, 等. 农田土壤有机碳积累和团聚体稳定过程及其相互作用关系[J]. 中国土壤与肥料, 2024(7): 208-220.]
(  0) 0) |
| [6] |
Lu Y, Wei Q Q, Xu Q S, et al. Effects of chemical fertilizer reduction combined with bio-organic fertilizer on rice yield, soil structure and soil carbon sequestration and sequestration capacity (In Chinese)[J]. Soil and Fertilizer Sciences in China, 2024(11): 114-121. [芦燕, 魏倩倩, 徐青山, 等. 化肥减量配施生物有机肥对水稻产量、土壤结构和土壤固碳增汇能力的影响[J]. 中国土壤与肥料, 2024(11): 114-121.]
(  0) 0) |
| [7] |
Wang W Y, Shen P F, Zhang H P, et al. Study on the relationship between total nitrogen and nitrogen functional microorganisms in soil aggregates under long-term conservation tillage (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(6): 1653-1667. DOI:10.11766/trxb202307120214 [王威雁, 沈鹏飞, 张侯平, 等. 长期保护性耕作下土壤团聚体全氮与氮功能微生物关系研究[J]. 土壤学报, 2024, 61(6): 1653-1667.]
(  0) 0) |
| [8] |
Chen W F, Zhang W M, Meng J. Research progress and prospect of agricultural biochar (In Chinese)[J]. Scientia Agricultura Sinica, 2013, 46(16): 3324-3333. [陈温福, 张伟明, 孟军. 农用生物炭研究进展与前景[J]. 中国农业科学, 2013, 46(16): 3324-3333.]
(  0) 0) |
| [9] |
Yue F X, Li J W, Qiao X X, et al. Effects of biochar on stability of soil aggregates and distribution of carbon and nitrogen in farmland in hilly areas of western Henan (In Chinese)[J]. Journal of Soil and Water Conservation, 2019, 33(6): 265-272. [悦飞雪, 李继伟, 乔鑫鑫, 等. 生物炭对豫西丘陵区农田土壤团聚体稳定性及碳、氮分布的影响[J]. 水土保持学报, 2019, 33(6): 265-272.]
(  0) 0) |
| [10] |
Chaplot V, Cooper M. Soil aggregate stability to predict organic carbon outputs from soils[J]. Geoderma, 2015, 243: 205-213.
(  0) 0) |
| [11] |
Keiluweit M, Nico P S, Kleber M, et al. Are oxygen limitations under recognized regulators of organic carbon turnover in upland soils?[J]. Biogeochemistry, 2016, 127(2/3): 157-171.
(  0) 0) |
| [12] |
Zhang X F, Xin X L, Zhu A N, et al. Linking macroaggregation to soil microbial community and organic carbon accumulation under different tillage and residue managements[J]. Soil & Tillage Research, 2018, 178: 99-107.
(  0) 0) |
| [13] |
Lehmann J, Kleber M. The contentious nature of soil organic matter[J]. Nature, 2015, 528(7580): 60-68. DOI:10.1038/nature16069
(  0) 0) |
| [14] |
Jiang Y J, Qian H Y, Wang X Y, et al. Nematodes and microbial community affect the sizes and turnover rates of organic carbon pools in soil aggregates[J]. Soil Biology & Biochemistry, 2018, 119: 22-31.
(  0) 0) |
| [15] |
Chen X X, Geng Z C, Wang S, et al. Characteristics of soil microbial and enzyme activities in soil after biochar application (In Chinese)[J]. Journal of Agro-Environment Science, 2014, 33(4): 751-758. [陈心想, 耿增超, 王森, 等. 施用生物炭后塿土土壤微生物及酶活性变化特征[J]. 农业环境科学学报, 2014, 33(4): 751-758.]
(  0) 0) |
| [16] |
Zhang J P, Su S P, Liu X E, et al. Soil organic carbon components and enzyme activities of different stand types in the north and south mountains of Lanzhou City (In Chinese)[J]. Chinese Journal of Ecology, 2024, 43(8): 2357-2367. [张建鹏, 苏世平, 刘小娥, 等. 兰州市南北两山不同林分类型土壤有机碳组分及酶活性[J]. 生态学杂志, 2024, 43(8): 2357-2367.]
(  0) 0) |
| [17] |
Jiang Y Z, Cui X Y, Zhang Y, et al. Effects of different organic materials on nutrient accumulation and soil microbial characteristics of maize (In Chinese)[J]. Journal of Plant Nutrition and Fertilizer, 2025, 31(5): 943-955. [蒋雨洲, 崔馨宇, 张燕, 等. 配施不同有机物料对玉米养分积累及土壤微生物特征的影响[J]. 植物营养与肥料学报, 2025, 31(5): 943-955.]
(  0) 0) |
| [18] |
Bao S D. Soil and agricultural chemistry analysis (In Chinese). 3rd ed[M]. Beijing: China Agriculture Press, 2000: 111-119. [鲍士旦. 土壤农化分析[M]. 3版. 北京: 中国农业出版社, 2000: 111-119.]
(  0) 0) |
| [19] |
Zhang H J, Wang S J, Zhang J X, et al. Biochar application enhances microbial interactions in mega-aggregates of farmland black soil[J]. Soil and Tillage Research, 2021, 213: 105145. DOI:10.1016/j.still.2021.105145
(  0) 0) |
| [20] |
Liu Y L, Wang P, Ding Y J, et al. Microbial activity promoted with organic carbon accumulation in macroaggregates of paddy soils under long-term rice cultivation[J]. Biogeosciences, 2016, 13(24): 6565-6586. DOI:10.5194/bg-13-6565-2016
(  0) 0) |
| [21] |
Wang P, Liu Y L, Li L Q, et al. Long-term rice cultivation stabilizes soil organic carbon and promotes soil microbial activity in a salt marsh derived soil chronosequence[J]. Scientific Reports, 2015, 5(1): 15704. DOI:10.1038/srep15704
(  0) 0) |
| [22] |
Zhu M T, Yuan L, Zhou F, et al. Time-dependent regulation of soil aggregates on fertilizer N retention and the influence of straw mulching[J]. Soil Biology & Biochemistry, 2024, 198: 109551.
(  0) 0) |
| [23] |
Kuzyakov Y, Bogomolova I, Glaser B, et al. Biochar stability in soil: Decomposition during eight years and transformation as assessed by compound-specific 14C analysis[J]. Soil Biology & Biochemistry, 2014, 70: 229-236.
(  0) 0) |
| [24] |
Zhao J X, Jiu J J, Li Y M, et al. Effects of maize–soybean intercropping on microbial biomass carbon and nitrogen of red soil aggregates on sloping farmland (In Chinese)[J]. Science of Soil and Water Conservation in China, 2025, 23(1): 150-158. [赵吉霞, 酒鹃鹃, 李永梅, 等. 玉米–大豆间作对坡耕地红壤团聚体微生物生物量碳氮的影响[J]. 中国水土保持科学, 2025, 23(1): 150-158.]
(  0) 0) |
| [25] |
Witzgall K, Vidal A, Schubert, D I, et al. Soil microaggregates store more carbon and are more sensitive to physical disturbance than macroaggregates in a conventional tillage system[J]. Science Advances, 2021, 7(5): eabd6806.
(  0) 0) |
| [26] |
Ye X M, Gao G N, Zhang W, et al. Effects of biochar addition on soil phosphorus fraction and transformation in eucalyptus plantation (In Chinese)[J]. Guangxi Botanical, 2024, 44(7): 1257-1268. [叶小敏, 高冠女, 张文, 等. 添加生物质炭对桉树人工林土壤磷组分及转化的影响[J]. 广西植物, 2024, 44(7): 1257-1268.]
(  0) 0) |
| [27] |
Jiang X M, Yang C H, Cheng S Y, et al. Effects of different tillage methods and biochar on soil nutrients, enzyme activities and maize yield (In Chinese)[J]. Soil and Fertilizer in China, 2024(10): 69-79. [姜晓敏, 杨彩红, 程生煜, 等. 不同耕作方式和生物炭对土壤养分、酶活性和玉米产量的影响[J]. 中国土壤与肥料, 2024(10): 69-79.]
(  0) 0) |
| [28] |
Zhang M M, Wang Y, Li S L, et al. Biochar modulates rhizosphere microbial community and alleviates peanut continuous cropping obstacle by altering soil microecology[J]. Science of The Total Environment, 2024, 946: 174175. DOI:10.1016/j.scitotenv.2024.174175
(  0) 0) |
| [29] |
Xu W H, Xu H M, Delgado-Baquerizo M, et al. Global meta-analysis reveals positive effects of biochar on soil microbial diversity[J]. Geoderma, 2023, 436: 116528. DOI:10.1016/j.geoderma.2023.116528
(  0) 0) |
| [30] |
Bai Y, Su X F, Gu X, et al. Research Progress on the Effect of Biochar Addition on Soil Microorganisms in Cultived Land (In Chinese)[J]. Environmental Science, 2025, 46(4): 2600-2610. [白艳, 苏小粉, 顾欣, 等. 生物炭影响耕地土壤微生物的研究进展[J]. 环境科学, 2025, 46(4): 2600-2610.]
(  0) 0) |
| [31] |
Fang J, Jin L, Cheng L L, et al. Research progress on the stability of biochar in the environment (In Chinese)[J]. Acta Pedologica Sinica, 2019, 56(5): 1034-1047. DOI:10.11766/trxb201808220426 [方婧, 金亮, 程磊磊, 等. 环境中生物质炭稳定性研究进展[J]. 土壤学报, 2019, 56(5): 1034-1047.]
(  0) 0) |
| [32] |
Lei T T, Chen L Z, Chen S X, et al. Progress in research on the adaptability of microorganisms to extremely cold environments (In Chinese)[J]. Acta Microbiologica Sinica, 2022, 62(6): 2150-2164. [雷婷婷, 陈良仲, 陈绍兴, 等. 微生物对低温极端环境适应性的研究进展[J]. 微生物学报, 2022, 62(6): 2150-2164.]
(  0) 0) |
| [33] |
Banerjee S, Kirkby C A, Schmutter D, et al. Network analysis reveals functional redundancy and keystone taxa amongst bacterial and fungal communities during organic matter decomposition in an arable soil[J]. Soil Biology & Biochemistry, 2016, 97: 188-198.
(  0) 0) |
| [34] |
Yao L R, Li W, Zhu Y Z, et al. Effects of biochar application on soil bacterial community diversity and winter wheat growth in wheat field (In Chinese)[J]. Environmental Science, 2023, 44(6): 3396-3407. [姚丽茹, 李伟, 朱员正, 等. 施用生物炭对麦田土壤细菌群落多样性和冬小麦生长的影响[J]. 环境科学, 2023, 44(6): 3396-3407.]
(  0) 0) |
| [35] |
Egidi E, Delgado-Baquerizo M, Plett J M, et al. A few Ascomycota taxa dominate soil fungal communities worldwide[J]. Nature Communications, 2019, 10(1): 2369. DOI:10.1038/s41467-019-10373-z
(  0) 0) |
| [36] |
Gao C, Guo L D. Research progress on microbial species diversity, community construction and functional traits (In Chinese)[J]. Biodiversity, 2022, 30(10): 168-180. [高程, 郭良栋. 微生物物种多样性、群落构建与功能性状研究进展[J]. 生物多样性, 2022, 30(10): 168-180.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


