2. 浙江农林大学森林食物资源挖掘与利用全国重点实验室, 杭州 311300;
3. 浙江农林大学林业与生物技术学院, 杭州 311300;
4. 庆元县生态林业发展中心, 浙江庆元 323800
2. National Key Laboratory for Development and Utilization of Forest Food Resources, Zhejiang A&F University, Hangzhou 311300, China;
3. College of Forestry and Biotechnology, Zhejiang A&F University, Hangzhou 311300, China;
4. Qingyuan County Ecological Forestry Development Center, Qingyuan, Zhejiang 323800, China
全球森林生态系统正面临诸多压力,如气候变化、生物多样性减少、森林砍伐、森林退化等,且呈现出日益严峻的态势。在这样的背景下,科学的林业管理实践的重要性愈发凸显。它对于提升森林的生态功能以及生物多样性有着不可替代的作用[1]。杉木(Cunninghamia lanceolata),作为中国南方地区的主要人工造林树种,在木材生产和生态工程中扮演着关键角色。然而,长期的单一杉木林经营模式导致了土壤退化、生物多样性下降以及生态系统服务功能的降低,对区域生态安全构成了威胁[2]。近年来,套种珍贵树种被视为改善人工林生态系统的重要策略[3],如田晓等[4]关于杉木林下套种不同比例楠木的研究结果表明,套种既可优化乔木碳储量,又能缓解土壤退化情况。然而,现有研究多聚焦于混交林对土壤理化性质和林分结构的直接影响,而对土壤微生物(细菌和真菌)群落的响应缺乏系统性探讨[5]。因此,有必要从多维度解析树种类型、土壤特性、微生物群落和土壤功能之间的内在联系。
土壤微生物群落作为森林生态系统功能的关键调节者,其多样性和稳定性直接关系到土壤养分循环和植物生长[6]。土壤微生物通过参与有机质分解、固氮、硝化等生态过程,影响森林生态系统的健康和生产力[7]。套种珍贵树种可改善土壤化学性质,调节土壤微生物群落的结构和功能,有利于特定功能微生物的富集和活性增强,从而加速土壤中有机物质的分解与转化,促进土壤碳、氮循环[8-9]。与单一种植相比,杉木-闽楠混交林的土壤理化性质更优、酶活性更高,土壤微生物的多样性和稳定性升高,与碳水化合物代谢和能量代谢有关的功能基因的相对丰度增加[10]。细菌和真菌群落结构可能会对套种树种的改变产生不同的响应。在红壤区不同生态恢复林分中,林分类型对土壤真菌丰富度和多样性的影响显著,但对土壤细菌丰富度和多样性几乎无影响[11]。这可能是因为细菌和真菌在资源利用和竞争方面存在显著差异。细菌在利用简单底物方面较真菌更胜一筹,且对氮的需求较高,因此在碳氮比较低的土壤中,细菌的生长和繁殖可能更为活跃。而真菌在分解复杂有机物质方面具有优势,因此在有机质丰富的土壤中,真菌的活性可能更强[12]。
本研究旨在解析套种珍贵树种对杉木林土壤化学性质、微生物群落结构及其功能特征的系统性影响,并基于此提出以下科学假设:(1)套种将重塑土壤微生物群落组成,增强细菌与真菌群落的多样性及互作网络复杂性;(2)套种可提高参与碳氮循环的关键功能微生物的丰度,进而显著提升土壤速效养分含量。
1 材料与方法 1.1 研究区概况本研究在百山祖国家公园毗邻区域浙江省庆元县庆元林场(27°28′N,119°03′E)进行,该区域属亚热带季风湿润气候,四季分明,降水充沛。年均降水量1 760 mm,年均气温17.4℃。年均无霜期245 d,年均日照1 800.9 h。土壤为酸性红壤。杉木林于2000年种植,整地方式采用全垦,初始种植密度为每公顷2 700株。2015年,以“砍密留稀,保优去劣”为原则对杉木林进行间伐,间伐面积10 hm2左右,间伐强度20%。2016年春,在间伐林分中按每公顷900株分别套种南方红豆杉、红豆树、浙江楠、厚朴等珍贵树种,构建“杉木+珍贵树种”二元混交样地。
1.2 试验设计2023年6月,在土壤类型、林龄和间伐强度一致的条件下,选取杉木纯林(PC)及4种混交林(南方红豆杉-杉木混交林(MTC)、红豆树-杉木混交林(MOC)、浙江楠-杉木混交林(MPC)、厚朴-杉木混交林(MHC))作为研究对象。每个处理设置3个20 m×20 m样地,采用“S”形多点采样。清除土层表面的凋落物后,使用土钻采集0~10 cm的土壤样品,每个土壤样品由5个子样品混合得到。样品充分混合后进行标记,冷冻处理后带回实验室。取部分新鲜土样,去除石块和植物根系,过2 mm筛后-80 ℃超低温保存,用于后续土壤细菌群落的高通量测序;余下鲜土自然风干、研磨,再分别过2 mm和0.149 mm筛,用于测定土壤理化指标。
1.3 分析测试方法土壤pH通过1︰5土水质量比悬液以pH计测定;土壤有机碳(SOC)采用重铬酸钾外加热氧化法测定;土壤碱解氮(AN)采用碱解扩散法测定;土壤有效磷(AP)经0.03 mol·L–1NH4F-0.025 mol·L–1 HCl溶液联合提取后,以钼锑抗比色法测定;土壤速效钾(AK)以1 mol·L–1乙酸铵溶液浸提—火焰光度法分析;土壤硝态氮(NO3–-N)和铵态氮(NH4+-N)经2 mol·L–1KCl溶液浸提后,分别采用紫外分光光度法和靛酚蓝比色法测定[13-14]。
采用十六烷基三甲基溴化铵(CTAB)标准法提取土样DNA,并通过Nanodrop 2000和1%琼脂糖凝胶电泳评估DNA浓度及完整性。采用针对V3~V4区域(341F和806R)的引物扩增16S rRNA基因[15]。同样,为了扩增内部转录间隔(ITS)rRNA,使用了ITS2区域的引物(ITS3-2024F和ITS4- 2409R)[16]。进行PCR反应并纯化产物以制备测序文库。然后在Illumina NovaSeq平台上对上述文库进行测序,生成原始序列文件。
1.4 数据处理使用QIIME2 dada2工具对每个样本的原始序列数据进行质量过滤、修剪、去噪和合并。随后,识别并剔除嵌合序列。根据Greengenes的16S rRNA基因序列和真菌ITS序列鉴定统一数据库(UNITE)的ITS序列,对序列进行分类,并使用QIIME2特征表插件过滤掉干扰序列。根据16S rRNA基因序列推断出的细菌群落中功能基因的丰度,使用原核功能预测工具(FAPROTAX)结合京都基因和基因组百科全书(KEGG)进行预测。此外,使用真菌功能分类工具(FUNGuild)对从ITS序列中确定的真菌物种的功能基因进行预测和注释。
使用SPSS 22软件评估土壤化学性质和微生物α多样性的正态性和方差齐性,并进行单因素方差分析(One-way ANOVA),采用邓肯检验(Duncan test)进行多重比较(P < 0.05),校正多重检验误差。使用Origin 2022软件绘制了土壤细菌和真菌的百分比堆叠条形图。使用R软件包“psych”分析相关热图,并使用R软件包“pheatmap”绘制相关热图。使用R软件包“vegan”进行主坐标分析(PCoA),计算Bray-Curtis相异度(Bray-Curtis dissimilarity),评估各混交林对土壤微生物群落的影响,并使用“ggplot2”软件包生成统计图。使用R软件包“igraph”对不同土壤细菌与真菌属间的斯皮尔曼相关性(Spearman correlation)进行分析,并借助Gephi-0.10.1软件构建土壤细菌和真菌的共现网络图。在此基础上,计算细菌、真菌群落的稳定性指标:涵盖度中心性(Degree centrality)、接近中心性(Closness centrality)和特征向量中心性(Eigenvector centrality),并依据度中心性值的大小进行排序,进而筛选出细菌、真菌关键种群。最后,运用SPSS 22软件对真菌群落的稳定性开展克鲁斯卡尔-沃利斯检验(Kruskal-Wallis)。在对因子进行分类后,使用R软件包“plspm”构建偏最小二乘路径模型(PLS-PM),解析各因子对土壤生态功能组的作用路径与相对贡献;使用Origin 2022软件绘制效应图,直观揭示不同因子对关键细菌潜在功能(Key Faprotax)与关键真菌功能类群(Key FUNGuild)的差异化影响。
2 结果 2.1 套种对土壤化学性质的影响套种不同珍贵树种对杉木林土壤部分化学性质具有显著调控作用(表 1)。MPC显著提升土壤pH至4.56(P < 0.05),较PC增幅达11.2%;MTC显著提高土壤有机碳(SOC)含量至31.8 g·kg–1(P < 0.05),较PC处理增加26.2%。MOC处理显著促进土壤有效磷(AP)释放(P < 0.01),其含量达3.17 mg·kg–1,较PC提升3.96倍。MPC、MTC速效钾(AK)含量分别为193.8 mg·kg–1和180.3 mg·kg–1,显著高于其他处理(P < 0.05),且MPC处理的铵态氮(NH4+-N)含量为20.16 mg·kg–1,显著高于PC(P < 0.05)。不同处理总氮(TN)、碱解氮(AN)含量在不同处理间的差异未达显著水平。
|
|
表 1 杉木-珍贵树种混交林土壤化学性质 Table 1 Soil chemical properties of Cunninghamia lanceolata-rare tree species mixed forests |
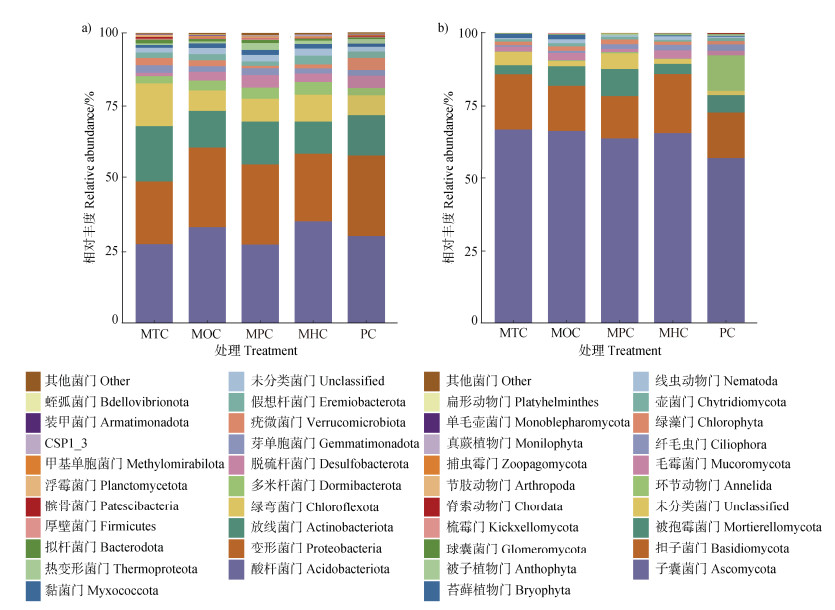
不同处理下可鉴定出的土壤细菌和真菌群落在门水平上的分类情况如图 1所示。细菌群落组成以酸杆菌门(Acidobacteriota,30.4%)、变形菌门(Proteobacteria,25.7%)、放线菌门(Actinobacteriota,14.3%)和绿弯菌门(Chloroflexota,9.1%)为主,其次是多米杆菌门(Dormibacterota,3.2%)、芽单胞菌门(Gemmatimonadota,3.0%)和疣微菌门(Verrucomicrobiota,2.3%)(图 1a)。真菌群落组成以子囊菌门(Ascomycota,63.8%)和担子菌门(Basidiomycota,17.0%)为主,其次是被孢霉门(Mortierellomycota,5.8%)和未分类真菌(Unclassified fungal,2.9%)(图 1b)。
|
图 1 土壤细菌(a)、真菌(b)群落在门水平上的相对丰度 Fig. 1 Relative abundance of soil bacterial(a)and fungal(b)communities at the phylum level |
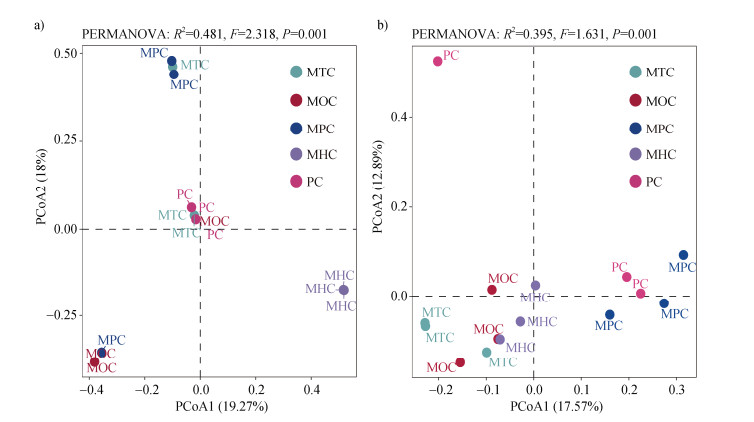
各处理间土壤微生物α多样性指数不存在显著差异(表 2,P > 0.05)。根据Bray-curtis距离对各处理的土壤细菌和真菌群落结构差异做PCoA分析(图 2),在土壤细菌群落中,MHC和PC的分布相较于其他处理呈现出较为明显的聚集性;而在土壤真菌群落中,各处理的分布则相对较为分散。
|
|
表 2 杉木-珍贵树种混交林土壤微生物α多样性 Table 2 Soil microbial alpha diversity of Cunninghamia lanceolata-rare tree species mixed forests |
|
注:PERMANOVA,置换多元方差分析;R2,决定系数;F,伪F统计量;P,显著性P值。 Note: PERMANOVA, Permutational multivariate analysis of variance; R2, Coefficient of determination; F, Pseudo-F statistic; P, P-value. 图 2 土壤细菌(a)、真菌(b)群落主坐标分析(PCoA) Fig. 2 Principal coordinates analysis(PCoA)results of soil bacterial(a)and fungal(b)communities |
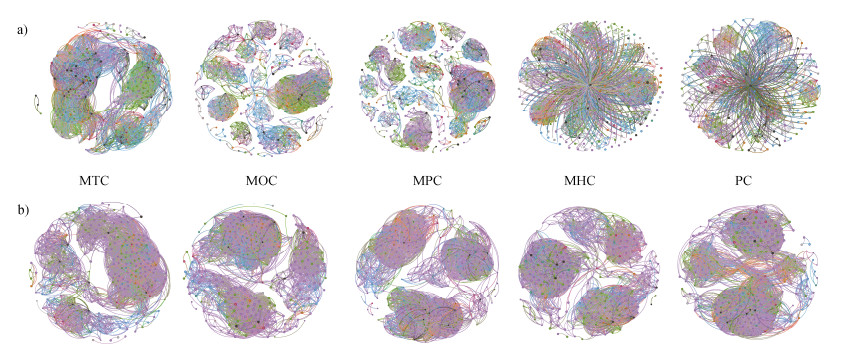
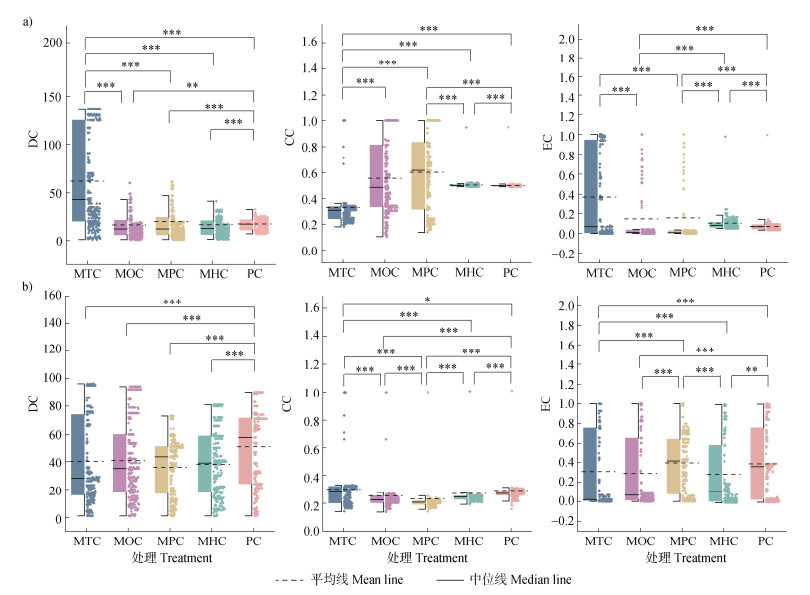
各混交林的细菌共现网络的节点数和边数较PC均有所增加,而真菌网络的边数均减少(图 3)。此外,各处理间的网络拓扑特征存在显著差异(图 4)。上述结果表明,混交林的微生物共现模式与纯林的网络模式有很大不同,且混交林的网络复杂性更高。
|
图 3 土壤细菌(a)、真菌(b)共现网络模式 Fig. 3 Co-occurrence network patterns of communities of soil bacterial(a)and fungal(b) |
|
注:DC,度中心性;CC,接近中心性;EC,特征向量中心性。*,P < 0.05;**,P < 0.01;***,P < 0.001。 Note: DC, degree centrality; CC, tightness centrality; EC, eigenvector centrality. *, P < 0.05;**, P < 0.01;***, P < 0.001. 图 4 土壤细菌(a)、真菌(b)的网络拓扑特征 Fig. 4 Network topological characteristics of soil bacterial(a)and fungal(b)communities |
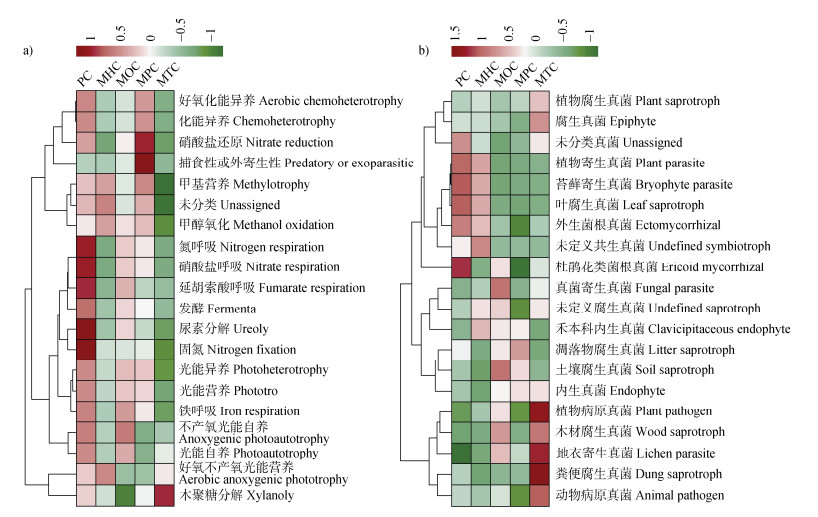
基于所有细菌功能群和真菌功能群建立了相应的分组聚类热图,反映了不同土壤样品中土壤细菌、真菌功能群相对丰度的差异。具体而言,在PC处理下氮呼吸(Nitrogen respiration)、硝酸盐呼吸(Nitrate respiration)、延胡索酸呼吸(Fumarate respiration)、尿素分解(Ureolysis)和固氮(Nitrogen fixation)功能较为活跃;而MPC处理下硝酸盐还原(Nitrate reduction)功能活跃;MTC处理下木聚糖分解(Xylanoly)功能活跃(图 5a)。真菌功能类群主要包括病理营养型(Pathotroph)、腐生营养型(Saprotroph)和共生营养型(Symbiotroph)。与PC相比,林下套种珍贵树种后,植物寄生真菌(Plant parasite)、苔藓寄生真菌(Bryophyte parasite)、叶腐生真菌(Leaf saprotroph)和杜鹃花类菌根真菌(Ericoid mycorrhizal)的丰度下降(图 5b)。
|
图 5 土壤细菌(a)、真菌(b)群落代谢功能群的变化 Fig. 5 Shifts in metabolic functional groups of bacterial(a)and fungal(b)communities |
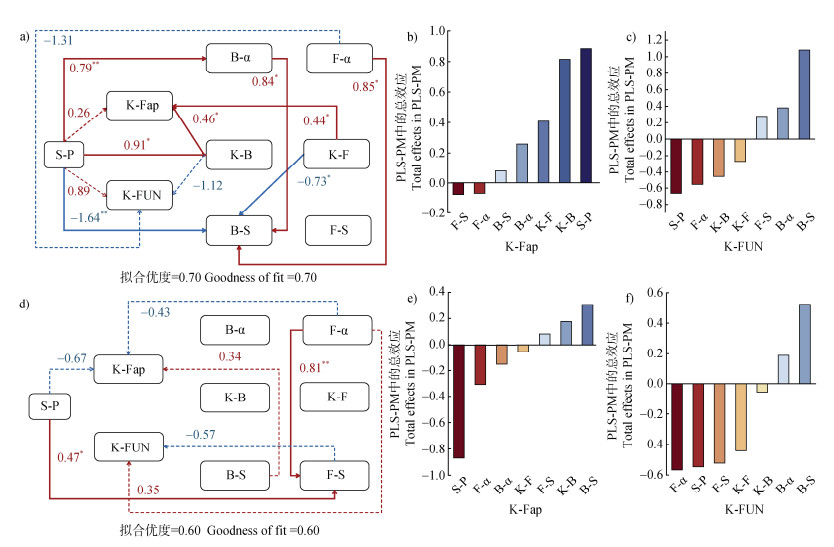
利用PLS-PM结构方程模型量化了土壤化学性质、土壤微生物群落和土壤微生物关键种群对关键细菌潜在功能(Key Faprotax,K-Fap)和关键真菌功能类群(Key FUNGuild,K-FUN)的直接效应和总体效应(图 6)。在MTC处理下,细菌关键种群和真菌关键种群对K-Fap有显著的正向直接影响(P < 0.05)。土壤化学性质对K-Fap的直接影响并不显著(图 6a),但其对K-Fap的总影响却很高(图 6b)。在PC处理下,细菌群落稳定性对K-Fap有正面影响,而土壤化学性质和真菌α多样性则有负向影响(图 6e)。与PC相比,MTC处理下各因素对K-FUN的影响变化不明显,仅有真菌群落稳定性的总影响由负变正(图 6f)。
|
注:S-P,土壤化学性质;B-α,细菌α多样性;K-B,细菌关键种群;B-S,细菌群落稳定性;F-α,真菌α多样性;K-F,真菌关键种群;F-S,真菌群落稳定性;K-Fap,关键细菌潜在功能;K-FUN,关键真菌功能类群。a)为MTC处理下的PLS-PM;d)为PC处理下的PLS-PM。红色表示负面影响,蓝色表示正面影响。实线表示显著影响,虚线表示影响不显著。b)、e)分别为在MTC和PC处理下对K-Fap的直接和间接影响的总效应。c)、f)分别为在MTC和PC处理下对K-FUN的直接和间接影响的总效应。*,P < 0.05;**,P < 0.01。 Note: S-P, soil chemical properties; B-α, bacterial α-diversity; K-B, bacterial key populations; B-S, bacterial community stability; F-α, fungal α-diversity; K-F, fungal key populations; F-S, fungal community stability; K-Fap, key bacterial putative functions; K-FUN, key fungal functional guilds. a)PLS-PM under MTC treatment; d)PLS-PM under PC treatment. Red colour indicates negative impacts, blue colour indicates positive impacts. Solid lines indicate significant effects and dashed lines indicate non-significant effects. b)and e)are the total effects of direct and indirect effects on Key Faprotax under MTC and PC treatments, respectively. c)and f)are the total effects of direct and indirect effects on Key FUNGuild under MTC and PC treatments, respectively. *, P < 0.05;**, P < 0.01。 图 6 基于偏最小二乘路径模型(PLS-PM)的土壤微生物多功能性总效应分析 Fig. 6 Total effect analysis of soil microbial multifunctionality based on partial least squares path modeling(PLS-PM) |
套种珍贵树种后,杉木林下土壤细菌、真菌在门水平上的相对丰度发生了变化(图 1)。在MPC处理下,随着浙江楠在混交林中的生长,其对酸性物质的吸收和转化,使得土壤中酸性物质的含量相对减少,土壤pH提升,酸杆菌门的相对丰度相应减少(表 1,图 1a),这与李厚春等[17]的研究结果一致,即酸杆菌门丰度与土壤pH呈显著负相关。MTC处理下,南方红豆杉作为针叶树种,其凋落物具有较高的C/N比,分解过程相对缓慢,可长期缓慢释放有机碳,从而显著提高了土壤有机碳含量(表 1)。这为土壤微生物提供了较为长期的碳源和养分,特别是那些能够分解木质素、纤维素等复杂有机物质的真菌(如子囊菌门)和细菌(如变形菌门)的种类和数量可能会增多(图 1)。MOC处理下,土壤pH虽无显著变化,但土壤有效磷含量却显著提高(表 1,P < 0.05)。这是因为在强酸性环境下,磷与Ca2+、Al3+和Fe3+结合的氧化物的分解速率增加,进而增强了磷的释放[18]。不同于针叶树种,红豆树和浙江楠作为阔叶树种,它们的凋落物具有较高的质量和较快的分解速率,能够较快地向土壤中释放养分,促进微生物的生长和活动。这与Uroz等[19]的研究结果一致,即树种和根系分泌物可能会影响杉木混交种植园的土壤微生物群落。
本研究发现套种对土壤细菌和真菌群落β-多样性的影响大于α-多样性(表 2,图 2),该结果与Ding等[10]的研究结果一致。这可能是因为微生物群落结构的变化并不一定会导致物种丰富度、多样性的变化,因为某些类群的变化可能会被其他类群的变化所补偿[20]。这种补偿现象很大程度上源于微生物群落普遍存在的功能冗余性,即不同分类群可能执行相似或相同的生态功能。因此,即使群落组成发生显著改变,只要关键功能类群存在或功能相似的类群能够填补空缺,生态系统的功能过程(如养分循环)和整体的物种丰富度水平就可能得以维持[21]。
3.2 套种影响了微生物共现网络网络分析揭示了微生物生态联系和过程之间复杂且潜在的相互作用。在本研究中,套种不同树种后,细菌、真菌网络结构发生了显著变化(图 3)。混交林中细菌网络的节点数、边数及路径长度均有所增加(图 3a),表明网络复杂性提升,这种复杂性可能与微生物群落结构的变化相关。某些关键类群相对丰度的增减,会影响网络的连接方式,如放线菌门、拟杆菌门等类群在微生物网络中常占据关键节点,其丰度变化会改变与其他细菌的相互关系,进而影响边数和路径长度[22]。微生物群落变化和细菌网络复杂性的变化共同驱动着土壤生态系统的功能。复杂的细菌网络能够更有效地进行养分循环、有机物分解、土壤结构维持等生态过程。随着微生物群落的变化和网络复杂性的提升,这些生态功能的效率和稳定性也会相应提高,从而维持土壤生态系统的健康和稳定[23]。例如,Yuan等[24]的研究结果证实了生态学中的关键理念:复杂性带来稳定性,即生态系统网络结构的复杂性与功能稳定性之间存在显著的正相关关系。本研究证实,混交林通过改变土壤环境(如提高pH、增加有机碳及有效磷含量),显著增强了生境异质性和资源可利用性(表 1)。这种生境优化直接驱动了微生物群落的多样性提升,并促使细菌共现网络的节点数、边数及路径长度上升。各处理下微生物共现网络的度中心性、接近中心性和特征向量中心性存在显著差异(图 4),例如MTC处理下,细菌网络的度中心性显著提高(P < 0.001),表明微生物互作强度与功能冗余性增强。这种高复杂性网络可通过“功能补偿效应”(Functional compensation effect)缓冲环境扰动,例如在养分波动时,关键菌群(如放线菌门)的代谢多样性可维持氮循环功能稳定[25]。偏最小二乘路径模型(PLS-PM)(图 6)显示,土壤化学性质通过影响关键微生物类群,间接提升碳氮循环相关功能基因的表达,最终使生态系统稳定性指数提高。
作为维系生物网络结构稳定性的核心枢纽,关键物种的存续直接决定生态网络功能的完整性,其一旦发生缺失,将引发网络拓扑结构失序并导致系统功能级联崩溃,最终威胁整个生态系统的稳定运行[26]。通过网络分析(图 4)发现,混交林生态系统相较于单一林型具有更丰富的高枢纽性类群分布,其空间配置模式与网络鲁棒性指标呈显著正相关,表明枢纽类群的多样性对网络稳定性具有正向调控作用。进一步分析确定了具有较高程度值的关键微生物群,这些枢纽类群主要隶属于变形菌门、放线菌门和芽单胞菌门三大系统发育类群(图 1a)。这些细菌门作为森林生态系统的功能基石,通过驱动木质素降解、氮素矿化等关键过程,在土壤有机质转化与养分循环中发挥核心作用。Yang等[27]研究发现,放线菌门的相对丰度与土壤有机质含量(SOC)及pH间存在显著正相关,显示其代谢活动可能通过调节土壤理化环境来维持营养供给的稳态。该发现与MTC处理组的实验结果(表 1,图 1a)相印证:当土壤pH因套种提升至4.38时,SOC含量同步增加26.2%,由此引发的放线菌门丰度激增(增幅达56.2%),从而增强了细菌群落的木聚糖分解功能(图 5)。
3.3 套种改变了土壤功能基因丰度土壤中的微生物在生物地球化学循环中发挥了核心作用,它们参与碳和氮的转化与固定,影响了生态系统的碳储存能力和养分供给[28]。PC处理下氮代谢功能特征(固氮、反硝化、脲解等功能活跃)是对高C/N比凋落物、土壤酸化的适应性响应(图 5a)。杉木凋落物的高C/N比导致其分解缓慢,释放氮的效率低,土壤有效氮匮乏[7]。微生物通过固氮和脲解主动补充氮源,同时依赖硝酸盐呼吸和氮呼吸获取能量,形成“开源节流”的氮代谢策略[29]。不仅如此,凋落物还会分解释放有机酸(如单宁酸),导致土壤pH降低,抑制硝化作用,促使硝酸盐通过反硝化(氮呼吸)或硝酸盐呼吸转化[30]。而反硝化过程产生的H⁺,进一步降低土壤pH,形成“凋落物酸化→反硝化活跃→酸化加剧”的恶性循环。MPC处理下硝酸盐还原功能活跃(图 5a),这是高碳输入、pH提高及微生物群落重组共同作用的结果。浙江楠作为阔叶树种,其凋落物C/N比低,木质素含量少,分解速率快,可释放大量易分解有机碳[31]。但土壤中SOC含量较PC低,可能是因为浙江楠凋落物提供大量易利用碳源,激活微生物(如变形菌门)分解原有土壤惰性有机碳(如杉木残留的木质素),微生物通过“共代谢”同时消耗新鲜凋落物碳和原有SOC,导致总SOC含量减少。在套种浙江楠后,土壤pH显著升高(表 1),这有利于促进反硝化菌的增殖,同时抑制极端酸敏感菌,优化硝酸盐还原酶的活性。MTC处理下木聚糖分解功能活跃(图 5a),这是因为南方红豆杉的凋落物含有丰富的可溶性有机物质和易于分解的碳水化合物,如木聚糖,这些物质为微生物提供了丰富的碳源,促进了木聚糖分解功能的活跃。
在杉木纯林中,由于植物种类相对单一,杉木及其伴生的苔藓植物成为寄生真菌的主要宿主。这种单一宿主环境有利于能够适应并利用杉木或苔藓植物的寄生真菌的定殖,导致这些寄生真菌在杉木纯林中的丰度较高。叶腐生真菌主要依赖植物凋落物中的叶片等有机物质作为营养来源[32]。在杉木纯林中,杉木叶片是主要的凋落物来源,其成分和性质相对一致,为叶腐生真菌提供了集中且稳定的营养资源。这种资源的集中性使得叶腐生真菌能够更好地适应环境并在林分中大量繁殖,进而表现出较高的丰度(图 5b)。杉木在生长过程中会向根际土壤分泌一些特定的化学物质,如酚类化合物等[33],这些分泌物对某些真菌具有吸引或抑制作用。例如,杜鹃花类菌根真菌可能受杉木分泌物的诱导而向杉木根系聚集,从而形成更紧密的共生关系,提高其丰度。
3.4 套种后土壤功能基因预测的变化不同混交林经营模式中,树种选择对土壤微生物功能预测指标(K-Fap和K-FUN)的调控效应凸显了适生树种配置的重要性。PLS-PM分析(图 6)表明,在MTC处理中,尽管土壤化学性质对K-Fap的直接效应未达显著水平(P > 0.05),但其总效应值却呈现显著正向贡献。通过路径分解可知,土壤化学性质通过显著促进细菌关键种群(如放线菌门)的增殖,进而间接驱动K-Fap的响应。该发现表明,混交林的构建需综合考虑树种对微生物功能的直接调控及其介导的土壤环境间接效应。在PC处理中,土壤化学性质与真菌α多样性对K-Fap均呈现总体的负向影响(图 6e)。这可能源于长期单一杉木林经营导致的土壤酸化与养分贫瘠化[34],其不仅抑制真菌群落的多样性维持,还通过改变微生物资源竞争格局削弱系统功能稳定性。因此,通过套种适生树种改善土壤理化性质并优化关键功能类群结构,是激活土壤生态功能潜力、实现人工林可持续经营的重要途径。综上所述,推荐在杉木林中套种南方红豆杉,并将浙江楠作为辅助树种协同套种,以实现土壤状况的协同优化,提升土壤生态功能潜力,为人工林的可持续经营提供有力支撑。
4 结论不同珍贵树种的套种组合通过各自特性改善了土壤化学性质。具体而言,浙江楠(MPC)通过吸收和转化土壤中的酸性物质,显著提升土壤pH;南方红豆杉(MTC)的高C/N比凋落物是其显著提升土壤有机质含量的关键;红豆树(MOC)则依赖根系分泌物中的有机酸竞争磷酸根吸附点位,从而明显增加土壤有效磷含量。套种增加了土壤细菌网络的节点数、边数和路径长度,提升了细菌网络的复杂性和稳定性。PLS-PM模型表明,套种通过直接改善土壤化学性质,间接促进与碳氮转化密切关联的微生物类群丰度上升,从而优化土壤生态功能网络的核心代谢途径。然而,结论受限于单季数据与区域样本,未来需结合多季节监测及跨区域验证,深入解析关键微生物的功能机制。建议在杉木林区优先套种南方红豆杉,并辅以浙江楠套种以协同优化土壤状况。
| [1] |
Huang L. Research progress on the ecological effects of forest management (In Chinese)[J]. Acta Ecologica Sinica, 2021, 41(10): 4226-4239. [黄麟. 森林管理的生态效应研究进展[J]. 生态学报, 2021, 41(10): 4226-4239.]
(  0) 0) |
| [2] |
Wang J, Fu R B, Hao Z D, et al. Characteristics of soil nitrogen transformation in different clonal chinese fir plantations (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(3): 802-812. DOI:10.11766/trxb202210150568 [王敬, 付瑞彪, 郝兆东, 等. 不同无性系杉木人工林土壤氮素转化特征[J]. 土壤学报, 2024, 61(3): 802-812.]
(  0) 0) |
| [3] |
Jiao J J, Sheng W X, Su G L, et al. Stand increment and diversity of understory species in Cunninghamia lanceolata plantation mixed with different rare tree species (In Chinese)[J]. Journal of Zhejiang Forestry Science and Technology, 2022, 42(3): 1-8. [焦洁洁, 盛卫星, 苏光浪, 等. 杉木人工林珍贵化改造对林分生长量与物种多样性的影响[J]. 浙江林业科技, 2022, 42(3): 1-8.]
(  0) 0) |
| [4] |
Tiao X, Hu J Y, Liu J B, et al. Effects of simulation of various initial planting densities of Chinese fir with Phoebe bournei mixed forest on its carbon storage (In Chinese)[J]. Southwest China Journal of Agricultural Sciences, 2018, 31(3): 598-604. [田晓, 胡靖宇, 刘静波, 等. 模拟不同初植密度杉木楠木混交林对碳储量的影响[J]. 西南农业学报, 2018, 31(3): 598-604.]
(  0) 0) |
| [5] |
Ming A G, Yang Y J, Liu S R, et al. A decade of close-to-nature transformation alters species composition and increases plant community diversity in two coniferous plantations[J]. Frontiers in Plant Science, 2020, 11: 1141. DOI:10.3389/fpls.2020.01141
(  0) 0) |
| [6] |
Hu Y X, Zhang X Q, Chen H Y, et al. Effects of forest age and season on soil microbial communities in Chinese fir plantations[J]. Microbiology Spectrum, 2024, 12(8): e04075-23.
(  0) 0) |
| [7] |
Zhang B B, Wang X H, Yang J Q, et al. Effects of litters different in quality on soil microbial community structure in Cunninghamia lanceolata plantation (In Chinese)[J]. Acta Pedologica Sinica, 2021, 58(4): 1040-1049. DOI:10.11766/trxb201912260562 [张冰冰, 万晓华, 杨军钱, 等. 不同凋落物质量对杉木人工林土壤微生物群落结构的影响[J]. 土壤学报, 2021, 58(4): 1040-1049.]
(  0) 0) |
| [8] |
Lei J, Duan A G, Guo W F, et al. Effects of tree species mixing and soil depth on the soil bacterial and fungal communities in Chinese fir(Cunninghamia lanceolata)plantations[J]. Applied Soil Ecology, 2024, 195: 105270. DOI:10.1016/j.apsoil.2024.105270
(  0) 0) |
| [9] |
Lu X G, Guo Y L, Yao X Y, et al. Mixed with broadleaf tree species changes soil microbial stoichiometric characteristics in Chinese fir plantations: Insights at the aggregate scale[J]. Journal of Soil Science and Plant Nutrition, 2025, 25(2): 3676-3689. DOI:10.1007/s42729-025-02359-2
(  0) 0) |
| [10] |
Ding K, Zhang Y T, Yrjälä K, et al. The introduction of Phoebe bournei into Cunninghamia lanceolata monoculture plantations increased microbial network complexity and shifted keystone taxa[J]. Forest Ecology and Management, 2022, 509: 120072. DOI:10.1016/j.foreco.2022.120072
(  0) 0) |
| [11] |
Hou X L, Yu J B, Han X J, et al. Dynamic shifts in soil fungal functional group characteristics across distinct vegetation types during ecological restoration in degraded red soil regions[J]. Forests, 2024, 15(1): 89. DOI:10.3390/f15010089
(  0) 0) |
| [12] |
Wang C Q, Kuzyakov Y. Mechanisms and implications of bacterial–fungal competition for soil resources[J]. The ISME Journal, 2024, 18(1): wrae073. DOI:10.1093/ismejo/wrae073
(  0) 0) |
| [13] |
Song G, Sun B, Jiao J Y. Comparison between ultraviolet spectrophotometry and other methods in determination of soil nitrate-N (In Chinese)[J]. Acta Pedologica Sinica, 2007, 44(2): 288-293. DOI:10.3321/j.issn:0564-3929.2007.02.014 [宋歌, 孙波, 教剑英. 测定土壤硝态氮的紫外分光光度法与其他方法的比较[J]. 土壤学报, 2007, 44(2): 288-293.]
(  0) 0) |
| [14] |
Lu R K. Analytical methods for soil and agro-chemistry (In Chinese). Beijing: China Agricultural Science and Technology Press, 2000. [鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000.]
(  0) 0) |
| [15] |
Logue J B, Stedmon C A, Kellerman A M, et al. Experimental insights into the importance of aquatic bacterial community composition to the degradation of dissolved organic matter[J]. The ISME Journal, 2016, 10(3): 533-545. DOI:10.1038/ismej.2015.131
(  0) 0) |
| [16] |
Lin Y X, Ye G P, Kuzyakov Y, et al. Long-term manure application increases soil organic matter and aggregation, and alters microbial community structure and keystone taxa[J]. Soil Biology & Biochemistry, 2019, 134: 187-196.
(  0) 0) |
| [17] |
Li H C, Li J J, Zhang H, et al. Effect of vegetation type on rhizosphere microorganisms of reclaimed soils in coal mining areas (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(5): 1455-1465. DOI:10.11766/trxb202303140100 [李厚春, 李君剑, 张红, 等. 植被类型对煤矿区复垦土壤根际微生物的影响[J]. 土壤学报, 2024, 61(5): 1455-1465.]
(  0) 0) |
| [18] |
Yuan S Y, He J, Su D R. Advances in the effects of precipitation pattern change and grazing on soil phosphorus conversion in grassland (In Chinese)[J]. Acta Agrestia Sinica, 2024, 32(1): 25-36. [袁淑雅, 贺晶, 苏德荣. 降水格局变化和放牧对草地土壤磷转化影响的研究进展[J]. 草地学报, 2024, 32(1): 25-36.]
(  0) 0) |
| [19] |
Uroz S, Oger P, Tisserand E, et al. Specific impacts of beech and Norway spruce on the structure and diversity of the rhizosphere and soil microbial communities[J]. Scientific Reports, 2016, 6(1): 27756. DOI:10.1038/srep27756
(  0) 0) |
| [20] |
Hartmann M, Widmer F. Community structure analyses are more sensitive to differences in soil bacterial communities than anonymous diversity indices[J]. Applied and Environmental Microbiology, 2006, 72(12): 7804-7812. DOI:10.1128/AEM.01464-06
(  0) 0) |
| [21] |
Ramond P, Galand P E, Logares R. Microbial functional diversity and redundancy: Moving forward[J]. FEMS Microbiology Reviews, 2024, 49: fuae031.
(  0) 0) |
| [22] |
Meng L X, Xu C X, Wu F L, et al. Microbial co-occurrence networks driven by low-abundance microbial taxa during composting dominate lignocellulose degradation[J]. Science of the Total Environment, 2022, 845: 157197. DOI:10.1016/j.scitotenv.2022.157197
(  0) 0) |
| [23] |
Qian J J, Akçay E. The balance of interaction types determines the assembly and stability of ecological communities[J]. Nature Ecology & Evolution, 2020, 4(3): 356-365.
(  0) 0) |
| [24] |
Yuan M M, Guo X, Wu L W, et al. Climate warming enhances microbial network complexity and stability[J]. Nature Climate Change, 2021, 11(4): 343-348. DOI:10.1038/s41558-021-00989-9
(  0) 0) |
| [25] |
Boubekri K, Soumare A, Mardad I, et al. Multifunctional role of Actinobacteria in agricultural production sustainability: A review[J]. Microbiological Research, 2022, 261: 127059. DOI:10.1016/j.micres.2022.127059
(  0) 0) |
| [26] |
Hu H X, Mo Y X, Shen T, et al. Simulated high-intensity phorophyte removal mitigates the robustness of epiphyte community and destroys commensal network structure[J]. Forest Ecology and Management, 2022, 526: 120586. DOI:10.1016/j.foreco.2022.120586
(  0) 0) |
| [27] |
Yang B, Feng W J, Zhou W J, et al. Association between soil physicochemical properties and bacterial community structure in diverse forest ecosystems[J]. Microorganisms, 2024, 12(4): 728. DOI:10.3390/microorganisms12040728
(  0) 0) |
| [28] |
Xi Y Q, Li X, Liu X F. Effects of simulated nitrogen addition on soil organic carbon mineralization in cubtropical Cunninghamia lanceolata plantation (In Chinese)[J]. Soils, 2023, 55(1): 196-204. [席颖青, 李晓, 刘小飞. 模拟氮添加对亚热带杉木人工林土壤有机碳矿化的影响[J]. 土壤, 2023, 55(1): 196-204.]
(  0) 0) |
| [29] |
Zhu L F, Chen X L. Research progress on the mechanism and applications of nitrate respiration and anaerobic ammonium oxidation (In Chinese)[J]. Chinese Bulletin of Life Sciences, 2021, 33(4): 428-437. [朱凌峰, 陈雪岚. 硝酸盐呼吸和厌氧氨氧化的机制及其应用研究进展[J]. 生命科学, 2021, 33(4): 428-437.]
(  0) 0) |
| [30] |
Wang M J, Huang Z Q, Zhang B B, et al. Soil nitrification and denitrification in Cunninghamia lanceolata plantations with different stand ages (In Chinese)[J]. Chinese Journal of Applied Ecology, 2023, 34(1): 18-24. [王梦娟, 黄志群, 张冰冰, 等. 不同林龄杉木人工林土壤硝化和反硝化作用[J]. 应用生态学报, 2023, 34(1): 18-24.]
(  0) 0) |
| [31] |
Jiang N C, Qiu Y B, Zhang N J, et al. Characteristics of litter and soil nutrient content and stoichiometric ratio in mixed forest Cunninghamia lanceolata and broadleaved trees (In Chinese)[J]. Journal of Zhejiang Forestry Science and Technology, 2024, 44(4): 1-6. [姜年春, 邱勇斌, 张能军, 等. 杉木-阔叶树复层混交林凋落物和土壤养分及化学计量特征[J]. 浙江林业科技, 2024, 44(4): 1-6.]
(  0) 0) |
| [32] |
Yang J T, Pan Y J, Chang C L, et al. Effects of native plant-soil microbe interaction on plant invasion (In Chinese)[J]. Chinese Journal of Plant Ecology, 2024, 48(12): 1547-1560. [杨佳婷, 潘应骥, 常春玲, 等. 本地植物与土壤微生物互作对植物入侵影响的研究进展[J]. 植物生态学报, 2024, 48(12): 1547-1560.]
(  0) 0) |
| [33] |
Lei J, Wu H B, Li X Y, et al. Response of rhizosphere bacterial communities to near-natural forest management and tree species within Chinese fir plantations[J]. Microbiology Spectrum, 2023, 11(1): e02328-22.
(  0) 0) |
| [34] |
Liu X, Wang Y Z, Liu Y H, et al. Response of bacterial and fungal soil communities to Chinese fir(Cunninghamia lanceolate)long-term monoculture plantations[J]. Frontiers in Microbiology, 2020, 11: 181. DOI:10.3389/fmicb.2020.00181
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


