2. 江苏大学农业工程学院, 江苏镇江 212013;
3. 苏州科技大学, 江苏水处理技术与材料协同创新中心, 江苏苏州 215009;
4. 江苏大学京江学院, 江苏镇江 212028
2. School of Agricultural Engineering, Jiangsu University, Zhenjiang, Jiangsu 212013, China;
3. Suzhou University of Science and Technology, Jiangsu Collaborative Innovation Center of Technology and Material for Water Treatment, Suzhou, Jiangsu 215009, China;
4. Jingjiang College, Jiangsu University, Zhenjiang, Jiangsu 212028, China
外来入侵植物已对本土物种造成全球性的负面影响[1],因其具有极强的适应性、强大的繁殖能力和传播能力,对本地生态系统、水质、土壤以及生物多样性构成巨大的威胁[2-3]。在中国温暖潮湿的东南沿海地区分布着最多的外来入侵植物,其中更是以来源美洲的菊科种类最多[4]。
根际微生物在植物-土壤生态系统的物质交换以及植物的养分吸收和生长发育中起着至关重要的作用[5-6]。植物-土壤反馈是植物介导土壤特性变化,进而影响植物的生长、演替和入侵的过程[7]。根据“共生促进假说”[8],外来物种通常可在入侵地与对其定殖有促进作用的微生物形成良好的共生关系,并且可通过调节根系分泌物、改变土壤物质循环等方式促进外来植物入侵[9]。同时,根际微生物对本地植物带来更大的负面影响,这也进一步加快了外来植物的入侵进程[10]。并且,入侵植物还可改变这些微生物群落,进而削弱本地物种对入侵者的竞争[11]。
根际微生物群落还可保护植物免受不利的环境胁迫影响[12]。而近期的研究表明,根际微生物可增强入侵植物对生物和非生物因素的响应[13],进而提高其在逆境中的适应能力[14]。然而,当前却少见有关根际微生物影响入侵植物响应寒冷胁迫的研究报道。
南美蟛蜞菊(Sphagneticola trilobata(L.)Pruski),一种原产于热带美洲的克隆植物,20世纪70年代作为园林绿化地被植物被引入中国,后来在中国低纬度地区迅速扩张[15],主要分布在海南、云南、广西、广东和福建等地。尽管孙蓓育等[16]的研究表明,南美蟛蜞菊对低温敏感、更适应南方地区高温强光的气候特征,且低温是限制其向北部更寒冷地区扩张的主要因素,但在全球气候变暖背景下,该物种进一步向北扩张的趋势似乎不可阻挡[17-18]。
近年来,许多生态学研究人员对南美蟛蜞菊的入侵机理、自身抗逆性及其对本地生态系统的影响展开了大量研究。研究发现,南美蟛蜞菊具有较高的表型可塑性和本地适应性,这些特征赋予其对新环境的快速适应能力,以及在逆境条件下表现出极强的抗胁迫能力[17,19]。同时,本研究组前期的研究表明,微生物对南美蟛蜞菊的生长、抗营养与病原胁迫等能力有明显的促进作用[20]。比如,内生固氮细菌能够影响南美蟛蜞菊的生长策略,这种影响有利于其地上部分的快速生长与扩张[21];丛枝菌根真菌促进南美蟛蜞菊在低磷水平下的生长和竞争力[22],以及抗病防御[23]。但上述研究均仅针对南美蟛蜞菊的单一种群进行研究。
本研究组近期开展的一项野外调查还发现,南美蟛蜞菊野外种群分布北缘已从福建福州向北扩散,在浙江温州一带亦分布有能够自然越冬的较为稳定的种群;并且,更高纬度的南美蟛蜞菊种群,具有更强壮的茎(更长的间隔子、更粗的茎),并且与其中基茎内生细菌的丰富度存在线性正相关关系[24]。而新近的一项分布预测研究表明,南美蟛蜞菊当前的适生区甚至已经包含了湖南、湖北、四川、贵州、安徽、河南、重庆、山东、西藏、陕西等地区[25]。上述研究暗示南美蟛蜞菊野外种群正朝着年均温及年最低温更低的北方适应性扩张,且与微生物的作用紧密相关。那么,南美蟛蜞菊是否可以招募特定微生物以提高其自身的耐寒能力呢?
因此,本文假设:经过寒冷胁迫驯化的根际土壤微生物对南美蟛蜞菊种群扩散至高纬度(更冷地区)的关键能力——耐寒性发挥了重要作用。为了验证该假设,本研究通过采集分布于我国最北(温州)和最南(三亚)的两个南美蟛蜞菊种群,利用其在长江沿线(镇江)的温室大棚进行自然过冬(低温胁迫适应)三年的同质园种植驯化土壤进行反馈试验,探究以下科学问题:(1)共驯化的根际土壤微生物是否能够促进入侵植物对低温的响应?(2)其中,南北种群所驯化的根际土壤微生物对入侵植物的低温响应的作用是否存在差异?研究结果拟从根际微生物-植物互作角度解决南美蟛蜞菊继续向高纬度入侵扩张的可能机理,为加强南美蟛蜞菊扩张边界区管控提供理论支持。
1 材料与方法 1.1 试验材料本研究两个阶段试验所用的不同地理种群南美蟛蜞菊植物材料均分别采集自浙江省温州市(27.92°N,120.70°E,年均温18℃,年最低温5℃)和海南省三亚市(18.28°N,109.51°E,年均温28℃,年最低温20℃)的野外生长种群。试验选取生长健康、长势一致带有2个茎节的去叶南美蟛蜞菊茎段,清洗消毒后备用。
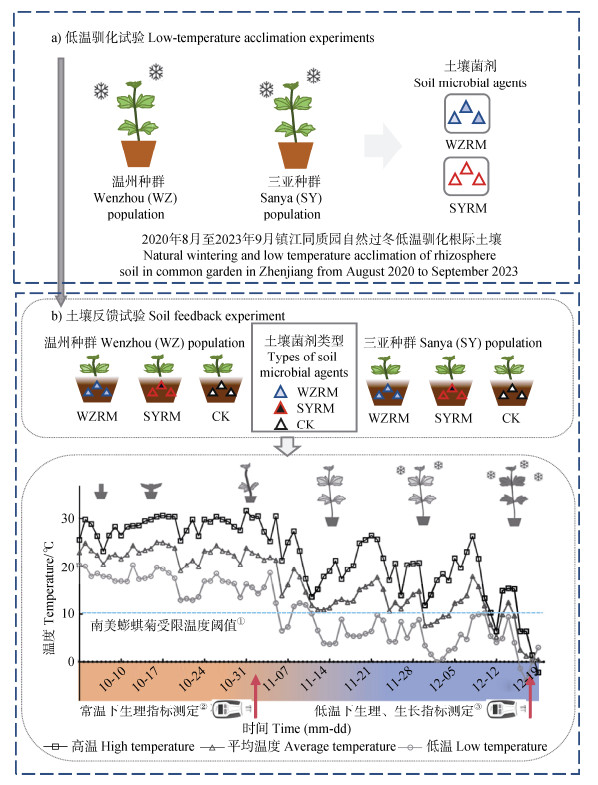
1.2 试验设计试验分为2阶段,低温驯化试验在镇江种植温州和三亚两个南美蟛蜞菊种群,并自然过冬、低温驯化三年(图 1a)和土壤反馈试验(图 1b),具体如下:
|
注:WZRM,温州种群来源的根际土壤菌剂;SYRM,三亚种群来源的根际土壤菌剂;CK,空白对照组(不添加土壤菌剂)。下同。 Note: WZRM, rhizosphere soil microbial agent(RM)sourced from Wenzhou(WZ)population; SYRM, rhizosphere soil microbial agent(RM)sourced from Sanya(SY)population; CK, blank control group(No rhizosphere soil microbial agent was added.). The same below. ①Limited temperature threshold of Sphagneticola trilobata; ②Determination of physiological indexes at normal temperature; ③Determination of physiological and growth indexes under low temperature. 图 1 试验设计(a. 不同种群南美蟛蜞菊根际土壤菌剂驯化,b. 土壤反馈试验) Fig. 1 Design of experiments(a. Acclimation of microbial agents in rhizosphere soil of different populations of Sphagneticola trilobata, b. Soil feedback experiment) |
将在镇江市(32.20°N,119.52°E,年均温15.4 ℃,年最低温–10℃)江苏大学环境与安全工程学院植物温室种植并经自然过冬三年(2020年8月—2023年9月)后的温州和三亚种群南美蟛蜞菊植株的根际土壤作为供试土壤,采用根际土壤悬液作为接种菌剂(图 1a)。
土壤悬液制备参考孙雨等[26]的方法,详细步骤如下:
试验采用统一基质土壤,其基本性状为:含水率218.5 g·kg–1,有机质116 g·kg–1,铵态氮0.35 mg·g–1,硝态氮0.42 mg·g–1。所有处理组的初始土壤均经过如下标准化处理:(1)2 mm筛网过滤去除杂质;(2)121℃高压灭菌1 h;(3)调节含水量至250 g·kg–1平衡48 h。将温州、三亚种群的南美蟛蜞菊洗净后扦插在装有营养土的花盆中心,置于江苏大学温室中自然过冬(未覆雪)培养,定期用自来水浇灌(保证水分供应)。培养三年后,于2023年10月10日(16.9 ℃ ~26.5 ℃)拔出植株,将根际土壤轻轻抖落在灭菌托盘中,每个种群取五盆根际土壤分别混匀,称取土样10 g,倒入100 mL带玻璃珠的无菌水锥形瓶中,振荡5 min,使土样充分打散,静置沉淀10 min后取上清液即为土壤悬液。其中,温州(WZ)种群来源根际土壤菌剂(Rhizosphere microorganisms,RM)命名为WZRM,三亚(SY)种群来源根际土壤菌剂命名为SYRM。
1.2.2 土壤反馈试验土壤反馈试验阶段共设置6个处理组,新种植温州、三亚两个种群植物植株分别接种WZRM菌剂、SYRM菌剂以及不接种菌剂的阴性对照组(CK)(图 1b),每个处理设置5个重复。
以200 g洗净烘干的河砂作为培养基质,在江苏大学植物培育温室中进行种植,试验时间为:2023年10月3日至2023年12月17日,反馈阶段持续75 d,试验期间环境温度如图 1b所示,相对湿度维持在75%±5%。选取植物茎段的生理学下端扦插于花盆中心,浇水浸透后置于自然环境下进行培育。每七天施加一次人工配制的霍格兰营养液[27],每天检查浇灌无菌水以保证每盆植物的水分充足。在植株长出第一对叶片后接种菌剂的处理组在植株根部施加10 mL根际土壤悬液,不接种菌剂的处理组在植株根部施加10 mL无菌水作为对照。植株生长两个半月后收获,测量植株各项生理、生长指标。
1.3 植物各项指标测定自然条件下,分别于2023年11月3日(15.6 ℃~ 27.3 ℃,常温条件,白天高温仍正常,仅夜晚低温降至约15 ℃)、2023年12月13日(4.9 ℃~ 14.9 ℃,低温胁迫,白天高温降至15 ℃以下,夜晚低温降至5 ℃以下)使用植物营养测定仪(TYS-3N,浙江托普仪器有限公司)测量植株叶片的总氮和叶绿素含量,使用多色素测量仪(MPM-100 GPS,捷克PSI,捷克)测量植株叶片的相对花青素含量;使用叶绿素荧光测定仪(FluorPen FP110,捷克PSI,捷克)测量植株叶片的光合指标。所测叶片均为从植株顶端向基端数的第二对叶片。于2023年12月17日进行全株收获,使用WinRHIZO根系扫描仪(Regent Instrument,Quebec,加拿大)扫描植株根系;完成根系扫描后置于烘箱65 ℃烘干72 h,然后分别称量地上部分和地下部分干物质量,二者之和为总生物量。
1.4 数据处理与分析采用SPSS 23.0统计软件对不同来源驯化根际菌剂处理及植物种群来源对南美蟛蜞菊生长、生理的影响进行双因素方差分析(Two-way ANOVA),使用邓肯(Duncan)检验进行多重比较,P < 0.05表明具有统计学意义,并在GraphPad Prism 9软件中进行绘图。快速荧光参数采用Min-Max归一化方法,将特征值缩放到[0,1]区间,以消除量纲影响。
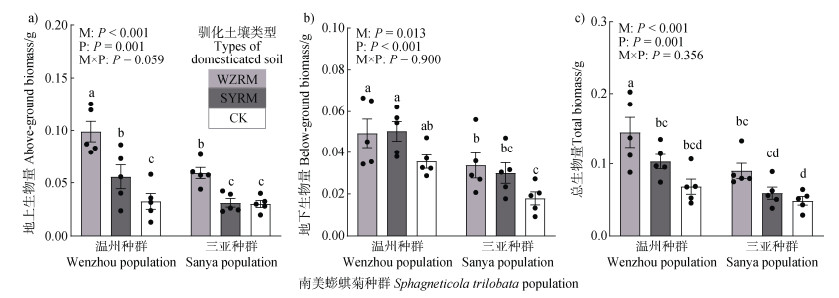
2 结果 2.1 低温胁迫下土壤微生物对不同种群南美蟛蜞菊生物量的影响在低温胁迫下,接种温州种群根际土壤微生物后,南北不同种群来源的南美蟛蜞菊地上生物量、地下生物量和总生物量与对照组相比均有明显增加,并且温州种群受到的促进作用高于三亚种群(图 2);接种三亚种群根际土壤微生物后,各种群的生物量也有所增长,但变化不如接种温州种群根际土壤微生物处理组显著,并且温州种群地上生物量(图 2a)、地下生物量(图 2b)受到的促进作用高于三亚种群(图 2);不加驯化根际土菌剂,北方(温州)种群来源的南美蟛蜞菊在地下根部生物量高于南方(三亚)种群(图 2b)。总体而言,不同根际土壤微生物对南美蟛蜞菊生物量的促进效果表现为由高到低依次为:温州种群根际土壤微生物、三亚种群根际土壤微生物、不接种根际土壤微生物。
|
注:不同字母表示不同处理间的差异显著(均值±标准误,n=5,P < 0.05)。M,菌剂;P,种群;M ×P,菌剂×种群。下同。 Note: Different letters indicated significant differences between different treatments(mean ± SE, n = 5, P < 0.05). M, Microbial agent; P, Population; M ×P, Microbial agent × population. The same below. 图 2 不同菌剂处理对南(三亚)北(温州)种群来源南美蟛蜞菊植株生物量的影响(a. 地上生物量,b. 地下生物量,c. 总生物量) Fig. 2 The effects of different microbial agents on the biomass of Sphagneticola trilobata from Southern(Sanya)and Northern(Wenzhou)populations(a. Above-ground biomass, b. Below-ground biomass, and c. Total biomass) |
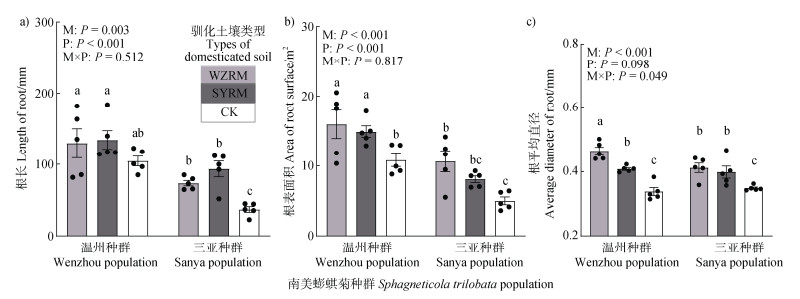
在低温胁迫下,两种来源根际土壤菌剂的施加总体上显著促进了各种群南美蟛蜞菊根系的生长(图 3),并且温州种群的根长和根表面积均明显高于三亚种群(图 3a,图 3b),根际土壤菌剂在温州种群内对根平均直径的促进效果由高到低依次为:温州种群根际土壤微生物、三亚种群根际土壤微生物、不接种根际土壤微生物;在三亚种群内对根平均直径的促进效果为:温州种群根际土壤微生物和三亚种群根际土壤微生物大于不接种根际土壤微生物(图 3c)。
|
图 3 不同菌剂处理对南(三亚)北(温州)种群来源南美蟛蜞菊根系的影响(a. 根长,b. 根表面积,c. 根平均直径) Fig. 3 The effects of different microbial agents on the roots of Sphagneticola trilobata from the Southern(Sanya)and Northern(Wenzhou)populations(a. Length of root, b. Area of root surface, and c. Average diameter of root) |
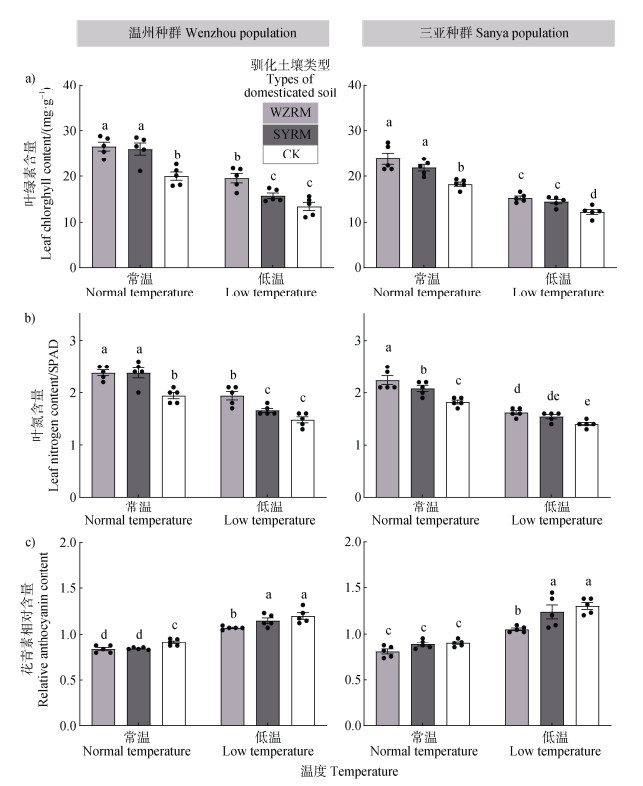
在常温(15.6 ℃~27.3 ℃)情况下,两种来源根际土壤菌剂均显著提高了植物体内叶绿素含量和叶片氮含量、显著降低花青素相对含量(图 4,表 1,P < 0.001)。随着温度降低,各种群南美蟛蜞菊的叶绿素和叶片氮含量逐渐降低、花青素相对含量逐渐升高,并且三亚种群根际土壤微生物菌剂的作用变得不显著,但温州种群根际土壤微生物菌剂对植物的作用仍然显著(图 4)。低温处理下(4.9 ℃~14.9 ℃)不加驯化根际土壤菌剂时,温州种群叶绿素含量(图 4a)和叶片氮含量(图 4b)显著高于三亚种群,花青素相对含量(图 4c)显著低于三亚种群。
|
图 4 不同菌剂处理对南(三亚)北(温州)种群来源南美蟛蜞菊叶片生理指标的影响(a. 叶绿素含量,b. 叶氮含量,c. 花青素相对含量) Fig. 4 The effects of different microbial agents on leaf physiological indexes of Sphagneticola trilobata from Southern(Sanya)and Northern(Wenzhou)populations(a.Leaf chlorophyll content, b. Leaf nitrogen content, and c. Relative anthocyanin content) |
|
|
表 1 双因素方差分析不同处理下不同种群南美蟛蜞菊的生理响应 Table 1 Two-way ANOVA for the physiological responses of Sphagneticola trilobata populations under different treatments |
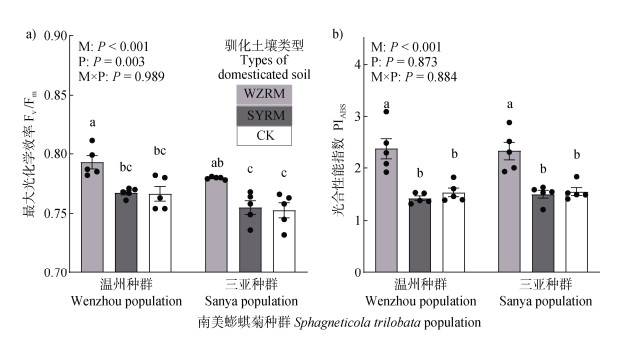
在低温胁迫下,接种温州种群根际土壤微生物菌剂的南北不同种群来源的南美蟛蜞菊的最大光化学效率(Fv /Fm)和叶片光合性能指数(PIABS)均显著高于接种三亚种群根际土壤微生物菌剂的南美蟛蜞菊和对照组,但在不同种群间根际土壤菌剂对南美蟛蜞菊的作用无显著差异(图 5)。
|
图 5 不同菌剂处理对南(三亚)北(温州)种群来源南美蟛蜞菊叶片光合指标的影响(a. 最大光化学效率Fv/Fm,b. 光合性能指数PIABS) Fig. 5 The effects of different microbial agents on leaf photosynthetic indexes of Sphagneticola trilobata from Southern(Sanya)and Northern(Wenzhou)populations(a. Maximum photochemical efficiency of photosystem Ⅱ, Fv/Fm, b. Performance index on absorption basis, PIABS) |
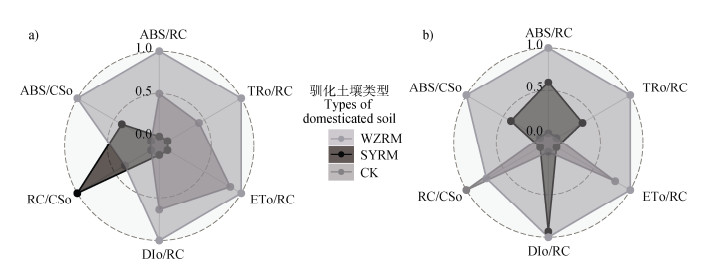
接种温州种群根际土壤微生物菌剂的南北不同种群来源的南美蟛蜞菊叶片单位面积吸收的光能(ABS/CSo)和4个代表单位反应中心性能的参数(反应中心吸收光能ABS/RC、PSⅡ的最大捕获量TRo/RC、用于电子传递的能量ETo/RC、单位反应中心的热耗散DIo/RC)均高于接种三亚种群根际土壤微生物菌剂和对照组(图 6)。
|
注:ABS/CSo,单位横截面积吸收的能量;ABS/RC,每个反应中心吸收的能量;TRo/RC,每个反应中心捕获的能量通量;ETo/RC,每个反应中心的电子传递通量;DIo/RC,每个反应中心耗散的能量通量;RC/CSo,单位横截面积的反应中心密度。 Note: ABS/CSo, Absorbed energy per unit cross section; ABS/RC, Absorbed energy per reaction center; TRo/RC, Trapped energy flux per reaction center; ETo/RC, Electron transport flux per reaction center; DIo/RC, Dissipated energy flux per reaction center; RC/CSo, Reaction center density per unit cross section. 图 6 不同菌剂处理对南(三亚)北(温州)种群来源南美蟛蜞菊叶片快速荧光参数的影响(n=5)(a. 温州种群,b. 三亚种群) Fig. 6 The effects of different microbial agents on the fast fluorescence parameters of leaves of Sphagneticola trilobata from Southern(Sanya)and Northern(Wenzhou)populations(n = 5)(a. Wenzhou population, b.Sanya population) |
本研究发现,经过低温驯化的南美蟛蜞菊根际土壤可显著促进南美蟛蜞菊在低温下的生长(图 2,图 3),并能缓解低温胁迫对南美蟛蜞菊光合系统的抑制(图 5,图 6),且高纬度温州种群的促进效果显著强于低纬度三亚种群。上述结果表明,经过低温驯化的高纬度(更冷地区)南美蟛蜞菊种群根际土壤微生物可能在南美蟛蜞菊抵抗低温胁迫、继续向高纬度地区扩张的进程中发挥重要作用。
本研究的自然过冬试验温度参考了南美蟛蜞菊自然分布区的冬季温度阈值(温州冬季气温平均在6 ℃~9 ℃,极端低温-5 ℃ ~ 0 ℃),因此,尽量保持培养环境平均温度介于8 ℃~23 ℃。尽管更强低温(如低于5 ℃)可能诱发更显著的微生物适应性变化,但本研究预试验表明,低于5 ℃时宿主植物存活率显著下降,故选择10 ℃以平衡驯化效果与植物耐受性。但对于三亚种群而言,其原生环境冬季气温平均22℃~25 ℃,最低温13.5 ℃~20 ℃,通常最低温不低于15 ℃,因此低温处理下三亚种群施加根际微生物处理组与对照组相比变化不如温州种群明显(图 4)。
有研究表明,微生物能够通过增强养分吸收、刺激根系生长来影响植物的生长和发育并提高抗逆性[28]。例如,Jo等[29]的研究发现,植物根际促生菌(PGPR)可增加积雪草(Centella asiatica(L.))叶生物量、根长。而耐寒根际微生物群落可促进植物对氮的吸收以促进植物的生长发育[30],进而有效帮助植物抵抗低温胁迫。加之,本课题组前期的研究也发现,内生菌Bacillus sp. WtEB-JS040 [31]、固氮细菌Kosakonia sp. WTB-JS007[21]等具有产吲哚-3-乙酸IAA、固氮等促生功能的微生物同样能够显著促进南美蟛蜞菊生长,而丛枝菌根真菌摩西管柄囊霉(Funneliformis mosseae)[32]及变形球囊霉(Glomus versiforme)[22]亦能够提高对营养的吸收而促进南美蟛蜞菊的生长或抗生物(病原)/非生物(氮、磷营养)胁迫。本研究发现,接种南美蟛蜞菊根际微生物后,显著提高了植株叶片氮含量(图 3)。因此,在面临低温胁迫时,接种经低温驯化的根际微生物很可能也通过促进营养吸收显著增加南美蟛蜞菊的生物量(图 2)和根系生长(图 3)。
3.2 高纬度种群根际微生物增强南美蟛蜞菊低温下的光合与代谢调控机制低温胁迫会降低植物叶绿素的含量并显著抑制植物光合系统[33],南美蟛蜞菊在面临高温、低温、干旱等胁迫时,其叶绿素荧光参数同样会明显降低[16]。然而,本研究发现,来自高纬度温州种群根际微生物能显著增加南美蟛蜞菊叶绿素含量的同时,也缓解了南美蟛蜞菊面对低温胁迫时叶绿素荧光参数的降低(图 4),提高了其最大光化学效率和光合性能指数(图 5)。这与范文强[34]发现根际微生物能够使紫花苜蓿(Medicago sativa L.)在面临非生物胁迫时展现出更高水平叶绿素含量和叶绿素荧光(Fv/Fm)的研究结果相似。
南美蟛蜞菊在受到更大的低温胁迫压力时,还可通过积累更多的花青素来减轻氧化应激,帮助其保持正常生长[17]。本研究也发现接种北方(温州)种群驯化土壤的南美蟛蜞菊花青素相对含量显著降低(图 4c),而接种南方(三亚)种群驯化土壤的南美蟛蜞菊花青素相对含量仅温州种群植株在常温下有降低,在其他处理下几乎无变化,这说明接种温州种群根际土壤微生物的南美蟛蜞菊受到了更小的低温胁迫,接种三亚种群根际土壤微生物对南美蟛蜞菊的低温响应无明显的缓解。这可能是不同纬度植物所招募的微生物群落存在差异[35]。而许多研究表明,特定的微生物群落能够通过增强光合作用来抵抗非生物胁迫[36]。例如,Chen等[37]发现PGPR通过改善微生物多样性、光合作用和酶活性来减轻盐胁迫对水稻(Orzya sativa)的影响。Xie等[38]研究发现根际细菌可通过增强与光合作用、能量代谢、固氮和防御有关基因的表达提高了水稻的耐寒性。因此,不同的微生物群落在植物应对气候变化的耐受性上有不同的效果[39]。本研究中,很可能是北方温州种群南美蟛蜞菊因长期处于更冷地带,经其驯化的土壤招募了能够帮助南美蟛蜞菊抵御寒冷胁迫的微生物群落,从而缓解南美蟛蜞菊PSII下游的电子传递过程在低温下受到的抑制,增强宿主植物活力。
当然,植物受到低温胁迫时,不止通过单一的机制来保护其免受伤害。根际微生物群落还可通过调控植物基因的转录水平、产生应激调节剂、次生代谢产物和信号分子等方式来保护植物免受不利环境的胁迫[12,40]。这些机制在未来的研究中值得进一步深入探讨。在未来的研究中可进一步添加灭菌根际土壤微生物作为土壤反馈试验的对照组,并结合多组学技术进一步解析关键微生物类群及其相应调控机制。
3.3 根际微生物驱动南美蟛蜞菊耐寒性分化与向高纬度地区扩张的潜力在全球气候变暖的大背景下,外来植物向高纬度地区扩张的趋势不容忽视。此前的研究发现,华南、东南为南美蟛蜞菊当前的适生区,但在未来气候持续变暖下,南美蟛蜞菊将持续向北扩张至华东长江沿线[18],并且,南美蟛蜞菊的生长特性表现出纬度格局,随着纬度升高耐寒性增强[24]。因此,本研究结果从根际微生物角度解释了不同种群南美蟛蜞菊耐寒性差异的可能原因,预示着驯化招募的耐寒根际微生物可促进南美蟛蜞菊向更高纬度地区扩张,为进一步加强南美蟛蜞菊入侵边界区的管控提供了理论依据。
4 结论本研究利用南北两个地理种群的南美蟛蜞菊,经过三个自然年过冬后的低温驯化的根际土壤进行土壤反馈试验,发现当南美蟛蜞菊面临低温胁迫时,其驯化招募的根际微生物能够通过促进南美蟛蜞菊根系对营养(氮)的吸收、缓解低温对南美蟛蜞菊光合系统的抑制来维持其生理过程,从而提高南美蟛蜞菊对低温环境的耐受性,最终积累了更多的生物量和维持更好的根系。北方(温州)种群南美蟛蜞菊由于本身长期处于相对更高纬度、更多受寒冷胁迫,从而进化出更强的耐寒根际微生物招募能力,并组装出更利于过冬的根际微生物群落,使其更易在寒冷的北方定殖成功。综上,南美蟛蜞菊可通过适应性调节并重新组装自身的根际微生物群落提高抗寒能力,从而具备了向更高纬度地区继续扩张的潜力。
| [1] |
Sun Y, Züst T, Silvestro D, et al. Climate warming can reduce biocontrol efficacy and promote plant invasion due to both genetic and transient metabolomic changes[J]. Ecology Letters, 2022, 25(6): 1387-1400. DOI:10.1111/ele.14000
(  0) 0) |
| [2] |
Nguyen D T C, van Tran T, Nguyen T T T, et al. New frontiers of invasive plants for biosynthesis of nanoparticles towards biomedical applications: A review[J]. Science of the Total Environment, 2023, 857: 159278. DOI:10.1016/j.scitotenv.2022.159278
(  0) 0) |
| [3] |
Li Y, Yue M, Wang Y C, et al. Invasive-plant traits, native-plant traits, and their divergences as invasion factors[J]. Ecology and Evolution, 2024, 14(6): e11525. DOI:10.1002/ece3.11525
(  0) 0) |
| [4] |
Dong B C, Yang Q, Kinlock N L, et al. Naturalization of introduced plants is driven by life-form-dependent cultivation biases[J]. Diversity and Distributions, 2024, 30(1): 55-70. DOI:10.1111/ddi.13788
(  0) 0) |
| [5] |
Xiong Y, Zheng L, Shen R F, et al. Effects of nitrogen deficiency on microbial community structure in rhizosphere soil of wheat (In Chinese)[J]. Acta Pedologica Sinica, 2022, 59(1): 218-230. DOI:10.11766/trxb202005080225 [熊艺, 郑璐, 沈仁芳, 等. 缺氮胁迫对小麦根际土壤微生物群落结构特征的影响[J]. 土壤学报, 2022, 59(1): 218-230.]
(  0) 0) |
| [6] |
Li X, Zhang Y, Kong F L, et al. Invasive plant Alternanthera philoxeroides benefits more competition advantage from rhizosphere bacteria regardless of the host source[J]. Plants, 2023, 12(11): 2085. DOI:10.3390/plants12112085
(  0) 0) |
| [7] |
Wei W, Zhu P, Chen P D, et al. Mixed evidence for plant–soil feedbacks in forest invasions[J]. Oecologia, 2020, 193(3): 665-676. DOI:10.1007/s00442-020-04703-y
(  0) 0) |
| [8] |
Reinhart K O, Callaway R M. Soil biota and invasive plants[J]. New Phytologist, 2006, 170(3): 445-457. DOI:10.1111/j.1469-8137.2006.01715.x
(  0) 0) |
| [9] |
Fu W, Wang N, Pang F, et al. Soil microbiota and plant invasions: Current and future (In Chinese)[J]. Biodiversity Science, 2017, 25(12): 1295-1302. [付伟, 王宁, 庞芳, 等. 土壤微生物与植物入侵: 研究现状与展望[J]. 生物多样性, 2017, 25(12): 1295-1302.]
(  0) 0) |
| [10] |
Yang J T, Pan Y J, Chang C L, et al. Effects of native plant-soil microbe interaction on plant invasion (In Chinese)[J]. Chinese Journal of Plant Ecology, 2024, 48(12): 1547-1560. [杨佳婷, 潘应骥, 常春玲, 等. 本地植物与土壤微生物互作对植物入侵影响的研究进展[J]. 植物生态学报, 2024, 48(12): 1547-1560.]
(  0) 0) |
| [11] |
Ettinger C L, LaForgia M L. Invasive plant species interact with drought to shift key functions and families in the native rhizosphere[J]. Plant and Soil, 2024, 494(1/2): 567-588.
(  0) 0) |
| [12] |
Vimal S R, Singh J S, Kumar A, et al. The plant endomicrobiome: Structure and strategies to produce stress resilient future crop[J]. Current Research in Microbial Sciences, 2024, 6: 100236. DOI:10.1016/j.crmicr.2024.100236
(  0) 0) |
| [13] |
Kong Y L, Qin H, Zhu C Q, et al. Research progress on the mechanism by which soil microorganisms affect soil health (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(2): 331-347. [孔亚丽, 秦华, 朱春权, 等. 土壤微生物影响土壤健康的作用机制研究进展[J]. 土壤学报, 2024, 61(2): 331-347.]
(  0) 0) |
| [14] |
Elsheikh E A E, El-Keblawy A, Mosa K A, et al. Role of endophytes and rhizosphere microbes in promoting the invasion of exotic plants in arid and semi-arid areas: A review[J]. Sustainability, 2021, 13(23): 13081. DOI:10.3390/su132313081
(  0) 0) |
| [15] |
Wu Y Q, Hu Y J, Liao F L. Wedelia trilobata—A species from introduced to potential invasive (In Chinese)[J]. Guihaia, 2005, 25(5): 413-418. [吴彦琼, 胡玉佳, 廖富林. 从引进到潜在入侵的植物——南美蟛蜞菊[J]. 广西植物, 2005, 25(5): 413-418.]
(  0) 0) |
| [16] |
Sun B Y, Sun L L, Song L Y, et al. Contrasting changes of chlorophyll fluorescence in leaves of invasive Wedelia trilobata at different temperatures under high irradiance stress (In Chinese)[J]. Journal of South China Normal University(Natural Science Edition), 2009, 41(4): 100-105. [孙蓓育, 孙兰兰, 宋莉英, 等. 入侵植物三裂叶蟛蜞菊叶片叶绿素荧光对温度的响应[J]. 华南师范大学学报(自然科学版), 2009, 41(4): 100-105.]
(  0) 0) |
| [17] |
Cai M L, Huang J D, Chen M H, et al. The role and synthesis mechanism of anthocyanins in Sphagneticola trilobata stems under low temperature[J]. Biological Invasions, 2024, 26(9): 2851-2867. DOI:10.1007/s10530-024-03348-9
(  0) 0) |
| [18] |
Liu Y T, Dai Z C, Xue Y L, et al. Prediction of suitable area of an alien invasive species(Wedelia trilobata)in China (In Chinese)[J]. Guangdong Agricultural Sciences, 2013, 40(14): 174-178. [刘勇涛, 戴志聪, 薛永来, 等. 外来入侵植物南美蟛蜞菊在中国的适生区预测[J]. 广东农业科学, 2013, 40(14): 174-178.]
(  0) 0) |
| [19] |
Dai Z C, Kong F L, Li Y F, et al. Strong invasive mechanism of Wedelia trilobata via growth and physiological traits under nitrogen stress condition[J]. Plants, 2024, 13(3): 355. DOI:10.3390/plants13030355
(  0) 0) |
| [20] |
Dai Z C, Wang X Y, Qi S S, et al. Effects of leaf litter on inter-specific competitive ability of the invasive plant Wedelia trilobata[J]. Ecological Research, 2016, 31(3): 367-374. DOI:10.1007/s11284-016-1344-0
(  0) 0) |
| [21] |
Wang J J, Wang J H, Huang Z Y, et al. Effects of endophytic nitrogen-fixing bacteria on the growth strategy of an invasive plant Sphagneticola trilobata under different nitrogen levels (In Chinese)[J]. Chinese Journal of Plant Ecology, 2023, 47(2): 195-205. [汪晶晶, 王嘉浩, 黄致云, 等. 不同氮水平下内生固氮菌对入侵植物南美蟛蜞菊生长策略的影响[J]. 植物生态学报, 2023, 47(2): 195-205.]
(  0) 0) |
| [22] |
Qi S S, He F R, Wang J J, et al. Effects of arbuscular mycorrhizal fungi on the growth and the competition of an invasive plant Wedelia trilobata (In Chinese)[J]. Microbiology China, 2020, 47(11): 3801-3810. [祁珊珊, 贺芙蓉, 汪晶晶, 等. 丛枝菌根真菌对入侵植物南美蟛蜞菊生长及竞争力的影响[J]. 微生物学通报, 2020, 47(11): 3801-3810.]
(  0) 0) |
| [23] |
Chen Q, Wu W W, Qi S S, et al. Arbuscular mycorrhizal fungi improve the growth and disease resistance of the invasive plant Wedelia trilobata[J]. Journal of Applied Microbiology, 2021, 130(2): 582-591. DOI:10.1111/jam.14415
(  0) 0) |
| [24] |
Mei Y H, Li X, Zhou J Y, et al. Both adaptability and endophytic bacteria are linked to the functional traits in the invasive clonal plant Wedelia trilobata[J]. Plants, 2022, 11(23): 3369. DOI:10.3390/plants11233369
(  0) 0) |
| [25] |
Xiao Y S, Zheng J N, Li H C, et al. Prediction of potential distribution of Wedelia trilobata in China under the background of climate change (In Chinese)[J]. Ecological Science, 2021, 40(4): 75-82. [肖雨沙, 郑洁宁, 李红春, 等. 气候变化背景下南美蟛蜞菊在中国的潜在适生区预测[J]. 生态科学, 2021, 40(4): 75-82.]
(  0) 0) |
| [26] |
Sun Y, Chang J J, Tian C J. Technical systems of reorganization and construction of crop rhizosphere microbiome (In Chinese)[J]. Biotechnology Bulletin, 2020, 36(9): 25-30. [孙雨, 常晶晶, 田春杰. 作物根际微生物组重组构建技术体系探讨[J]. 生物技术通报, 2020, 36(9): 25-30.]
(  0) 0) |
| [27] |
Wang J H, Hu D, Shi X N, et al. Different responses of invasive weed Alternanthera philoxeroides and Oryza sativa to plant growth regulators[J]. Life, 2022, 12(7): 1069. DOI:10.3390/life12071069
(  0) 0) |
| [28] |
Jiang P, Zhou Y Y, Yang K W, et al. Biodiversity and network complexity of rhizosphere soil microbiomes regulate the differentiation of Capsicum growth strategies[J]. Plant and Soil, 2025, 509(1/2): 327-345.
(  0) 0) |
| [29] |
Jo H, Lim K, Ibal J C, et al. Growth increase in the herbaceous plant Centella asiatica by the plant growth-promoting rhizobacteria Priestia megaterium HyangYak-01[J]. Plants, 2023, 12(13): 2398. DOI:10.3390/plants12132398
(  0) 0) |
| [30] |
Zhang J F, Song K J, Jin F Y, et al. A novel strategy of artificially regulating plant rhizosphere microbial community to promote plant tolerance to cold stress[J]. Science of the Total Environment, 2024, 949: 175184. DOI:10.1016/j.scitotenv.2024.175184
(  0) 0) |
| [31] |
Dai Z C, Fu W, Wan L Y, et al. Different growth promoting effects of endophytic bacteria on invasive and native clonal plants[J]. Frontiers in Plant Science, 2016, 7: 706.
(  0) 0) |
| [32] |
Li Q, Chen Q, He F R, et al. Arbuscular mycorrhizal fungi promote the growth of Wedelia trilobata and the absorption of insoluble phosphorus (In Chinese)[J]. Journal of Tropical and Subtropical Botany, 2020, 28(4): 339-346. [李琴, 陈琪, 贺芙蓉, 等. 丛枝菌根真菌促进南美蟛蜞菊生长及对难溶磷的吸收[J]. 热带亚热带植物学报, 2020, 28(4): 339-346.]
(  0) 0) |
| [33] |
Aazami M A, Asghari-Aruq M, Hassanpouraghdam M B, et al. Low temperature stress mediates the antioxidants pool and chlorophyll fluorescence in Vitis vinifera L. cultivars[J]. Plants, 2021, 10(9): 1877. DOI:10.3390/plants10091877
(  0) 0) |
| [34] |
Fan W Q. Study on the mechanism of alfalfa recruited rhizosphere microbiome in response to drought and salt stress[D]. Hohhot: Inner Mongolia Agricultural University, 2024.[范文强. 苜蓿招募根际微生物响应干旱和盐胁迫的机制研究[D]. 呼和浩特: 内蒙古农业大学, 2024.]
(  0) 0) |
| [35] |
Ma J M, Ma K, Liu J L, et al. Rhizosphere soil microbial community under ice in a high-latitude wetland: Different community assembly processes shape patterns of rare and abundant microbes[J]. Frontiers in Microbiology, 2022, 13: 783371. DOI:10.3389/fmicb.2022.783371
(  0) 0) |
| [36] |
Su F, Jacquard C, Villaume S, et al. Burkholderia phytofirmans PsJN reduces impact of freezing temperatures on photosynthesis in Arabidopsis thaliana[J]. Frontiers in Plant Science, 2015, 6: 810.
(  0) 0) |
| [37] |
Chen Z J, Zhang P, Wang B, et al. Harnessing the role of rhizo-bacteria to mitigate salinity stress in rice(Orzya sativa); focus on antioxidant defense system, photosynthesis response, and rhizosphere microbial diversity[J]. Rhizosphere, 2025, 33: 101043. DOI:10.1016/j.rhisph.2025.101043
(  0) 0) |
| [38] |
Xie Y B, Waqas M, Khan M U, et al. Overexpression of the rice gene Lsi1(low silicon gene 1)enhances plant-microbe interactions that result in improved chilling tolerance[J]. Plant Growth Regulation, 2022, 98(3): 525-538. DOI:10.1007/s10725-022-00890-1
(  0) 0) |
| [39] |
Allsup C M, George I, Lankau R A. Shifting microbial communities can enhance tree tolerance to changing climates[J]. Science, 2023, 380(6647): 835-840. DOI:10.1126/science.adf2027
(  0) 0) |
| [40] |
Zhou F F, Li X T, Tang L. Growth promotion and stress resistance of synthetic microbial community: A review (In Chinese)[J]. Soils, 2023, 55(6): 1170-1175. [周芳芳, 李晓婷, 汤利. 合成菌群促生抗逆功能的研究进展[J]. 土壤, 2023, 55(6): 1170-1175.]
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


