2. 安徽省农业科学院土壤肥料研究所, 合肥 230031;
3. 北方干旱半干旱耕地高效利用全国重点实验室(中国农业科学院农业资源与农业区划研究所), 北京 100081;
4. 中国科学院大学, 北京 100049
2. Soil and Fertilizer Research Institute, Anhui Academy of Agricultural Sciences, Hefei 230031, China;
3. State Key Laboratory of Efficient Utilization of Arable Land in China, Institute of Agricultural Resources and Regional Planning, Beijing 100081, China;
4. University of Chinese Academy of Sciences, Beijing 100049, China
土壤孔隙结构是指由土壤颗粒排列组合形成的多孔介质系统,其空间配置直接影响土壤水分入渗、气体交换和养分的动态变化[1-2]。在农业生态系统中,优化土壤孔隙结构不仅能够促进作物根系发育,还能提高养分利用效率,保障作物高产稳产[3-4]。根据孔隙的形成机制和形态特征,土壤孔隙可分为生物成因孔隙和非生物成因孔隙两大类。生物孔隙由土壤生物活动直接形成,区别于干湿交替或冻融等物理过程产生的裂隙等非生物孔隙[5-6]。生物孔隙主要由根系穿插、根系腐解遗留通道以及蚯蚓等土壤动物活动产生,通常呈连续的柱状,并在土壤剖面中形成连续的垂直空间网络[5-8]。此外,部分生物孔隙也可能呈现弯曲、分枝或局部膨大等不规则形态[9]。相较于非生物孔隙,生物孔隙在面对自然沉降、机械压实等外部扰动因素时表现出显著的结构稳定性,对维持土壤孔隙网络的完整性具有重要作用[10-11]。
近年来,X射线CT技术已成为定量表征土壤孔隙结构的重要工具。然而,由于土壤孔隙具有高度复杂的空间异质性和连通性,生物孔隙图像分割仍面临显著挑战,目前研究主要集中于管状生物孔隙的分割和量化。例如,Zhang等[5]基于形态学参数(长度/等效半径比 > 20)实现了生物孔隙的快速识别,但难以有效分离与非生物孔隙相连的生物通道。Lucas等[12]引入医学领域的“Tubeness”管状滤波器,通过多尺度σ参数检测不同直径的生物孔隙,但频繁的滤波处理会导致孔隙表面形变,显著影响比表面积等关键参数的量化精度,同时在检测粗孔隙时易造成细小孔隙的丢失。此外,Han等[13]采用基于卷积神经网络的RootPainter图像分析软件虽能准确识别二维图像中的生物孔隙,但该方法在三维空间的可视化重建方面仍存在局限。目前,生物孔隙和非生物孔隙相连,尤其是生物孔隙与裂缝垂直相交的情形,构成CT图像分割的主要技术障碍[14-15]。
砂姜黑土是典型的中低产田土壤类型之一,有机质含量低、土壤强度高、且富含黏土矿物。淮北平原砂姜黑土区长期普遍实行冬小麦-夏玉米轮作制度,高强度集约化农业管理导致土壤压实、耕层变浅等结构性障碍,加剧了土壤物理质量退化,进而制约作物产量提升[16-17]。覆盖作物种植作为一种可持续农业措施,其发达的根系系统可促进生物孔隙的形成,从而优化土壤孔隙网络[18-19]。Lucas等[20]研究发现,与种植黑麦草相比,种植油菜使5~10 cm土层生物孔隙度提高了25.0%;Zhu等[21]报道了与裸地相比,苜蓿种植使0~20 cm土层团聚体细长生物孔隙显著增加了16.6%。目前,针对土壤生物孔隙结构的研究多集中在单一尺度下的分析,尚缺乏从微尺度团聚体到大尺度土柱对覆盖作物轮作下生物孔隙的系统性比较与分析[6,20,22]。单一尺度的定量分析方法难以充分揭示生物孔隙在不同尺度上的形态特征及空间分布规律。因此,本研究利用X射线CT扫描技术,分别从大土柱尺度(直径10 cm、高20 cm),小土柱尺度(直径5 cm、高5 cm)及团聚体尺度(3~5 mm)对不同轮作模式下砂姜黑土生物孔隙结构进行系统比较分析。通过多尺度分析,本研究旨在探究覆盖作物轮作对砂姜黑土生物孔隙结构特征的影响机制,并为优化区域轮作制度提供理论依据。同时,本研究还将明确不同尺度下生物孔隙分析的优势与局限性,揭示生物孔隙的跨尺度分布特征及空间网络结构差异,为今后开展多尺度生物孔隙的定量表征提供方法支持与理论参考。
1 材料与方法 1.1 研究区概况与试验设计轮作定位试验于2019年在安徽蒙城县马店农业生态试验站开展(33°13′ N,116°33′ E)。该区属于暖温带半湿润季风气候,年均气温为14.8 ℃,年均降水量900 mm。土壤类型为河湖相石灰性沉积物发育而成的砂姜黑土,土壤颗粒组成中砂粒为8.0%、粉粒为54.1%、黏粒为37.9%。
试验采用单因素随机区组设计,共设置小麦-玉米轮作(WM)、小麦-羊角豆(Cassia occidentalis)轮作(WY)和小麦-决明子(Cassia tora Linn.)轮作(WJ)3个处理,3次重复,共计9个小区,小区面积为20 m2(4 m×5 m)。羊角豆和决明子为豆科固氮植物,兼具药用价值与生态功能[23-24],作为夏季绿肥引入轮作体系有助于缓解土壤结构退化、促进生物孔隙形成[18-19]。三种轮作处理的管理措施一致:秋季(10月)在播种冬小麦前,均采用小型微耕机进行耕作,耕作深度为0~20 cm;次年5月小麦收获后秸秆全部移除。夏季作物(玉米、羊角豆、决明子)均采用免耕直播,玉米收获后秸秆移除,羊角豆和决明子收获后秸秆切至10~15 cm并全量还田。小麦每季施用氮肥(N)138 kg·hm–2,磷肥(P2O5)120 kg·hm–2,钾肥(K2O)207 kg·hm–2作基肥,拔节期追施氮肥82.8 kg·hm–2;玉米季施用专用缓释肥(氮210 kg·hm–2,磷42 kg·hm–2,钾84 kg·hm–2)。羊角豆和决明子每季施用复合肥(氮45 kg·hm–2、磷45 kg·hm–2和钾45 kg·hm–2),播种量均为12 kg·hm–2,采用人工开沟覆土条播方式播种。
1.2 样品采集2024年9月下旬,在夏季作物收获前,于各小区作物行间随机采集土壤样品。使用PVC大环刀(大土柱:直径10 cm、高20 cm)采集0~20 cm原状土柱,使用PVC小环刀(小土柱:直径5 cm、高5 cm)在7.5 cm~12.5 cm处采集原状土柱以代表 0~20 cm土层,用保鲜膜将原状样品包裹以防止水分蒸发,每个处理3个重复,共计9个大土柱和9个小土柱样品,用于CT扫描。此外,采集0~20 cm混合土样带回实验室、风干。将样品过5 mm筛,并从每个处理中随机选取5个3~5 mm团聚体用于CT扫描。大土柱尺度以完整呈现耕层(0~20 cm)中粗大生物孔隙的连续分布特征;小土柱适用于田间批量采样及水气传输性质的快速测定分析;而3~5 mm团聚体常被用于研究微孔隙结构。基于此,本研究在3种典型尺度下对比分析生物孔隙特征,以全面理解多尺度空间分布规律。
1.3 CT扫描与图像处理使用工业CT扫描大土柱、小土柱和团聚体样品,CT仪器和扫描参数如表 1所示,大土柱、小土柱和团聚体的分辨率分别为60 μm,30 μm和6 μm,利用Datos | x2 Rec软件进行图像重建,得到8位灰度图像,以tiff格式导出。
|
|
表 1 3个尺度下样品信息和CT扫描参数 Table 1 Sample information and CT scan parameters at three scales |
使用Fiji和VG Studio Max 3.4软件进行图像处理和分析。将图像导入到Fiji软件中,首先调整亮度和对比度以增强图像,并利用中值滤波器进行降噪[25]。对于大土柱和小土柱样品,选取图像的中心区域作为感兴趣区域(Region of interest,ROI),ROI大小如表 2所示。将团聚体样品的图像导入到VG Studio Max 3.4,利用自适应矩形工具裁剪团聚体(灰度阈值为110,深度为3),以去除团聚体外部图像对图像分割的干扰,并将图像导出为tiff格式。在Fiji软件中采用全局阈值分割法将3个尺度下的样品图像分割为孔隙和土壤固相两部分[26]。
|
|
表 2 用于随机森林分类的生物孔隙特征参数 Table 2 Morphological traits of biopore objects used for random forest classification |
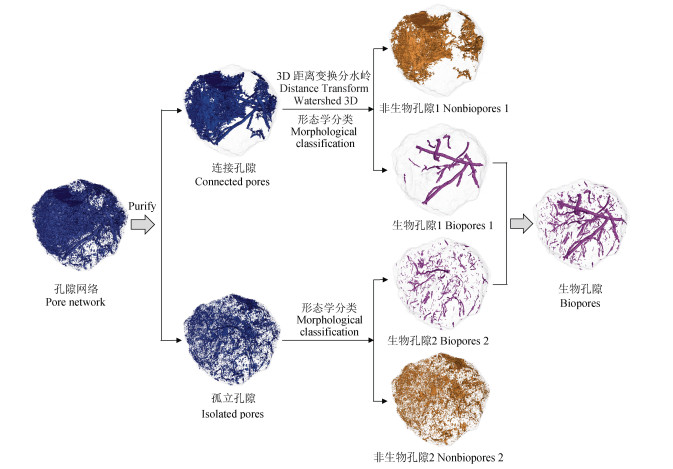
因大土柱、小土柱与团聚体的分割流程一致,下文以团聚体为例详述方法(图 1):将孔隙图像导入到Fiji软件中,利用“Purify”功能将孔隙分为连接孔隙和孤立孔隙,分别对其中的生物孔隙分离。连接孔隙中生物孔隙的分割步骤如下:首先对连接孔隙进行腐蚀(Erode),采用“MorphoLibJ”插件中3D距离变换分水岭(Distance Transform Watershed 3D)实现生物孔隙和非生物孔隙分离;采用“MorphoLibj”插件中“Connected Components Labeling”和“Analyze Regions 3D”功能计算每个孔隙的形态特征参数[27],根据以下特征参数将生物孔隙和非生物孔隙进行分离[28-30]:体积、团块性、紧密性、球形度和板状性(表 2)。从团聚体、大土柱和小土柱中手动选取典型生物孔隙和非生物孔隙(图 2),计算形态特征以建立数据集,并初步应用到部分样品生物孔隙分类中,经不断修改和完善,最终得到一个807个包含生物孔隙和非生物孔隙样本的数据集。使用该数据集结合随机森林分类器进行分类和预测:将预先分配的807样本划分为数据训练集(565个样本)和验证集(242个样本),采用决策树数量为200随机森林分类器对数据训练集进行分类训练,在数据验证集使用分类器,预测准确率为96.3%,然后在所有数据集(807个样本)上训练,袋外误差(Out-of-Bag error,OOB)为4.09%。将该分类算法应用到所有团聚体样品中,以实现生物孔隙和非生物孔隙的分割,少数孔隙分割出现错误,需要手动校正。将分割后的生物孔隙进行膨胀(Dilate),得到最终连通孔隙中的生物孔隙1(图 1)。对于孤立孔隙中生物孔隙的分割步骤如下:首先确定孤立孔隙中是否存在生物孔隙与非生物孔隙相连,如果存在则需要进行“Purify”提取最大孔隙网络或者手动筛选相连孔隙,将它们归于连接孔隙分割流程中;对于剩余孤立孔隙,则直接计算每个孔隙的形态特征,并采用与连接孔隙相同的基于随机森林模型的形态学分类流程,得到生物孔隙2。将生物孔隙1和生物孔隙2结合即可分离出完整团聚体样品中的生物孔隙网络。生物孔隙三维可视化采用VG Studio Max 3.4软件完成。
|
图 1 生物孔隙分割流程(以团聚体为例) Fig. 1 Biopore segmentation process (as an example of aggregate) |
|
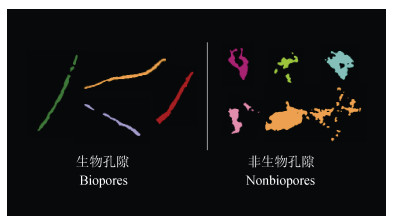
图 2 生物孔隙和非生物孔隙示例 Fig. 2 Examples of biopores and nonbiopores |
利用Fiji软件计算生物孔隙形态特征参数。利用“Analyze Regions 3D”计算孔隙体积、生物孔隙体积、生物孔隙表面积和生物孔隙平均宽度,并进一步标准化为单位体积参数;表面积密度和平均宽度密度用于衡量生物孔隙形态特征。采用“Local Thickness”算法计算生物孔隙孔径分布、平均直径和最大直径;使用“Skeletonise”和“Analyze Skeleton”得到生物孔隙长度密度,用于表征生物孔隙的长度。生物孔隙占比定义为生物孔隙体积与基于CT图像得到的孔隙体积的比值。
1.4 数据处理与分析利用SPSS 21.0软件进行单因素方差分析(One-Way ANOVA),采用最小差异显著法进行多重比较(Least Significance Difference,LSD),检验各处理间差异,显著性水平为0.05;采用Python 3.12软件进行生物孔隙形态学分类。
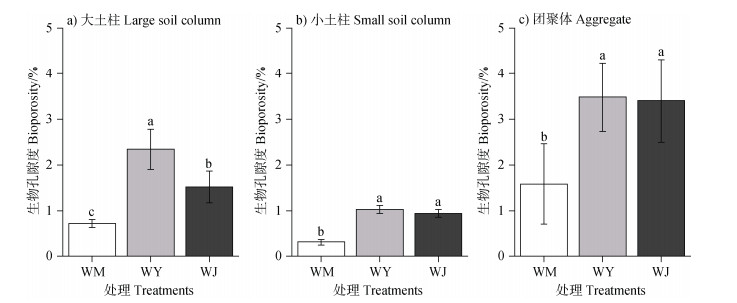
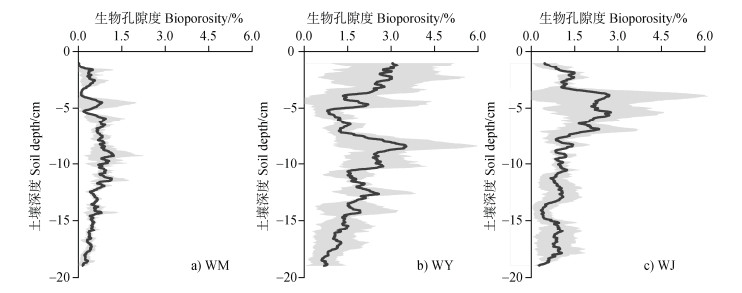
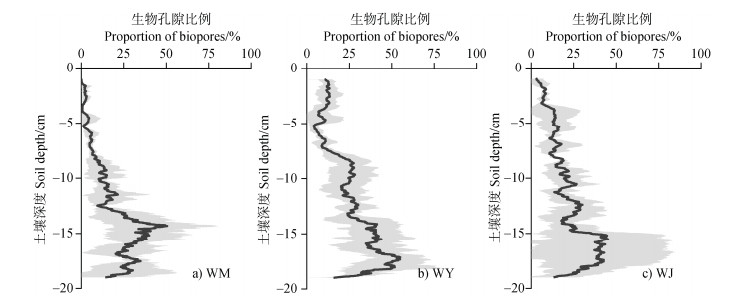
2 结果 2.1 大土柱尺度下生物孔隙特征大土柱尺度下,不同轮作模式对生物孔隙特征具有显著影响(图 3a)。与WM处理相比,WY和WJ处理的生物孔隙度分别显著增加111%和237%(P < 0.05)。从三维重构图像可知(图 4a),WM处理以细小生物孔隙为主,而WY和WJ处理在1~10 cm土层中存在部分较粗的生物孔隙,并于15 cm以下深度逐渐转为细小生物孔隙。由生物孔隙随土层深度的垂直分布可知,WY和WJ处理下生物孔隙度的最大值均集中在0~10 cm土层(图 5),而生物孔隙所占比例的最大值则集中在15~20 cm深度(图 6)。
|
注:WM—小麦-玉米轮作;WY—小麦-羊角豆轮作;WJ—小麦-决明子轮作。下同。不同小写字母表示同一尺度下不同轮作处理间存在显著性差异(P < 0.05)。 Note: WM—wheat-maize rotation; WY—wheat- Cassia occidentalis rotation; WJ—wheat-Cassia tora Linn. rotation. The same below. Different lowercase letters indicate significant differences (P < 0.05)under different crop rotations at the same scale. 图 3 不同轮作处理下大土柱、小土柱和团聚体中生物孔隙度 Fig. 3 Bioporosity under different crop rotations at large soil column, small soil column, and aggregate scales |
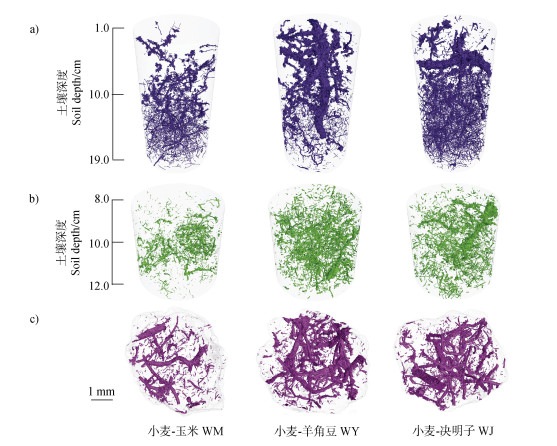
|
注:紫色部分(图a)、绿色部分(图b)和粉色部分(图c)分别表示大土柱、小土柱和团聚体中生物孔隙。 Note: The purple part, green part, and pink part indicate biopores at large soil column (Fig. a), small soil column (Fig. b)and aggregate(Fig. c)scales. 图 4 3个尺度下不同轮作处理生物孔隙三维图像 Fig. 4 Three-dimensional images of biopores under different crop rotations at three scales |
|
图 5 大土柱中生物孔隙度随土壤深度的分布 Fig. 5 Distributions of bioporosity with soil depth at large soil column scale |
|
图 6 大土柱中生物孔隙度占孔隙度的比例随土壤深度的分布 Fig. 6 Distributions of the proportion of bioporosity to porosity with soil depth at large soil column scale |
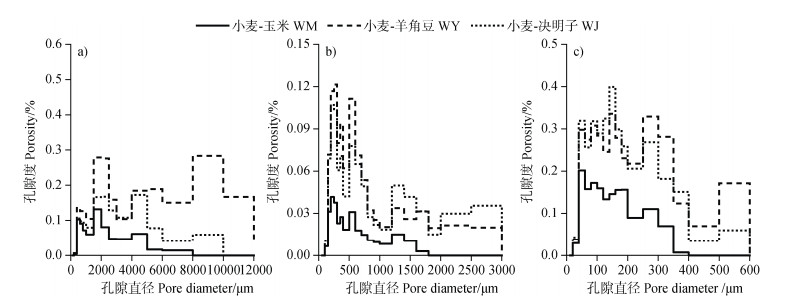
此外,相较于WM处理,WY处理显著提升了生物孔隙的平均直径、长度密度和表面积密度,分别增加了134%、83.7%和86.0%(表 3,P < 0.05);WY和WJ处理分别使生物孔隙最大孔径提高了84.8%和53.6%(P < 0.05)。就孔径分布而言,WY处理显著增加了400~2500 μm和3000~8000 μm范围内的生物孔隙度,而WJ处理显著增加了2000~2500 μm和3000~5000 μm范围内的生物孔隙度(图 7a,P < 0.05)。
|
|
表 3 3个尺度下不同轮作处理生物孔隙特征参数 Table 3 Biopore characteristic parameter under different crop rotations at three scales |
|
图 7 3个尺度下不同轮作处理生物孔隙孔径分布 Fig. 7 The distribution of biopore aperture sizes under different crop rotations at three scales |
小土柱尺度下,各轮作处理的生物孔隙特征差异显著(图 3b)。与WM处理相比,WY处理显著提高了生物孔隙度和生物孔隙占比,分别增加了243%和161%;而WJ处理则分别提高了217%和170%(表 3,P < 0.05)。由三维图像可知(图 4b),各处理均以较细生物孔隙为主,但WY和WJ处理中出现部分粗大生物孔隙。此外,相较于WM处理,WY和WJ处理显著提高了生物孔隙最大直径、长度密度、表面积密度和平均宽度(表 3,P < 0.05)。由孔径分布可知(图 7b),WY和WJ处理使100~900 μm孔隙度显著提升了220%和165%,且WJ处理使1 000~1 400 μm孔隙度显著增加了267%(P < 0.05)。
2.3 团聚体尺度下生物孔隙特征团聚体尺度下,各轮作处理对生物孔隙的影响也表现出明显差异(图 3c)。与WM处理相比,WY和WJ处理使生物孔隙度显著提升了119%和114%(P < 0.05)。团聚体内生物孔隙占孔隙度的比例为21.6%~34.4%(表 3)。就生物孔隙的三维分布而言,WY和WJ处理的生物孔隙呈现相互缠绕的网络结构,贯穿整个团聚体(图 4c)。进一步分析发现,WY处理使生物孔隙平均直径和生物孔隙长度密度显著提高了43.1%和79.9%,而WJ处理则使生物孔隙平均宽度显著提高了79.4%(表 3,P < 0.05)。同时,WY和WJ处理均显著增加了生物孔隙最大直径和表面积密度(P < 0.05)。孔径分布显示(图 7c),WY处理显著增加了20~40 μm、100~140 μm和300~350 μm孔隙度,而WJ处理则显著增加了180~300 μm以及350~400 μm孔隙度(P < 0.05)。
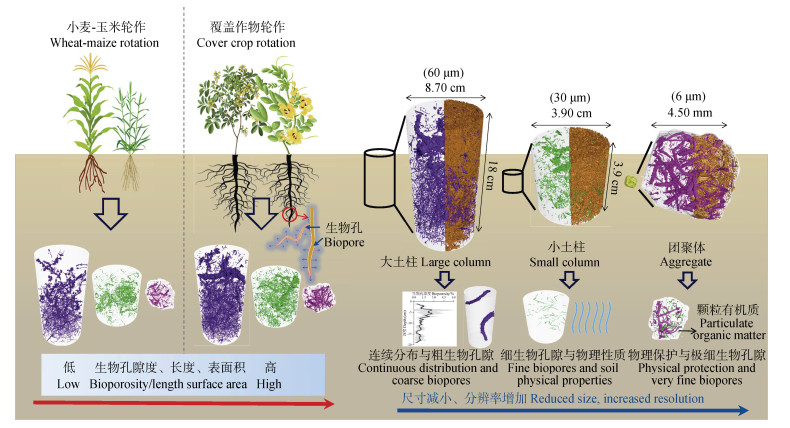
3 讨论 3.1 不同轮作模式对生物孔隙形态特征的影响本研究结果表明,与传统的小麦-玉米轮作相比,小麦-羊角豆和小麦-决明子轮作系统在3个观测尺度下均显著提高了土壤生物孔隙度(P < 0.05),表明覆盖作物轮作有助于改善砂姜黑土生物孔隙结构(图 8),这与Lucas等[20]和Zhu等[21]报道的结果类似。在小麦-玉米轮作体系中,生物孔隙的形成主要依赖于作物根系的穿插延伸、垂直下扎以及根系凋亡腐解过程。然而,小麦和玉米均为须根系作物,根系主要分布在表层,缺乏深扎的主根,极大地限制了生物孔隙的形成。而在小麦-羊角豆和小麦-决明子轮作体系中,覆盖作物较粗的主根能够最大程度穿透0~20 cm土层,形成较粗的生物孔隙,导致生物孔隙平均直径和最大直径均高于小麦-玉米轮作体系(表 3)。此外,覆盖作物发达的侧根系统通过根-土界面的挤压作用诱导产生了多级分叉生物孔隙网络[7,31],显著增加了生物孔隙的长度密度(表 3)。作为豆科作物,羊角豆和决明子能够通过自身生物固氮并以残体返还至土壤中的形式增加土壤氮库,能够调节微生物之间的协同作用[21],从而加速对根系的分解并产生大量新的生物孔隙[8,32]。同时,其秸秆还田为土壤输入了丰富的有机物质,促进团聚体的形成并增强孔隙结构的机械稳定性[33-34],从而构建了具有较高结构稳定性和抗扰动能力的生物孔隙网络[10]。综上,覆盖作物轮作通过优化根系构型与有机质输入,显著改善了砂姜黑土的生物孔隙结构。
|
注:图中括号内60 μm、30 μm、6 μm分别代表大土柱、小土柱、团聚体尺度扫描分辨率。 Note: The 60 μm, 30 μm, and 6 μm in the bracket indicate the resolutions of the large column, small column, and aggregate, respectively. 图 8 三个尺度下小麦-玉米轮作和覆盖作物轮作体系生物孔隙分布概念图 Fig. 8 Diagram of the biopore distribution under wheat-maize rotation and cover crop rotation systems at three scales |
本研究结合3D距离变换分水岭算法与随机森林分类器的CT图像分割方法,对大土柱、小土柱及团聚体三种典型尺度下生物孔隙特征进行了系统分析。虽然各尺度下的生物孔隙变化趋势一致,但所揭示的信息具有明显差异(图 8)。
大土柱尺度能够完整呈现耕作层生物孔隙的三维网络结构,尤其是在揭示生物孔隙垂直连续性分布特征方面具有显著优势。本研究发现,0~10 cm土层分布大量生物孔隙,而10~20 cm土层中孔隙数量减少但生物孔隙占比增加,表明亚表层生物孔隙在缓解土壤压实和物理结构障碍方面具有重要作用。本研究中,大土柱尺度生物孔隙的平均直径(1444~3374 μm)和最大直径(4792~8854 μm)远高于其他尺度,原因在于该尺度能够有效捕获较粗根系(> 3000 μm)的孔隙,如主根等生长、分解产生的生物孔隙。然而,受限于较低的分辨率(60 μm),该尺度难以识别细生物孔隙(< 60 μm),尤其是团聚体内部的微孔隙,且扫描和分析过程较为耗时。
小土柱尺度可有效检测较细生物孔隙(30~60 μm),并能在一定程度上降低团聚体尺度的随机性误差。此外,小土柱样品广泛应用于土壤孔隙结构及水气传输性质研究[35-36],该尺度下的生物孔隙特征对预测土壤饱和导水率和导气性具有较高的准确性[37]。然而,小土柱尺度也存在一定的局限性:样品尺寸(以5 cm高度代表20 cm或者10 cm土层)相对较小,难以完整代表整个耕作层生物孔隙的分布特征,尤其难以捕捉较长和较粗的生物孔隙,且易受局部耕作扰动影响,导致该尺度下生物孔隙占比明显低于大土柱尺度(表 3)。
团聚体尺度能够实现较高分辨率探测,特别适用于根毛等微细生物孔(6~30 μm)的量化,使其表面积密度、长度密度和平均宽度密度均显著高于其他两个尺度(表 3)。作为土壤结构的基本单元,团聚体尺度的分析对于阐明根系与土壤结构之间的互作机制及土壤有机碳的物理保护机制具有重要意义[38-39]。本研究结果表明,团聚体尺度的生物孔隙占总孔隙度比例高达21.6%~34.4%,远高于大、小土柱尺度(表 3)。与非生物孔隙相比,团聚体尺度的生物孔隙对机械扰动的抗压性更强[10],在维持团聚体稳定性中发挥重要作用。然而,该尺度无法反映团聚体间大孔隙的连通性特征,且受样品尺寸限制,存在较高的随机性,需增加样品数量以提高统计结果的可靠性。
综上,不同尺度下生物孔隙分割与定量各具优势与局限。应根据研究目标合理选择适当尺度,并推荐采用多尺度联合分析,以全面、深入地揭示土壤生物孔隙的结构特征以及生态功能。需指出,本研究所用分割方法对训练样本集依赖性较强,后续应用中应优化样本构建以提升分类精度;此外,对于非管状生物孔隙(如圆形洞穴)的识别,未来可结合三维卷积神经网络等深度学习方法进行进一步探索。
4 结论本研究基于X射线CT扫描技术结合随机森林分类,从大土柱(10 cm×20 cm)、小土柱(5 cm×5 cm)和团聚体(3~5 mm)3个尺度系统评价了不同轮作模式对砂姜黑土生物孔隙结构的影响。结果表明,覆盖作物轮作显著提升了各尺度的生物孔隙度,有效改善了砂姜黑土区土壤结构。在尺度对比上,大土柱尺度能够反映耕层生物孔隙连续性,且能捕捉粗大孔隙(> 3000 μm);小土柱尺度适用于捕捉较细孔隙(30~60 μm),为揭示生物孔隙与水气传输性质之间的定量关系提供了可靠的分析手段;团聚体尺度可识别极细孔隙(6~30 μm),揭示其在团聚体结构与有机碳保护中的重要作用。建议未来研究采用多尺度CT分析与高精度图像识别技术,以全面深入地解析土壤生物孔隙的形成机制及其生态功能,为砂姜黑土区土壤结构改良与可持续农田管理提供理论支撑。
| [1] |
Rabot E, Wiesmeier M, Schlüter S, et al. Soil structure as an indicator of soil functions: A review[J]. Geoderma, 2018, 314: 122-137. DOI:10.1016/j.geoderma.2017.11.009
(  0) 0) |
| [2] |
Li B G, Zhou H, Wang G, et al. Explore the "transparent" soils: Soilporelogy has sailed (In Chinese)[J]. Acta Pedologica Sinica, 2023, 60(5): 1221-1230. DOI:10.11766/trxb202305310215 [李保国, 周虎, 王钢, 等. 探索"透明" 土壤体: 土壤孔隙学的时代已经启航[J]. 土壤学报, 2023, 60(5): 1221-1230.]
(  0) 0) |
| [3] |
Zhang Z B, Peng X H. Bio-tillage: A new perspective for sustainable agriculture[J]. Soil and Tillage Research, 2021, 206: 104844. DOI:10.1016/j.still.2020.104844
(  0) 0) |
| [4] |
Liu C Z, Si B C, Zhao Y, et al. Drivers of soil quality and maize yield under long-term tillage and straw incorporation in Mollisols[J]. Soil and Tillage Research, 2025, 246: 106360. DOI:10.1016/j.still.2024.106360
(  0) 0) |
| [5] |
Zhang Z B, Liu K L, Zhou H, et al. Three dimensional characteristics of biopores and non-biopores in the subsoil respond differently to land use and fertilization[J]. Plant and Soil, 2018, 428(1): 453-467.
(  0) 0) |
| [6] |
Wang S, Zhang S, Zhang Y, et al. Effects of different tillage practices of soil biopores and nonbiopores structures in sugarcane field soils of Guangxi (In Chinese)[J]. Journal of Southern Agriculture, 2024, 55(9): 2613-2622. [王松, 张硕, 张钰, 等. 不同耕作方式对广西蔗田土壤生物性和非生物性孔隙结构的影响[J]. 南方农业学报, 2024, 55(9): 2613-2622.]
(  0) 0) |
| [7] |
Wendel A S, Bauke S L, Amelung W, et al. Root-rhizosphere-soil interactions in biopores[J]. Plant and Soil, 2022, 475(1): 253-277.
(  0) 0) |
| [8] |
Haling R E, Tighe M K, Flavel R J, et al. Application of X-ray computed tomography to quantify fresh root decomposition in situ[J]. Plant and Soil, 2013, 372(1): 619-627.
(  0) 0) |
| [9] |
Mele G, Buscemi G, Gargiulo L, et al. Soil burrow characterization by 3D image analysis: Prediction of macroinvertebrate groups from biopore size distribution parameters[J]. Geoderma, 2021, 404: 115292. DOI:10.1016/j.geoderma.2021.115292
(  0) 0) |
| [10] |
Tian M, Whalley W R, Zhou H, et al. Does no-tillage mitigate the negative effects of harvest compaction on soil pore characteristics in Northeast China[J]. Soil and Tillage Research, 2023, 233: 105787. DOI:10.1016/j.still.2023.105787
(  0) 0) |
| [11] |
Phalempin M, Jentzsch N, Köhne J M, et al. Soil structure development in a five-year chronosequence of maize cropping on two contrasting soil textures[J]. Soil and Tillage Research, 2025, 251: 106561. DOI:10.1016/j.still.2025.106561
(  0) 0) |
| [12] |
Lucas M, Schlüter S, Vogel H J, et al. Soil structure formation along an agricultural chronosequence[J]. Geoderma, 2019, 350: 61-72. DOI:10.1016/j.geoderma.2019.04.041
(  0) 0) |
| [13] |
Han E, Kirkegaard J A, White R, et al. Deep learning with multisite data reveals the lasting effects of soil type, tillage and vegetation history on biopore genesis[J]. Geoderma, 2022, 425: 116072. DOI:10.1016/j.geoderma.2022.116072
(  0) 0) |
| [14] |
Garbout A, Munkholm L J, Hansen S B. Tillage effects on topsoil structural quality assessed using X-ray CT, soil cores and visual soil evaluation[J]. Soil and Tillage Research, 2013, 128: 104-109. DOI:10.1016/j.still.2012.11.003
(  0) 0) |
| [15] |
Rooney E C, Bailey V L, Patel K F, et al. Soil pore network response to freeze-thaw cycles in permafrost aggregates[J]. Geoderma, 2022, 411: 115674. DOI:10.1016/j.geoderma.2021.115674
(  0) 0) |
| [16] |
Xiong P, Guo Z C, Li W, et al. Regional analysis of maize yield and physiochemical properties of Shajiang black soil(vertisol)in Huaibei Plain (In Chinese)[J]. Soils, 2021, 53(2): 391-397. [熊鹏, 郭自春, 李玮, 等. 淮北平原砂姜黑土玉米产量与土壤性质的区域分析[J]. 土壤, 2021, 53(2): 391-397.]
(  0) 0) |
| [17] |
Wang Y K, Guo Z C, Zhang Z B, et al. Effect of tillage practices on soil physical properties and maize growth in Shajiang black soil (vertisol) (In Chinese)[J]. Acta Pedologica Sinica, 2019, 56(6): 1370-1380. DOI:10.11766/trxb201902280624 [王玥凯, 郭自春, 张中彬, 等. 不同耕作方式对砂姜黑土物理性质和玉米生长的影响[J]. 土壤学报, 2019, 56(6): 1370-1380.]
(  0) 0) |
| [18] |
Budhathoki S, Lamba J, Srivastava P, et al. Impact of land use and tillage practice on soil macropore characteristics inferred from X-ray computed tomography[J]. Catena, 2022, 210: 105886. DOI:10.1016/j.catena.2021.105886
(  0) 0) |
| [19] |
Singh J, Singh N, Kumar S. X-ray computed tomography–measured soil pore parameters as influenced by crop rotations and cover crops[J]. Soil Science Society of America Journal, 2020, 84(4): 1267-1279. DOI:10.1002/saj2.20105
(  0) 0) |
| [20] |
Lucas M, Nguyen L T T, Guber A, et al. Cover crop influence on pore size distribution and biopore dynamics: Enumerating root and soil faunal effects[J]. Frontiers in Plant Science, 2022, 13: 928569. DOI:10.3389/fpls.2022.928569
(  0) 0) |
| [21] |
Zhu D, Sun L, Mao L N, et al. Combined effects of cropping alfalfa (Medicago sativa L.) on the soil pore structure, microbial communities and organic carbon fractions in saline soils[J]. Applied Soil Ecology, 2025, 208: 105993. DOI:10.1016/j.apsoil.2025.105993
(  0) 0) |
| [22] |
Casali E, Larsbo M, Koestel J, et al. Macropore flow in relation to the geometry and topology of soil macropore networks: re-visiting the kinematic wave equation[J]. Journal of Hydrology, 2024, 630: 130732. DOI:10.1016/j.jhydrol.2024.130732
(  0) 0) |
| [23] |
Cheng W L, Li M, Han S, et al. Effect of different kinds of summer green manure on improvement of protected soil (In Chinese)[J]. Soil and Fertilizer Sciences in China, 2021(4): 83-87. [程文龙, 李敏, 韩上, 等. 不同种类夏绿肥对设施土壤的改良效应[J]. 中国土壤与肥料, 2021(4): 83-87.]
(  0) 0) |
| [24] |
Pal S, Kumar P, Ramakrishna E, et al. Extract and fraction of Cassia occidentalis L. (a synonym of Senna occidentalis) have osteogenic effect and prevent glucocorticoid-induced osteopenia[J]. Journal of Ethnopharmacology, 2019, 235: 8-18. DOI:10.1016/j.jep.2019.01.029
(  0) 0) |
| [25] |
Schindelin J, Arganda-Carreras I, Frise E, et al. Fiji: An open-source platform for biological-image analysis[J]. Nature Methods, 2012, 9(7): 676-682. DOI:10.1038/nmeth.2019
(  0) 0) |
| [26] |
Otsu N. A threshold selection method from gray-level histograms[J]. IEEE Transactions on Systems, Man, and Cybernetics, 1979, 9(1): 62-66. DOI:10.1109/TSMC.1979.4310076
(  0) 0) |
| [27] |
Legland D, Arganda-Carreras I, Andrey P. MorphoLibJ: Integrated library and plugins for mathematical morphology with ImageJ[J]. Bioinformatics, 2016, 32(22): 3532-3534. DOI:10.1093/bioinformatics/btw413
(  0) 0) |
| [28] |
Schlüter S, Leuther F, Albrecht L, et al. Microscale carbon distribution around pores and particulate organic matter varies with soil moisture regime[J]. Nature Communications, 2022, 13: 2098. DOI:10.1038/s41467-022-29605-w
(  0) 0) |
| [29] |
Leuther F, Wolff M, Kaiser K, et al. Response of subsoil organic matter contents and physical properties to long-term, high-rate farmyard manure application[J]. European Journal of Soil Science, 2022, 73(2): e13233. DOI:10.1111/ejss.13233
(  0) 0) |
| [30] |
Ding T Y, Guo Z C, Wang Y K, et al. The spatial distribution of particulate organic matter within aggregates of Shajiang black soil under various straw return practices based on X-ray CT technology and machine learning (In Chinese)[J]. Acta Pedologica Sinica, 2025, 62(2): 375-387. DOI:10.11766/trxb202401310052 [丁天宇, 郭自春, 王玥凯, 等. 不同秸秆还田方式下砂姜黑土团聚体内颗粒有机质的空间分布特征——基于X射线CT技术和机器学习[J]. 土壤学报, 2025, 62(2): 375-387.]
(  0) 0) |
| [31] |
Bodner G, Leitner D, Kaul H P. Coarse and fine root plants affect pore size distributions differently[J]. Plant and Soil, 2014, 380(1): 133-151.
(  0) 0) |
| [32] |
Phalempin M, Landl M, Wu G M, et al. Maize root-induced biopores do not influence root growth of subsequently grown maize plants in well aerated, fertilized and repacked soil columns[J]. Soil and Tillage Research, 2022, 221: 105398. DOI:10.1016/j.still.2022.105398
(  0) 0) |
| [33] |
Sodhi G P S, Beri V, Benbi D K. Soil aggregation and distribution of carbon and nitrogen in different fractions under long-term application of compost in rice–wheat system[J]. Soil and Tillage Research, 2009, 103(2): 412-418. DOI:10.1016/j.still.2008.12.005
(  0) 0) |
| [34] |
Witzgall K, Vidal A, Schubert D I, et al. Particulate organic matter as a functional soil component for persistent soil organic carbon[J]. Nature Communications, 2021, 12: 4115. DOI:10.1038/s41467-021-24192-8
(  0) 0) |
| [35] |
Koestel J, Larsbo M, Jarvis N. Scale and REV analyses for porosity and pore connectivity measures in undisturbed soil[J]. Geoderma, 2020, 366: 114206. DOI:10.1016/j.geoderma.2020.114206
(  0) 0) |
| [36] |
Qian Y Q, Xiong P, Wang Y K, et al. Effect of tillage practices on soil pore structure characteristics in Shajiang black soil (In Chinese)[J]. Acta Pedologica Sinica, 2024, 61(1): 52-63. DOI:10.11766/trxb202201190027 [钱泳其, 熊鹏, 王玥凯, 等. 不同耕作方式对砂姜黑土孔隙结构特征的影响[J]. 土壤学报, 2024, 61(1): 52-63.]
(  0) 0) |
| [37] |
Zhang Z B, Liu K L, Zhou H, et al. Linking saturated hydraulic conductivity and air permeability to the characteristics of biopores derived from X-ray computed tomography[J]. Journal of Hydrology, 2019, 571: 1-10.
(  0) 0) |
| [38] |
Six J, Elliott E T, Paustian K. Soil macroaggregate turnover and microaggregate formation: A mechanism for C sequestration under no-tillage agriculture[J]. Soil Biology & Biochemistry, 2000, 32(14): 2099-2103.
(  0) 0) |
| [39] |
Guo Z C, Ding T Y, Wang Y K, et al. Quantifying and visualizing soil macroaggregate pore structure and particulate organic matter in a Vertisol under various straw return practices using X-ray computed tomography[J]. Geoderma, 2024, 452: 117105. DOI:10.1016/j.geoderma.2024.117105
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


