2. 南京师范大学地理科学学院, 南京 210023;
3. 江苏省地理信息资源开发与利用协同创新中心, 南京 210023;
4. 海南大学南繁学院, 海南三亚 572025
2. School of Geography Science, Nanjing Normal University, Nanjing 210023, China;
3. Jiangsu Center for Collaborative Innovation in Geographical Information Resource Development and Application, Nanjing 210023, China;
4. College of Breeding and Multiplication, Hainan University, Sanya, Hainan 572025, China
稳定同位素技术是研究土壤氮循环的重要方法[1],铵态氮(NH4+-N)作为重要的无机氮形态,其氮(N)同位素丰度的准确测定对深入理解土壤氮转化过程、植物氮源偏好以及温室气体(N2O)排放等方面均有重要意义。从样品中有效地提取NH4+是准确测定土壤浸提液中NH4+-15N丰度的前提[2],目前主要有三种土壤NH4+-15N丰度分析预处理方法:蒸馏法(Kjeldahl distillation)[3]、气体产生法[4]和扩散法(Ammonia diffusion)[5]。蒸馏法由于所需样品量大,且易交叉污染而被逐渐淘汰。气体产生法是通过次溴酸钠等强氧化剂,将浸提液中的NH4+氧化为N2或N2O,一般用于浓度适宜的标记NH4+-15N丰度测定,对于低浓度或自然丰度NH4+,可能因浸提液的胶体特性,无法完全氧化NH4+造成同位素分馏[6]。扩散法是目前唯一可有效分离土壤NH4+-N的方法,可单独或与其他方法联用测定NH4+-15N丰度[7-8]。其原理是:通过MgO、NaOH等提高pH,将NH4+转化为气态NH3后,被加酸滤纸片收集。干燥后的滤纸片经联用元素分析仪的同位素比值质谱仪(EA-IRMS)测定,得到NH4+-15N丰度。该方法操作简便,样品间不易交叉污染[8-10],适用于不同浓度、不同丰度的NH4+-15N测定。
扩散法最常用于标记NH4+-15N样品转化,NH4+-N浓度在1 mg·L–1以上时单独使用扩散法(体积20~50 mL)即可完成转化[11-12]。低于1 mg·L–1的NH4+-N标记样品,扩大样品体积可满足扩散N量要求,但测量值与理论值之间的误差会随样品丰度升高而明显增大[13]。然而,实际土壤环境中常有NH4+-N浓度较低的情况,如:碱性紫色土因NH4+-N快速转化为硝态氮(NO3–-N)而浓度极低;排水期的水稻土因硝化作用增强、与反硝化耦合,也会造成NH4+-N浓度低[14]。低浓度下继续使用20~50 mL的扩散体系,通常因氮量不足而受分馏效应及杂质氮干扰,导致精密度和准确度显著下降[5]。虽然扩散法联合化学法[15-16]或反硝化细菌法[17-20],能够大幅提高测定低浓度NH4+-N的灵敏度,但是操作步骤繁琐,涉及多种试剂,对操作人员要求甚高,难免会增加反应体系的空白,多个反应过程也会加剧同位素分馏[16]。显然,单独使用扩散法仍然是分离、转化NH4+-N的最佳方法。有少量研究尝试在水体样品中使用扩散法转化更低浓度、更大体积的NH4+-N[21-22],那么在土壤浸提液中,是否也能通过优化扩散体系,有效提高扩散法的灵敏度和准确度,实现对更低浓度NH4+-15N的测定?
自然丰度技术在氮循环的研究中日益受到关注,一般认为扩散法不适用于自然丰度NH4+-15N测定[6,23]。近年来,有个别研究尝试将其用于海水样品,发现扩散体系N量达到50 µg以上,其误差(SD)为0.20‰~1.30‰[24],通过浓缩样品体积再扩散,甚至能实现5 µmol·L–1 NO3–的准确测定。但是,尚不能明了扩散法能否单独用于高盐体系土壤浸提液中自然丰度NH4+-15N的测定。也有研究建议,将低浓度的自然丰度NH4+先扩散法分离,经碱性过硫酸钾(K2S2O8)或次溴酸钠(NaBrO)将其氧化为NO3–或NO2–后,结合反硝化细菌法或化学法生成N2O进行15N丰度测定[16–18]。其中,反硝化细菌法对反应氮量要求极低[18](≥10 nmol),可大幅提高测定的灵敏度,但是扩散-氧化-反硝化涉及多个反应步骤[20],各类试剂中的杂质氮难免增加反应体系的空白,需要使用极高纯度、N杂质含量极低的试剂,才能不影响低浓度样品的测定;每一反应步骤中的不完全转化,亦会加剧同位素分馏,降低结果的准确度和精密度[18]。相比之下,扩散法步骤简单、易于操作,因此探讨其在自然丰度土壤浸提液样品中的适用性,明确其最佳反应条件、反应浓度,有助于推动土壤氮转化研究的方法技术。
低浓度NH4+-N样品,通常需要较大反应体积才能获得所需的N量,体积变大扩散效率下降,受回收不完全的影响和杂质氮的干扰,15N测定值出现偏低或偏离[25-26]。改进扩散法的回收方式有助于提高回收率,减小误差。悬挂式和扩散包式是目前扩散体系常见的两种酸阱。虽然悬挂式酸阱成本低廉、制作简便,但相同培养条件下扩散包式酸阱的氮回收率显著高于悬挂法[9]。扩散包通常由透气疏水的聚四氟乙烯薄膜(PTFE)制作,文献中多使用Millipore公司生产的膜[27-28],价格昂贵,为降低成本甚至回收利用[18]。如果有性能相近却价格低廉的替代品,可大幅节约实验成本。此外,在加大样品体积的同时,延长培养时间也可提高回收率[9,16],升高培养温度可加快扩散进程、缩短周期,但可溶性有机氮(DON)也可能转化为NH4+,干扰测定[12-13]。上述均为低浓度NH4+-15N扩散方法的进一步优化提供了思路。事实上,100%的回收率并非扩散法的必需条件[27,29],在样品的测定结果精密度良好的情况下,通过同批次标样的标准曲线[25]或使用测得的分馏系数[24],可以校正因回收不完全或杂质氮干扰的测定结果偏差,保证低浓度NH4+-15N分析的准确性。
因此,本文的研究目的为:(1)优化酸阱设计;(2)探讨适合土壤浸提液中低浓度标记NH4+-15N的扩散体积-培养温度-扩散时间条件;(3)探讨单独使用扩散法能否用于土壤浸提液中自然丰度NH4+-15N测定。
1 材料与方法 1.1 扩散法操作步骤 1.1.1 酸阱制作本试验对比了四种酸阱放置方式:悬挂法、瓶口夹层法、信封法和双层膜法。
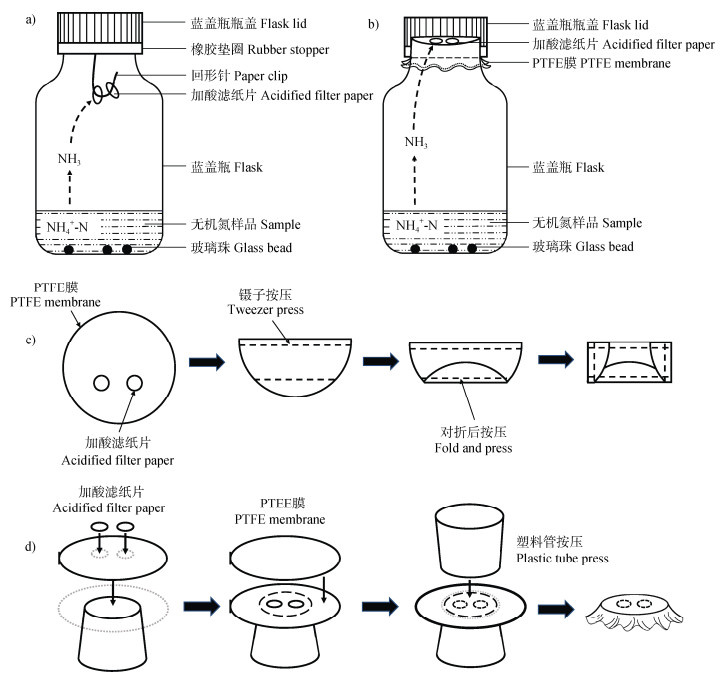
悬挂式酸阱[5](图 1a):将回形针弯成挂钩状,穿过硅橡胶垫圈并固定,再将垫圈在瓶盖底部按压固定,用镊子在挂钩上穿进两片直径约7 mm的小圆滤纸片(Whatman No.42 Cat No. 1442-055),每片用移液枪均匀润湿10 μL的1 mol·L–1 H2C2O4,最后将带有硅橡胶垫圈和滤纸片的瓶盖旋紧即可密封。
|
注:PTFE为聚四氟乙烯薄膜。a)b)c)d)分别为悬挂式酸阱、瓶口夹层式酸阱、信封式酸阱及双层膜式酸阱。 Note: Figure a), b), c)and d)depicts the suspended acidified filter paper, the fixed polytetrafluoroethylene(PTFE)trap on the opening of the bottle, the envelope made by PTFE and the doubling layer of PTFE trap, respectively. 图 1 扩散法的酸阱制作示意图 Fig. 1 Schematic diagrams of acid traps fabrication by diffusion method |
信封式酸阱(图 1c):夹取两片滤纸片于PTFE膜上,同上用10 μL的1 mol·L–1 H2C2O4均匀润湿,使用干净的镊子以信封方式密封加酸滤纸片,小心将扩散包放入样品瓶中,确保其漂浮于样品溶液上。
瓶口夹层式酸阱[9](图 1b):同上夹取两张加酸滤纸片于一张PTFE膜上,再盖上一张PTFE,将含滤纸片的两层膜置于瓶口,旋紧瓶盖,即可在瓶口处作为酸阱吸收NH3。
双层膜式酸阱(图 1d):取一直径约为1.5 cm的塑料接头作为母头,在母头上放置一片PTFE膜和两片加酸滤纸,再覆盖一张PTFE膜,用公头(直径约为1.8 cm)手动按压,使两层PTFE膜包裹住滤纸片并将其密封在内,轻轻旋转确保膜沿整个圆周密封,将扩散包放入样品瓶中。
1.1.2 扩散法分离转化NH4+-15N用1 mol·L–1 KCl(国药分析纯,450℃高温灼烧48 h)配制自然丰度或标记丰度(NH4)2SO4溶液,实验用水均为超纯水。根据样品溶液浓度移取适量体积于250 mL蓝盖瓶中,瓶内放入3颗玻璃珠及一个扩散包(悬挂式酸阱直接盖上瓶盖),加入0.3 g MgO(国药分析纯,450℃高温灼烧6 h)后立即旋紧摇匀,放入恒温摇床140 r·min–1培养若干时间后,取出扩散包,用镊子取出滤纸片放入96孔板内(悬挂法则从挂钩上用镊子取下),放入无NH3的真空干燥器内至少干燥24 h后[27],用锡杯包样,通过EA-IRMS测定15N丰度,即为样品中的NH4+-N的15N丰度。
1.2 扩散法测定低浓度土壤标记样品NH4+-15N优化方案 1.2.1 酸阱优化以往制作扩散包所用的0.22 μm 47 mm PTFE膜来自Merck Millipore公司,价格昂贵(每片大于等于40 yuan)。为了能找到性能相近且价格低廉的平替,本研究采用了透气更佳、材质柔软的国产纯聚PTFE膜(海宁市桃园医疗化工仪器厂)(每片约0.4 yuan),结合1.1.1中酸阱的不同制作方式对比其15N测定值和回收率。具体如下:用1 mol·L–1 KCl溶液配制3 mg·L–1N 0.510 atom%的(NH4)2SO4(上海化工研究院),取20 mL如1.1.2扩散,25 ℃摇床培养(以下简称“摇培”)48 h后干燥包样,通过EA-IRMS测定15N丰度和峰面积。为比较不同酸阱的回收率,在锡杯中放置2片小圆滤纸片,滴入5 μL与扩散体系N量相当的0.510 atom%的(NH4)2SO4溶液,干燥后经EA-IRMS测定得到峰面积,即为扩散体系的总氮量。
1.2.2 培养时间和培养体积优化在1.2.1基础上选择效果最优的酸阱,将5.200 atom%(NH4)2SO4,配制成0.1、0.2、0.3、0.4和0.5 mg·L–1的低浓度标记样品,25 ℃扩散摇培。首先取50 mL,摇培扩散2、4 d;接着,将0.1 mg·L–1样品扩大体积至200 mL,0.2~0.3 mg·L–1样品扩大体积至100 mL,摇培扩散4、6、8 d。由于扩大体积后培养8 d的测定结果准确度和精密度最佳,又比较了100 mL、200 mL体积下扩散8 d的15N测定结果,同时设置同浓度已知丰度的(NH4)2SO4(4.960 atom%、6.010 atom%)作为标样,制作标准曲线校正15N测定结果[25]。
1.2.3 培养温度优化通过1.2.1和1.2.2确定了最佳酸阱、培养时间和样品体积后,研究提高培养温度能否缩短扩散时间、提高回收率。具体方案为:取0.2 mg·L–1、0.5 mg·L–1N 5.200 atom%的(NH4)2 SO4 100 mL,在37 ℃下扩散3、6 d,在50 ℃下扩散2、4 d,经EA-IRMS得到15N丰度和峰面积,以探索最佳实验温度和培养时间。回收率计算同1.2.1。
1.3 扩散法测定自然丰度样品δ15N-NH4+优化方案 1.3.1 静置和摇培优化扩散法很少单独用于自然丰度NH4+的δ15N值测定,为比较静置和摇培方式的影响,采用以下方法:实验室(NH4)2SO4标准样品(经EA-IRMS测定,δ15N-NH4+=4.22‰±0.22‰),以3 mg·L–1 20 mL和1.2 mg·L–1 50 mL扩散(均含60 μg N),摇培或静置2、4、6、8 d。所有样品均使用2 mol·L–1 KCl溶液配置。
1.3.2 培养温度优化为了试验升高培养温度能否缩短扩散所需时间、提高回收率,用2 mol·L–1 KCl溶液配置0.2和0.5 mg·L–1N的实验室(NH4)2SO4标准样品,以100 mL反应体积,分别在37 ℃下扩散3 d和6 d,在50 ℃下扩散2 d和4 d。
1.3.3 单独扩散包法测定以往自然丰度NH4+-N样品极少单独使用扩散法。为试验1.1.1中优化的酸阱扩散包能否实现对低浓度自然丰度NH4+-N测定,用2 mol·L–1 KCl溶液分别配置了0.1、0.2、0.5、1.0、2.0 mg·L–1N的自然丰度(NH4)2SO4,摇培扩散6 d。
1.4 数据分析和校正以上实验每个处理均设置5个重复。
本文中测定值与理论值的比值均利用式(1)计算绝对差距[13]:
| $ \lambda {\text{ = }}\frac{M}{{\text{E}}} $ | (1) |
式中,λ表示15N测定值与理论值的比值;M表示测量值,atom%或‰;E表示理论值,atom%或‰。
试验数据处理采用SPSS 26.0进行单因素方差分析(ANOVA)检验差异显著性,使用Origin 2021进行图像绘制。
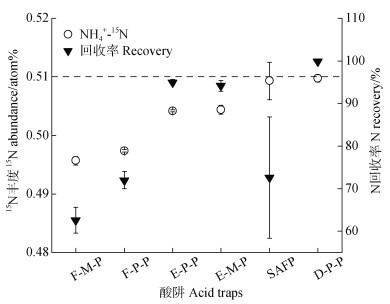
2 结果 2.1 扩散法中不同酸阱对NH4+-15N测定效果的影响本文试验了四种不同酸阱制作方式和两种不同价格的PTFE膜对3 mg·L–1 0.510 atom% NH4+-15N的测定影响,结果(图 2)表明:瓶口夹层法的15N测定准确度、回收率均为最低,回收率不足70.0%,使用Millipore和纯PTFE膜的15N测定值与理论值比值分别为0.972和0.975;悬挂法回收率变化较大(58.3%~86.9%),总体略高于瓶口夹层法,15N测定值很接近理论值,SD显著降低,均不超过0.003 atom%;信封法制备的扩散包回收率显著上升,两种PTFE膜均几乎达到95%,15N测定值与理论值比值均为0.989,SD均小于0.001 atom%;双层膜法的N回收率最高(99.8%),测定值最为接近理论值(0.999),SD最低(0.00011 atom%)。综上,两种PTFE膜性能无差异,双层膜法制作扩散包的回收率、准确度和精密度均最高,悬挂法的准确度较好,但回收率变化大,精密度也低于双层膜法。
|
注:图中虚线为理论丰度0.510 atom%。F-M-P、F-P-P为使用Millipore PTFE、国产纯PTFE制作的瓶口夹层式酸阱,E-P-P、E-M-P为使用纯PTFE、Millipore PTFE制作的信封式酸阱,SAFP代表悬挂式酸阱,D-P-P代表使用纯PTFE制作的双层膜式酸阱。 Note: The dashed line in the figure indicates the expected value of 0.510 atom%. The acid traps include: F-M-P(fixed Millipore PTFE trap on the bottle opening), F-P-P(fixed pure PTFE trap on the bottle opening), E-M-P(envelope made of Millipore PTFE), E-P-P(envelope made of pure PTFE), SAFP(suspended acidified filter paper), and D-P-P(doubling layer of pure PTFE trap). 图 2 不同酸阱制作方式下测定3 mg·L–1 0.510 atom% NH4+-15N效果对比 Fig. 2 Comparison of the effect of determining 3 mg·L–1 0.510 atom% NH4+-15N under different acid trap making methods |
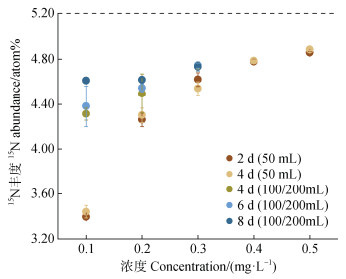
低浓度NH4+-N(0.1~0.5 mg·L–1)通常需要扩大体积以满足所需氮量,扩散时间相应增加。悬挂滤纸片长时间培养易吸水饱和回滴,反而降低回收率,本研究尝试了不同体积、培养时间下的信封扩散包培养(图 3)。50 mL低浓度样品25 ℃摇培2、4 d,所测15N丰度差异不显著(P > 0.05),均低于理论丰度(5.200 atom%),且N浓度越低与理论值比值越小,仅为0.653,精密度SD≤0.050 atom%。将0.1 mg·L–1 NH4+-15N扩大体积至200 mL、0.2~0.3 mg·L–1扩大体积至100 mL,分别摇培4、6、8 d。200 mL 0.1 mg·L–1第4天的15N测定值已较50 mL明显提高(P < 0.001),从3.440 atom%升高至4.310 atom%,SD从0.056 atom%减小为0.052 atom%;培养8 d的测定值明显高于6 d的测定值(P < 0.05),更加接近理论值。0.2~0.3 mg·L–1 NH4+-N也呈现出与0.1 mg·L–1相似的变化趋势,100 mL均显著高于50 mL的测定值(P < 0.001),虽然4、6、8 d的差异不如0.1 mg·L–1显著,但8 d的精密度和准确度最高。显然,扩大样品体积、延长培养时间可提高低浓度NH4+-15N测定值的准确度和精密度。
|
注:图中虚线为理论丰度5.200 atom%。下同。 Note: The dashed line in the figure indicates expected value of 5.200 atom%. The same below. 图 3 0.1~0.5 mg·L–1 5.200 atom%(NH4)2SO4样品在不同扩散时间和体积下的15N测定结果 Fig. 3 15N determination of 0.1-0.5 mg·L–1 5.200 atom%(NH4)2SO4 samples at different diffusion times and volumes |
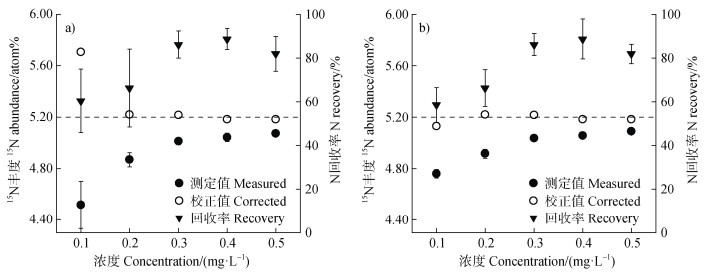
比较0.1~0.5 mg·L–1 NH4+-N在100 mL和200 mL扩散8 d的结果(图 4)发现,两种体积下,不同浓度的N回收率变化趋势相似,均随着浓度升高回收率增加,扩大体积并未能明显提高回收率。不同浓度下NH4+-15N的测定值也随浓度升高而增大,且精密度较好,大于等于0.2 mg·L–1 NH4+-N扩散8 d后的SD均小于0.060 atom%,尽管与理论值有明显差距,经标样校正后基本与理论值吻合,校正值与理论值比值大于等于0.997,且100 mL和200 mL体系的校正值无明显差异;对于0.1 mg·L–1、200 mL体系的校正值(5.130 atom%)已基本接近理论值,而100 mL体系则明显偏离理论值(5.710 atom%)。
|
图 4 0.1~0.5 mg·L–1 5.200 atom%(NH4)2SO4样品25 ℃摇培8 d后的测定值、校正值和回收率(a. 100 mL扩散体系;b. 200 mL扩散体系) Fig. 4 The measured values, corrected values and recovery of 0.1-0.5 mg·L–1 5.200 atom%(NH4)2SO4 after 25 ℃ and 8 days diffusion(a. 100 mL volume; b. 200 mL volume) |
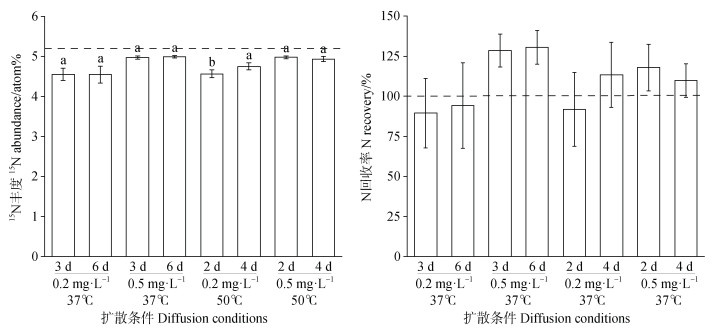
升高温度可有效缩短扩散时间、提高回收率。图 5表明,100 mL 0.2 mg·L–1 NH4+-N在37 ℃下扩散3 d,回收率已提高至85%,远高于25 ℃下扩散8 d的66.3%(图 4),15N测定值(4.552 atom%)与25 ℃下扩散8 d相近(4.869 atom%,表 1)。延长扩散时间至6 d,回收率提高至90%以上,15N测定值与3 d无明显区别(P > 0.05);当温度提高至50 ℃,培养2 d回收率已达90%,与37 ℃下3 d的回收率相当(P > 0.05),培养4 d回收率继续升高至超过100%,但是15N测定值与37 ℃无明显差异(P > 0.05)。0.5 mg·L–1 NH4+-N,37 ℃培养3 d和50 ℃培养2 d,15N测定值与25 ℃下8 d测定值相近(P > 0.05),但是加温后回收率均超过100%。与25 ℃相比,加温会导致SD升高,0.2 mg·L–1样品在37 ℃下扩散3 d和6 d的SD分别为0.158 atom%和0.212 atom%,在50 ℃下扩散2 d SD为0.097 atom%,均高于25 ℃下的SD(0.056 atom%)。
|
注:a)图中虚线为理论丰度5.200 atom%。图中不同小写字母表示差异显著(P < 0.05)。 Note: The dashed line in Figure a)indicates the expected value of 5.200 atom%. The lowercase letters indicate significant differences(P < 0.05). 图 5 0.2 mg·L–1和0.5 mg·L–1 NH4+-15N在37 ℃和50 ℃下(100 mL)分别扩散3、6 d和2、4 d的测定值(a)与回收率(b) Fig. 5 The measured values(a)and recovery(b)of 0.2 mg·L–1 and 0.5 mg·L–1 NH4+-15N in 100 mL after diffusion at 37 ℃ for 3 and 6 days or 50 ℃ for 2 and 4 days |
|
|
表 1 0.2和0.5 mg·L–1 5.200 atom% 100 mL(NH4)2SO4样品在不同温度下扩散摇培测定值 Table 1 The measured values of 0.2 and 0.5 mg·L–1 5.200 atom% 100 mL(NH4)2SO4 after diffusion at different temperatures/atom% |
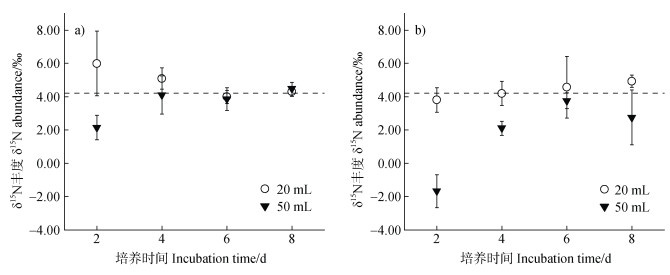
静置与摇培均可用于扩散法,自然丰度NH4+通常需长时间扩散,本研究发现摇培更适合自然丰度样品(图 6),NH4+的δ15N测定值精密度和准确度均随摇培时间延长而明显提高:20 mL 3 mg·L–1 NH4+-N的δ15N测定值在8 d为4.29‰,与理论值比值为1.016,其SD从第2天的1.95‰,下降至第8天的0.26‰;50 mL 1.2 mg·L–1 NH4+-N的δ15N测定值从第2天的2.15‰升高至第9天的4.48‰,与理论值比值为1.062,SD从0.74‰下降至0.38‰。与之相反,静置培养20 mL 3 mg·L–1 NH4+-N的δ15N测定值第2天即为3.81‰,随着时间延长至8 d,δ15N-NH4+测定值为4.93‰,明显高于理论值;静置培养50 mL 1.2 mg·L–1 NH4+-N的测定值第2天远低于理论值,仅为–1.67‰;第6天升高至3.76‰,与理论值的比值为0.892;第8天的测定值又下降至2.76‰,且SD骤增至1.65‰。因此,摇培8 d可较好实现对适宜浓度的自然丰度δ15N-NH4+的测定。
|
注:图中虚线为理论丰度4.220 atom%。下同。 Note: The dashed line in the figure indicates the expected value of 4.220 atom%. The same below. 图 6 1.2 mg·L–1 50 mL和3 mg·L–1 20 mL自然丰度δ15N-NH4+在不同培养方式(a. 摇培;b. 静置)和时间下的悬挂扩散效果 Fig. 6 Effect of different incubation types(a. shaking; b. standing)with prolonged times on δ15N-NH4+ values of 1.2 and 3 mg·L–1 NH4+-15N using suspending diffusion |
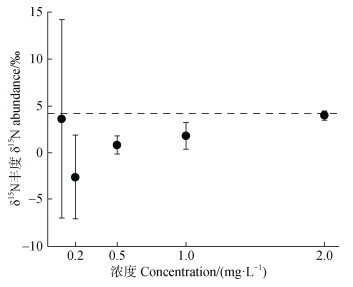
扩散包法虽能用于低浓度标记样品的测定,却不适用于低浓度自然丰度样品。扩散包法摇培0.1~2 mg·L–1自然丰度NH4+-N至6 d,结果(图 7)表明:0.1~0.2 mg·L–1δ15N-NH4+测定值误差极大,SD高达4.51‰~10.58‰;0.5 mg·L–1的测定误差减小,但与理论值比值仍为0.200;当浓度升高至1 mg·L–1,与理论值比值为0.429;仅有当浓度为2 mg·L–1时,测定值为3.98‰,与理论值基本吻合,且SD仅为0.50‰。因此,即使是回收率较好的扩散包培养6 d,也无法实现浓度小于等于1 mg·L–1的自然丰度δ15N-NH4+测定。因此,扩散法可准确测定适宜浓度的自然丰度δ15N-NH4+,但对低浓度自然丰度样品并不适用。
|
图 7 0.1~2 mg·L–1自然丰度(NH4)2SO4信封包扩散法摇培6 d的δ15N-NH4+测定值 Fig. 7 The measured δ15N-NH4+ values of 0.1-2 mg·L–1 natural abundance(NH4)2SO4 after enveloped diffusion for 6 days |
扩散法的准确度和精密度受N回收率影响,虽无需达到100%回收,但回收率过低会加剧同位素分馏,加大测定误差[27]。改进酸阱制作方法、样品培养方式和培养温度均为常见的提高回收率的方法。
3.1.1 酸阱的改进悬挂法[5-6]和扩散包法[2,27]是目前最常见的两种酸阱。悬挂法操作简便、成本低廉,但对于低氮样品(≤50 μg N),扩散包法的回收率(> 90%)显著优于变化较大的悬挂法(57%~98%)(图 2)。Stark和Hart[8]也发现小于等于0.8 mg·L–1N的样品中,扩散包法回收率明显优于悬挂法,这是因为扩散包密封良好,避免了其他吸收源竞争NH3,以及滤纸吸水饱和回滴造成的氮损失[10]。扩散包还可倒置摇培,减少瓶内气压引起的NH3泄露,应是一种更适合自然丰度和低浓度标记丰度样品的酸阱制作方式[23,27,29]。通常使用信封法制作扩散包,操作人员需使用镊子小心包裹压实,方能有效密封[27],通常耗时较长。为提高效率,有研究尝试了较为简便的瓶口夹层法[9]和双层膜法[27]。本文中瓶口夹层法可能因蓝盖瓶瓶口和体积较大,气密性不够,造成回收率最低且误差最大。不同于Sigman等[27]用金属圆筒压成的双层膜,本研究采用了一种特殊简易装置(图 1d),可在30 s内完成一个双层膜扩散包制作,且密封严实,回收率几乎为100%,测定的结果准确度和精密度也最高。
目前所用的扩散包材料几乎均为Merck Millipore公司生产的LCWP 02500膜[27-28],价格昂贵,本实验采用了无支撑的纯PTFE膜制作酸阱,价格约为Millipore膜的0.1%,在回收率和15N测定准确度上均表现良好,不添加聚丙烯作为支撑结构,延展性好,更易于密封,几乎无空白氮,本研究认为其可代替价格昂贵的Milipore PTFE。
3.1.2 培养方式、培养温度和培养体积摇培、静置是广泛采用的培养方法,摇培虽占用摇床,却能加速NH3挥发,使酸阱在短时内获得足量氮,回收率明显提高。在标记样品中摇培较静置培养更高效:Saghir等[7]发现同等氮量在25 ℃下以75~85 r·min–1摇培仅需18、28和72 h,而静置则需24、36和86 h;Mulvaney等[11]在25 ℃静置培养需66 h才能回收75~85 r·min–1摇培36 h的同等氮量;MacKown等[12]在室温下静置扩散50~200 μg标记NH4+-15N,7 d后回收率不足60%,而60 r·min–1摇培7 d回收率可达94%。由于自然丰度样品通常需要更长时间的扩散以减少同位素分馏的影响,为避免占用摇床,有研究推荐静置培养[29]。本研究发现,自然丰度样品静置培养的扩散效率明显低于摇培,通常需要大于等于14 d的培养(图 6),反而增加在实际土壤样品中DON降解的风险。扩散的速度与摇培速度有关[23],先前研究摇培速度多在50~100 r·min–1[12-13],本研究提高至140 r·min–1后,发现无论是足量N样品20 mL(样品浓度大于等于2 mg·L–1)还是低N样品50 mL(样品浓度低于2 mg·L–1),均可在8 d内完成,且测定结果的精密度和准确度均明显提高,分别为0.26‰和0.38‰(图 6),显著低于Stephan和Kavanagh[29]报道的0.20‰~1.30‰,也优于Holmes等[23]的结果。
对于低氮量的样品,通常需要扩大样品体积以获得足够氮量。体积增大会减小顶空,气体饱和后扩散速率下降,因此,样品的表面积和体积的比值是决定扩散速度的关键。在大体积实验中,本研究发现,200 mL回收率低于100 mL(图 4),很可能是表面积/体积比值降低减缓了氮回收进度[9]。Holmes等[23]对4 L 2 μmol·L–1 NH4+扩散,发现回收率下降损失的氮较体积增加的氮量更多。现有研究大多使用不超过200 mL的扩散体系,偶有更大体积的扩散需辅以加热或浓缩[21-22,27]。扩大体积也需同时扩大培养瓶的体积,不仅增加时间成本,也增加测试成本,所以本研究推荐样品体积应小于等于200 mL。
扩散法中最常使用25 ℃室温培养,提高温度可加速扩散、缩短时间、提高回收率,也会增大杂质氮。Zhang等[6]曾比较3个温度梯度(25 ℃、35 ℃、45 ℃)下2~6 mg·L–1 NH4+-N的扩散培养,发现25 ℃下NH4+-15N丰度相对最接近理论丰度(5 atom%),而35 ℃和45 ℃下均明显低于理论丰度,温度越高组内误差越大,杂质氮量随温度升高而明显增加是最主要的原因。对于悬挂法,温度超过55 ℃后,高温产生的冷凝水与酸阱竞争吸收NH3,反而降低回收率[12]。但是,对于极低浓度和自然丰度的样品,所需扩散时间很长,适当提高温度有助于提高样品处理效率,使用密封性良好的扩散包,也能减少冷凝水的影响。Lachouani等[16]在37 ℃下摇培(100 r·min–1),将扩散所需时间从5 d缩短为3 d。本研究发现,提高温度的确有效缩短了低氮量的扩散时间,37 ℃3 d、50 ℃2 d的测定结果与25 ℃8 d无明显差异,但误差却明显变大(图 5)。50 ℃下和37 ℃下6 d的回收率均超过100%(图 5),显然是扩散试剂(KCl、MgO)和水里的杂质氮因升温释放造成误差变大,在天然土壤或水体样品时,升温还会促进DON降解[23]。Sigman等[27]扩散培养海水中的自然丰度NH4+-N、NO3–-N时,也建议高温加热需控制培养时间,减少DON的影响。因此,需根据具体样品情况评估加温的适用性,如需加热,应注意控制加热时间。
3.2 扩散法对低氮标记样品的适用性以往扩散法测定土壤浸提液,NH4+-N浓度一般在1 mg·L–1以上[8-9,12],当样品的总NH4+-N含量低于300 μg时,易因回收率不足而同位素分馏明显[25]。Bradley和Fyles[26]利用悬挂法在室温(22 ℃)下对20 μg N摇动扩散14 d,发现15N丰度低于实际值。本研究也发现,对于低氮量样品,未经校正的测定结果明显低于理论值(图 4)。低氮量标记样还易受到空白氮的稀释和干扰[29-30],浸提液使用的KCl、MgO存在微量NH4+-N,使用高纯试剂也难以完全避免,需在450 ℃下高温灼烧降低干扰[6-8,30]。土壤和水体天然样品中的DON在碱性环境下易降解或被残存微生物分解为NH4+,也会干扰低浓度样品的测定。
亦有研究表明,合适的校正方法可有效降低回收率及空白氮的影响,发现当回收率大于45%,分馏系数稳定,测定值线性变化,可通过标样校正[23]。通常有三类校正方法:(1)根据实际测定的空白氮的值进行校正[14,29],该法工作量大,因为不同厂家甚至同一厂家不同批次试剂中的杂质氮含量均有差异[31],而扩散体系中杂质氮的信号通常较低,准确测定困难;(2)根据同位素分馏系数校正[23],当扩散过程进入一定进程后,分馏系数相对稳定,且不随NH4+-N浓度变化,可通过封闭系统或开放系统的分馏方程校正,该法要明确反应进程,不同批次间分馏系数虽较稳定,仍在一定范围内变异,可能增加误差;(3)根据同批次操作的相近浓度、丰度标样测定值构建标准曲线校正,该方法最早由Lory和Russelle[25]提出,根据标样在扩散、非扩散下的值绘制标准曲线,可有效避免回收率不足及空白氮的影响,Stark和Hart[8]验证了该方法的精密度和准确性,本文也用该法校正了测定数据(图 4)。
综上,本研究发现采用扩散包法、扩大反应体积至100 mL、室温下培养8 d,或37 ℃下培养3 d,并经同批次同体系标准曲线校正,可准确测定土壤浸提液中大于等于0.2 mg·L–1的标记NH4+-15N,大大降低了扩散法测定土壤浸提液中标记NH4+-15N的氮量下限。
3.3 扩散法在自然丰度测定中的适用性自然丰度δ15N-NH4+的测定对回收率要求更高,Chen和Dittert[13]发现,自然丰度大于等于0.8 mg·L–1 NH4+-N培养72 h后所有氮回收率均保持在95%以上,说明扩散法可能也适用于自然丰度样品。当底物完全转化为产物时,同位素分馏可忽略,仅需排除杂质氮干扰。Stephen和Kavanagh[29]认为在分离自然丰度的土壤NH4+-N时,扩散是唯一有效、不受其他物质干扰的方法。本研究表明,采用悬挂法或扩散包法摇培8 d即可准确测定浓度在1 mg·L–1及以上的自然丰度NH4+-N,精密度小于等于0.50‰(图 6),低于该浓度,则需联合反硝化细菌法[18,20,32]。即,扩散、干燥后的滤纸片加水重溶,调整为约20 nmol N后,使用碱性过硫酸钾将NH4+转化为NO3–,再通过反硝化细菌Pseudomonas aureofaciens将其转化为N2O [32]。反硝化细菌法灵敏度极高,能实现大于等于10 nmol N的灵敏测定[18],但是反应步骤复杂,涉及试剂较多,试剂中的杂质氮也会被灵敏检测,干扰测定结果[33]。因此,该方法的有效性仍需进一步探讨,但是在适宜浓度范围内,选择单独扩散法可高效、准确测定土壤浸提液中自然丰度的δ15N-NH4+。
4 结论本研究优化了酸阱制作方式、培养时间、反应体积和培养温度,在降低实验成本、简化实验操作的同时,实现了对低至0.2 mg·L–1土壤中标记NH4+-15N的准确、灵敏测定,发现单独使用扩散法仍可用于不低于1 mg·L–1自然丰度δ15N-NH4+的测定。这不仅拓展了扩散法在NH4+-15N测定上的适合浓度、丰度范围,也建立了明确的扩散方法体系以保证测定结果的准确度和灵敏度。对于更低浓度的自然丰度、标记NH4+-N,扩散法仍然是分离土壤NH4+的最佳方法,可再将其氧化为NO3–或NO2–后联合其他方法测定。但是,在不影响方法灵敏度的基础上,如何降低多种反应试剂中的杂质氮以及反应步骤中的同位素分馏对测定结果的影响,仍然是需要深入探讨的技术难题。
| [1] |
Jeong Y J, Seo B S, Baek N, et al. Methods for the determination of stable isotope ratios of multiple nitrogen species in rainwater using distillation and evaporation[J]. Frontiers in Environmental Science, 2022, 10: 877055. DOI:10.3389/fenvs.2022.877055
(  0) 0) |
| [2] |
Sebilo M, Mayer B, Grably M, et al. The use of the 'ammonium diffusion' method for δ15N-NH4+ and δ15N- NO3– measurements: Comparison with other techniques[J]. Environmental Chemistry, 2004, 1(2): 99. DOI:10.1071/EN04037
(  0) 0) |
| [3] |
Ramadhanty O C, Rohmatullaily, Legasari L. Analisis Kadar nitrogen total pada pupuk urea menggunakan metode kjedahl di PT pupuk sriwidjaja Palembang[J]. Sains: Jurnal Kimia Dan Pendidikan Kimia, 2024, 13(1): 6-11. DOI:10.36709/sains.v13i1.52
(  0) 0) |
| [4] |
Cao Y C, Zhong M, Gong H, et al. Determining 15N abundance in ammonium, nitrate and nitrite in soil by measuring nitrous oxide produced (In Chinese)[J]. Acta Pedologica Sinica, 2013, 50(1): 113-119. DOI:10.11766/trxb201204160136 [曹亚澄, 钟明, 龚华, 等. N2O产生法测定土壤无机态氮15N丰度[J]. 土壤学报, 2013, 50(1): 113-119.]
(  0) 0) |
| [5] |
Zhang P Y, Wen T, Zhang J B, et al. On improving the diffusion method for determination of δ15N-NH4+ and δ15N-NO3– in soil extracts (In Chinese)[J]. Acta Pedologica Sinica, 2017, 54(4): 948-957. DOI:10.11766/trxb201611250485 [张珮仪, 温腾, 张金波, 等. 扩散法测定土壤无机氮15N丰度方法优化研究[J]. 土壤学报, 2017, 54(4): 948-957.]
(  0) 0) |
| [6] |
Zhang S S, Fang Y T, Xi D. Adaptation of micro-diffusion method for the analysis of 15N natural abundance of ammonium in samples with small volume[J]. Rapid Communications in Mass Spectrometry, 2015, 29(14): 1297-1306. DOI:10.1002/rcm.7224
(  0) 0) |
| [7] |
Saghir N S, Mungwari F P, Mulvaney R L, et al. Determination of nitrogen by microdiffusion in mason jars: Ⅱ. Inorganic nitrogen-15 in soil extracts[J]. Communications in Soil Science and Plant Analysis, 1993, 24(19/20): 2747-2763.
(  0) 0) |
| [8] |
Stark J M, Hart S C. Diffusion technique for preparing salt solutions, Kjeldahl digests, and persulfate digests for nitrogen-15 analysis[J]. Soil Science Society of America Journal, 1996, 60(6): 1846-1855. DOI:10.2136/sssaj1996.03615995006000060033x
(  0) 0) |
| [9] |
Goerges T, Dittert K. Improved diffusion technique for 15N: 14N analysis of ammonium and nitrate from aqueous samples by stable isotope spectrometry[J]. Communications in Soil Science and Plant Analysis, 1998, 29(3/4): 361-368.
(  0) 0) |
| [10] |
Wen T, Cao Y C, Zhang P Y, et al. On progress in use of micro-diffusion method in δ15N-NH4+ and δ15N- NO3– measurements (In Chinese)[J]. Soils, 2016, 48(4): 634-640. [温腾, 曹亚澄, 张珮仪, 等. 微扩散法测定铵态氮、硝态氮的15N稳定同位素研究综述[J]. 土壤, 2016, 48(4): 634-640.]
(  0) 0) |
| [11] |
Mulvaney R L, Khan S A, Stevens W B, et al. Improved diffusion methods for determination of inorganic nitrogen in soil extracts and water[J]. Biology and Fertility of Soils, 1997, 24(4): 413-420. DOI:10.1007/s003740050266
(  0) 0) |
| [12] |
MacKown C T, Brooks P D, Smith M S. Diffusion of nitrogen-15 Kjeldahl digests for isotope analysis[J]. Soil Science Society of America Journal, 1987, 51(1): 87-90. DOI:10.2136/sssaj1987.03615995005100010018x
(  0) 0) |
| [13] |
Chen R R, Dittert K. Diffusion technique for 15N and inorganic N analysis of low-N aqueous solutions and Kjeldahl digests[J]. Rapid Communications in Mass Spectrometry, 2008, 22(11): 1727-1734. DOI:10.1002/rcm.3525
(  0) 0) |
| [14] |
Wang X Q, Yao Y Y, Chen B C, et al. Effects of combined application of nitrate and ammonium on rice growth and soil nutrients under flooding conditions (In Chinese)[J]. Soils, 2020, 52(2): 254-261. [王晓琪, 姚媛媛, 陈宝成, 等. 淹水条件硝态氮和铵态氮配施对水稻生长与土壤养分的影响[J]. 土壤, 2020, 52(2): 254-261.]
(  0) 0) |
| [15] |
Wang X, Cao Y C, Han Y, et al. Determination of nitrogen and oxygen isotope ratio of nitrate in water (In Chinese)[J]. Acta Pedologica Sinica, 2015, 52(3): 558-566. DOI:10.11766/trxb201405080224 [王曦, 曹亚澄, 韩勇, 等. 化学转化法测定水体中硝酸盐的氮氧同位素比值[J]. 土壤学报, 2015, 52(3): 558-566.]
(  0) 0) |
| [16] |
Lachouani P, Frank A H, Wanek W. A suite of sensitive chemical methods to determine the δ15N of ammonium, nitrate and total dissolved N in soil extracts[J]. Rapid Communications in Mass Spectrometry, 2010, 24: 3615-3623. DOI:10.1002/rcm.4798
(  0) 0) |
| [17] |
Knapp A N, Sigman D M, Lipschultz F. N isotopic composition of dissolved organic nitrogen and nitrate at the Bermuda Atlantic Time-series Study site[J]. Global Biogeochemical Cycles, 2005, 19(1): 2004GB002320. DOI:10.1029/2004GB002320
(  0) 0) |
| [18] |
Sigman D M, Casciotti K L, Andreani M, et al. A bacterial method for the nitrogen isotopic analysis of nitrate in seawater and freshwater[J]. Analytical Chemistry, 2001, 73(17): 4145-4153. DOI:10.1021/ac010088e
(  0) 0) |
| [19] |
Liu D W, Fang Y T, Tu Y, et al. Chemical method for nitrogen isotopic analysis of ammonium at natural abundance[J]. Analytical Chemistry, 2014, 86(8): 3787-3792. DOI:10.1021/ac403756u
(  0) 0) |
| [20] |
Moretti S, Duprey N N, Foreman A D, et al. Analytical improvements and assessment of long-term performance of the oxidation–denitrifier method[J]. Rapid Communications in Mass Spectrometry, 2024, 38(1): e9650. DOI:10.1002/rcm.9650
(  0) 0) |
| [21] |
Diaconu C, Brion N, Elskens M, et al. Validation of a dynamic ammonium extraction technique for the determination of 15N at enriched abundances[J]. Analytica Chimica Acta, 2005, 554(1/2): 113-122.
(  0) 0) |
| [22] |
Jia M R, Bol R, Kooijman A, et al. A decision support tool for the selection of 15N analysis methods of ammonium and nitrate[J]. Nutrient Cycling in Agroecosystems, 2023, 125(2): 309-343. DOI:10.1007/s10705-022-10227-z
(  0) 0) |
| [23] |
Holmes R M, McClelland J W, Sigman D M, et al. Measuring 15N–NH4 + in marine, estuarine and fresh waters: An adaptation of the ammonia diffusion method for samples with low ammonium concentrations[J]. Marine Chemistry, 1998, 60(3/4): 235-243.
(  0) 0) |
| [24] |
Liu D W, Tu Y, Fang Y T. Isotope analysis of ammonium and nitrate: A review on measured methods and their application (In Chinese)[J]. Chinese Journal of Applied Ecology, 2017, 28(7): 2353-2360. [刘冬伟, 图影, 方运霆. 铵盐和硝酸盐稳定同位素丰度测定方法及其应用案例[J]. 应用生态学报, 2017, 28(7): 2353-2360.]
(  0) 0) |
| [25] |
Lory J A, Russelle M P. Evaluation of a diffusion method for preparing low-nitrogen samples for nitrogen-15 analysis[J]. Soil Science Society of America Journal, 1994, 58(5): 1400-1404. DOI:10.2136/sssaj1994.03615995005800050017x
(  0) 0) |
| [26] |
Bradley R L, Fyles J W. Method to avoid isotope discrimination during the diffusion of NH4 + from 15N-labelled soil extracts[J]. Soil Biology and Biochemistry, 1996, 28(4/5): 695-697.
(  0) 0) |
| [27] |
Sigman D M, Altabet M A, Michener R, et al. Natural abundance-level measurement of the nitrogen isotopic composition of oceanic nitrate: An adaptation of the ammonia diffusion method[J]. Marine Chemistry, 1997, 57(3/4): 227-242.
(  0) 0) |
| [28] |
Sun J F, Bai E, Dai W W, et al. Improvements of the diffusion method to measure inorganic nitrogen isotope of 15N labeled soil (In Chinese)[J]. Chinese Journal of Ecology, 2014, 33(9): 2574-2580. [孙建飞, 白娥, 戴崴巍, 等. 15N标记土壤连续培养过程中扩散法测定无机氮同位素方法改进[J]. 生态学杂志, 2014, 33(9): 2574-2580.]
(  0) 0) |
| [29] |
Stephan K, Kavanagh K L. Suitability of the diffusion method for natural abundance nitrogen-15 analysis[J]. Soil Science Society of America Journal, 2009, 73(1): 293-302. DOI:10.2136/sssaj2007.0079
(  0) 0) |
| [30] |
Bell M D, Sickman J O. Correcting for background nitrate contamination in KCl-extracted samples during isotopic analysis of oxygen and nitrogen by the denitrifier method: Correcting for background nitrate contamination in KCl samples[J]. Rapid Communications in Mass Spectrometry, 2014, 28(5): 520-526. DOI:10.1002/rcm.6824
(  0) 0) |
| [31] |
Zhang Y L, Xu A M, Shang H B, et al. Ammonium contents in potassium chloride impurities and its impact on soil NH4+-N determination (In Chinese)[J]. Chinese Journal of Soil Science, 2010, 41(5): 1134-1137. [张英利, 许安民, 尚浩博, 等. 氯化钾中杂质铵含量及对土壤铵态氮测定的影响[J]. 土壤通报, 2010, 41(5): 1134-1137.]
(  0) 0) |
| [32] |
Stock P, Roder S, Burghardt D. Further optimisation of the denitrifier method for the rapid 15N and 18O analysis of nitrate in natural water samples[J]. Rapid Communications in Mass Spectrometry, 2021, 35(1): e8931. DOI:10.1002/rcm.8931
(  0) 0) |
| [33] |
Biasi C, Jokinen S, Prommer J, et al. Challenges in measuring nitrogen isotope signatures in inorganic nitrogen forms: An interlaboratory comparison of three common measurement approaches[J]. Rapid Communications in Mass Spectrometry, 2022, 36(22): e9370. DOI:10.1002/rcm.9370
(  0) 0) |
 2026, Vol. 63
2026, Vol. 63


